Элементы_I_Б_группы.ppt
- Количество слайдов: 41

d-Элементы

Общая характеристика группы. Cu 1 s 22 p 63 s 23 p 63 d 104 s 1; 28 [Ar] 3 d 104 s 1 Ag 1 s 22 p 63 s 23 p 63 d 104 s 24 p 64 d 105 s 1; [Kr] 4 d 105 s 1 47 Au 1 s 22 p 63 s 23 p 63 d 104 s 24 p 64 d 104 f 145 s 25 p 65 d 106 s 1; 79 [Xe] 4 f 145 d 106 s 2
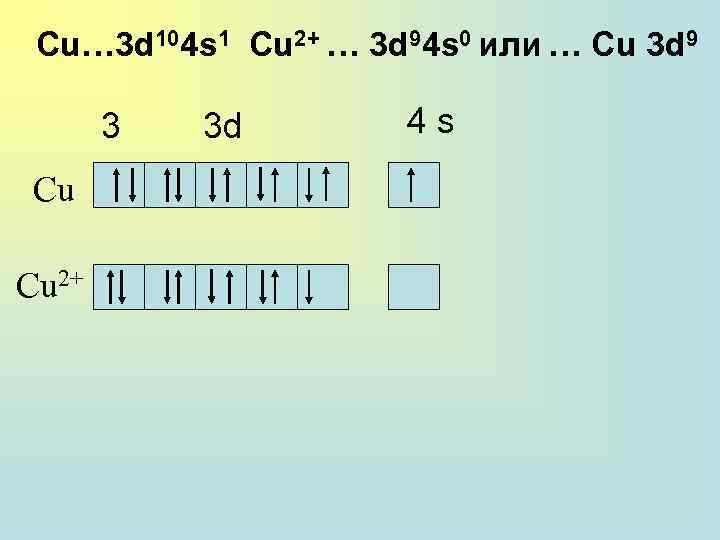
Cu… 3 d 104 s 1 Cu 2+ … 3 d 94 s 0 или … Cu 3 d 9 3 Cu Cu 2+ 3 d 4 s

Стандартные электродные потенциалы d-элементов 1 Б группы Процесс. E 0298, B Cu 2+ + 2 e- = Cu 0, 337 Ag 1+ + 1 e- = Ag 0, 799 Au 3+ + 3 e- = Au 1, 5 . . H 2 … Cu … Ag… Au …

Для меди наиболее характерна степень окисления +2, для серебра +1, для золота +3. Особая устойчивость степени окисления +1 у серебра объясняется большей прочностью конфигурации 4 d 10, т. к. эта конфигурация образуется уже у Pd, предшествующего серебру в периодической системе.

Радиусы атомов элементов побочной подгруппы I группы гораздо меньше, чем у металлов главной подгруппы, поэтому медь, серебро и золото отличаются большей плотностью, высокими температурами плавления.

При переходе от меди к серебру радиус атомов увеличивается, а у золота не изменяется, т. к. золото расположено в периодической системе после лантаноидов и еще испытывает эффект лантаноидного сжатия. Плотность золота очень велика. Химическая активность этих элементов невелика и убывает с возрастанием порядкового номера элемента.

Нахождение в природе. В природе встречается в виде различных соединений, Cu 2 S - медный блеск, Cu. Fe. S 2 - медный колчедан (халькопирит), Cu 3 Fe. S 3 - борнит, Сu 2 (ОН)2 СО 3 или Сu. СО 3 Сu(ОН)2 малахит.

Медь Сu ü довольно мягкий металл красного цвета, ü Tпл = 1083°С, üобладает высокой электро- и теплопроводностью, üобразует различные сплавы.

Способы получения. Продувание О 2 через расплав сульфида меди (I): 2 Cu 2 S + 3 О 2 = 2 Cu 2 O + 2 SO 2; 2 Cu 2 O + Cu 2 S = 6 Cu + SO 2.

Химические свойства

2 Сu + О 2 = 2 Сu. О (800°С); Сu + S = Cu. S (350°C); Сu + Сl 2 =Сu. Сl 2; 2 Сu + О 2 + H 2 О + СО 2 = (Сu. ОН)2 СО 3 (пленка зеленого цвета – образуется на воздухе);
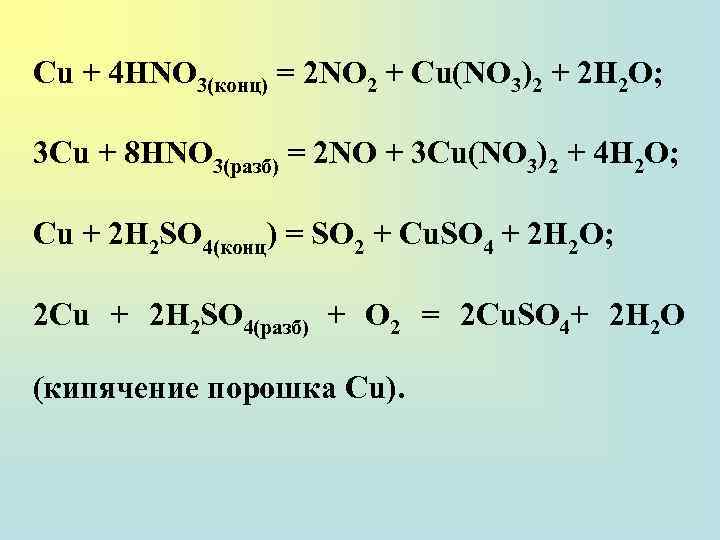
Сu + 4 НNО 3(конц) = 2 NO 2 + Cu(NO 3)2 + 2 Н 2 О; 3 Сu + 8 НNО 3(разб) = 2 NO + 3 Cu(NO 3)2 + 4 Н 2 О; Сu + 2 H 2 SO 4(конц) = SO 2 + Cu. SO 4 + 2 H 2 О; 2 Сu + 2 H 2 SO 4(paзб) + О 2 = 2 Cu. SO 4+ 2 H 2 O (кипячение порошка Сu).

Оксид меди (I) Сu 2 О - твердое вещество темно-красного цвета, обладает основными свойствами. Часть солей меди (I) растворима в воде, но легко окисляется кислородом воздуха, устойчивы комплексные соединения меди (I) [Cu(NH 3)2]+:

Сu 2 О + 2 НСl(разб) = 2 Cu. Cl + H 2 O; Сu 2 О + 4 НСl(изб. ) = 2 H[Cu. Cl 2] + H 2 O; 2 Сu 2 О + 8 НСl(разб) + О 2 = 4 Cu. Cl 2 + 4 Н 2 О; 2 Сu 2 О + 4 Н 2 О + О 2 = 4 Сu(ОН)2; Сu 2 О + СО = 2 Сu + СО 2. Гидроксид Cu(OH) не стоек и быстро окисляется.

Оксид меди (II) Сu. О - твердое вещество красно-коричневого цвета, проявляет основные свойства. 4 Cu. O = 2 Cu 2 O+ O 2; Сu. О + Н 2 = Сu + Н 2 О; 3 Сu. О + 2 А 1 = 3 Сu + Аl 2 О 3; Сu. О + С = Сu + СО;

Сu. О + СО = Сu + СО 2; 3 Сu. О + 2 NH 3(г) = N 2 + 3 Сu + 3 H 2 О; Сu. О + 2 НС 1 = Сu. Сl 2 + Н 2 O Слабые амфотерные свойства проявляются при сплавлении со щелочами: Сu. О + 2 Na. OH = Na 2 Сu. O 2 + Н 2 O

Гидроксид меди (II) Сu(ОН)2 - соединение голубого цвета, не растворим в воде, термически неустойчив, преобладают основные свойства, слабый окислитель: Cu. SO 4 + 2 Na. OH(разб. ) = Cu(OH)2↓ + Na 2 SO 4; Cu(OH)2 + 2 HCl = Cu. Cl 2 + 2 H 2 O; Cu(OH)2 + 2 Na. OH(конц. ) = Na 2[Cu(OH)4]; Купраты щелочных металлов имеют синюю окраску

2 Cu(OH)2 + CO 2 = Cu 2 ( ОН)2 СО 3 - + H 2 O; Cu(OH)2 = Cu. O + 2 H 2 O; Cu(OH)2 + 4 NH 4 OH = [Cu(NH 3)4](OH)2 + 4 H 2 O; качественная реакция на альдегиды: 2 Cu(OH)2 + СН 3 СНО = Cu 2 O + СН 3 СООН + 2 H 2 O
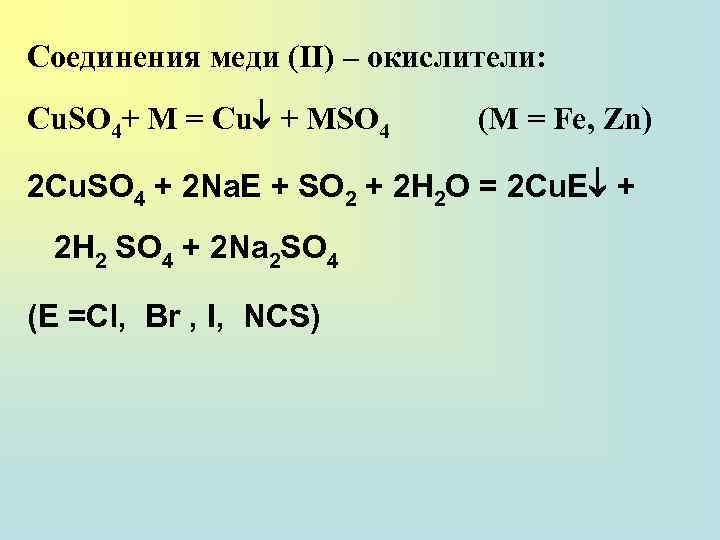
Соединения меди (II) – окислители: Cu. SO 4+ M = Cu + MSO 4 (М = Fе, Zn) 2 Cu. SO 4 + 2 Na. E + SO 2 + 2 H 2 O = 2 Cu. E + 2 H 2 SO 4 + 2 Na 2 SO 4 (E =Cl, Br , I, NCS)

Соли меди (II) сильных кислот подвергаются в водных растворах значительному гидролизу. Катион находится в гидратированном состоянии: Cu 2+ + Н 2 О Cu. OH + + Н+; Сu 2++ 4 Н 2 О [Cu(H 2 O)4]3+ [Cu(H 2 O)4]2+ + Н 2 О [Cu(OH)(H 2 O)3]+ + Н 3 О+ гидролиз в протолитической форме
2 Свойство Сu (ΙΙ) Комплексные соединения меди (II) с аммиаком, аминокислотами, многоатомными спиртами. [Cu(NH 3)4](OH)2 Свойство Сu (ΙΙ)](https://present5.com/presentation/48524624_179469548/image-22.jpg)
Комплексные соединения меди (II) с аммиаком, аминокислотами, многоатомными спиртами. [Cu(NH 3)4](OH)2 Свойство Сu (ΙΙ) реагировать с белками и пептидами, а также с биуретом (NH 2 –CO–NH– CO–NH 2) в щелочной среде с образованием окрашенных в сине-фиолетовый цвет комплексных соединений, используют для доказательства наличия пептидных связей. Реакция Сu (ΙΙ) с биуретом и белками называется биуретовой.

Серебро Ag - тяжелый пластичный металл с характерным блеском, Тпл = 962°С, обладает наибольшей среди металлов электро- и теплопроводностью, образует сплавы со многими металлами.

Химические свойства

Является малоактивным (благородным) металлом, непосредственно не взаимодействует с О 2, не реагирует с разбавленными растворами НСl, H 2 SO 4
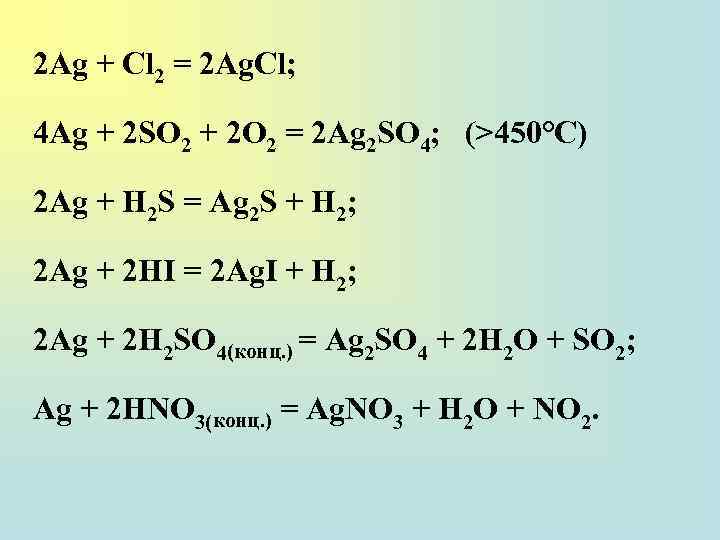
2 Ag + Cl 2 = 2 Ag. Cl; 4 Ag + 2 SO 2 + 2 O 2 = 2 Ag 2 SO 4; (>450°C) 2 Ag + H 2 S = Ag 2 S + H 2; 2 Ag + 2 HI = 2 Ag. I + H 2; 2 Ag + 2 H 2 SO 4(конц. ) = Ag 2 SO 4 + 2 H 2 O + SO 2; Ag + 2 НNO 3(конц. ) = Ag. NO 3 + H 2 O + NO 2.

Оксид серебра Ag 2 O - твердое вещество темнокоричневого цвета, Øразлагается при нагревании, проявляет основные свойства, Øплохо растворяется в НСI и H 2 SO 4 за счет образования на поверхности солей Ag. Cl и Ag 2 SO 4,
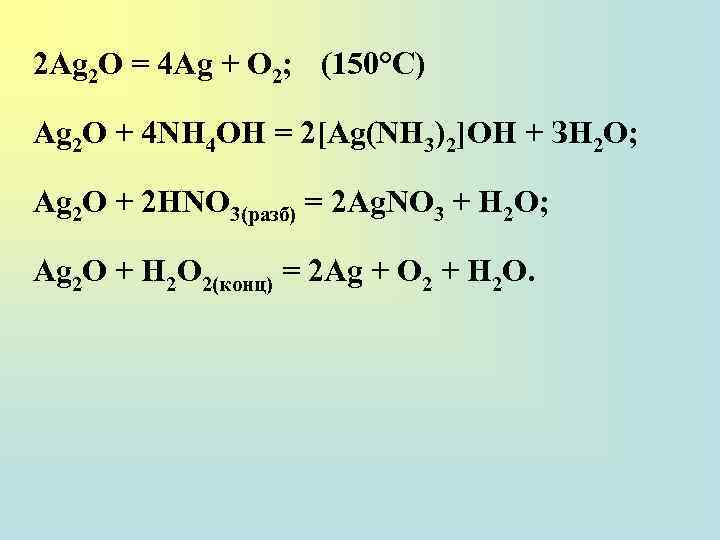
2 Ag 2 O = 4 Ag + О 2; (150°С) Ag 2 O + 4 NH 4 OH = 2[Ag(NH 3)2]OH + ЗН 2 О; Ag 2 O + 2 НNО 3(разб) = 2 Ag. NO 3 + Н 2 О; Ag 2 O + H 2 О 2(конц) = 2 Ag + О 2 + Н 2 О.

Соли серебра. ØСоли серебра не растворимы в воде, исключение составляют Ag. F, Ag. NO 3, Ag. Cl. O 4. ØВзаимодействие с гидратом аммиака, тиосульфатом натрия, карбонатом аммония (повторить качественные реакции на галогениды – НЛВ).

качественная реакция на хлорид-ион: HCl + Ag. NO 3 → Ag. Cl↓ + HNO 3 Na. Cl + Ag. NO 3 → Ag. Cl↓ + Na. NO 3 Ag. Cl + 2 NH 3 • H 2 O → [Ag(NH 3)2]Cl + 2 H 2 O Ag. Cl + (NH 4)2 СO 3 → [Ag(NH 3)2]Cl + СO 2↑ + H 2 O Ag. Cl + 2 Na 2 S 2 O 3 → Na 3[Ag(S 2 O 3)2] + Na. Cl

качественная реакция на бромид-ион: Na. Br + Ag. NO 3 → Ag. Br↓ + Na. NO 3 Ag. Br + 2 NH 3 • H 2 O → [Ag(NH 3)2]Br + 2 H 2 O Ag. Br + (NH 4)2 СO 3 ≠ Ag. Br + 2 Na 2 S 2 O 3 → Na 3[Ag(S 2 O 3)2] + Na. Br

качественная реакция на иодид-ион: Na. I + Ag. NO 3 → Ag. I↓ + Na. NO 3 Ag. I + 2 NH 3 • H 2 O ≠ Ag. I + (NH 4)2 СO 3 ≠ Ag. I + 2 Na 2 S 2 O 3 → Na 3[Ag(S 2 O 3)2] + Na. I

Химические основы применения соединений серебра в качестве лечебных препаратов в фармацевтическом анализе ØРастворимые соли серебра, попадая в организм в больших дозах, вызывают острое отравление, подобно другим тяжелым элементам-металлам. При этом, как правило, серебро связывается атомами серы белков. В результате инактивируются соответствующие ферменты, свертываются белки.

ØВода, содержащая ионы серебра порядка 10 -8 ммоль/л, обладает бактерицидным действием, что обусловлено образованием нерастворимых альбуминатов. ØЭффективность бактерицидного действия серебра выше, чем у хлора, хлорной извести, карболовой кислоты.

Золото Au – Øжелтый, ковкий, тяжелый металл, Ø Тпл = 1064°С, Øблагородный металл. Нахождение в природе. Встречается в виде самородного золота

Химические свойства

ØНе реагирует с водой, кислотами, щелочами, кислородом, азотом, углеродом, серой. ØПереводится в раствор "царской водкой", Ø со ртутью образует амальгаму, Øпри нагревании взаимодействует с галогенами.
![Au + НNО 3(конц) + 4 НСl(конц) = H[Au. Cl 4] + NO + Au + НNО 3(конц) + 4 НСl(конц) = H[Au. Cl 4] + NO +](https://present5.com/presentation/48524624_179469548/image-38.jpg)
Au + НNО 3(конц) + 4 НСl(конц) = H[Au. Cl 4] + NO + 2 H 2 О; 2 Au + 3 Сl 2 = 2 Au. Cl 3 (130°С)

Оксид и гидроксид золота (III) нерастворимы в воде, проявляют амфотерные свойства: Au(OH)3 + 3 HCl = Au. Cl 3 + 3 H 2 O Au(OH)3 + 4 HNO 3 = H[Au(NO 3)4] + 3 H 2 O Au(OH)3 + Na. OH = Na[Au(OH)4] гидроксоаурат (III)

Соединения Au (III) проявляют окислительные свойства: Подобрать коэффициенты: Au. Cl 3 + H 2 O 2 (конц. ) → Au (коллоид) +O 2 + HCl H[Au. Cl 4] +SO 2+H 2 O →H[Au. Cl 2]+H 2 SO 4 + HCl
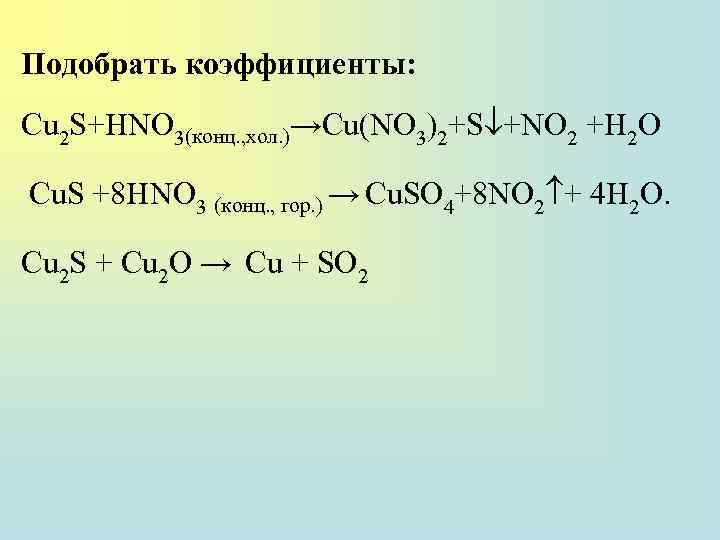
Подобрать коэффициенты: Cu 2 S+HNO 3(конц. , хол. )→Cu(NO 3)2+S +NO 2 +H 2 O Cu. S +8 HNO 3 (конц. , гор. ) → Cu. SO 4+8 NO 2 + 4 Н 2 О. Cu 2 S + Cu 2 O → Cu + SO 2
Элементы_I_Б_группы.ppt