d-Элементы.ppt
- Количество слайдов: 67
 d-Элементы
d-Элементы
 Классификация Первый ряд (3 d-элементы): Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn Второй ряд (4 d-элементы): Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd – кроме s- и pэлектронов имеют заполненную 3 d-электронную оболочку Третий ряд (5 d-элементы): La, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg – кроме s- и pэлектронов имеют заполненные 3 d-, 4 d- и 4 f-электронные оболочки Четвёртый ряд (6 d-элементы): Ac, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn – нет устойчивых изотопов
Классификация Первый ряд (3 d-элементы): Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn Второй ряд (4 d-элементы): Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd – кроме s- и pэлектронов имеют заполненную 3 d-электронную оболочку Третий ряд (5 d-элементы): La, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg – кроме s- и pэлектронов имеют заполненные 3 d-, 4 d- и 4 f-электронные оболочки Четвёртый ряд (6 d-элементы): Ac, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn – нет устойчивых изотопов
![Общие свойства Электронные формулы: ns 2(n-1)d 1 -10 Cr — [Ar]3 d 54 s Общие свойства Электронные формулы: ns 2(n-1)d 1 -10 Cr — [Ar]3 d 54 s](https://present5.com/presentation/72381937_151120358/image-3.jpg) Общие свойства Электронные формулы: ns 2(n-1)d 1 -10 Cr — [Ar]3 d 54 s 1 Cu — [Ar]3 d 104 s 1 Nb — [Kr]4 d 45 s 1 Mo — [Kr]4 d 55 s 1 Tc — [Kr]4 d 65 s 1 Ru — [Kr]4 d 75 s 1 Rh — [Kr]4 d 85 s 1 Pd — [Kr]4 d 105 s 0 Ag — [Kr]4 d 105 s 1 Pt — [Xe]4 f 145 s 2 p 6 d 96 s 1 Au — [Xe]4 f 145 s 2 p 6 d 106 s 1
Общие свойства Электронные формулы: ns 2(n-1)d 1 -10 Cr — [Ar]3 d 54 s 1 Cu — [Ar]3 d 104 s 1 Nb — [Kr]4 d 45 s 1 Mo — [Kr]4 d 55 s 1 Tc — [Kr]4 d 65 s 1 Ru — [Kr]4 d 75 s 1 Rh — [Kr]4 d 85 s 1 Pd — [Kr]4 d 105 s 0 Ag — [Kr]4 d 105 s 1 Pt — [Xe]4 f 145 s 2 p 6 d 96 s 1 Au — [Xe]4 f 145 s 2 p 6 d 106 s 1
 Общие свойства Все d-элементы – металлы Относительно высокая ОЭО 1, 5 ± 0, 3 Большинство d-элементов образуют устойчивые в водных кислых растворах ионы Э 2+ В пределах периода свойства d-элементов изменяются в меньшей степени, чем свойства элементов главных подгрупп
Общие свойства Все d-элементы – металлы Относительно высокая ОЭО 1, 5 ± 0, 3 Большинство d-элементов образуют устойчивые в водных кислых растворах ионы Э 2+ В пределах периода свойства d-элементов изменяются в меньшей степени, чем свойства элементов главных подгрупп
 Различия свойств d-элементов разных рядов Свойства элементов первого ряда значительно отличаются от свойств элементов второго и третьего рядов Свойства элементов второго и третьего рядов близки У элементов первого ряда более устойчивы более низкие состояния окисления, а у элементов второго и третьего рядов – высшие состояния окисления
Различия свойств d-элементов разных рядов Свойства элементов первого ряда значительно отличаются от свойств элементов второго и третьего рядов Свойства элементов второго и третьего рядов близки У элементов первого ряда более устойчивы более низкие состояния окисления, а у элементов второго и третьего рядов – высшие состояния окисления
 ОЭО Sc Ti V Cr Mn Fe Co Ni Cu Zn 1, 2 1, 3 1, 5 1, 6 1, 7 1, 8 1, 7 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd 1, 1 1, 2 1, 3 1, 4 1, 5 La Hf Ta W Re Os Ir Pt Au Hg 1, 1 1, 2 1, 4 1, 5 1, 6 1, 5 1, 4 1, 5
ОЭО Sc Ti V Cr Mn Fe Co Ni Cu Zn 1, 2 1, 3 1, 5 1, 6 1, 7 1, 8 1, 7 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd 1, 1 1, 2 1, 3 1, 4 1, 5 La Hf Ta W Re Os Ir Pt Au Hg 1, 1 1, 2 1, 4 1, 5 1, 6 1, 5 1, 4 1, 5
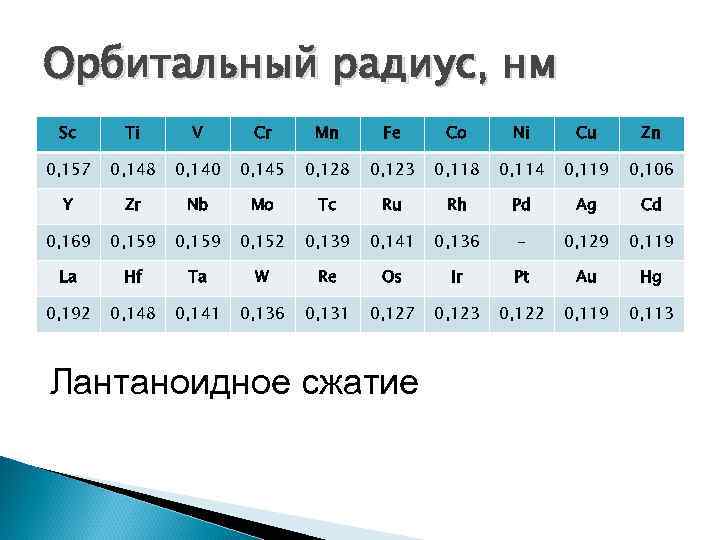 Орбитальный радиус, нм Sc Ti V Cr Mn Fe Co Ni Cu Zn 0, 157 0, 148 0, 140 0, 145 0, 128 0, 123 0, 118 0, 114 0, 119 0, 106 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd 0, 169 0, 159 0, 152 0, 139 0, 141 0, 136 - 0, 129 0, 119 La Hf Ta W Re Os Ir Pt Au Hg 0, 192 0, 148 0, 141 0, 136 0, 131 0, 127 0, 123 0, 122 0, 119 0, 113 Лантаноидное сжатие
Орбитальный радиус, нм Sc Ti V Cr Mn Fe Co Ni Cu Zn 0, 157 0, 148 0, 140 0, 145 0, 128 0, 123 0, 118 0, 114 0, 119 0, 106 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd 0, 169 0, 159 0, 152 0, 139 0, 141 0, 136 - 0, 129 0, 119 La Hf Ta W Re Os Ir Pt Au Hg 0, 192 0, 148 0, 141 0, 136 0, 131 0, 127 0, 123 0, 122 0, 119 0, 113 Лантаноидное сжатие
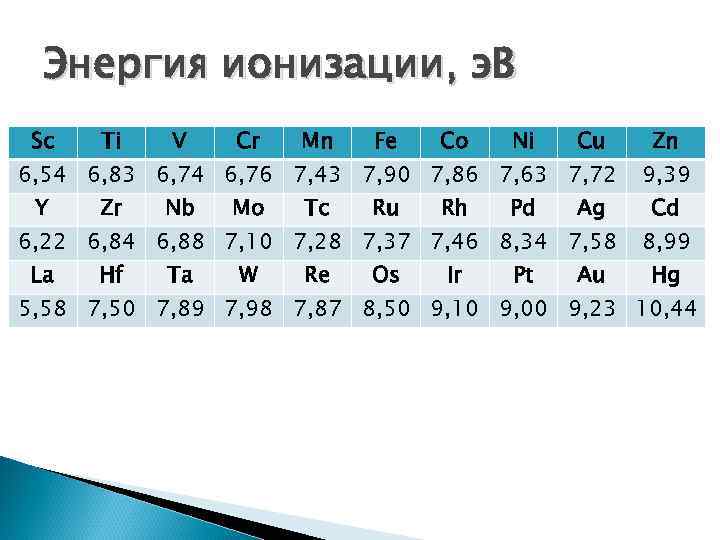 Энергия ионизации, э. В Sc Ti V Cr Mn Fe Co Ni Cu Y Zr Nb Mo Tc Ru Rh Pd Ag La Hf Ta W Re Os Ir Pt Au Zn 6, 54 6, 83 6, 74 6, 76 7, 43 7, 90 7, 86 7, 63 7, 72 9, 39 6, 22 6, 84 6, 88 7, 10 7, 28 7, 37 7, 46 8, 34 7, 58 8, 99 Cd Hg 5, 58 7, 50 7, 89 7, 98 7, 87 8, 50 9, 10 9, 00 9, 23 10, 44
Энергия ионизации, э. В Sc Ti V Cr Mn Fe Co Ni Cu Y Zr Nb Mo Tc Ru Rh Pd Ag La Hf Ta W Re Os Ir Pt Au Zn 6, 54 6, 83 6, 74 6, 76 7, 43 7, 90 7, 86 7, 63 7, 72 9, 39 6, 22 6, 84 6, 88 7, 10 7, 28 7, 37 7, 46 8, 34 7, 58 8, 99 Cd Hg 5, 58 7, 50 7, 89 7, 98 7, 87 8, 50 9, 10 9, 00 9, 23 10, 44
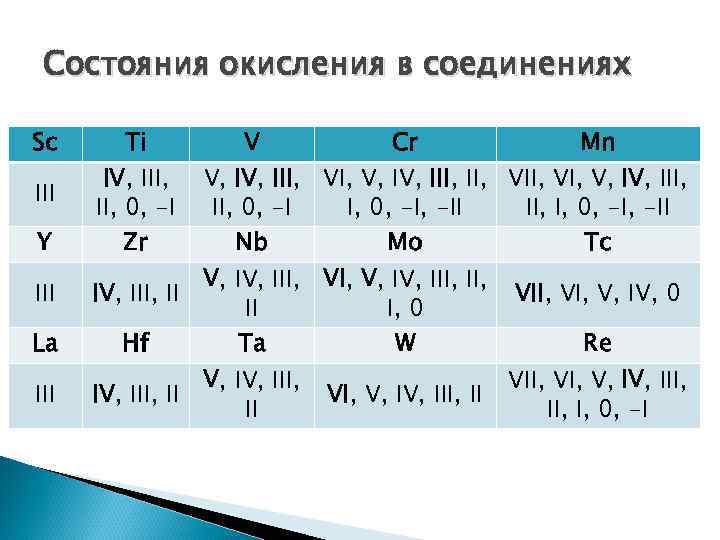 Состояния окисления в соединениях Sc III Y III La III Ti IV, III, 0, -I Zr V Cr Mn V, III, V, IV, III, VII, V, IV, III, 0, -II II, I, 0, -II Nb Mo V, III, V, IV, III, II II I, 0 Hf Ta V, III, IV, III, II II W VI, V, III, II Tc VII, V, IV, 0 Re VII, V, IV, III, I, 0, -I
Состояния окисления в соединениях Sc III Y III La III Ti IV, III, 0, -I Zr V Cr Mn V, III, V, IV, III, VII, V, IV, III, 0, -II II, I, 0, -II Nb Mo V, III, V, IV, III, II II I, 0 Hf Ta V, III, IV, III, II II W VI, V, III, II Tc VII, V, IV, 0 Re VII, V, IV, III, I, 0, -I
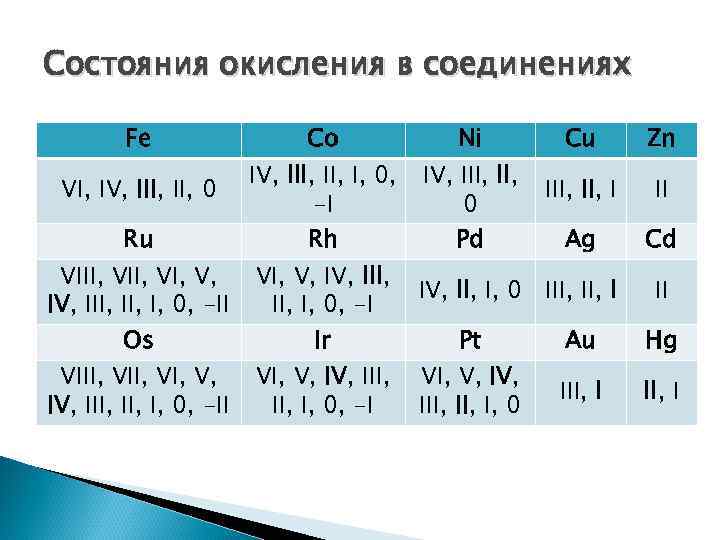 Состояния окисления в соединениях Fe Co Ni Cu IV, III, I, 0, IV, III, VI, IV, III, 0 III, I -I 0 Ru Rh Pd Ag VIII, VI, V, III, IV, II, I, 0 III, I IV, III, I, 0, -II II, I, 0, -I Os Ir Pt Au VIII, VI, V, IV, III, I, 0, -II II, I, 0, -I III, I, 0 Zn II Cd II Hg II, I
Состояния окисления в соединениях Fe Co Ni Cu IV, III, I, 0, IV, III, VI, IV, III, 0 III, I -I 0 Ru Rh Pd Ag VIII, VI, V, III, IV, II, I, 0 III, I IV, III, I, 0, -II II, I, 0, -I Os Ir Pt Au VIII, VI, V, IV, III, I, 0, -II II, I, 0, -I III, I, 0 Zn II Cd II Hg II, I
 3 d-Элементы – активные металлы и реагируют с разбавленными кислотами (кроме Cu), вытесняя водород и образуя соли с низкими степенями окисления металла Cr + 2 HCl(разб. ) = Cr. Cl 2 + H 2 Cr + H 2 SO 4(разб. ) = Cr. SO 4 + H 2
3 d-Элементы – активные металлы и реагируют с разбавленными кислотами (кроме Cu), вытесняя водород и образуя соли с низкими степенями окисления металла Cr + 2 HCl(разб. ) = Cr. Cl 2 + H 2 Cr + H 2 SO 4(разб. ) = Cr. SO 4 + H 2
 4 d- и 5 d-Элементы реагируют с концентрированными кислотами- окислителями или щелочами в присутствии окислителей, образуя анионные соли с высокими степенями окисления металлов При нагревании Mo + 3 H 2 SO 4(конц. ) = Mo. O 3 + 3 SO 2 + 3 H 2 O W + 2 HNO 3 + 8 HF = H 2[WF 8] + 2 NO + 4 H 2 O Э + 2 Na. OH + 3 Na. NO 3 = Na 2 ЭO 4 + 3 Na. NO 2 + H 2 O Э = Mo, W
4 d- и 5 d-Элементы реагируют с концентрированными кислотами- окислителями или щелочами в присутствии окислителей, образуя анионные соли с высокими степенями окисления металлов При нагревании Mo + 3 H 2 SO 4(конц. ) = Mo. O 3 + 3 SO 2 + 3 H 2 O W + 2 HNO 3 + 8 HF = H 2[WF 8] + 2 NO + 4 H 2 O Э + 2 Na. OH + 3 Na. NO 3 = Na 2 ЭO 4 + 3 Na. NO 2 + H 2 O Э = Mo, W
 Низшие оксиды и гидроксиды MO, M 2 O 3, M(OH)2, M(OH)3 – слабые основания Zn. O, Cr 2 O 3, Fe 2 O 3 – амфотерные оксиды Zn(OH)2, Cr(OH)3, Fe(OH)3 – амфотерные гидроксиды Все плохо растворяются в воде
Низшие оксиды и гидроксиды MO, M 2 O 3, M(OH)2, M(OH)3 – слабые основания Zn. O, Cr 2 O 3, Fe 2 O 3 – амфотерные оксиды Zn(OH)2, Cr(OH)3, Fe(OH)3 – амфотерные гидроксиды Все плохо растворяются в воде
 Оксиды и гидроксиды MO 2, M(OH)4 Mn. O 2 – амфотерный оксид, но инертен к действию кислот и оснований При сплавлении Mn. O 2 + Ca. O = Ca. O·n. Mn. O 2 (n = 0, 5; 1; 2; 3; 5) В концентрированной H 2 SO 4 3 Mn. SO 4 + 2 KMn. O 4 + 8 H 2 SO 4 = = 5 Mn(SO 4)2 + K 2 SO 4 + 8 H 2 O
Оксиды и гидроксиды MO 2, M(OH)4 Mn. O 2 – амфотерный оксид, но инертен к действию кислот и оснований При сплавлении Mn. O 2 + Ca. O = Ca. O·n. Mn. O 2 (n = 0, 5; 1; 2; 3; 5) В концентрированной H 2 SO 4 3 Mn. SO 4 + 2 KMn. O 4 + 8 H 2 SO 4 = = 5 Mn(SO 4)2 + K 2 SO 4 + 8 H 2 O
 Высшие оксиды и гидроксиды обладают типичными кислотными свойствами и напоминают соответствующие оксиды и гидроксиды элементов главных подгрупп Растворяются в воде V 2 O 5, Cr. O 3, Mn 2 O 7 V 2 O 5 + 3 H 2 O = 2 H 3 VO 4 Cr. O 3 + H 2 O = H 2 Cr. O 4 Mn 2 O 7 + H 2 O = 2 HMn. O 4 В горячей воде 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2
Высшие оксиды и гидроксиды обладают типичными кислотными свойствами и напоминают соответствующие оксиды и гидроксиды элементов главных подгрупп Растворяются в воде V 2 O 5, Cr. O 3, Mn 2 O 7 V 2 O 5 + 3 H 2 O = 2 H 3 VO 4 Cr. O 3 + H 2 O = H 2 Cr. O 4 Mn 2 O 7 + H 2 O = 2 HMn. O 4 В горячей воде 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2
 Окислительно-восстановительные свойства оксидов и гидроксидов Некоторые низшие оксиды и гидроксиды проявляют восстановительные свойства: Cr(OH)2, Mn. O, Mn(OH)2, Fe(OH)2 Высшие оксиды, гидроксиды и соли этих гидроксидов 3 d-элементов – сильные окислители: V 2 O 5, Cr. O 3, K 2 Cr. O 4, K 2 Cr 2 O 7, KMn. O 4, Na 2 Fe. O 4,
Окислительно-восстановительные свойства оксидов и гидроксидов Некоторые низшие оксиды и гидроксиды проявляют восстановительные свойства: Cr(OH)2, Mn. O, Mn(OH)2, Fe(OH)2 Высшие оксиды, гидроксиды и соли этих гидроксидов 3 d-элементов – сильные окислители: V 2 O 5, Cr. O 3, K 2 Cr. O 4, K 2 Cr 2 O 7, KMn. O 4, Na 2 Fe. O 4,
 Соли 3 d-элементов в низших степенях оксиления (I-III) гидролизуются в водных растворах. p. H < 7 Катионы металлов образуют в воде аквакомплексы
Соли 3 d-элементов в низших степенях оксиления (I-III) гидролизуются в водных растворах. p. H < 7 Катионы металлов образуют в воде аквакомплексы
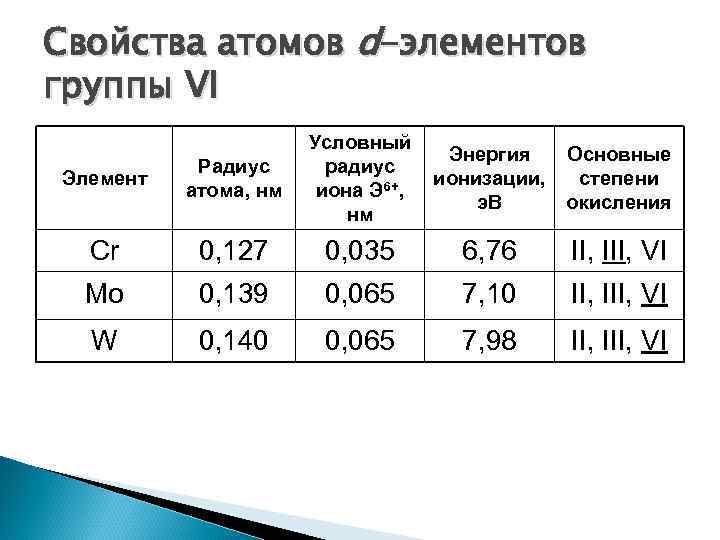 Свойства атомов d-элементов группы VI Элемент Радиус атома, нм Условный радиус иона Э 6+, нм Энергия ионизации, э. В Основные степени окисления Cr 0, 127 0, 035 6, 76 II, III, VI Mo 0, 139 0, 065 7, 10 II, III, VI W 0, 140 0, 065 7, 98 II, III, VI
Свойства атомов d-элементов группы VI Элемент Радиус атома, нм Условный радиус иона Э 6+, нм Энергия ионизации, э. В Основные степени окисления Cr 0, 127 0, 035 6, 76 II, III, VI Mo 0, 139 0, 065 7, 10 II, III, VI W 0, 140 0, 065 7, 98 II, III, VI
 Реакции с простыми веществами При нагревании 4 Cr + 3 O 2 = 2 Cr 2 O 3 2 Cr + 3 S = Cr 2 S 3 Cr + 2 F 2 = Cr. F 4 2 Cr + 3 Hlg 2 = 2 Cr. Hlg 3; Hlg = Cl, Br, I 2 Cr + N 2 = 2 Cr. N
Реакции с простыми веществами При нагревании 4 Cr + 3 O 2 = 2 Cr 2 O 3 2 Cr + 3 S = Cr 2 S 3 Cr + 2 F 2 = Cr. F 4 2 Cr + 3 Hlg 2 = 2 Cr. Hlg 3; Hlg = Cl, Br, I 2 Cr + N 2 = 2 Cr. N
 Реакции с кислотами Пассивируется на холоду HNO 3(разб. ), HNO 3(конц. ), «царской водкой» На холоду Cr + 2 HCl(разб. ) = Cr. Cl 2 + H 2 Cr + H 2 SO 4(разб. ) = Cr. SO 4 + H 2 При нагревании 2 Cr + 6 H 2 SO 4(конц. ) = = Cr 2(SO 4)3 + 3 SO 2 + 6 H 2 O Cr + 6 HNO 3(конц. ) = = Cr(NO 3)3 + 3 NO 2 + 6 H 2 O
Реакции с кислотами Пассивируется на холоду HNO 3(разб. ), HNO 3(конц. ), «царской водкой» На холоду Cr + 2 HCl(разб. ) = Cr. Cl 2 + H 2 Cr + H 2 SO 4(разб. ) = Cr. SO 4 + H 2 При нагревании 2 Cr + 6 H 2 SO 4(конц. ) = = Cr 2(SO 4)3 + 3 SO 2 + 6 H 2 O Cr + 6 HNO 3(конц. ) = = Cr(NO 3)3 + 3 NO 2 + 6 H 2 O
 Cr, Mo, W При нагревании Mo + 3 H 2 SO 4(конц. ) = Mo. O 3 + 3 SO 2 + 3 H 2 O W + 2 HNO 3 + 8 HF = H 2[WF 8] + 2 NO + 4 H 2 O Э + 2 Na. OH + 3 Na. NO 3 = = Na 2 ЭO 4 + 3 Na. NO 2 + H 2 O Э = Mo, W
Cr, Mo, W При нагревании Mo + 3 H 2 SO 4(конц. ) = Mo. O 3 + 3 SO 2 + 3 H 2 O W + 2 HNO 3 + 8 HF = H 2[WF 8] + 2 NO + 4 H 2 O Э + 2 Na. OH + 3 Na. NO 3 = = Na 2 ЭO 4 + 3 Na. NO 2 + H 2 O Э = Mo, W
 Соединения хрома(II) Cr + 2 HCl = Cr. Cl 2 + H 2 (в токе H 2) 2 Cr. Cl 3 + H 2 = 2 Cr. Cl 2 + 2 HCl 2 Cr. Cl 3 + Zn = 2 Cr. Cl 2 + Zn. Cl 2 Cr. Cl 2 + H 2 O = Cr. OHCl + HCl Cr. Cl 2 + 2 Na. OH = Cr(OH)2↓ + 2 Na. Cl Медленно 2 Cr. IICl 2 + 2 H 2 O = 2 Cr. IIIOHCl 2 + H 2
Соединения хрома(II) Cr + 2 HCl = Cr. Cl 2 + H 2 (в токе H 2) 2 Cr. Cl 3 + H 2 = 2 Cr. Cl 2 + 2 HCl 2 Cr. Cl 3 + Zn = 2 Cr. Cl 2 + Zn. Cl 2 Cr. Cl 2 + H 2 O = Cr. OHCl + HCl Cr. Cl 2 + 2 Na. OH = Cr(OH)2↓ + 2 Na. Cl Медленно 2 Cr. IICl 2 + 2 H 2 O = 2 Cr. IIIOHCl 2 + H 2
 Соединения хрома(III) Оксид хрома(III), Cr 2 O 3, — тугоплавкое тёмнозеленое вещество, нерастворимое в воде, кислотах и щелочах, обладает амфотерными свойствами. Кислотные свойства (при сплавлении) Cr 2 O 3 + Na 2 CO 3 = 2 Na. Cr. O 2 + CO 2 Основные свойства (при сплавлении) Cr 2 O 3 + 3 K 2 S 2 O 7 = Cr 2(SO 4)3 + 3 K 2 SO 4 Восстановительные свойства (при сплавлении) Cr 2 O 3 + 4 Na. OH + KCl. O 3 = = 2 Na 2 Cr. O 4 + KCl + 2 H 2 O
Соединения хрома(III) Оксид хрома(III), Cr 2 O 3, — тугоплавкое тёмнозеленое вещество, нерастворимое в воде, кислотах и щелочах, обладает амфотерными свойствами. Кислотные свойства (при сплавлении) Cr 2 O 3 + Na 2 CO 3 = 2 Na. Cr. O 2 + CO 2 Основные свойства (при сплавлении) Cr 2 O 3 + 3 K 2 S 2 O 7 = Cr 2(SO 4)3 + 3 K 2 SO 4 Восстановительные свойства (при сплавлении) Cr 2 O 3 + 4 Na. OH + KCl. O 3 = = 2 Na 2 Cr. O 4 + KCl + 2 H 2 O
 Гидроксид хрома(III) Получение Cr. Cl 3 + 3 Na. OH = Cr(OH)3↓ + 3 Na. Cl Гидроксид хрома(III), Cr(OH)3, труднорастворим в воде, амфотерен с преобладанием основных свойств Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + 3 Na. OH = Na 3[Cr(OH)6]
Гидроксид хрома(III) Получение Cr. Cl 3 + 3 Na. OH = Cr(OH)3↓ + 3 Na. Cl Гидроксид хрома(III), Cr(OH)3, труднорастворим в воде, амфотерен с преобладанием основных свойств Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + 3 Na. OH = Na 3[Cr(OH)6]
 Соли хрома(III) Гидролиз Катионые соли – частичный гидролиз Cr 3+ + H 2 O = Cr. OH 2+ + H+ Анионые соли – полный гидролиз [Cr(OH)6]3– = Cr(OH)3 + 3 OH– Необратимый гидролиз 2 Cr 3+ + 3 CO 32 - + 3 H 2 O = 2 Cr(OH)3 + 3 CO 2 2 Cr 3+ + 3 S 2– + 6 H 2 O = 2 Cr(OH)3 + 3 H 2 S Окисление 2 Cr. Cl 3 + 10 Na. OH + 3 H 2 O 2 = = 2 Na 2 Cr. O 4 + 8 H 2 O + 6 Na. Cl
Соли хрома(III) Гидролиз Катионые соли – частичный гидролиз Cr 3+ + H 2 O = Cr. OH 2+ + H+ Анионые соли – полный гидролиз [Cr(OH)6]3– = Cr(OH)3 + 3 OH– Необратимый гидролиз 2 Cr 3+ + 3 CO 32 - + 3 H 2 O = 2 Cr(OH)3 + 3 CO 2 2 Cr 3+ + 3 S 2– + 6 H 2 O = 2 Cr(OH)3 + 3 H 2 S Окисление 2 Cr. Cl 3 + 10 Na. OH + 3 H 2 O 2 = = 2 Na 2 Cr. O 4 + 8 H 2 O + 6 Na. Cl
 Комплексные соединения хрома(III) Координационное число 6: Аквакомплексы (переходят друг в друга при нагревании: [Cr(H 2 O)6]Cl 3 – серо-голубой, [Cr(H 2 O)5 Cl]Cl 2 – светло-зелёный, [Cr(H 2 O)4 Cl 2]Cl – тёмно-зелёный Гидроксидокомплексы при p. H > 7: [Cr(OH)6]3– - зелёный двойные соли (хромовые квасцы) : Ме. Cr(SO 4)2· 12 H 2 O; Me = K, NH 4
Комплексные соединения хрома(III) Координационное число 6: Аквакомплексы (переходят друг в друга при нагревании: [Cr(H 2 O)6]Cl 3 – серо-голубой, [Cr(H 2 O)5 Cl]Cl 2 – светло-зелёный, [Cr(H 2 O)4 Cl 2]Cl – тёмно-зелёный Гидроксидокомплексы при p. H > 7: [Cr(OH)6]3– - зелёный двойные соли (хромовые квасцы) : Ме. Cr(SO 4)2· 12 H 2 O; Me = K, NH 4
 Соединения хрома(VI) Оксид хрома(VI), хромовый ангидрид, Cr. O 3 + H 2 O = H 2 Cr. O 4 Хромовая кислота, H 2 Cr. O 4 – сильная кислота, жёлтая, полимеризуется в кислой среде 2 H 2 Cr. O 4 = H 2 O + H 2 Cr 2 O 7 — дихромовая кислота, оранжевая H 2 Cr 2 O 7 + H 2 Cr. O 4 = H 2 O + H 2 Cr 3 O 10 — трихромовая кислота H 2 Cr 3 O 10 + H 2 Cr. O 4 = H 2 O + H 2 Cr 4 O 10 — тетрахромовая кислота, коричневая H 2 O·n. ЭO 3; Э = Cr, Mo, W
Соединения хрома(VI) Оксид хрома(VI), хромовый ангидрид, Cr. O 3 + H 2 O = H 2 Cr. O 4 Хромовая кислота, H 2 Cr. O 4 – сильная кислота, жёлтая, полимеризуется в кислой среде 2 H 2 Cr. O 4 = H 2 O + H 2 Cr 2 O 7 — дихромовая кислота, оранжевая H 2 Cr 2 O 7 + H 2 Cr. O 4 = H 2 O + H 2 Cr 3 O 10 — трихромовая кислота H 2 Cr 3 O 10 + H 2 Cr. O 4 = H 2 O + H 2 Cr 4 O 10 — тетрахромовая кислота, коричневая H 2 O·n. ЭO 3; Э = Cr, Mo, W
 Хроматы и дихроматы 2 Cr. O 42 - + 2 H+ = Cr 2 O 72 - + H 2 O Cr 2 O 72 - + 2 OH– = 2 Cr. O 42 - + H 2 O Сильные окислители Cr 2 O 72 - + 14 H+ + 6ē = 2 Cr 3+ + 7 H 2 O; φ° = 1, 33 В K 2 Cr 2 O 7 + 3 H 2 S + 4 H 2 SO 4 = = 3 S + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O K 2 Cr 2 O 7 + 3 H 2 S + H 2 O = 3 S + 2 Cr(OH)3 + 2 KOH K 2 Cr 2 O 7 + H 2 SO 4(конц. ) – хромовая смесь
Хроматы и дихроматы 2 Cr. O 42 - + 2 H+ = Cr 2 O 72 - + H 2 O Cr 2 O 72 - + 2 OH– = 2 Cr. O 42 - + H 2 O Сильные окислители Cr 2 O 72 - + 14 H+ + 6ē = 2 Cr 3+ + 7 H 2 O; φ° = 1, 33 В K 2 Cr 2 O 7 + 3 H 2 S + 4 H 2 SO 4 = = 3 S + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O K 2 Cr 2 O 7 + 3 H 2 S + H 2 O = 3 S + 2 Cr(OH)3 + 2 KOH K 2 Cr 2 O 7 + H 2 SO 4(конц. ) – хромовая смесь
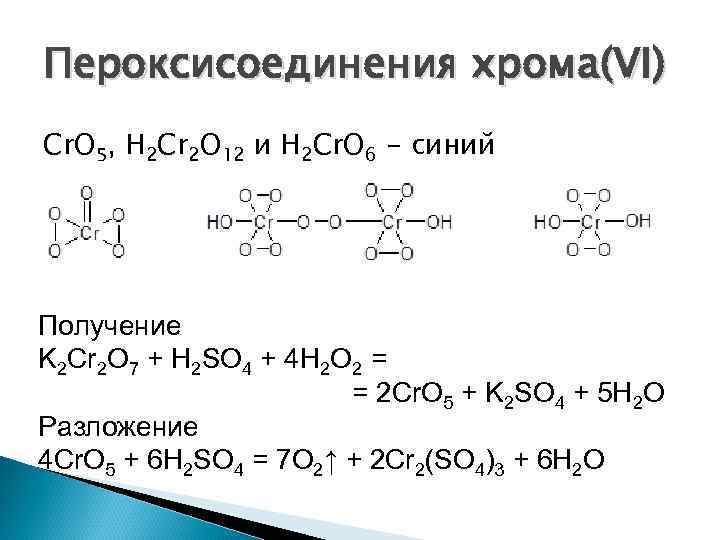 Пероксисоединения хрома(VI) Cr. O 5, H 2 Cr 2 O 12 и H 2 Cr. O 6 - синий Получение K 2 Cr 2 O 7 + H 2 SO 4 + 4 H 2 O 2 = = 2 Cr. O 5 + K 2 SO 4 + 5 H 2 O Разложение 4 Cr. O 5 + 6 H 2 SO 4 = 7 O 2↑ + 2 Cr 2(SO 4)3 + 6 H 2 O
Пероксисоединения хрома(VI) Cr. O 5, H 2 Cr 2 O 12 и H 2 Cr. O 6 - синий Получение K 2 Cr 2 O 7 + H 2 SO 4 + 4 H 2 O 2 = = 2 Cr. O 5 + K 2 SO 4 + 5 H 2 O Разложение 4 Cr. O 5 + 6 H 2 SO 4 = 7 O 2↑ + 2 Cr 2(SO 4)3 + 6 H 2 O
 Галогениды и оксидогалогениды ЭO 2 Hlg 2, ЭОHlg 4, ЭHlg 6; Э = Cr, Mo, W Гидролиз ЭO 2 Hlg 2 + 2 H 2 O = H 2 ЭO 4 + 2 HHlg Окислительные свойства 2 Cr. O 2 Cl 2 + 8 HCl = 3 Cl 2 + 2 Cr. Cl 3 + 4 H 2 O
Галогениды и оксидогалогениды ЭO 2 Hlg 2, ЭОHlg 4, ЭHlg 6; Э = Cr, Mo, W Гидролиз ЭO 2 Hlg 2 + 2 H 2 O = H 2 ЭO 4 + 2 HHlg Окислительные свойства 2 Cr. O 2 Cl 2 + 8 HCl = 3 Cl 2 + 2 Cr. Cl 3 + 4 H 2 O
 Марганец φ°(Mn 2+/Mn) = – 1, 18 В Mn + 2 H 2 O = Mn(OH)2 + H 2↑ Mn + 4 HNO 3 = Mn(NO 3)2 + 2 NO 2↑ + 2 H 2 O Э + 7 HNO 3 = HЭO 4 + 7 NO 2↑ + 3 H 2 O; Э = Tc, Re
Марганец φ°(Mn 2+/Mn) = – 1, 18 В Mn + 2 H 2 O = Mn(OH)2 + H 2↑ Mn + 4 HNO 3 = Mn(NO 3)2 + 2 NO 2↑ + 2 H 2 O Э + 7 HNO 3 = HЭO 4 + 7 NO 2↑ + 3 H 2 O; Э = Tc, Re
 Соединения марганца(II) Mn. O, Mn(OH)2 и соли катионного типа При нагревании Mn. CO 3 = Mn. O + CO 2 Mn. O + H 2 O = Mn(OH)2↓ Mn. SO 4 + 2 Na. OH = Mn(OH)2↓ + Na 2 SO 4 2 Mn. SO 4 + 2 H 2 O = (Mn. OH)2 SO 4 + H 2 SO 4
Соединения марганца(II) Mn. O, Mn(OH)2 и соли катионного типа При нагревании Mn. CO 3 = Mn. O + CO 2 Mn. O + H 2 O = Mn(OH)2↓ Mn. SO 4 + 2 Na. OH = Mn(OH)2↓ + Na 2 SO 4 2 Mn. SO 4 + 2 H 2 O = (Mn. OH)2 SO 4 + H 2 SO 4
 Соединения марганца(II) Восстановительные свойства 2 Mn(OH)2 + O 2 = 2 Mn. O 2 + 2 H 2 O 2 Mn(NO 3)2 + 5 Na. Bi. O 3 + 16 HNO 3 = = 2 HMn. O 4 + 5 Bi(NO 3)3 + 5 Na. NO 3 + 7 H 2 O 3 Mn. SO 4 + 2 KMn. O 4 + 2 H 2 O = = 5 Mn. O 2 + K 2 SO 4 + 2 H 2 SO 4
Соединения марганца(II) Восстановительные свойства 2 Mn(OH)2 + O 2 = 2 Mn. O 2 + 2 H 2 O 2 Mn(NO 3)2 + 5 Na. Bi. O 3 + 16 HNO 3 = = 2 HMn. O 4 + 5 Bi(NO 3)3 + 5 Na. NO 3 + 7 H 2 O 3 Mn. SO 4 + 2 KMn. O 4 + 2 H 2 O = = 5 Mn. O 2 + K 2 SO 4 + 2 H 2 SO 4
 Соединения марганца(III) Mn 2 O 3, слабое основание Mn(OH)3 и соли Соединения марганца(III) легко диспропорционируют 2 Mn. Cl 3 + 2 H 2 O = Mn. Cl 2 + Mn. O 2 + 4 HCl
Соединения марганца(III) Mn 2 O 3, слабое основание Mn(OH)3 и соли Соединения марганца(III) легко диспропорционируют 2 Mn. Cl 3 + 2 H 2 O = Mn. Cl 2 + Mn. O 2 + 4 HCl
 Соединения марганца(IV) Mn. O 2 – чёрно-бурый, Mn(SO 4)2, Na 2 Mn. O 3 (манганит натрия Окислительные свойства Mn. O 2 + 4 H+ + 2ē = Mn 2+ + 2 H 2 O; φ° = 1, 23 В Mn. O 2 + 4 HCl = Mn. Cl 2 + Cl 2↑ + 2 H 2 O Mn. O 2 + 2 KBr + H 2 SO 4 = Mn. SO 4 + Br 2 + K 2 SO 4 + H 2 O Восстановительные свойства Mn. O 2 3 Mn. O 2 + 6 KOH + KCl. O 3 = 3 K 2 Mn. O 4 + 3 H 2 O + KCl
Соединения марганца(IV) Mn. O 2 – чёрно-бурый, Mn(SO 4)2, Na 2 Mn. O 3 (манганит натрия Окислительные свойства Mn. O 2 + 4 H+ + 2ē = Mn 2+ + 2 H 2 O; φ° = 1, 23 В Mn. O 2 + 4 HCl = Mn. Cl 2 + Cl 2↑ + 2 H 2 O Mn. O 2 + 2 KBr + H 2 SO 4 = Mn. SO 4 + Br 2 + K 2 SO 4 + H 2 O Восстановительные свойства Mn. O 2 3 Mn. O 2 + 6 KOH + KCl. O 3 = 3 K 2 Mn. O 4 + 3 H 2 O + KCl
 Соединения марганца(IV) Гидролиз Mn(SO 4)2 + 2 H 2 O = Mn. O 2 + 2 H 2 SO 4 При сплавлении Mn. O 2 + 2 KOH = K 2 Mn. O 3 + H 2 O Гидролиз K 2 Mn. O 3 + H 2 O = Mn. O 2 + 2 KOH
Соединения марганца(IV) Гидролиз Mn(SO 4)2 + 2 H 2 O = Mn. O 2 + 2 H 2 SO 4 При сплавлении Mn. O 2 + 2 KOH = K 2 Mn. O 3 + H 2 O Гидролиз K 2 Mn. O 3 + H 2 O = Mn. O 2 + 2 KOH
 Соединения марганца(VI) Соли марганцовистой кислоты (H 2 Mn. O 4) – манганаты Получение При сплавлении 2 KMn. O 4 + 2 KOH + KNO 2 = 2 K 2 Mn. O 4 + KNO 3 + H 2 O Mn. SO 4 + 4 KOH + 2 KNO 3 = = K 2 Mn. O 4 + 2 KNO 2 + K 2 SO 4 + 2 H 2 O Mn. SO 4 + 2 Br 2 + 8 Na. OH = = Na 2 Mn. O 4 + 4 Na. Br + Na 2 SO 4 + 4 H 2 O Диспропорционирование 3 K 2 Mn. O 4 + 2 H 2 O = Mn. O 2 + 2 KMn. O 4 + 4 KOH
Соединения марганца(VI) Соли марганцовистой кислоты (H 2 Mn. O 4) – манганаты Получение При сплавлении 2 KMn. O 4 + 2 KOH + KNO 2 = 2 K 2 Mn. O 4 + KNO 3 + H 2 O Mn. SO 4 + 4 KOH + 2 KNO 3 = = K 2 Mn. O 4 + 2 KNO 2 + K 2 SO 4 + 2 H 2 O Mn. SO 4 + 2 Br 2 + 8 Na. OH = = Na 2 Mn. O 4 + 4 Na. Br + Na 2 SO 4 + 4 H 2 O Диспропорционирование 3 K 2 Mn. O 4 + 2 H 2 O = Mn. O 2 + 2 KMn. O 4 + 4 KOH
 Соединения марганца(VI) Окислительные свойства K 2 Mn. O 4 + 2 K 2 SO 3 + 2 H 2 SO 4 = Mn. SO 4 + 3 K 2 SO 4 + 2 H 2 O K 2 Mn. O 4 + K 2 SO 3 + H 2 O = Mn. O 2 + K 2 SO 4 + 2 KOH Восстановительные свойства 2 K 2 Mn. O 4 + Cl 2 = 2 KMn. O 4 + 2 KCl Разложение при нагревании (500 °C) 2 K 2 Mn. O 4 = 2 K 2 Mn. O 3 + O 2
Соединения марганца(VI) Окислительные свойства K 2 Mn. O 4 + 2 K 2 SO 3 + 2 H 2 SO 4 = Mn. SO 4 + 3 K 2 SO 4 + 2 H 2 O K 2 Mn. O 4 + K 2 SO 3 + H 2 O = Mn. O 2 + K 2 SO 4 + 2 KOH Восстановительные свойства 2 K 2 Mn. O 4 + Cl 2 = 2 KMn. O 4 + 2 KCl Разложение при нагревании (500 °C) 2 K 2 Mn. O 4 = 2 K 2 Mn. O 3 + O 2
 Соединения марганца(VII) Mn 2 O 7, HMn. O 4 и её соли перманганаты Получение 2 Mn. SO 4 + 5 Na. Bi. O 3 + 16 HNO 3 = = 2 HMn. O 4 + 5 Bi(NO 3)3 + Na. NO 3 + 2 Na 2 SO 4 + 7 H 2 O 2 Mn. SO 4 + 5 K 2 S 2 O 8 + 8 H 2 O = 2 HMn. O 4 + 5 K 2 SO 4 + 7 H 2 SO 4 2 KMn. O 4 + H 2 SO 4(конц. ) = Mn 2 O 7 + K 2 SO 4 + H 2 O Сильные окислители, особенно в кислой среде Mn. O 4 - + 2 H 2 O + 3ē = Mn. O 2 + 4 OH–; φ° = +0, 60 В; Mn. O 4 - + ē = Mn. O 42 -; φ° = +0, 56 В; Mn. O 4 - + 8 H+ + 5 ē = Mn 2+ + 4 H 2 O; φ° = +1, 51 В
Соединения марганца(VII) Mn 2 O 7, HMn. O 4 и её соли перманганаты Получение 2 Mn. SO 4 + 5 Na. Bi. O 3 + 16 HNO 3 = = 2 HMn. O 4 + 5 Bi(NO 3)3 + Na. NO 3 + 2 Na 2 SO 4 + 7 H 2 O 2 Mn. SO 4 + 5 K 2 S 2 O 8 + 8 H 2 O = 2 HMn. O 4 + 5 K 2 SO 4 + 7 H 2 SO 4 2 KMn. O 4 + H 2 SO 4(конц. ) = Mn 2 O 7 + K 2 SO 4 + H 2 O Сильные окислители, особенно в кислой среде Mn. O 4 - + 2 H 2 O + 3ē = Mn. O 2 + 4 OH–; φ° = +0, 60 В; Mn. O 4 - + ē = Mn. O 42 -; φ° = +0, 56 В; Mn. O 4 - + 8 H+ + 5 ē = Mn 2+ + 4 H 2 O; φ° = +1, 51 В
 Соединения марганца(VII) Окислительные свойства 2 KMn. O 4 + 6 KI + 4 H 2 O = 2 Mn. O 2 + 3 I 2 + 8 KOH 6 KMn. O 4 + KI + 6 KOH = 6 K 2 Mn. O 4 + KIO 3 + 3 H 2 O 2 KMn. O 4 + 10 KI + 8 H 2 SO 4 = = 2 Mn. SO 4 + 5 I 2 + 6 K 2 SO 4 + 8 H 2 O Термическое разложение (выше 250 °C) 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 Водные растворы неустойчивы 4 KMn. O 4 + 2 H 2 O = 4 Mn. O 2 + 4 KOH + 3 O 2 Разложение Mn 2 O 7 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2
Соединения марганца(VII) Окислительные свойства 2 KMn. O 4 + 6 KI + 4 H 2 O = 2 Mn. O 2 + 3 I 2 + 8 KOH 6 KMn. O 4 + KI + 6 KOH = 6 K 2 Mn. O 4 + KIO 3 + 3 H 2 O 2 KMn. O 4 + 10 KI + 8 H 2 SO 4 = = 2 Mn. SO 4 + 5 I 2 + 6 K 2 SO 4 + 8 H 2 O Термическое разложение (выше 250 °C) 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 Водные растворы неустойчивы 4 KMn. O 4 + 2 H 2 O = 4 Mn. O 2 + 4 KOH + 3 O 2 Разложение Mn 2 O 7 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2
 Кислотно-основные свойства гидроксидов марганца Mn(OH)2, Mn(OH)3, Mn(OH)4, (H 2 Mn. O 4), HMn. O 4 Основные свойства ослабевают Кислотные свойства усиливаются
Кислотно-основные свойства гидроксидов марганца Mn(OH)2, Mn(OH)3, Mn(OH)4, (H 2 Mn. O 4), HMn. O 4 Основные свойства ослабевают Кислотные свойства усиливаются
 d-Элементы группы VIII Триада железа: Fe, Ru, Os – возможны высокие степени окисления, устойчивые оксиды, неустойчивые сульфиды Триада кобальта: Co, Rh, Ir Триада никеля: Ni, Pd, Pt – низкие степени окисления, устойчивые сульфиды, неустойчивые оксиды
d-Элементы группы VIII Триада железа: Fe, Ru, Os – возможны высокие степени окисления, устойчивые оксиды, неустойчивые сульфиды Триада кобальта: Co, Rh, Ir Триада никеля: Ni, Pd, Pt – низкие степени окисления, устойчивые сульфиды, неустойчивые оксиды
 d-Элементы группы VIII Семейство железа: Fe, Co, Ni Семейство платиновых металлов: Ru, Rh, Pd, Os, Ir, Pt
d-Элементы группы VIII Семейство железа: Fe, Co, Ni Семейство платиновых металлов: Ru, Rh, Pd, Os, Ir, Pt
 Семейство железа φ°(Fe 2+/Fe) = – 0, 44 В; φ°(Fe 3+/Fe) = – 0, 04 В; φ°(Co 2+/Co) = – 0, 28 В; φ°(Ni 2+/Ni) = – 0, 25 В 4 Fe + 2 H 2 O + 3 O 2 = 2 Fe 2 O 3·H 2 O или (Fe. O(OH))2 Co и Ni с водой не реагируют 2 Fe + 3 O 2 = Fe 2 O 3 6 Fe 2 O 3 = 4 Fe 3 O 4 + O 2 (при 400 °C) 2 Fe 3 O 4 = 6 Fe. O + O 2 (при 575 °C)
Семейство железа φ°(Fe 2+/Fe) = – 0, 44 В; φ°(Fe 3+/Fe) = – 0, 04 В; φ°(Co 2+/Co) = – 0, 28 В; φ°(Ni 2+/Ni) = – 0, 25 В 4 Fe + 2 H 2 O + 3 O 2 = 2 Fe 2 O 3·H 2 O или (Fe. O(OH))2 Co и Ni с водой не реагируют 2 Fe + 3 O 2 = Fe 2 O 3 6 Fe 2 O 3 = 4 Fe 3 O 4 + O 2 (при 400 °C) 2 Fe 3 O 4 = 6 Fe. O + O 2 (при 575 °C)
 Семейство железа 6 Co + 4 O 2 = 2 Co 3 O 4 2 Ni + O 2 = 2 Ni. O При нагревании Fe + S = Fe. S Co + S = Co. S Ni + S = Ni. S
Семейство железа 6 Co + 4 O 2 = 2 Co 3 O 4 2 Ni + O 2 = 2 Ni. O При нагревании Fe + S = Fe. S Co + S = Co. S Ni + S = Ni. S
 Семейство железа Не реагируют со щелочами Реакции с кислотами Э + НСl = ЭCl 2 + H 2; Э = Fe, Co, Ni При нагревании Co + 2 H 2 SO 4(конц. ) = Co. SO 4 + SO 2 + 2 H 2 O Fe + 6 HNO 3(конц. ) = Fe(NO 3)3 + 3 NO 2 + 3 H 2 O 4 Fe + 10 HNO 3(оч. разб. ) = = 4 Fe(NO 3)2 + NH 4 NO 3 + 3 H 2 O
Семейство железа Не реагируют со щелочами Реакции с кислотами Э + НСl = ЭCl 2 + H 2; Э = Fe, Co, Ni При нагревании Co + 2 H 2 SO 4(конц. ) = Co. SO 4 + SO 2 + 2 H 2 O Fe + 6 HNO 3(конц. ) = Fe(NO 3)3 + 3 NO 2 + 3 H 2 O 4 Fe + 10 HNO 3(оч. разб. ) = = 4 Fe(NO 3)2 + NH 4 NO 3 + 3 H 2 O
 Семейство железа Fe. SO 4 + 2 Na. OH = Fe(OH)2↓ + Na 2 SO 4 Fe. Cl 3 + 3 Na. OH = Fe(OH)3↓ + 2 Na. Cl 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3 Fe. O и Fe(OH)2 – основные Fe(OH)2 + H 2 SO 4 = Fe. SO 4 + 2 H 2 O Fe 2 O 3 и Fe(OH)3 – амфотерные 2 Fe(OH)3 + 3 H 2 SO 4 = Fe 2(SO 4)3 + 3 H 2 O При сплавлении Fe 2 O 3 + Na 2 CO 3 = 2 Na. Fe. O 2 + CO 2
Семейство железа Fe. SO 4 + 2 Na. OH = Fe(OH)2↓ + Na 2 SO 4 Fe. Cl 3 + 3 Na. OH = Fe(OH)3↓ + 2 Na. Cl 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3 Fe. O и Fe(OH)2 – основные Fe(OH)2 + H 2 SO 4 = Fe. SO 4 + 2 H 2 O Fe 2 O 3 и Fe(OH)3 – амфотерные 2 Fe(OH)3 + 3 H 2 SO 4 = Fe 2(SO 4)3 + 3 H 2 O При сплавлении Fe 2 O 3 + Na 2 CO 3 = 2 Na. Fe. O 2 + CO 2
 Семейство железа Fe(OH)2, Co(OH)2, Ni(OH)2 Устойчивость возрастает Восстановительные свойства ослабевают 2 Ni(OH)2 + Na. Cl. O + H 2 O = 2 Ni(OH)3 + Na. Cl
Семейство железа Fe(OH)2, Co(OH)2, Ni(OH)2 Устойчивость возрастает Восстановительные свойства ослабевают 2 Ni(OH)2 + Na. Cl. O + H 2 O = 2 Ni(OH)3 + Na. Cl
 Семейство железа Fe(OH)3, Co(OH)3, Ni(OH)3 Устойчивость снижается Окислительные свойства возрастают 2 Ni(OH)3 + 6 HCl = 2 Ni. Cl 2 + 6 H 2 O 4 Ni(OH)3 + 4 H 2 SO 4 = 4 Ni. SO 4 + O 2 + 10 H 2 O Fe(OH)3 + 3 HCl = Fe. Cl 3 + 3 H 2 O
Семейство железа Fe(OH)3, Co(OH)3, Ni(OH)3 Устойчивость снижается Окислительные свойства возрастают 2 Ni(OH)3 + 6 HCl = 2 Ni. Cl 2 + 6 H 2 O 4 Ni(OH)3 + 4 H 2 SO 4 = 4 Ni. SO 4 + O 2 + 10 H 2 O Fe(OH)3 + 3 HCl = Fe. Cl 3 + 3 H 2 O
 Ферраты H 2 Fe. O 4 – железная кислота 2 Fe(OH)3 + 10 KOH + 3 Br 2 = = 2 K 2 Fe. O 4 + 6 KBr + 8 H 2 O Fe 2 O 3 + 3 Ba. O 2 = 2 Ba. Fe. O 4 + Ba. O Ферраты – сильные окислители Fe. O 42 - + 8 H+ + 3ē = Fe 3+ + 4 H 2 O; φ° = +1, 7 В 2 K 2 Fe. O 4 + 2 NH 3 + 2 H 2 O = 4 KOH +N 2 + 2 Fe(OH)3 4 K 2 Fe. O 4 + 10 H 2 O = 8 KOH + 4 Fe(OH)3 + 3 O 2
Ферраты H 2 Fe. O 4 – железная кислота 2 Fe(OH)3 + 10 KOH + 3 Br 2 = = 2 K 2 Fe. O 4 + 6 KBr + 8 H 2 O Fe 2 O 3 + 3 Ba. O 2 = 2 Ba. Fe. O 4 + Ba. O Ферраты – сильные окислители Fe. O 42 - + 8 H+ + 3ē = Fe 3+ + 4 H 2 O; φ° = +1, 7 В 2 K 2 Fe. O 4 + 2 NH 3 + 2 H 2 O = 4 KOH +N 2 + 2 Fe(OH)3 4 K 2 Fe. O 4 + 10 H 2 O = 8 KOH + 4 Fe(OH)3 + 3 O 2
![Комплексные соединения K 4[Fe(CN)6] - гексацианидоферрат(II) калия, жёлтая кровяная соль K 3[Fe(CN)6] - гексацианидоферрат(III) Комплексные соединения K 4[Fe(CN)6] - гексацианидоферрат(II) калия, жёлтая кровяная соль K 3[Fe(CN)6] - гексацианидоферрат(III)](https://present5.com/presentation/72381937_151120358/image-51.jpg) Комплексные соединения K 4[Fe(CN)6] - гексацианидоферрат(II) калия, жёлтая кровяная соль K 3[Fe(CN)6] - гексацианидоферрат(III) калия, красная кровяная соль Fe. Cl 3 + K 4[Fe(CN)6] = = KFe[Fe(CN)6] (берлинская лазурь) + 3 KCl Fe. Cl 2 + K 3[Fe(CN)6] = = KFe[Fe(CN)6] (турнбулева синь) + 2 KCl W + 6 K 3[Fe(CN)6] + 8 KOH = = 6 K 4[Fe(CN)6] + K 2 WO 4 + 4 H 2 O
Комплексные соединения K 4[Fe(CN)6] - гексацианидоферрат(II) калия, жёлтая кровяная соль K 3[Fe(CN)6] - гексацианидоферрат(III) калия, красная кровяная соль Fe. Cl 3 + K 4[Fe(CN)6] = = KFe[Fe(CN)6] (берлинская лазурь) + 3 KCl Fe. Cl 2 + K 3[Fe(CN)6] = = KFe[Fe(CN)6] (турнбулева синь) + 2 KCl W + 6 K 3[Fe(CN)6] + 8 KOH = = 6 K 4[Fe(CN)6] + K 2 WO 4 + 4 H 2 O
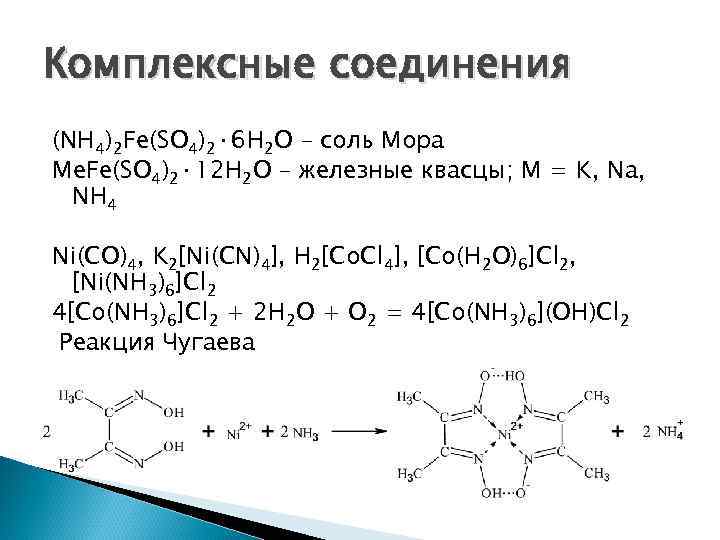 Комплексные соединения (NH 4)2 Fe(SO 4)2· 6 H 2 O – соль Мора Me. Fe(SO 4)2· 12 H 2 O – железные квасцы; M = K, Na, NH 4 Ni(CO)4, K 2[Ni(CN)4], H 2[Co. Cl 4], [Co(H 2 O)6]Cl 2, [Ni(NH 3)6]Cl 2 4[Co(NH 3)6]Сl 2 + 2 H 2 O + O 2 = 4[Co(NH 3)6](ОН)Cl 2 Реакция Чугаева
Комплексные соединения (NH 4)2 Fe(SO 4)2· 6 H 2 O – соль Мора Me. Fe(SO 4)2· 12 H 2 O – железные квасцы; M = K, Na, NH 4 Ni(CO)4, K 2[Ni(CN)4], H 2[Co. Cl 4], [Co(H 2 O)6]Cl 2, [Ni(NH 3)6]Cl 2 4[Co(NH 3)6]Сl 2 + 2 H 2 O + O 2 = 4[Co(NH 3)6](ОН)Cl 2 Реакция Чугаева
 Cu, Ag, Au φ°(Cu 2+/Cu) = +0, 34 В; φ°(Cu+/Cu) = +0, 52 В; φ°(Ag+/Ag) = +0, 80 В; φ°(Au 3+/Au) = +1, 45 В [Cu(CN)2]– + ē = Cu + 2 CN–; φ° = – 0, 43 В 4 Cu + O 2 = 2 Cu 2 O 2 Cu + O 2 = 2 Cu. O 2 Cu + O 2 + H 2 O + CO 2 = (Cu. OH)2 CO 3
Cu, Ag, Au φ°(Cu 2+/Cu) = +0, 34 В; φ°(Cu+/Cu) = +0, 52 В; φ°(Ag+/Ag) = +0, 80 В; φ°(Au 3+/Au) = +1, 45 В [Cu(CN)2]– + ē = Cu + 2 CN–; φ° = – 0, 43 В 4 Cu + O 2 = 2 Cu 2 O 2 Cu + O 2 = 2 Cu. O 2 Cu + O 2 + H 2 O + CO 2 = (Cu. OH)2 CO 3
 Cu, Ag, Au 4 Au + O 2 + 8 KCN + 2 H 2 O = = 4 K[Au(CN)2] + 4 KOH 4 Ag + O 2 + 2 H 2 S = 2 Ag 2 S + 2 H 2 O При нагревании 2 Cu + S = Cu 2 S 2 Ag + S = Ag 2 S Cu + Cl 2 = Cu. Cl 2 2 Ag + Cl 2 = 2 Ag. Cl 2 Au + 3 Cl 2 = 2 Au. Cl 3
Cu, Ag, Au 4 Au + O 2 + 8 KCN + 2 H 2 O = = 4 K[Au(CN)2] + 4 KOH 4 Ag + O 2 + 2 H 2 S = 2 Ag 2 S + 2 H 2 O При нагревании 2 Cu + S = Cu 2 S 2 Ag + S = Ag 2 S Cu + Cl 2 = Cu. Cl 2 2 Ag + Cl 2 = 2 Ag. Cl 2 Au + 3 Cl 2 = 2 Au. Cl 3
 Cu, Ag, Au Cu + 4 HNO 3 = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O Ag + 2 HNO 3 = Ag. NO 3 + NO 2 + H 2 O Cu + 2 H 2 SO 4 = Cu. SO 4 + SO 2 + 2 H 2 O 2 Ag + 2 H 2 SO 4 = Ag 2 SO 4 + SO 2 + 2 H 2 O 2 Au + 6 H 2 Se. O 4 = = Au 2(Se. O 4)3 + 3 Se. O 2 + 6 H 2 O Au + HNO 3 + 4 HCl = H[Au. Cl 4] + NO + 2 H 2 O
Cu, Ag, Au Cu + 4 HNO 3 = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O Ag + 2 HNO 3 = Ag. NO 3 + NO 2 + H 2 O Cu + 2 H 2 SO 4 = Cu. SO 4 + SO 2 + 2 H 2 O 2 Ag + 2 H 2 SO 4 = Ag 2 SO 4 + SO 2 + 2 H 2 O 2 Au + 6 H 2 Se. O 4 = = Au 2(Se. O 4)3 + 3 Se. O 2 + 6 H 2 O Au + HNO 3 + 4 HCl = H[Au. Cl 4] + NO + 2 H 2 O
 Гидроксиды меди, серебра и золота Cu(OH)2 (синий) и Cu. OH (жёлтый) 2 Cu. SO 4 + H 2 CO + 5 Na. OH = = 2 Cu. OH + HCOONa + 2 Na 2 SO 4 + 2 H 2 O 2 Cu. OH = Cu 2 O + H 2 O Cu. SO 4 + 2 KOH = Cu(OH)2 + K 2 SO 4 [Cu(NH 3)4]SO 4 + 2 Na. OH = Cu(OH)2 + Na 2 SO 4 + 4 NH 3 Cu(OH)2 + 2 Na. OH(конц. ) = Na 2[Cu(OH)4] Cu(OH)2 + H 2 SO 4 = Cu. SO 4 + 2 H 2 O 2 Ag. NO 3 + 2 Na. OH = Ag 2 O + 2 Na. NO 3 + H 2 O
Гидроксиды меди, серебра и золота Cu(OH)2 (синий) и Cu. OH (жёлтый) 2 Cu. SO 4 + H 2 CO + 5 Na. OH = = 2 Cu. OH + HCOONa + 2 Na 2 SO 4 + 2 H 2 O 2 Cu. OH = Cu 2 O + H 2 O Cu. SO 4 + 2 KOH = Cu(OH)2 + K 2 SO 4 [Cu(NH 3)4]SO 4 + 2 Na. OH = Cu(OH)2 + Na 2 SO 4 + 4 NH 3 Cu(OH)2 + 2 Na. OH(конц. ) = Na 2[Cu(OH)4] Cu(OH)2 + H 2 SO 4 = Cu. SO 4 + 2 H 2 O 2 Ag. NO 3 + 2 Na. OH = Ag 2 O + 2 Na. NO 3 + H 2 O
 Гидроксиды меди, серебра и золота Au. Cl 3 + Na. OH = Au(OH)3 + 3 Na. Cl Au(OH)3 + Na. OH = Na[Au(OH)4] Au(OH)3 + 4 HCl = H[Au. Cl 4] + 3 H 2 O
Гидроксиды меди, серебра и золота Au. Cl 3 + Na. OH = Au(OH)3 + 3 Na. Cl Au(OH)3 + Na. OH = Na[Au(OH)4] Au(OH)3 + 4 HCl = H[Au. Cl 4] + 3 H 2 O
 Соли Cu 2+ + H 2 O = Cu. OH+ + H+ 2 Cu 2+ + 2 CO 32 - + H 2 O = (Cu. OH)2 CO 3 + CO 2 Cu. SO 4· 5 H 2 O - медный купорос (синий) [Cu(H 2 O)4]2+ Cu. Cl + 2 Na 2 S 2 O 3 = Na 3[Cu(S 2 O 3)2] + Na. Cl Cu. Cl + 2 NH 3 = [Cu(NH 3)2]Cl Cu. Cl + HCl = H[Cu. Cl 2] Cu. Cl + 2 KCN = K[Cu(CN)2] + KCl 4 Cu. I + 5 H 2 SO 4(гор. , конц. ) = = 4 Cu. SO 4 + 2 I 2 + H 2 S + 4 H 2 O
Соли Cu 2+ + H 2 O = Cu. OH+ + H+ 2 Cu 2+ + 2 CO 32 - + H 2 O = (Cu. OH)2 CO 3 + CO 2 Cu. SO 4· 5 H 2 O - медный купорос (синий) [Cu(H 2 O)4]2+ Cu. Cl + 2 Na 2 S 2 O 3 = Na 3[Cu(S 2 O 3)2] + Na. Cl Cu. Cl + 2 NH 3 = [Cu(NH 3)2]Cl Cu. Cl + HCl = H[Cu. Cl 2] Cu. Cl + 2 KCN = K[Cu(CN)2] + KCl 4 Cu. I + 5 H 2 SO 4(гор. , конц. ) = = 4 Cu. SO 4 + 2 I 2 + H 2 S + 4 H 2 O
![Соли В насыщенном растворе 2 Cu. Cl 2 = Cu[Cu. Cl 4] Купраты 2 Соли В насыщенном растворе 2 Cu. Cl 2 = Cu[Cu. Cl 4] Купраты 2](https://present5.com/presentation/72381937_151120358/image-59.jpg) Соли В насыщенном растворе 2 Cu. Cl 2 = Cu[Cu. Cl 4] Купраты 2 Cu. O + Na 2 O 2 = 2 Na. Cu. O 2 2 Cu(OH)2 + Ba(OH)2 + Na. OCl = = Ba(Cu. O 2)2 + Na. Cl + 3 H 2 O 2 Na. Cu. O 2 + 8 HCl = = 2 Cu. Cl 2 + 2 Na. Cl + 4 H 2 O + Cl 2
Соли В насыщенном растворе 2 Cu. Cl 2 = Cu[Cu. Cl 4] Купраты 2 Cu. O + Na 2 O 2 = 2 Na. Cu. O 2 2 Cu(OH)2 + Ba(OH)2 + Na. OCl = = Ba(Cu. O 2)2 + Na. Cl + 3 H 2 O 2 Na. Cu. O 2 + 8 HCl = = 2 Cu. Cl 2 + 2 Na. Cl + 4 H 2 O + Cl 2
 Соли Ag. F, Ag. Cl, Ag. Br, Ag. I Растворимость в воде уменьшается Ag. Cl + 2 NH 3 = [Ag(NH 3)2]Cl Ag. Br + 2 NH 3 = [Ag(NH 3)2]Br Ag. I в аммиаке не растворяется Ag. Hlg + 2 Na 2 S 2 O 3 = Na 3[Ag(S 2 O 3)2] + Na. Hlg
Соли Ag. F, Ag. Cl, Ag. Br, Ag. I Растворимость в воде уменьшается Ag. Cl + 2 NH 3 = [Ag(NH 3)2]Cl Ag. Br + 2 NH 3 = [Ag(NH 3)2]Br Ag. I в аммиаке не растворяется Ag. Hlg + 2 Na 2 S 2 O 3 = Na 3[Ag(S 2 O 3)2] + Na. Hlg
 Zn, Cd, Hg Легко 2 Zn + O 2 = 2 Zn. O 2 Cd + O 2 = 2 Cd. O С трудом 2 Hg + O 2 = 2 Hg. O При нагревании Zn + S = Zn. S Cd + S = Cd. S На холоду Hg + S = Hg. S
Zn, Cd, Hg Легко 2 Zn + O 2 = 2 Zn. O 2 Cd + O 2 = 2 Cd. O С трудом 2 Hg + O 2 = 2 Hg. O При нагревании Zn + S = Zn. S Cd + S = Cd. S На холоду Hg + S = Hg. S
 Zn, Cd, Hg С водой не реагируют Zn + 4 NH 3 +2 H 2 O = Zn(NH 3)4 (OH)2 + H 2 Zn +2 KOH + 2 H 2 O = K 2 Zn(OH)4 + H 2 Zn +2 HCl = Zn. Cl 2 + H 2 Cd +2 HCl = Cd. Cl 2 + H 2 При нагревании 4 Zn + 5 Н 2 SO 4(конц. ) = = 4 Zn. SO 4 + H 2 S +4 H 2 O На холоду Zn + 2 H 2 SO 4(конц. ) = Zn. SO 4 + SO 2 + 2 H 2 O Cd + 2 H 2 SO 4(конц. ) = Cd. SO 4 + SO 2 + 2 H 2 O
Zn, Cd, Hg С водой не реагируют Zn + 4 NH 3 +2 H 2 O = Zn(NH 3)4 (OH)2 + H 2 Zn +2 KOH + 2 H 2 O = K 2 Zn(OH)4 + H 2 Zn +2 HCl = Zn. Cl 2 + H 2 Cd +2 HCl = Cd. Cl 2 + H 2 При нагревании 4 Zn + 5 Н 2 SO 4(конц. ) = = 4 Zn. SO 4 + H 2 S +4 H 2 O На холоду Zn + 2 H 2 SO 4(конц. ) = Zn. SO 4 + SO 2 + 2 H 2 O Cd + 2 H 2 SO 4(конц. ) = Cd. SO 4 + SO 2 + 2 H 2 O
 Zn, Cd, Hg 4 Zn + 10 HNO 3(разб. ) = = 4 Zn(NO 3)2 + NH 4 NO 3 +3 H 2 O Hg + 4 HNO 3 = Hg(NO 3)2 + 2 NO 2 + 2 H 2 O 6 Hg(изб. ) + 8 НNО 3 = = 3 Hg 2(NO 3)2 + 2 NO + 4 Н 2 O Zn. SO 4 + 2 Na. OH = Zn(OH)2↓ + Na 2 SO 4 Cd. SO 4 + 2 Na. OH = Cd(OH)2↓ + Na 2 SO 4
Zn, Cd, Hg 4 Zn + 10 HNO 3(разб. ) = = 4 Zn(NO 3)2 + NH 4 NO 3 +3 H 2 O Hg + 4 HNO 3 = Hg(NO 3)2 + 2 NO 2 + 2 H 2 O 6 Hg(изб. ) + 8 НNО 3 = = 3 Hg 2(NO 3)2 + 2 NO + 4 Н 2 O Zn. SO 4 + 2 Na. OH = Zn(OH)2↓ + Na 2 SO 4 Cd. SO 4 + 2 Na. OH = Cd(OH)2↓ + Na 2 SO 4
 Zn, Cd, Hg Амфотерность гидроксидов Zn(OН)2 + 2 НCl = Zn. Cl 2 + 2 H 2 O Zn(OH)2 + 2 Na. OH = Na 2 Zn(OH)4 Cd(OН)2 + 2 НCl = Cd. Cl 2 + 2 H 2 O При нагревании Cd(OH)2 + 2 Na. OH(конц. ) = Na 2 Cd(OH)4 Э(OН)2 + 4 NH 3 = Э(NH 3)4 (OH)2
Zn, Cd, Hg Амфотерность гидроксидов Zn(OН)2 + 2 НCl = Zn. Cl 2 + 2 H 2 O Zn(OH)2 + 2 Na. OH = Na 2 Zn(OH)4 Cd(OН)2 + 2 НCl = Cd. Cl 2 + 2 H 2 O При нагревании Cd(OH)2 + 2 Na. OH(конц. ) = Na 2 Cd(OH)4 Э(OН)2 + 4 NH 3 = Э(NH 3)4 (OH)2
 Zn, Cd, Hg Hg(NO 3)2 + 2 Nа. OН = Hg. O + 2 H 2 O + 2 Na. NO 3 Hg 2(NO 3)2 + 2 Na. OH = Hg 2 O + H 2 O + 2 Na. NO 3 Гидролиз солей Э 2+ + Н 2 O = ЭОН+ + Н+; Э = Zn, Cd 2 Э 2+ + 2 CO 32 - + Н 2 O = (ЭOН)2 СO 3↓ + СO 2 2 Hg 2+ + H 2 O + 2 NO 3 - = Hg 2 O(NO 3)2 + 2 Hg 22+ + Н 2 O + 2 NO 3 - = Hg 4 O(NO 3)2 + 2 H+ Hg. S, Hg 2 Cl 2 (каломель), Hg. Cl 2 (сулема) – труднорастворимы и не гидролизуются
Zn, Cd, Hg Hg(NO 3)2 + 2 Nа. OН = Hg. O + 2 H 2 O + 2 Na. NO 3 Hg 2(NO 3)2 + 2 Na. OH = Hg 2 O + H 2 O + 2 Na. NO 3 Гидролиз солей Э 2+ + Н 2 O = ЭОН+ + Н+; Э = Zn, Cd 2 Э 2+ + 2 CO 32 - + Н 2 O = (ЭOН)2 СO 3↓ + СO 2 2 Hg 2+ + H 2 O + 2 NO 3 - = Hg 2 O(NO 3)2 + 2 Hg 22+ + Н 2 O + 2 NO 3 - = Hg 4 O(NO 3)2 + 2 H+ Hg. S, Hg 2 Cl 2 (каломель), Hg. Cl 2 (сулема) – труднорастворимы и не гидролизуются
 Zn, Cd, Hg 2 Hg. Cl 2 + SO 2 +2 H 2 O = Hg 2 Cl 2 + H 2 SO 4 + 2 HCl Hg 2(NO 3)2 + 4 HNO 3 = 2 Hg(NO 3)2 +2 NO 2 +2 H 2 O Hg 2 Cl 2 + Sn. Cl 2 = Sn. Cl 4 + 2 Hg Hg. SO 4 + 4 NH 3 = [Hg(NH 3)4]SO 4 Hg(Cl. O 4)2 + 4 NH 3 = [Hg(NH 3)4](Cl. O 4)2 При избытке NH 4 Cl Hg. Cl 2 + 2 NH 3 = [Hg(NH 3)2]Cl 2 – плавкий белый преципитат [Hg(NH 3)2]Cl 2 = NH 4 Cl + [H 2 NHg. Cl - неплавкий белый преципитат
Zn, Cd, Hg 2 Hg. Cl 2 + SO 2 +2 H 2 O = Hg 2 Cl 2 + H 2 SO 4 + 2 HCl Hg 2(NO 3)2 + 4 HNO 3 = 2 Hg(NO 3)2 +2 NO 2 +2 H 2 O Hg 2 Cl 2 + Sn. Cl 2 = Sn. Cl 4 + 2 Hg Hg. SO 4 + 4 NH 3 = [Hg(NH 3)4]SO 4 Hg(Cl. O 4)2 + 4 NH 3 = [Hg(NH 3)4](Cl. O 4)2 При избытке NH 4 Cl Hg. Cl 2 + 2 NH 3 = [Hg(NH 3)2]Cl 2 – плавкий белый преципитат [Hg(NH 3)2]Cl 2 = NH 4 Cl + [H 2 NHg. Cl - неплавкий белый преципитат
![Zn, Cd, Hg Реактив Несслера K 2[Hg. I 4(H 2 O)2] NH 3 + Zn, Cd, Hg Реактив Несслера K 2[Hg. I 4(H 2 O)2] NH 3 +](https://present5.com/presentation/72381937_151120358/image-67.jpg) Zn, Cd, Hg Реактив Несслера K 2[Hg. I 4(H 2 O)2] NH 3 + K 2[Hg. I 4(H 2 O)2] → [OHg 2 NH 2]I или [I 2 Hg 2 NH 2]I Красно-коричневый осадок
Zn, Cd, Hg Реактив Несслера K 2[Hg. I 4(H 2 O)2] NH 3 + K 2[Hg. I 4(H 2 O)2] → [OHg 2 NH 2]I или [I 2 Hg 2 NH 2]I Красно-коричневый осадок


