20_d-елементи_VIIIВ_групи.ppt
- Количество слайдов: 31
 d-елементи VІІІВ групи. Ферум та його сполуки. dелементи VІІІВ групи. Кобальт і Нікол. d-елементи VІІІВ групи. Платинові метали підготувала к. х. н. , доц. Демид А. Є.
d-елементи VІІІВ групи. Ферум та його сполуки. dелементи VІІІВ групи. Кобальт і Нікол. d-елементи VІІІВ групи. Платинові метали підготувала к. х. н. , доц. Демид А. Є.
 Загальна характеристика елементів сімейства заліза і платинових металів. До VIII групи належать дев’ять d-елементів, які утворюють три підгрупи – підгрупу Fe (Fe, Ru, Os), підгрупу Co (Co, Rh, Ir) і підгрупу нікелю (Ni, Pd, Pt). Інакше VIII групу класифікують в сімейства (родини): заліза (Fe, Co, Ni) і платинових металів (Ru, Rh, Pd, Os, Ir, Pt). По мірі заповнення (n-1) d-орбіталей другим електроном посилюється подібність сусідніх d-елементів по періоду. Так, нікель проявляє велику подібність як з Co так і з Fe, а також з Cu. Крім того, внаслідок лантаноїдного стиснення особлива схожість властивостей спостерігається в діадах: Ru-Os, Rh-Ir, Pd-Pt. Саме через це елементи 5 -го і 6 -го періодів об’єднують у сімейство платинових металів. Подібність розміщених один за другим елементів ніде більше в періодичній системі не виражено так сильно, як в цій групі.
Загальна характеристика елементів сімейства заліза і платинових металів. До VIII групи належать дев’ять d-елементів, які утворюють три підгрупи – підгрупу Fe (Fe, Ru, Os), підгрупу Co (Co, Rh, Ir) і підгрупу нікелю (Ni, Pd, Pt). Інакше VIII групу класифікують в сімейства (родини): заліза (Fe, Co, Ni) і платинових металів (Ru, Rh, Pd, Os, Ir, Pt). По мірі заповнення (n-1) d-орбіталей другим електроном посилюється подібність сусідніх d-елементів по періоду. Так, нікель проявляє велику подібність як з Co так і з Fe, а також з Cu. Крім того, внаслідок лантаноїдного стиснення особлива схожість властивостей спостерігається в діадах: Ru-Os, Rh-Ir, Pd-Pt. Саме через це елементи 5 -го і 6 -го періодів об’єднують у сімейство платинових металів. Подібність розміщених один за другим елементів ніде більше в періодичній системі не виражено так сильно, як в цій групі.
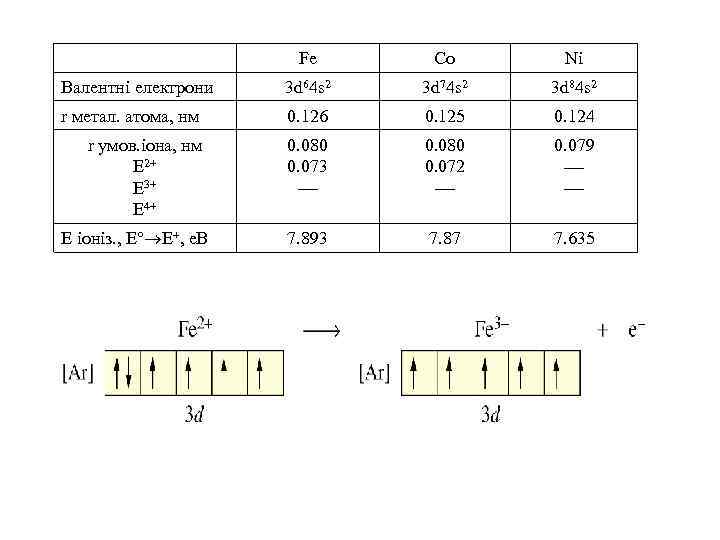 Fe Co Ni Валентні електрони 3 d 64 s 2 3 d 74 s 2 3 d 84 s 2 r метал. атома, нм 0. 126 0. 125 0. 124 r умов. іона, нм E 2+ E 3+ E 4+ 0. 080 0. 073 0. 080 0. 072 0. 079 7. 893 7. 87 7. 635 E іоніз. , Е Е+, е. В
Fe Co Ni Валентні електрони 3 d 64 s 2 3 d 74 s 2 3 d 84 s 2 r метал. атома, нм 0. 126 0. 125 0. 124 r умов. іона, нм E 2+ E 3+ E 4+ 0. 080 0. 073 0. 080 0. 072 0. 079 7. 893 7. 87 7. 635 E іоніз. , Е Е+, е. В
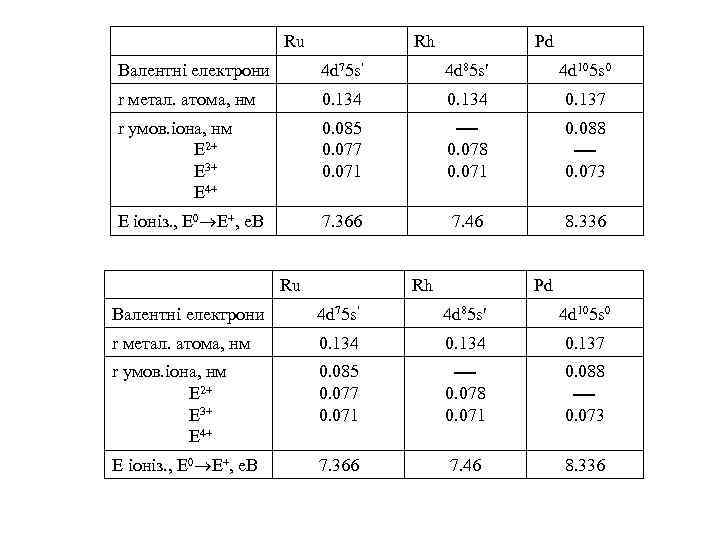 Ru Rh Pd Валентні електрони 4 d 75 s 4 d 85 s 4 d 105 s 0 r метал. атома, нм 0. 134 0. 137 r умов. іона, нм Е 2+ Е 3+ Е 4+ 0. 085 0. 077 0. 071 0. 078 0. 071 0. 088 0. 073 Е іоніз. , Е 0 Е+, е. В 7. 366 7. 46 8. 336
Ru Rh Pd Валентні електрони 4 d 75 s 4 d 85 s 4 d 105 s 0 r метал. атома, нм 0. 134 0. 137 r умов. іона, нм Е 2+ Е 3+ Е 4+ 0. 085 0. 077 0. 071 0. 078 0. 071 0. 088 0. 073 Е іоніз. , Е 0 Е+, е. В 7. 366 7. 46 8. 336
 d-елементи VІІI В групи Елемент 26 Fe 27 Co 28 Ni Розподіл електронів на зовнішньому рівні 3 d 6 4 s 2 3 d 7 4 s 2 3 d 8 4 s 2 Атомний радіус, нм 0. 126 0. 125 0. 124 Характерні с. о. +6, +3, +2, 0 +4, +3, +2, 0 Основні мінерали Fe 3 O 4 - магнетит Fe 2 O 3 – гематит Fe 2 O 3*H 2 O- лімоніт Co. As. S - кобальніт Co. As 2 - скутерудит Ni. As – нікелін Ni 2 S 4 - полідеміт Стабільні ізотопи 56 Fe 59 Co 58 Ni 60 Ni
d-елементи VІІI В групи Елемент 26 Fe 27 Co 28 Ni Розподіл електронів на зовнішньому рівні 3 d 6 4 s 2 3 d 7 4 s 2 3 d 8 4 s 2 Атомний радіус, нм 0. 126 0. 125 0. 124 Характерні с. о. +6, +3, +2, 0 +4, +3, +2, 0 Основні мінерали Fe 3 O 4 - магнетит Fe 2 O 3 – гематит Fe 2 O 3*H 2 O- лімоніт Co. As. S - кобальніт Co. As 2 - скутерудит Ni. As – нікелін Ni 2 S 4 - полідеміт Стабільні ізотопи 56 Fe 59 Co 58 Ni 60 Ni
 Fe - Залізо - Fe Залізо (САМОРОДНЕ) Синонім: Ферит кобальт нікель
Fe - Залізо - Fe Залізо (САМОРОДНЕ) Синонім: Ферит кобальт нікель
 Залізна колона Катуб Мінар коло Делі
Залізна колона Катуб Мінар коло Делі
 До тріади Феруму відносяться Ферум, Кобальт і Нікель. Зовнішні електронні оболонки ізольованих атомів Fe, Co, Ni мають однаковий склад (4 s 2), а розміри атомів від Fe до Ni дещо зменшується по мірі заповнення електронами 3 d-підрівня. Залізо (26 Fe) і нікель (28 Ni) – парні елементи, що обумовлює велику плеяду стабільних ізотопів, а нікель – непарний (елементодинак). Найважливіші з них (для добування металічного заліза): гематит – Fe 2 O 3 магнітний залізняк – Fe 3 O 4 пірит – Fe. S 2 бурий залізняк – Fe(OH)3 сидерит – Fe. CO 3 Для заліза характерні три валентні стани – +2, +3, +6. У сполуках з низькими ступенями окиснення (+2, +3) буде переважати іонний зв′язок (Fe 2 O 3, Fe. O, Fe(OH)2, Fe(OH)3), а в сполуках з високими ступенями окиснення (+6) – переважно ковалентний зв′язок (ферати – M 2 Fe. O 4). Металічне залізо утворює декілька кристалічних модифікацій, які стійкі в певних температурних інтервалах. Стабільне в звичайних умовах залізо при нагріванні проходить такі етапи: -Fe (7000 C) -Fe (9100 C) -Fe (14000 C) -Fe (15860 C) Fe
До тріади Феруму відносяться Ферум, Кобальт і Нікель. Зовнішні електронні оболонки ізольованих атомів Fe, Co, Ni мають однаковий склад (4 s 2), а розміри атомів від Fe до Ni дещо зменшується по мірі заповнення електронами 3 d-підрівня. Залізо (26 Fe) і нікель (28 Ni) – парні елементи, що обумовлює велику плеяду стабільних ізотопів, а нікель – непарний (елементодинак). Найважливіші з них (для добування металічного заліза): гематит – Fe 2 O 3 магнітний залізняк – Fe 3 O 4 пірит – Fe. S 2 бурий залізняк – Fe(OH)3 сидерит – Fe. CO 3 Для заліза характерні три валентні стани – +2, +3, +6. У сполуках з низькими ступенями окиснення (+2, +3) буде переважати іонний зв′язок (Fe 2 O 3, Fe. O, Fe(OH)2, Fe(OH)3), а в сполуках з високими ступенями окиснення (+6) – переважно ковалентний зв′язок (ферати – M 2 Fe. O 4). Металічне залізо утворює декілька кристалічних модифікацій, які стійкі в певних температурних інтервалах. Стабільне в звичайних умовах залізо при нагріванні проходить такі етапи: -Fe (7000 C) -Fe (9100 C) -Fe (14000 C) -Fe (15860 C) Fe
 Хімічні властивості металічного заліза визначаються положенням в ряді напруг. Оскільки в ряді напруг Fe знаходиться до водню, то залізо витісняє водень із води. Дійсно, на вологому повітрі в нейтральному середовищі проходить реакція: Fe + 3 H 2 O Fe(OH)3 + 3/2 H 2 В кислому середовищі (наприклад, в присутності води і СО 2) утворюється двохвалентне залізо: Fe + 2 H+ Fe 2+ + H 2 При нагріванні в атмосфері сухого повітря залізо окиснюється: 2 Fe + 3/2 O 2 Fe 2 O 3 Для промислових цілей основним методом відновлення заліза і його сполук був доменний процес. Як відомо, в доменних печах, які можуть сягати 30 і більше метрів у висоту, оксиди заліза перетворюються під дією вуглецю і його сполук в чугун. Головними процесами є наступні: Fe 2 O 3 + 3 C 2 Fe + 3 CO Fe 2 O 3 + 3 CO 2 Fe + 3 CO 2 C + CO 2 2 CO Чугун, який одержують при доменному процесі, надзвичайно крихкий, оскільки, як домішку, він містить Fe 3 C. Для усунення крихкості чугун потрібно звільнити від Fe 3 C (при нагріванні Fe 3 C розкладається на залізо і вуглець, який розчиняється тільки в - Fe).
Хімічні властивості металічного заліза визначаються положенням в ряді напруг. Оскільки в ряді напруг Fe знаходиться до водню, то залізо витісняє водень із води. Дійсно, на вологому повітрі в нейтральному середовищі проходить реакція: Fe + 3 H 2 O Fe(OH)3 + 3/2 H 2 В кислому середовищі (наприклад, в присутності води і СО 2) утворюється двохвалентне залізо: Fe + 2 H+ Fe 2+ + H 2 При нагріванні в атмосфері сухого повітря залізо окиснюється: 2 Fe + 3/2 O 2 Fe 2 O 3 Для промислових цілей основним методом відновлення заліза і його сполук був доменний процес. Як відомо, в доменних печах, які можуть сягати 30 і більше метрів у висоту, оксиди заліза перетворюються під дією вуглецю і його сполук в чугун. Головними процесами є наступні: Fe 2 O 3 + 3 C 2 Fe + 3 CO Fe 2 O 3 + 3 CO 2 Fe + 3 CO 2 C + CO 2 2 CO Чугун, який одержують при доменному процесі, надзвичайно крихкий, оскільки, як домішку, він містить Fe 3 C. Для усунення крихкості чугун потрібно звільнити від Fe 3 C (при нагріванні Fe 3 C розкладається на залізо і вуглець, який розчиняється тільки в - Fe).
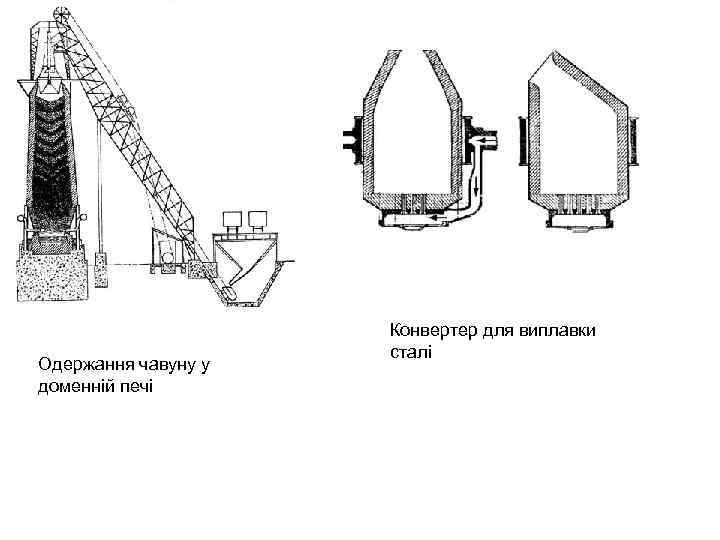 Одержання чавуну у доменній печі Конвертер для виплавки сталі
Одержання чавуну у доменній печі Конвертер для виплавки сталі
 Сполуки Феруму(ІІ) найчастіше добувають, діючи на метал неокиснюючими кислотами (HCl) або розбавленими розчинами кислотокисників (H 2 SO 4, HNO 3) у середовищі де є відновник: Fe + 2 HCl Fe. Cl 2 + H 2 Сполуки Fe(II) можна добути шляхом відновлення сполук Fe(IIІ), наприклад металом: 2 Fe. Cl 3 + Fe 3 Fe. Cl 2 Найважливіші сполуки заліза: Fe. SO 4 7 H 2 O, Fe. SO 4 (NH 4)2 SO 4 6 H 2 O, Fe. Cl 2, Fe. F 2 8 H 2 O, Fe. Br 2 6 H 2 O. Солі заліза (ІІ) у водних розчинах і при нагріванні кристалогідратів піддаються слабкому гідролізу: Fe 2+ + 2 H 2 O Fe(OH)2 + 2 H+ Рівновага реакції в нейтральних і кислих середовищах майже повністю зсунута вліво.
Сполуки Феруму(ІІ) найчастіше добувають, діючи на метал неокиснюючими кислотами (HCl) або розбавленими розчинами кислотокисників (H 2 SO 4, HNO 3) у середовищі де є відновник: Fe + 2 HCl Fe. Cl 2 + H 2 Сполуки Fe(II) можна добути шляхом відновлення сполук Fe(IIІ), наприклад металом: 2 Fe. Cl 3 + Fe 3 Fe. Cl 2 Найважливіші сполуки заліза: Fe. SO 4 7 H 2 O, Fe. SO 4 (NH 4)2 SO 4 6 H 2 O, Fe. Cl 2, Fe. F 2 8 H 2 O, Fe. Br 2 6 H 2 O. Солі заліза (ІІ) у водних розчинах і при нагріванні кристалогідратів піддаються слабкому гідролізу: Fe 2+ + 2 H 2 O Fe(OH)2 + 2 H+ Рівновага реакції в нейтральних і кислих середовищах майже повністю зсунута вліво.
 Гідроксид заліза (ІІ) (Fe(OH)2) – біла речовина, яка на повітрі швидко міняє забарвлення, перетворюючись спочатку у синьо-зелений, змішано-валентний гідратований оксид складу Fe 3 O 4 x. H 2 O, а потім в частково дегідратований Fe(OH)3 бурого кольору. Fe. O – оксид заліза (ІІ) – сильний відновник. Це чорна речовина, яка проявляє пірофорні властивості. Дегідратацією Fe(OH)2 Fe. O добути не вдається. Його синтезують шляхом відновлення оксиду заліза (ІІІ): Fe 2 O 3 + H 2 2 Fe. O + H 2 O (3000 C), або шляхом термолізу оксалату: Fe. C 2 O 4 Fe. O + CO 2 + CO В нейтральних середовищах, наприклад, при взаємодії Fe. Cl 2 з Na. HCO 3 утворюється осад середнього карбонату заліза Fe. CO 3, а в кислому середовищі, наприклад, при пропусканні струму СО 2 через водну суспензію Fe. CO 3, одержуємо кислий карбонат Fe(HCO 3)2. В присутності О 2 відбувається окиснення кислого карбонату: 2 Fe(HCO 3)2 + 1/2 O 2 + H 2 O 2 Fe(OH)3 + 4 CO 2
Гідроксид заліза (ІІ) (Fe(OH)2) – біла речовина, яка на повітрі швидко міняє забарвлення, перетворюючись спочатку у синьо-зелений, змішано-валентний гідратований оксид складу Fe 3 O 4 x. H 2 O, а потім в частково дегідратований Fe(OH)3 бурого кольору. Fe. O – оксид заліза (ІІ) – сильний відновник. Це чорна речовина, яка проявляє пірофорні властивості. Дегідратацією Fe(OH)2 Fe. O добути не вдається. Його синтезують шляхом відновлення оксиду заліза (ІІІ): Fe 2 O 3 + H 2 2 Fe. O + H 2 O (3000 C), або шляхом термолізу оксалату: Fe. C 2 O 4 Fe. O + CO 2 + CO В нейтральних середовищах, наприклад, при взаємодії Fe. Cl 2 з Na. HCO 3 утворюється осад середнього карбонату заліза Fe. CO 3, а в кислому середовищі, наприклад, при пропусканні струму СО 2 через водну суспензію Fe. CO 3, одержуємо кислий карбонат Fe(HCO 3)2. В присутності О 2 відбувається окиснення кислого карбонату: 2 Fe(HCO 3)2 + 1/2 O 2 + H 2 O 2 Fe(OH)3 + 4 CO 2
 Сполуки заліза (ІІІ) Добування сполук заліза (ІІІ) здійснюють, діючи окисниками (HNO 3, Cl 2, Br 2) на металічне залізо, або похідні заліза (ІІ): 2 Fe. Cl 2 + Cl 2 2 Fe. Cl 3 Найвідоміші сполуки заліза (ІІІ): Fe 2 O 3, Fe 2 O 3 x. H 2 O, Fe. Cl 3 6 H 2 O (жовтобурого кольору), Fe 2(SO 4)3 10 H 2 O (жовтого кольору), Fe(NO 3)3 9 H 2 O (жовто-бурого кольору); залізо-аміачні квасці – (NH 4)2 SO 4 Fe 2(SO 4)3 24 H 2 O (жовто-бурого кольору). Акваіон Fe 3+ aq забарвлює водні розчини солей заліза (ІІІ) у червоно-бурий колір, який змінює свою інтенсивність в залежності від ступеня гідролізу. Сполуки заліза (ІІІ) сильніше гідролізують, ніж солі Fe(II) в аналогічних умовах. Внаслідок гідролізу водні розчини солей заліза (ІІІ) мають кислу реакцію, в залежності від концентрації їх р. Н складає приблизо 2 -3. Оксид заліза (ІІІ) добувають прожарюванням гідроксиду Fe(OH)3: 2 Fe(OH)3 Fe 2 O 3 + 3 H 2 O Fe 2 O 3 проявляє амфотерні властивості, утворюючи ферити електропозитивних металів, наприклад лужних: Fe 2 O 3 + Na 2 CO 3 2 Na. Fe. O 2 + CO 2
Сполуки заліза (ІІІ) Добування сполук заліза (ІІІ) здійснюють, діючи окисниками (HNO 3, Cl 2, Br 2) на металічне залізо, або похідні заліза (ІІ): 2 Fe. Cl 2 + Cl 2 2 Fe. Cl 3 Найвідоміші сполуки заліза (ІІІ): Fe 2 O 3, Fe 2 O 3 x. H 2 O, Fe. Cl 3 6 H 2 O (жовтобурого кольору), Fe 2(SO 4)3 10 H 2 O (жовтого кольору), Fe(NO 3)3 9 H 2 O (жовто-бурого кольору); залізо-аміачні квасці – (NH 4)2 SO 4 Fe 2(SO 4)3 24 H 2 O (жовто-бурого кольору). Акваіон Fe 3+ aq забарвлює водні розчини солей заліза (ІІІ) у червоно-бурий колір, який змінює свою інтенсивність в залежності від ступеня гідролізу. Сполуки заліза (ІІІ) сильніше гідролізують, ніж солі Fe(II) в аналогічних умовах. Внаслідок гідролізу водні розчини солей заліза (ІІІ) мають кислу реакцію, в залежності від концентрації їх р. Н складає приблизо 2 -3. Оксид заліза (ІІІ) добувають прожарюванням гідроксиду Fe(OH)3: 2 Fe(OH)3 Fe 2 O 3 + 3 H 2 O Fe 2 O 3 проявляє амфотерні властивості, утворюючи ферити електропозитивних металів, наприклад лужних: Fe 2 O 3 + Na 2 CO 3 2 Na. Fe. O 2 + CO 2
 Ферит натрію (Na. Fe. O 2) – жовта тверда речовина, в якій залізо виконує аніонну функцію – входить в склад оксоаніону Fe. O 2–. Ферити в присутності води повністю гідролізують: Na. Fe. O 2 + 2 H 2 O Fe(OH)3 + Na. OH Ферити різноманітних металів широко використовуються в мікроелектроніці як магнітні матеріали. Fe 2 O 3 застосовують у лако-фарбовій промисловості (охра – жовта фарба) і як матеріал для полірування скла. Сполуки заліза (VI) Для заліза характерний ступінь окиснення +6, який воно проявляє у фератах складу M 2 Fe. O 4. Існує кілька способів добування фератів. Наприклад, прожарювання твердих реагентів: Fe 2 O 3+3 KNO 3+4 KOH 2 K 2 Fe. O 4+3 KNO 2+2 H 2 O При нагріванні розчину K 2 Fe. O 4 відбувається розкладання за схемою: 2 K 2 Fe. O 4 + 5 H 2 O 2 Fe(OH)3 + 3/2 O 2 + 4 KOH Комплексні сполуки заліза Жовта K 4[Fe(CN)6] і червона K 3[Fe(CN)6] кров’яна сіль називаються, відповідно, гексаціаноферат і гексаціаноферит калію. В лабораторії K 4[Fe(CN)6] добувають в два етапи: (І) Fe 2+ + 2 CN– Fe(CN)2 (жовто-бурий осад) (ІІ) Fe(CN)2 + 4 KCN K 4[Fe(CN)6] Для добування червоної кров’яної солі окиснюють K 4[Fe(CN)6]: 2 K 4[Fe(CN)6] + Cl 2 2 K 3[Fe(CN)6] + 2 KCl Жовту і червону кров’яні солі використовують в якісному аналізі для визначення заліза: 4 Fe 3+ + 3[Fe(CN)6]4– Fe 4[Fe(CN)6]3 (берлінська лазур) 3 Fe 2+ + 2[Fe(CN)6]3– Fe 3[Fe(CN)6]2 (турнбуллева синь)
Ферит натрію (Na. Fe. O 2) – жовта тверда речовина, в якій залізо виконує аніонну функцію – входить в склад оксоаніону Fe. O 2–. Ферити в присутності води повністю гідролізують: Na. Fe. O 2 + 2 H 2 O Fe(OH)3 + Na. OH Ферити різноманітних металів широко використовуються в мікроелектроніці як магнітні матеріали. Fe 2 O 3 застосовують у лако-фарбовій промисловості (охра – жовта фарба) і як матеріал для полірування скла. Сполуки заліза (VI) Для заліза характерний ступінь окиснення +6, який воно проявляє у фератах складу M 2 Fe. O 4. Існує кілька способів добування фератів. Наприклад, прожарювання твердих реагентів: Fe 2 O 3+3 KNO 3+4 KOH 2 K 2 Fe. O 4+3 KNO 2+2 H 2 O При нагріванні розчину K 2 Fe. O 4 відбувається розкладання за схемою: 2 K 2 Fe. O 4 + 5 H 2 O 2 Fe(OH)3 + 3/2 O 2 + 4 KOH Комплексні сполуки заліза Жовта K 4[Fe(CN)6] і червона K 3[Fe(CN)6] кров’яна сіль називаються, відповідно, гексаціаноферат і гексаціаноферит калію. В лабораторії K 4[Fe(CN)6] добувають в два етапи: (І) Fe 2+ + 2 CN– Fe(CN)2 (жовто-бурий осад) (ІІ) Fe(CN)2 + 4 KCN K 4[Fe(CN)6] Для добування червоної кров’яної солі окиснюють K 4[Fe(CN)6]: 2 K 4[Fe(CN)6] + Cl 2 2 K 3[Fe(CN)6] + 2 KCl Жовту і червону кров’яні солі використовують в якісному аналізі для визначення заліза: 4 Fe 3+ + 3[Fe(CN)6]4– Fe 4[Fe(CN)6]3 (берлінська лазур) 3 Fe 2+ + 2[Fe(CN)6]3– Fe 3[Fe(CN)6]2 (турнбуллева синь)
 Схеми деяких реакцій заліза
Схеми деяких реакцій заліза
![Характерні реакції іонів Fe 2+ Калій гексаціаноферат (III) K 3[Fe(CN)6] (фармакопейна реакція) утворює з Характерні реакції іонів Fe 2+ Калій гексаціаноферат (III) K 3[Fe(CN)6] (фармакопейна реакція) утворює з](https://present5.com/presentation/92741772_400224488/image-16.jpg) Характерні реакції іонів Fe 2+ Калій гексаціаноферат (III) K 3[Fe(CN)6] (фармакопейна реакція) утворює з іонами Fe 2+ синій осад Fe 3[Fe(CN)6]2, так звану турнбулеву синь: 3 Fe 2+ + 2[Fe(CN)6]3– = Fe 3[Fe(CN)6]2. Осад не розчиняється у кислотах, але розкладається в лугах, у результаті чого утворюється Fe(OH)2. Виконання реакції. До 2 -3 крапель досліджуваного розчину додають стільки ж крапель Калій гексаціаноферату (III). Якщо є Fe 2+, то утворюється темносиній осад (реакцію проводять при p. H 3).
Характерні реакції іонів Fe 2+ Калій гексаціаноферат (III) K 3[Fe(CN)6] (фармакопейна реакція) утворює з іонами Fe 2+ синій осад Fe 3[Fe(CN)6]2, так звану турнбулеву синь: 3 Fe 2+ + 2[Fe(CN)6]3– = Fe 3[Fe(CN)6]2. Осад не розчиняється у кислотах, але розкладається в лугах, у результаті чого утворюється Fe(OH)2. Виконання реакції. До 2 -3 крапель досліджуваного розчину додають стільки ж крапель Калій гексаціаноферату (III). Якщо є Fe 2+, то утворюється темносиній осад (реакцію проводять при p. H 3).
![Характерні реакції іонів Fe 3+ Калій гексаціаноферат (II) K 4[Fe(CN)6] (фармакопейна реакція) утворює з Характерні реакції іонів Fe 3+ Калій гексаціаноферат (II) K 4[Fe(CN)6] (фармакопейна реакція) утворює з](https://present5.com/presentation/92741772_400224488/image-17.jpg) Характерні реакції іонів Fe 3+ Калій гексаціаноферат (II) K 4[Fe(CN)6] (фармакопейна реакція) утворює з іонами Fe 3+ темно-синій осад Fe 4[Fe(CN)6]3, так звану берлінську блакить: 4 Fe 3+ + 3[Fe(CN)6]4– = Fe 4[Fe(CN)6]3. Осад Fe 4[Fe(CN)6]3, не розчиняється у розведених мінеральних кислотах; луги розкладають Fe 4[Fe(CN)6]3, утворюючи Fe(OH)3: Fe 4[Fe(CN)6]3 + 12 KOH = 4 Fe(OH)3 + 3 K 4[Fe(CN)6]. Перебігу реакції заважають іони (фосфат-, оксалат-, фторид- тощо), які утворюють з Fe 3+ комплексні сполуки. Калій або амоній тіоціанат KSCN або NH 4 SCN (фармакопейна реакція) – з іонами Fe 3+ утворює низку забарвлених у червоний колір розчинних комплексних сполук: [Fe. SCN]2+, [Fe(SCN)2]+, [Fe(SCN)3], [Fe(SCN)4]- тощо. Чутливість реакції виявлення іонів Fe 3+ за допомогою тіоціанату збільшується у процесі екстракції продукту реакції органічним розчинником, наприклад, ефіром, бутиловим та ізобутиловим спиртами.
Характерні реакції іонів Fe 3+ Калій гексаціаноферат (II) K 4[Fe(CN)6] (фармакопейна реакція) утворює з іонами Fe 3+ темно-синій осад Fe 4[Fe(CN)6]3, так звану берлінську блакить: 4 Fe 3+ + 3[Fe(CN)6]4– = Fe 4[Fe(CN)6]3. Осад Fe 4[Fe(CN)6]3, не розчиняється у розведених мінеральних кислотах; луги розкладають Fe 4[Fe(CN)6]3, утворюючи Fe(OH)3: Fe 4[Fe(CN)6]3 + 12 KOH = 4 Fe(OH)3 + 3 K 4[Fe(CN)6]. Перебігу реакції заважають іони (фосфат-, оксалат-, фторид- тощо), які утворюють з Fe 3+ комплексні сполуки. Калій або амоній тіоціанат KSCN або NH 4 SCN (фармакопейна реакція) – з іонами Fe 3+ утворює низку забарвлених у червоний колір розчинних комплексних сполук: [Fe. SCN]2+, [Fe(SCN)2]+, [Fe(SCN)3], [Fe(SCN)4]- тощо. Чутливість реакції виявлення іонів Fe 3+ за допомогою тіоціанату збільшується у процесі екстракції продукту реакції органічним розчинником, наприклад, ефіром, бутиловим та ізобутиловим спиртами.
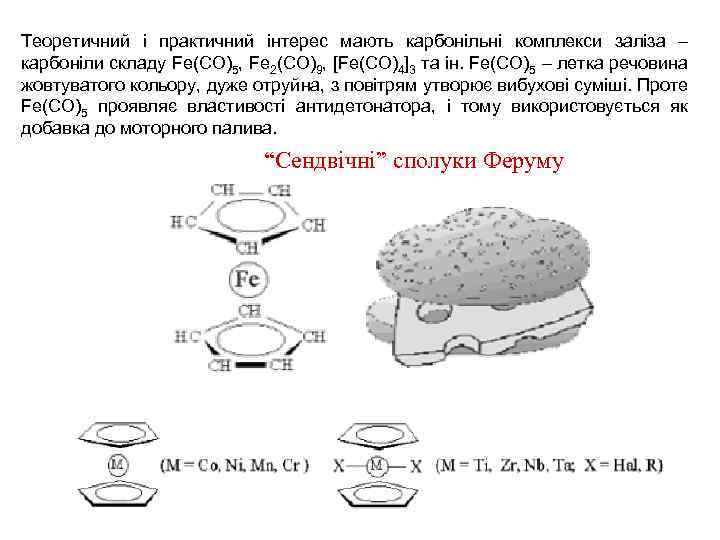 Теоретичний і практичний інтерес мають карбонільні комплекси заліза – карбоніли складу Fe(CO)5, Fe 2(CO)9, [Fe(CO)4]3 та ін. Fe(CO)5 – летка речовина жовтуватого кольору, дуже отруйна, з повітрям утворює вибухові суміші. Проте Fe(CO)5 проявляє властивості антидетонатора, і тому використовується як добавка до моторного палива. “Сендвічні” сполуки Феруму
Теоретичний і практичний інтерес мають карбонільні комплекси заліза – карбоніли складу Fe(CO)5, Fe 2(CO)9, [Fe(CO)4]3 та ін. Fe(CO)5 – летка речовина жовтуватого кольору, дуже отруйна, з повітрям утворює вибухові суміші. Проте Fe(CO)5 проявляє властивості антидетонатора, і тому використовується як добавка до моторного палива. “Сендвічні” сполуки Феруму
 Гемоглобін
Гемоглобін
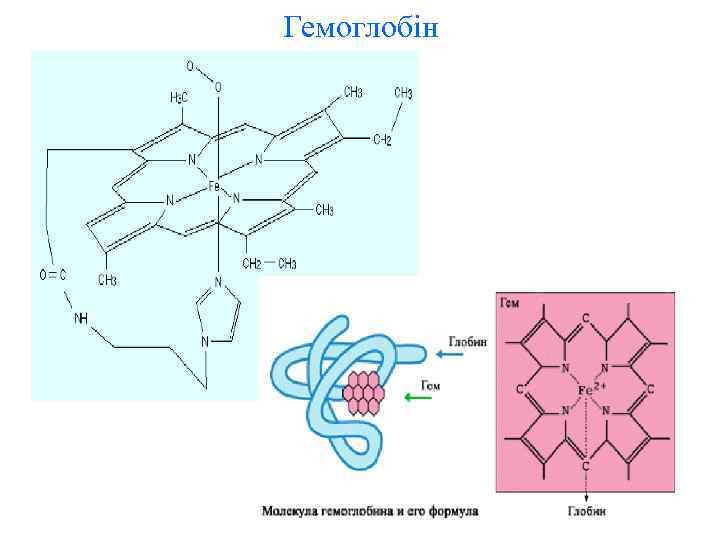
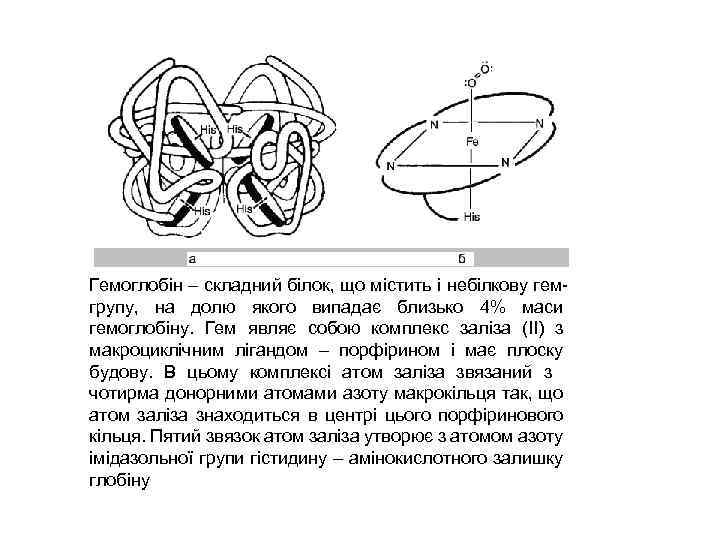 Гемоглобін – складний білок, що містить і небілкову гемгрупу, на долю якого випадає близько 4% маси гемоглобіну. Гем являє собою комплекс заліза (II) з макроциклічним лігандом – порфірином і має плоску будову. В цьому комплексі атом заліза звязаний з чотирма донорними атомами азоту макрокільця так, що атом заліза знаходиться в центрі цього порфіринового кільця. Пятий звязок атом заліза утворює з атомом азоту імідазольної групи гістидину – амінокислотного залишку глобіну
Гемоглобін – складний білок, що містить і небілкову гемгрупу, на долю якого випадає близько 4% маси гемоглобіну. Гем являє собою комплекс заліза (II) з макроциклічним лігандом – порфірином і має плоску будову. В цьому комплексі атом заліза звязаний з чотирма донорними атомами азоту макрокільця так, що атом заліза знаходиться в центрі цього порфіринового кільця. Пятий звязок атом заліза утворює з атомом азоту імідазольної групи гістидину – амінокислотного залишку глобіну
 Препарати заліза та продукти харчування, що містять залізо
Препарати заліза та продукти харчування, що містять залізо
 Хімічні властивості кобальту і його сполук Кобальт – білий метал з сіруватим відтінком. Має дві алатропні модифікації -Со і -кобальт (гексагональна гранецентрична кубічна решітка). За хімічною активністю кобальт дещо поступається залізу: 2 Co + O 2 = 2 Co. O. При нагріванні взаємодіє майже з усіма неметалами. Концентрована сульфатна і хлоридна кислоти пасивують кобальт, кислоти середньої концентрації розчиняють кобальт: 3 Co+8 HNO 3=3 Co(NO 3)2+2 NO+ 4 H 2 O; Co + 2 H 2 SO 4 = Co. SO 4 + SO 2 + 2 H 2 O. Для простих солей Со характерний с. о. +2, а для координаційних +3.
Хімічні властивості кобальту і його сполук Кобальт – білий метал з сіруватим відтінком. Має дві алатропні модифікації -Со і -кобальт (гексагональна гранецентрична кубічна решітка). За хімічною активністю кобальт дещо поступається залізу: 2 Co + O 2 = 2 Co. O. При нагріванні взаємодіє майже з усіма неметалами. Концентрована сульфатна і хлоридна кислоти пасивують кобальт, кислоти середньої концентрації розчиняють кобальт: 3 Co+8 HNO 3=3 Co(NO 3)2+2 NO+ 4 H 2 O; Co + 2 H 2 SO 4 = Co. SO 4 + SO 2 + 2 H 2 O. Для простих солей Со характерний с. о. +2, а для координаційних +3.
 Карбоніли. Простіший карбоніл Со 2(СО)8 двоядерний комплекс Будову молекули октакарбонілу можна пояснити наступним чином: в ній атоми Со утворюють 6 -зв’язків: 4 за донорно-акцепторним механізмом 4 молекул СО і вільних орбіталей Со; п’ятий зв’язок утворюється при участі однієї d-електронної пари атома Co і вільної -орбіталі молекули Со. Зв’язок Со – Со утворюється за рахунок непарних електронів двох атомів Со. Стабілізація молекули досягається за рахунок -зв’язків, на утворення яких застосовуються 3 d 6 -електрони атома кобальту. Co(O), d 9 3 d 4 s 4 p на -зв’язок Октакарбоніл отримують нагріванням порошку Со в атмосфері СО (при 1500 -2000 С і р = 2, 5 107 Па). Це оранжеві кристали, нерозчинні у воді, але добре розчинні в органічних розчинниках. При 600 С октакарбоніл Со починає розкпадатися.
Карбоніли. Простіший карбоніл Со 2(СО)8 двоядерний комплекс Будову молекули октакарбонілу можна пояснити наступним чином: в ній атоми Со утворюють 6 -зв’язків: 4 за донорно-акцепторним механізмом 4 молекул СО і вільних орбіталей Со; п’ятий зв’язок утворюється при участі однієї d-електронної пари атома Co і вільної -орбіталі молекули Со. Зв’язок Со – Со утворюється за рахунок непарних електронів двох атомів Со. Стабілізація молекули досягається за рахунок -зв’язків, на утворення яких застосовуються 3 d 6 -електрони атома кобальту. Co(O), d 9 3 d 4 s 4 p на -зв’язок Октакарбоніл отримують нагріванням порошку Со в атмосфері СО (при 1500 -2000 С і р = 2, 5 107 Па). Це оранжеві кристали, нерозчинні у воді, але добре розчинні в органічних розчинниках. При 600 С октакарбоніл Со починає розкпадатися.
 Сполуки Co(II). КЧ = 6, 4. с. о. +2 характерна у Со. О – сіро-зелені кристали: 2 Co + O 2 2 Co. O Co(OH)2 = Co. O + H 2 O Co. CO 3 = Co. O + CO 2. Дигаліди отримують взаємодією простих речовин: Co + Hal 2 = Co. Hal 2. Дигаліди, крім Co. F 2, розчинні у воді. Гідроксид Co(OH)2 утворюється при дії лугів на солі Co(II): Co. Cl 2 + 2 Na. OH = Co(OH)2 + 2 Na. Cl За хімічною природою Со і Со(ОН)2 – амфотерні сполуки з домінуванням основних властивостей.
Сполуки Co(II). КЧ = 6, 4. с. о. +2 характерна у Со. О – сіро-зелені кристали: 2 Co + O 2 2 Co. O Co(OH)2 = Co. O + H 2 O Co. CO 3 = Co. O + CO 2. Дигаліди отримують взаємодією простих речовин: Co + Hal 2 = Co. Hal 2. Дигаліди, крім Co. F 2, розчинні у воді. Гідроксид Co(OH)2 утворюється при дії лугів на солі Co(II): Co. Cl 2 + 2 Na. OH = Co(OH)2 + 2 Na. Cl За хімічною природою Со і Со(ОН)2 – амфотерні сполуки з домінуванням основних властивостей.
![З катіонних комплексів для Co (II) найбільш характерні аквакомплекси [Co(OH 2)6]2+, які надають розчинам З катіонних комплексів для Co (II) найбільш характерні аквакомплекси [Co(OH 2)6]2+, які надають розчинам](https://present5.com/presentation/92741772_400224488/image-25.jpg) З катіонних комплексів для Co (II) найбільш характерні аквакомплекси [Co(OH 2)6]2+, які надають розчинам яскраво-рожевого забарвлення. Безводні галіди, роданід, сульфат та інші похідні можуть приєднувати молекули аміаку з утворенням: Co 2+ + 6 NH 3 = [Co(NH 3)6]2+. Аміакати Со (ІІ) стійкіші, ніж Fe (ІІ), але водою руйнуються: [Co(NH 3)6]Cl 2 + H 2 O Co(OH)2 + 4 NH 3 + 2 NH 4 Cl. Аміакати Со (ІІ) в розчинах легко окиснюються навіть молекулярним киснем повітря: [Co(NH 3)6]3+ + e = [Co(NH 3)6]2+, 4[Co(NH 3)6]2+ + O 2 + 2 H 2 O = 4[Co(NH 3)6]3+ + 4 OH-.
З катіонних комплексів для Co (II) найбільш характерні аквакомплекси [Co(OH 2)6]2+, які надають розчинам яскраво-рожевого забарвлення. Безводні галіди, роданід, сульфат та інші похідні можуть приєднувати молекули аміаку з утворенням: Co 2+ + 6 NH 3 = [Co(NH 3)6]2+. Аміакати Со (ІІ) стійкіші, ніж Fe (ІІ), але водою руйнуються: [Co(NH 3)6]Cl 2 + H 2 O Co(OH)2 + 4 NH 3 + 2 NH 4 Cl. Аміакати Со (ІІ) в розчинах легко окиснюються навіть молекулярним киснем повітря: [Co(NH 3)6]3+ + e = [Co(NH 3)6]2+, 4[Co(NH 3)6]2+ + O 2 + 2 H 2 O = 4[Co(NH 3)6]3+ + 4 OH-.
![Аніонні комплекси Co (II) за звичай мають тетраедричну структуру [Co. X 4]2 - (X Аніонні комплекси Co (II) за звичай мають тетраедричну структуру [Co. X 4]2 - (X](https://present5.com/presentation/92741772_400224488/image-26.jpg) Аніонні комплекси Co (II) за звичай мають тетраедричну структуру [Co. X 4]2 - (X = Cl-, Br-, I-, SCN-, OH-) і забарвлені в синій та фіолетові кольори: 2 Na. OH + Co(OH)2 = Na 2[Co(OH)4]. Co. Cl 2(нас. ) + HCl(конц. ) = [Co. Cl 4]2 - + 2 H+. Co(SCN)2 + 2 KSCN = K 2[Co(SCN)4]2 - + 6 H 2 O [Co(H 2 O)6]2+ + 4 SCNРозглянуті октаедричні комплекси – високоспінові коиплекси. Низькоспінові октаедричні комплекси для Co (II) не характерні. Вони є сильними відновниками: [Co(CN)6]3 - + 1 e = [Co(CN)6]4 -, E 0 = -0. 83 B тому утворюються низькоспінові октаедричні комплекси Co (III): [Co(CN)6]4 - - 1 e = [Co(CN)6]3 -. Високоспінові комплекси, навпаки, характеризуються деякою інертністю і окиснюються тільки найбільш сильними окиснювачами: 2 K 4[Co. F 6] + F 2 = 2 KF + 2 K 3 Co. F 6. Сполуки Co (III). КЧ = 6, дуже характерні комплексні сполуки. Бінарні сполуки і солі Co (III) нехарактерні.
Аніонні комплекси Co (II) за звичай мають тетраедричну структуру [Co. X 4]2 - (X = Cl-, Br-, I-, SCN-, OH-) і забарвлені в синій та фіолетові кольори: 2 Na. OH + Co(OH)2 = Na 2[Co(OH)4]. Co. Cl 2(нас. ) + HCl(конц. ) = [Co. Cl 4]2 - + 2 H+. Co(SCN)2 + 2 KSCN = K 2[Co(SCN)4]2 - + 6 H 2 O [Co(H 2 O)6]2+ + 4 SCNРозглянуті октаедричні комплекси – високоспінові коиплекси. Низькоспінові октаедричні комплекси для Co (II) не характерні. Вони є сильними відновниками: [Co(CN)6]3 - + 1 e = [Co(CN)6]4 -, E 0 = -0. 83 B тому утворюються низькоспінові октаедричні комплекси Co (III): [Co(CN)6]4 - - 1 e = [Co(CN)6]3 -. Високоспінові комплекси, навпаки, характеризуються деякою інертністю і окиснюються тільки найбільш сильними окиснювачами: 2 K 4[Co. F 6] + F 2 = 2 KF + 2 K 3 Co. F 6. Сполуки Co (III). КЧ = 6, дуже характерні комплексні сполуки. Бінарні сполуки і солі Co (III) нехарактерні.
 Co 3 O 4 – відносно стійкий Co(Co. O 2)2. Його отримують нагріванням Co(NO 3)2. Цей оксид – сильний окиснювач. Гідроксиди Co (III) добувають окисненням гідроксиду кобальту (II) киснем повітря: 4 Co(OH)2 + O 2 + 2 H 2 O = 4 Co(OH)3. Особливо легко окиснення проходить в слабколужному середовищі. Co(OH)3 проявляє значно меншу основну функцію, ніж Co(OH)2; проявляють окиснювальні властивості: 2 Co(OH)3 + 6 HCl = 2 Co. Cl 2 + 6 H 2 O. При сплавленні з лугами або содою утворюють кобальтит: 2 Co(OH)3 + Na 2 CO 3 = 2 Na. Co. O 2 + CO 2 + 3 H 2 O. Координаційні сполуки Co (III) утворюються при окисненні солей Co (II) у слабколужному середовищах різними окиснювачами і навіть киснем повітря: 4 Сo. Cl 2 + O 2 + 20 NH 3 + 4 NH 4 Cl = 4[Co(NH 3)6]Cl 3 + 2 H 2 O Co. Cl 2+ 7 KNO 2 + 2 CH 3 COOH = K 3[Co(NO 2)6] + NO + 2 CH 3 COOK + 2 KCl + H 2 O. Дуже характерні змішанолігандні комплекси: [Co(NH 3)6]3+ - жовті [Co(NH 3)5 H 2 O]3+, [Co(NH 3)5 Cl]2+ - червоні [Co(NH 3)4 Cl 2]+ - зелені і фіалкові.
Co 3 O 4 – відносно стійкий Co(Co. O 2)2. Його отримують нагріванням Co(NO 3)2. Цей оксид – сильний окиснювач. Гідроксиди Co (III) добувають окисненням гідроксиду кобальту (II) киснем повітря: 4 Co(OH)2 + O 2 + 2 H 2 O = 4 Co(OH)3. Особливо легко окиснення проходить в слабколужному середовищі. Co(OH)3 проявляє значно меншу основну функцію, ніж Co(OH)2; проявляють окиснювальні властивості: 2 Co(OH)3 + 6 HCl = 2 Co. Cl 2 + 6 H 2 O. При сплавленні з лугами або содою утворюють кобальтит: 2 Co(OH)3 + Na 2 CO 3 = 2 Na. Co. O 2 + CO 2 + 3 H 2 O. Координаційні сполуки Co (III) утворюються при окисненні солей Co (II) у слабколужному середовищах різними окиснювачами і навіть киснем повітря: 4 Сo. Cl 2 + O 2 + 20 NH 3 + 4 NH 4 Cl = 4[Co(NH 3)6]Cl 3 + 2 H 2 O Co. Cl 2+ 7 KNO 2 + 2 CH 3 COOH = K 3[Co(NO 2)6] + NO + 2 CH 3 COOK + 2 KCl + H 2 O. Дуже характерні змішанолігандні комплекси: [Co(NH 3)6]3+ - жовті [Co(NH 3)5 H 2 O]3+, [Co(NH 3)5 Cl]2+ - червоні [Co(NH 3)4 Cl 2]+ - зелені і фіалкові.
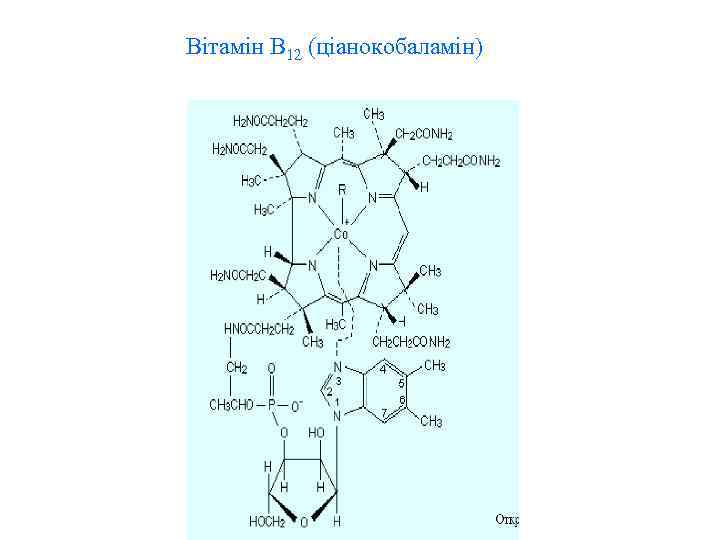 Вітамін В 12 (ціанокобаламін)
Вітамін В 12 (ціанокобаламін)
 Хімічні властивості Ni і його сполук Ni - блискучо-білий із сріблястим відтінком метал. Дещо пасивний: 2 Ni + O 2 2 Ni. O При нагріванні реагує з Hal 2, S, Se, P, As, Sb і т. д. Пасивується конц. H 2 SO 4 і HNO 3, але розчинний в середньої концентрації розчинах їх з утворенням похідних Ni (II). Сполуки Ni (0). С. о. 0 проявляється в карбонілах: Ni(CO)4 – безколірна рідина. Ni(CO)4 Ni + 4 CO добувають чистий Ni, а карбоніл отримують досить легко: Ni + CO Ni(CO)4 При дії розчинів лугів на солі Ni (II) в осад випадає гідроксид нікелю: Ni 2++2 OH- Ni(OH)2. При нагріванні Ni(OH)2 розкладається: Ni(OH)2 Ni. O + H 2 O.
Хімічні властивості Ni і його сполук Ni - блискучо-білий із сріблястим відтінком метал. Дещо пасивний: 2 Ni + O 2 2 Ni. O При нагріванні реагує з Hal 2, S, Se, P, As, Sb і т. д. Пасивується конц. H 2 SO 4 і HNO 3, але розчинний в середньої концентрації розчинах їх з утворенням похідних Ni (II). Сполуки Ni (0). С. о. 0 проявляється в карбонілах: Ni(CO)4 – безколірна рідина. Ni(CO)4 Ni + 4 CO добувають чистий Ni, а карбоніл отримують досить легко: Ni + CO Ni(CO)4 При дії розчинів лугів на солі Ni (II) в осад випадає гідроксид нікелю: Ni 2++2 OH- Ni(OH)2. При нагріванні Ni(OH)2 розкладається: Ni(OH)2 Ni. O + H 2 O.
 Гідроксид Ni(OH)2 не окиснюється киснем повітря. У цьому проявляється більш висока стійкість до окиснення сполук Ni (II), порівняно з аналогічними сполуками Fe і Co. За рахунок утворення аміакатів Ni(OH)2 легко З аніонних комплексів Ni (II) найбільш стійкі [Ni(CN)4]2 - - жовтого кольору: Ni. SO 4 + 2 KCN = Ni(CN)2 + K 2 SO 4; Ni(CN)2 + 2 KCN = K 2[Ni(CN)4]. С. о. +3. Нечисленні аніонні комплекси. 2 Ni(OH)2 + 2 Na. OH + Br 2 = 2 Ni(OH)3 + 2 Na. Br Ni(OH)3 + 3 Na. OH Na 3[Ni(OH)6]. Проявляє окисні властивості: 2 Ni(OH)3 + 6 HCl = 2 Ni. Cl 2 + 6 H 2 O
Гідроксид Ni(OH)2 не окиснюється киснем повітря. У цьому проявляється більш висока стійкість до окиснення сполук Ni (II), порівняно з аналогічними сполуками Fe і Co. За рахунок утворення аміакатів Ni(OH)2 легко З аніонних комплексів Ni (II) найбільш стійкі [Ni(CN)4]2 - - жовтого кольору: Ni. SO 4 + 2 KCN = Ni(CN)2 + K 2 SO 4; Ni(CN)2 + 2 KCN = K 2[Ni(CN)4]. С. о. +3. Нечисленні аніонні комплекси. 2 Ni(OH)2 + 2 Na. OH + Br 2 = 2 Ni(OH)3 + 2 Na. Br Ni(OH)3 + 3 Na. OH Na 3[Ni(OH)6]. Проявляє окисні властивості: 2 Ni(OH)3 + 6 HCl = 2 Ni. Cl 2 + 6 H 2 O
 Характерні реакції іона Co 2+ Амоній тіоціанат NH 4 CNS утворює з іонами Co 2+ комплексний аніон складу [Co(CNS)4]2 -, який забарвлює розчин в рожевий колір: Co 2+ + 4 CNS- = [Co(CNS)4]2 -. Якщо до отриманого розчину додати аміловий спирт (або його суміш з диетиловим ефіром), то цей комплексний аніон вилучається (екстрагується) вказаними органічними розчинниками і забарвлює органічний шар в інтенсивний синій колір. Реакції заважають іони Fe 3+, які утворюють з тіоціанат-іонами комплексний іон інтенсивно червоного забарвлення. Характерні реакції іонів Ni 2+ Реактив Чугайова (диметилгліоксим). Іони Ніколу (ІІ) з реактивом Чугайова дають забарвлений в яскраво червоний колір осад внутрішньокомплексної солі. Реакції заважають іони Fe 2+, які з розчином реактиву дають забарвлену в червоний колір розчинну внутрішньокомплексну сіль. Заважають проведенню реакції також всі іони, які з розчином аміаку утворюють забарвлені осади гідроксидів, що можуть маскувати забарвлення осаду з Ніколом. Ni 2+ + 4 NH 3 [Ni(NH 3)4]2+;
Характерні реакції іона Co 2+ Амоній тіоціанат NH 4 CNS утворює з іонами Co 2+ комплексний аніон складу [Co(CNS)4]2 -, який забарвлює розчин в рожевий колір: Co 2+ + 4 CNS- = [Co(CNS)4]2 -. Якщо до отриманого розчину додати аміловий спирт (або його суміш з диетиловим ефіром), то цей комплексний аніон вилучається (екстрагується) вказаними органічними розчинниками і забарвлює органічний шар в інтенсивний синій колір. Реакції заважають іони Fe 3+, які утворюють з тіоціанат-іонами комплексний іон інтенсивно червоного забарвлення. Характерні реакції іонів Ni 2+ Реактив Чугайова (диметилгліоксим). Іони Ніколу (ІІ) з реактивом Чугайова дають забарвлений в яскраво червоний колір осад внутрішньокомплексної солі. Реакції заважають іони Fe 2+, які з розчином реактиву дають забарвлену в червоний колір розчинну внутрішньокомплексну сіль. Заважають проведенню реакції також всі іони, які з розчином аміаку утворюють забарвлені осади гідроксидів, що можуть маскувати забарвлення осаду з Ніколом. Ni 2+ + 4 NH 3 [Ni(NH 3)4]2+;


