 ЦВА Виды импульсов 1
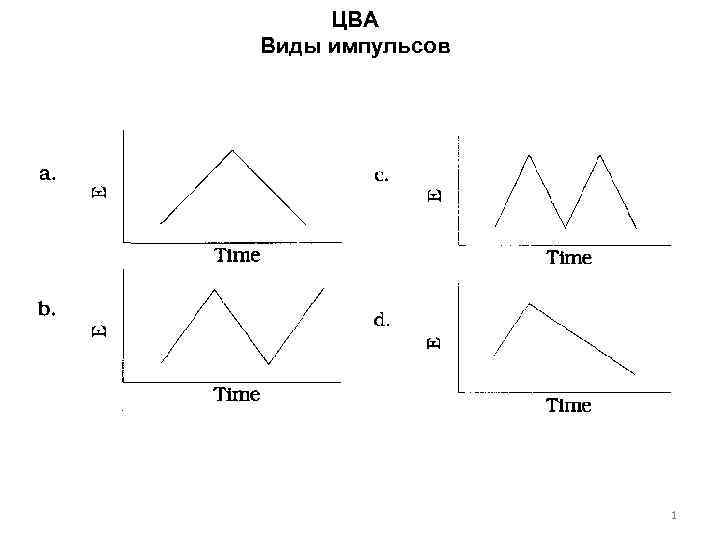
ЦВА Виды импульсов 1
 Классическая ЦВА кривая 2
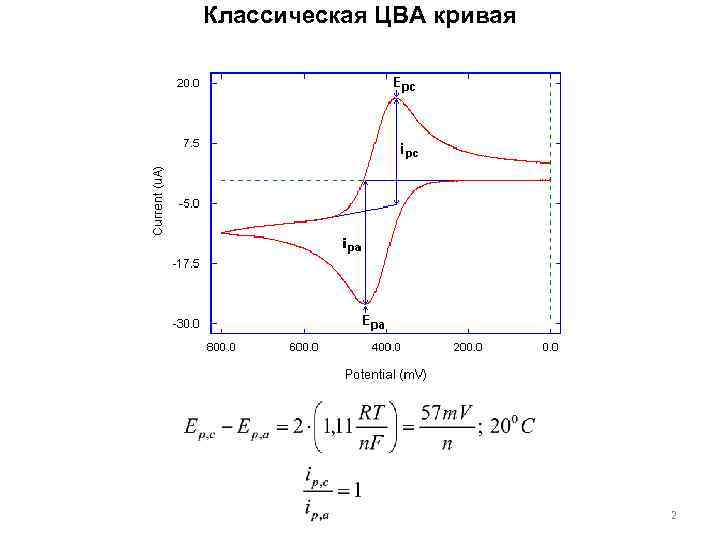
Классическая ЦВА кривая 2
 Необратимая электрохимическая реакция Ep~ln 3
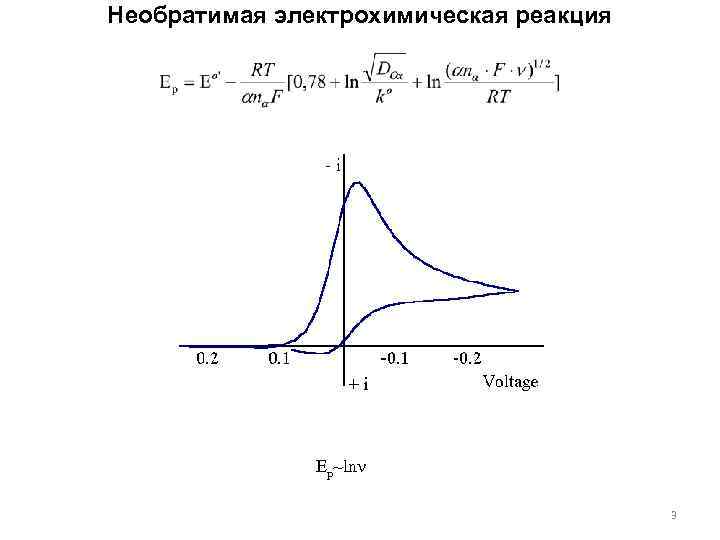
Необратимая электрохимическая реакция Ep~ln 3
 Необратимая электрохимическая реакция Замедленная обратная реакция Необратимая электрохимическая реакция 4
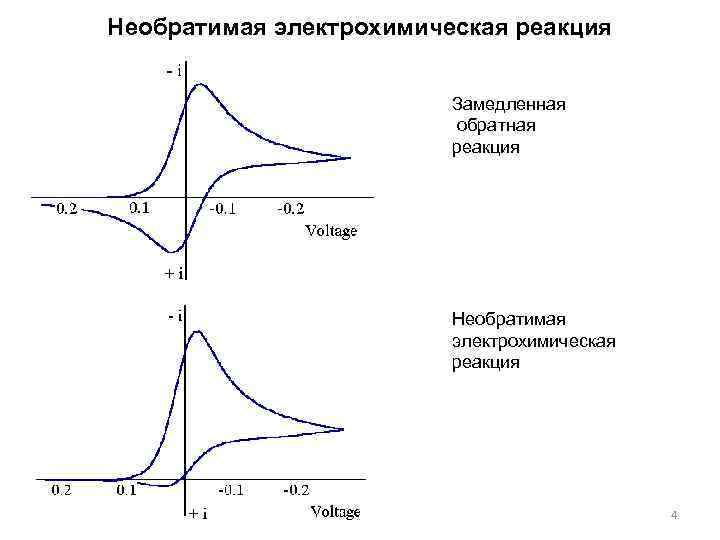
Необратимая электрохимическая реакция Замедленная обратная реакция Необратимая электрохимическая реакция 4
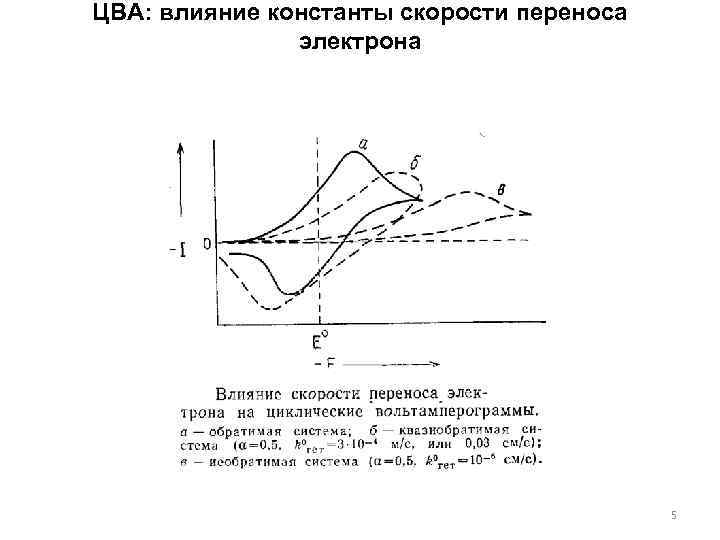 ЦВА: влияние константы скорости переноса электрона 5
ЦВА: влияние константы скорости переноса электрона 5
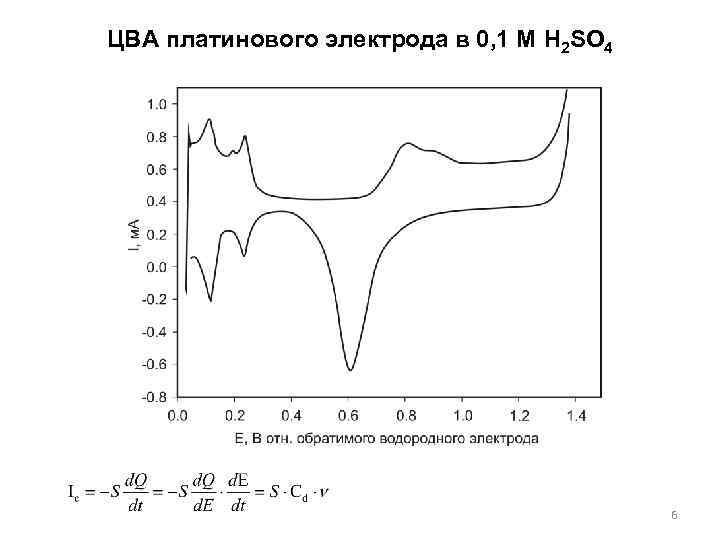 ЦВА платинового электрода в 0, 1 М H 2 SO 4 6
ЦВА платинового электрода в 0, 1 М H 2 SO 4 6
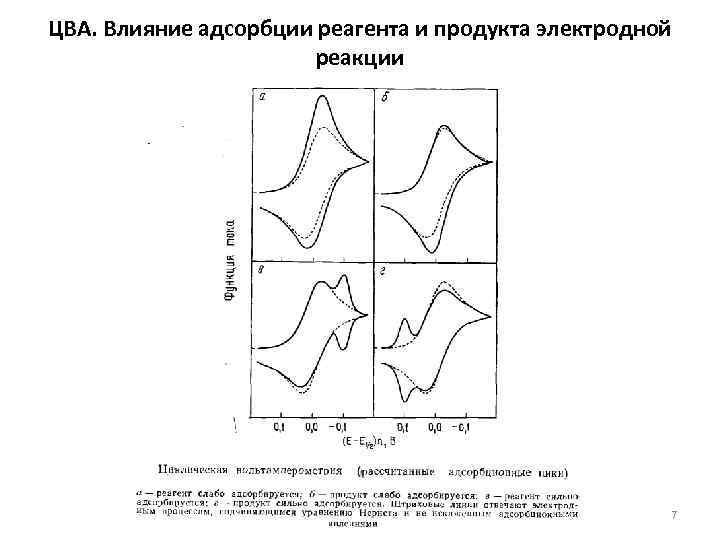 ЦВА. Влияние адсорбции реагента и продукта электродной реакции 7
ЦВА. Влияние адсорбции реагента и продукта электродной реакции 7
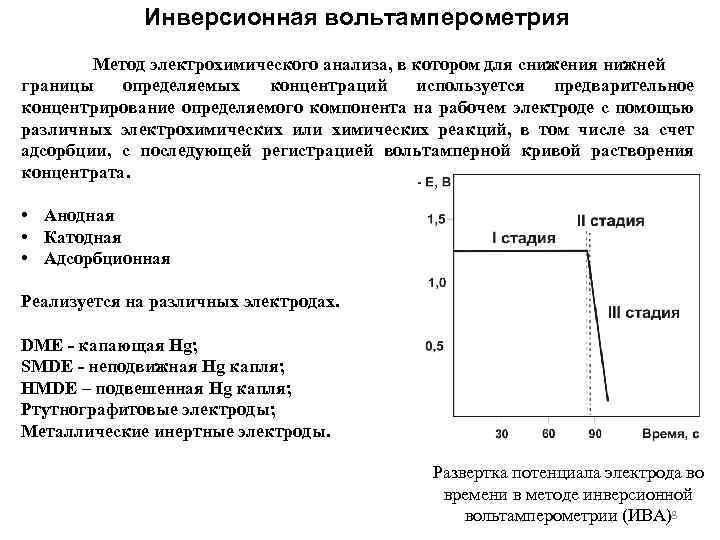 Инверсионная вольтамперометрия Метод электрохимического анализа, в котором для снижения нижней границы определяемых концентраций используется предварительное концентрирование определяемого компонента на рабочем электроде с помощью различных электрохимических или химических реакций, в том числе за счет адсорбции, с последующей регистрацией вольтамперной кривой растворения концентрата. • Анодная • Катодная • Адсорбционная Реализуется на различных электродах. DME - капающая Hg; SMDE - неподвижная Hg капля; HMDE – подвешенная Hg капля; Ртутнографитовые электроды; Металлические инертные электроды. Развертка потенциала электрода во времени в методе инверсионной вольтамперометрии (ИВА)8
Инверсионная вольтамперометрия Метод электрохимического анализа, в котором для снижения нижней границы определяемых концентраций используется предварительное концентрирование определяемого компонента на рабочем электроде с помощью различных электрохимических или химических реакций, в том числе за счет адсорбции, с последующей регистрацией вольтамперной кривой растворения концентрата. • Анодная • Катодная • Адсорбционная Реализуется на различных электродах. DME - капающая Hg; SMDE - неподвижная Hg капля; HMDE – подвешенная Hg капля; Ртутнографитовые электроды; Металлические инертные электроды. Развертка потенциала электрода во времени в методе инверсионной вольтамперометрии (ИВА)8
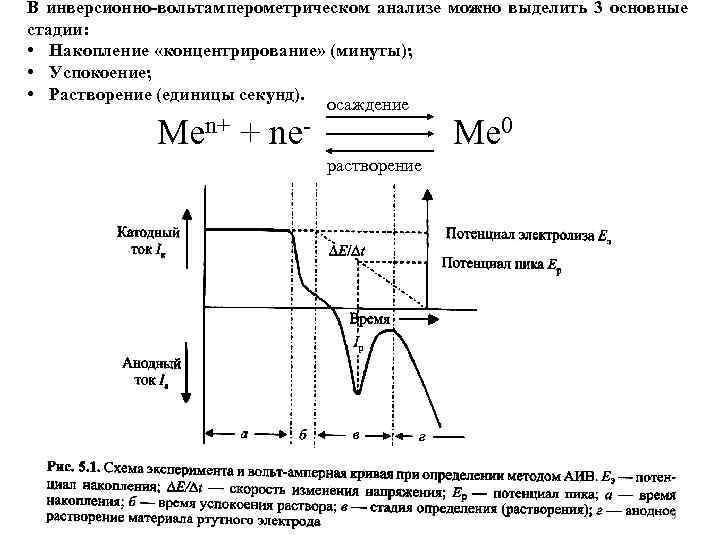 В инверсионно-вольтамперометрическом анализе можно выделить 3 основные стадии: • Накопление «концентрирование» (минуты); • Успокоение; • Растворение (единицы секунд). осаждение Men+ + ne- Me 0 растворение 9
В инверсионно-вольтамперометрическом анализе можно выделить 3 основные стадии: • Накопление «концентрирование» (минуты); • Успокоение; • Растворение (единицы секунд). осаждение Men+ + ne- Me 0 растворение 9
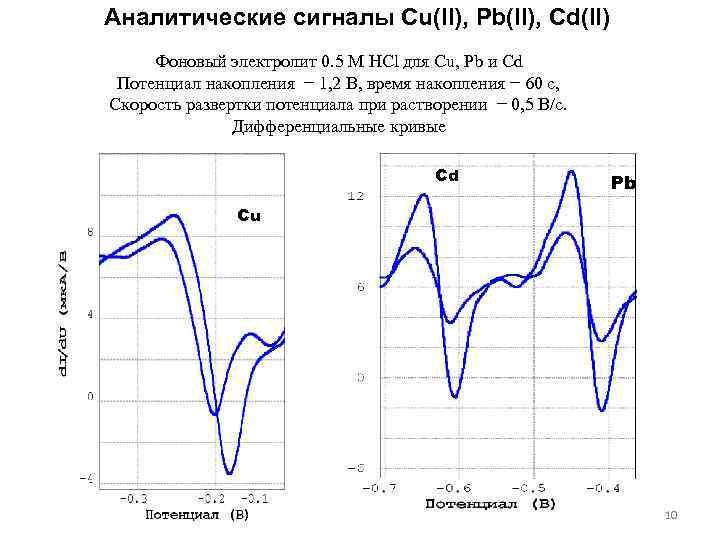 Аналитические сигналы Cu(II), Pb(II), Cd(II) Фоновый электролит 0. 5 M HCl для Cu, Pb и Cd Потенциал накопления − 1, 2 В, время накопления − 60 с, Скорость развертки потенциала при растворении − 0, 5 В/с. Дифференциальные кривые Cd Pb Cu 10
Аналитические сигналы Cu(II), Pb(II), Cd(II) Фоновый электролит 0. 5 M HCl для Cu, Pb и Cd Потенциал накопления − 1, 2 В, время накопления − 60 с, Скорость развертки потенциала при растворении − 0, 5 В/с. Дифференциальные кривые Cd Pb Cu 10
 Способы концентрирования определяемых веществ и сигналобразующие реакции в ИВА Ионы металла восстанавливаются на электроде (ртутном, ртутнопленочном, графитовом, ртутнографитовом) до металла с последующим анодным окислением: 1) Men+ + ne- Meo 2) Meo – ne- Men+- анодный сигнал. На ртутном и ртутнопленочном электродах можно определить: Sb, Bi, Cu, Pb, Sn, Tl, In, Cd, Zn, Ga, Mg, Ge и др. (всего 25 элементов). На фоне неводных растворов определяют: K, Na, Mg, Ba и РЗЭ. На графитовом и модифицированном металлом электродах определяют: Hg, Au, Pt, Ir, Pd. 11
Способы концентрирования определяемых веществ и сигналобразующие реакции в ИВА Ионы металла восстанавливаются на электроде (ртутном, ртутнопленочном, графитовом, ртутнографитовом) до металла с последующим анодным окислением: 1) Men+ + ne- Meo 2) Meo – ne- Men+- анодный сигнал. На ртутном и ртутнопленочном электродах можно определить: Sb, Bi, Cu, Pb, Sn, Tl, In, Cd, Zn, Ga, Mg, Ge и др. (всего 25 элементов). На фоне неводных растворов определяют: K, Na, Mg, Ba и РЗЭ. На графитовом и модифицированном металлом электродах определяют: Hg, Au, Pt, Ir, Pd. 11
 Выбор фонового электролита Фоновый электролит выполняет несколько функций в инверсионновольтамперометрическом анализе: Уменьшает сопротивление раствора как проводник второго рода; Образует комплексы с определяемыми или мешающими ионами; Если необходимо, создает буферную среду для постоянства р. Н раствора (NH 4 OH+NH 4 Cl, ацетатный буфер и др. ) ; Предотвращает гидролиз многовалентных ионов (HCl. O 4, H 2 SO 4); Предотвращает гидролиз и образует комплексы (HCl, HBr, H 3 PO 4). Химический состав фона влияет на потенциал пика (Ер). Если электролит содержит лиганды L и образует комплекс MLp, то Ep = Eo + 0. 059/n ln. KCA – p 0. 059/n ln. CL (CA – концентрация аналита в исследуемом растворе, CL – концентрация лиганда). От фона зависят также обратимость электродного процесса; вязкость раствора и коэффициент диффузии ионов, а значит на потенциал и величину аналитического сигнала; адсорбцию ионов/молекул фона или комплекса MLp на поверхности электрода, а следовательно, на величину остаточного тока и полезного сигнала; ширину области потенциалов поляризации рабочего электрода.
Выбор фонового электролита Фоновый электролит выполняет несколько функций в инверсионновольтамперометрическом анализе: Уменьшает сопротивление раствора как проводник второго рода; Образует комплексы с определяемыми или мешающими ионами; Если необходимо, создает буферную среду для постоянства р. Н раствора (NH 4 OH+NH 4 Cl, ацетатный буфер и др. ) ; Предотвращает гидролиз многовалентных ионов (HCl. O 4, H 2 SO 4); Предотвращает гидролиз и образует комплексы (HCl, HBr, H 3 PO 4). Химический состав фона влияет на потенциал пика (Ер). Если электролит содержит лиганды L и образует комплекс MLp, то Ep = Eo + 0. 059/n ln. KCA – p 0. 059/n ln. CL (CA – концентрация аналита в исследуемом растворе, CL – концентрация лиганда). От фона зависят также обратимость электродного процесса; вязкость раствора и коэффициент диффузии ионов, а значит на потенциал и величину аналитического сигнала; адсорбцию ионов/молекул фона или комплекса MLp на поверхности электрода, а следовательно, на величину остаточного тока и полезного сигнала; ширину области потенциалов поляризации рабочего электрода.
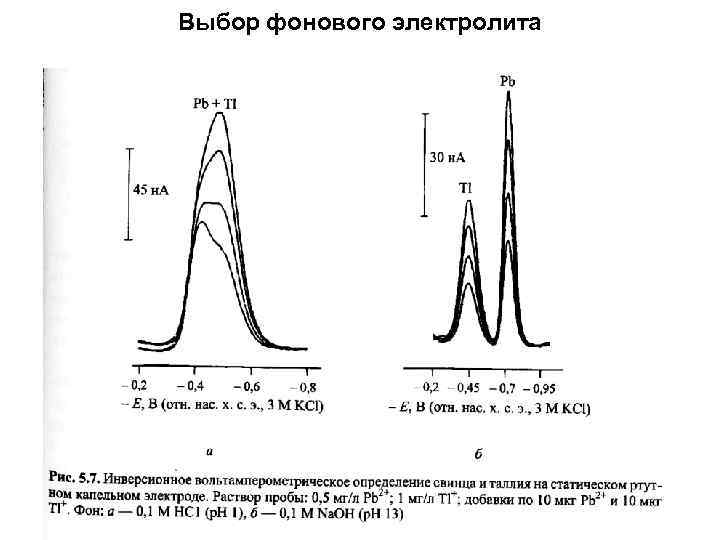 Выбор фонового электролита
Выбор фонового электролита
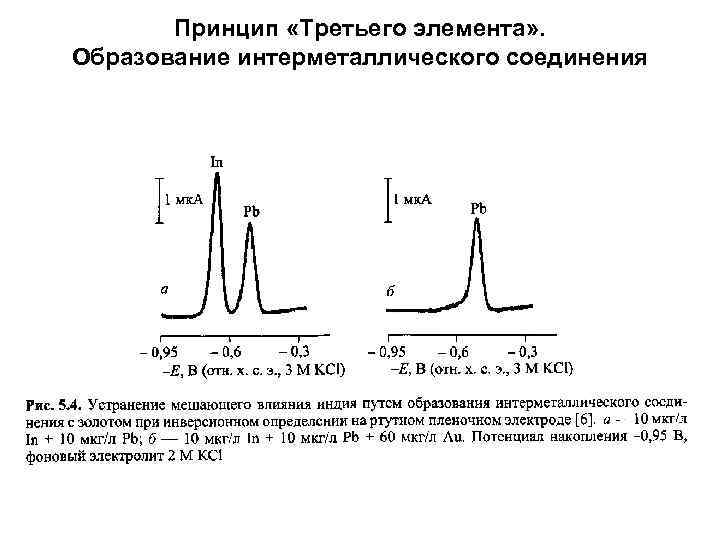 Принцип «Третьего элемента» . Образование интерметаллического соединения
Принцип «Третьего элемента» . Образование интерметаллического соединения
 Катодная инверсионная вольтамперометрия Концентрирование: Определение: 2 Hg →Hg 22+ + 2 A- → Hg 2 A 2 + 2 e- → 2 Hg + 2 A- Галогениды, кислородсодержащие анионы, органические анионы Определение тиолов 2 R─SH + Hg Hg(RS)2 +2 H+ + 2 e- Накопление Ag + Cl-→Ag. Cl + e. Растворение Ag. Cl + e- → Ag + Cl- 15
Катодная инверсионная вольтамперометрия Концентрирование: Определение: 2 Hg →Hg 22+ + 2 A- → Hg 2 A 2 + 2 e- → 2 Hg + 2 A- Галогениды, кислородсодержащие анионы, органические анионы Определение тиолов 2 R─SH + Hg Hg(RS)2 +2 H+ + 2 e- Накопление Ag + Cl-→Ag. Cl + e. Растворение Ag. Cl + e- → Ag + Cl- 15
 Ионы металлов, имеющих несколько степеней окисления, концентрируются на поверхности электрода в виде осадка малорастворимых гидрооксидов или неорганических соединений: 1) Mez+n + ne- – в приэлектродном слое; 2) Mez+n + (z+n)X- Me. X(z+n) - образование малорастворимого соединения на поверхности электрода; 3) Me. X(z+n) + (n-z)e- Mez+ + n. X- - катодный сигнал. Например, Mn 2+ + 4 OH- Mn(OH)4 + 2 e- ; Mn 2+ + 4 IO 4 - Mn(IO 4 -)4 + 2 e-. Таким способом определяют Pb, Cr, Mn, Mo, Ce, Re, Fe… (всего около 12 элементов). Вариант катодной инверсионной вольтамперометрии (КИВ)
Ионы металлов, имеющих несколько степеней окисления, концентрируются на поверхности электрода в виде осадка малорастворимых гидрооксидов или неорганических соединений: 1) Mez+n + ne- – в приэлектродном слое; 2) Mez+n + (z+n)X- Me. X(z+n) - образование малорастворимого соединения на поверхности электрода; 3) Me. X(z+n) + (n-z)e- Mez+ + n. X- - катодный сигнал. Например, Mn 2+ + 4 OH- Mn(OH)4 + 2 e- ; Mn 2+ + 4 IO 4 - Mn(IO 4 -)4 + 2 e-. Таким способом определяют Pb, Cr, Mn, Mo, Ce, Re, Fe… (всего около 12 элементов). Вариант катодной инверсионной вольтамперометрии (КИВ)
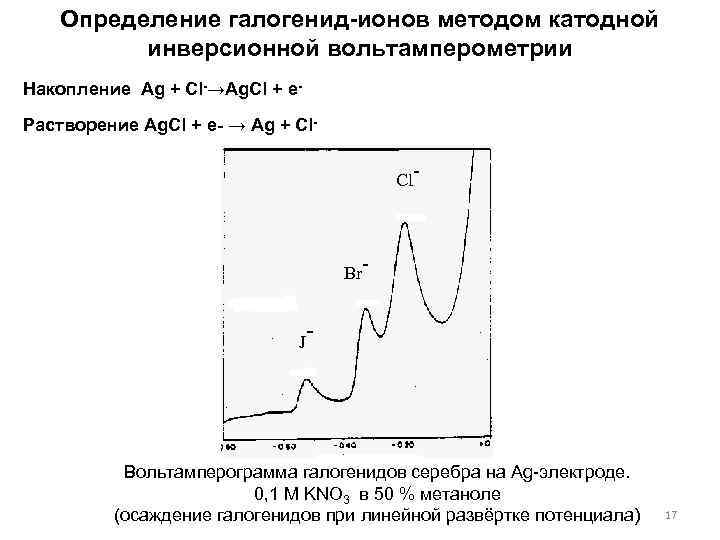 Определение галогенид-ионов методом катодной инверсионной вольтамперометрии Накопление Ag + Cl-→Ag. Cl + e. Растворение Ag. Cl + e- → Ag + Cl. Cl Br J - - - Вольтамперограмма галогенидов серебра на Ag-электроде. 0, 1 М KNO 3 в 50 % метаноле (осаждение галогенидов при линейной развёртке потенциала) 17
Определение галогенид-ионов методом катодной инверсионной вольтамперометрии Накопление Ag + Cl-→Ag. Cl + e. Растворение Ag. Cl + e- → Ag + Cl. Cl Br J - - - Вольтамперограмма галогенидов серебра на Ag-электроде. 0, 1 М KNO 3 в 50 % метаноле (осаждение галогенидов при линейной развёртке потенциала) 17
 Адсорбционная инверсионная вольтамперометрия Ионы металлов концентрируются на электроде в виде комплекса или осадка с лигандом L-, способным адсорбироваться на поверхности электрода и образовывать комплекс: y. L- р-р y. L-адс – адсорбция аниона L- на поверхности электрода; x. Mez+ + y. L-адс [Mex. Ly]xz-yадс – образование комплекса; [Mex. Ly]xz-yадс xe- x. Mez 1 + y. L- - сигнал восстановления (окисления). Этим способом определяют: щелочные и щелочноземельные элементы, в том числе Rb и Ce, Al (солохромфиолетовый), Ni (диметилглиоксим), Co (дифенилкарбазон), Fe, Cu, Sn 4+, Cr 6+ (дифенилкарбазид), Mo 6+ (капралактам), Th 4+ (теноилтрифторацетон), UO 22+, Zr 4+ солохромфиолетовый) и др.
Адсорбционная инверсионная вольтамперометрия Ионы металлов концентрируются на электроде в виде комплекса или осадка с лигандом L-, способным адсорбироваться на поверхности электрода и образовывать комплекс: y. L- р-р y. L-адс – адсорбция аниона L- на поверхности электрода; x. Mez+ + y. L-адс [Mex. Ly]xz-yадс – образование комплекса; [Mex. Ly]xz-yадс xe- x. Mez 1 + y. L- - сигнал восстановления (окисления). Этим способом определяют: щелочные и щелочноземельные элементы, в том числе Rb и Ce, Al (солохромфиолетовый), Ni (диметилглиоксим), Co (дифенилкарбазон), Fe, Cu, Sn 4+, Cr 6+ (дифенилкарбазид), Mo 6+ (капралактам), Th 4+ (теноилтрифторацетон), UO 22+, Zr 4+ солохромфиолетовый) и др.
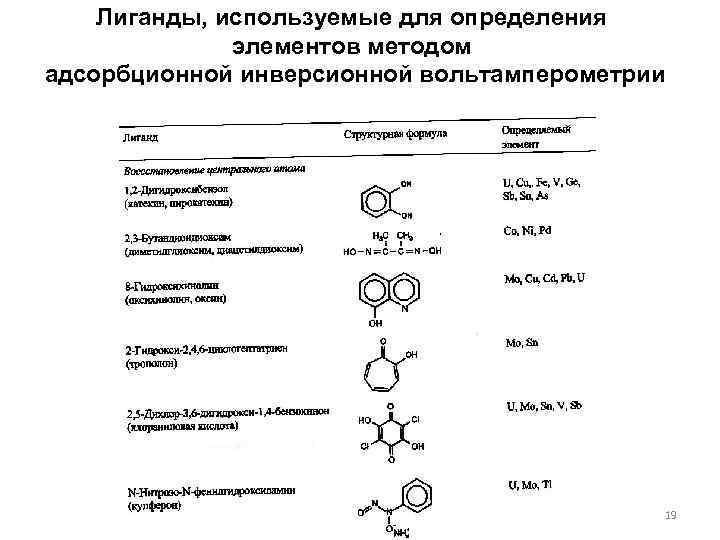 Лиганды, используемые для определения элементов методом адсорбционной инверсионной вольтамперометрии 19
Лиганды, используемые для определения элементов методом адсорбционной инверсионной вольтамперометрии 19
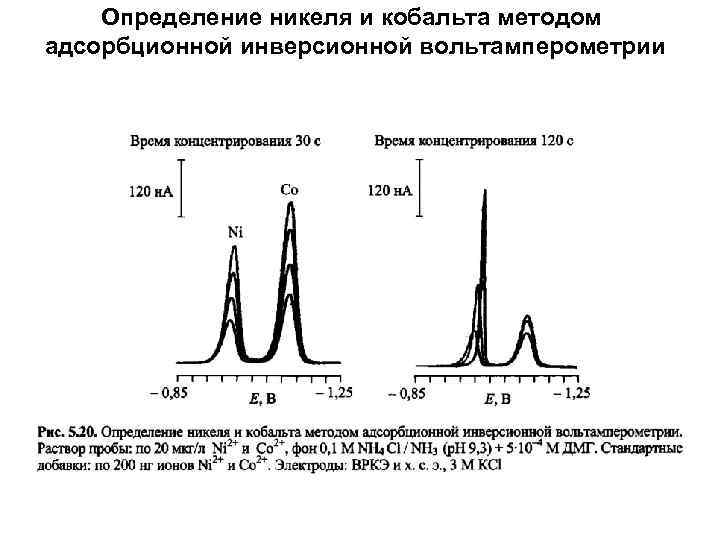 Определение никеля и кобальта методом адсорбционной инверсионной вольтамперометрии
Определение никеля и кобальта методом адсорбционной инверсионной вольтамперометрии
 Определение платины методом адсорбционной инверсионной вольтамперометрии
Определение платины методом адсорбционной инверсионной вольтамперометрии
 Уравнение обратимой поляризационной кривой В области диффузионной кинетики предельный диффузионный ток: Если k велика (10– 2 см/с), то вблизи электрода устанавливается равновесие форм Ox и Red и потенциал электрода описывается уравнением Нернста, только под ln записывается отношение концентраций электроактивных веществ на поверхности электрода С(0) 22
Уравнение обратимой поляризационной кривой В области диффузионной кинетики предельный диффузионный ток: Если k велика (10– 2 см/с), то вблизи электрода устанавливается равновесие форм Ox и Red и потенциал электрода описывается уравнением Нернста, только под ln записывается отношение концентраций электроактивных веществ на поверхности электрода С(0) 22
 Измеряемый катодный ток для процесса восстановления: Измеряемый анодный ток для процесса окисления: Если в начальный момент времени Red в растворе отсутствует, СRed* =0. Выразим СОх(0) и СRed(0) через измеряемый ток i и предельный диффузионный ток id: 23
Измеряемый катодный ток для процесса восстановления: Измеряемый анодный ток для процесса окисления: Если в начальный момент времени Red в растворе отсутствует, СRed* =0. Выразим СОх(0) и СRed(0) через измеряемый ток i и предельный диффузионный ток id: 23
 Подставим данные выражения для поверхностных концентраций в уравнение Нернста и получим уравнение обратимой поляризационной кривой: Для обратимой электродной реакции Ox. Z + ne– Red. Z–n потенциал полуволны E½ равен: 24
Подставим данные выражения для поверхностных концентраций в уравнение Нернста и получим уравнение обратимой поляризационной кривой: Для обратимой электродной реакции Ox. Z + ne– Red. Z–n потенциал полуволны E½ равен: 24
 Выведите уравнение поляризационной кривой для обратимой электродной реакции X + 2 e 2 Y. В начальный момент времени (t = 0) концентрация вещества Y в растворе равна нулю (CY * = 0). Диффузия стационарная. X + 2 e 2 Y Для обратимой реакции справедливо уравнение Нернста: Однако необходимо помнить, что 1 X + ne- 2 Y. Измеряемый катодный ток : 25
Выведите уравнение поляризационной кривой для обратимой электродной реакции X + 2 e 2 Y. В начальный момент времени (t = 0) концентрация вещества Y в растворе равна нулю (CY * = 0). Диффузия стационарная. X + 2 e 2 Y Для обратимой реакции справедливо уравнение Нернста: Однако необходимо помнить, что 1 X + ne- 2 Y. Измеряемый катодный ток : 25
 Выразим СX(0) и СY(0) через измеряемый ток с учетом CY * = 0, t = 0 : Получим следующие выражения: и подставим в уравнение Нернста: 26
Выразим СX(0) и СY(0) через измеряемый ток с учетом CY * = 0, t = 0 : Получим следующие выражения: и подставим в уравнение Нернста: 26
 Аналогично для полярографии: А + 2 е 2 В где KI – константа Ильковича. 27
Аналогично для полярографии: А + 2 е 2 В где KI – константа Ильковича. 27
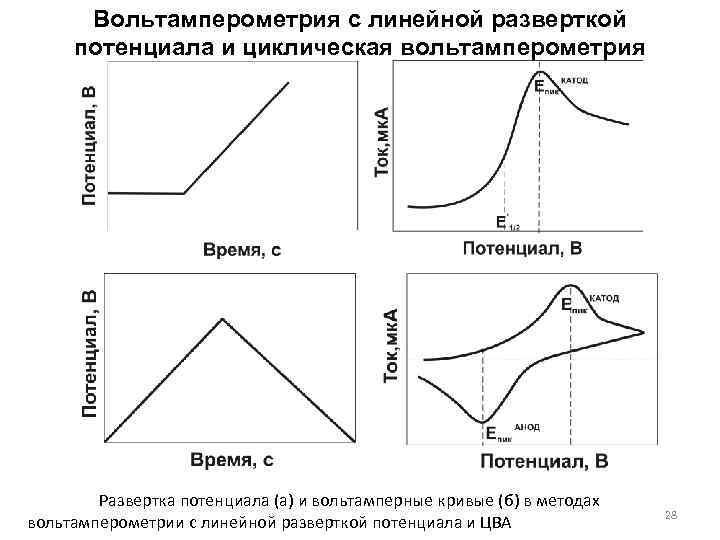 Вольтамперометрия с линейной разверткой потенциала и циклическая вольтамперометрия Развертка потенциала (а) и вольтамперные кривые (б) в методах вольтамперометрии с линейной разверткой потенциала и ЦВА 28
Вольтамперометрия с линейной разверткой потенциала и циклическая вольтамперометрия Развертка потенциала (а) и вольтамперные кривые (б) в методах вольтамперометрии с линейной разверткой потенциала и ЦВА 28
 Фарадеевский диффузионный ток пика: где Ip – фарадеевский диффузионный ток (А); S – площадь электрода (см 2); DOx – коэффициент диффузии (см 2/с); ν – скорость развертки потенциала (В/с); – концентрация аналита (моль/см 3). Величина численного коэффициента в приведенном уравнении зависит от размерностей используемых величин. В уравнение Рэндлса – Шевчика используются другие размерности: где D – коэффициент диффузии (см 2/с); ν – скорость развертки потенциала выражена (м. В/с); – концентрация аналита (моль/см 3). 29
Фарадеевский диффузионный ток пика: где Ip – фарадеевский диффузионный ток (А); S – площадь электрода (см 2); DOx – коэффициент диффузии (см 2/с); ν – скорость развертки потенциала (В/с); – концентрация аналита (моль/см 3). Величина численного коэффициента в приведенном уравнении зависит от размерностей используемых величин. В уравнение Рэндлса – Шевчика используются другие размерности: где D – коэффициент диффузии (см 2/с); ν – скорость развертки потенциала выражена (м. В/с); – концентрация аналита (моль/см 3). 29
 Инверсионная вольтамперометрия Количество электричества, затраченное на электролиз аналита, вычисляют из площади пика растворения, где h – высота пика, b – его полуширина, ν – скорость развертки потенциала. Плотность предельного диффузионного тока на стадии накопления равна: td – время накопления С другой стороны: id =n·F·m·C, де m – коэффициент массопереноса, С – концентрация аналита. моль/см 3 30
Инверсионная вольтамперометрия Количество электричества, затраченное на электролиз аналита, вычисляют из площади пика растворения, где h – высота пика, b – его полуширина, ν – скорость развертки потенциала. Плотность предельного диффузионного тока на стадии накопления равна: td – время накопления С другой стороны: id =n·F·m·C, де m – коэффициент массопереноса, С – концентрация аналита. моль/см 3 30
 Вращающийся дисковый электрод. Уравнение Левича.
Вращающийся дисковый электрод. Уравнение Левича.
 Кулонометрия. Оценка количества электричества: задачи 1 типа. 32
Кулонометрия. Оценка количества электричества: задачи 1 типа. 32
 Сколько времени потребуется для того, чтобы выделить на электроде 99 % присутствующего в растворе кадмия, если при электролизе в потенциостатических условиях концентрация Cd. SO 4 за 10 мин уменьшилась в 3 раза?
Сколько времени потребуется для того, чтобы выделить на электроде 99 % присутствующего в растворе кадмия, если при электролизе в потенциостатических условиях концентрация Cd. SO 4 за 10 мин уменьшилась в 3 раза?


