Modificational_Variability_03.ppt
- Количество слайдов: 40

Craig Mello & Andrew Fire Нобелевская премия по физиологии и медицине 2006


Nobel Prize in Physiology or Medicine 2006 Craig C. Mello (1960), Andrew Z. Fire (1959) “for their discovery of RNA interference – gene silencing by doublestranded RNA” “за открытие интерференции РНК – подавление экспрессии генов при помощи двуцепочечной РНК”
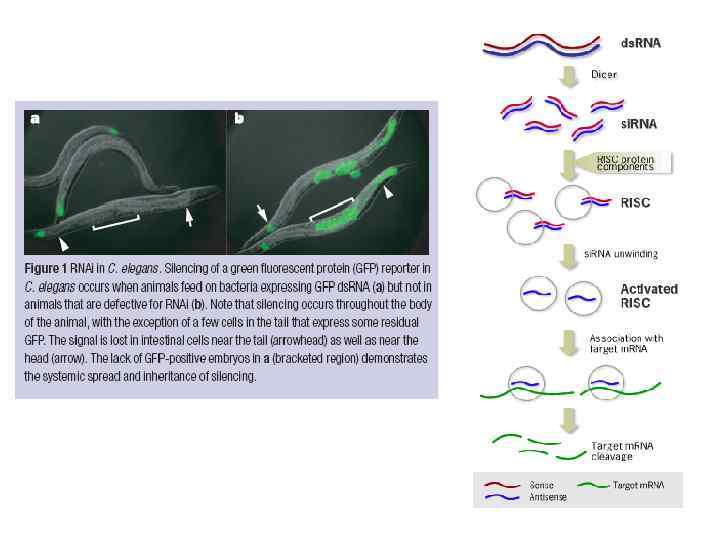
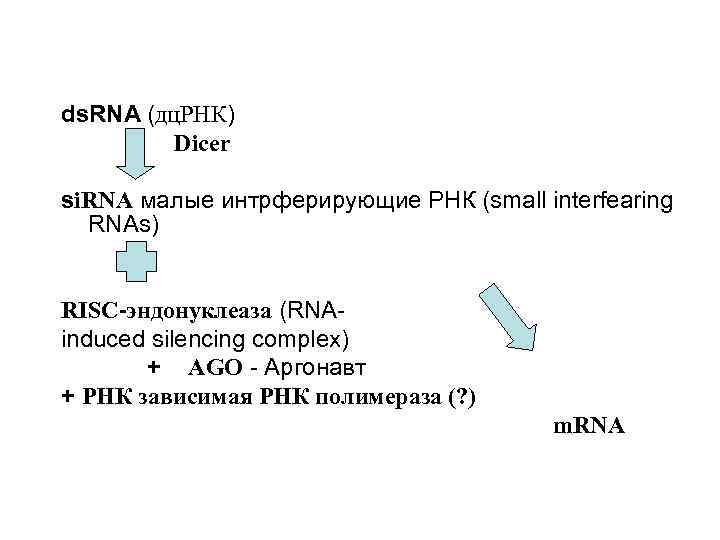
ds. RNA (дц. РНК) Dicer si. RNA малые интрферирующие РНК (small interfearing RNAs) RISC-эндонуклеаза (RNAinduced silencing complex) + AGO - Аргонавт + РНК зависимая РНК полимераза (? ) m. RNA
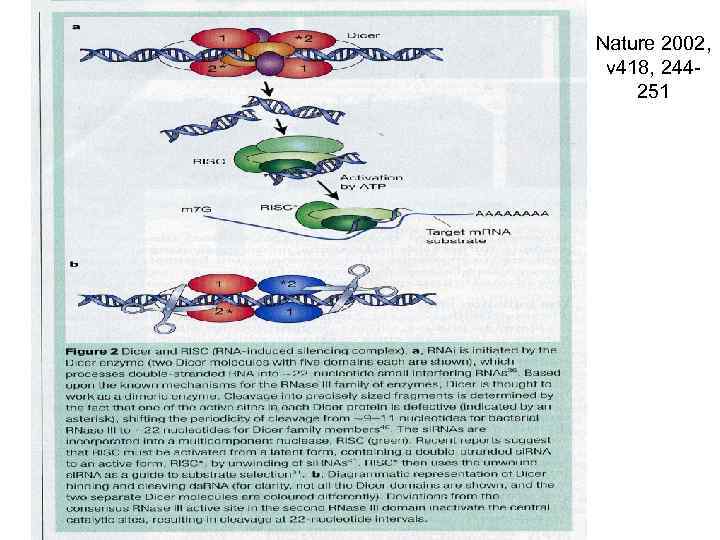
Nature 2002, v 418, 244251
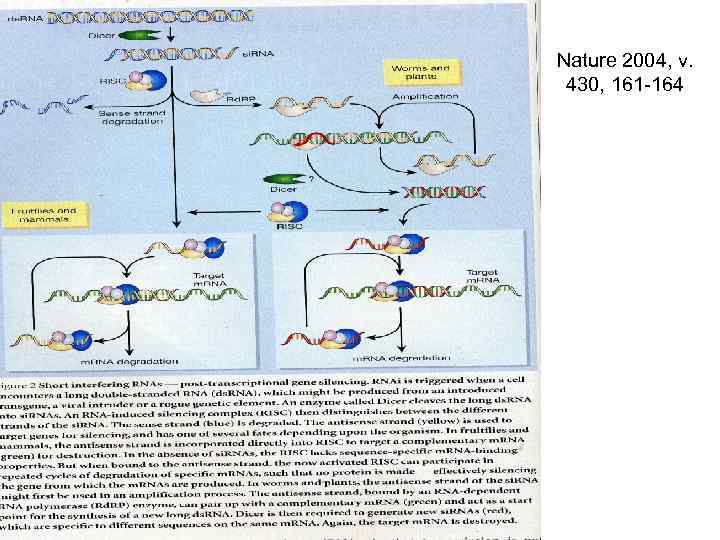
Nature 2004, v. 430, 161 -164
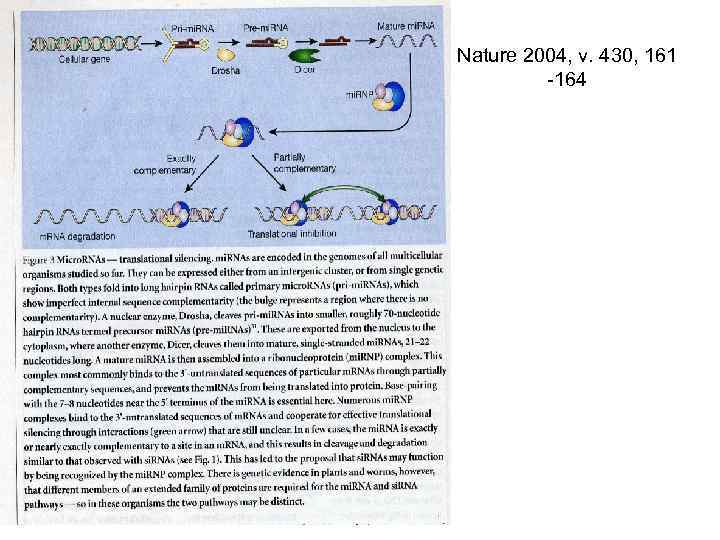
Nature 2004, v. 430, 161 -164
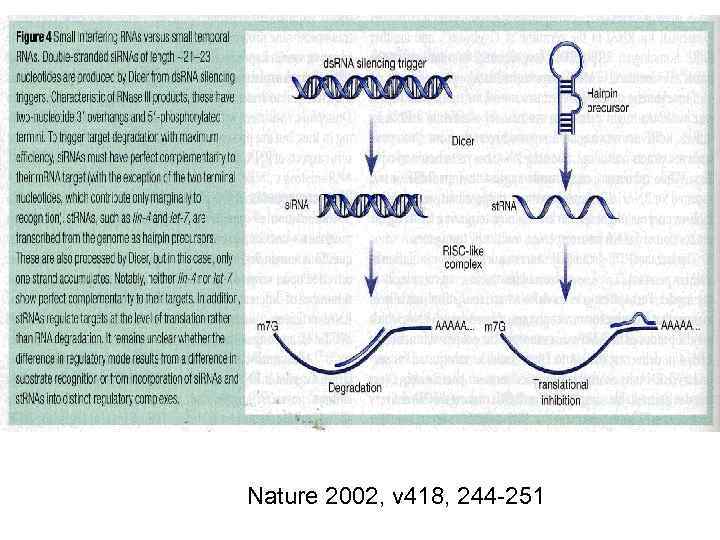
Nature 2002, v 418, 244 -251
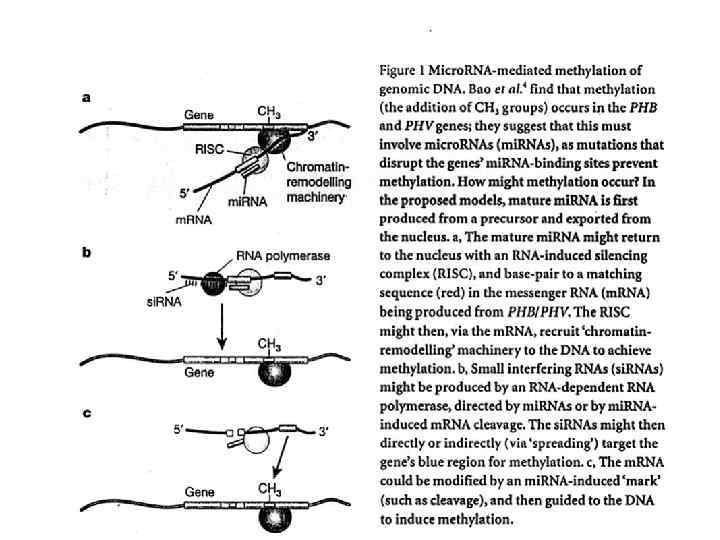

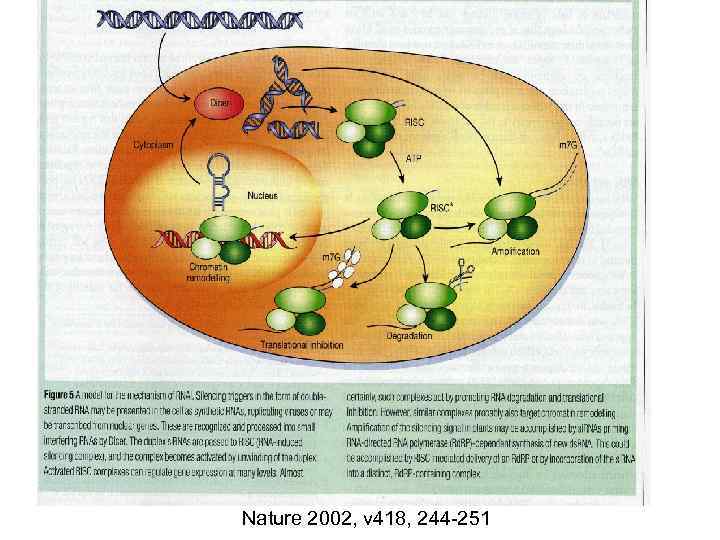
Nature 2002, v 418, 244 -251
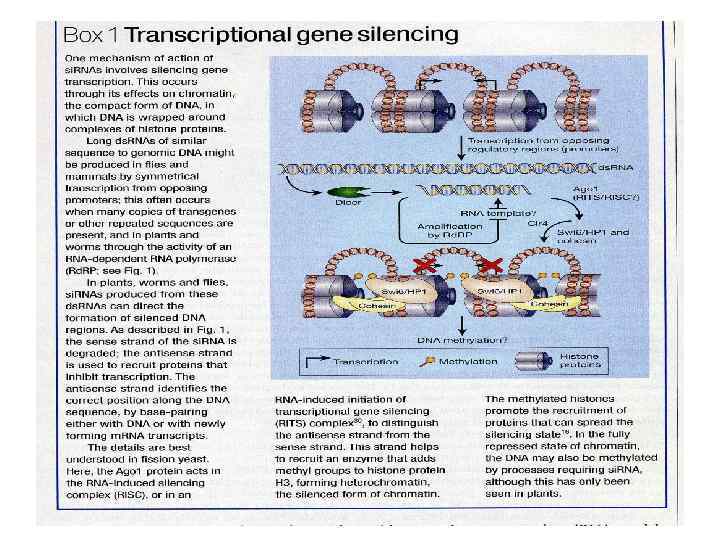
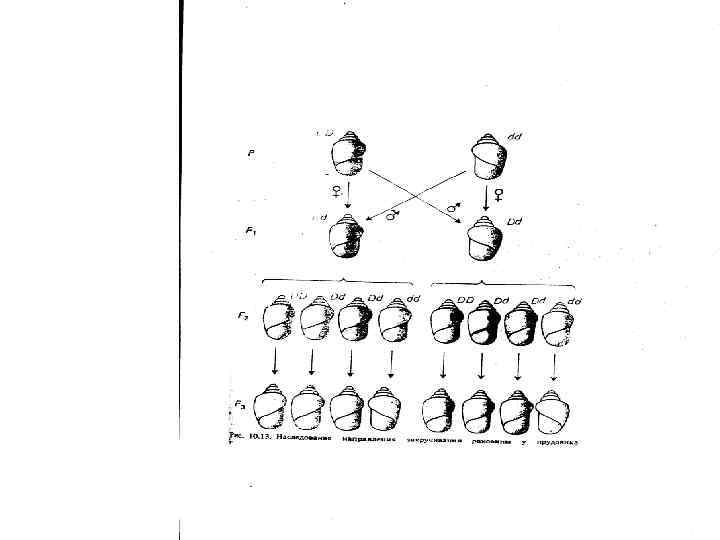

«БЕЛКОВАЯ» ЭПИГЕНЕТИКА Амилоидозы, прионы и «белковая наследственность»

Стенли Прузинер

ИНФЕКЦИОННЫЕ ГУБЧАТЫЕ ЭНЦЕФАЛОПАТИИ (ПРИОННЫЕ БОЛЕЗНИ МЛЕКОПИТАЮЩИХ) Куру Смертельная семейная бессоница (FFI) Болезнь Герштмана-Штросслера-Шайнкера (GSS) Болезнь Кройцфельда-Якоба (CJD) Бычья губчатая энцефалопатия ( «Коровье бешенство» ) Скрэпи (овцы, козы, олени) Инфекционный агент прионных заболеваний млекопитающих – белок Pr. P (Prion Protein) proteinecious infection = pro-in prion
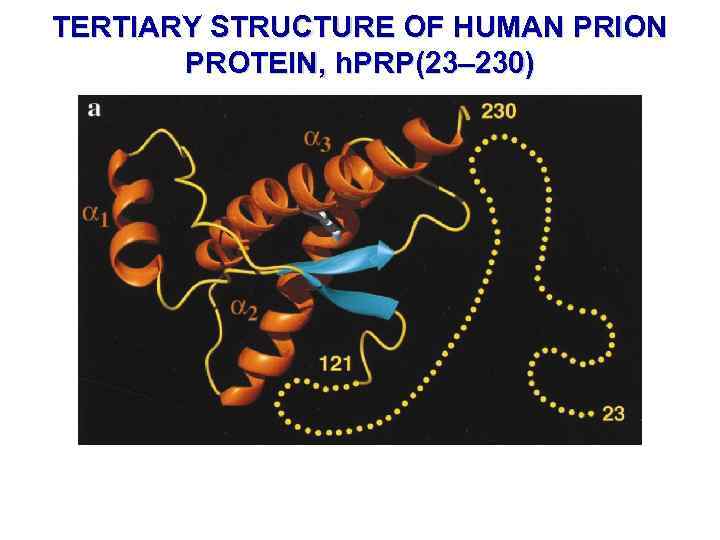
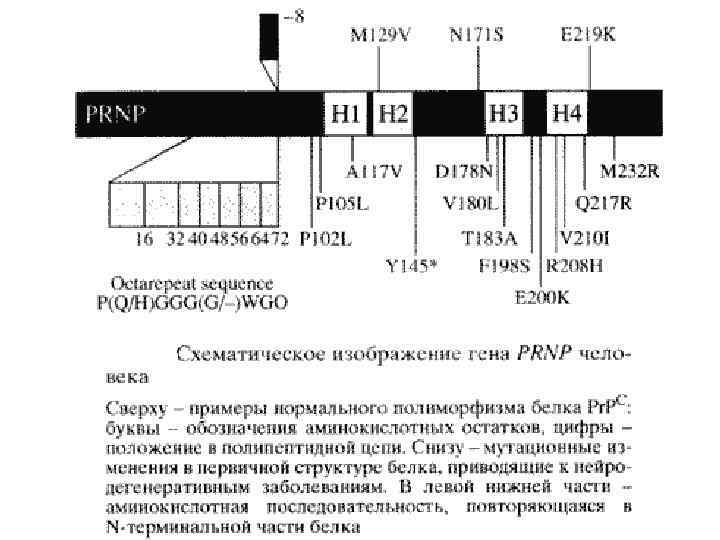
TERTIARY STRUCTURE OF HUMAN PRION PROTEIN, h. PRP(23– 230)
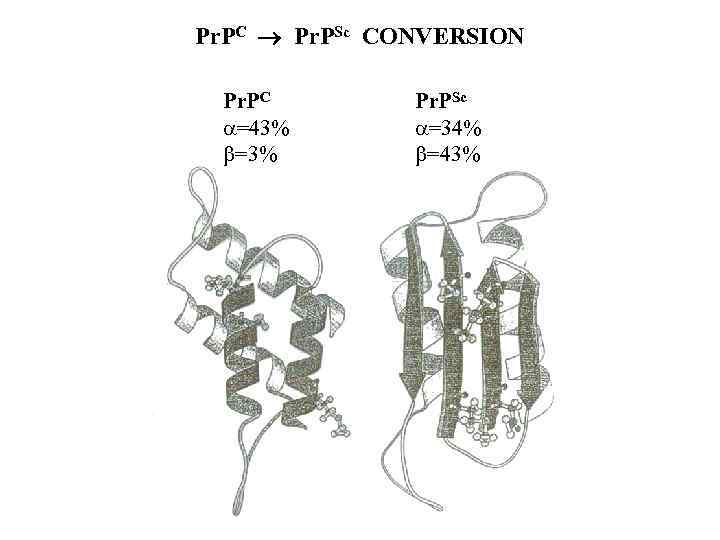
Pr. PC Pr. PSc CONVERSION Pr. PC =43% =3% Pr. PSc =34% =43%
![ПРИОНЫ ГРИБОВ Нехромосоный детерминант (Прион) Ген Виды [PSI+] SUP 35 S. cerevisiae [URE 3] ПРИОНЫ ГРИБОВ Нехромосоный детерминант (Прион) Ген Виды [PSI+] SUP 35 S. cerevisiae [URE 3]](https://present5.com/presentation/14039172_157762545/image-22.jpg)
ПРИОНЫ ГРИБОВ Нехромосоный детерминант (Прион) Ген Виды [PSI+] SUP 35 S. cerevisiae [URE 3] URE 2 S. cerevisiae [PIN+] RNQ 1 S. cerevisiae [Het-s] Het-s P. anserina [ISP+] ? S. cerevisiae [ASP+] ? ? S. cerevisiae
![СУПРЕССИЯ НОНСЕНС – МУТАЦИЙ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] и. РНК ade СУПРЕССИЯ НОНСЕНС – МУТАЦИЙ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] и. РНК ade](https://present5.com/presentation/14039172_157762545/image-23.jpg)
СУПРЕССИЯ НОНСЕНС – МУТАЦИЙ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] и. РНК ade 1 -14 UGA Функциональный белок Sup 35 узнает стоп-кодон UGA, возникший на месте значащего. В результате синтезируется усеченный нефункциональный белок Ade 1 и дрожжи не растут на среде без аденина Прионные агрегаты Sup 35 не узнают стоп-кодон UGA, и он прочитывается как значащий. В результате синтезируется полный функциональный белок Ade 1 и дрожжи растут на среде без аденина
![ВИЗУАЛИЗАЦИЯ ПРИОННЫХ АГРЕГАТОВ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] Растворимые молекулы Sup 35 ВИЗУАЛИЗАЦИЯ ПРИОННЫХ АГРЕГАТОВ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] Растворимые молекулы Sup 35](https://present5.com/presentation/14039172_157762545/image-24.jpg)
ВИЗУАЛИЗАЦИЯ ПРИОННЫХ АГРЕГАТОВ В КЛЕТКАХ [PSI+] клетки [psi-] клетки [PSI+] Растворимые молекулы Sup 35 N-GFP равномерно распределяются по цитоплазме. Прионные молекулы Sup 35 N-GFP образуют бляшки агрегатов. Sup 35 + Sup 35 N-GFP
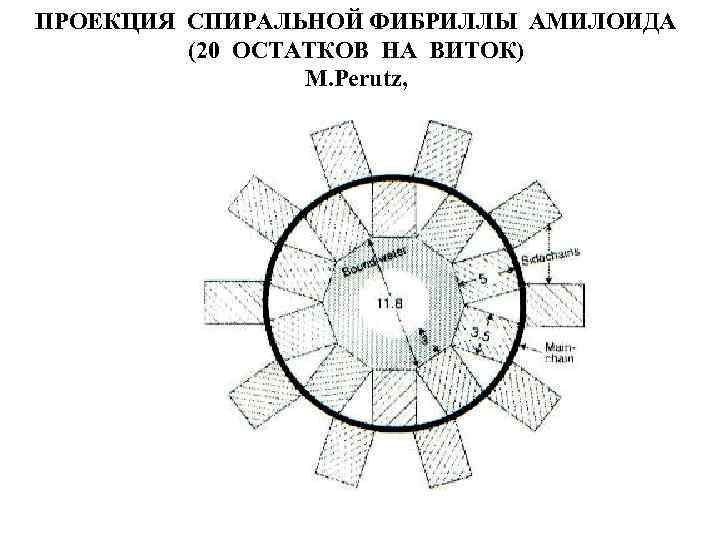
ПРОЕКЦИЯ СПИРАЛЬНОЙ ФИБРИЛЛЫ АМИЛОИДА (20 ОСТАТКОВ НА ВИТОК) M. Perutz,
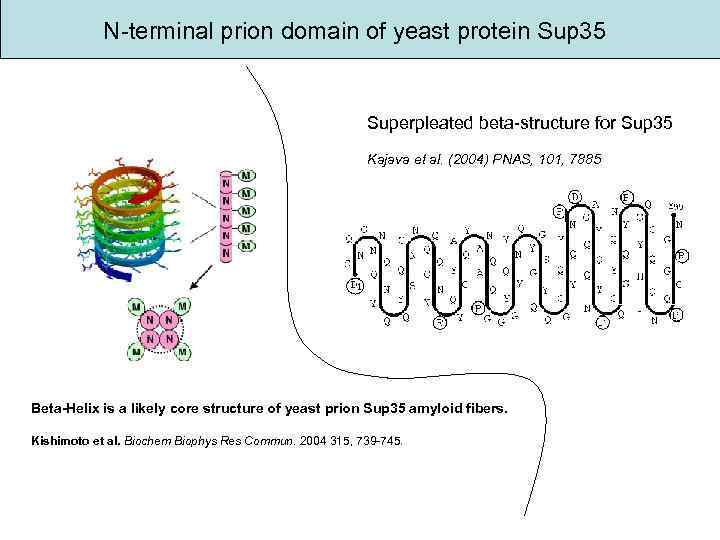
N-terminal prion domain of yeast protein Sup 35 Superpleated beta-structure for Sup 35 Kajava et al. (2004) PNAS, 101, 7885 Beta-Helix is a likely core structure of yeast prion Sup 35 amyloid fibers. Kishimoto et al. Biochem Biophys Res Commun. 2004 315, 739 -745.
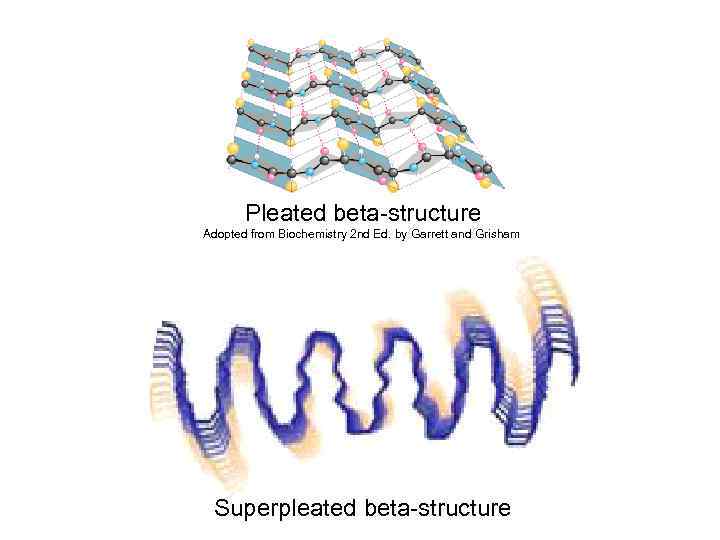
Pleated beta-structure Adopted from Biochemistry 2 nd Ed. by Garrett and Grisham Superpleated beta-structure
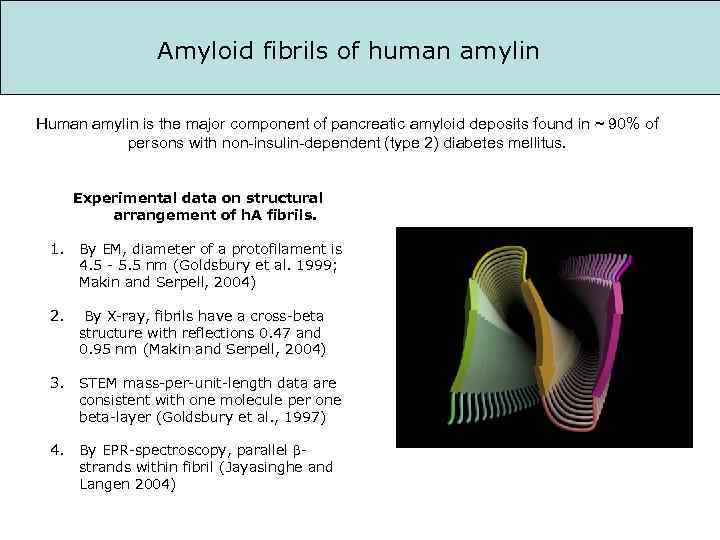
Amyloid fibrils of human amylin Human amylin is the major component of pancreatic amyloid deposits found in ~ 90% of persons with non-insulin-dependent (type 2) diabetes mellitus. Experimental data on structural arrangement of h. A fibrils. 1. By EM, diameter of a protofilament is 4. 5 - 5. 5 nm (Goldsbury et al. 1999; Makin and Serpell, 2004) 2. By X-ray, fibrils have a cross-beta structure with reflections 0. 47 and 0. 95 nm (Makin and Serpell, 2004) 3. STEM mass-per-unit-length data are consistent with one molecule per one beta-layer (Goldsbury et al. , 1997) 4. By EPR-spectroscopy, parallel strands within fibril (Jayasinghe and Langen 2004)
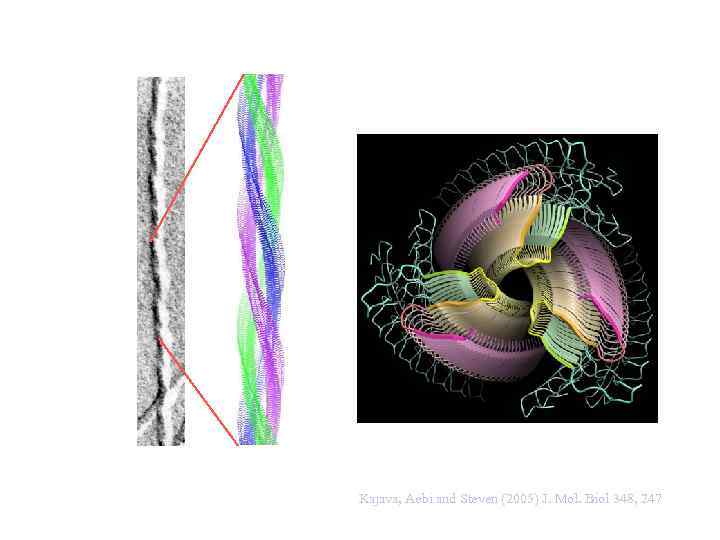
Parallel Superpleated Beta-structure as a Model for Amyloid Fibrils of Human Amylin Kajava, Aebi and Steven (2005) J. Mol. Biol 348, 247
![STRUCTURAL AND FUNCTIONAL ORGANIZATION OF THE Sup 35 PROTEIN AND ITS PRION-FORMING DOMAIN [PSI+] STRUCTURAL AND FUNCTIONAL ORGANIZATION OF THE Sup 35 PROTEIN AND ITS PRION-FORMING DOMAIN [PSI+]](https://present5.com/presentation/14039172_157762545/image-30.jpg)
STRUCTURAL AND FUNCTIONAL ORGANIZATION OF THE Sup 35 PROTEIN AND ITS PRION-FORMING DOMAIN [PSI+] induction and propagation 1 Unknown function 124 N Prion-forming domain 6 28 QN-stretch Essential for viability and translation termination 254 685 M C 41 Imperfect repeats (PQGGYQQ-YN) R 1 *R 6 is an incomplete repeat (PQGG) R 2 R 3 R 4 R 5 97 R 6*
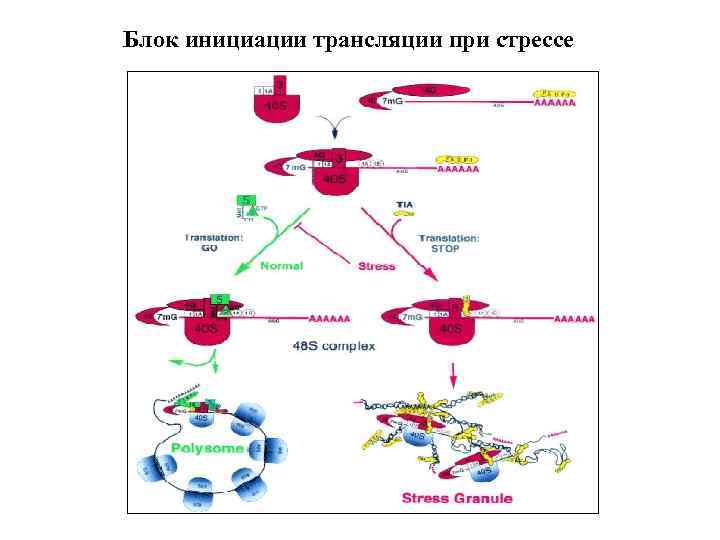
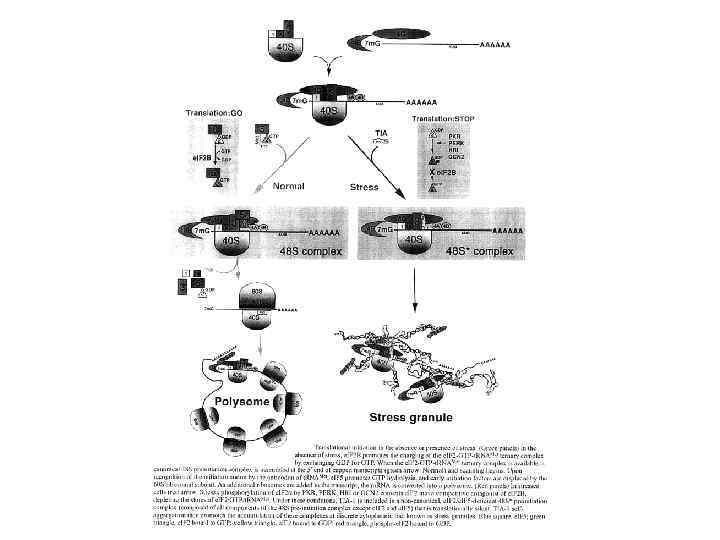
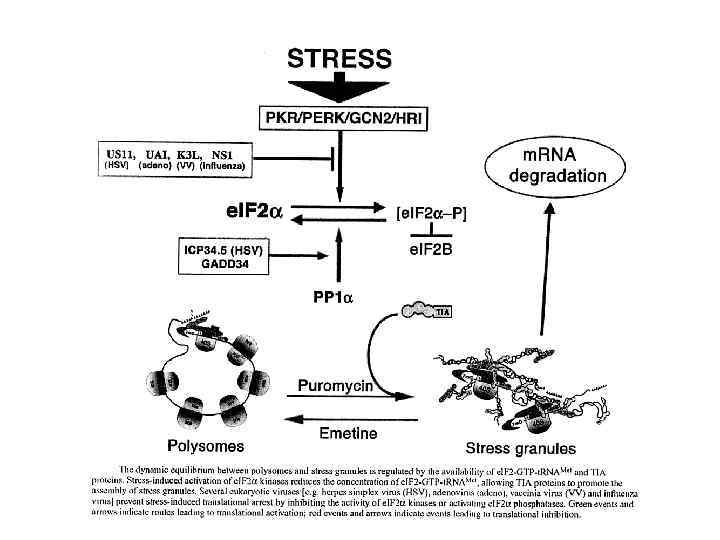
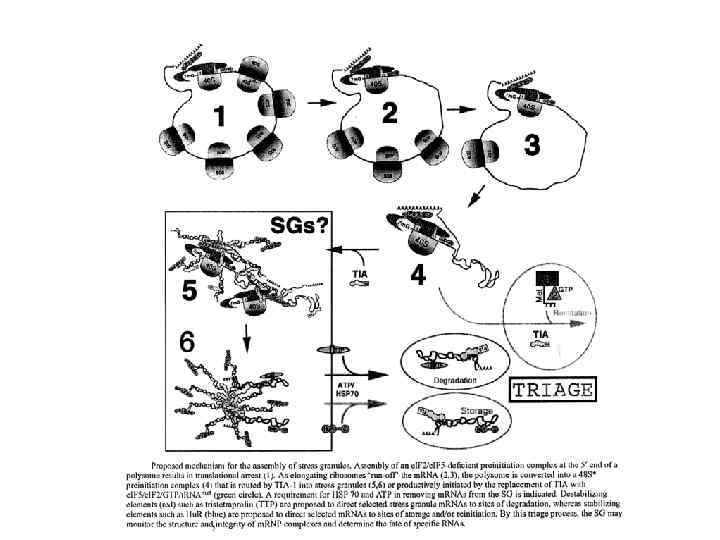
Блок инициации трансляции при стрессе
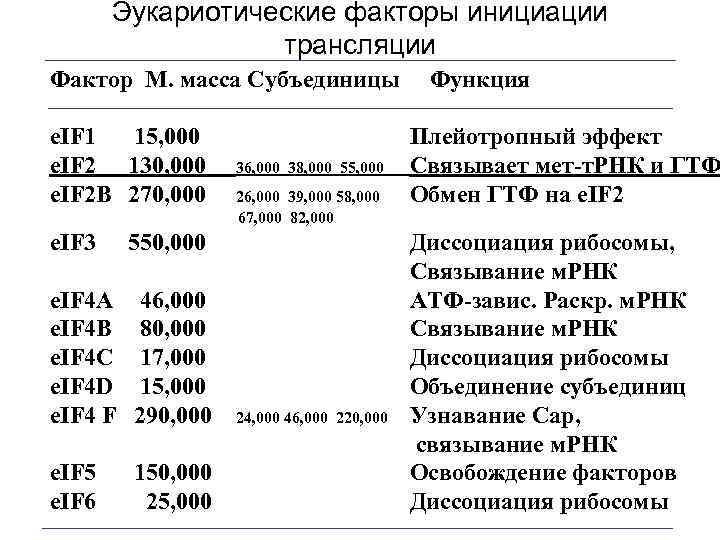
Эукариотические факторы инициации трансляции Фактор М. масса Субъединицы e. IF 1 15, 000 e. IF 2 130, 000 e. IF 2 B 270, 000 e. IF 3 46, 000 80, 000 17, 000 15, 000 290, 000 e. IF 5 e. IF 6 150, 000 25, 000 26, 000 39, 000 58, 000 67, 000 82, 000 550, 000 e. IF 4 A e. IF 4 B e. IF 4 C e. IF 4 D e. IF 4 F 36, 000 38, 000 55, 000 24, 000 46, 000 220, 000 Функция Плейотропный эффект Связывает мет-т. РНК и ГТФ Обмен ГТФ на e. IF 2 Диссоциация рибосомы, Связывание м. РНК АТФ-завис. Раскр. м. РНК Связывание м. РНК Диссоциация рибосомы Объединение субъединиц Узнавание Cap, связывание м. РНК Освобождение факторов Диссоциация рибосомы
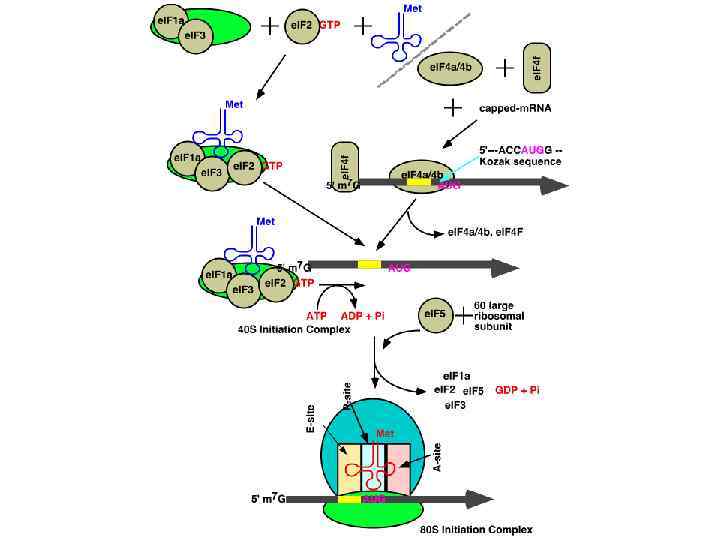
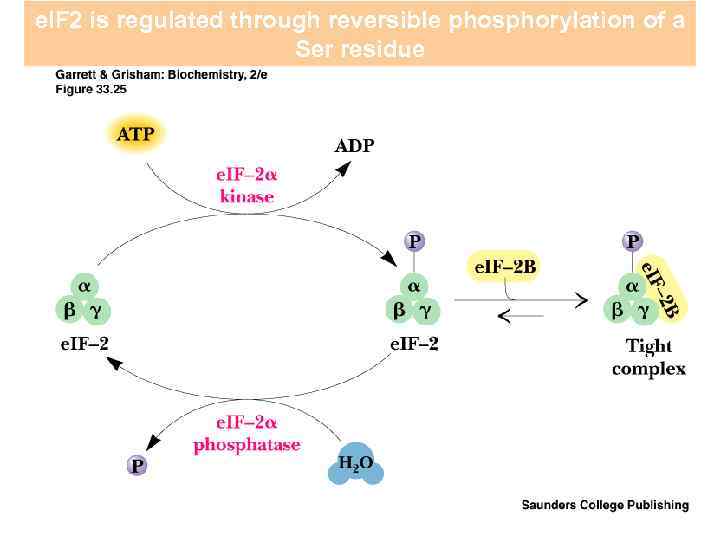
e. IF 2 is regulated through reversible phosphorylation of a Ser residue

Aplysia californica • Sea snail • Large nerve cells

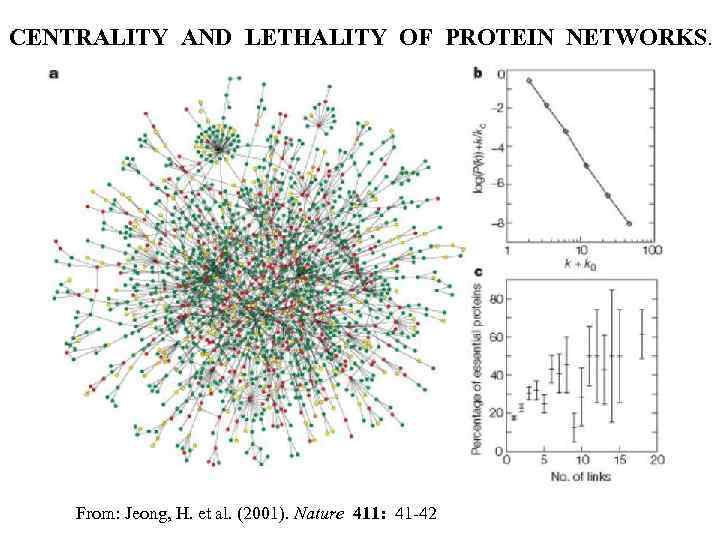
CENTRALITY AND LETHALITY OF PROTEIN NETWORKS. From: Jeong, H. et al. (2001). Nature 411: 41 -42
Modificational_Variability_03.ppt