feb5e09f32e478cb183361b096dd3abb.ppt
- Количество слайдов: 86

Cobertura social de los medicamentos: aspectos médicos, legales y organizativos. Martín A. Urtasun - 2010

Cobertura de medicamentos • Aspectos médicos: ¿Para qué sirven los medicamentos? ¿Es necesario cubrirlos a todos? El concepto de medicamentos esenciales • Aspectos legales: ¿Cuál es el marco legal que rige en nuestro país el registro, la prescripción y la cobertura? • Aspectos organizativos: ¿Cuáles son las opciones para implementar la cobertura? ¿Qué variables monitorear y cómo interpretarlas?

¿Para qué sirven los medicamentos? • Desde la Medicina: Para prolongar y/o mejorar la calidad de vida de las personas. • Desde la Antropología: Para responder a las demandas de alivio y de curación frente a la realidad de la vejez, la enfermedad y la muerte. • Desde la Economía: Para generar un importante sector industrial, con alto nivel de innovación y óptimo margen de rentabilidad.
Necesidad Oferta Demanda

Fases del desarrollo de un nuevo medicamento • Investigación pre-clínica Estudios in vitro Estudios de eficacia y toxicidad en animales • Investigación clínica Fase 1: voluntarios sanos: seguridad, metabolismo Fase 2: pacientes seleccionados: eficacia, rango de dosis Fase 3: grandes muestras de pacientes: eficacia, seguridad Fase 4: vigilancia post-comercialización: seguridad

Fases del desarrollo de un nuevo medicamento (2) Problemas: • No hay pruebas de eficacia en Fase 3: – Se comercializan drogas que nunca demostraron eficacia en estudios controlados, bien diseñados y conducidos. – Se comercializan combinaciones de drogas que no han sido estudiadas en fase 3. • No hay vigilancia / control en Fase 4: – No se vigilan los efectos adversos de las drogas nuevas con su uso masivo post- comercialización. – No se controla el uso de las drogas autorizadas con dosis/ indicaciones / pacientes para las que nunca fueron evaluadas.

¡No todos los medicamentos tienen el mismo valor terapéutico potencial ! • VTP elevado: drogas con eficacia demostrada en ensayos clínicos controlados. • VTP relativo: combinaciones de drogas de VTP elevado con otras de valor dudoso/nulo. • VTP dudoso/nulo: eficacia no demostrada en ensayos controlados, pero sin efectos adversos graves o frecuentes. • VTP inaceptable: la relación beneficio/riesgo es claramente desfavorable.
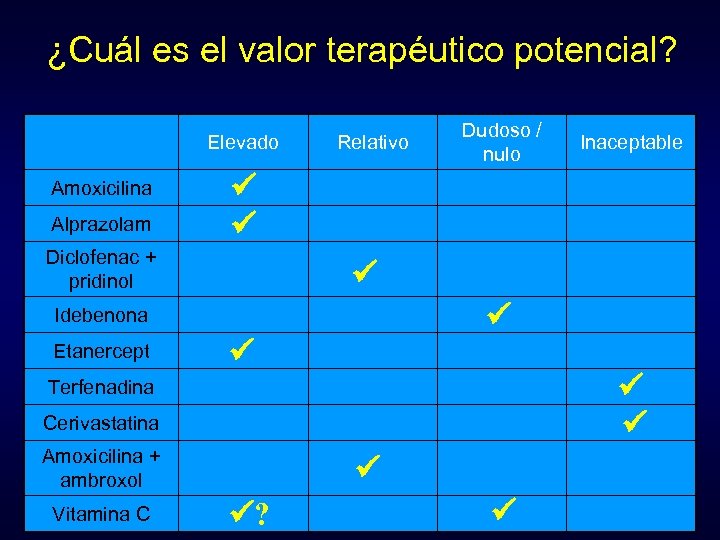
¿Cuál es el valor terapéutico potencial? Elevado Amoxicilina Alprazolam Relativo Idebenona Terfenadina Cerivastatina Amoxicilina + ambroxol Vitamina C Inaceptable Diclofenac + pridinol Etanercept Dudoso / nulo ?
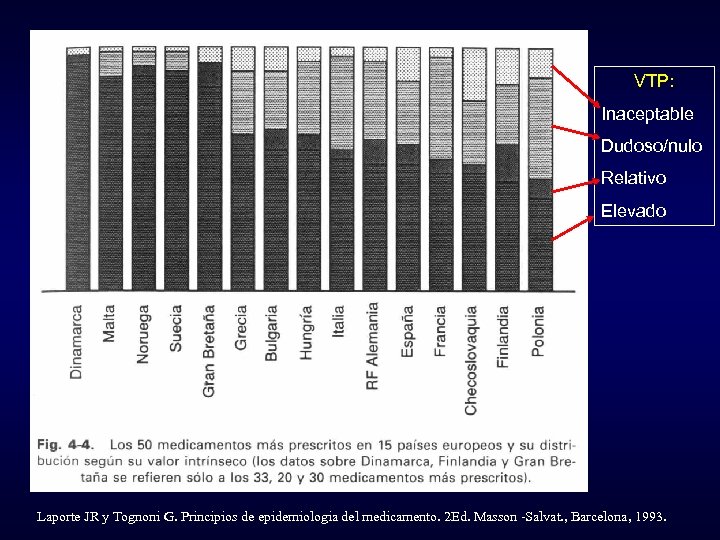
VTP: Inaceptable Dudoso/nulo Relativo Elevado Laporte JR y Tognoni G. Principios de epidemiologia del medicamento. 2 Ed. Masson -Salvat. , Barcelona, 1993.

Medicamentos esenciales • La OMS los define como: “. . . los medicamentos que sirven para satisfacer las necesidades de atención de salud de la mayor parte de la población. " • Por lo tanto: – No es una “receta” única, sino que debe adaptarse a las necesidades de salud locales. – Recordar que puede haber casos de excepción que no se resuelven con el listado básico.

¿Cuántos son los medicamentos disponibles en el país? Principios activos 1. 750 Marcas comerciales 6. 600 Presentaciones 13. 300
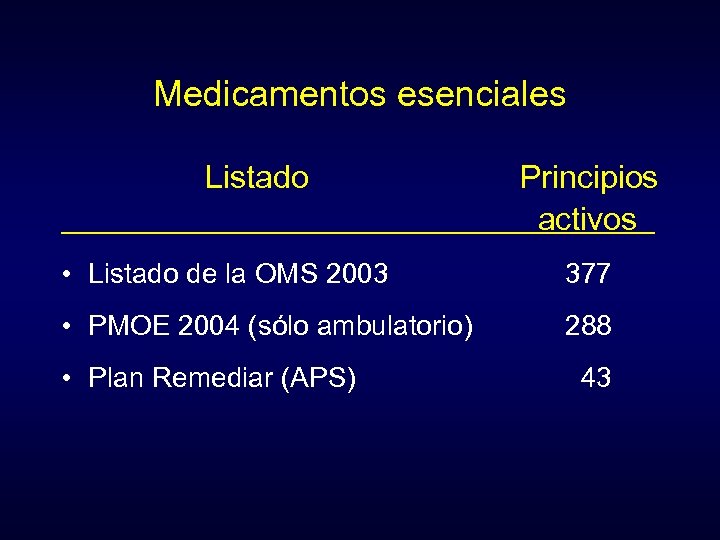
Medicamentos esenciales Listado Principios activos • Listado de la OMS 2003 377 • PMOE 2004 (sólo ambulatorio) 288 • Plan Remediar (APS) 43

Medicamentos del botiquín Remediar AMOXICILINA ERITROMICINA MEBENDAZOL GLIBENCLAMIDA HIOSCINA FUROSEMIDA DIGOXINA ENALAPRIL BETAMETASONA IBUPROFENO CARBAMACEPINA METRONIDAZOL GENTAMICINA DIFENHIDRAMINA CEFALEXINA COTRIMOXAZOL NORFLOXACINA PENICILINA G BENZ. METRONIDAZOL POLIVITAMINICO METFORMINA RANITIDINA NISTATINA SALES DE REHIDROCLOROTIAZIDA AMIODARONA ISOSORBIDE DINITR. ATENOLOL SULFATO FERROSO SULFATO FE+FOLICO DEXAMETASONA LEVOTIROXINA PARACETAMOL AC. VALPROICO FENITOINA LEVODOPA+CARBID. NISTATINA ERGONOVINA BUDESONIDE SALBUTAMOL CLOTRIMAZOL

Aspectos médicos: conclusiones • El uso de los medicamentos resulta de la interacción entre las necesidades sanitarias, las demandas de los usuarios y la presión de la industria. • Hay muchos más medicamentos en el mercado de los que son necesarios. Algunos son efectivos pero redundantes, muchos son inútiles y unos pocos son peligrosos. • La cobertura social debe limitarse a los medicamentos efectivos y evitar las duplicaciones innecesarias.

Aspectos legales • Registro de medicamentos: La ANMAT y los requisitos para registrar un nuevo producto. • Prescripción por nombre genérico: Ley 25. 649 • Dispensa exclusiva en farmacias: Ley 26. 567 • Cobertura social de los medicamentos: - Programa Médico Obligatorio - Listado de medicamentos - Niveles de cobertura - Normas de uso

Registro de Medicamentos Decreto 150/92: se autorizan automáticamente los medicamentos que estén comercializados en al menos uno de los siguientes países: – – – – Estados Unidos Japón Suecia Confederación Helvética Israel Canadá Austria Alemania – Francia – Reino Unido – Países Bajos – Bélgica – Dinamarca – España – Italia

Medicamentos genéricos

Medicamentos genéricos 1) “Nombre genérico” vs “medicamento genérico”. 2) El problema de la intercambiabilidad. 3) Marco legal vigente. 4) Algunos resultados de su aplicación.

Medicamentos genéricos 1) “Nombre genérico” vs “medicamento genérico”. 2) El problema de la intercambiabilidad. 3) Marco legal vigente. 4) Algunos resultados de su aplicación.

• Nombre genérico = denominación oficialmente aceptada en cada país para un principio activo (que puede ser o no la Denominación Común Internacional de la OMS). • Medicamento genérico = aquél que ha demostrado equivalencia terapéutica con otro que es utilizado como referencia legal. • Es una categoría legal prevista en el marco regulatorio de los países que tienen una “ley de genéricos”. • En la Argentina no existe esa ley, por lo que no existen tampoco medicamentos genéricos. • Una presentación comercial cuyo nombre es el nombre genérico de la droga más el del laboratorio productor, no es por este motivo un medicamento genérico.
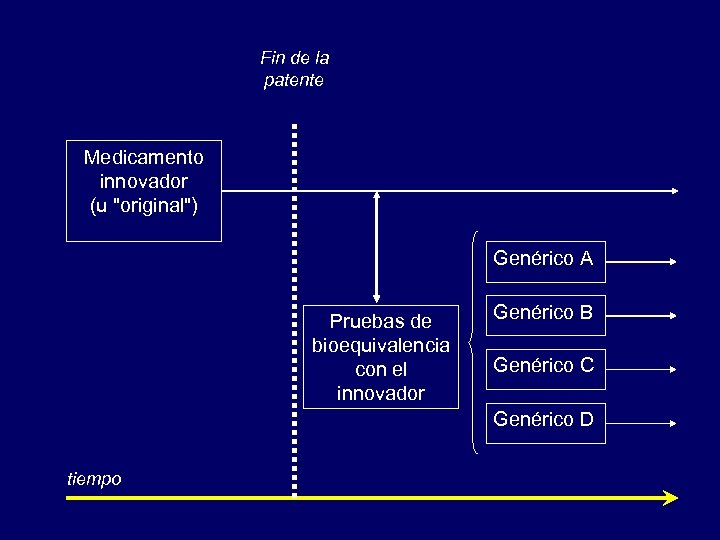
Fin de la patente Medicamento innovador (u "original") Genérico A Pruebas de bioequivalencia con el innovador Genérico B Genérico C Genérico D tiempo
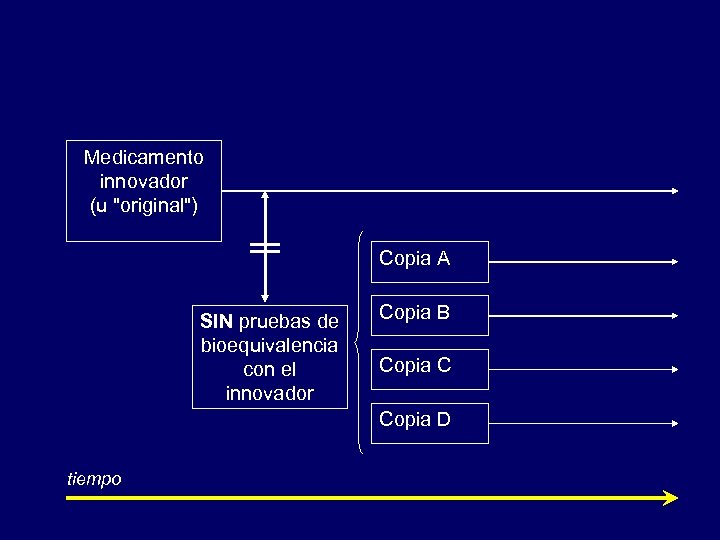
Medicamento innovador (u "original") Copia A SIN pruebas de bioequivalencia con el innovador Copia B Copia C Copia D tiempo

Equivalentes farmacéuticos: igual Principio activo Forma farmacéutica Concentración (No necesariamente son equivalentes terapéuticos ni intercambiables) Medicamentos bioequivalentes: Equivalentes farmacéuticos + Igual biodisponibilidad (Los medicamentos bioequivalentes se asumen como equivalentes terapéuticos y por lo tanto como intercambiables). Medicamento genérico: aquél que ha demostrado equivalencia terapéutica con otro que es utilizado como referencia legal (puede ser el medicamento "innovador" u otro de referencia) y por lo tanto es intercambiable.

Medicamentos genéricos 1) “Nombre genérico” vs “medicamento genérico”. 2) El problema de la intercambiabilidad. 3) Marco legal vigente. 4) Algunos resultados de su aplicación.

¿Es seguro intercambiar productos en ausencia de pruebas de bioequivalencia? Depende. . . 1) Hay formas farmacéuticas y/o vías de administración que NO requieren estudios de bioequivalencia. 2) El resto de los medicamentos se puede clasificar según su riesgo sanitario: alto intermedio bajo

Formas farmacéuticas y/o vías de administración que NO requieren estudios de bioequivalencia (1) 1) Soluciones acuosas que se administran por vía parenteral (intravenosa, intramuscular, subcutánea o intratecal), que contengan idénticos principios activos en las mismas concentraciones y esencialmente los mismos excipientes. 2) Soluciones para uso oral que contienen idénticos principios activos en la misma concentración. 3) Polvos o granulados para ser reconstituidos como solución, cuando la solución satisfaga los criterios anteriores.

Formas farmacéuticas y/o vías de administración que NO requieren estudios de bioequivalencia (2) 4) Gases de uso medicinal. 5) Especialidades medicinales óticas u oftálmicas que contengan idénticos principios activos en las mismas concentraciones y esencialmente los mismos excipientes. 6) Medicamentos de aplicación tópica, dérmica o mucosa sin efecto terapéutico sistémico que contengan idénticos principios activos en las mismas concentraciones y esencialmente los mismos excipientes.

Formas farmacéuticas y/o vías de administración que NO requieren estudios de bioequivalencia (3) 7) Especialidades medicinales inhalables o aerosoles nasales en soluciones acuosas que contengan idénticos principios activos en las mismas concentraciones por unidad de dosis de administración. 8) Especialidades medicinales de administración oral cuyos principios activos no necesiten ser absorbidos para ejercer su acción terapéutica.

Clasificación de los medicamentos según su RIESGO SANITARIO (RS) Si la concentración sanguínea de esta droga NO se encuentra en la ventana terapéutica, ¿qué puede suceder? Complicaciones de la enfermedad que amenazan la vida o la integridad psicofísica de la persona y/o RS Alto reacciones adversas graves. Complicaciones de la enfermedad que no amenazan la vida o la integridad psicofísica de la persona y/o reacciones adversas no graves. RS Inter medio Complicaciones menores de la enfermedad y/o reacciones adversas leves. RS Bajo

Drogas de riesgo sanitario alto • • Carbamazepina Oxcarbazepina Etosuximida Fenitoína Valproato Lamotrigina Topiramato • Antirretrovirales • • Insulinas Tolbutamida • • • Ciclosporina Tacrolimus Sirolimus Everolimus Micofenolato Quinidina Verapamilo Digoxina • • Piridostigmina Levodopa-carbidopa Levodopa-benserazida Carbonato de litio • • todas deben realizar estudios de bioequivalencia Warfarina (an. Mat) Procainamida Isotretinoína Teofilina

Drogas de riesgo sanitario intermedio: ejemplos • • • Amitriptilina Atenolol Azatioprina Biperideno Carbidopa Clomipramina Diazepam Etambutol Etinilestradiol • • • Levodopa Levonorgestrel Mefloquina Mercaptopurina Metildopa Metotrexate Noretisterona Propranolol Tamoxifeno

Drogas de riesgo sanitario bajo: ejemplos • • • Allopurinol Amilorida Amoxicilina Cimetidina Ciprofloxacina Clorpromazina Dinitrato de isosorbide Furosemida Haloperidol • • • Ibuprofeno Isoniazida Ketoconazol Mebendazol Metoclopramida Nifedipina Nitrofurantoína Prednisolona Tetraciclina

Medicamentos genéricos 1) “Nombre genérico” vs “medicamento genérico”. 2) El problema de la intercambiabilidad. 3) Marco legal vigente. 4) Algunos resultados de su aplicación.

Promoción de la utilización de medicamentos por su nombre genérico Ley 25. 649 Sancionada: agosto de 2002 Reglamentada: abril de 2003

Puntos principales • Toda receta debe contener: – Nombre genérico del principio activo – Forma farmacéutica – Concentración – Cantidad de unidades por envase • La receta que sólo consigne la marca se tendrá por no prescripta, no siendo válida para el expendio del medicamento.

Puntos principales (2) • Puede colocarse la marca o nombre comercial a continuación del genérico. • Si el prescriptor considera indispensable prescribir por marca, debe agregar una justificación que avale tal decisión, de su puño y letra, firmando nuevamente.

Puntos principales (3) • El farmacéutico debe asesorar sobre las especialidades que contengan el principio activo recetado y sus distintos precios. • Sólo puede ofrecer especialidades inscriptas en la ANMAT. • A pedido del consumidor, debe dispensar el medicamento con menor precio que el prescripto, registrándolo en la receta, con su firma y sello.

Puntos principales (4) • Si se prescribió con “justificación de marca” y el adquirente solicita otro medicamento de menor precio, el farmacéutico puede reemplazarlo si el consumidor firma su conformidad. • La ANMAT mantendrá un listado de aquellas especialidades medicinales que se desaconseja reemplazar, por razones de biodisponibilidad o estrecho margen terapéutico.
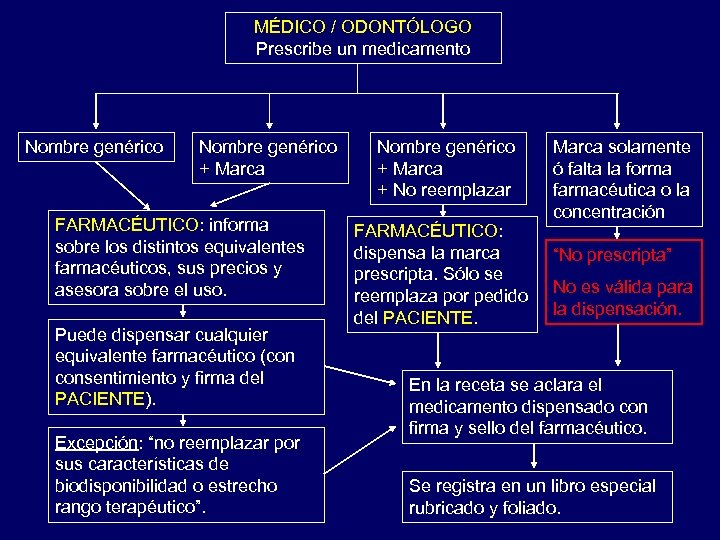
MÉDICO / ODONTÓLOGO Prescribe un medicamento Nombre genérico + Marca FARMACÉUTICO: informa sobre los distintos equivalentes farmacéuticos, sus precios y asesora sobre el uso. Puede dispensar cualquier equivalente farmacéutico (con consentimiento y firma del PACIENTE). Excepción: “no reemplazar por sus características de biodisponibilidad o estrecho rango terapéutico”. Nombre genérico + Marca + No reemplazar FARMACÉUTICO: dispensa la marca prescripta. Sólo se reemplaza por pedido del PACIENTE. Marca solamente ó falta la forma farmacéutica o la concentración “No prescripta” No es válida para la dispensación. En la receta se aclara el medicamento dispensado con firma y sello del farmacéutico. Se registra en un libro especial rubricado y foliado.

Medicamentos genéricos 1) “Nombre genérico” vs “medicamento genérico”. 2) El problema de la intercambiabilidad. 3) Marco legal vigente. 4) Algunos resultados de su aplicación.
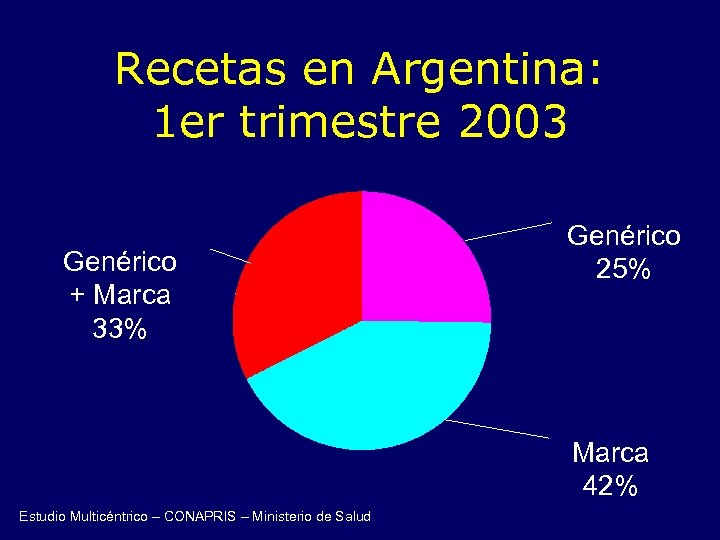
Recetas en Argentina: 1 er trimestre 2003 Genérico + Marca 33% Genérico 25% Marca 42% Estudio Multicéntrico – CONAPRIS – Ministerio de Salud
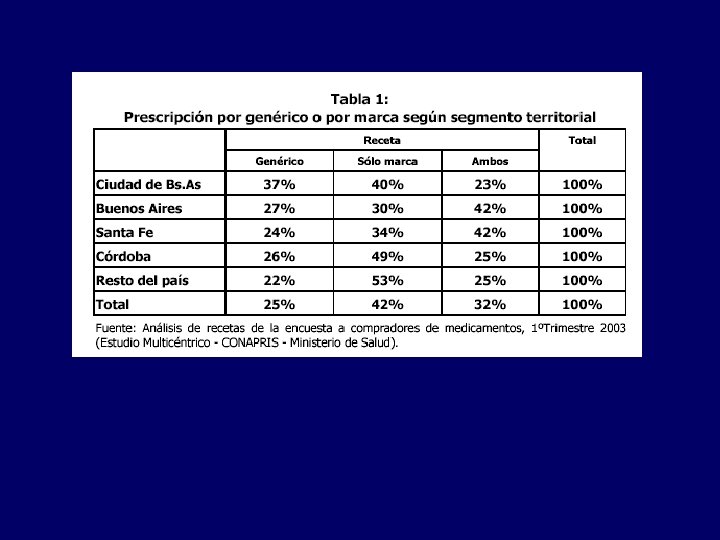
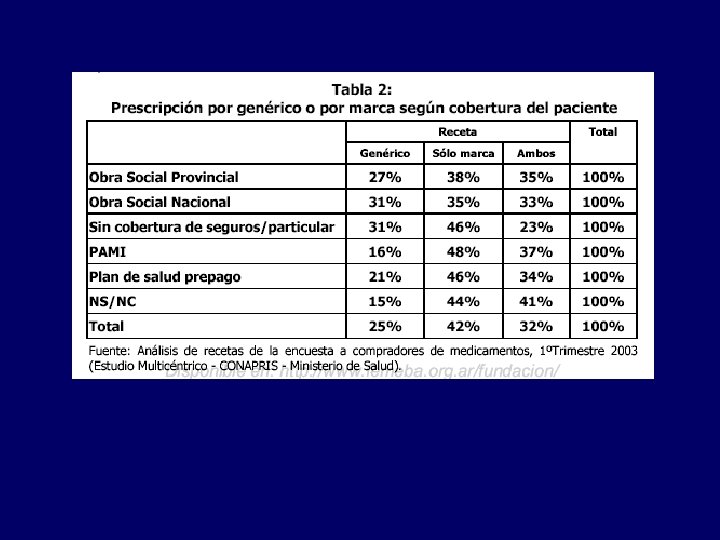
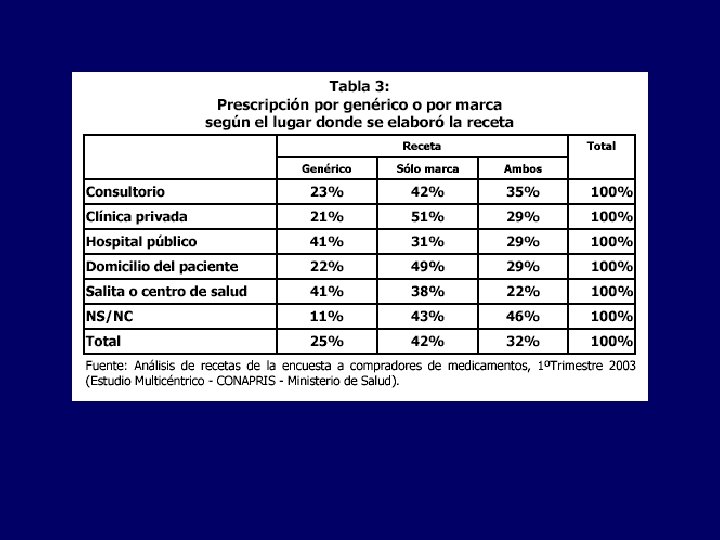
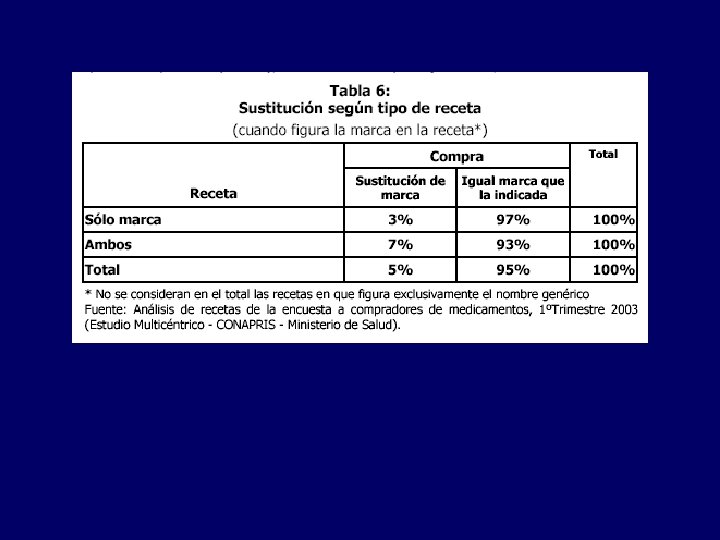
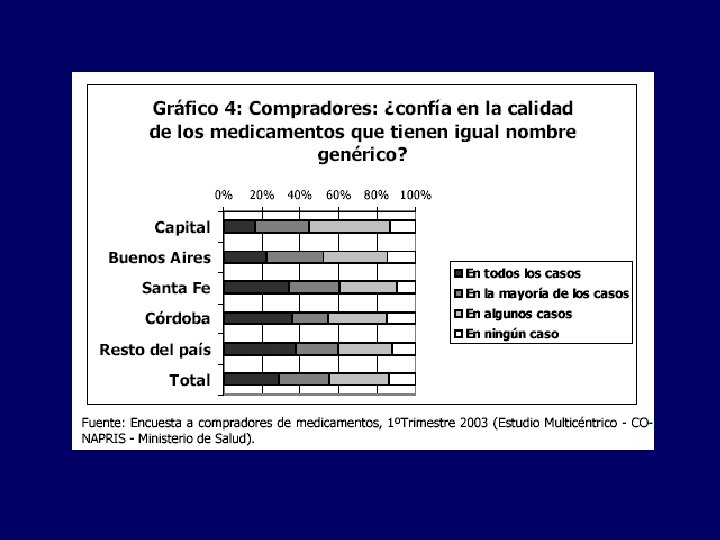
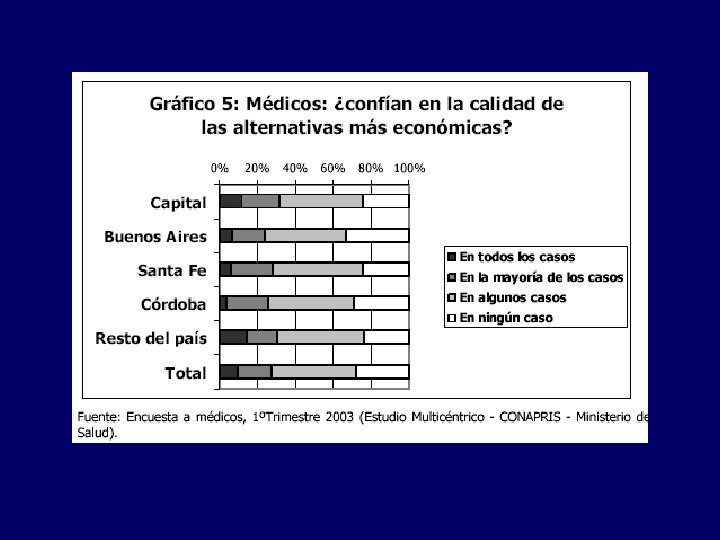
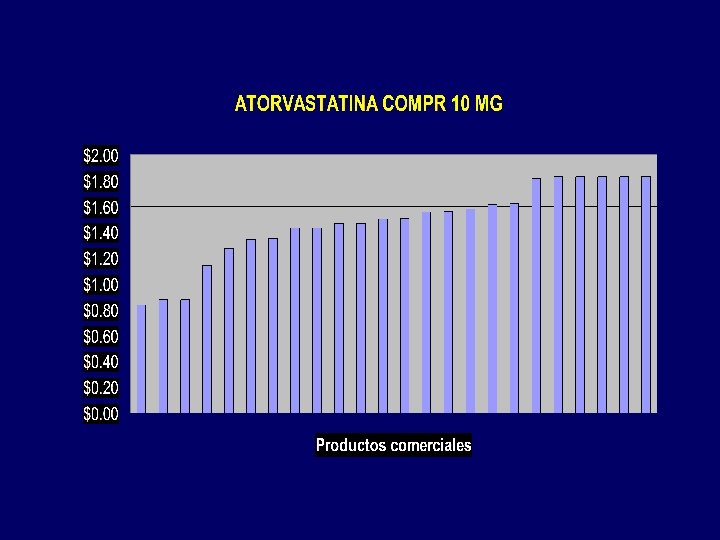
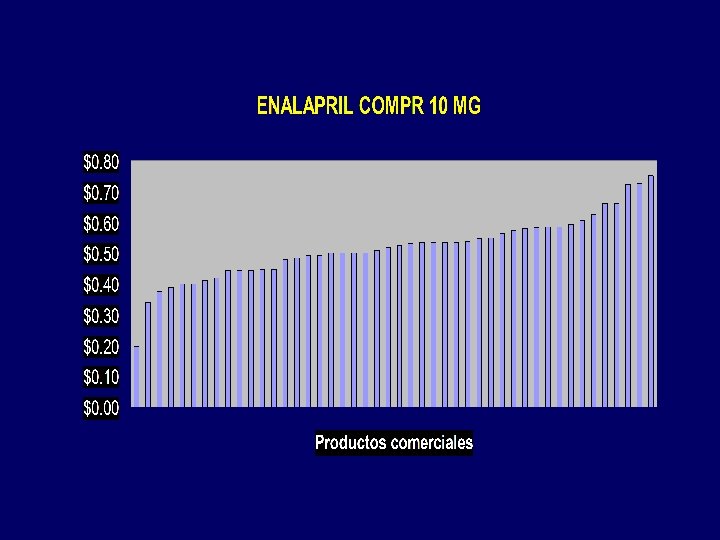
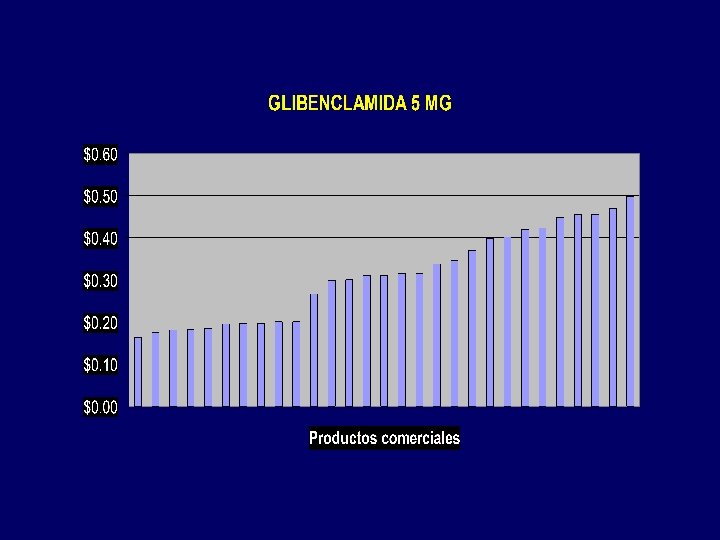

Aspectos legales: Dispensa

Ley 26. 567 (nov 2009): modifica la Ley Nº 17. 565 de Ejercicio de la actividad farmacéutica • Artículo 1º: La preparación de recetas, la dispensa de drogas, medicamentos, incluidos los denominados de venta libre y de especialidades farmacéuticas, cualquiera sea su condición de expendio, sólo podrán ser efectuadas en todo el territorio de la Nación, en farmacias habilitadas. • Los medicamentos denominados de venta libre deberán ser dispensados personalmente en mostrador por farmacéuticos o personas autorizadas para el expendio. • La autoridad sanitaria competente podrá disponer la incorporación de otro tipo de productos al presente régimen. • Su venta y despacho fuera de estos establecimientos se considera ejercicio ilegal de la farmacia y, sin perjuicio de las sanciones establecidas por la ley, los que la efectúen podrán ser denunciados por infracción al Código Penal.

Cobertura obligatoria de medicamentos en la seguridad social

Medicamentos en el PMOE • Alcance: el PMO es obligatorio para las obras sociales nacionales y las empresas de medicina prepaga. • Medicamentos en internación: cobertura del 100%; no hay un listado oficial. • Tratamientos oncológicos: según protocolos (que no están vigentes actualmente). • Medicamentos ambulatorios (Res 310/04): – Un listado de medicamentos. – Con distintos niveles de cobertura (40, 70 o 100%). – Con recomendaciones de uso para algunas drogas. – El monto a cubrir por la seguridad social.

Ambulatorio: Resolución 310/04 • Listado: 288 principios activos, distribuidos en un listado principal y otro complementario. • Incluye: Patologías prevalentes Diabetes mellitus VIH / SIDA; Lepra; Tuberculosis Vacunas Anticonceptivos Drogas de alto costo/baja prevalencia

Ambulatorio: Resolución 310/04 (2) • Cobertura: es un monto fijo para las distintas marcas de una misma droga, que calcula el Ministerio como un porcentaje del precio promedio de las presentaciones comerciales. • Por lo tanto, el porcentaje de cobertura variará según la marca: Droga Marca PVP Amlodipina (10 mg x 30) A B C $35 $45 $60 Monto fijo $30 $30 • Por Resol. 82/2005: cobertura máxima del 70% % 86% 67% 50%

Ambulatorio: Resolución 310/04 (3) • Cobertura: hay 3 niveles: 40, 70 y 100%. 40%: Es la cobertura base. 70%: Para enfermedades crónicas: Hipertensión arterial Enfermedad coronaria Insuficiencia cardíaca Arritmias Hiperlipidemia 100%: Diabetes (orales) Artritis reumatoidea Gota Hipo/hipertiroidismo Enf de Crohn /CU Para patologías especiales Plan Materno-Infantil Asma Glaucoma Psicosis Epilepsia

Ambulatorio: Resolución 310/04 (4) • Cobertura del 100%: Insulina Anticonceptivos VIH/SIDA Teicoplanina TBC Interferón (hepatitis viral) Factor antihemofílico Interferón/glatiramer (E. múltiple) Eritropoyetina en IRC Factor estimulante de colonias Somatotrofina Ondansetron (en oncológicos) Octreotide Morfina (en cuidados paliativos) Inmunosupresión para trasplantes Inmunoglobulina anti-RHO Miastenia gravis (piridostigmina) Inmunoglobulina anti-hepatitis B Imiglucerasa (enf de Gaucher) Alfa-dornasa (fibrosis quística) Efalizumab (psoriasis) Glucagon

Plan Materno Infantil • Cobertura del 100% durante el embarazo y primer mes de puerperio, y todo el primer año del niño. • Para la madre: “. . . medicamentos exclusivamente relacionados con el embarazo y el parto. . . ” • Para el hijo: “. . . siempre que figure en el listado de medicamentos esenciales. ” • “No se cubrirán las leches maternizadas o de otro tipo, salvo expresa indicación médica, con evaluación de la auditoría médica. ”

Aspectos organizativos • Cobertura: ¿sólo el PMO o algo más? • Provisión: farmacias propias y convenidas; redes. • Funciones de Auditoría: - Confección y actualización de los distintos listados. - Normatización - Autorizaciones - Monitoreo

Cobertura • La base es el Programa Médico Obligatorio. • Considerar además la cobertura de: ¿El resto de los medicamentos “usuales”, al 40%? ¿Los productos de venta bajo receta para uso cosmético? ¿Los tratamientos para infertilidad? ¿Vacunas fuera del calendario oficial? ¿Los medicamentos de alto costo no incluidos en el PMO, como etanercept, infliximab, palivizumab, etc. . . ?

Provisión • Farmacias propias. • Convenio con redes de farmacias: Pago porcentual sobre lo facturado Capitación por monto fijo mensual • Planes especiales: Oncológicos Diabetes etc.

Funciones de la auditoría 1. Confección y actualización de listados. 2. Normatizaciones. 3. Autorizaciones. 4. Monitoreo.

Funciones de la auditoría 1. Confección y actualización de listados • Las farmacias deben contar con el listado de los medicamentos que tienen cobertura, y su porcentaje. • Puede haber varios listados para planes distintos de un mismo agente del seguro de salud. • Listados para la madre y el hijo en el PMI. • Cada mes se actualizan todos listados con las novedades del mercado farmacéutico.

Funciones de la auditoría (2) 2. Normatizaciones: fuentes a considerar • Las “recomendaciones de uso” de la Res. 310/04. • Las normas del Programa Nacional de Garantía de Calidad de la Atención Médica. • Las normas de sociedades científicas locales (*) • Los informes del IECS. • Normativas internacionales accesibles por Internet.

Funciones de la auditoría (3) 3. Autorizaciones • De los programas al 100% (oncología, VIH, insulina, etc) • De las coberturas al 70% para tratamientos crónicos. • De coberturas al 40% que llevan autorización previa: usos no oncológicos de medicamentos oncológicos medicamentos de alto costo (ej: Heparinas BPM) • De los pedidos de excepción para medicamentos no incluidos en los listados. • De los pedidos de excepción para mayor cobertura.

Funciones de la auditoría (4) 4. Monitoreo • Los datos para el monitoreo surgen de la facturación de las farmacias. • Indicadores: Envases / afiliado / mes Monto total / afiliado / mes Monto a cargo de la institución / afiliado / mes Costo promedio del envase

Funciones de la auditoría (5) 4. Monitoreo (cont. ) • Los programas especiales (diabetes, oncológicos, VIH) pueden tener indicadores específicos por programa. • Se evalúa el ranking de afiliados con mayor consumo, para detectar situaciones átípicas. • Se evalúa el ranking de prescriptores, comparando dentro de la misma especialidad, con indicadores como: - costo promedio de la receta - costo de medicamentos recetados/pacientes atendidos

Algunos resultados
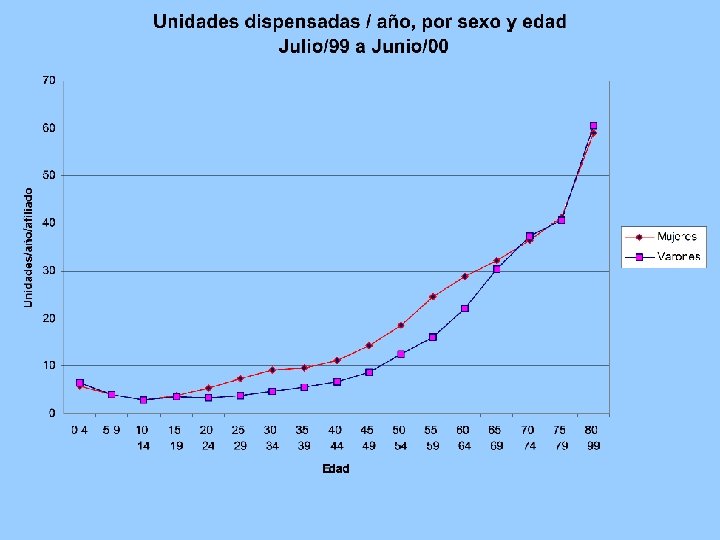
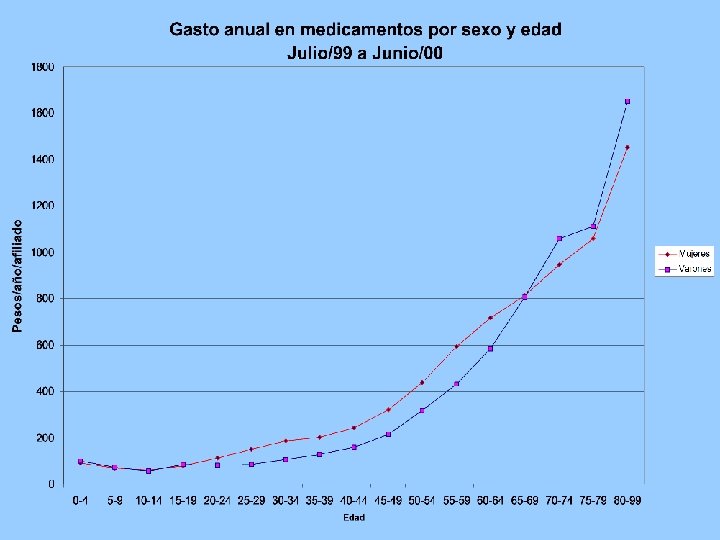

Análisis • El consumo de medicamentos crece en forma sostenida con la edad. • Entre los 15 y los 65 años el consumo en las mujeres supera al de los hombres. • Para comparar entre distintas poblaciones hay que considerar la distribución de sexo y edad.
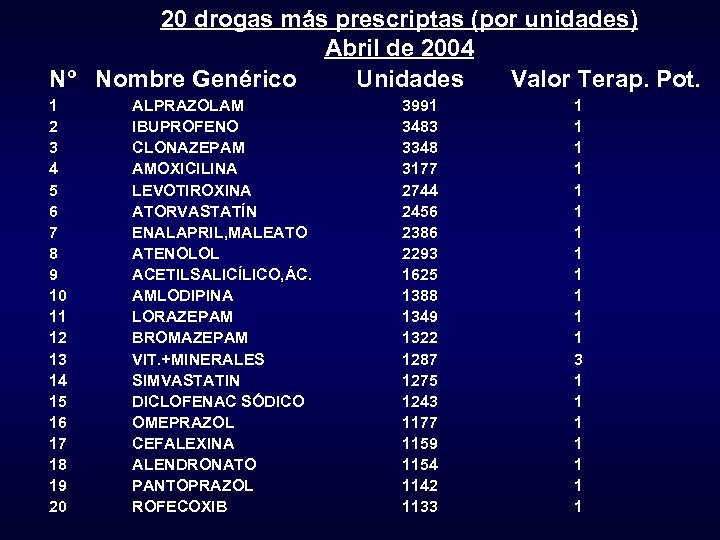
20 drogas más prescriptas (por unidades) Abril de 2004 Nº Nombre Genérico Unidades Valor Terap. Pot. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 ALPRAZOLAM IBUPROFENO CLONAZEPAM AMOXICILINA LEVOTIROXINA ATORVASTATÍN ENALAPRIL, MALEATO ATENOLOL ACETILSALICÍLICO, ÁC. AMLODIPINA LORAZEPAM BROMAZEPAM VIT. +MINERALES SIMVASTATIN DICLOFENAC SÓDICO OMEPRAZOL CEFALEXINA ALENDRONATO PANTOPRAZOL ROFECOXIB 3991 3483 3348 3177 2744 2456 2386 2293 1625 1388 1349 1322 1287 1275 1243 1177 1159 1154 1142 1133 1 1 1 3 1 1 1 1
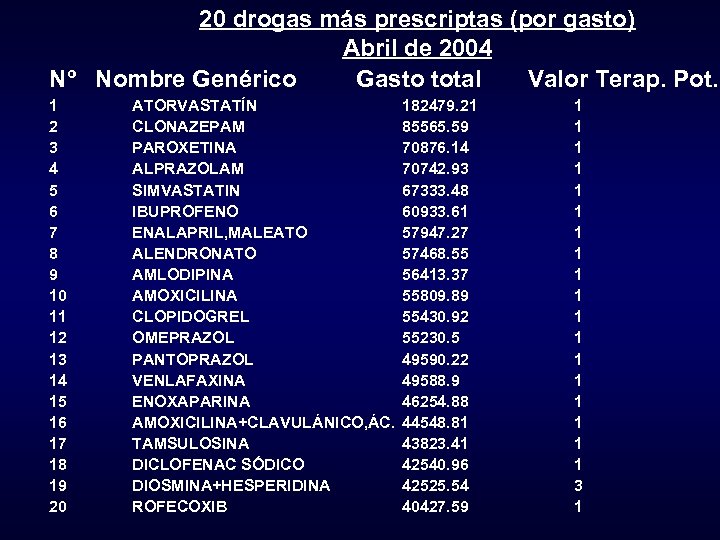
20 drogas más prescriptas (por gasto) Abril de 2004 Nº Nombre Genérico Gasto total Valor Terap. Pot. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 ATORVASTATÍN CLONAZEPAM PAROXETINA ALPRAZOLAM SIMVASTATIN IBUPROFENO ENALAPRIL, MALEATO ALENDRONATO AMLODIPINA AMOXICILINA CLOPIDOGREL OMEPRAZOL PANTOPRAZOL VENLAFAXINA ENOXAPARINA AMOXICILINA+CLAVULÁNICO, ÁC. TAMSULOSINA DICLOFENAC SÓDICO DIOSMINA+HESPERIDINA ROFECOXIB 182479. 21 85565. 59 70876. 14 70742. 93 67333. 48 60933. 61 57947. 27 57468. 55 56413. 37 55809. 89 55430. 92 55230. 5 49590. 22 49588. 9 46254. 88 44548. 81 43823. 41 42540. 96 42525. 54 40427. 59 1 1 1 1 1 3 1
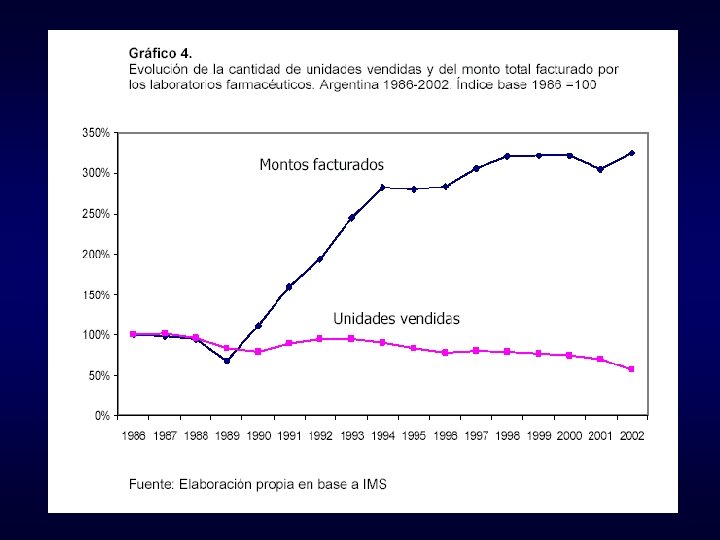
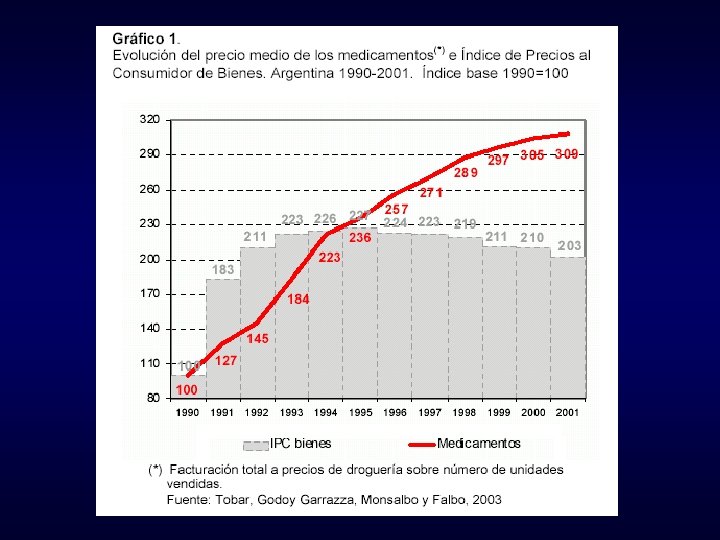
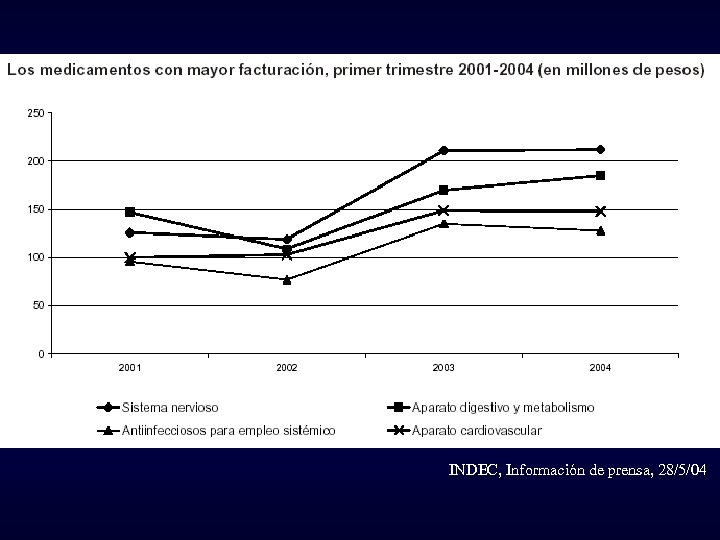
INDEC, Información de prensa, 28/5/04

Algunas ideas tomadas de: Estrategias económicas y financiamiento del medicamento Federico Tobar y Lucas Godoy Garraza (2002)
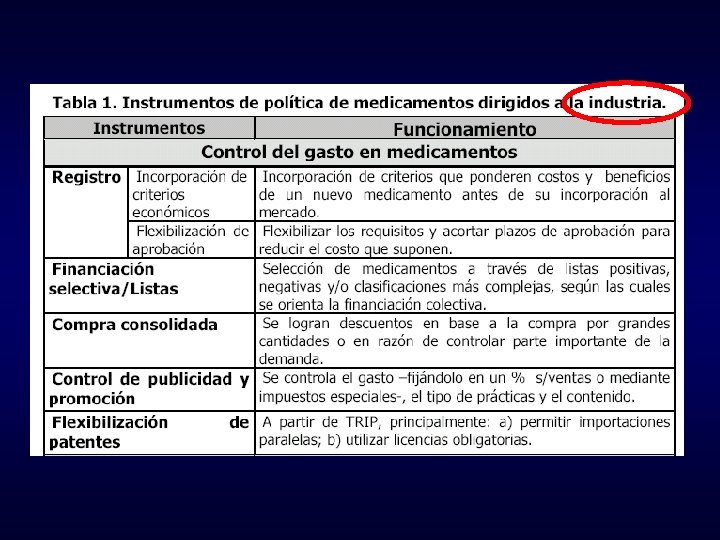



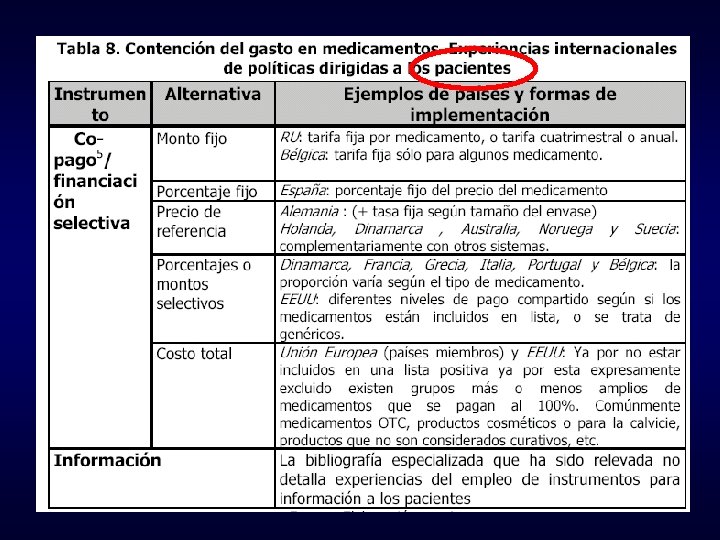
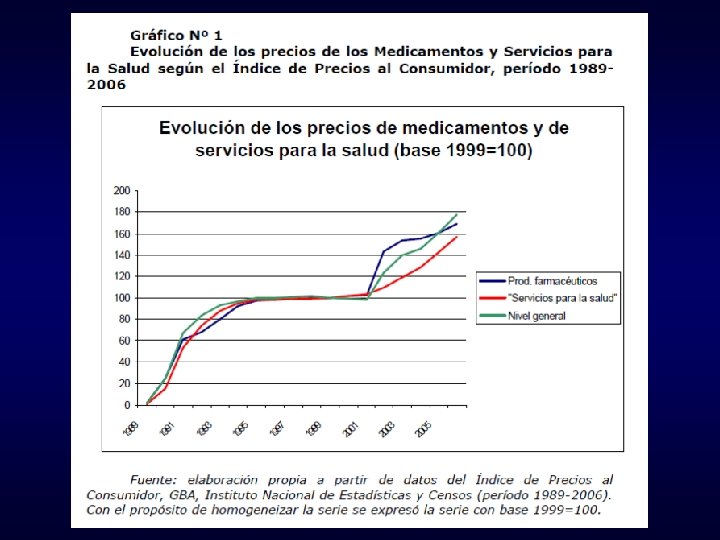
feb5e09f32e478cb183361b096dd3abb.ppt