Апластич. анемия и агранулоцитоз.ppt
- Количество слайдов: 73
 Цитопенический синдром (апластическая анемия, агранулоцитоз, миелодиспластический синдром) ассистент кафедры факультетской терапии, проф. болезней, клинической иммунологии и эндокринологии к. м. н. Павлова Вера Юрьевна
Цитопенический синдром (апластическая анемия, агранулоцитоз, миелодиспластический синдром) ассистент кафедры факультетской терапии, проф. болезней, клинической иммунологии и эндокринологии к. м. н. Павлова Вера Юрьевна
 Апластическая (гипопластическая) анемия – это заболевание для которого характерны: - качественные и количественные изменения стволовых клеток гемопоэза, - развивающиеся под влиянием большого количества эндогенных и экзогенных факторов и характеризующееся уменьшением (до полного отсутствия) клеток крови с замещением клеток костного мозга жировыми и с развитием панцитопении в периферической крови.
Апластическая (гипопластическая) анемия – это заболевание для которого характерны: - качественные и количественные изменения стволовых клеток гемопоэза, - развивающиеся под влиянием большого количества эндогенных и экзогенных факторов и характеризующееся уменьшением (до полного отсутствия) клеток крови с замещением клеток костного мозга жировыми и с развитием панцитопении в периферической крови.
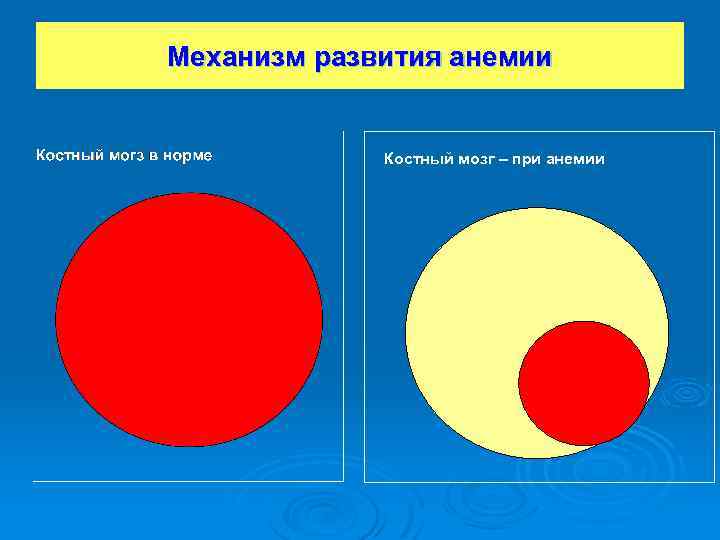 Механизм развития анемии Костный мозг – при анемии
Механизм развития анемии Костный мозг – при анемии
 Классификация апластической анемии Патогенетическая Анемии, связанные с костномозговой недостаточностью. - Гипопластическая (апластическая) анемия. -Рефрактерная анемия при миелодиспластическом синдроме.
Классификация апластической анемии Патогенетическая Анемии, связанные с костномозговой недостаточностью. - Гипопластическая (апластическая) анемия. -Рефрактерная анемия при миелодиспластическом синдроме.
 Классификация анемии (продолжение) Морфологическая I. ) Нормоцитарная анемия (диаметр эритроцитов 7. 2 -7. 5 мкм) Ø Ø Ø Ø Ø Недавняя кровопотеря Значительное увеличение объема плазмы (беременность, гипергидратация) Гемолиз эритроцитов Гипо- и апластическая анемия Инфильтративные изменения в костном мозге (лейкемия, множественная миелома, миелофиброз) Эндокринная патология (гипотиреоз, надпочечниковая недостаточность) Различные хронические заболевания Болезни почек Цирроз печени
Классификация анемии (продолжение) Морфологическая I. ) Нормоцитарная анемия (диаметр эритроцитов 7. 2 -7. 5 мкм) Ø Ø Ø Ø Ø Недавняя кровопотеря Значительное увеличение объема плазмы (беременность, гипергидратация) Гемолиз эритроцитов Гипо- и апластическая анемия Инфильтративные изменения в костном мозге (лейкемия, множественная миелома, миелофиброз) Эндокринная патология (гипотиреоз, надпочечниковая недостаточность) Различные хронические заболевания Болезни почек Цирроз печени
 Классификация анемии (продолжение) По цветовому показателю: I. Анемия нормохромная Ø Анемия при хронической почечной недостаточности. Ø Анемия при гипофизарной недостаточности. Ø Гипопластическая (апластическая) анемия. Ø Анемия при миелодиспластическом синдроме. Ø Лекарственная и лучевая цитостатическая болезнь. Ø Анемия при злокачественных новообразованиях и гемобластозах. Ø Анемия при системных заболеваниях соединительной ткани. Ø Анемия при хроническом активном гепатите и циррозе печени (кроме хронической постгеморрагической анемии). Ø Гемолитическая анемия (кроме талассемии). Ø Острая поттеморрагическая анемия.
Классификация анемии (продолжение) По цветовому показателю: I. Анемия нормохромная Ø Анемия при хронической почечной недостаточности. Ø Анемия при гипофизарной недостаточности. Ø Гипопластическая (апластическая) анемия. Ø Анемия при миелодиспластическом синдроме. Ø Лекарственная и лучевая цитостатическая болезнь. Ø Анемия при злокачественных новообразованиях и гемобластозах. Ø Анемия при системных заболеваниях соединительной ткани. Ø Анемия при хроническом активном гепатите и циррозе печени (кроме хронической постгеморрагической анемии). Ø Гемолитическая анемия (кроме талассемии). Ø Острая поттеморрагическая анемия.
 Эпидемиология Встречается редко- 4 -13 случаев в год на 1 млн. жителей (по разным странам); Ø Два пика заболеваемости: 20 (воздействие вирусов) и 65 лет (химические вещества); Ø В Китае и Юго – Восточной Азии – распространенность в 3 -4 раза выше других регионов.
Эпидемиология Встречается редко- 4 -13 случаев в год на 1 млн. жителей (по разным странам); Ø Два пика заболеваемости: 20 (воздействие вирусов) и 65 лет (химические вещества); Ø В Китае и Юго – Восточной Азии – распространенность в 3 -4 раза выше других регионов.
 Этиология Ø Экзогенные факторы: Ионизирующее излучение; - Токсическое действия (органические растоврители и. т. д); - Лекарственные препараты сульфаниламиды антитериоидные (мерказолил) гипотензивные (каптоприл, эналаприл, допегит) НПВП цитостатики - Идиосинкрозия (повышенная чувствительность); -Вирусные заболевания (гепатит, герпес, ЦМВ и. т. д) -
Этиология Ø Экзогенные факторы: Ионизирующее излучение; - Токсическое действия (органические растоврители и. т. д); - Лекарственные препараты сульфаниламиды антитериоидные (мерказолил) гипотензивные (каптоприл, эналаприл, допегит) НПВП цитостатики - Идиосинкрозия (повышенная чувствительность); -Вирусные заболевания (гепатит, герпес, ЦМВ и. т. д) -
 Этиология продолжение Ø Эндогенные: - Аутоиммунные процессы и заболевания - Гипофункция щитовидной железы - Беременность - Генетическая предрасположенность Иммунный процесс зависит от степени реактивности: нормо-, гипо – или гиперреакция.
Этиология продолжение Ø Эндогенные: - Аутоиммунные процессы и заболевания - Гипофункция щитовидной железы - Беременность - Генетическая предрасположенность Иммунный процесс зависит от степени реактивности: нормо-, гипо – или гиперреакция.
 АА – при лечение в течение 8 лет и более у 75% больных переходит в один из гемобластозов. В настоящее время в основе развития АА лежит мутация стволовой клетки. Гипофункция иммунной системы Нормофункция лейкоз дефект элиминируется; Гиперфункция будет заблокирована как матировавшая клетка, так и нормальные клетки костного мозга;
АА – при лечение в течение 8 лет и более у 75% больных переходит в один из гемобластозов. В настоящее время в основе развития АА лежит мутация стволовой клетки. Гипофункция иммунной системы Нормофункция лейкоз дефект элиминируется; Гиперфункция будет заблокирована как матировавшая клетка, так и нормальные клетки костного мозга;
 Патогенез 1. 2. 3. 4. Внутренний дефект стволовой клетки крови Иммунная реакция на гемопоэтическую ткань. Дефект поддерживающей функции микроокружения. Наследственный генетический дефект ; Пути реализации патогенетических механизмов 1. Укорочение продолжительности жизни эритроцитов; 2. Снижение утилизации железа костным мозгом; 3. Снижение скорости синтеза клеток в костном мозге; 4. Внутрикостномозговой гемолиз;
Патогенез 1. 2. 3. 4. Внутренний дефект стволовой клетки крови Иммунная реакция на гемопоэтическую ткань. Дефект поддерживающей функции микроокружения. Наследственный генетический дефект ; Пути реализации патогенетических механизмов 1. Укорочение продолжительности жизни эритроцитов; 2. Снижение утилизации железа костным мозгом; 3. Снижение скорости синтеза клеток в костном мозге; 4. Внутрикостномозговой гемолиз;
 Классификация по механизму развития 1) Наследственные 2) Приобретенные 3) Иммунные
Классификация по механизму развития 1) Наследственные 2) Приобретенные 3) Иммунные
 Клинические проявления апластической анемии Ø Анемический синдром Ø Геморрагический синдром Ø Иммунодефицит Ø Синдром интоксикации
Клинические проявления апластической анемии Ø Анемический синдром Ø Геморрагический синдром Ø Иммунодефицит Ø Синдром интоксикации
 Клиника Классический анемический синдром (гипоксия): - Слабость Головокружение Тахикардия Шум в ушах Мелькание мушек перед глазами Одышка Сонливость - Обморочные состояния -
Клиника Классический анемический синдром (гипоксия): - Слабость Головокружение Тахикардия Шум в ушах Мелькание мушек перед глазами Одышка Сонливость - Обморочные состояния -
 Клиника Гемаррогический синдром: В норме тромбоциты: 180 -320* 109/л - 60 -50* 109/л – нет проявлений - 49 -20* 109/л – только увеличение длительности кровотечения при повреждениях; - ниже 20* 109/л – самопроизвольные кровотечения и гематомы без внешних воздействий.
Клиника Гемаррогический синдром: В норме тромбоциты: 180 -320* 109/л - 60 -50* 109/л – нет проявлений - 49 -20* 109/л – только увеличение длительности кровотечения при повреждениях; - ниже 20* 109/л – самопроизвольные кровотечения и гематомы без внешних воздействий.
 Степень тромбоцитопении Ø 10 -20*109/л – тяжелая тромбоцитопения 4 Ø 20 -50*109/л – выраженная тромбоцитопения; Ø 50 - 100 *109/л – умеренная тромбоцитопения;
Степень тромбоцитопении Ø 10 -20*109/л – тяжелая тромбоцитопения 4 Ø 20 -50*109/л – выраженная тромбоцитопения; Ø 50 - 100 *109/л – умеренная тромбоцитопения;
 Клиника Иммунодефицит: Функции лейкоцитов: -нейтрофилы – фагацитоз, цитотоксический эффект, синтез провоспалительных цитокинов (преимущественно клеточный иммунитет); -базофилы – очищение организма от большого количества биологически активных веществ, повреждающих организм (особенно при аллергических реакциях); -эозинофилы – фагацитоз, инактивация продуктов, выделяемых эозинофилами (повышение при всех аллергических состояних, а так же в период выздоровления после тяжелого инфекционного процесса; -моноциты (макрофаги) – фагацитоз, противоинфекционный и противораковый иммуниетет, синтез цитокинов; -лимфоциты – выработка АТ (гуморальный иммунитет),
Клиника Иммунодефицит: Функции лейкоцитов: -нейтрофилы – фагацитоз, цитотоксический эффект, синтез провоспалительных цитокинов (преимущественно клеточный иммунитет); -базофилы – очищение организма от большого количества биологически активных веществ, повреждающих организм (особенно при аллергических реакциях); -эозинофилы – фагацитоз, инактивация продуктов, выделяемых эозинофилами (повышение при всех аллергических состояних, а так же в период выздоровления после тяжелого инфекционного процесса; -моноциты (макрофаги) – фагацитоз, противоинфекционный и противораковый иммуниетет, синтез цитокинов; -лимфоциты – выработка АТ (гуморальный иммунитет),
 Программа обследования 1) 2) 3) 4) 5) 6) Общий анализ крови Развернутая иммунограмма Общий анализ мочи Стернальная пункция Трепанобиопсия – основной метод для верификации диагноза. Дополнительные исследования в зависимости от причины анемии
Программа обследования 1) 2) 3) 4) 5) 6) Общий анализ крови Развернутая иммунограмма Общий анализ мочи Стернальная пункция Трепанобиопсия – основной метод для верификации диагноза. Дополнительные исследования в зависимости от причины анемии
 Ø Основные критерии диагноза апластической анемии: трехростковая цитопения: -анемия -гранулоцитопения -тромбоцитопения Ø аплазия костного мозга: преобладание жирового костного мозга над деятельным в биоптате подвздошной кости.
Ø Основные критерии диагноза апластической анемии: трехростковая цитопения: -анемия -гранулоцитопения -тромбоцитопения Ø аплазия костного мозга: преобладание жирового костного мозга над деятельным в биоптате подвздошной кости.
 Критерии тяжести апластической анемии ( B. Camitta et al; EBMT SAA): Ø тяжелая апластическая анемия: -гранулоцитопения – до 0, 5 х 109 / л -тромбоцитопения – до 20, 0 х 109 / л Ø очень тяжелая апластическая анемия: -гранулоцитопения - менее 0, 2 х 109 / л -тромбоцитопения - менее 20, 0 х 109 / л -в сочетании с аплазией костного мозга в биоптате подвздошной кости.
Критерии тяжести апластической анемии ( B. Camitta et al; EBMT SAA): Ø тяжелая апластическая анемия: -гранулоцитопения – до 0, 5 х 109 / л -тромбоцитопения – до 20, 0 х 109 / л Ø очень тяжелая апластическая анемия: -гранулоцитопения - менее 0, 2 х 109 / л -тромбоцитопения - менее 20, 0 х 109 / л -в сочетании с аплазией костного мозга в биоптате подвздошной кости.
 Лечение 1) Поиск и устранение этиологических факторов; 2) ГКС; 3) При иммунном генезе – цитостатики; 4) Трансфузия компонентов крови 5) Лечение колонийстимулирующими факторами 6) Пересадка костного мозга; 7) Посиндромное лечение (геморрагический, лейкопения)
Лечение 1) Поиск и устранение этиологических факторов; 2) ГКС; 3) При иммунном генезе – цитостатики; 4) Трансфузия компонентов крови 5) Лечение колонийстимулирующими факторами 6) Пересадка костного мозга; 7) Посиндромное лечение (геморрагический, лейкопения)
 Показания к цитостатикам Ø Первичная тяжелая АА Ø Тяжелая анемия рефрактерная к терапии АЛГ Ø Тяжелая АА при повышенной чувствительности к АЛГ; Циклоспорин – А (Сандимун - неорал) Доза – 5 - 10 мг/кг/сут – общепринятой дозы и длительности терапии нет. Длительность не менее 3 х месяцев.
Показания к цитостатикам Ø Первичная тяжелая АА Ø Тяжелая анемия рефрактерная к терапии АЛГ Ø Тяжелая АА при повышенной чувствительности к АЛГ; Циклоспорин – А (Сандимун - неорал) Доза – 5 - 10 мг/кг/сут – общепринятой дозы и длительности терапии нет. Длительность не менее 3 х месяцев.
 Комбинированная терапия Ø антилимфоцитарный или антитимоцитарный глобулин -АЛГ/АТГ Ø через 2 недели от начала курса АЛГ/АТГ после купирования симптомов сывороточной болезни начинается терапия циклоспорином А (Су. А), курс лечения продолжается не менее 12 месяцев. Ø Через 3 , 6 месяцев от начала иммуносупрессивной терапии при отсутствии положительной клинико-гематологической динамики – спленэктомия
Комбинированная терапия Ø антилимфоцитарный или антитимоцитарный глобулин -АЛГ/АТГ Ø через 2 недели от начала курса АЛГ/АТГ после купирования симптомов сывороточной болезни начинается терапия циклоспорином А (Су. А), курс лечения продолжается не менее 12 месяцев. Ø Через 3 , 6 месяцев от начала иммуносупрессивной терапии при отсутствии положительной клинико-гематологической динамики – спленэктомия
 Атгам (Antilymphocyte immunoglobulin (horse)) Форма выпуска: Раствор для инъекций: 1 мл 1 амп. 50 мг 250 мг 5 мл - ампулы (5) - пачки картонные.
Атгам (Antilymphocyte immunoglobulin (horse)) Форма выпуска: Раствор для инъекций: 1 мл 1 амп. 50 мг 250 мг 5 мл - ампулы (5) - пачки картонные.
 Стимуляторы ростков кроветворения Ø гранулоцитарный колониестимулирующий фактор (Г-КСФ) (филграстим), Ø Молграмостим -колониестимулирующий фактор. Стимулирует пролиферацию и дифференцировку предшественников кроветворных клеток. Стимулирует рост гранулоцитов, моноцитов, Тлимфоцитов, не влияя на рост В-лимфоцитов Ø Нейпоген Ø Эпоэтин альфа (Эритростим, Эпокрин) рекомбинантный эритропоэтин, стимулирующий образование эритроцитов из клетокпредшественников.
Стимуляторы ростков кроветворения Ø гранулоцитарный колониестимулирующий фактор (Г-КСФ) (филграстим), Ø Молграмостим -колониестимулирующий фактор. Стимулирует пролиферацию и дифференцировку предшественников кроветворных клеток. Стимулирует рост гранулоцитов, моноцитов, Тлимфоцитов, не влияя на рост В-лимфоцитов Ø Нейпоген Ø Эпоэтин альфа (Эритростим, Эпокрин) рекомбинантный эритропоэтин, стимулирующий образование эритроцитов из клетокпредшественников.
 Трансплантация костного мозга Источники стволовых клеток: костный мозг донора, кровь, пуповинная кровь, печень плодов человека, Виды трансплантации костного мозга: Ø Аллогенная – от другого человека; Ø Изотрансплантация – от однояйцовых близнецов; Ø Аутотрансплантация – из собственных не пораженных клеток больного; Стволовые клетки вводятся в/в.
Трансплантация костного мозга Источники стволовых клеток: костный мозг донора, кровь, пуповинная кровь, печень плодов человека, Виды трансплантации костного мозга: Ø Аллогенная – от другого человека; Ø Изотрансплантация – от однояйцовых близнецов; Ø Аутотрансплантация – из собственных не пораженных клеток больного; Стволовые клетки вводятся в/в.
 Этапы проведения трансплантации костного мозга Ø Высокодозная ПХТ с облучением всей поврехности тела (полное удаление собственного костного мозга и максимальное снижение иммунитета) Ø Заготовка костного мозга (проводится в течение нескольких дней – из гребня подвздошной кости донора); Ø Трансплантация Ø Заместительная и симптоматическая терапия
Этапы проведения трансплантации костного мозга Ø Высокодозная ПХТ с облучением всей поврехности тела (полное удаление собственного костного мозга и максимальное снижение иммунитета) Ø Заготовка костного мозга (проводится в течение нескольких дней – из гребня подвздошной кости донора); Ø Трансплантация Ø Заместительная и симптоматическая терапия
 Осложнения трансплантации костного мозга Ø 1. 2. 3. 4. 5. Ø 1. 2. 3. 4. Ранние: Воспалительные процессы; Нефротоксичность; Нейротоксичность; Кровоточивость; Отторжение трансплантата; Поздние: Эндокринные нарушения; Бесплодие; Хр. воспалительные процессы; Рецидив онкологический процессов и вторичные опухоли;
Осложнения трансплантации костного мозга Ø 1. 2. 3. 4. 5. Ø 1. 2. 3. 4. Ранние: Воспалительные процессы; Нефротоксичность; Нейротоксичность; Кровоточивость; Отторжение трансплантата; Поздние: Эндокринные нарушения; Бесплодие; Хр. воспалительные процессы; Рецидив онкологический процессов и вторичные опухоли;
 Особенности фармакотерапии ГКС (преднизалон) Расчет дозы: Легкая степень тяжести - 0, 3 -0, 5 мг/кг/сут Средняя степень тяжести - 0, 5 -0, 7 мг/кг/сут Тяжелая степень тяжести - 0, 7 -1, 0 мг/кг/сут Распределение в течение дня: утро : обед : вечер – 3: 2 : 1. Обязательно после еды, запивать стаканом воды
Особенности фармакотерапии ГКС (преднизалон) Расчет дозы: Легкая степень тяжести - 0, 3 -0, 5 мг/кг/сут Средняя степень тяжести - 0, 5 -0, 7 мг/кг/сут Тяжелая степень тяжести - 0, 7 -1, 0 мг/кг/сут Распределение в течение дня: утро : обед : вечер – 3: 2 : 1. Обязательно после еды, запивать стаканом воды
 Пульс – терапия ГКС Пульс – терапия – введение больших доз ГКС для обрыва высокой степени активности иммунного процесса. Метилпреднизалон (метипред, солу-медрол): по 1000 мг вв капельно ежедневно в течение 3 -х дней подряд, с последующим переходом на поддерживающую дозу таблетировнного ГКС ( преднизалон -5 – 15 мг/сут)
Пульс – терапия ГКС Пульс – терапия – введение больших доз ГКС для обрыва высокой степени активности иммунного процесса. Метилпреднизалон (метипред, солу-медрол): по 1000 мг вв капельно ежедневно в течение 3 -х дней подряд, с последующим переходом на поддерживающую дозу таблетировнного ГКС ( преднизалон -5 – 15 мг/сут)
 Специфические побочные действия ГКС Ульцерогенное действие на всем протяжении ЖКТ; Ø Объем зависимая АГ; Ø Стероидный сахарный диабет; Ø Остеопроз; Ø Повышение чувствительности рецепторов к КА Ø При очень больших дозах (80 – 90 мг/сут – per os – развитие психозов; Ø
Специфические побочные действия ГКС Ульцерогенное действие на всем протяжении ЖКТ; Ø Объем зависимая АГ; Ø Стероидный сахарный диабет; Ø Остеопроз; Ø Повышение чувствительности рецепторов к КА Ø При очень больших дозах (80 – 90 мг/сут – per os – развитие психозов; Ø
 Полная ремиссия: Ø гемоглобин > 100, 0 г/ л Ø гранулоциты > 1, 5 х 109/ л Ø тромбоциты > 100, 0 х 109/ л Ø отсутствие потребности в гемотрансфузиях.
Полная ремиссия: Ø гемоглобин > 100, 0 г/ л Ø гранулоциты > 1, 5 х 109/ л Ø тромбоциты > 100, 0 х 109/ л Ø отсутствие потребности в гемотрансфузиях.
 Компоненты крови: Ø Эритроцитарная масса Ø Отмытые эритроциты Ø Свежезамороженная плазма Ø Тромбоконцентрат Ø Лейкоцитраная масса Ø Концентрат нативной плазмы Ø Криоприципитат
Компоненты крови: Ø Эритроцитарная масса Ø Отмытые эритроциты Ø Свежезамороженная плазма Ø Тромбоконцентрат Ø Лейкоцитраная масса Ø Концентрат нативной плазмы Ø Криоприципитат
 Агранулоцитоз
Агранулоцитоз
 Агранулоцитоз – снижение или общего количества лейкоцитов менее 1, 0 *109/л или снижение абсолютного количества нейтрофилов менее 0, 75 *109/л под действием различных факторов, чаще экзогенных. Гранулоциты: -эозинофилы, -базофилы - нейтрофилы
Агранулоцитоз – снижение или общего количества лейкоцитов менее 1, 0 *109/л или снижение абсолютного количества нейтрофилов менее 0, 75 *109/л под действием различных факторов, чаще экзогенных. Гранулоциты: -эозинофилы, -базофилы - нейтрофилы
 ОАК
ОАК
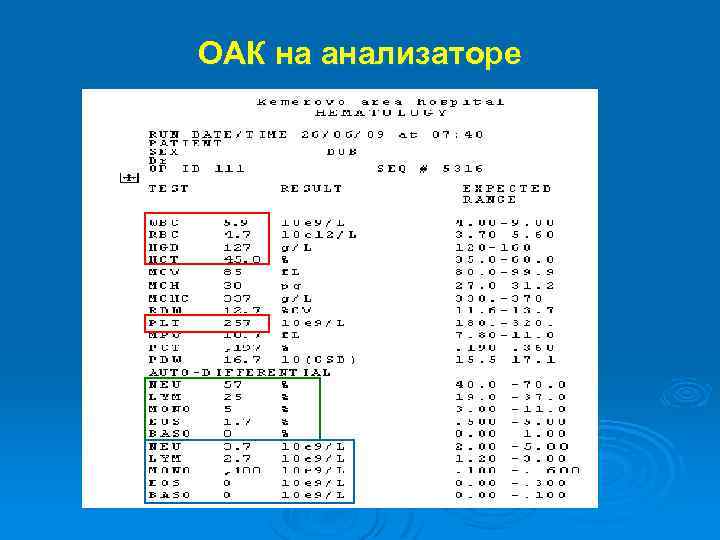 ОАК на анализаторе
ОАК на анализаторе

 Патогенез 1. Иммунный- срыв иммунной системы, выработка АТ против нейтрофилов (гаптеновый механизм, аутоиммуный механизм) 2. Миелотоксический – химические вещества, цитостатики, физические факторы 3. Генуинный – нет явных причин.
Патогенез 1. Иммунный- срыв иммунной системы, выработка АТ против нейтрофилов (гаптеновый механизм, аутоиммуный механизм) 2. Миелотоксический – химические вещества, цитостатики, физические факторы 3. Генуинный – нет явных причин.
 Клинические проявления агранулоцитоза Ø Тяжело протекающие инфекции любой локализации; Ø Некротические процессы (некротический стоматит, некротическая ангина, некротическая энтеропатия); Ø Сепсис (грибоковый – 100% летальность)
Клинические проявления агранулоцитоза Ø Тяжело протекающие инфекции любой локализации; Ø Некротические процессы (некротический стоматит, некротическая ангина, некротическая энтеропатия); Ø Сепсис (грибоковый – 100% летальность)
 Клинические формы агранулоцитоза: Ø Острейший (молниеносный); Ø Острый; Ø Подострый; Ø Рецидивирующий; Ø Циклический
Клинические формы агранулоцитоза: Ø Острейший (молниеносный); Ø Острый; Ø Подострый; Ø Рецидивирующий; Ø Циклический
 Общий анализ крови Ø Снижение общего уровня лейкоцитов до 1, 0 * 109/л; Ø Единичные нейтрофилы (за счет сегментоядерных, единичные базофилы и базофилы), преобладают лимфоциты.
Общий анализ крови Ø Снижение общего уровня лейкоцитов до 1, 0 * 109/л; Ø Единичные нейтрофилы (за счет сегментоядерных, единичные базофилы и базофилы), преобладают лимфоциты.
 Ø В отсутствии эффективного лечения летальный исход практически неизбежен. Ø Степень и длительность нейтропеии обуславливает число инфекционный осложнений и их тяжесть. Ø У больных с гемобластозами уменьшается количестов нейтрофилов и развиваются качественные дефекты: нарушение процессов хемотаксиса и фагацитоза. Ø Аналогичные эффекты дает проводимая специфическая цитостатическая терапия.
Ø В отсутствии эффективного лечения летальный исход практически неизбежен. Ø Степень и длительность нейтропеии обуславливает число инфекционный осложнений и их тяжесть. Ø У больных с гемобластозами уменьшается количестов нейтрофилов и развиваются качественные дефекты: нарушение процессов хемотаксиса и фагацитоза. Ø Аналогичные эффекты дает проводимая специфическая цитостатическая терапия.
 Особенности развития инфекционных осложнений Ø Осложнения могут быть вызваны нормальной флоры кожи, слизистых, ЖКТ и. т. д. Ø Организм не может препятствовать как проникновению, так и размножению микроорганизмов; Ø Самые тяжелые процессы на фоне агранулоцитоза протекают с минимальными клиническими проявлениями; Ø Атипичность проявления.
Особенности развития инфекционных осложнений Ø Осложнения могут быть вызваны нормальной флоры кожи, слизистых, ЖКТ и. т. д. Ø Организм не может препятствовать как проникновению, так и размножению микроорганизмов; Ø Самые тяжелые процессы на фоне агранулоцитоза протекают с минимальными клиническими проявлениями; Ø Атипичность проявления.
 Лечение Ø Поиск и устранение причины развития; Ø Создание асептических условий; Ø Профилактика и лечение инфекционных процессов (комбинированная а/м терапия, обязательно антигрибковые препараты); Ø Деконтоминация кишечника (полимиксин, мономиксин) Ø ГКС Ø Стимуляторы лейкопоэза Ø Дезинтоксикация Ø Симптоматическая терапия.
Лечение Ø Поиск и устранение причины развития; Ø Создание асептических условий; Ø Профилактика и лечение инфекционных процессов (комбинированная а/м терапия, обязательно антигрибковые препараты); Ø Деконтоминация кишечника (полимиксин, мономиксин) Ø ГКС Ø Стимуляторы лейкопоэза Ø Дезинтоксикация Ø Симптоматическая терапия.
 Антибактериальные препараты, используемые для деконтаминации: Ø - неабсорбируемые антибиотики (1 или 2: канамицин 1, 5 г/сут. , полимиксин В или М (по 0, 5 х 4 раза в день), гентамицин (200 мг/сут) Ø триметоприм- сульфаметоксазал (по 960 мг х 2 раза в день) Ø ципрофлоксацин (по 250 мг х 2 раза в день)
Антибактериальные препараты, используемые для деконтаминации: Ø - неабсорбируемые антибиотики (1 или 2: канамицин 1, 5 г/сут. , полимиксин В или М (по 0, 5 х 4 раза в день), гентамицин (200 мг/сут) Ø триметоприм- сульфаметоксазал (по 960 мг х 2 раза в день) Ø ципрофлоксацин (по 250 мг х 2 раза в день)
 Стимуляторы ростков кроветворения Ø гранулоцитарный колониестимулирующий фактор (Г-КСФ) (филграстим), Ø Молграмостим -колониестимулирующий фактор. Стимулирует пролиферацию и дифференцировку предшественников кроветворных клеток. Стимулирует рост гранулоцитов, моноцитов, Тлимфоцитов, не влияя на рост В-лимфоцитов Ø Нейпоген - 10 ампул – Ø Эпоэтин альфа (Эритростим, Эпокрин) рекомбинантный эритропоэтин, стимулирующий образование эритроцитов из клетокпредшественников - 10 ампул
Стимуляторы ростков кроветворения Ø гранулоцитарный колониестимулирующий фактор (Г-КСФ) (филграстим), Ø Молграмостим -колониестимулирующий фактор. Стимулирует пролиферацию и дифференцировку предшественников кроветворных клеток. Стимулирует рост гранулоцитов, моноцитов, Тлимфоцитов, не влияя на рост В-лимфоцитов Ø Нейпоген - 10 ампул – Ø Эпоэтин альфа (Эритростим, Эпокрин) рекомбинантный эритропоэтин, стимулирующий образование эритроцитов из клетокпредшественников - 10 ампул
 ГРАНОЦИТ Форма выпуска Лиофилизированный порошок для инъекций 1 фл. ленограстим 33. 6 млн. МЕ 42 936. 16 руб Режим дозирования: 150 мкг (19. 2 млн. МЕ)/м 2 поверхности тела, T 1/2 при: -п/к введении составляет 3 -4 ч, -5 -6 раз в сутки -при в/в - 1 -1. 5 ч – около 8 - 9 раз в сутки
ГРАНОЦИТ Форма выпуска Лиофилизированный порошок для инъекций 1 фл. ленограстим 33. 6 млн. МЕ 42 936. 16 руб Режим дозирования: 150 мкг (19. 2 млн. МЕ)/м 2 поверхности тела, T 1/2 при: -п/к введении составляет 3 -4 ч, -5 -6 раз в сутки -при в/в - 1 -1. 5 ч – около 8 - 9 раз в сутки
 Нейпоген (filgrastim) для в/в и п/к введения 30 млн. ЕД/1 мл: фл. 1 или 5 шт. – 25 000 руб в/в и п/к введения 48 млн. ЕД/1. 6 мл: фл. 1 или 5 шт. - 35 000 руб п/к введения 48 млн. ЕД/0. 5 мл: шприц-тюбики 1 или 5 шт. п/к введения 30 млн. ЕД/0. 5 мл: шприц-тюбики 1 или 5 шт. 6634. 38 руб
Нейпоген (filgrastim) для в/в и п/к введения 30 млн. ЕД/1 мл: фл. 1 или 5 шт. – 25 000 руб в/в и п/к введения 48 млн. ЕД/1. 6 мл: фл. 1 или 5 шт. - 35 000 руб п/к введения 48 млн. ЕД/0. 5 мл: шприц-тюбики 1 или 5 шт. п/к введения 30 млн. ЕД/0. 5 мл: шприц-тюбики 1 или 5 шт. 6634. 38 руб
 Нейпомакс (filgrastim) · р-р -в/в и п/к введения 30 млн. ЕД/1 мл: фл. 5 шт. – 3351. 8 руб · р-р -в/в и п/к введения 48 млн. ЕД/1. 6 мл: фл. 5 шт. - 5151. 31 руб
Нейпомакс (filgrastim) · р-р -в/в и п/к введения 30 млн. ЕД/1 мл: фл. 5 шт. – 3351. 8 руб · р-р -в/в и п/к введения 48 млн. ЕД/1. 6 мл: фл. 5 шт. - 5151. 31 руб
 Стимуляторы гемопоэза Ø Epoetin beta (эритростим): Раствор для инъекций прозрачный, бесцветный. 1 мл эритропоэтин человека рекомбинантный -500 МЕ-2000 МЕ-3000 МЕ-4000 МЕ-10 000 МЕ
Стимуляторы гемопоэза Ø Epoetin beta (эритростим): Раствор для инъекций прозрачный, бесцветный. 1 мл эритропоэтин человека рекомбинантный -500 МЕ-2000 МЕ-3000 МЕ-4000 МЕ-10 000 МЕ
 Epoetin alfa (эритростим): 2500 -3000 руб 1 шприц – 2, 5 тыс МЕ 1 шприц – 10 тыс МЕ При в/в введении T 1/2 составляет 5 -6 ч, вне зависимости от тяжести заболевания. При п/к введения через 12 -18 ч Раствор для инъекций 1 мл 1 тыс. МЕ -"- 2 тыс. МЕ -"- 4 тыс. МЕ -"- 10 тыс. МЕ
Epoetin alfa (эритростим): 2500 -3000 руб 1 шприц – 2, 5 тыс МЕ 1 шприц – 10 тыс МЕ При в/в введении T 1/2 составляет 5 -6 ч, вне зависимости от тяжести заболевания. При п/к введения через 12 -18 ч Раствор для инъекций 1 мл 1 тыс. МЕ -"- 2 тыс. МЕ -"- 4 тыс. МЕ -"- 10 тыс. МЕ
 Миелодиспластический синдром
Миелодиспластический синдром
 Миелодиспластические синдромы объединяют группу злокачественных опухолевых заболеваний системы кроветворения. При этих заболеваниях происходит нарушение созревания клеток костного мозга с изменением их строения и функциональных свойств.
Миелодиспластические синдромы объединяют группу злокачественных опухолевых заболеваний системы кроветворения. При этих заболеваниях происходит нарушение созревания клеток костного мозга с изменением их строения и функциональных свойств.
 Эпидемиология МДС Ø Заболеваемость в среднем составляет 3 -4 случая на 100 000 населения в год и увеличивается с возрастом. Ø Основной контингент больных МДС составляют пожилые люди (средний возраст - 70 лет). Ø Заболеваемость мужчин незначительно преобладает над заболеваемостью женщин. МДС в детском возрасте встречается крайне редко. Ø 10 -15% случаев МДС является осложнением проведенной химиотерапии и облучения по поводу другого онкологического заболевания.
Эпидемиология МДС Ø Заболеваемость в среднем составляет 3 -4 случая на 100 000 населения в год и увеличивается с возрастом. Ø Основной контингент больных МДС составляют пожилые люди (средний возраст - 70 лет). Ø Заболеваемость мужчин незначительно преобладает над заболеваемостью женщин. МДС в детском возрасте встречается крайне редко. Ø 10 -15% случаев МДС является осложнением проведенной химиотерапии и облучения по поводу другого онкологического заболевания.
 Факторы риска Ø Генетическая предрасположенность отмечена и у лиц зрелого возраста, родители которых страдали МДС. Ø Ионизирующее излучение, Ø Ø Химические факторы: -органические соединения (бензин и его производные, пестициды, растворители), -неорганические (асбест, кварц, мышьяк) вещества. МДС развивается чаще у курящих по сравнению с некурящими. Более высокий риск возникновения МДС отмечен у работников сельского хозяйства, текстильной промышленности, лечебных учреждений, операторов машин, у лиц, проживающих вблизи заводов. Ø Влияние химиопрепаратов и лучевого лечения.
Факторы риска Ø Генетическая предрасположенность отмечена и у лиц зрелого возраста, родители которых страдали МДС. Ø Ионизирующее излучение, Ø Ø Химические факторы: -органические соединения (бензин и его производные, пестициды, растворители), -неорганические (асбест, кварц, мышьяк) вещества. МДС развивается чаще у курящих по сравнению с некурящими. Более высокий риск возникновения МДС отмечен у работников сельского хозяйства, текстильной промышленности, лечебных учреждений, операторов машин, у лиц, проживающих вблизи заводов. Ø Влияние химиопрепаратов и лучевого лечения.
 Патогенез Ø Возникновение в результате мутации стволовой клетки крови неопластического клона с частично нарушенной способностью к созреванию. Ø Опухолевый клон вытесняет из костного мозга нормальные гемопоэтические клетки, Ø Гемопоэз в костном мозге осуществляется только потомками мутировавшей клетки.
Патогенез Ø Возникновение в результате мутации стволовой клетки крови неопластического клона с частично нарушенной способностью к созреванию. Ø Опухолевый клон вытесняет из костного мозга нормальные гемопоэтические клетки, Ø Гемопоэз в костном мозге осуществляется только потомками мутировавшей клетки.
 Патогенез (проложение) Ø Зрелые клетки крови имеют опухолевой происхождение, уменьшены в количестве и ослаблены в функции. Ø С течением времени в опухолевых клетках могут произойти вторичные мутации, что приводит к полной утрате этими клетками способности созревать - наступает конечная фаза развития МДС для обозначения который используют термин "острый лейкоз развившийся из предшествующего МДС".
Патогенез (проложение) Ø Зрелые клетки крови имеют опухолевой происхождение, уменьшены в количестве и ослаблены в функции. Ø С течением времени в опухолевых клетках могут произойти вторичные мутации, что приводит к полной утрате этими клетками способности созревать - наступает конечная фаза развития МДС для обозначения который используют термин "острый лейкоз развившийся из предшествующего МДС".
 FAB-классификация МДС Категория Периферическая кровь Костный мозг Рефрактерная анемия <1% бластов <5% бластов Рефрактерная анемия с кольцевидными сидеробластами <1% бластов <5% бластов, >15% кольцевидных сидеробластов Рефрактерная анемия с избытком бластов <5% бластов 5 – 20% бластов Рефрактерная анемия с избытком бластов в трансформации >5% бластов 21 – 30% бластов Хронический миеломоноцитарный лейкоз >1. 109/л моноцитов
FAB-классификация МДС Категория Периферическая кровь Костный мозг Рефрактерная анемия <1% бластов <5% бластов Рефрактерная анемия с кольцевидными сидеробластами <1% бластов <5% бластов, >15% кольцевидных сидеробластов Рефрактерная анемия с избытком бластов <5% бластов 5 – 20% бластов Рефрактерная анемия с избытком бластов в трансформации >5% бластов 21 – 30% бластов Хронический миеломоноцитарный лейкоз >1. 109/л моноцитов
 Клиника Угнетение всех ростков крови: 1) 2) 3) Анемия Лейкопения Тромбоцитопения
Клиника Угнетение всех ростков крови: 1) 2) 3) Анемия Лейкопения Тромбоцитопения
 Течение и прогноз Ø Клиническое течение МДС отличается большим разнообразием. Ø Примерно две трети больных погибают вследствие недостаточности костного мозга. Ø Медиана продолжительности жизни в целом составляет 20 мес. Ø Прогноз для каждого пациента определяется количеством бластов в костном мозге, количеством и особенностями хромосомных аномалий и количеством заинтересованных ростков кроветворения.
Течение и прогноз Ø Клиническое течение МДС отличается большим разнообразием. Ø Примерно две трети больных погибают вследствие недостаточности костного мозга. Ø Медиана продолжительности жизни в целом составляет 20 мес. Ø Прогноз для каждого пациента определяется количеством бластов в костном мозге, количеством и особенностями хромосомных аномалий и количеством заинтересованных ростков кроветворения.
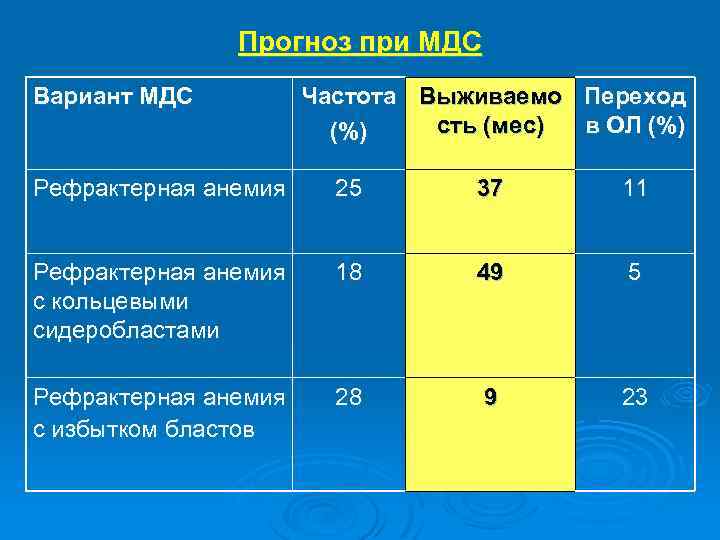 Прогноз при МДС Вариант МДС Частота Выживаемо Переход сть (мес) в ОЛ (%) Рефрактерная анемия 25 37 11 Рефрактерная анемия с кольцевыми сидеробластами 18 49 5 Рефрактерная анемия с избытком бластов 28 9 23
Прогноз при МДС Вариант МДС Частота Выживаемо Переход сть (мес) в ОЛ (%) Рефрактерная анемия 25 37 11 Рефрактерная анемия с кольцевыми сидеробластами 18 49 5 Рефрактерная анемия с избытком бластов 28 9 23
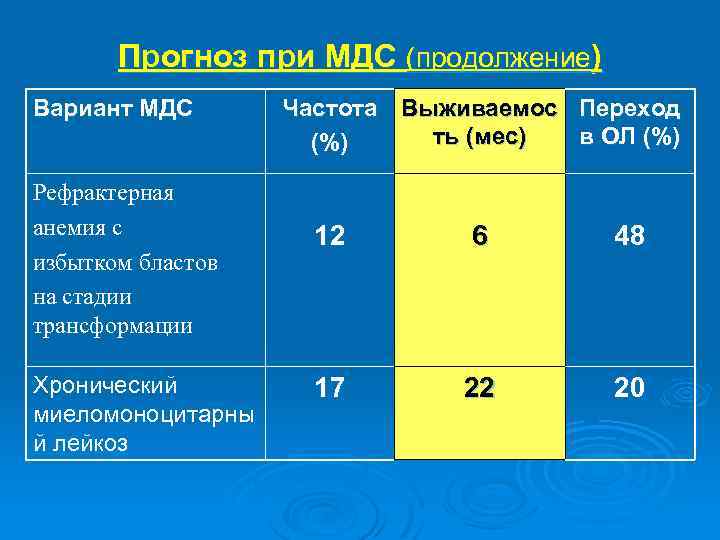 Прогноз при МДС (продолжение) Вариант МДС Рефрактерная анемия с избытком бластов на стадии трансформации Хронический миеломоноцитарны й лейкоз Частота Выживаемос Переход ть (мес) в ОЛ (%) 12 6 48 17 22 20
Прогноз при МДС (продолжение) Вариант МДС Рефрактерная анемия с избытком бластов на стадии трансформации Хронический миеломоноцитарны й лейкоз Частота Выживаемос Переход ть (мес) в ОЛ (%) 12 6 48 17 22 20
 Протокол обследования больных рефрактерными анемиями Ø Общий анализ периферической крови, с подсчетом количества тромбоцитов и ретикулоцитов. Биохимический анализ крови: общий белок, альбумины, глобулины, мочевина, креатинин, билирубин, В-липопротеиды, холестерин, калий, натрий, кальций, железо и обмен железа (ОЖСС, ЛЖСС, насыщение трансферрина железом), щелочная фосфотаза, АСТ, АЛТ, ЛДГ. Ø
Протокол обследования больных рефрактерными анемиями Ø Общий анализ периферической крови, с подсчетом количества тромбоцитов и ретикулоцитов. Биохимический анализ крови: общий белок, альбумины, глобулины, мочевина, креатинин, билирубин, В-липопротеиды, холестерин, калий, натрий, кальций, железо и обмен железа (ОЖСС, ЛЖСС, насыщение трансферрина железом), щелочная фосфотаза, АСТ, АЛТ, ЛДГ. Ø
 Ø Коагулограмма+агрегация тромбоцитов. Ø Антитела к эритроцитам: прямая и непрямая пробы Кумбса. Ø Антитела к тромбоцитам и к лейкоцитам. Ø Иммунохимическое исследование крови и мочи. Ø Маркеры вирусных гепатитов "В" и "С", сифилиса, синдрома приобретенного иммунодефицита.
Ø Коагулограмма+агрегация тромбоцитов. Ø Антитела к эритроцитам: прямая и непрямая пробы Кумбса. Ø Антитела к тромбоцитам и к лейкоцитам. Ø Иммунохимическое исследование крови и мочи. Ø Маркеры вирусных гепатитов "В" и "С", сифилиса, синдрома приобретенного иммунодефицита.
 Ø Определение маркеров системных заболеваний соединительной ткани (антинуклеарный фактор, антитела к ДНК, ревматоидный фактор, антистрептолизин-О). Ø Стернальная пункция Ø Трепанобиопсия Ø УЗИ Ø Эхо-кардиография и УЗИ средостения. Ø Рентгенография грудной клетки. Ø Иммунограмма
Ø Определение маркеров системных заболеваний соединительной ткани (антинуклеарный фактор, антитела к ДНК, ревматоидный фактор, антистрептолизин-О). Ø Стернальная пункция Ø Трепанобиопсия Ø УЗИ Ø Эхо-кардиография и УЗИ средостения. Ø Рентгенография грудной клетки. Ø Иммунограмма
 Лечение Ø Циклоспорин А Ø Малые дозы Цитозара Ø Схема « 7+3» Ø Интерферон - альфа
Лечение Ø Циклоспорин А Ø Малые дозы Цитозара Ø Схема « 7+3» Ø Интерферон - альфа
 Схема 7+3
Схема 7+3
 Трепан
Трепан

 Всякое настоящее образование добывается только путем самообразования. Рубакин Н. А. (1862 - 1946 гг. ) библиограф и писатель
Всякое настоящее образование добывается только путем самообразования. Рубакин Н. А. (1862 - 1946 гг. ) библиограф и писатель
 Образование - клад, труд - ключ к нему. ПЬЕР БУАСТ (1765 - 1824 гг. ) лексикограф, автор
Образование - клад, труд - ключ к нему. ПЬЕР БУАСТ (1765 - 1824 гг. ) лексикограф, автор
 Образование должно быть: истинным ясным полным прочным ЯН АМОС КОМЕНСКИЙ (1592 - 1670 гг. ) мыслитель-гуманист, педагог, писатель
Образование должно быть: истинным ясным полным прочным ЯН АМОС КОМЕНСКИЙ (1592 - 1670 гг. ) мыслитель-гуманист, педагог, писатель


