 Цинк и Титан
Цинк и Титан
 • Степень окисления: +2; 0 • Степень окисления: +2; +4; 0 ; +3 (редко)
• Степень окисления: +2; 0 • Степень окисления: +2; +4; 0 ; +3 (редко)
 • Голубовато - серебристый металл. • Хрупкий • Хорошо прокатывается в листы (при 100 -150 °С) • Плавится при 419, 5 ° С • Серебристо-белый. • Легкий, немного тяжелее Al • Тугоплавкий (1665 °С) • Прочный и вязкий • Поддается различным видам обработки
• Голубовато - серебристый металл. • Хрупкий • Хорошо прокатывается в листы (при 100 -150 °С) • Плавится при 419, 5 ° С • Серебристо-белый. • Легкий, немного тяжелее Al • Тугоплавкий (1665 °С) • Прочный и вязкий • Поддается различным видам обработки
 • Цинк встречается только в виде соединений: • Zn. S – цинковая обманка • Zn. CO 3 – цинковый шпат • Титановые руды распространены широко, но содержание в них титана невелико: • Fe. Ti. O 3 • n. Fe 2 O 3– титаномагнетит • Fe. Ti. O 3 – ильменит • Ti. O 2 - рутил
• Цинк встречается только в виде соединений: • Zn. S – цинковая обманка • Zn. CO 3 – цинковый шпат • Титановые руды распространены широко, но содержание в них титана невелико: • Fe. Ti. O 3 • n. Fe 2 O 3– титаномагнетит • Fe. Ti. O 3 – ильменит • Ti. O 2 - рутил
 • Получение Цинка: 2 Zn. S + 3 O 2 → 2 Zn. O + 2 SO 2↑ Zn. CO 3 → Zn. O + CO 2↑ Zn. O + C → Zn + CO • Получение Титана: • Руды обогащают. Хлорируют рудные концентраты с последующим восстановлением магнием. Ti. O 2 + 4 HCl → Ti. Cl 4 + 2 H 2 O↑ Ti. Cl 4 + 2 Mg → Ti + 2 Mg. Cl 2 • Для выделения чистого титана образующуюся смесь нагревают в вакууме. При этом магний и хлорид магния испаряются.
• Получение Цинка: 2 Zn. S + 3 O 2 → 2 Zn. O + 2 SO 2↑ Zn. CO 3 → Zn. O + CO 2↑ Zn. O + C → Zn + CO • Получение Титана: • Руды обогащают. Хлорируют рудные концентраты с последующим восстановлением магнием. Ti. O 2 + 4 HCl → Ti. Cl 4 + 2 H 2 O↑ Ti. Cl 4 + 2 Mg → Ti + 2 Mg. Cl 2 • Для выделения чистого титана образующуюся смесь нагревают в вакууме. При этом магний и хлорид магния испаряются.
 Химические свойства (цинк) • Взаимодействие с простыми веществами. • Zn + Cl 2 → Zn. Cl 2 • 2 Zn + O 2 → 2 Zn. O • Zn + S → Zn. S • Взаимодействие со сложными веществами. • Zn + 2 Na. OH → Na 2 Zn. O 2 + H 2 • Zn + 2 Na. OH + 2 H 2 O → Na 2[Zn(OH)4] + H 2 • Zn + H 2 O → Zn. O + H 2 (при нагревании)
Химические свойства (цинк) • Взаимодействие с простыми веществами. • Zn + Cl 2 → Zn. Cl 2 • 2 Zn + O 2 → 2 Zn. O • Zn + S → Zn. S • Взаимодействие со сложными веществами. • Zn + 2 Na. OH → Na 2 Zn. O 2 + H 2 • Zn + 2 Na. OH + 2 H 2 O → Na 2[Zn(OH)4] + H 2 • Zn + H 2 O → Zn. O + H 2 (при нагревании)
 Химические свойства (титан) • Благодаря оксидной пленки, титан стоек против коррозии. При обычных условиях на Ti не действуют ни кислород воздуха, ни морская вода, ни «царская водка» . • При нагревании его химическая активность повышается. • Ti + 2 Cl 2 → Ti+4 Cl 4 • Ti + O 2 → Ti+4 O 2 (при нагревании) • Азотная кислота на титан не действует, а с разбавленной серной реагирует. • 2 Ti + 3 H 2 SO 4 → Ti 2+3(SO 4)3 + 3 H 2
Химические свойства (титан) • Благодаря оксидной пленки, титан стоек против коррозии. При обычных условиях на Ti не действуют ни кислород воздуха, ни морская вода, ни «царская водка» . • При нагревании его химическая активность повышается. • Ti + 2 Cl 2 → Ti+4 Cl 4 • Ti + O 2 → Ti+4 O 2 (при нагревании) • Азотная кислота на титан не действует, а с разбавленной серной реагирует. • 2 Ti + 3 H 2 SO 4 → Ti 2+3(SO 4)3 + 3 H 2
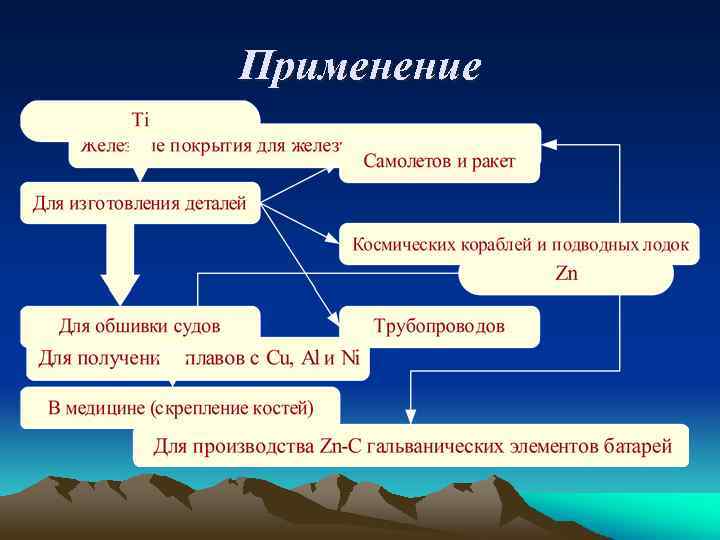 Применение
Применение
 Домашнее задание • § 24, 25, повторить § 23 • Стр. 118 упр. 6.
Домашнее задание • § 24, 25, повторить § 23 • Стр. 118 упр. 6.