Ph_Chem_Biol_3_2014.pptx
- Количество слайдов: 37
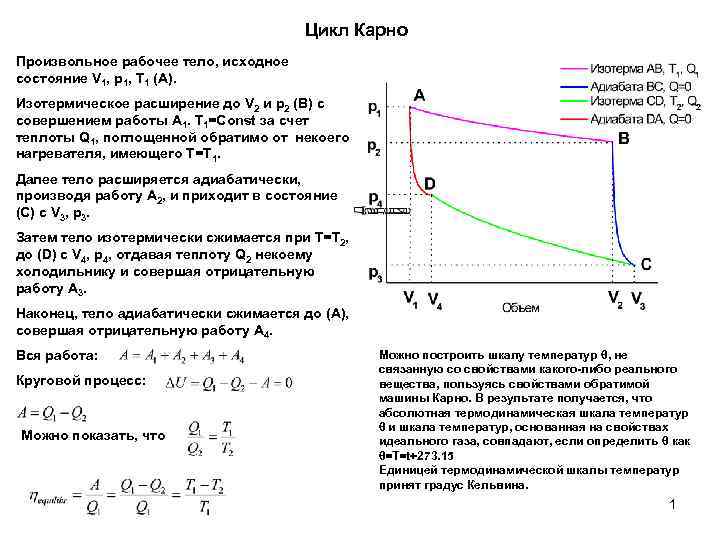
Цикл Карно Произвольное рабочее тело, исходное состояние V 1, p 1, T 1 (A). Изотермическое расширение до V 2 и p 2 (B) с совершением работы A 1. T 1=Const за счет теплоты Q 1, поглощенной обратимо от некоего нагревателя, имеющего T=T 1. Далее тело расширяется адиабатически, производя работу A 2, и приходит в состояние (C) c V 3, p 3. Затем тело изотермически сжимается при T=T 2, до (D) c V 4, p 4, отдавая теплоту Q 2 некоему холодильнику и совершая отрицательную работу A 3. Наконец, тело адиабатически сжимается до (A), совершая отрицательную работу A 4. Вся работа: Круговой процесс: Можно показать, что Можно построить шкалу температур θ, не связанную со свойствами какого-либо реального вещества, пользуясь свойствами обратимой машины Карно. В результате получается, что абсолютная термодинамическая шкала температур θ и шкала температур, основанная на свойствах идеального газа, совпадают, если определить θ как θ=T=t+273. 15 Единицей термодинамической шкалы температур принят градус Кельвина. 1

Количественная формулировка 2 -го начала термодинамики, энтропия Для обратимой машины Карно , а для необратимой Отношение Q/T называют приведенной теплотой. В обратимом циклическом процессе , а в необратимом Разбивая круговой интеграл на два криволинейных для двух произвольных путей получим Таким образом, величина является функцией состояния. (полученная в условиях обратимости) Эту функцию называют энтропией. Можно показать, что в необратимых процессах энтропия всегда возрастает. В изолированных системах изменение энтропии – критерий самопроизвольности процесса: энтропия должна возрастать. 2
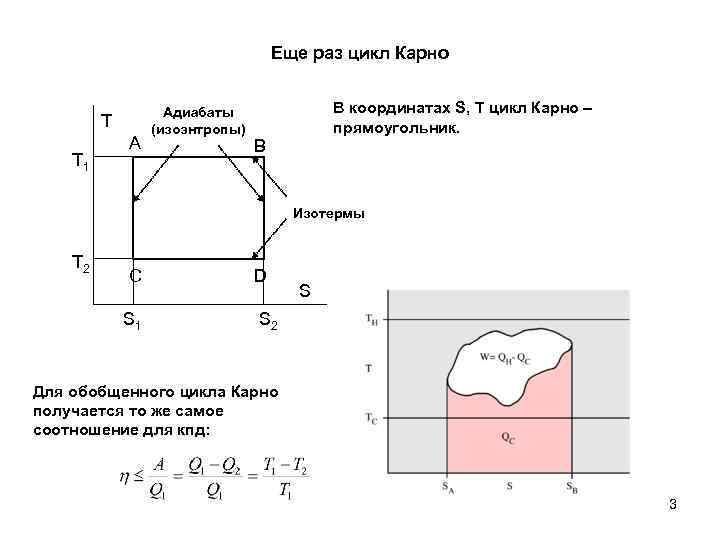
Еще раз цикл Карно T T 1 A Адиабаты (изоэнтропы) В координатах S, T цикл Карно – прямоугольник. B Изотермы T 2 C S 1 D S S 2 Для обобщенного цикла Карно получается то же самое соотношение для кпд: 3

Энтропия и вероятность В статистической термодинамике показывается, что энтропия и вероятность состояния системы связаны уравнением вида , здесь W – вероятность состояния, A и B – некоторые константы. Почему логарифмическая связь? В принципе, это понятно т. к. энтропия системы аддитивна (складывается из энтропий ее частей), а вероятность конечного события – это произведение вероятностей отдельных событий. 2 -й закон термодинамики – статистический закон, он строго соблюдается только для ансамблей из большого числа частиц (вспомним падение одиночного шарика и распределение шариков в коробке с емкостями). Пример: подбрасывание монет. 10 монет подбрасываем 500 раз. Вероятность выпасть поровну 5 орлов и 5 решек (5/5) – 24. 6%, а 9 орлов и 1 решка или наоборот (9/1) – 1%. Различие между наиболее и наименее вероятными исходами всего 24. 6 раза. Сделаем то же самое со 100 монетами – различие между 50/50 и 90/10 уже 10 16 раз! В реальных системах число частиц порядка 1020, даже в нано-системах содержится порядка 103 частиц, поэтому 2 -е начало соблюдается. 4

Возрастание энтропии при равновесном изотермическом расширении идеального газа Феноменологический подход Работа равновесного расширения газа Теплота равна работе с обр. знаком Получаем энтропию: (1) Статистический подход Как рассчитать отношение вероятностей? Мысленно разбиваем начальный и конечный объемы V 1 и V 2 на маленькие кубики одинаковых размеров. В V 1 будет n 1 кубиков, в V 2 – n 2. Поскольку кубики одинаковые, n 2/n 1 = V 2/V 1. Число способов размещения 1 -й молекулы газа в V 1 равно n 1, а N молекул – n 1 N/N! Деление на N! – т. к. молекулы одинаковы. Аналогично для объема V 2 – получим n 2 N/N!. Вероятность состояния пропорциональна числу способов его осуществления, поэтому (2) Сравнивая (1) и (2) получим NA=R. Если был 1 моль газа, то N – число Авогадро NA, след. постоянная A=R/NA=k – постоянная Больцмана. 5

Знание о том, как меняется энтропия в том или ином процессе позволяет предвидеть, пойдет ли такой процесс самопроизвольно, или нет. Проблема в том, что надо знать общее изменение энтропии – не только рассматриваемой системы, но и окружающей ее среды. ΔSsyst+ΔSenvir=0 система находится в равновесии сама и с окружающей средой ΔSsyst+ΔSenvir>0 процесс может проходить самопроизвольно ΔSsyst+ΔSenvir<0 процесс не может проходить самопроизвольно Поэтому пользоваться энтропией как таковой неудобно. Удобнее использовать другую термодинамическую функцию – свободную энергию. Растения и животные самопроизвольно развиваются в очень сложные, высокоупорядоченные структуры. Энтропия – мера хаотичности, разупорядоченности. Находятся ли закономерности биологических систем в противоречии со 2 -м началом? Считается, что противоречия нет, т. к. энтропия организма уменьшается, а энтропия окружающей среды при этом увеличивается, причем в большей степени. 6

Самопроизвольное возникновение упорядоченной структуры в неживом объекте 7
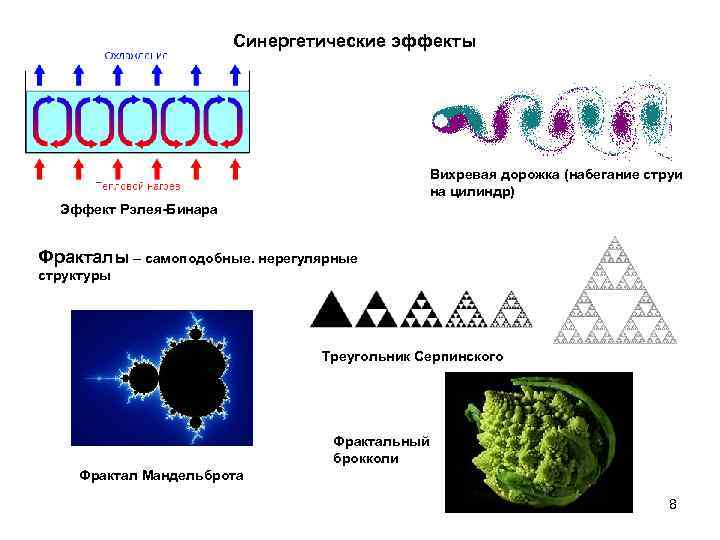
Синергетические эффекты Вихревая дорожка (набегание струи на цилиндр) Эффект Рэлея-Бинара Фракталы – самоподобные. нерегулярные структуры Треугольник Серпинского Фрактальный брокколи Фрактал Мандельброта 8
9
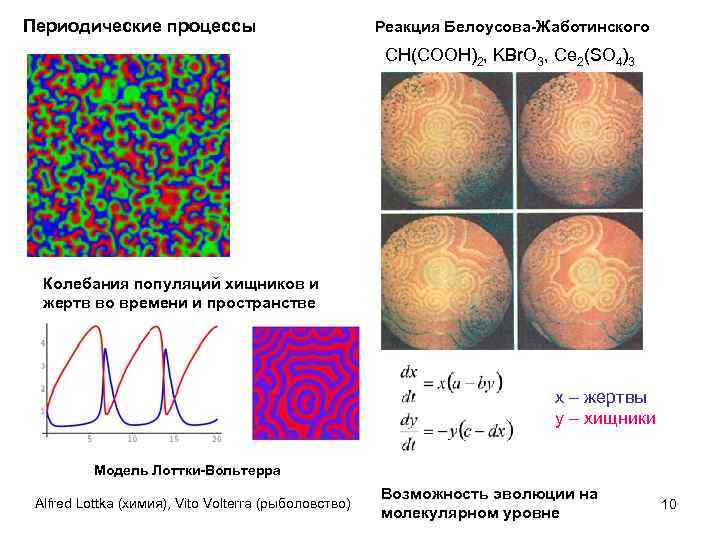
Периодические процессы Реакция Белоусова-Жаботинского CH(COOH)2, KBr. O 3, Ce 2(SO 4)3 Колебания популяций хищников и жертв во времени и пространстве x – жертвы y – хищники Модель Лоттки-Вольтерра Alfred Lottka (химия), Vito Volterra (рыболовство) Возможность эволюции на молекулярном уровне 10

3 -й закон термодинамики Нернст (1906 г. ) экспериментально обнаружил, что при стремлении температуры к абсолютному нулю энтропия химических реакций также стремится к нулю. Планк (1912 г. ) на основании данных Нернста выдвинул гипотезу (постулат): «Энтропия индивидуальных кристаллических веществ при абсолютном нуле равна нулю» Это – гипотеза, проверить ее невозможно т. к. абсолютный нуль недостижим: нет холодильника с отрицательной абсолютной температурой, которому можно было бы отдать последние остатки тепла. Если поверить в гипотезу Планка, то можно вычислить абсолютную энтропию. Например, некий кристалл плавится при 15 K. Хотим вычислить его энтропию при 273 K. Теплоемкость при сравнительно высоких температурах измеряют экспериментально, а вблизи абсолютного нуля обычно считают по теории теплоемкости Дебая. 11

Термодинамические потенциалы – это функции состояния системы, имеющие размерность энергии. Они являются критериями направления процесса, их экстремальные значения при соответствующих условиях отвечают равновесию и являются условиями равновесия. Бесконечно малая работа , при S, V=Const , дифференциал внутренней энергии. В равновесии , Внутренняя энергия – изохорно-изоэнтропийный потенциал. Для энтальпии: равновесии , при S, p=Const , при , Энтальпия – изобарно-изоэнтропийный потенциал. В принципе, можно пользоваться этими потенциалами как критериями самопроизвольного протекания процесса и условиями равновесия. Но поддерживать энтропию постоянной крайне трудно. Поэтому использовать внутреннюю энергию или энтальпию в качестве потенциалов неудобно. Гораздо удобнее свободная энергия Гельмгольца, и особенно – свободная энергия Гиббса. 12

Изохорно-изотермический потенциал (V, T=Const) – свободная энергия Гельмгольца (формально – объединение 1 -го и 2 -го начал) В общем случае: При равновесии: Проинтегрируем от состояния 1 до состояния 2, получим: Вполне логично: максимальная работа, которую может совершить система при переходе из состояния 1 в состояние 2 равна убыли ее внутренней энергии за вычетом некой части энергии, которую превратить в работу нельзя ( «связанной энергии» ). Величины в скобках – комбинации функций состояния, следовательно – сами по себе также функции состояния, Внутренняя энергия состоит из свободной и связанной: Связанная (TS) может переходить только в теплоту, TΔS=Q. Свободная энергия F в равновесном процессе переходит в работу, в неравновесном – частично также в теплоту. Если T≠Const, U нельзя разделить на свободную и связанную. Можно показать, что и . Это значит, что F падает с ростом объема и температуры. 13

Изобарно-изотермический потенциал (p, T=Const) – свободная энергия Гиббса Свободная энергия Гиббса применяется в химии чаще, чем свободная энергия Гельмгольца т. к. химические процессы обычно идут при постоянном давлении, в частности – атмосферном, но вовсе не при постоянном объеме. Среди всех возможных работ A выделим работу расширения p. V. Остальные работы A’ считают «полезными» : δA=pd. V+δA’. Интегрируя при p, T=Const, получим Таким образом, имеем новую функцию состояния: свободную энергию Гиббса Полезная работа, которую может совершить система В равновесном процессе: Можно показать, что и . Таким образом, G увеличивается с ростом давления и уменьшается с ростом температуры. 14
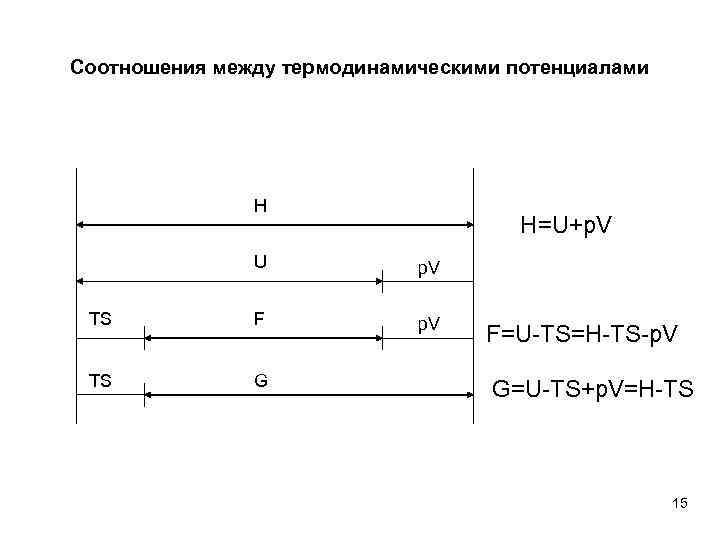
Соотношения между термодинамическими потенциалами H H=U+p. V U p. V TS F p. V TS G F=U-TS=H-TS-p. V G=U-TS+p. V=H-TS 15

Характеристические функции и естественные переменные Две пары переменных: S, T – пара, связанная с теплотой и p, V – пара, связанная с работой, дают все возможные сочетания для построения термодинамических потенциалов. Можно выбрать ту или иную функцию, в зависимости от конкретной задачи. Частные производные этих функций при характерном для них наборе параметров дают величины основных параметров состояния. Таким образом, через эти функции и их производные можно выразить в явной форме любое термодинамическое свойство системы. В этом состоит характеристичность. Замена этих переменных другими (в принципе – вполне возможная) лишает их характеристичности. Поэтому такие переменные называются естественными. 16

Условия самопроизвольного протекания процессов ΔU < 0 при S, V=Const ΔH < 0 при S, p=Const ΔF < 0 при T, V=Const ΔG < 0 при p, T=Const Условия равновесия В состоянии равновесия системы ее термодинамические потенциалы имеют минимальные значения при постоянстве своих естественных переменных, а энтропия имеет максимальное значение (при своих естественных переменных – U, V или H, p). Убыль т. д. потенциалов в равновесном процессе при постоянстве естественных переменных равна максимальной работе, которую может совершить система. 17
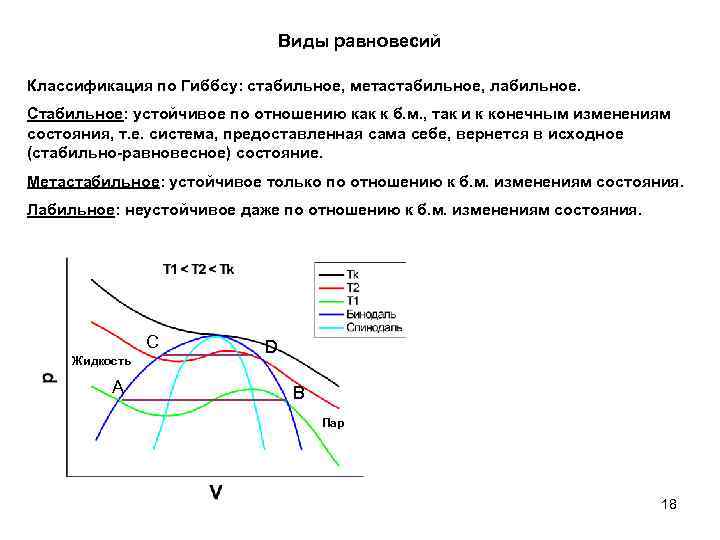
Виды равновесий Классификация по Гиббсу: стабильное, метастабильное, лабильное. Стабильное: устойчивое по отношению как к б. м. , так и к конечным изменениям состояния, т. е. система, предоставленная сама себе, вернется в исходное (стабильно-равновесное) состояние. Метастабильное: устойчивое только по отношению к б. м. изменениям состояния. Лабильное: неустойчивое даже по отношению к б. м. изменениям состояния. C Жидкость A D B Пар 18

Уравнение Гиббса-Гельмгольца Для свободной энергии Гиббса справедливо выражение Гиббс и Гельмгольц независимо получили отсюда полезное выражение для энтальпии – теплового эффекта химической реакции. Поскольку , можно записать Для конечных приращений можно, соответственно, записать Зная ΔG, можно вычислить ΔH реакции, если известна температурная зависимость ΔG при постоянном давлении – надо получить зависимость ΔG/T от 1/T. ΔG= -RTln. K, K – константа равновесия химической реакции. 19

Фазовые переходы в «чистом виде» : в системе только 1 вещество, возможно наличие нескольких фаз – различных агрегатных состояний этого вещества. 1 моль вещества переходит из состояния 1 в состояние 2. p, T=Const Работа – только расширение. Рассмотрим изменение внутренней энергии. Потенциал Гиббса для 1 моля (или 1 ед. массы) вещества в двух фазах, при равновесии один и тот же. Если фазы находятся в равновесии, то p, T не могут меняться независимо. Меняются так, что при 20

Уравнение Клаузиуса-Клапейрона λ – теплота фазового перехода Фазовые переходы 1 -го рода: плавление, испарение, возгонка. Интенсивные параметры меняются скачкообразно, а экстенсивные – непрерывно. Правило Трутона: кал/моль∙град При фазовом переходе энтальпия изменяется скачком. Это значит, что Подводимое к системе тепло затрачивается на совершение фазового перехода, а не на подъем температуры. Откуда может взяться эта закономерность, и на что могут указывать отклонения от нее? 21

Фазовые переходы 2 -го рода При фазовых переходах 1 -го рода потенциал Гиббса (G) сохраняется, но другие потенциалы – F, U, H и энтропия S – изменяются. Но есть и фазовые переходы иного типа, когда все потенциалы сохраняются, даже объем не изменяется! Такие переходы – фазовые переходы 2 -го рода. Скачкообразно изменяются 2 -е производные т-д потенциалов, например функции претерпевают разрыв Cp T λ – кривая гелия 22

Первое знакомство с правилом фаз Чистое вещество, 1 фаза – p, T могут изменяться независимо в некотором интервале – 2 степени свободы системы. 2 фазы в равновесии: 1 степень свободы. Если меняем температуру, то давление не любое, а такое, что отвечает линии на фазовой диаграмме, и наоборот. 3 фазы в равновесии: степеней свободы нет, система инвариантна (нонвариантна). p Вода 1 атм Лед Пар T Фазовая диаграмма воды Тройная точка: 0. 01 0 С, 0. 006 атм. 23

Многокомпонентные системы Система содержит k компонентов ni – число молей i-го компонента Если процесс равновесный и работа только расширения, то Химический потенциал i-го компонента Дифференциал функции Гиббса при p, T = Const 24

Уравнение Гиббса-Дюгема Что произойдет если массу системы увеличить в q раз, сохраняя пропорции между ее компонентами? Все экстенсивные параметры системы – V, U, S, H, F, G также возрастут в q раз. Таким образом, эти величины, в т. ч. G – линейные однородные функции. Однородная функция мерности m (1) Функция Гиббса как линейная однородная функция: Дифференциал выражения (1): Дифференциал функции Гиббса по определению химического потенциала: (2) (3) Комбинируем (2) и (3): 25

Равенство значений интенсивных параметров в сосуществующих фазах при равновесии Равенство температур. Из фазы (1) в фазу (2) перенесли тепло δQ, не нарушая равновесия, т. е. d. S=0 Равенство давлений. Объем фазы (1) вырос на d. V, а фазы (2) уменьшился на d. V, не нарушая равновесия, т. е. d. F=0 Равенство химических потенциалов. Равновесно перенесли dni молей i-го компонента из фазы (1) в фазу (2), d. G=0 26

Правило фаз Гиббса Система, находящаяся в состоянии равновесия, содержит Φ фаз и k компонентов. Сколько степеней свободы может быть у такой системы? Давление и температура во всех Φ фазах одинаковы. Химические потенциалы каждого из компонентов также одинаковы во всех фазах. Всего имеем k+2 переменных: k компонентов, их концентрации могут изменяться независимо, + давление, + температура. Уравнений связи между переменными – Φ. Следовательно, число независимых переменных (степеней свободы) равно f = k – Φ + 2 p Вода Как это согласуется со льдинами, плывущими по Неве? 1 атм Лед Пар T 27

Идеальные газовые смеси Идеальная газовая смесь объема V: Энтропия как функция парциального объема и/или парциального давления i-го газа в смеси. Свободная энергия Гельмгольца как функция парциального давления i-го газа в смеси. Химический потенциал i-го газа в идеальной газовой смеси. 28

Неидеальные газовые смеси, фугитивность Фугитивность (летучесть) – вместо парциального давления, для математически простого описания неидеальных газовых смесей Стандартизация фугитивности – на разреженный газ, т. е. Уравнение Гиббса-Дюгема: 29

Растворы неэлектролитов Раствор: жидкая фаза, состав которой (в некоторых пределах) можно изменять непрерывно. Неэлектролит: вещество, которое при растворении не распадается на ионные (заряженные) составляющие, неионогенное вещество. Равновесие жидкий раствор – насыщенный пар. p p 1 0 p 2 0 Хим. потенциал i-го компонента пара: p 2 p 1 1 Пар над раствором – смесь газов, в равновесии с раствором: 2 Следовательно, химический потенциал чистого жидкого i-го компонента x Хим. потенциал i-го компонента в растворе: 30
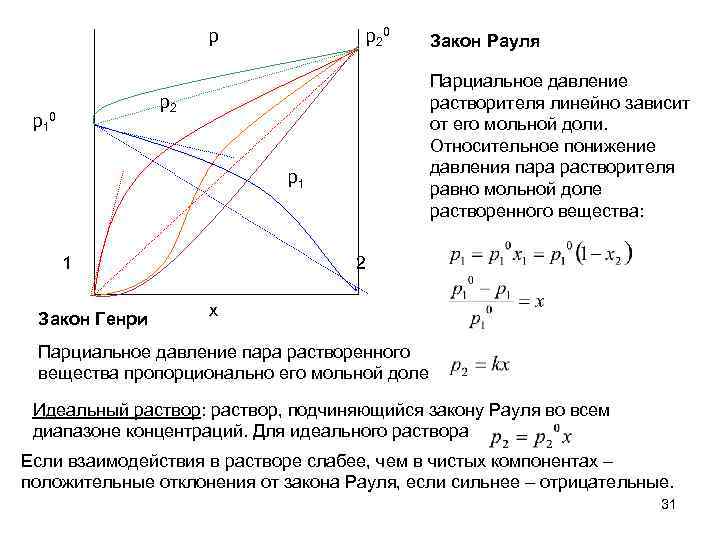
p p 2 0 Парциальное давление растворителя линейно зависит от его мольной доли. Относительное понижение давления пара растворителя равно мольной доле растворенного вещества: p 2 p 1 0 p 1 1 Закон Генри Закон Рауля 2 x Парциальное давление пара растворенного вещества пропорционально его мольной доле Идеальный раствор: раствор, подчиняющийся закону Рауля во всем диапазоне концентраций. Для идеального раствора Если взаимодействия в растворе слабее, чем в чистых компонентах – положительные отклонения от закона Рауля, если сильнее – отрицательные. 31

Активность компонента раствора Идеальная газовая смесь: Реальная газовая смесь: Идеальный раствор: Реальный раствор: вводим функцию «активность» , которая выражена через p или f: Получим: Можно ввести параметр «коэффициент активности» : γi > или < 1 соответственно при «+» или «-» отклонениях от закона Рауля. Стандартизация активности Предельно разбавленный раствор – закон Рауля выполнен, Для растворенного вещества сложнее: Стандартное состояние растворенного вещества – такое, когда его летучесть 32 равна коэффициенту Генри в предельно разбавленном растворе.

Коллигативные свойства растворов Эбуллиоскопия Жидкость кипит, когда давление ее нас. пара становится равным внешнему давлению. Если растворенное вещество нелетучее, то в паре только растворитель. По закону Рауля: Ищем зависимость Ткип от состава раствора, пользуясь ур. Клаузиуса-Клапейрона Можно получить, что понижение Ткип пропорционально моляльности растворенного вещества, это позволяет найти его молярную массу Криоскопия Температура начала затвердевания раствора – Т, при которой раствор стал насыщенным по отношению к чистому растворителю. При Ткр давление пара растворителя над раствором и над твердым растворителем одинаково. T Эвтектика Te 1 xe 33 2
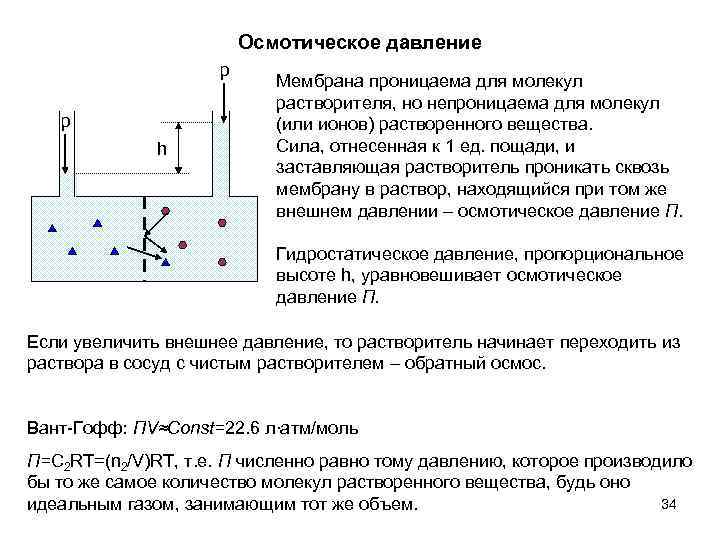
Осмотическое давление p p h Мембрана проницаема для молекул растворителя, но непроницаема для молекул (или ионов) растворенного вещества. Сила, отнесенная к 1 ед. пощади, и заставляющая растворитель проникать сквозь мембрану в раствор, находящийся при том же внешнем давлении – осмотическое давление Π. Гидростатическое давление, пропорциональное высоте h, уравновешивает осмотическое давление Π. Если увеличить внешнее давление, то растворитель начинает переходить из раствора в сосуд с чистым растворителем – обратный осмос. Вант-Гофф: ΠV≈Const=22. 6 л∙атм/моль Π=С 2 RT=(n 2/V)RT, т. е. Π численно равно тому давлению, которое производило бы то же самое количество молекул растворенного вещества, будь оно 34 идеальным газом, занимающим тот же объем.

Термодинамика осмотического давления Осмотическая мембрана: в сущности, «продолжение» фазы растворителя. Потому фаз 2, компонентов 2, при фиксации p, T система становится нонвариантной: f=0. Чистый растворитель: Раствор: Равновесие по чистому растворителю: Осмотический коэффициент 35

Химическое равновесие Равновесие химической реакции: νAA + νBB ↔ νCC + νDD В состоянии равновесия То есть получаем: Если реакция не в равновесии: Для реакции в растворе: 36

Принцип Ле-Шателье - Брауна • Для экзотермических реакций, когда изменения энтальпии меньше нуля, производная константы равновесия по температуре меньше нуля, т. е. с увеличением температуры уменьшается глубина протекания процесса, идущего с выделением тепла (константа уменьшается) • Для эндотермических процессов когда изменения энтальпии больше нуля, производная константы равновесия по температуре больше нуля, т. е с увеличением температуры увеличивается глубина протекания процесса, идущего с поглощением тепла (константа растет). 37
Ph_Chem_Biol_3_2014.pptx