Биогеохимический цикл азота.ppt
- Количество слайдов: 15

 Цикл азота состоит в следующем. Его главная роль заключается в том, что он входит в состав жизненно важных структур организма аминокислот белка, а также нуклеиновых кислот. В живых организмах содержится примерно 3% всего активного фонда азота. Растения потребляют примерно 1% азота; время его круговорота составляет 100 лет.
Цикл азота состоит в следующем. Его главная роль заключается в том, что он входит в состав жизненно важных структур организма аминокислот белка, а также нуклеиновых кислот. В живых организмах содержится примерно 3% всего активного фонда азота. Растения потребляют примерно 1% азота; время его круговорота составляет 100 лет.
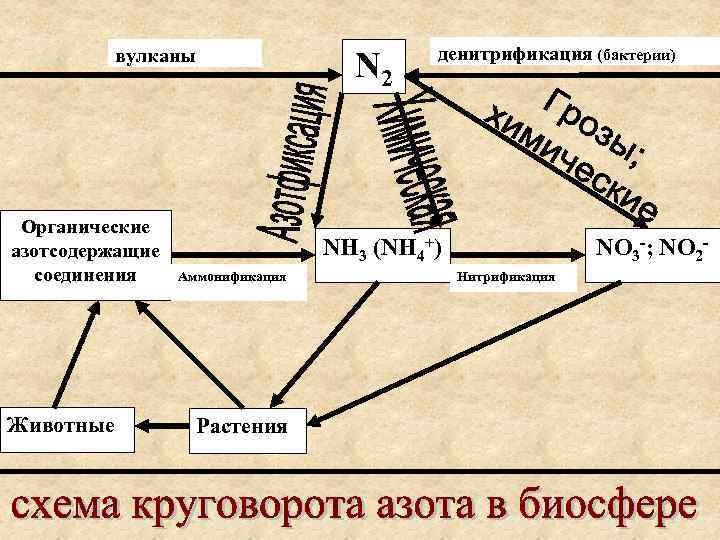 вулканы Органические азотсодержащие соединения Животные N 2 денитрификация (бактерии) NH 3 (NH 4+) Аммонификация Растения NO 3 -; NO 2 Нитрификация
вулканы Органические азотсодержащие соединения Животные N 2 денитрификация (бактерии) NH 3 (NH 4+) Аммонификация Растения NO 3 -; NO 2 Нитрификация
 Денитрификация - Процесс потери экосистемой «доступного» азота. Он может происходить в анаэробных условиях, например в болотах: Pseudomonas 2 NO 3 - N 2 + 3 O 2 денитрификатор ( этот кислород требуется для окисления углеводов бактерий ) Серобактерия S + N 2 2 NO 3 денитрификатор + O 2
Денитрификация - Процесс потери экосистемой «доступного» азота. Он может происходить в анаэробных условиях, например в болотах: Pseudomonas 2 NO 3 - N 2 + 3 O 2 денитрификатор ( этот кислород требуется для окисления углеводов бактерий ) Серобактерия S + N 2 2 NO 3 денитрификатор + O 2
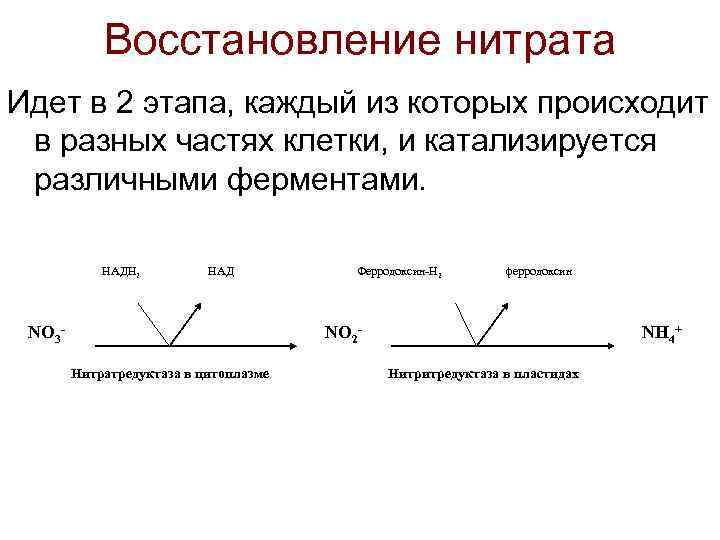 Восстановление нитрата Идет в 2 этапа, каждый из которых происходит в разных частях клетки, и катализируется различными ферментами. НАДН 2 НАД NO 3 - Ферродоксин-Н 2 ферродоксин NO 2 Нитратредуктаза в цитоплазме NH 4+ Нитритредуктаза в пластидах
Восстановление нитрата Идет в 2 этапа, каждый из которых происходит в разных частях клетки, и катализируется различными ферментами. НАДН 2 НАД NO 3 - Ферродоксин-Н 2 ферродоксин NO 2 Нитратредуктаза в цитоплазме NH 4+ Нитритредуктаза в пластидах
 Фиксация азота Процесс превращения азота, содержащегося в ризосфере (газы в почве), в ионы аммония. Таким путем в почву ежегодно вносится около 25 кг азота на 1 га. Основной процесс: 12 АТФ N 2 + 6 H+ + 6 e- 12 АДФ + 12 Pн 2 NH 3 Этот многоступенчатый процесс катализируется ферментным комплексом, называемым нитрогеназой, который для выполнения своих функций нуждается в Fe и Mo. Существует несколько видов свободноживущих азотфиксирующих бактерий, таких, как Azotbacter, но значительно большую роль в фиксации азота играют симбиотические бактерии (рода Rhizobium) и цианобактерии, например, Nostoc.
Фиксация азота Процесс превращения азота, содержащегося в ризосфере (газы в почве), в ионы аммония. Таким путем в почву ежегодно вносится около 25 кг азота на 1 га. Основной процесс: 12 АТФ N 2 + 6 H+ + 6 e- 12 АДФ + 12 Pн 2 NH 3 Этот многоступенчатый процесс катализируется ферментным комплексом, называемым нитрогеназой, который для выполнения своих функций нуждается в Fe и Mo. Существует несколько видов свободноживущих азотфиксирующих бактерий, таких, как Azotbacter, но значительно большую роль в фиксации азота играют симбиотические бактерии (рода Rhizobium) и цианобактерии, например, Nostoc.
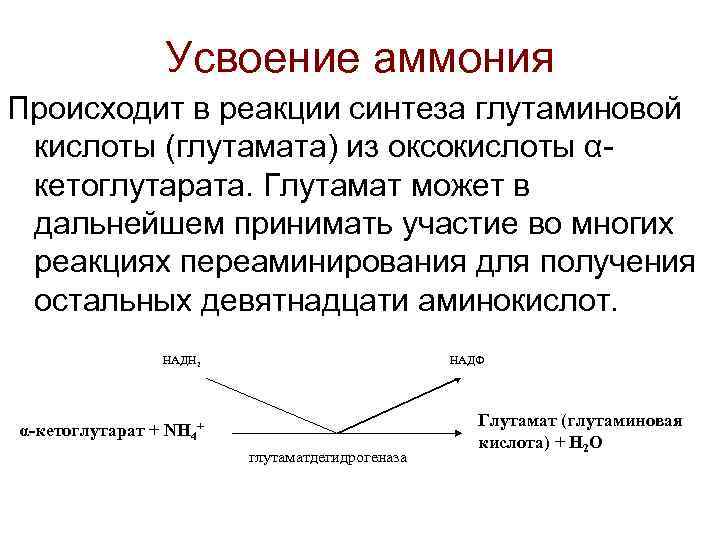 Усвоение аммония Происходит в реакции синтеза глутаминовой кислоты (глутамата) из оксокислоты αкетоглутарата. Глутамат может в дальнейшем принимать участие во многих реакциях переаминирования для получения остальных девятнадцати аминокислот. НАДН 2 НАДФ α-кетоглутарат + NH 4+ глутаматдегидрогеназа Глутамат (глутаминовая кислота) + Н 2 О
Усвоение аммония Происходит в реакции синтеза глутаминовой кислоты (глутамата) из оксокислоты αкетоглутарата. Глутамат может в дальнейшем принимать участие во многих реакциях переаминирования для получения остальных девятнадцати аминокислот. НАДН 2 НАДФ α-кетоглутарат + NH 4+ глутаматдегидрогеназа Глутамат (глутаминовая кислота) + Н 2 О
 Гниение Высвобождает азот из сложных органических веществ, например: протеазы Белок аминокислоты дезаминазы аминокислоты NH 4+ + оксокислоты уреазы мочевина NH 4+ + углекислый газ Этот процесс ведется сапрофитными бактериями и грибами (редуцентами) и иногда называется аммонификацией, так как аммоний NH 4+ является его конечным продуктом.
Гниение Высвобождает азот из сложных органических веществ, например: протеазы Белок аминокислоты дезаминазы аминокислоты NH 4+ + оксокислоты уреазы мочевина NH 4+ + углекислый газ Этот процесс ведется сапрофитными бактериями и грибами (редуцентами) и иногда называется аммонификацией, так как аммоний NH 4+ является его конечным продуктом.
 Нитрификация: Последовательность двух окислительных процессов, которые превращают соединения аммония в нитраты. При этом выделяется энергия для хемоавтотрофных бактерий нитрификаторов, которые Бактерии Nitrosomonas NH 4+ NO 2 - + энергия Бактерии Nitrobacter NO 2 - NO 3 - + энергия Эти реакции преобразуют азотсодержащие вещества в нитраты, которые легче всего усваиваются корнями растений.
Нитрификация: Последовательность двух окислительных процессов, которые превращают соединения аммония в нитраты. При этом выделяется энергия для хемоавтотрофных бактерий нитрификаторов, которые Бактерии Nitrosomonas NH 4+ NO 2 - + энергия Бактерии Nitrobacter NO 2 - NO 3 - + энергия Эти реакции преобразуют азотсодержащие вещества в нитраты, которые легче всего усваиваются корнями растений.
 Молния может фиксировать атмосферный азот. В условиях высокоэнергетического разряда в атмосфере может происходить реакция соединения азота и кислорода. Полученное соединение растворяется в дождевой воде и выпадает на землю в виде слабокислого раствора. H 2 O N 2 + 2 O 2 2 NO 2 2 HNO 3 H 2 O N 2 + O 2 2 NO 2 HNO 2
Молния может фиксировать атмосферный азот. В условиях высокоэнергетического разряда в атмосфере может происходить реакция соединения азота и кислорода. Полученное соединение растворяется в дождевой воде и выпадает на землю в виде слабокислого раствора. H 2 O N 2 + 2 O 2 2 NO 2 2 HNO 3 H 2 O N 2 + O 2 2 NO 2 HNO 2
 Вулканы Потеря азота уравновешивается поступлением в атмосферу так называемого «ювенильного азота» из вулканов. Этим путем в круговорот ежегодно возвращается 2… 3 млн. т фиксированного азота.
Вулканы Потеря азота уравновешивается поступлением в атмосферу так называемого «ювенильного азота» из вулканов. Этим путем в круговорот ежегодно возвращается 2… 3 млн. т фиксированного азота.
 Из всех видов вмешательства человека в естественный круговорот веществ промышленная фиксация азота – самое крупное по масштабам. С 1950 года ежегодное количество азота, фиксируемого в процессе производства удобрений, возросло примерно в 5 раз. В 1968 году мировая промышленность дала около 30 млн. т фиксированного азота; к 2000 году эта цифра превысила 1000 млн. т.
Из всех видов вмешательства человека в естественный круговорот веществ промышленная фиксация азота – самое крупное по масштабам. С 1950 года ежегодное количество азота, фиксируемого в процессе производства удобрений, возросло примерно в 5 раз. В 1968 году мировая промышленность дала около 30 млн. т фиксированного азота; к 2000 году эта цифра превысила 1000 млн. т.
 Круговорот азота в настоящее время подвергается сильному воздействию со стороны человека. С одной стороны, массовое производство азотных удобрений и их использование приводит к избыточному накоплению нитратов. Азот, поступающий на поля в виде удобрений, теряется из-за отчуждения урожая, выщелачивания и денитрификации. С другой стороны, при снижении скорости превращения аммиака в нитраты аммонийные удобрения накапливаются в почве. Возможно подавление деятельности микроорганизмов в результате загрязнения почвы отходами промышленности. Однако эти процессы носят локальный характер. Гораздо большее значение имеет поступление оксидов азота в атмосферу при сжигании топлива на ТЭЦ, транспорте, заводах ( «лисий хвост» ). В промышленных районах их концентрация в воздухе становится очень опасной. Под воздействием излучения происходят реакции органики (углеводородов) с оксидами азота с образованием высокотоксичных и канцерогенных соединений.
Круговорот азота в настоящее время подвергается сильному воздействию со стороны человека. С одной стороны, массовое производство азотных удобрений и их использование приводит к избыточному накоплению нитратов. Азот, поступающий на поля в виде удобрений, теряется из-за отчуждения урожая, выщелачивания и денитрификации. С другой стороны, при снижении скорости превращения аммиака в нитраты аммонийные удобрения накапливаются в почве. Возможно подавление деятельности микроорганизмов в результате загрязнения почвы отходами промышленности. Однако эти процессы носят локальный характер. Гораздо большее значение имеет поступление оксидов азота в атмосферу при сжигании топлива на ТЭЦ, транспорте, заводах ( «лисий хвост» ). В промышленных районах их концентрация в воздухе становится очень опасной. Под воздействием излучения происходят реакции органики (углеводородов) с оксидами азота с образованием высокотоксичных и канцерогенных соединений.
 Антропогенное влияние на круговорот азота определяется следующими процессами:
Антропогенное влияние на круговорот азота определяется следующими процессами:



