sirs 2015.ppt
- Количество слайдов: 94
 Что такое воспаление ? Клинически острое воспаление характеризуется 5 кардинальными признаками: rubor (покраснение), calor (увеличение температуры), tumor (припухлость), dolor (боль), и functio laesa (нарушение функции).
Что такое воспаление ? Клинически острое воспаление характеризуется 5 кардинальными признаками: rubor (покраснение), calor (увеличение температуры), tumor (припухлость), dolor (боль), и functio laesa (нарушение функции).
 Признаки ССВО /СВР - температура тела больше 38 С или менее 36 С; - частота сердечных сокращений более 90 в минуту; -частота дыханий более 20 в минуту или артериальная гипокапния менее 32 мм рт ст; - лейкоцитоз более 12 000 в мм или лейкопения менее 4 000 мм или наличие более 10 % незрелых форм нейтрофилов;
Признаки ССВО /СВР - температура тела больше 38 С или менее 36 С; - частота сердечных сокращений более 90 в минуту; -частота дыханий более 20 в минуту или артериальная гипокапния менее 32 мм рт ст; - лейкоцитоз более 12 000 в мм или лейкопения менее 4 000 мм или наличие более 10 % незрелых форм нейтрофилов;
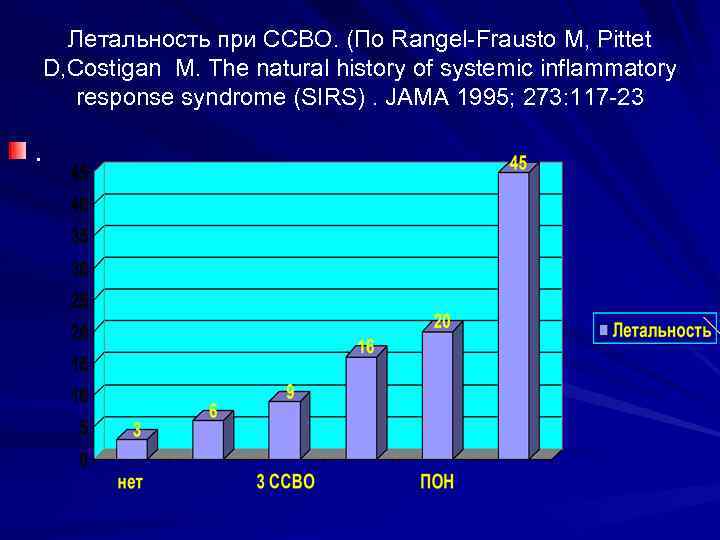 Летальность при ССВО. (По Rangel-Frausto M, Pittet D, Costigan M. The natural history of systemic inflammatory response syndrome (SIRS). JAMA 1995; 273: 117 -23 .
Летальность при ССВО. (По Rangel-Frausto M, Pittet D, Costigan M. The natural history of systemic inflammatory response syndrome (SIRS). JAMA 1995; 273: 117 -23 .
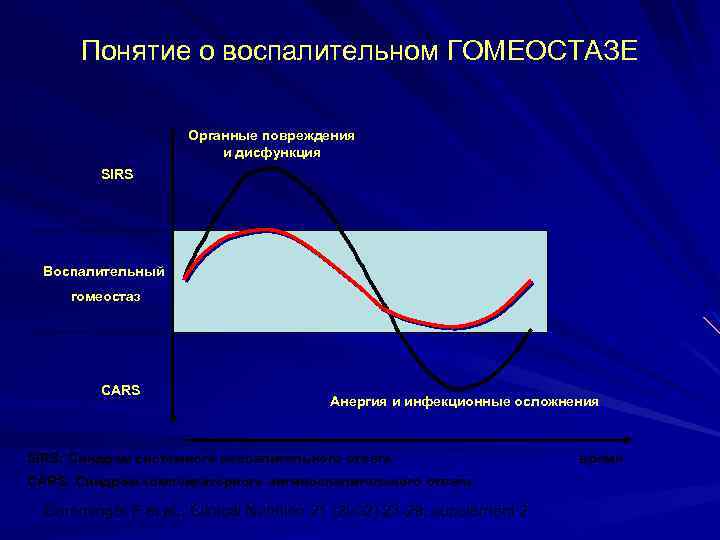 Понятие о воспалительном ГОМЕОСТАЗЕ Oрганные повреждения и дисфункция SIRS Воспалительный гомеостаз CARS Анергия и инфекционные осложнения SIRS: Синдром системного воспалительного ответа CARS: Синдром компенсаторного антивоспалительного ответа Grimminger F et al. , Clinical Nutrition 21 (2002) 23 -29, supplement 2 время
Понятие о воспалительном ГОМЕОСТАЗЕ Oрганные повреждения и дисфункция SIRS Воспалительный гомеостаз CARS Анергия и инфекционные осложнения SIRS: Синдром системного воспалительного ответа CARS: Синдром компенсаторного антивоспалительного ответа Grimminger F et al. , Clinical Nutrition 21 (2002) 23 -29, supplement 2 время
 Причины СВР Механическое повреждение тканей (ожоги, крашсиндром, хирургическое вмешательство). Глобальный дефицит перфузии ( шоковый синдром, остановка кровообращения). Региональный перфузионный дефицит (сосудистая травма, тромбоэмболия). Наличие ишемизированныхнекротических тканей (инфаркт миокарда, панкреатит, ДВС-синдром). Микробная инвазия (иммунодефициты, хирургиятравма, экстрагоспитальное инфицирование, нозокомиальное инфицирование). Выброс эндотоксина (грам-отрицательный сепсис, кишечная транслокация). Абсцессы ( интраабдоминальные, интракраниальные).
Причины СВР Механическое повреждение тканей (ожоги, крашсиндром, хирургическое вмешательство). Глобальный дефицит перфузии ( шоковый синдром, остановка кровообращения). Региональный перфузионный дефицит (сосудистая травма, тромбоэмболия). Наличие ишемизированныхнекротических тканей (инфаркт миокарда, панкреатит, ДВС-синдром). Микробная инвазия (иммунодефициты, хирургиятравма, экстрагоспитальное инфицирование, нозокомиальное инфицирование). Выброс эндотоксина (грам-отрицательный сепсис, кишечная транслокация). Абсцессы ( интраабдоминальные, интракраниальные).
 Медиаторы СВР 1. Цитокины -хемокины, -колоний стимулирующий фактор, интерлейкины, интерфероны, фактор некроза опухоли, 2. Плазматические энзимные факторы комплемент, факторы свертывания, фибринолитические факторы, калликреинкинины, 3. Медиаторы липидного происхождения Метаболиты арахидоновой кислоты ( эйкозаноиды) -лейкотриены, -простогландины, -тромбоксаны, Фактор активирующий тромбоциты, 4. Токсические продукты кислородного обмена -перекиси, -гидроксид радикалы, -супероксид анионы, 5. Другие -эндотелин , -окись азота, -протеазы
Медиаторы СВР 1. Цитокины -хемокины, -колоний стимулирующий фактор, интерлейкины, интерфероны, фактор некроза опухоли, 2. Плазматические энзимные факторы комплемент, факторы свертывания, фибринолитические факторы, калликреинкинины, 3. Медиаторы липидного происхождения Метаболиты арахидоновой кислоты ( эйкозаноиды) -лейкотриены, -простогландины, -тромбоксаны, Фактор активирующий тромбоциты, 4. Токсические продукты кислородного обмена -перекиси, -гидроксид радикалы, -супероксид анионы, 5. Другие -эндотелин , -окись азота, -протеазы
 Фактор некроза опухоли Гипотензия Острое легочное повреждение Коагулопатия Анорексия Кахексия Гипертриглицеридемия Инсулинорезистентность Выброс острофазовых протеинов Активация глюконеогенеза Нейтропения
Фактор некроза опухоли Гипотензия Острое легочное повреждение Коагулопатия Анорексия Кахексия Гипертриглицеридемия Инсулинорезистентность Выброс острофазовых протеинов Активация глюконеогенеза Нейтропения
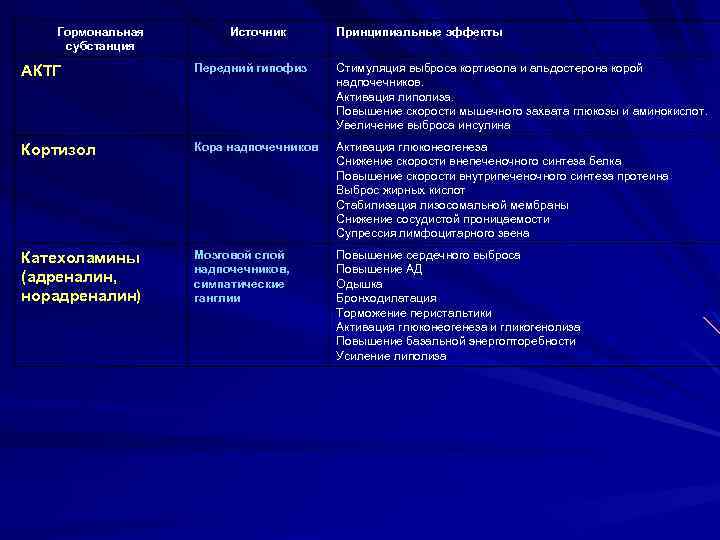 Гормональная субстанция Источник Принципиальные эффекты АКТГ Передний гипофиз Стимуляция выброса кортизола и альдостерона корой надпочечников. Активация липолиза. Повышение скорости мышечного захвата глюкозы и аминокислот. Увеличение выброса инсулина Кортизол Кора надпочечников Активация глюконеогенеза Снижение скорости внепеченочного синтеза белка Повышение скорости внутрипеченочного синтеза протеина Выброс жирных кислот Стабилизация лизосомальной мембраны Снижение сосудистой проницаемости Супрессия лимфоцитарного звена Катехоламины (адреналин, норадреналин) Мозговой слой надпочечников, симпатические ганглии Повышение сердечного выброса Повышение АД Одышка Бронходилатация Торможение перистальтики Активация глюконеогенеза и гликогенолиза Повышение базальной энергопторебности Усиление липолиза
Гормональная субстанция Источник Принципиальные эффекты АКТГ Передний гипофиз Стимуляция выброса кортизола и альдостерона корой надпочечников. Активация липолиза. Повышение скорости мышечного захвата глюкозы и аминокислот. Увеличение выброса инсулина Кортизол Кора надпочечников Активация глюконеогенеза Снижение скорости внепеченочного синтеза белка Повышение скорости внутрипеченочного синтеза протеина Выброс жирных кислот Стабилизация лизосомальной мембраны Снижение сосудистой проницаемости Супрессия лимфоцитарного звена Катехоламины (адреналин, норадреналин) Мозговой слой надпочечников, симпатические ганглии Повышение сердечного выброса Повышение АД Одышка Бронходилатация Торможение перистальтики Активация глюконеогенеза и гликогенолиза Повышение базальной энергопторебности Усиление липолиза
 Гормон роста Передний гипофиз Повышение скорости синтеза протеина Акивация выброса жирных кислот Снижение скорости потребления глюкозы Эндорфины Гипоталамус, передний гипофиз, поджелудочная железа, ЖКТ Повышение секреции АКТГ Анальгезия Уменьшение уровней кортизола в кровотоке Эйфория Глюкагон Альфа клетки поджелудочной железы Активное разрушение запасов гликогена в печени, сопровождающееся гипергликемией Активация глюконеогенеза Альдостерон Кора надпочечников Повышенная тубулярная реабсорбция натрия и воды Повышенная секреция калия и водорода АДГ Задний гипофиз Повышение реабсорбции воды Повышение концентрации вторичной мочи
Гормон роста Передний гипофиз Повышение скорости синтеза протеина Акивация выброса жирных кислот Снижение скорости потребления глюкозы Эндорфины Гипоталамус, передний гипофиз, поджелудочная железа, ЖКТ Повышение секреции АКТГ Анальгезия Уменьшение уровней кортизола в кровотоке Эйфория Глюкагон Альфа клетки поджелудочной железы Активное разрушение запасов гликогена в печени, сопровождающееся гипергликемией Активация глюконеогенеза Альдостерон Кора надпочечников Повышенная тубулярная реабсорбция натрия и воды Повышенная секреция калия и водорода АДГ Задний гипофиз Повышение реабсорбции воды Повышение концентрации вторичной мочи
 Оксид азота как эндотелиальный фактор расслабления был открыт в 1980 г. Р. Фешготтом и И. Завадски. При изучении релаксирующего эффекта ацетилхолина на артериальных гладких мышцах выявлялась некая эндотелиальная субстанция. Вещество синтезировалось из L-аргинина под действием фермента синтаза азота. Различают три ее изоформы, две из которых обнаружены в нервной ткани и в эндотелии; третья — во многих клетках иного типа (например, в почечных канальцах). Оксид азота тормозит работу сократительного аппарата сосудистых гладкомышечных элементов; при этом активируется фермент гуанилатциклаза и образуется вторичный (скорее, “третичный”) посредник — циклический 3’-5’гуанозинмонофосфат. NO препятствует адгезии циркулирующих тромбоцитов и лейкоцитов к эндотелию; эта функция сопряжена с простациклином, который препятствует агрегации и адгезии клеток
Оксид азота как эндотелиальный фактор расслабления был открыт в 1980 г. Р. Фешготтом и И. Завадски. При изучении релаксирующего эффекта ацетилхолина на артериальных гладких мышцах выявлялась некая эндотелиальная субстанция. Вещество синтезировалось из L-аргинина под действием фермента синтаза азота. Различают три ее изоформы, две из которых обнаружены в нервной ткани и в эндотелии; третья — во многих клетках иного типа (например, в почечных канальцах). Оксид азота тормозит работу сократительного аппарата сосудистых гладкомышечных элементов; при этом активируется фермент гуанилатциклаза и образуется вторичный (скорее, “третичный”) посредник — циклический 3’-5’гуанозинмонофосфат. NO препятствует адгезии циркулирующих тромбоцитов и лейкоцитов к эндотелию; эта функция сопряжена с простациклином, который препятствует агрегации и адгезии клеток
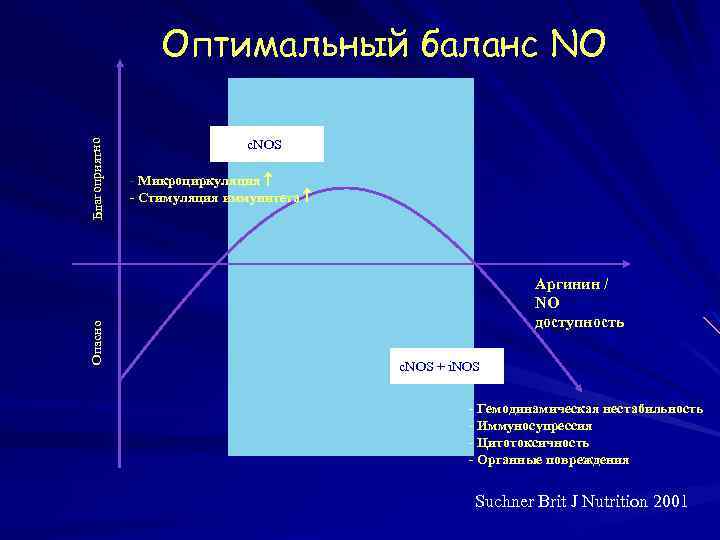 Опасно Благоприятно Oптимальный баланс NO c. NOS - Микроциркуляция - Стимуляция иммунитета Aргинин / NO доступность c. NOS + i. NOS - Гемодинамическая нестабильность - Иммуносупрессия - Цитотоксичность - Органные повреждения Suchner Brit J Nutrition 2001
Опасно Благоприятно Oптимальный баланс NO c. NOS - Микроциркуляция - Стимуляция иммунитета Aргинин / NO доступность c. NOS + i. NOS - Гемодинамическая нестабильность - Иммуносупрессия - Цитотоксичность - Органные повреждения Suchner Brit J Nutrition 2001
 Стадийность течения СВР Стадия 1. Локальная продукция медиаторов провоспалительной и антивоспалительной систем в ответ на травму инфекцию ишемию; Стадия 2. Выброс малого количества медиаторов ССВО в системный кровоток; Стадия 3. Генерализация воспалительной реакции ; Стадия 4. Развитие компенсаторной антивоспалительной реакции и вторичного иммунодефицита (“иммунного паралича”). Стадия 5. Финальная стадия полиорганного повреждения. Стадия «иммунного диссонанса»
Стадийность течения СВР Стадия 1. Локальная продукция медиаторов провоспалительной и антивоспалительной систем в ответ на травму инфекцию ишемию; Стадия 2. Выброс малого количества медиаторов ССВО в системный кровоток; Стадия 3. Генерализация воспалительной реакции ; Стадия 4. Развитие компенсаторной антивоспалительной реакции и вторичного иммунодефицита (“иммунного паралича”). Стадия 5. Финальная стадия полиорганного повреждения. Стадия «иммунного диссонанса»
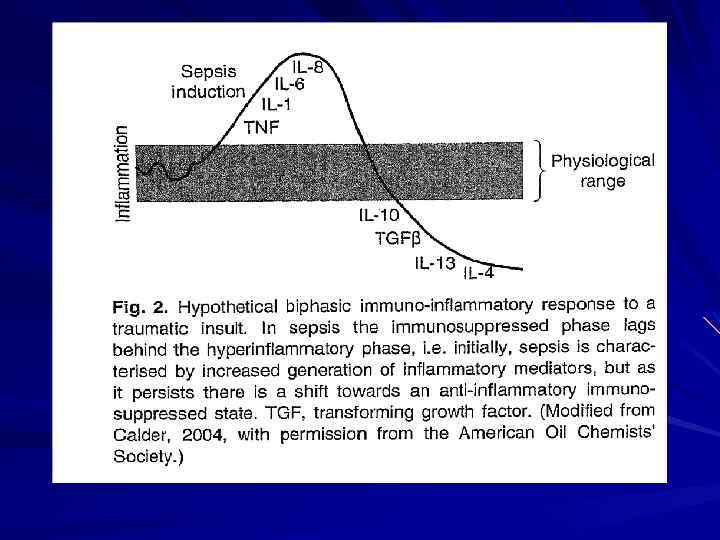
 Стадия 1. Локальная продукция медиаторов провоспалительной и антивоспалительной систем в ответ на травму инфекцию ишемию; Первичный ответ организма на повреждение любой этиологии заключается в выбросе провоспалительных медиаторов, которые позволяют ограничить очаг повреждения, разрушить пораженные ткани, внедрившиеся микроорганизмы. К ним относят –ФНО, ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-15, гамма интерферон и др. Компенсаторный выброс антивоспалительных субстанций (ИЛ 4, ИЛ-10, ИЛ-11, ИЛ-13 и др. ) призван ограничить возможное повреждающее действие провоспалительных медиаторов.
Стадия 1. Локальная продукция медиаторов провоспалительной и антивоспалительной систем в ответ на травму инфекцию ишемию; Первичный ответ организма на повреждение любой этиологии заключается в выбросе провоспалительных медиаторов, которые позволяют ограничить очаг повреждения, разрушить пораженные ткани, внедрившиеся микроорганизмы. К ним относят –ФНО, ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-15, гамма интерферон и др. Компенсаторный выброс антивоспалительных субстанций (ИЛ 4, ИЛ-10, ИЛ-11, ИЛ-13 и др. ) призван ограничить возможное повреждающее действие провоспалительных медиаторов.
 Стадия 2. Выброс малого количества медиаторов ССВО в системный кровоток; Даже малые количества медиаторов способны активизировать макрофаги, тромбоциты, продукцию гормона роста. Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами и их эндогенными антагонистами, такими как антагонисты интерлейкина -1, 10, 13, фактора некроза опухоли. За счет баланса между цитокинами , антагонистами медиаторных рецепторов и антителами в нормальных условиях создаются предпосылки для заживления ран, уничтожения патогенных микроорганизмов, поддержания гомеостаза. Первую и вторую стадии ССВО следует расценивать как нормальные физиологические механизмы регуляции взаимодействия человеческого организма с окружающей средой , позволяющие оптимально реагировать на разнообразные экзогенные и эндогенные повреждающие факторы и препятствовать развитию патологического процесса.
Стадия 2. Выброс малого количества медиаторов ССВО в системный кровоток; Даже малые количества медиаторов способны активизировать макрофаги, тромбоциты, продукцию гормона роста. Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами и их эндогенными антагонистами, такими как антагонисты интерлейкина -1, 10, 13, фактора некроза опухоли. За счет баланса между цитокинами , антагонистами медиаторных рецепторов и антителами в нормальных условиях создаются предпосылки для заживления ран, уничтожения патогенных микроорганизмов, поддержания гомеостаза. Первую и вторую стадии ССВО следует расценивать как нормальные физиологические механизмы регуляции взаимодействия человеческого организма с окружающей средой , позволяющие оптимально реагировать на разнообразные экзогенные и эндогенные повреждающие факторы и препятствовать развитию патологического процесса.
 Стадия 3. Генерализация воспалительной реакции ; В том случае, если регулирующие системы не способны поддерживать гомеостаз , деструктивные эффекты провоспалительных цитокинов и других медиаторов начинают доминировать над гуморальными и нейроэндокринными агентами противовоспалительной фазы , что приводит к нарушению проницаемости и функции эндотелия капилляров, агрегации тромбоцитов и блокаде системы микроциркуляции, активации коагуляционных систем и повреждению протеина С , выраженной вазодилатации, формированию отдаленных очагов воспаления, развитию моно- и полиорганной дисфункции
Стадия 3. Генерализация воспалительной реакции ; В том случае, если регулирующие системы не способны поддерживать гомеостаз , деструктивные эффекты провоспалительных цитокинов и других медиаторов начинают доминировать над гуморальными и нейроэндокринными агентами противовоспалительной фазы , что приводит к нарушению проницаемости и функции эндотелия капилляров, агрегации тромбоцитов и блокаде системы микроциркуляции, активации коагуляционных систем и повреждению протеина С , выраженной вазодилатации, формированию отдаленных очагов воспаления, развитию моно- и полиорганной дисфункции
 Стадия 4. Развитие компенсаторной антивоспалительной реакции и вторичного иммунодефицита (“иммунного паралича”). В нормальных условиях вслед за развитием системной воспалительной реакции происходит выброс в системный кровоток каскада антивоспалительных цитокинов. Наиболее активными являются : интерлейкин-4, интерлейкин-10, трансформированный фактор роста-бета. Эти иммуномодулирующие субстанции подавляют секрецию макрофагами медиаторов провоспалительной фазы. Избыточная, вследствие грубой дисрегуляции, продукция медаторов антивоспалительной фазы получила название “синдрома компенсаторного антивоспалительного ответа” (CARS-КАВСО). Основным признаком развития КАВСО является снижение (менее 30 %) активности поверхностного комплекса рецепторов моноцитов HLA-DR и существенное снижение способности моноцитов продуцировать ФНО и интерлейкин-6 в ответ на повреждение. Формирование данного синдрома приводит к развитию иммунодефицитного состояния (“иммунного паралича”), что сопровождается высокой вероятностью прогрессирования инфекционного процесса или возникновению тяжелой суперинфекции
Стадия 4. Развитие компенсаторной антивоспалительной реакции и вторичного иммунодефицита (“иммунного паралича”). В нормальных условиях вслед за развитием системной воспалительной реакции происходит выброс в системный кровоток каскада антивоспалительных цитокинов. Наиболее активными являются : интерлейкин-4, интерлейкин-10, трансформированный фактор роста-бета. Эти иммуномодулирующие субстанции подавляют секрецию макрофагами медиаторов провоспалительной фазы. Избыточная, вследствие грубой дисрегуляции, продукция медаторов антивоспалительной фазы получила название “синдрома компенсаторного антивоспалительного ответа” (CARS-КАВСО). Основным признаком развития КАВСО является снижение (менее 30 %) активности поверхностного комплекса рецепторов моноцитов HLA-DR и существенное снижение способности моноцитов продуцировать ФНО и интерлейкин-6 в ответ на повреждение. Формирование данного синдрома приводит к развитию иммунодефицитного состояния (“иммунного паралича”), что сопровождается высокой вероятностью прогрессирования инфекционного процесса или возникновению тяжелой суперинфекции
 Стадия 5. Финальная стадия полиорганного повреждения. Основной патофизиологической характеристикой данной фазы следует считать, так называемый, синдром «иммунного диссонанса» , характеризующийся абсолютным дисбалансом во всех звеньях иммунного ответа организма , существенно повышающем вероятность неблагоприятного исхода
Стадия 5. Финальная стадия полиорганного повреждения. Основной патофизиологической характеристикой данной фазы следует считать, так называемый, синдром «иммунного диссонанса» , характеризующийся абсолютным дисбалансом во всех звеньях иммунного ответа организма , существенно повышающем вероятность неблагоприятного исхода
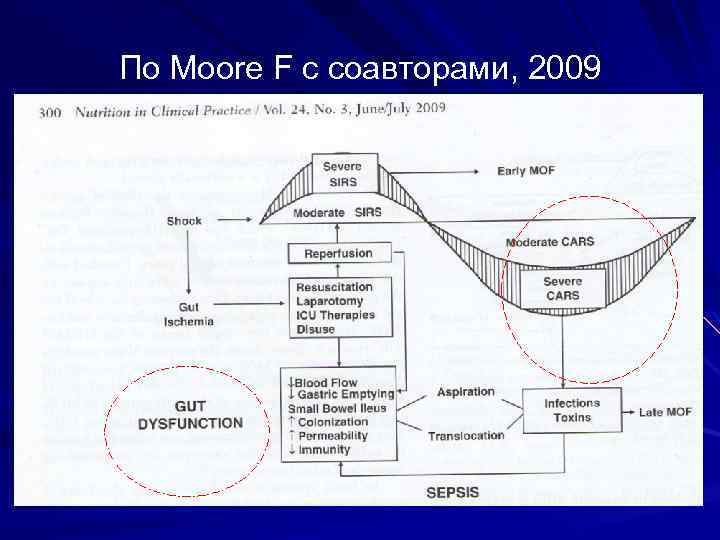 По Moore F c соавторами, 2009
По Moore F c соавторами, 2009
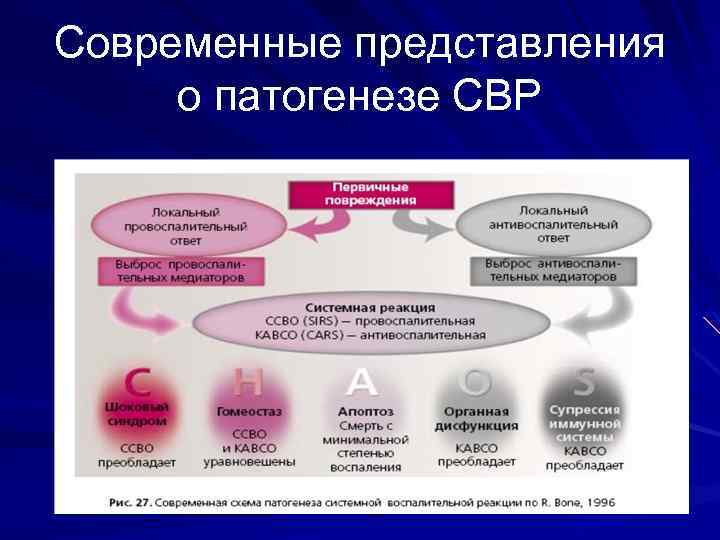 Современные представления о патогенезе СВР
Современные представления о патогенезе СВР

 Концепция системной антивоспалительной реакции (CARS) – закономерность или особый вариант течения сепсиса?
Концепция системной антивоспалительной реакции (CARS) – закономерность или особый вариант течения сепсиса?
 Какая стадия СВР?
Какая стадия СВР?
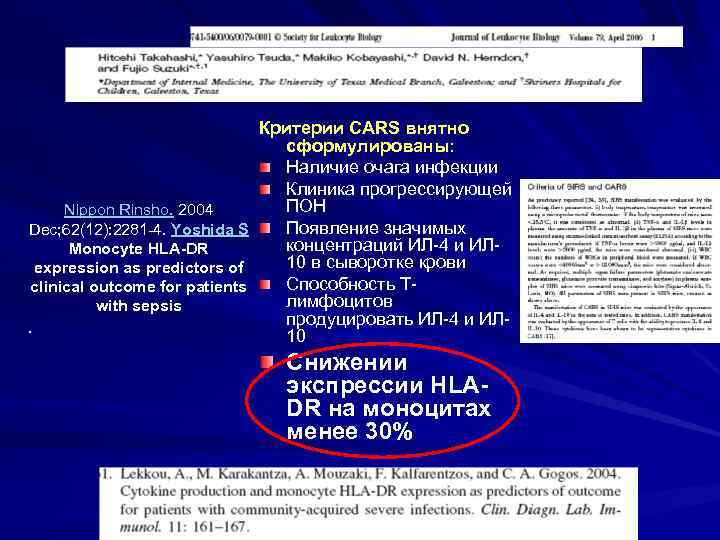 Критерии СARS внятно сформулированы: Наличие очага инфекции Клиника прогрессирующей ПОН Nippon Rinsho. 2004 Появление значимых Dec; 62(12): 2281 -4. Yoshida S концентраций ИЛ-4 и ИЛMonocyte HLA-DR 10 в сыворотке крови expression as predictors of Способность Тclinical outcome for patients лимфоцитов with sepsis продуцировать ИЛ-4 и ИЛ. 10 Снижении экспрессии HLADR на моноцитах менее 30%
Критерии СARS внятно сформулированы: Наличие очага инфекции Клиника прогрессирующей ПОН Nippon Rinsho. 2004 Появление значимых Dec; 62(12): 2281 -4. Yoshida S концентраций ИЛ-4 и ИЛMonocyte HLA-DR 10 в сыворотке крови expression as predictors of Способность Тclinical outcome for patients лимфоцитов with sepsis продуцировать ИЛ-4 и ИЛ. 10 Снижении экспрессии HLADR на моноцитах менее 30%
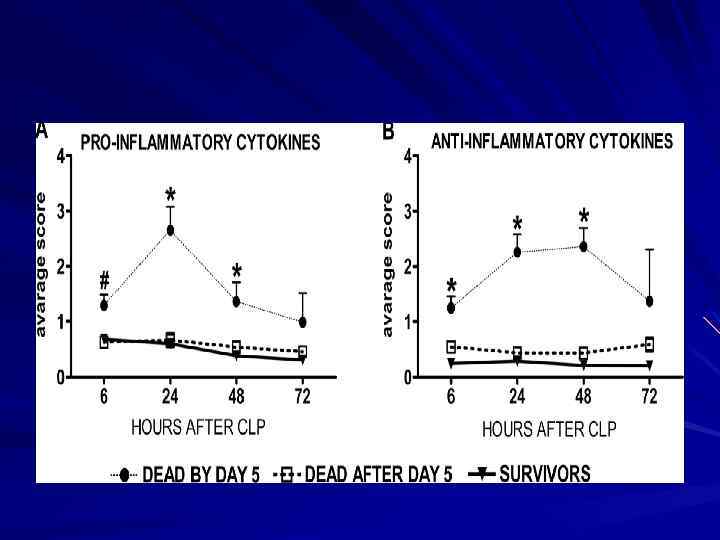
 Экспрессия HLA-DR на моноцитах Отражает способность лейкоцитов к секреции провоспалительных медиаторов Диагностика фазы СВР(гипервоспаление, иммуносупресия) Пороговый уровень 30% Сохранение экспрессии HLA-DR менее 30% в течение 5 дней сопровождается летальностью в 88%, при отсутствии – 12% Docke et al. , Nat Med 1997; 3: 678 -681
Экспрессия HLA-DR на моноцитах Отражает способность лейкоцитов к секреции провоспалительных медиаторов Диагностика фазы СВР(гипервоспаление, иммуносупресия) Пороговый уровень 30% Сохранение экспрессии HLA-DR менее 30% в течение 5 дней сопровождается летальностью в 88%, при отсутствии – 12% Docke et al. , Nat Med 1997; 3: 678 -681
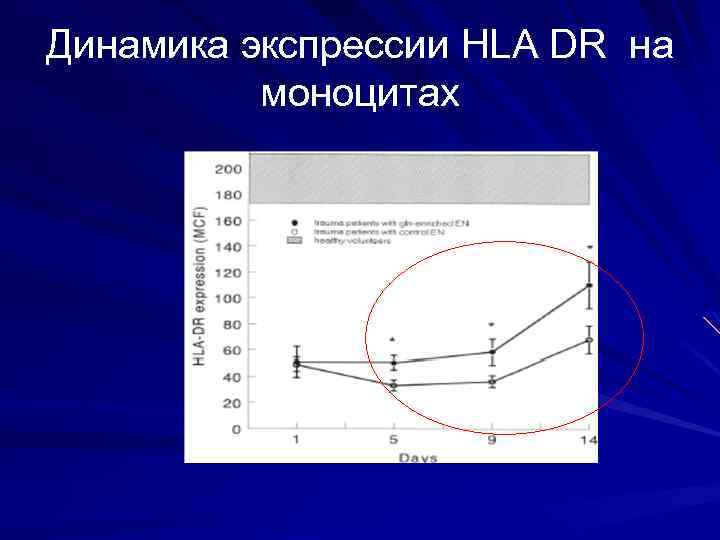 Динамика экспрессии HLA DR на моноцитах
Динамика экспрессии HLA DR на моноцитах
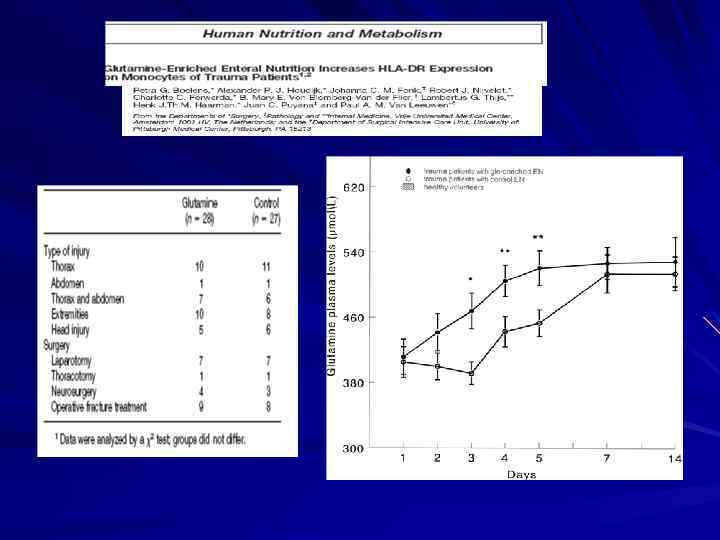
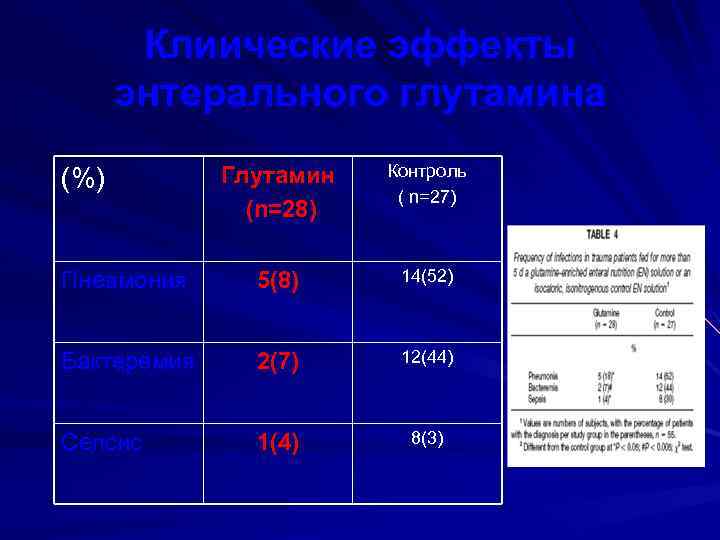 Клиические эффекты энтерального глутамина Глутамин (n=28) Контроль ( n=27) Пневмония 5(8) 14(52) Бактеремия 2(7) 12(44) Сепсис 1(4) 8(3) (%)
Клиические эффекты энтерального глутамина Глутамин (n=28) Контроль ( n=27) Пневмония 5(8) 14(52) Бактеремия 2(7) 12(44) Сепсис 1(4) 8(3) (%)
 Основной целью интенсивной терапии является предотвращение развития моно или полиорганной недостаточности иили лечение и адекватное протезирование поврежденной функции органов и систем
Основной целью интенсивной терапии является предотвращение развития моно или полиорганной недостаточности иили лечение и адекватное протезирование поврежденной функции органов и систем
 Синдром полиорганной недостаточности (ПОН) основную причину смерти больных в ОРИТ- следует рассматривать, как частный случай и наиболее тяжелую степень СВР- генерализованное воспаление, вызывающее множественные повреждения органных функций
Синдром полиорганной недостаточности (ПОН) основную причину смерти больных в ОРИТ- следует рассматривать, как частный случай и наиболее тяжелую степень СВР- генерализованное воспаление, вызывающее множественные повреждения органных функций
 Шоковый синдром, моно и полиорганная дисфункция- наиболее яркие клинические проявления критического состояния- классической постагрессивной реакции. Суммарные эффекты оказываемые медиаторами повреждения формируют системную воспалительную реакцию или синдром системного воспалительного ответа
Шоковый синдром, моно и полиорганная дисфункция- наиболее яркие клинические проявления критического состояния- классической постагрессивной реакции. Суммарные эффекты оказываемые медиаторами повреждения формируют системную воспалительную реакцию или синдром системного воспалительного ответа
 Патофизиологические составляющие SIRS Secor VH. Multiple organ dysfunction and failure. Mosby Year Book: Second edition, 1996. – 457 p. n Перераспределение ПЕРЕРАСПРЕДЕЛЕНИЕ ОЦК Дисбаланс транспортапотребления О 2 Метаболическая дисфункция
Патофизиологические составляющие SIRS Secor VH. Multiple organ dysfunction and failure. Mosby Year Book: Second edition, 1996. – 457 p. n Перераспределение ПЕРЕРАСПРЕДЕЛЕНИЕ ОЦК Дисбаланс транспортапотребления О 2 Метаболическая дисфункция
 Волемические расстройства и перераспределение ОЦК Рост капиллярной проницаемости Вазодилатация Селективная вазоконстрикция Потеря ауторегуляции Микрососудистый тромбоз Тканевой отек Клеточная аггрегация Дисфункция миокарда Жидкостный дисбаланс
Волемические расстройства и перераспределение ОЦК Рост капиллярной проницаемости Вазодилатация Селективная вазоконстрикция Потеря ауторегуляции Микрососудистый тромбоз Тканевой отек Клеточная аггрегация Дисфункция миокарда Жидкостный дисбаланс

 Факторы сокращения и расслабления сосудистой стенки КОНСТРИКТОРЫ ДИЛАТАТОРЫ Эндотелин Ангиотензин II Тромбоксан (TXA 2) Простагландин Н 2 Оксид азота Эндотелин Простациклин (PGI 2) Эндотелиновый фактор деполяризации (EDHF)
Факторы сокращения и расслабления сосудистой стенки КОНСТРИКТОРЫ ДИЛАТАТОРЫ Эндотелин Ангиотензин II Тромбоксан (TXA 2) Простагландин Н 2 Оксид азота Эндотелин Простациклин (PGI 2) Эндотелиновый фактор деполяризации (EDHF)
 Факторы гемостаза и антитромбоза ПРОТРОМБОГЕННЫЕ АНТИТРОМБОГЕННЫЕ Тромбоцитарный ростовой фактор (PDGF) Ингибитор активатора плазминогена Фактор Виллебранда (VIII фактор свертывания) Ангиотензин IV Эндотелин 1 Оксид азота Тканевой активатор плазминогена (TPA) Простациклин (PGI 2)
Факторы гемостаза и антитромбоза ПРОТРОМБОГЕННЫЕ АНТИТРОМБОГЕННЫЕ Тромбоцитарный ростовой фактор (PDGF) Ингибитор активатора плазминогена Фактор Виллебранда (VIII фактор свертывания) Ангиотензин IV Эндотелин 1 Оксид азота Тканевой активатор плазминогена (TPA) Простациклин (PGI 2)
 Факторы, влияющие на рост сосудов СТИМУЛЯТОРЫ ИНГИБИТОРЫ Эндотелин 1 Ангиотензин II Супероксидные радикалы Оксид азота Простациклин (PGI 2) С натриуретический пептид
Факторы, влияющие на рост сосудов СТИМУЛЯТОРЫ ИНГИБИТОРЫ Эндотелин 1 Ангиотензин II Супероксидные радикалы Оксид азота Простациклин (PGI 2) С натриуретический пептид
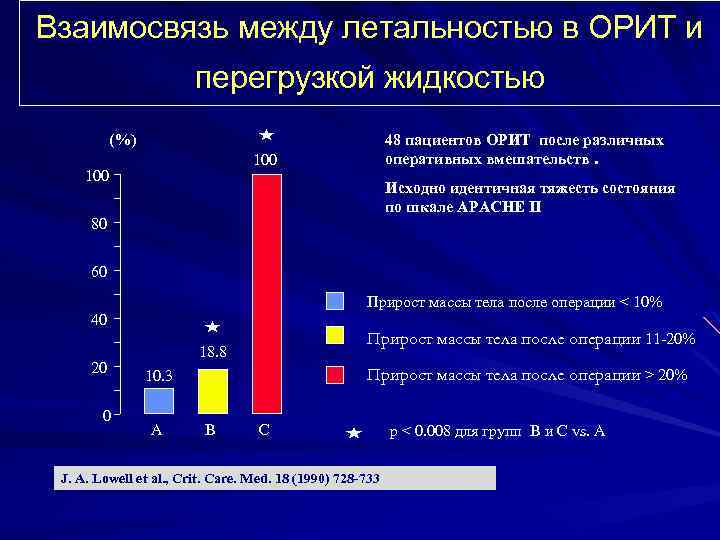 Взаимосвязь между летальностью в ОРИТ и перегрузкой жидкостью (%) 48 пациентов ОРИТ после различных оперативных вмешательств. 100 Исходно идентичная тяжесть состояния по шкале APACHE II 80 60 Прирост массы тела после операции < 10% 40 20 0 Прирост массы тела после операции 11 20% 18. 8 Прирост массы тела после операции > 20% 10. 3 A B C J. A. Lowell et al. , Crit. Care. Med. 18 (1990) 728 -733 p < 0. 008 для групп B и C vs. A
Взаимосвязь между летальностью в ОРИТ и перегрузкой жидкостью (%) 48 пациентов ОРИТ после различных оперативных вмешательств. 100 Исходно идентичная тяжесть состояния по шкале APACHE II 80 60 Прирост массы тела после операции < 10% 40 20 0 Прирост массы тела после операции 11 20% 18. 8 Прирост массы тела после операции > 20% 10. 3 A B C J. A. Lowell et al. , Crit. Care. Med. 18 (1990) 728 -733 p < 0. 008 для групп B и C vs. A
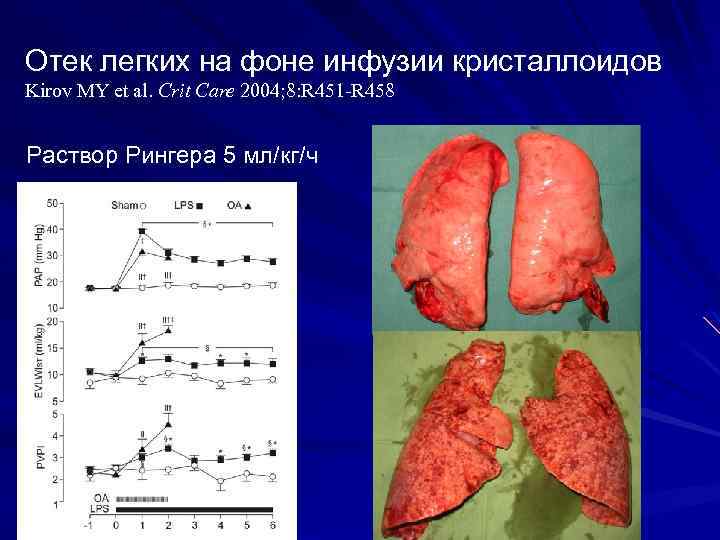 Отек легких на фоне инфузии кристаллоидов Kirov MY et al. Crit Care 2004; 8: R 451 R 458 Раствор Рингера 5 мл/кг/ч
Отек легких на фоне инфузии кристаллоидов Kirov MY et al. Crit Care 2004; 8: R 451 R 458 Раствор Рингера 5 мл/кг/ч
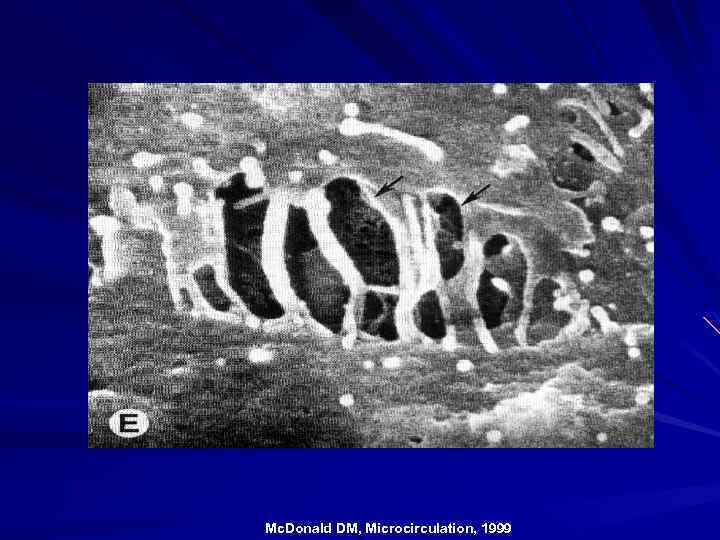 Mc. Donald DM, Microcirculation, 1999
Mc. Donald DM, Microcirculation, 1999
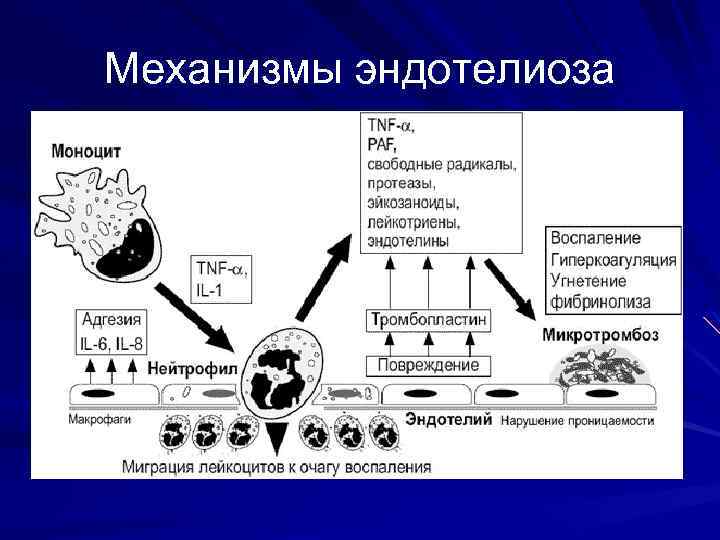 Механизмы эндотелиоза
Механизмы эндотелиоза
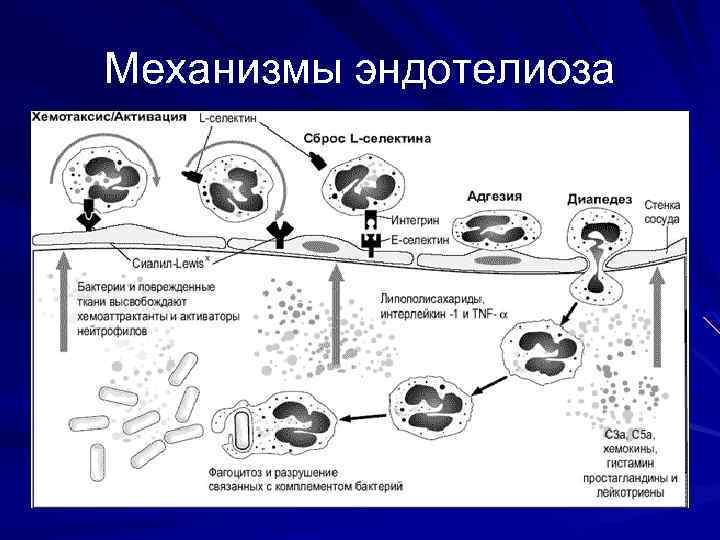 Механизмы эндотелиоза
Механизмы эндотелиоза
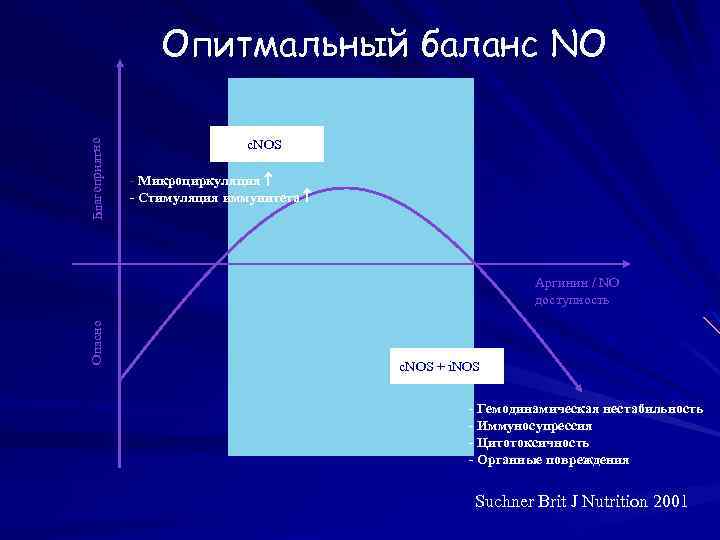 Благоприятно Oпитмальный баланс NO c. NOS - Микроциркуляция - Стимуляция иммунитета Опасно Aргинин / NO доступность c. NOS + i. NOS - Гемодинамическая нестабильность - Иммуносупрессия - Цитотоксичность - Органные повреждения Suchner Brit J Nutrition 2001
Благоприятно Oпитмальный баланс NO c. NOS - Микроциркуляция - Стимуляция иммунитета Опасно Aргинин / NO доступность c. NOS + i. NOS - Гемодинамическая нестабильность - Иммуносупрессия - Цитотоксичность - Органные повреждения Suchner Brit J Nutrition 2001
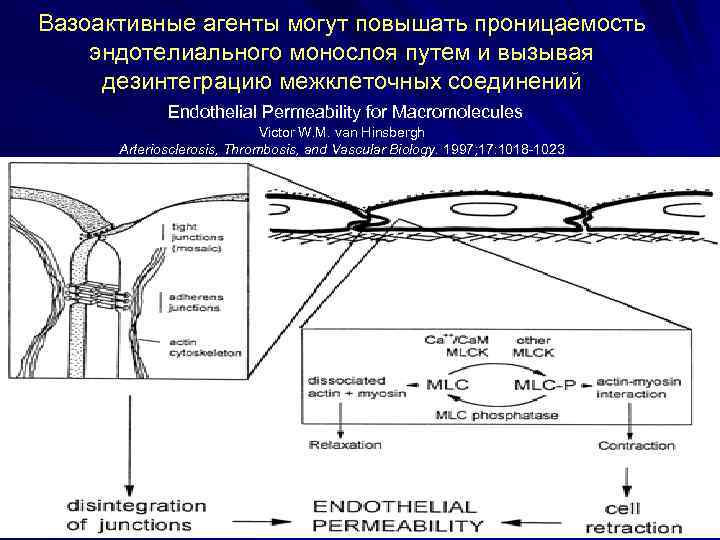 Вазоактивные агенты могут повышать проницаемость эндотелиального монослоя путем и вызывая дезинтеграцию межклеточных соединений Endothelial Permeability for Macromolecules Victor W. M. van Hinsbergh Arteriosclerosis, Thrombosis, and Vascular Biology. 1997; 17: 1018 -1023
Вазоактивные агенты могут повышать проницаемость эндотелиального монослоя путем и вызывая дезинтеграцию межклеточных соединений Endothelial Permeability for Macromolecules Victor W. M. van Hinsbergh Arteriosclerosis, Thrombosis, and Vascular Biology. 1997; 17: 1018 -1023
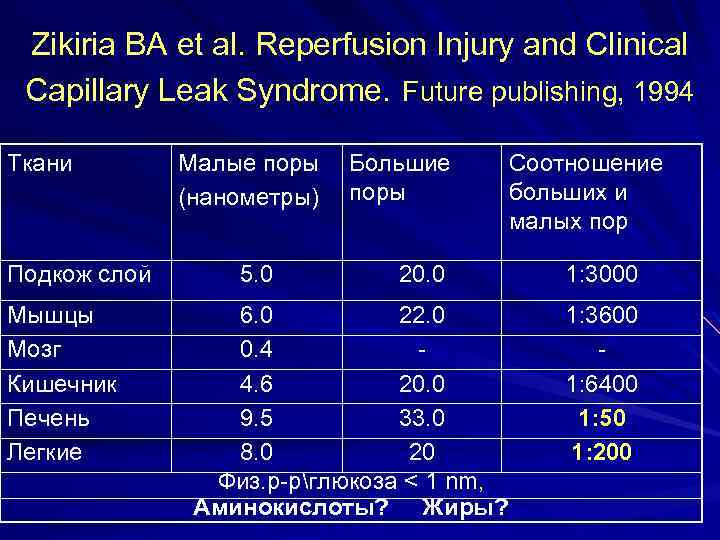 Zikiria BA et al. Reperfusion Injury and Clinical Capillary Leak Syndrome. Future publishing, 1994 Ткани Подкож слой Мышцы Мозг Кишечник Печень Легкие Малые поры (нанометры) 5. 0 Большие поры Соотношение больших и малых пор 20. 0 6. 0 22. 0 0. 4 4. 6 20. 0 9. 5 33. 0 8. 0 20 Физ. р-рглюкоза < 1 nm, Аминокислоты? Жиры? 1: 3000 1: 3600 1: 6400 1: 50 1: 200
Zikiria BA et al. Reperfusion Injury and Clinical Capillary Leak Syndrome. Future publishing, 1994 Ткани Подкож слой Мышцы Мозг Кишечник Печень Легкие Малые поры (нанометры) 5. 0 Большие поры Соотношение больших и малых пор 20. 0 6. 0 22. 0 0. 4 4. 6 20. 0 9. 5 33. 0 8. 0 20 Физ. р-рглюкоза < 1 nm, Аминокислоты? Жиры? 1: 3000 1: 3600 1: 6400 1: 50 1: 200
 Клиническая диагностика синдрома «капиллярной утечки» ? R. Webb. Intravenous Fluid Therapy. Aesculap Academy, 2003. Альбумин/креатинин мочи ( норма <2. 3 mg/mmol) Микроальбумин мочи – менее 20 мгл Тест с коллоидом и pa. O 2Fi. O 2 ? ? ? Тест с ЦВД (инвазивным) ? ? ? Гемодинамический мониторинг Picco PLUS: – ELWI-индекс внесосудистой воды в легких – PVPI- индекс легочной сосудистой проницаемости
Клиническая диагностика синдрома «капиллярной утечки» ? R. Webb. Intravenous Fluid Therapy. Aesculap Academy, 2003. Альбумин/креатинин мочи ( норма <2. 3 mg/mmol) Микроальбумин мочи – менее 20 мгл Тест с коллоидом и pa. O 2Fi. O 2 ? ? ? Тест с ЦВД (инвазивным) ? ? ? Гемодинамический мониторинг Picco PLUS: – ELWI-индекс внесосудистой воды в легких – PVPI- индекс легочной сосудистой проницаемости
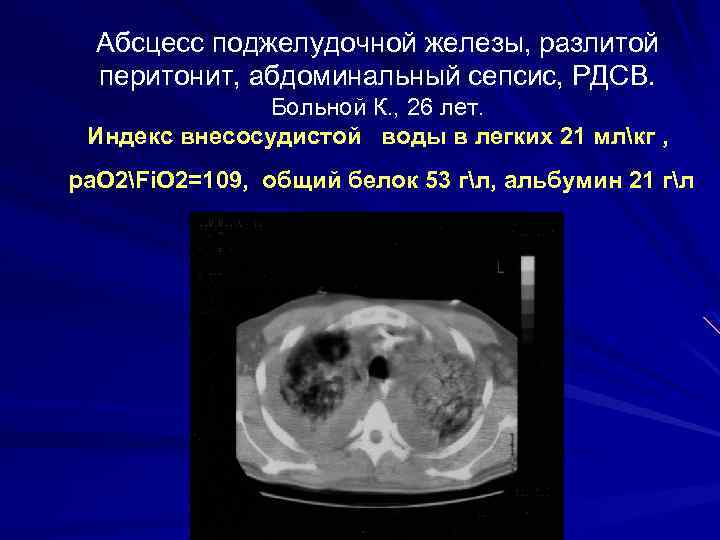 Абсцесс поджелудочной железы, разлитой перитонит, абдоминальный сепсис, РДСВ. Больной К. , 26 лет. Индекс внесосудистой воды в легких 21 млкг , pa. O 2Fi. O 2=109, общий белок 53 гл, альбумин 21 гл
Абсцесс поджелудочной железы, разлитой перитонит, абдоминальный сепсис, РДСВ. Больной К. , 26 лет. Индекс внесосудистой воды в легких 21 млкг , pa. O 2Fi. O 2=109, общий белок 53 гл, альбумин 21 гл
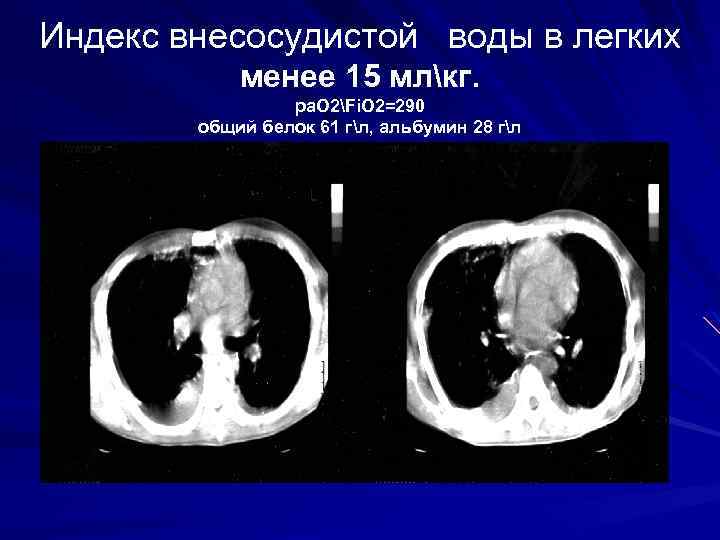 Индекс внесосудистой воды в легких менее 15 млкг. pa. O 2Fi. O 2=290 общий белок 61 гл, альбумин 28 гл
Индекс внесосудистой воды в легких менее 15 млкг. pa. O 2Fi. O 2=290 общий белок 61 гл, альбумин 28 гл
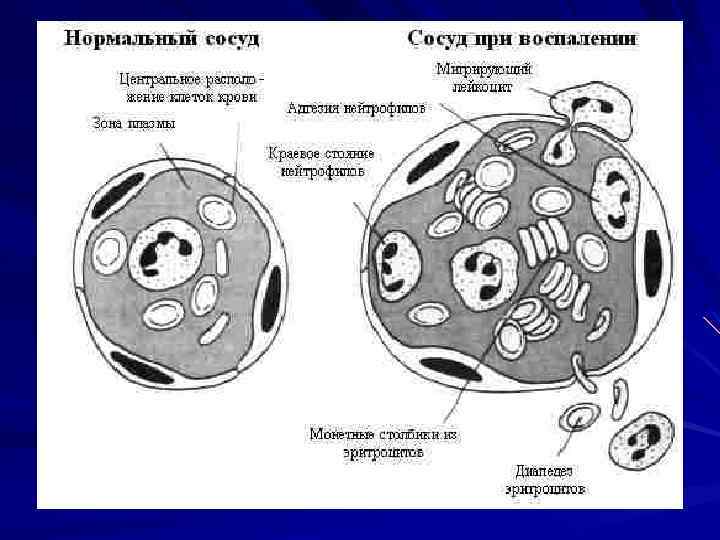
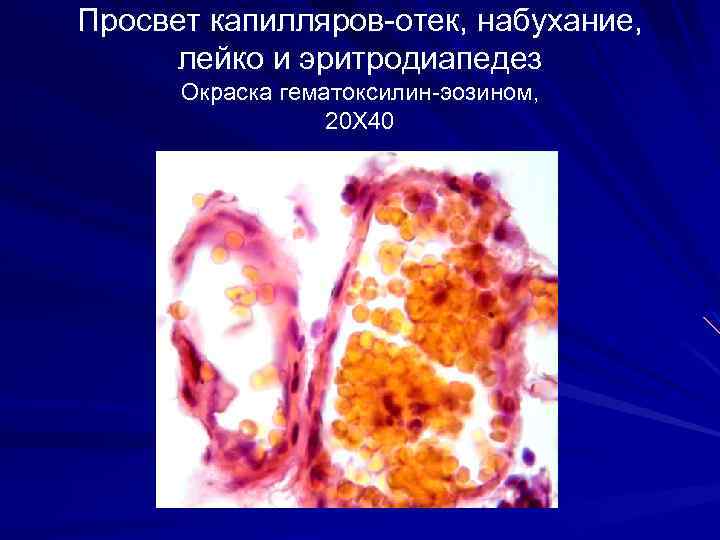 Просвет капилляров-отек, набухание, лейко и эритродиапедез Окраска гематоксилин-эозином, 20 Х 40
Просвет капилляров-отек, набухание, лейко и эритродиапедез Окраска гематоксилин-эозином, 20 Х 40
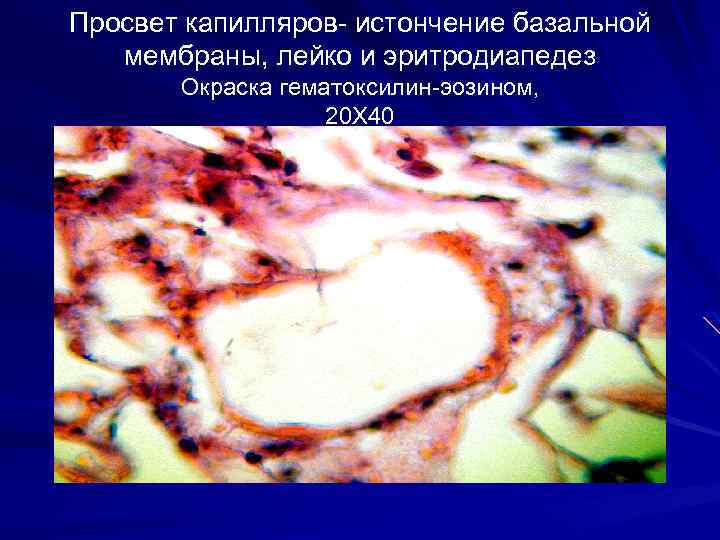 Просвет капилляров- истончение базальной мембраны, лейко и эритродиапедез Окраска гематоксилин-эозином, 20 Х 40
Просвет капилляров- истончение базальной мембраны, лейко и эритродиапедез Окраска гематоксилин-эозином, 20 Х 40
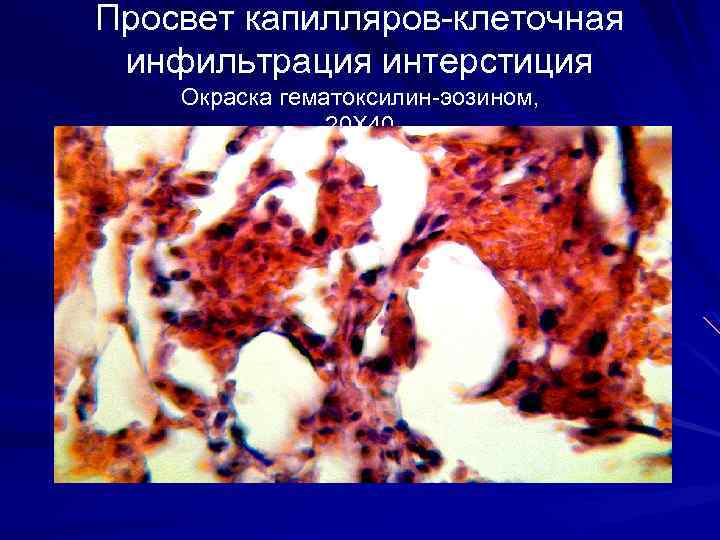 Просвет капилляров-клеточная инфильтрация интерстиция Окраска гематоксилин-эозином, 20 Х 40
Просвет капилляров-клеточная инфильтрация интерстиция Окраска гематоксилин-эозином, 20 Х 40
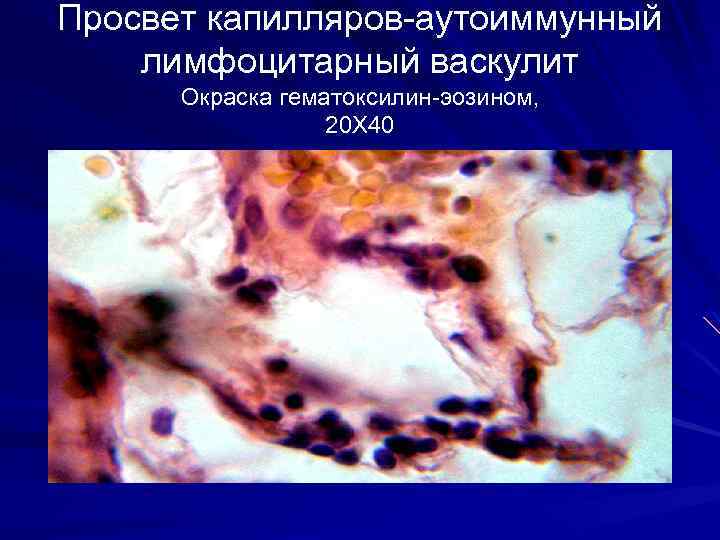 Просвет капилляров-аутоиммунный лимфоцитарный васкулит Окраска гематоксилин-эозином, 20 Х 40
Просвет капилляров-аутоиммунный лимфоцитарный васкулит Окраска гематоксилин-эозином, 20 Х 40
 Увеличение перехода жидкости из микроциркуляторного русла в ткани из-за увеличения сосудистой проницаемости называется экссудацией
Увеличение перехода жидкости из микроциркуляторного русла в ткани из-за увеличения сосудистой проницаемости называется экссудацией
 Трансудация - это процесс увеличенного перехода жидкости в ткани через сосуды с нормальной проницаемостью Сила, под влиянием которой происходит переход жидкости из кровотока в ткани, обусловлена увеличением гидростатического давления или уменьшением осмотического давления коллоидов плазмы.
Трансудация - это процесс увеличенного перехода жидкости в ткани через сосуды с нормальной проницаемостью Сила, под влиянием которой происходит переход жидкости из кровотока в ткани, обусловлена увеличением гидростатического давления или уменьшением осмотического давления коллоидов плазмы.
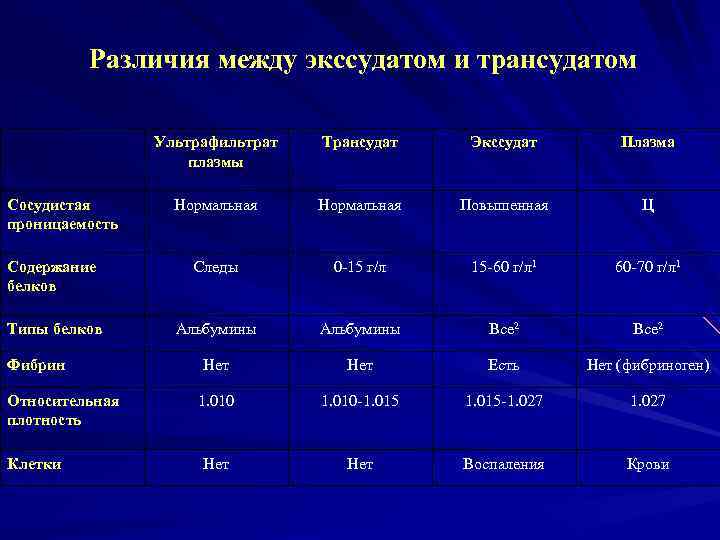 Различия между экссудатом и трансудатом Ультрафильтрат плазмы Трансудат Экссудат Плазма Нормальная Повышенная Ц Содержание белков Следы 0 15 г/л 15 60 г/л 1 60 70 г/л 1 Типы белков Альбумины Все 2 Нет Есть Нет (фибриноген) 1. 010 1. 015 1. 027 Нет Воспаления Крови Сосудистая проницаемость Фибрин Относительная плотность Клетки
Различия между экссудатом и трансудатом Ультрафильтрат плазмы Трансудат Экссудат Плазма Нормальная Повышенная Ц Содержание белков Следы 0 15 г/л 15 60 г/л 1 60 70 г/л 1 Типы белков Альбумины Все 2 Нет Есть Нет (фибриноген) 1. 010 1. 015 1. 027 Нет Воспаления Крови Сосудистая проницаемость Фибрин Относительная плотность Клетки
 Дисбаланс в системе кислородного бюджета Нарушение вентиляционно-перфузионных взаимоотношений Шунт Секвестрация волемического обьема Микроциркуляторные расстройства Нарушения экстракции кислорода Повышенное потребление кислорода вследствие: -Боли -Лихорадки -Тахикардии -Повышенной работы дыхания
Дисбаланс в системе кислородного бюджета Нарушение вентиляционно-перфузионных взаимоотношений Шунт Секвестрация волемического обьема Микроциркуляторные расстройства Нарушения экстракции кислорода Повышенное потребление кислорода вследствие: -Боли -Лихорадки -Тахикардии -Повышенной работы дыхания
 Метаболический дисбаланс Гиперметаболизм Неадекватная утилизация субстратов Гиперкатаболизм Печеночная дисфункция Нарушения межклеточного обмена Толерантность к эндогенным нутриентам
Метаболический дисбаланс Гиперметаболизм Неадекватная утилизация субстратов Гиперкатаболизм Печеночная дисфункция Нарушения межклеточного обмена Толерантность к эндогенным нутриентам
 Клинико-лабораторные последствия ССВО • Скорость обменных процессов • Потребление кислорода • Окисление глюкозы • Распад мышечного и висцерального пула белка • Синтезе белков острой фазы • Кетогенез • Липолиз
Клинико-лабораторные последствия ССВО • Скорость обменных процессов • Потребление кислорода • Окисление глюкозы • Распад мышечного и висцерального пула белка • Синтезе белков острой фазы • Кетогенез • Липолиз
 Обмен белка при СВР и голодании
Обмен белка при СВР и голодании
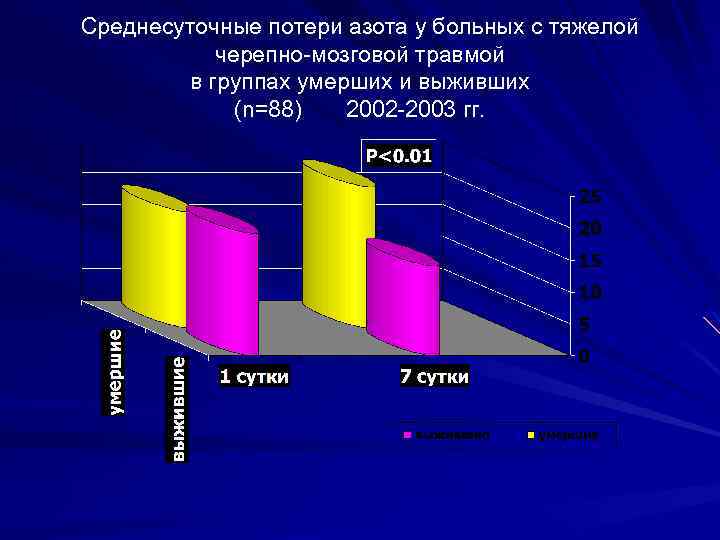 Среднесуточные потери азота у больных с тяжелой черепно-мозговой травмой в группах умерших и выживших (n=88) 2002 -2003 гг.
Среднесуточные потери азота у больных с тяжелой черепно-мозговой травмой в группах умерших и выживших (n=88) 2002 -2003 гг.
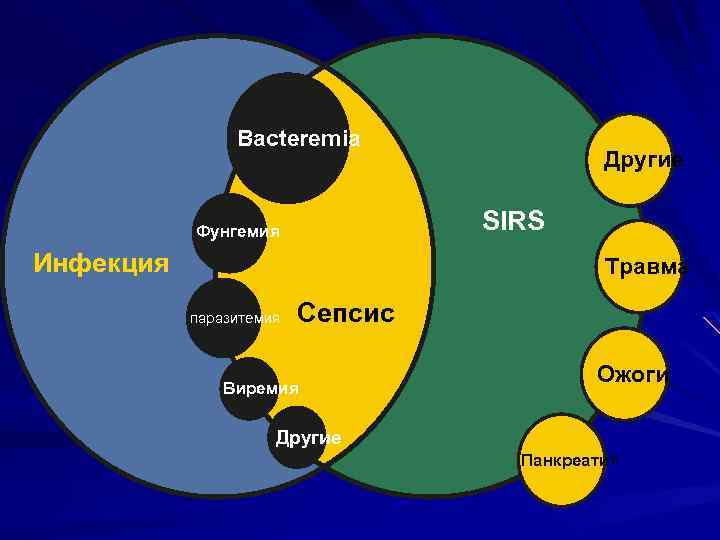 Bacteremia Другие SIRS Фунгемия Инфекция Травма паразитемия Сепсис Виремия Ожоги Другие Панкреатит
Bacteremia Другие SIRS Фунгемия Инфекция Травма паразитемия Сепсис Виремия Ожоги Другие Панкреатит
 Синдром полиорганной недостаточности (ПОН) – основную причину смерти больных в ОРИТ- следует рассматривать, как частный случай и наиболее тяжелую степень ССВО- генерализованное воспаление, вызывающее множественные повреждения органных функций
Синдром полиорганной недостаточности (ПОН) – основную причину смерти больных в ОРИТ- следует рассматривать, как частный случай и наиболее тяжелую степень ССВО- генерализованное воспаление, вызывающее множественные повреждения органных функций
 Основные задачи проведении интенсивной терапии в хирургическом ОРИТ Наиболее распространенными в Европе и США являются шкалы АРАСНЕ-II и III, SAPS, LOD. В последние 5 -7 лет широко используется шкала SOFA, удобная для оценки органной дисфункции при ССВО и ПОН септического генеза. Существуют и применяются также специальные шкалы, адаптированные для отдельных нозологических форм. Шкала Рэнсона представляет собой специфическую оценочную систему для определения тяжести панкреатита по некоторым выбранным параметрам (сывороточный кальций, мочевина мочи, падение гематокрита, дефицит оснований, артериальный р. О 2 и тканевая секвестрация) в первые 48 часов развития процесса. Шкалы абсолютно необходимы для сравнения разных проблемных пациентов, которые лечатся в центрах с различной хирургической стратегией.
Основные задачи проведении интенсивной терапии в хирургическом ОРИТ Наиболее распространенными в Европе и США являются шкалы АРАСНЕ-II и III, SAPS, LOD. В последние 5 -7 лет широко используется шкала SOFA, удобная для оценки органной дисфункции при ССВО и ПОН септического генеза. Существуют и применяются также специальные шкалы, адаптированные для отдельных нозологических форм. Шкала Рэнсона представляет собой специфическую оценочную систему для определения тяжести панкреатита по некоторым выбранным параметрам (сывороточный кальций, мочевина мочи, падение гематокрита, дефицит оснований, артериальный р. О 2 и тканевая секвестрация) в первые 48 часов развития процесса. Шкалы абсолютно необходимы для сравнения разных проблемных пациентов, которые лечатся в центрах с различной хирургической стратегией.
 Полиорганная недостаточность «Полиорганная недостаточность это универсальное поражение всех органов и тканей агрессивными медиаторами критического состояния с временным преобладанием симптомов той или иной недостаточности легочной, сердечной, почечной и т. д. » . А. П. Зильбер, 1995
Полиорганная недостаточность «Полиорганная недостаточность это универсальное поражение всех органов и тканей агрессивными медиаторами критического состояния с временным преобладанием симптомов той или иной недостаточности легочной, сердечной, почечной и т. д. » . А. П. Зильбер, 1995
 Как оценить степень тяжести ПОН? Прогностические шкалы не могут быть рекомендованы для оценки конкретного больного и не могут быть рутинной основой для принятия решения в клинической практике. Нужна объективная интегральная и количественная оценка тяжести состояния. По количеству вовлеченных в патологический процесс систем.
Как оценить степень тяжести ПОН? Прогностические шкалы не могут быть рекомендованы для оценки конкретного больного и не могут быть рутинной основой для принятия решения в клинической практике. Нужна объективная интегральная и количественная оценка тяжести состояния. По количеству вовлеченных в патологический процесс систем.
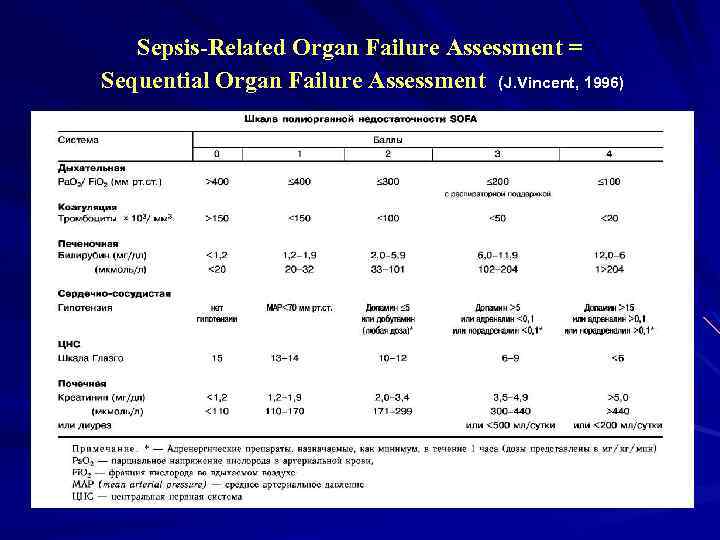 Sepsis-Related Organ Failure Assessment = Sequential Organ Failure Assessment (J. Vincent, 1996)
Sepsis-Related Organ Failure Assessment = Sequential Organ Failure Assessment (J. Vincent, 1996)
 Шкала SOFA Задача – описание органной дисфункции/недостаточности Может быть использоваться в оценке эволюции органной дисфункции в течение определенного временного отрезка у постели больного. Вычисляется на основании оценки дисфункции шести органных систем от 0 до 4 баллов соответственно степени дисфункции/недостаточности системы. Несмотря на то, что первичной задачей шкалы SOFA не являлось предсказывание летальности, существует тесная взаимосвязь между органной недостаточностью и летальностью. В недавно проведенном исследовании было показано, что максимальное число баллов по шкале SOFA имеет очень хорошую корреляцию с летальностью в ОРИТ (от 3, 2% при отсутствии органной недостаточности до 91, 3% при недостаточности шести органных систем).
Шкала SOFA Задача – описание органной дисфункции/недостаточности Может быть использоваться в оценке эволюции органной дисфункции в течение определенного временного отрезка у постели больного. Вычисляется на основании оценки дисфункции шести органных систем от 0 до 4 баллов соответственно степени дисфункции/недостаточности системы. Несмотря на то, что первичной задачей шкалы SOFA не являлось предсказывание летальности, существует тесная взаимосвязь между органной недостаточностью и летальностью. В недавно проведенном исследовании было показано, что максимальное число баллов по шкале SOFA имеет очень хорошую корреляцию с летальностью в ОРИТ (от 3, 2% при отсутствии органной недостаточности до 91, 3% при недостаточности шести органных систем).
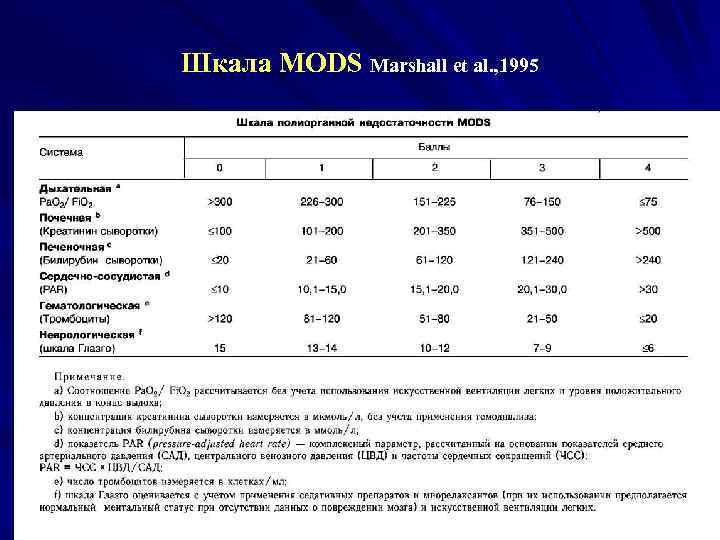 Шкала MODS Marshall et al. , 1995
Шкала MODS Marshall et al. , 1995
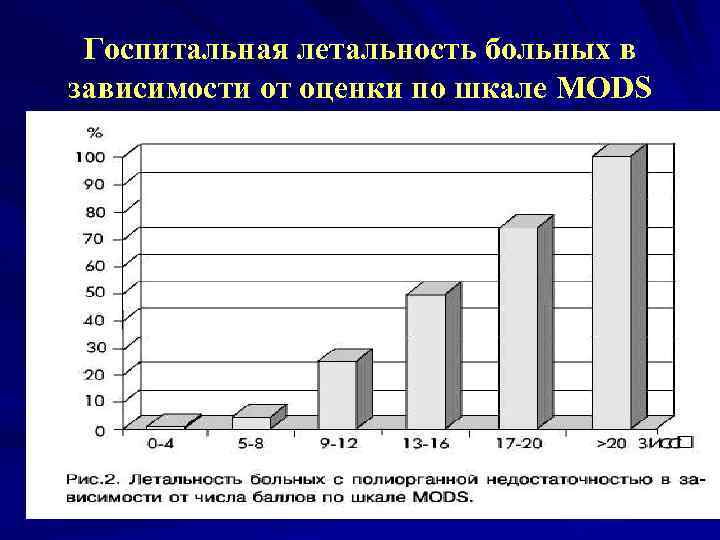 Госпитальная летальность больных в зависимости от оценки по шкале MODS
Госпитальная летальность больных в зависимости от оценки по шкале MODS
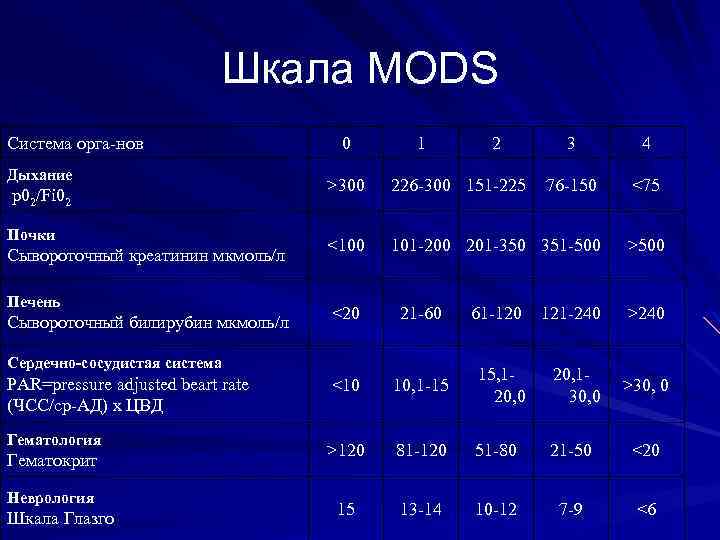 Шкала MODS Система орга нов Дыхание р02/Fi 02 Почки Сывороточный креатинин мкмоль/л Печень Сывороточный билирубин мкмоль/л 0 1 Гематология Гематокрит Неврология Шкала Глазго 3 4 >300 226 300 151 225 76 150 <75 <100 101 200 201 350 351 500 >500 <20 21 60 61 120 121 240 >240 <10 10, 1 15 15, 1 20, 0 20, 1 30, 0 >120 81 120 51 80 21 50 <20 15 13 14 10 12 7 9 <6 Сердечно-сосудистая система PAR=pressure adjusted beart rate (ЧСС/ср АД) x ЦВД 2
Шкала MODS Система орга нов Дыхание р02/Fi 02 Почки Сывороточный креатинин мкмоль/л Печень Сывороточный билирубин мкмоль/л 0 1 Гематология Гематокрит Неврология Шкала Глазго 3 4 >300 226 300 151 225 76 150 <75 <100 101 200 201 350 351 500 >500 <20 21 60 61 120 121 240 >240 <10 10, 1 15 15, 1 20, 0 20, 1 30, 0 >120 81 120 51 80 21 50 <20 15 13 14 10 12 7 9 <6 Сердечно-сосудистая система PAR=pressure adjusted beart rate (ЧСС/ср АД) x ЦВД 2
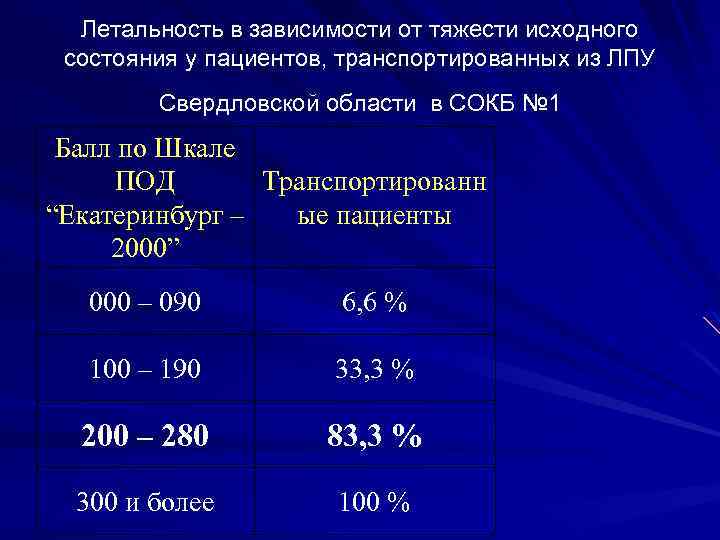 Летальность в зависимости от тяжести исходного состояния у пациентов, транспортированных из ЛПУ Свердловской области в CОКБ № 1 Балл по Шкале ПОД Транспортированн “Екатеринбург – ые пациенты 2000” 000 – 090 6, 6 % 100 – 190 33, 3 % 200 – 280 83, 3 % 300 и более 100 %
Летальность в зависимости от тяжести исходного состояния у пациентов, транспортированных из ЛПУ Свердловской области в CОКБ № 1 Балл по Шкале ПОД Транспортированн “Екатеринбург – ые пациенты 2000” 000 – 090 6, 6 % 100 – 190 33, 3 % 200 – 280 83, 3 % 300 и более 100 %
 Проведение мониторинга органных дисфункций Сразу после поступления пациента в отделение интенсивной терапии начинается определение степени повреждения органных функций и грубых расстройств водноэлектролитного, кислотно-щелочного, белково-энергетического обмена. Качественное проведение хирургического вмешательства перед поступлением в ИТ часто влияет на дальнейший исход.
Проведение мониторинга органных дисфункций Сразу после поступления пациента в отделение интенсивной терапии начинается определение степени повреждения органных функций и грубых расстройств водноэлектролитного, кислотно-щелочного, белково-энергетического обмена. Качественное проведение хирургического вмешательства перед поступлением в ИТ часто влияет на дальнейший исход.
 Перечень реанимационных синдромов 1. Острая сердечно – сосудистая недостаточность 1. 1 Кардиогенный шок 1. 2 Некардиогенный шок 2. Острая дыхательная недостаточность 3. Инфекционно - воспалительный синдром 4. Острая почечная недостаточность 5. Острая печеночная недостаточность 6. Острая церебральная недостаточность 7. Послеоперационный синдром
Перечень реанимационных синдромов 1. Острая сердечно – сосудистая недостаточность 1. 1 Кардиогенный шок 1. 2 Некардиогенный шок 2. Острая дыхательная недостаточность 3. Инфекционно - воспалительный синдром 4. Острая почечная недостаточность 5. Острая печеночная недостаточность 6. Острая церебральная недостаточность 7. Послеоперационный синдром
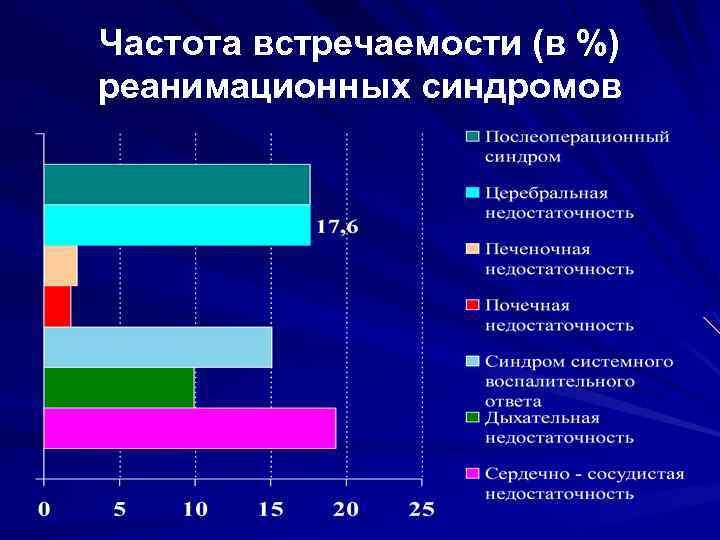 Частота встречаемости (в %) реанимационных синдромов
Частота встречаемости (в %) реанимационных синдромов
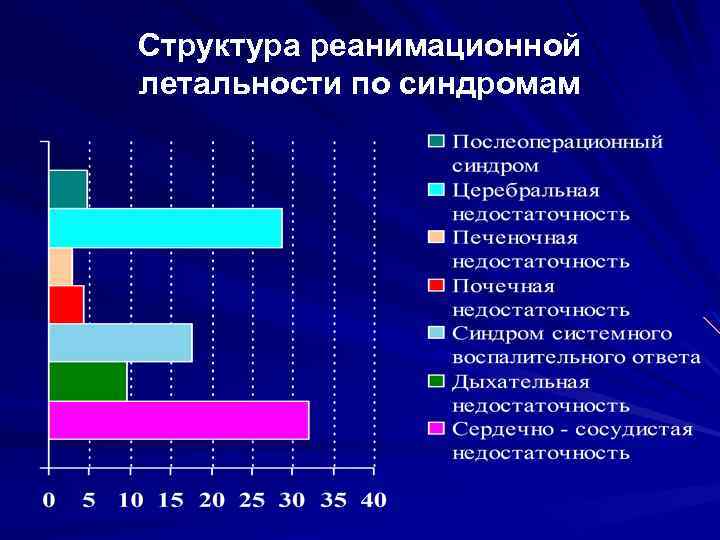 Структура реанимационной летальности по синдромам
Структура реанимационной летальности по синдромам

 Сердечно-сосудистая недостаточность – инфузионная терапия и инотропная поддержка Две основные цели циркуляторной поддержки: Поддерживать нормальный гемодинамический статус и обеспечивать необходимую доставку кислорода. Хотя до настоящего времени точно не определено, каким должен быть кислородный транспорт — нормальным или супранормальным, большинство интенсивистов пытаются достичь супранормальных величин.
Сердечно-сосудистая недостаточность – инфузионная терапия и инотропная поддержка Две основные цели циркуляторной поддержки: Поддерживать нормальный гемодинамический статус и обеспечивать необходимую доставку кислорода. Хотя до настоящего времени точно не определено, каким должен быть кислородный транспорт — нормальным или супранормальным, большинство интенсивистов пытаются достичь супранормальных величин.

 ЧСС <120, СИ>4, 5, САД >70 мм. рт. ст. , среднее давление в легочной артерии < 20 мм. рт. ст. , ДЗКЛА 12 -16 мм. рт. ст. , транспорт кислорода >600 млминм 2, потребление кислорода более 170 млминм 2 и сатурация смешанной венозной крови > 70 %.
ЧСС <120, СИ>4, 5, САД >70 мм. рт. ст. , среднее давление в легочной артерии < 20 мм. рт. ст. , ДЗКЛА 12 -16 мм. рт. ст. , транспорт кислорода >600 млминм 2, потребление кислорода более 170 млминм 2 и сатурация смешанной венозной крови > 70 %.
 Дыхательная дисфункция и респираторная поддержка Дыхательная дисфункция наиболее часто проявляется в виде развившегося респираторного дистресс-синдрома. Наличие дыхательной дисфункции можно определять при наличие тахипноэ больше 20 в минуту, снижение артериальной сатурации меньше 90% и р. О 2 арт. меньше 50 мм. рт. ст. pa. O 2Fi. O 2<300 и pa. O 2Fi. O 2<200
Дыхательная дисфункция и респираторная поддержка Дыхательная дисфункция наиболее часто проявляется в виде развившегося респираторного дистресс-синдрома. Наличие дыхательной дисфункции можно определять при наличие тахипноэ больше 20 в минуту, снижение артериальной сатурации меньше 90% и р. О 2 арт. меньше 50 мм. рт. ст. pa. O 2Fi. O 2<300 и pa. O 2Fi. O 2<200


 Почечная дисфункция и ее коррекция Почечная дисфункция может проявляться как олигурическая либо неолигурическая. Причины развития в большинстве случаев преренальные или ренальные. Снижение ОЦК и снижение сердечного выброса являются типичными факторами развития почечной дисфункции в неотложной хирургии. Токсические повреждения паренхимы почек, например, за счет нефротоксических антибиотиков тоже могут играть роль в развитии и течении дисфункции. Для предотвращения дисфункции используются малые дозы диуретиков на фоне нормоволемии, а также поддержание сердечного индекса более 4, 5 и среднего артериального давления выше 70 мм. рт. ст. Также необходимо избегать использования нефротоксических веществ и лекарств (гентамицина, амикацина, диокисдина).
Почечная дисфункция и ее коррекция Почечная дисфункция может проявляться как олигурическая либо неолигурическая. Причины развития в большинстве случаев преренальные или ренальные. Снижение ОЦК и снижение сердечного выброса являются типичными факторами развития почечной дисфункции в неотложной хирургии. Токсические повреждения паренхимы почек, например, за счет нефротоксических антибиотиков тоже могут играть роль в развитии и течении дисфункции. Для предотвращения дисфункции используются малые дозы диуретиков на фоне нормоволемии, а также поддержание сердечного индекса более 4, 5 и среднего артериального давления выше 70 мм. рт. ст. Также необходимо избегать использования нефротоксических веществ и лекарств (гентамицина, амикацина, диокисдина).

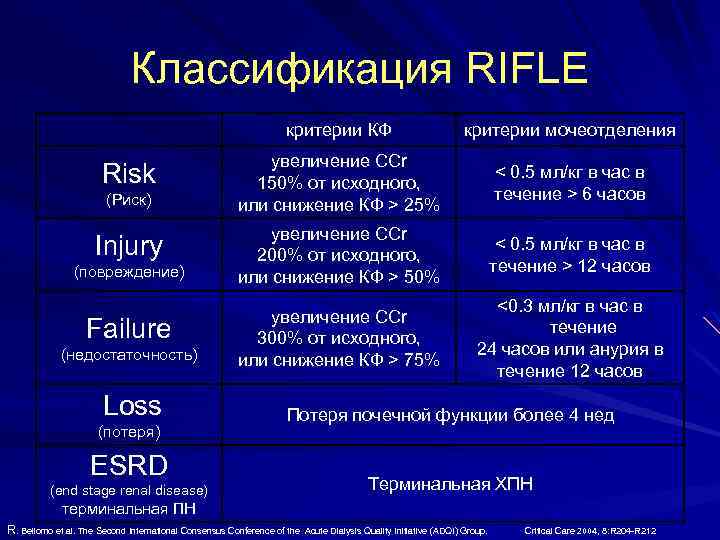 Классификация RIFLE критерии КФ Risk (Риск) Injury (повреждение) Failure (недостаточность) Loss (потеря) ESRD (end stage renal disease) критерии мочеотделения увеличение СCr < 0. 5 мл/кг в час в 150% от исходного, течение > 6 часов или снижение КФ > 25% увеличение СCr < 0. 5 мл/кг в час в 200% от исходного, течение > 12 часов или снижение КФ > 50% <0. 3 мл/кг в час в увеличение СCr течение 300% от исходного, 24 часов или анурия в или снижение КФ > 75% течение 12 часов Потеря почечной функции более 4 нед Терминальная ХПН терминальная ПН R. Bellomo et al. The Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Critical Care 2004, 8: R 204 -R 212
Классификация RIFLE критерии КФ Risk (Риск) Injury (повреждение) Failure (недостаточность) Loss (потеря) ESRD (end stage renal disease) критерии мочеотделения увеличение СCr < 0. 5 мл/кг в час в 150% от исходного, течение > 6 часов или снижение КФ > 25% увеличение СCr < 0. 5 мл/кг в час в 200% от исходного, течение > 12 часов или снижение КФ > 50% <0. 3 мл/кг в час в увеличение СCr течение 300% от исходного, 24 часов или анурия в или снижение КФ > 75% течение 12 часов Потеря почечной функции более 4 нед Терминальная ХПН терминальная ПН R. Bellomo et al. The Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Critical Care 2004, 8: R 204 -R 212
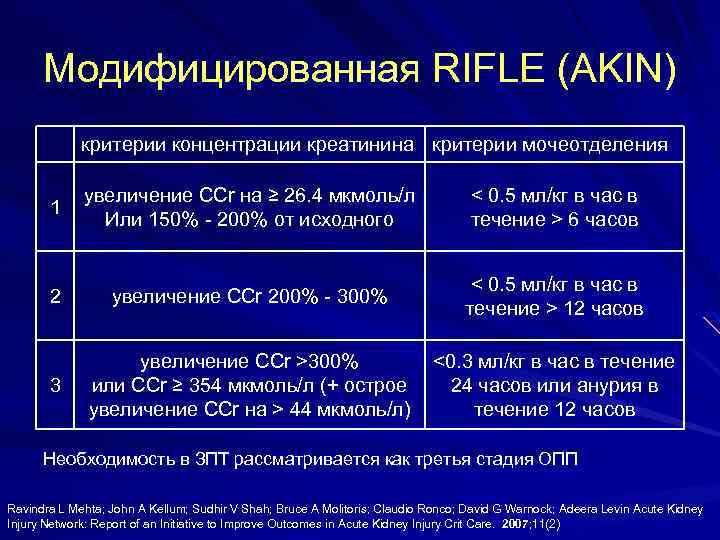 Модифицированная RIFLE (AKIN) критерии концентрации креатинина критерии мочеотделения 1 увеличение СCr на ≥ 26. 4 мкмоль/л Или 150% - 200% от исходного < 0. 5 мл/кг в час в течение > 6 часов 2 увеличение СCr 200% - 300% < 0. 5 мл/кг в час в течение > 12 часов 3 увеличение СCr >300% или СCr ≥ 354 мкмоль/л (+ острое увеличение СCr на > 44 мкмоль/л) <0. 3 мл/кг в час в течение 24 часов или анурия в течение 12 часов Необходимость в ЗПТ рассматривается как третья стадия ОПП Ravindra L Mehta; John A Kellum; Sudhir V Shah; Bruce A Molitoris; Claudio Ronco; David G Warnock; Adeera Levin Acute Kidney Injury Network: Report of an Initiative to Improve Outcomes in Acute Kidney Injury Crit Care. 2007; 11(2)
Модифицированная RIFLE (AKIN) критерии концентрации креатинина критерии мочеотделения 1 увеличение СCr на ≥ 26. 4 мкмоль/л Или 150% - 200% от исходного < 0. 5 мл/кг в час в течение > 6 часов 2 увеличение СCr 200% - 300% < 0. 5 мл/кг в час в течение > 12 часов 3 увеличение СCr >300% или СCr ≥ 354 мкмоль/л (+ острое увеличение СCr на > 44 мкмоль/л) <0. 3 мл/кг в час в течение 24 часов или анурия в течение 12 часов Необходимость в ЗПТ рассматривается как третья стадия ОПП Ravindra L Mehta; John A Kellum; Sudhir V Shah; Bruce A Molitoris; Claudio Ronco; David G Warnock; Adeera Levin Acute Kidney Injury Network: Report of an Initiative to Improve Outcomes in Acute Kidney Injury Crit Care. 2007; 11(2)
 Печеночная дисфункция и расстройства коагуляции Частота ОПеч. Н по последним данным составляет порядка 10%. Нужно учитывать, что причиной печеночной дисфункции могут явиться хронические заболевания печени — алкогольный, вирусный гепатит или цирроз печени. Именно поэтому важным является определение факторов свертывания крови. Для профилактики развития ДВС-синдрома применяют низкомолекулярный гепарин под контролем лабораторных показателей свертывания.
Печеночная дисфункция и расстройства коагуляции Частота ОПеч. Н по последним данным составляет порядка 10%. Нужно учитывать, что причиной печеночной дисфункции могут явиться хронические заболевания печени — алкогольный, вирусный гепатит или цирроз печени. Именно поэтому важным является определение факторов свертывания крови. Для профилактики развития ДВС-синдрома применяют низкомолекулярный гепарин под контролем лабораторных показателей свертывания.

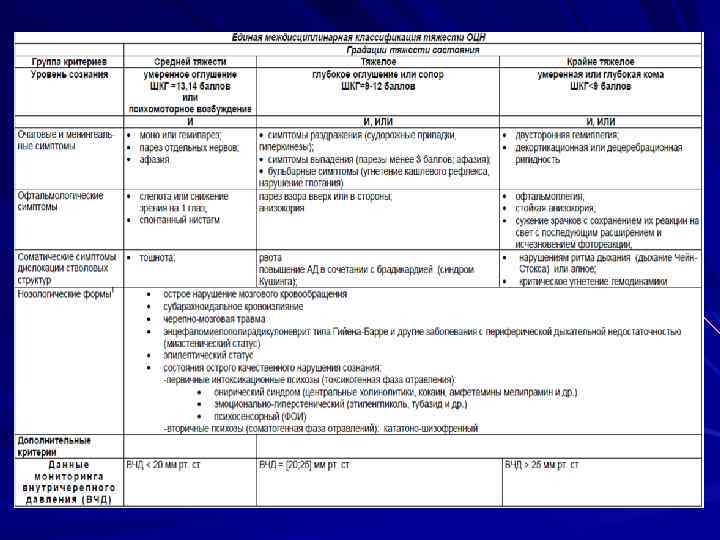
 Шкала гастроинтестинальной недостаточности A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90 баллы Клинические симптомы 0 Нормальная функция ЖКТ 1 Усваивает 50% расчетной дозы или 3 дня без кормления после абдоминальной операции 2 Непереносимость питания (большой сброс из желудка, рвота, вздутие, сильная диарея) или с-м Аб. Г 3 Непереносимость питания и с-м Аб. Г 4 Abdominal compartment syndrome
Шкала гастроинтестинальной недостаточности A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90 баллы Клинические симптомы 0 Нормальная функция ЖКТ 1 Усваивает 50% расчетной дозы или 3 дня без кормления после абдоминальной операции 2 Непереносимость питания (большой сброс из желудка, рвота, вздутие, сильная диарея) или с-м Аб. Г 3 Непереносимость питания и с-м Аб. Г 4 Abdominal compartment syndrome
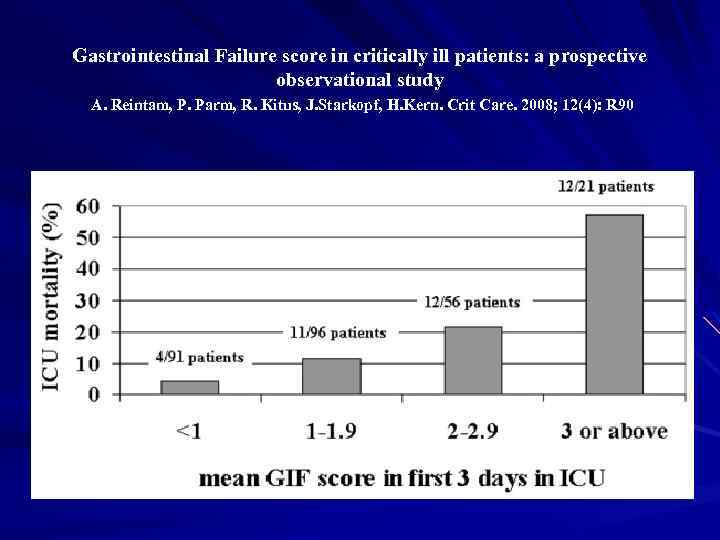 Gastrointestinal Failure score in critically ill patients: a prospective observational study A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90
Gastrointestinal Failure score in critically ill patients: a prospective observational study A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90
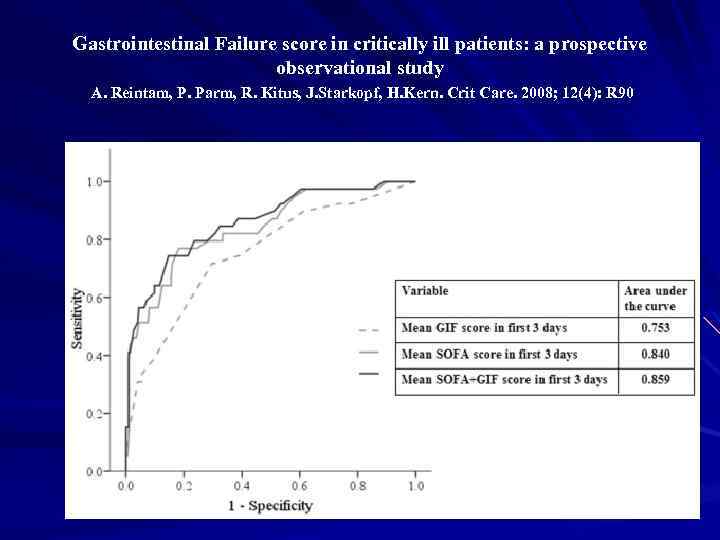 Gastrointestinal Failure score in critically ill patients: a prospective observational study A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90
Gastrointestinal Failure score in critically ill patients: a prospective observational study A. Reintam, P. Parm, R. Kitus, J. Starkopf, H. Kern. Crit Care. 2008; 12(4): R 90


