Lecture_5_4Nuclear.ppt
- Количество слайдов: 42

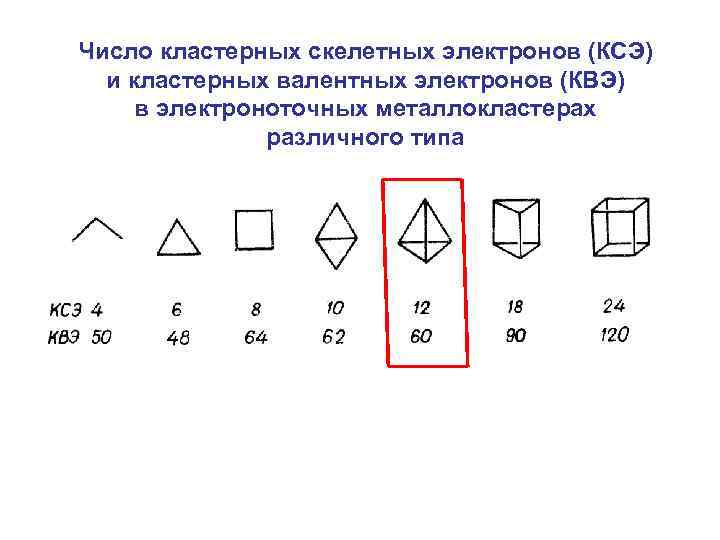 Число кластерных скелетных электронов (КСЭ) и кластерных валентных электронов (КВЭ) в электроноточных металлокластерах различного типа
Число кластерных скелетных электронов (КСЭ) и кластерных валентных электронов (КВЭ) в электроноточных металлокластерах различного типа
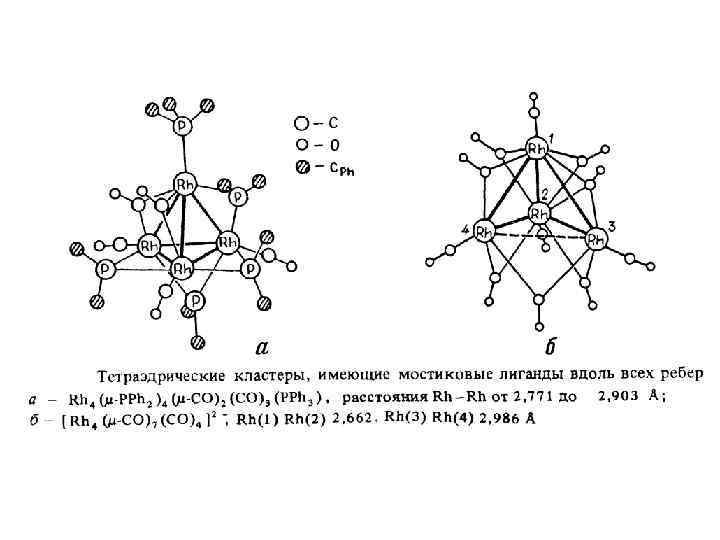
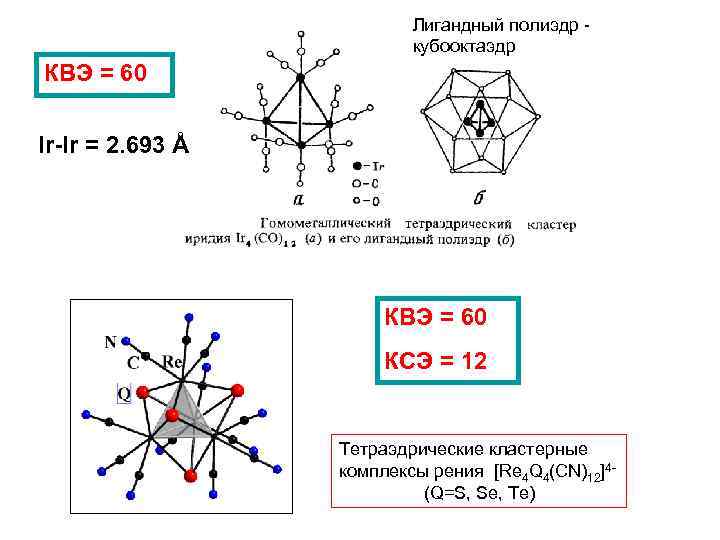 Лигандный полиэдр кубооктаэдр КВЭ = 60 Ir-Ir = 2. 693 Å КВЭ = 60 КСЭ = 12 Тетраэдрические кластерные комплексы рения [Re 4 Q 4(CN)12]4(Q=S, Se, Te)
Лигандный полиэдр кубооктаэдр КВЭ = 60 Ir-Ir = 2. 693 Å КВЭ = 60 КСЭ = 12 Тетраэдрические кластерные комплексы рения [Re 4 Q 4(CN)12]4(Q=S, Se, Te)
![КВЭ=60 Ir 4(CO)12 [( 3 -H)4 Co 4(Cp)4] КВЭ=60 Ir 4(CO)12 [( 3 -H)4 Co 4(Cp)4]](https://present5.com/presentation/5652994_182163056/image-4.jpg) КВЭ=60 Ir 4(CO)12 [( 3 -H)4 Co 4(Cp)4]
КВЭ=60 Ir 4(CO)12 [( 3 -H)4 Co 4(Cp)4]

 56 КВЭ 50 КВЭ
56 КВЭ 50 КВЭ
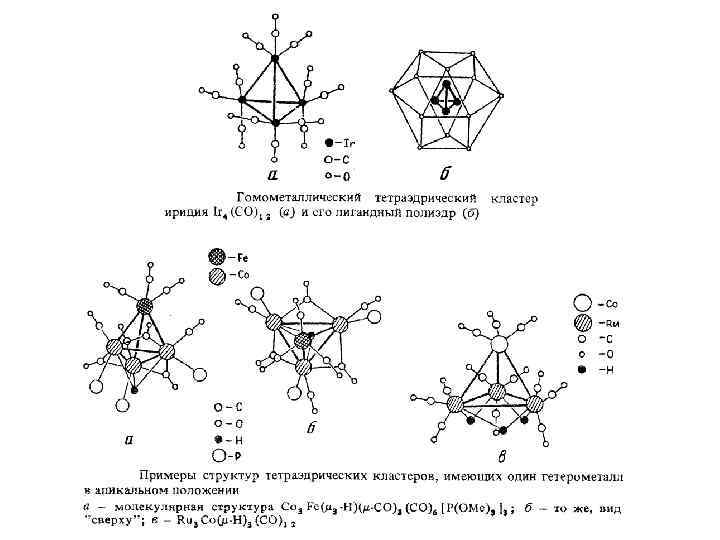
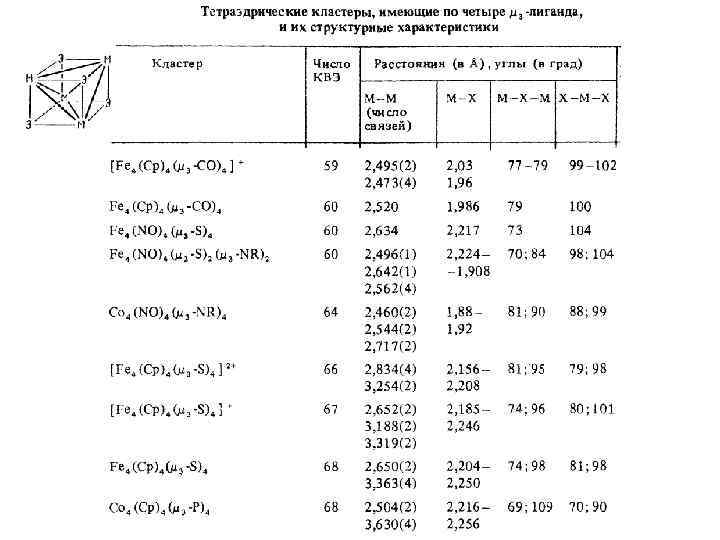
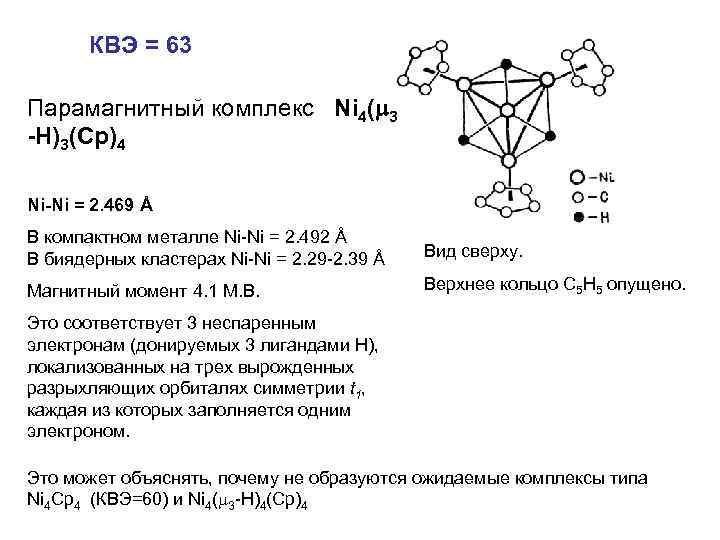 КВЭ = 63 Парамагнитный комплекс Ni 4( 3 -H)3(Cp)4 Ni-Ni = 2. 469 Å В компактном металле Ni-Ni = 2. 492 Å В биядерных кластерах Ni-Ni = 2. 29 -2. 39 Å Вид сверху. Магнитный момент 4. 1 М. В. Верхнее кольцо С 5 Н 5 опущено. Это соответствует 3 неспаренным электронам (донируемых 3 лигандами Н), локализованных на трех вырожденных разрыхляющих орбиталях симметрии t 1, каждая из которых заполняется одним электроном. Это может объяснять, почему не образуются ожидаемые комплексы типа Ni 4 Cp 4 (КВЭ=60) и Ni 4( 3 -H)4(Cp)4
КВЭ = 63 Парамагнитный комплекс Ni 4( 3 -H)3(Cp)4 Ni-Ni = 2. 469 Å В компактном металле Ni-Ni = 2. 492 Å В биядерных кластерах Ni-Ni = 2. 29 -2. 39 Å Вид сверху. Магнитный момент 4. 1 М. В. Верхнее кольцо С 5 Н 5 опущено. Это соответствует 3 неспаренным электронам (донируемых 3 лигандами Н), локализованных на трех вырожденных разрыхляющих орбиталях симметрии t 1, каждая из которых заполняется одним электроном. Это может объяснять, почему не образуются ожидаемые комплексы типа Ni 4 Cp 4 (КВЭ=60) и Ni 4( 3 -H)4(Cp)4
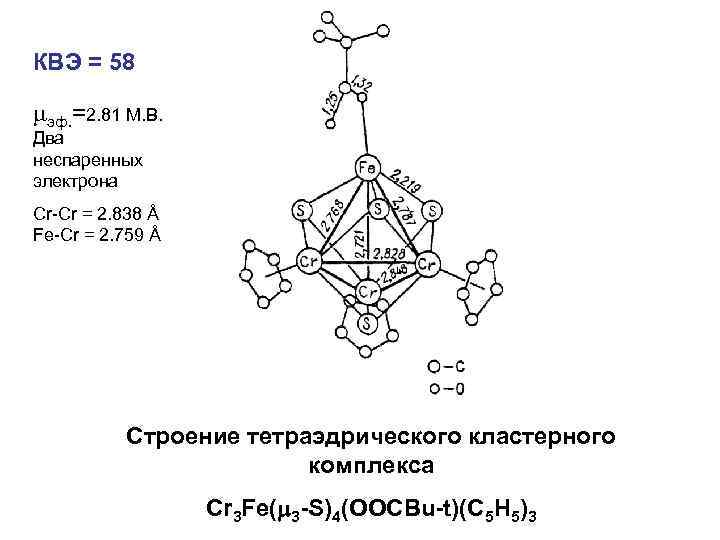 КВЭ = 58 эф. =2. 81 М. В. Два неспаренных электрона Cr-Cr = 2. 838 Å Fe-Cr = 2. 759 Å Строение тетраэдрического кластерного комплекса Cr 3 Fe( 3 -S)4(OOCBu-t)(C 5 H 5)3
КВЭ = 58 эф. =2. 81 М. В. Два неспаренных электрона Cr-Cr = 2. 838 Å Fe-Cr = 2. 759 Å Строение тетраэдрического кластерного комплекса Cr 3 Fe( 3 -S)4(OOCBu-t)(C 5 H 5)3
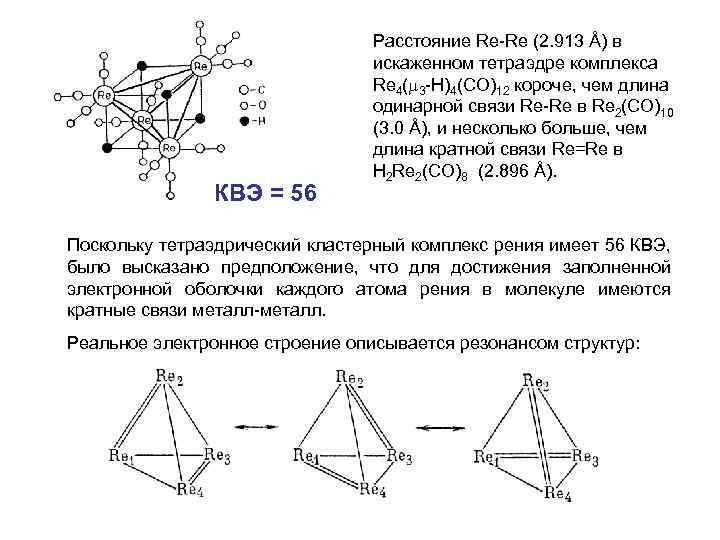 КВЭ = 56 Расстояние Re-Re (2. 913 Å) в искаженном тетраэдре комплекса Re 4( 3 -Н)4(CO)12 короче, чем длина одинарной связи Re-Re в Re 2(CO)10 (3. 0 Å), и несколько больше, чем длина кратной связи Re=Re в H 2 Re 2(CO)8 (2. 896 Å). Поскольку тетраэдрический кластерный комплекс рения имеет 56 КВЭ, было высказано предположение, что для достижения заполненной электронной оболочки каждого атома рения в молекуле имеются кратные связи металл-металл. Реальное электронное строение описывается резонансом структур:
КВЭ = 56 Расстояние Re-Re (2. 913 Å) в искаженном тетраэдре комплекса Re 4( 3 -Н)4(CO)12 короче, чем длина одинарной связи Re-Re в Re 2(CO)10 (3. 0 Å), и несколько больше, чем длина кратной связи Re=Re в H 2 Re 2(CO)8 (2. 896 Å). Поскольку тетраэдрический кластерный комплекс рения имеет 56 КВЭ, было высказано предположение, что для достижения заполненной электронной оболочки каждого атома рения в молекуле имеются кратные связи металл-металл. Реальное электронное строение описывается резонансом структур:
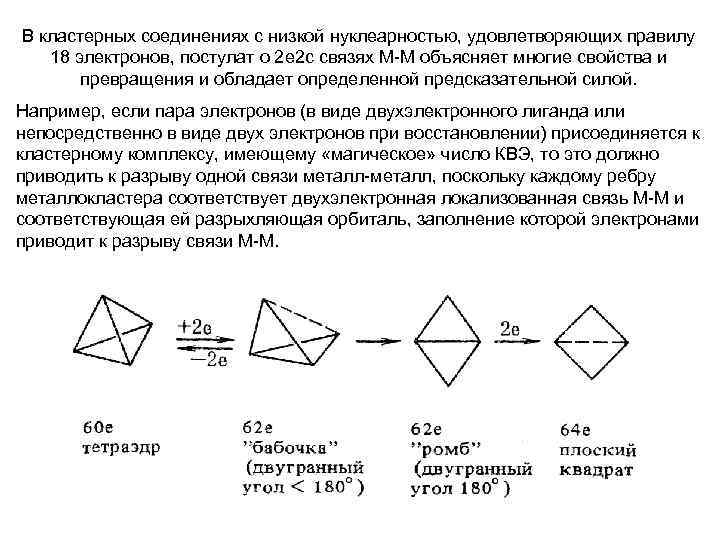 В кластерных соединениях с низкой нуклеарностью, удовлетворяющих правилу 18 электронов, постулат о 2 е 2 с связях M-M объясняет многие свойства и превращения и обладает определенной предсказательной силой. Например, если пара электронов (в виде двухэлектронного лиганда или непосредственно в виде двух электронов при восстановлении) присоединяется к кластерному комплексу, имеющему «магическое» число КВЭ, то это должно приводить к разрыву одной связи металл-металл, поскольку каждому ребру металлокластера соответствует двухэлектронная локализованная связь М-М и соответствующая ей разрыхляющая орбиталь, заполнение которой электронами приводит к разрыву связи М-М.
В кластерных соединениях с низкой нуклеарностью, удовлетворяющих правилу 18 электронов, постулат о 2 е 2 с связях M-M объясняет многие свойства и превращения и обладает определенной предсказательной силой. Например, если пара электронов (в виде двухэлектронного лиганда или непосредственно в виде двух электронов при восстановлении) присоединяется к кластерному комплексу, имеющему «магическое» число КВЭ, то это должно приводить к разрыву одной связи металл-металл, поскольку каждому ребру металлокластера соответствует двухэлектронная локализованная связь М-М и соответствующая ей разрыхляющая орбиталь, заполнение которой электронами приводит к разрыву связи М-М.


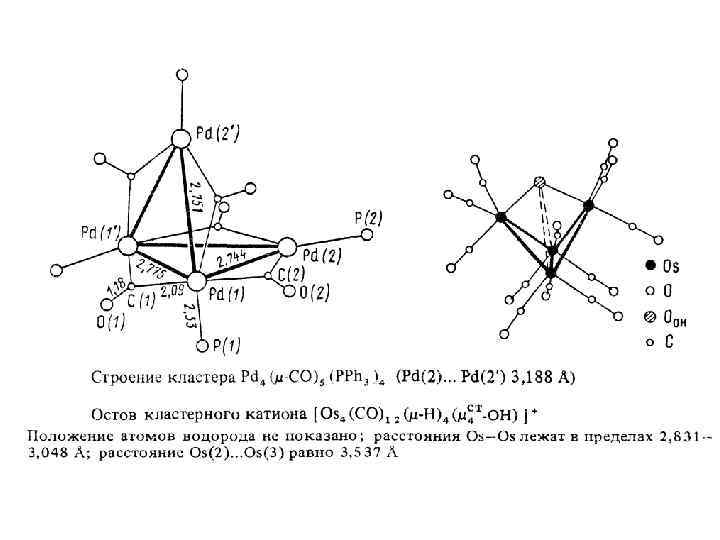
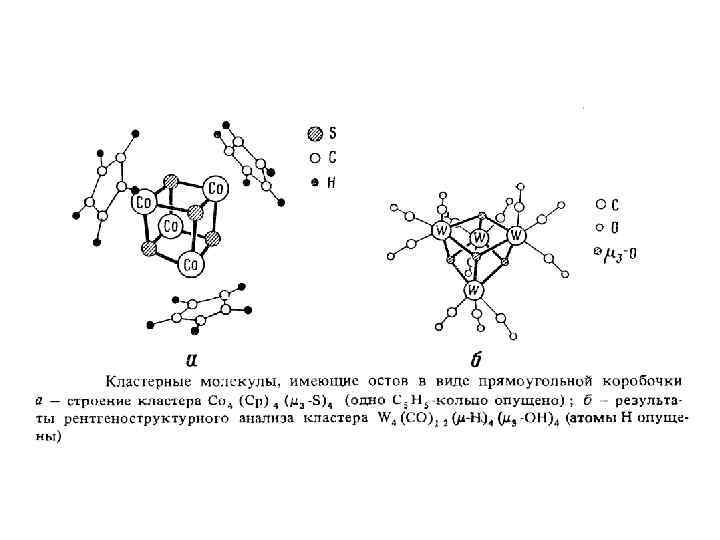
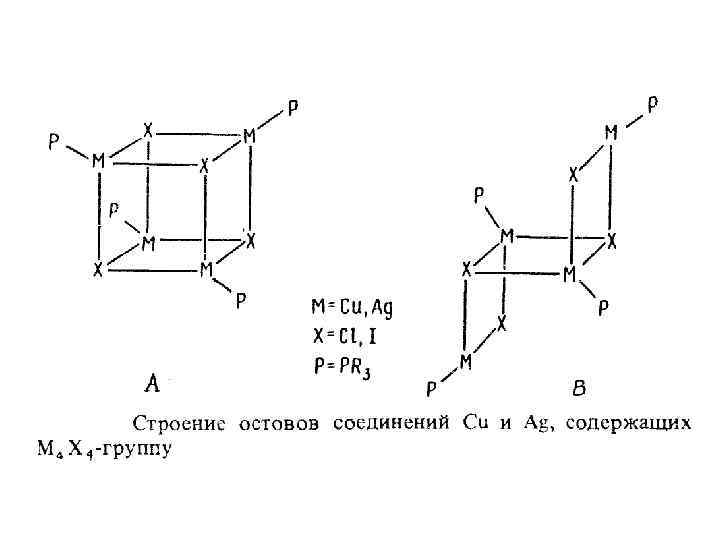
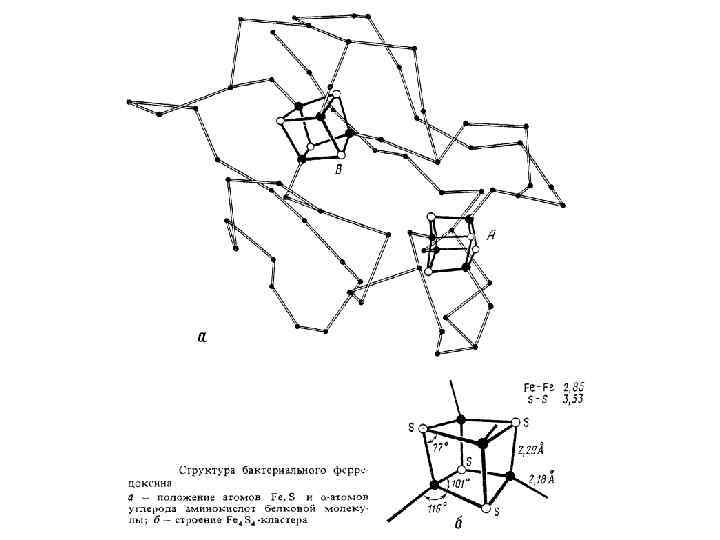
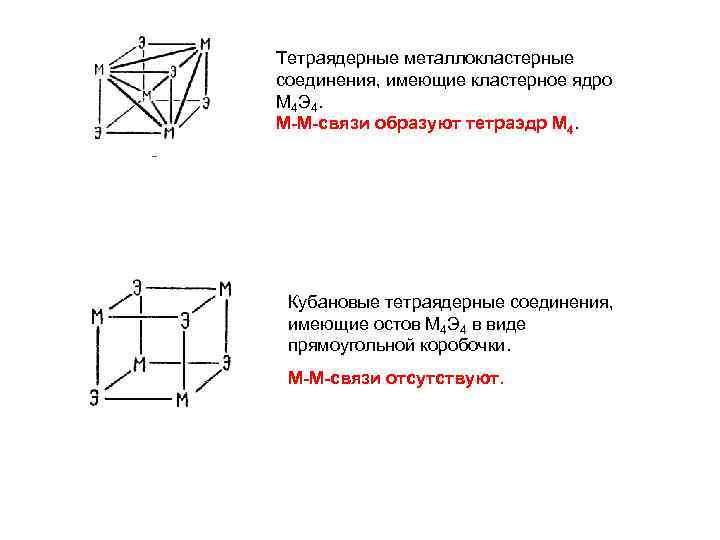 Тетраядерные металлокластерные соединения, имеющие кластерное ядро М 4 Э 4. М-М-связи образуют тетраэдр М 4. Кубановые тетраядерные соединения, имеющие остов М 4 Э 4 в виде прямоугольной коробочки. М-М-связи отсутствуют.
Тетраядерные металлокластерные соединения, имеющие кластерное ядро М 4 Э 4. М-М-связи образуют тетраэдр М 4. Кубановые тетраядерные соединения, имеющие остов М 4 Э 4 в виде прямоугольной коробочки. М-М-связи отсутствуют.
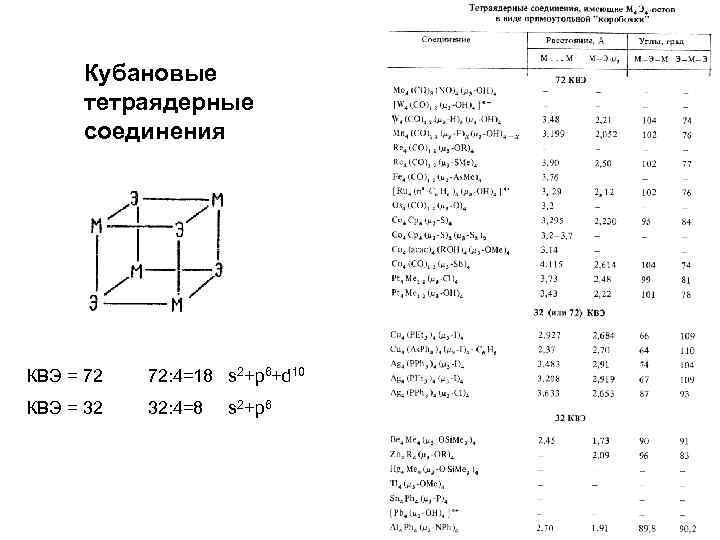 Кубановые тетраядерные соединения КВЭ = 72 72: 4=18 s 2+p 6+d 10 КВЭ = 32 32: 4=8 s 2+p 6
Кубановые тетраядерные соединения КВЭ = 72 72: 4=18 s 2+p 6+d 10 КВЭ = 32 32: 4=8 s 2+p 6
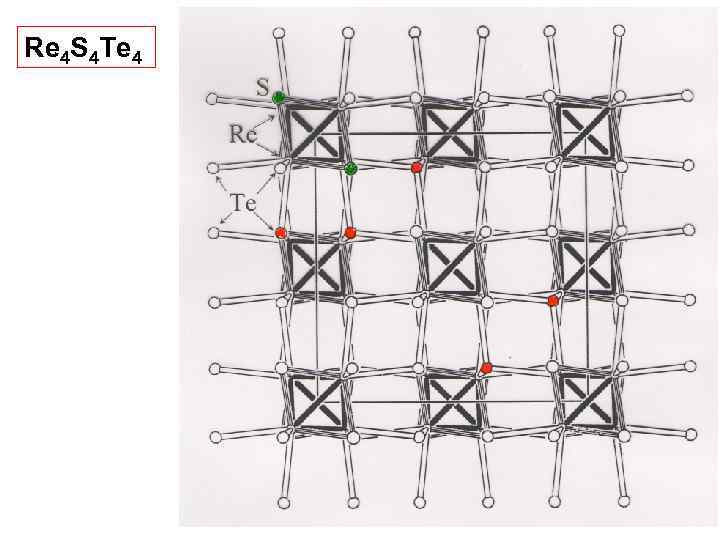 Re 4 S 4 Te 4
Re 4 S 4 Te 4
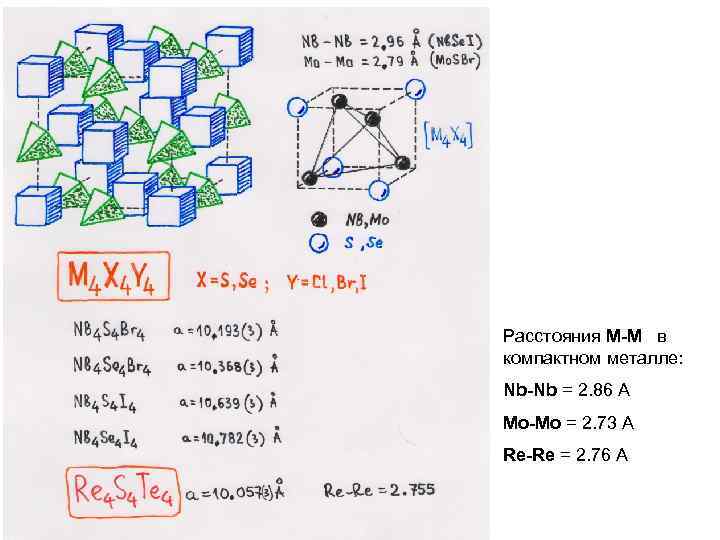 Расстояния M-M в компактном металле: Nb-Nb = 2. 86 A Mo-Mo = 2. 73 A Re-Re = 2. 76 A
Расстояния M-M в компактном металле: Nb-Nb = 2. 86 A Mo-Mo = 2. 73 A Re-Re = 2. 76 A

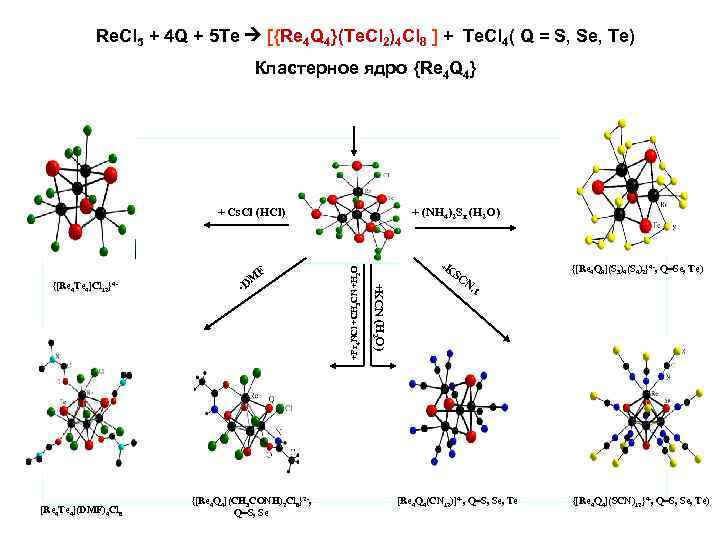 Re. Cl 5 + 4 Q + 5 Te [{Re 4 Q 4}(Te. Cl 2)4 Cl 8 ] + Te. Cl 4( Q = S, Se, Te) Кластерное ядро {Re 4 Q 4} F [Re 4 Te 4](DMF)4 Cl 8 + {[Re 4 Q 4](CH 3 CONH)2 Cl 8}2 -, Q=S, Se + +KCN (H 2 O) {[Re 4 Te 4]Cl 12}4 - DM + (NH 4)2 Sx (H 2 O) +Pr 4 NCl +CH 3 CN +H 2 O + Cs. Cl (HCl) KS CN , {[Re 4 Q 4](S 3)4(S 4)2}4 -, Q=Se, Te) t [Re 4 Q 4(CN 12)]4 -, Q=S, Se, Te {[Re 4 Q 4](SCN)12}4 -, Q=S, Se, Te)
Re. Cl 5 + 4 Q + 5 Te [{Re 4 Q 4}(Te. Cl 2)4 Cl 8 ] + Te. Cl 4( Q = S, Se, Te) Кластерное ядро {Re 4 Q 4} F [Re 4 Te 4](DMF)4 Cl 8 + {[Re 4 Q 4](CH 3 CONH)2 Cl 8}2 -, Q=S, Se + +KCN (H 2 O) {[Re 4 Te 4]Cl 12}4 - DM + (NH 4)2 Sx (H 2 O) +Pr 4 NCl +CH 3 CN +H 2 O + Cs. Cl (HCl) KS CN , {[Re 4 Q 4](S 3)4(S 4)2}4 -, Q=Se, Te) t [Re 4 Q 4(CN 12)]4 -, Q=S, Se, Te {[Re 4 Q 4](SCN)12}4 -, Q=S, Se, Te)
![Цепочечные структуры на основе халькоцианидных анионов [Re 4 Q 4(CN)12]4 - [{Cu(trien) }2 Re Цепочечные структуры на основе халькоцианидных анионов [Re 4 Q 4(CN)12]4 - [{Cu(trien) }2 Re](https://present5.com/presentation/5652994_182163056/image-28.jpg) Цепочечные структуры на основе халькоцианидных анионов [Re 4 Q 4(CN)12]4 - [{Cu(trien) }2 Re 4 Te 4(CN)12] [{Cu 2(dien)3}Re 4 S 4(CN)12]
Цепочечные структуры на основе халькоцианидных анионов [Re 4 Q 4(CN)12]4 - [{Cu(trien) }2 Re 4 Te 4(CN)12] [{Cu 2(dien)3}Re 4 S 4(CN)12]
![C 2/c Цепочка {[{Ln(H 2 O)6}Re 4 Te 4(CN)12] -}∞ в соединениях (H 3 C 2/c Цепочка {[{Ln(H 2 O)6}Re 4 Te 4(CN)12] -}∞ в соединениях (H 3](https://present5.com/presentation/5652994_182163056/image-29.jpg) C 2/c Цепочка {[{Ln(H 2 O)6}Re 4 Te 4(CN)12] -}∞ в соединениях (H 3 O)[{Ln(H 2 O)6}Re 4 Q 4(CN)12] x. H 2 O Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
C 2/c Цепочка {[{Ln(H 2 O)6}Re 4 Te 4(CN)12] -}∞ в соединениях (H 3 O)[{Ln(H 2 O)6}Re 4 Q 4(CN)12] x. H 2 O Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
![Синтез хиральных кластерных полимеров на основе тетрааминобутана [Re 4 Q 4(CN)12]4 - + Cu Синтез хиральных кластерных полимеров на основе тетрааминобутана [Re 4 Q 4(CN)12]4 - + Cu](https://present5.com/presentation/5652994_182163056/image-30.jpg) Синтез хиральных кластерных полимеров на основе тетрааминобутана [Re 4 Q 4(CN)12]4 - + Cu 2+ + NH 3 aq [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H 2 O [{Cu 2(NH 3) (threo-tab)2}Re 4 Te 4(CN)12] 4 H 2 O
Синтез хиральных кластерных полимеров на основе тетрааминобутана [Re 4 Q 4(CN)12]4 - + Cu 2+ + NH 3 aq [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H 2 O [{Cu 2(NH 3) (threo-tab)2}Re 4 Te 4(CN)12] 4 H 2 O
![Строение цепочек в соединениях разного состава [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H Строение цепочек в соединениях разного состава [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H](https://present5.com/presentation/5652994_182163056/image-31.jpg) Строение цепочек в соединениях разного состава [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H 2 O [{Cu 2(NH 3) (threo-tab)2}Re 4 Te 4(CN)12] 4 H 2 O Re black Te red Cu cyan N blue C black
Строение цепочек в соединениях разного состава [{Cu(threo-tab)}2 Re 4 Te 4(CN)12] 6, 5 H 2 O [{Cu 2(NH 3) (threo-tab)2}Re 4 Te 4(CN)12] 4 H 2 O Re black Te red Cu cyan N blue C black
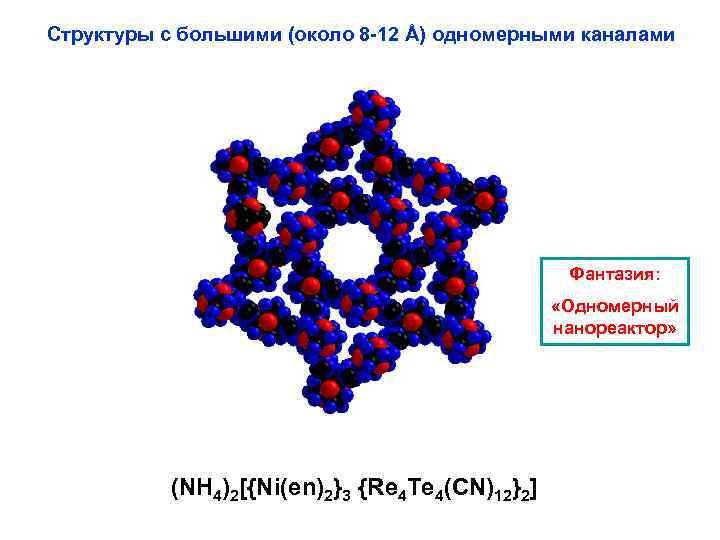 Структуры с большими (около 8 -12 Å) одномерными каналами Фантазия: «Одномерный нанореактор» (NH 4)2[{Ni(en)2}3 {Re 4 Te 4(CN)12}2]
Структуры с большими (около 8 -12 Å) одномерными каналами Фантазия: «Одномерный нанореактор» (NH 4)2[{Ni(en)2}3 {Re 4 Te 4(CN)12}2]
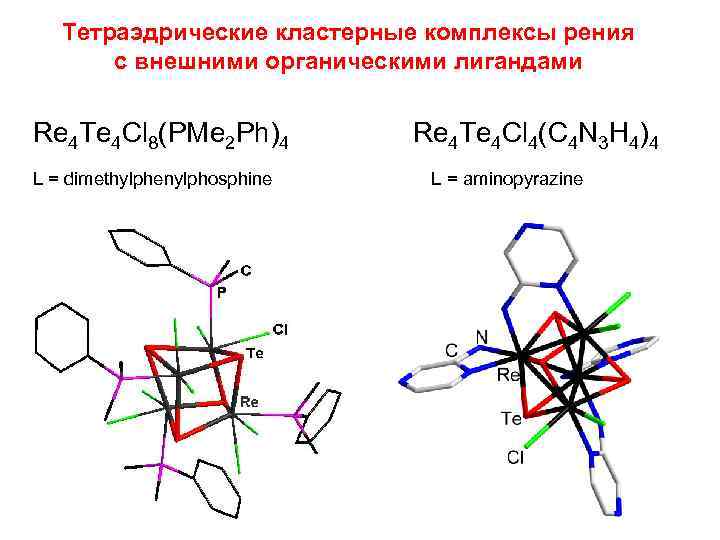 Тетраэдрические кластерные комплексы рения с внешними органическими лигандами Re 4 Te 4 Cl 8(PMe 2 Ph)4 L = dimethylphenylphosphine Re 4 Te 4 Cl 4(C 4 N 3 H 4)4 L = aminopyrazine
Тетраэдрические кластерные комплексы рения с внешними органическими лигандами Re 4 Te 4 Cl 8(PMe 2 Ph)4 L = dimethylphenylphosphine Re 4 Te 4 Cl 4(C 4 N 3 H 4)4 L = aminopyrazine








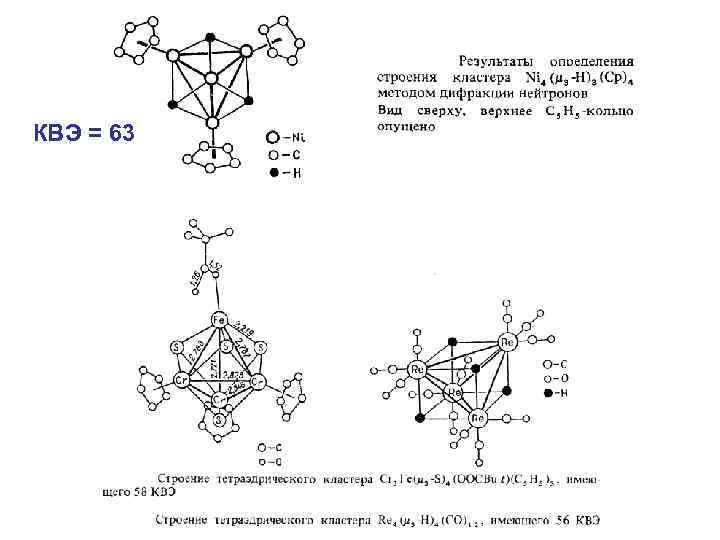 КВЭ = 63
КВЭ = 63


