lecture_2_2.pptx
- Количество слайдов: 28
 Chelating Agent Второй семестр 2013 ФАРМАКОКИНЕТИКА ЛЕКЦИЯ 2 Часть II Drug Metabolism & Toxicity
Chelating Agent Второй семестр 2013 ФАРМАКОКИНЕТИКА ЛЕКЦИЯ 2 Часть II Drug Metabolism & Toxicity
![competitive inhibition uncompetitive inhibition for tightly bound inhibitors enzyme concentration [E], substrate concentration [S], competitive inhibition uncompetitive inhibition for tightly bound inhibitors enzyme concentration [E], substrate concentration [S],](https://present5.com/presentation/8535518_308844475/image-2.jpg) competitive inhibition uncompetitive inhibition for tightly bound inhibitors enzyme concentration [E], substrate concentration [S], Michaelis Menten constant Km for tightly bound inhibitors inhibitor binds only to the complex formed between the enzyme and the substrate (the E S complex). For total concentrations, E is replaced by P and S is replaced by L. As in classic enzyme–substrate systems the relation of Ki and IC 50 in competitive inhibition is: noncompetitive inhibition
competitive inhibition uncompetitive inhibition for tightly bound inhibitors enzyme concentration [E], substrate concentration [S], Michaelis Menten constant Km for tightly bound inhibitors inhibitor binds only to the complex formed between the enzyme and the substrate (the E S complex). For total concentrations, E is replaced by P and S is replaced by L. As in classic enzyme–substrate systems the relation of Ki and IC 50 in competitive inhibition is: noncompetitive inhibition
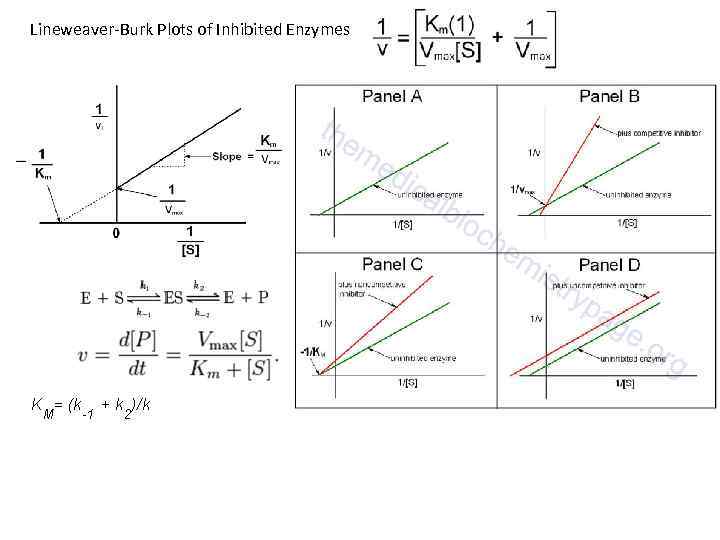 Lineweaver Burk Plots of Inhibited Enzymes
Lineweaver Burk Plots of Inhibited Enzymes
 ► Низкая метаболическая стабильность критическим образом ограничивает системную экспозицию ЛС, проявившего высокую активность в первоначальных in vitro испытаниях, уменьшает время ее действия и, как следствие, необратимо снижает ценность такого соединения в качестве фармацевтического препарата ► Эффект "первого прохождения" через печень, при котором многие ЛС способны подвергаться интенсивной метаболической деградации под действием различных ферментов, является еще одним примером критического влияния метаболизма на фармакокинетические параметры ЛС ► В научной литературе описано значительное количество примеров, в которых метаболиты высоко активных субстанций оказывались высокотоксичными агентами, что препятствовало их дальнейшему продвижению ► Знание потенциальных сайтов метаболизма низкомолекулярных органических соединений может быть использовано для химической модификации их структуры таким образом, чтобы исключить этот участок из структуры активной молекулы, либо защитить его, например, путем уменьшения его стерической доступности по отношению к центру связывания фермента или же путем различных биоизостерных модификаций ► Хрестоматийными примерами такого рода модификаций являются замена сложноэфирной группы прокаина на амидную группу, ведущая к метаболически устойчивому прокаинамиду, или же введение объемистой N изопропильной группы (вместо N метильной или N этильной) вблизи сайта метаболической реакции N деалкилирования известных ингибиторов адренорецепторов блокирует Na+ каналы
► Низкая метаболическая стабильность критическим образом ограничивает системную экспозицию ЛС, проявившего высокую активность в первоначальных in vitro испытаниях, уменьшает время ее действия и, как следствие, необратимо снижает ценность такого соединения в качестве фармацевтического препарата ► Эффект "первого прохождения" через печень, при котором многие ЛС способны подвергаться интенсивной метаболической деградации под действием различных ферментов, является еще одним примером критического влияния метаболизма на фармакокинетические параметры ЛС ► В научной литературе описано значительное количество примеров, в которых метаболиты высоко активных субстанций оказывались высокотоксичными агентами, что препятствовало их дальнейшему продвижению ► Знание потенциальных сайтов метаболизма низкомолекулярных органических соединений может быть использовано для химической модификации их структуры таким образом, чтобы исключить этот участок из структуры активной молекулы, либо защитить его, например, путем уменьшения его стерической доступности по отношению к центру связывания фермента или же путем различных биоизостерных модификаций ► Хрестоматийными примерами такого рода модификаций являются замена сложноэфирной группы прокаина на амидную группу, ведущая к метаболически устойчивому прокаинамиду, или же введение объемистой N изопропильной группы (вместо N метильной или N этильной) вблизи сайта метаболической реакции N деалкилирования известных ингибиторов адренорецепторов блокирует Na+ каналы
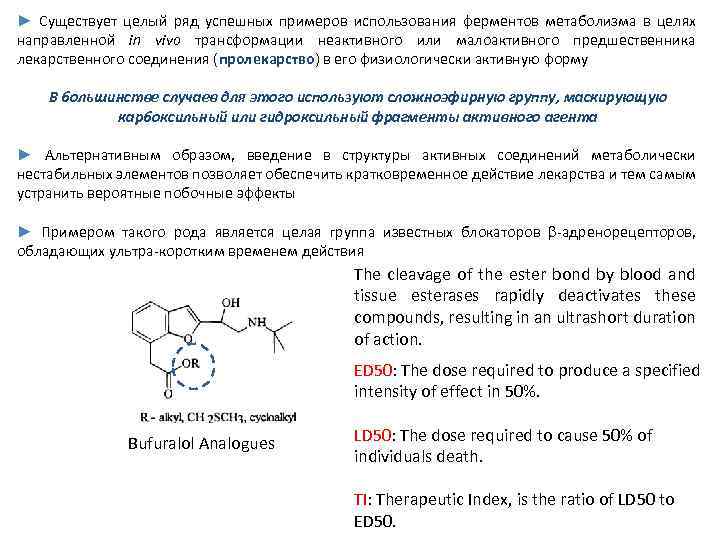 ► Существует целый ряд успешных примеров использования ферментов метаболизма в целях направленной in vivo трансформации неактивного или малоактивного предшественника лекарственного соединения (пролекарство) в его физиологически активную форму В большинстве случаев для этого используют сложноэфирную группу, маскирующую карбоксильный или гидроксильный фрагменты активного агента ► Альтернативным образом, введение в структуры активных соединений метаболически нестабильных элементов позволяет обеспечить кратковременное действие лекарства и тем самым устранить вероятные побочные эффекты ► Примером такого рода является целая группа известных блокаторов адренорецепторов, обладающих ультра коротким временем действия The cleavage of the ester bond by blood and tissue esterases rapidly deactivates these compounds, resulting in an ultrashort duration of action. ED 50: The dose required to produce a specified intensity of effect in 50%. Bufuralol Analogues LD 50: The dose required to cause 50% of individuals death. TI: Therapeutic Index, is the ratio of LD 50 to ED 50.
► Существует целый ряд успешных примеров использования ферментов метаболизма в целях направленной in vivo трансформации неактивного или малоактивного предшественника лекарственного соединения (пролекарство) в его физиологически активную форму В большинстве случаев для этого используют сложноэфирную группу, маскирующую карбоксильный или гидроксильный фрагменты активного агента ► Альтернативным образом, введение в структуры активных соединений метаболически нестабильных элементов позволяет обеспечить кратковременное действие лекарства и тем самым устранить вероятные побочные эффекты ► Примером такого рода является целая группа известных блокаторов адренорецепторов, обладающих ультра коротким временем действия The cleavage of the ester bond by blood and tissue esterases rapidly deactivates these compounds, resulting in an ultrashort duration of action. ED 50: The dose required to produce a specified intensity of effect in 50%. Bufuralol Analogues LD 50: The dose required to cause 50% of individuals death. TI: Therapeutic Index, is the ratio of LD 50 to ED 50.
 Печень самая крупная железа пищеварительного тракта. Она выполняет в организме функцию биохимической лаборатории и играет важную роль в белковом, углеводном и липидном обменах. В печени синтезируются важнейшие белки плазмы крови: альбумин, фибриноген, протромбин, церулоплазмин, трансферрин, ангиотензиноген и др. С участием этих белков регулируются важные процессы в организме, такие как поддержание онкотического давления, регуляция артериального давления и объёма циркулирующей крови, свёртывание крови, метаболизм железа и др. В печени происходит обезвреживание таких веществ, как билирубин и продукты катаболизма аминокислот в кишечнике, а также инактивируются ЛС и токсические вещества экзогенного происхождения, NH 3 продукт азотистого обмена, который в результате ферментативных реакций превращается в нетоксичную мочевину, гормоны и биогенные амины. Гидрофильные ксенобиотики выводятся из организма в, как правило, неизменённом виде с мочой, гидрофобные могут задерживаться в тканях, связываясь с белками или образуя комплексы с липидами клеточных мембран. Со временем накопление в клетках тканей чужеродного вещества приведёт к нарушению их функций. Для удаления таких ненужных для организма веществ в процессе эволюции выработались механизмы их детоксикации и выведения из организма путем специальных метаболических путей. Система обезвреживания включает множество разнообразных ферментов, под действием которых практически любой ксенобиотик может быть модифицирован. В метаболизме могут принимать участие ферменты почек, лёгких, кожи и ЖКТ, но наиболее активны они в печени, где микросомальные ферменты играют наиболее значимую роль. Важнейшие свойства ферментов микросомального окисления: широкая субстратная специфичность, которая позволяет обезвреживать самые разнообразные по строению вещества, и регуляция активности по механизму индукции.
Печень самая крупная железа пищеварительного тракта. Она выполняет в организме функцию биохимической лаборатории и играет важную роль в белковом, углеводном и липидном обменах. В печени синтезируются важнейшие белки плазмы крови: альбумин, фибриноген, протромбин, церулоплазмин, трансферрин, ангиотензиноген и др. С участием этих белков регулируются важные процессы в организме, такие как поддержание онкотического давления, регуляция артериального давления и объёма циркулирующей крови, свёртывание крови, метаболизм железа и др. В печени происходит обезвреживание таких веществ, как билирубин и продукты катаболизма аминокислот в кишечнике, а также инактивируются ЛС и токсические вещества экзогенного происхождения, NH 3 продукт азотистого обмена, который в результате ферментативных реакций превращается в нетоксичную мочевину, гормоны и биогенные амины. Гидрофильные ксенобиотики выводятся из организма в, как правило, неизменённом виде с мочой, гидрофобные могут задерживаться в тканях, связываясь с белками или образуя комплексы с липидами клеточных мембран. Со временем накопление в клетках тканей чужеродного вещества приведёт к нарушению их функций. Для удаления таких ненужных для организма веществ в процессе эволюции выработались механизмы их детоксикации и выведения из организма путем специальных метаболических путей. Система обезвреживания включает множество разнообразных ферментов, под действием которых практически любой ксенобиотик может быть модифицирован. В метаболизме могут принимать участие ферменты почек, лёгких, кожи и ЖКТ, но наиболее активны они в печени, где микросомальные ферменты играют наиболее значимую роль. Важнейшие свойства ферментов микросомального окисления: широкая субстратная специфичность, которая позволяет обезвреживать самые разнообразные по строению вещества, и регуляция активности по механизму индукции.
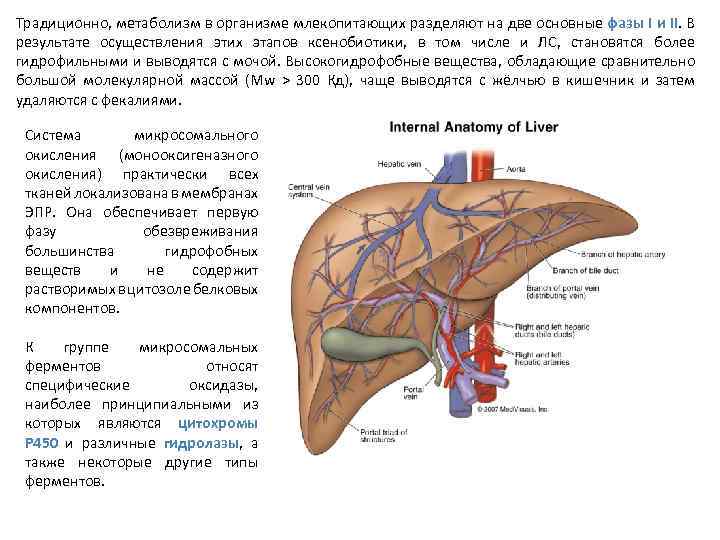 Традиционно, метаболизм в организме млекопитающих разделяют на две основные фазы I и II. В результате осуществления этих этапов ксенобиотики, в том числе и ЛС, становятся более гидрофильными и выводятся с мочой. Высокогидрофобные вещества, обладающие сравнительно большой молекулярной массой (Mw > 300 Кд), чаще выводятся с жёлчью в кишечник и затем удаляются с фекалиями. Система микросомального окисления (монооксигеназного окисления) практически всех тканей локализована в мембранах ЭПР. Она обеспечивает первую фазу обезвреживания большинства гидрофобных веществ и не содержит растворимых в цитозоле белковых компонентов. К группе микросомальных ферментов относят специфические оксидазы, наиболее принципиальными из которых являются цитохромы P 450 и различные гидролазы, а также некоторые другие типы ферментов.
Традиционно, метаболизм в организме млекопитающих разделяют на две основные фазы I и II. В результате осуществления этих этапов ксенобиотики, в том числе и ЛС, становятся более гидрофильными и выводятся с мочой. Высокогидрофобные вещества, обладающие сравнительно большой молекулярной массой (Mw > 300 Кд), чаще выводятся с жёлчью в кишечник и затем удаляются с фекалиями. Система микросомального окисления (монооксигеназного окисления) практически всех тканей локализована в мембранах ЭПР. Она обеспечивает первую фазу обезвреживания большинства гидрофобных веществ и не содержит растворимых в цитозоле белковых компонентов. К группе микросомальных ферментов относят специфические оксидазы, наиболее принципиальными из которых являются цитохромы P 450 и различные гидролазы, а также некоторые другие типы ферментов.
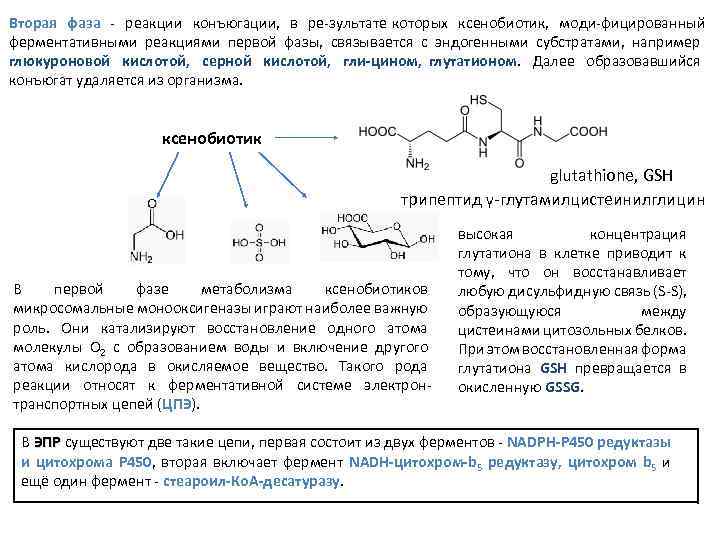 Вторая фаза реакции конъюгации, в ре зультате которых ксенобиотик, моди фицированный ферментативными реакциями первой фазы, связывается с эндогенными субстратами, например глюкуроновой кислотой, серной кислотой, гли цином, глутатионом. Далее образовавшийся конъюгат удаляется из организма. ксенобиотик glutathione, GSH трипептид γ глутамилцистеинилглицин В первой фазе метаболизма ксенобиотиков микросомальные монооксигеназы играют наиболее важную роль. Они катализируют восстановление одного атома молекулы О 2 с образованием воды и включение другого атома кислорода в окисляемое вещество. Такого рода реакции относят к ферментативной системе электрон транспортных цепей (ЦПЭ). высокая концентрация глутатиона в клетке приводит к тому, что он восстанавливает любую дисульфидную связь (S S), образующуюся между цистеинами цитозольных белков. При этом восстановленная форма глутатиона GSH превращается в окисленную GSSG. В ЭПР существуют две такие цепи, первая состоит из двух ферментов NADPH Р 450 редуктазы и цитохрома Р 450, вторая включает фермент NADH цитохром b 5 редуктазу, цитохром b 5 и ещё один фермент стеароил Ко. А десатуразу.
Вторая фаза реакции конъюгации, в ре зультате которых ксенобиотик, моди фицированный ферментативными реакциями первой фазы, связывается с эндогенными субстратами, например глюкуроновой кислотой, серной кислотой, гли цином, глутатионом. Далее образовавшийся конъюгат удаляется из организма. ксенобиотик glutathione, GSH трипептид γ глутамилцистеинилглицин В первой фазе метаболизма ксенобиотиков микросомальные монооксигеназы играют наиболее важную роль. Они катализируют восстановление одного атома молекулы О 2 с образованием воды и включение другого атома кислорода в окисляемое вещество. Такого рода реакции относят к ферментативной системе электрон транспортных цепей (ЦПЭ). высокая концентрация глутатиона в клетке приводит к тому, что он восстанавливает любую дисульфидную связь (S S), образующуюся между цистеинами цитозольных белков. При этом восстановленная форма глутатиона GSH превращается в окисленную GSSG. В ЭПР существуют две такие цепи, первая состоит из двух ферментов NADPH Р 450 редуктазы и цитохрома Р 450, вторая включает фермент NADH цитохром b 5 редуктазу, цитохром b 5 и ещё один фермент стеароил Ко. А десатуразу.
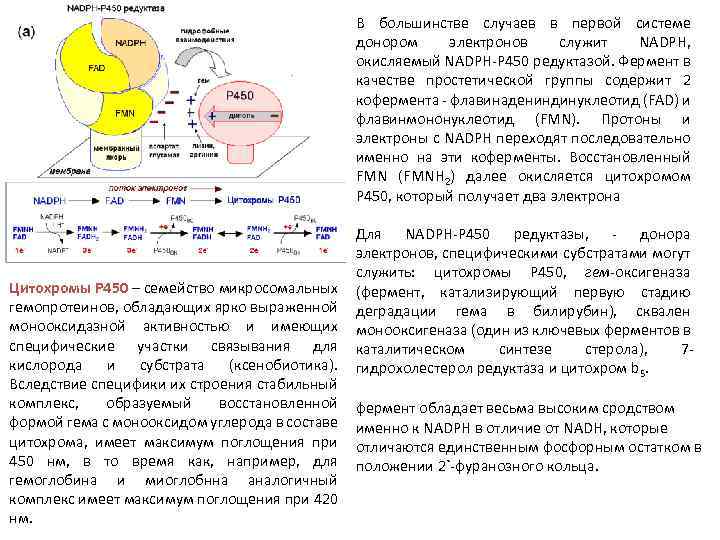 В большинстве случаев в первой системе донором электронов служит NADPH, окисляемый NADPH P 450 peдуктазой. Фермент в качестве простетической группы содержит 2 кофермента флавинадениндинуклеотид (FAD) и флавинмононуклеотид (FMN). Протоны и электроны с NADPH переходят последовательно именно на эти коферменты. Восстановленный FMN (FMNH 2) далее окисляется цитохромом Р 450, который получает два электрона Цитохромы Р 450 – семейство микросомальных гемопротеинов, обладающих ярко выраженной монооксидазной активностью и имеющих специфические участки связывания для кислорода и субстрата (ксенобиотика). Вследствие специфики их строения стабильный комплекс, образуемый восстановленной формой гема с монооксидом углерода в составе цитохрома, имеет максимум поглощения при 450 нм, в то время как, например, для гемоглобина и миоглобнна аналогичный комплекс имеет максимум поглощения при 420 нм. Для NADPH P 450 peдуктазы, донора электронов, специфическими субстратами могут служить: цитохромы P 450, гем оксигеназа (фермент, катализирующий первую стадию деградации гема в билирубин), сквален монооксигеназа (один из ключевых ферментов в каталитическом синтезе стерола), 7 гидрохолестерол редуктаза и цитохром b 5. фермент обладает весьма высоким сродством именно к NADPH в отличие от NADH, которые отличаются единственным фосфорным остатком в положении 2` фуранозного кольца.
В большинстве случаев в первой системе донором электронов служит NADPH, окисляемый NADPH P 450 peдуктазой. Фермент в качестве простетической группы содержит 2 кофермента флавинадениндинуклеотид (FAD) и флавинмононуклеотид (FMN). Протоны и электроны с NADPH переходят последовательно именно на эти коферменты. Восстановленный FMN (FMNH 2) далее окисляется цитохромом Р 450, который получает два электрона Цитохромы Р 450 – семейство микросомальных гемопротеинов, обладающих ярко выраженной монооксидазной активностью и имеющих специфические участки связывания для кислорода и субстрата (ксенобиотика). Вследствие специфики их строения стабильный комплекс, образуемый восстановленной формой гема с монооксидом углерода в составе цитохрома, имеет максимум поглощения при 450 нм, в то время как, например, для гемоглобина и миоглобнна аналогичный комплекс имеет максимум поглощения при 420 нм. Для NADPH P 450 peдуктазы, донора электронов, специфическими субстратами могут служить: цитохромы P 450, гем оксигеназа (фермент, катализирующий первую стадию деградации гема в билирубин), сквален монооксигеназа (один из ключевых ферментов в каталитическом синтезе стерола), 7 гидрохолестерол редуктаза и цитохром b 5. фермент обладает весьма высоким сродством именно к NADPH в отличие от NADH, которые отличаются единственным фосфорным остатком в положении 2` фуранозного кольца.
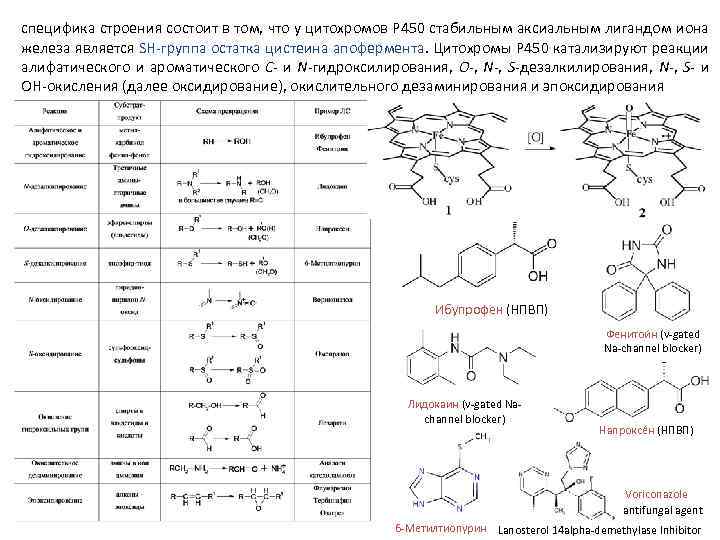 специфика строения состоит в том, что у цитохромов P 450 стабильным аксиальным лигандом иона железа является SН группа остатка цистеина апофермента. Цитохромы P 450 катализируют реакции алифатического и ароматического С и N гидроксилирования, О , N , S дезалкилирования, N , S и OH окисления (далее оксидирование), окислительного дезаминирования и эпоксидирования Ибупрофен (НПВП) Фенитои н (v gated Na channel blocker) Лидокаин (v gated Na channel blocker) Напроксе н (НПВП) Voriconazole antifungal agent 6 Метилтиопурин Lanosterol 14 alpha demethylase Inhibitor
специфика строения состоит в том, что у цитохромов P 450 стабильным аксиальным лигандом иона железа является SН группа остатка цистеина апофермента. Цитохромы P 450 катализируют реакции алифатического и ароматического С и N гидроксилирования, О , N , S дезалкилирования, N , S и OH окисления (далее оксидирование), окислительного дезаминирования и эпоксидирования Ибупрофен (НПВП) Фенитои н (v gated Na channel blocker) Лидокаин (v gated Na channel blocker) Напроксе н (НПВП) Voriconazole antifungal agent 6 Метилтиопурин Lanosterol 14 alpha demethylase Inhibitor
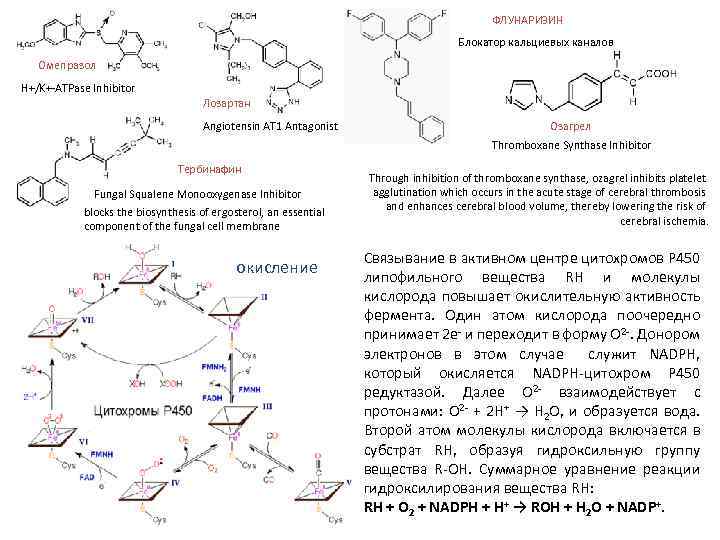 ФЛУНАРИЗИН Блокатор кальциевых каналов Омепразол H+/K+ ATPase Inhibitor Лозартан Angiotensin AT 1 Antagonist Озагрел Thromboxane Synthase Inhibitor Тербинафин Fungal Squalene Monooxygenase Inhibitor blocks the biosynthesis of ergosterol, an essential component of the fungal cell membrane окисление Through inhibition of thromboxane synthase, ozagrel inhibits platelet agglutination which occurs in the acute stage of cerebral thrombosis and enhances cerebral blood volume, thereby lowering the risk of cerebral ischemia. Связывание в активном центре цитохромов Р 450 липофильного вещества RH и молекулы кислорода повышает окислительную активность фермента. Один атом кислорода поочередно принимает 2 e и переходит в форму О 2. Донором электронов в этом случае служит NADPH, который окисляется NADPH цитохром Р 450 редуктазой. Далее О 2 взаимодействует с протонами: О 2 + 2 Н+ → Н 2 О, и образуется вода. Второй атом молекулы кислорода включается в субстрат RH, образуя гидроксильную группу вещества R OH. Суммарное уравнение реакции гидроксилирования вещества RH: RH + O 2 + NADPH + Н+ → ROH + Н 2 O + NADP+.
ФЛУНАРИЗИН Блокатор кальциевых каналов Омепразол H+/K+ ATPase Inhibitor Лозартан Angiotensin AT 1 Antagonist Озагрел Thromboxane Synthase Inhibitor Тербинафин Fungal Squalene Monooxygenase Inhibitor blocks the biosynthesis of ergosterol, an essential component of the fungal cell membrane окисление Through inhibition of thromboxane synthase, ozagrel inhibits platelet agglutination which occurs in the acute stage of cerebral thrombosis and enhances cerebral blood volume, thereby lowering the risk of cerebral ischemia. Связывание в активном центре цитохромов Р 450 липофильного вещества RH и молекулы кислорода повышает окислительную активность фермента. Один атом кислорода поочередно принимает 2 e и переходит в форму О 2. Донором электронов в этом случае служит NADPH, который окисляется NADPH цитохром Р 450 редуктазой. Далее О 2 взаимодействует с протонами: О 2 + 2 Н+ → Н 2 О, и образуется вода. Второй атом молекулы кислорода включается в субстрат RH, образуя гидроксильную группу вещества R OH. Суммарное уравнение реакции гидроксилирования вещества RH: RH + O 2 + NADPH + Н+ → ROH + Н 2 O + NADP+.
 Для реакции дезалкилирования был предложен иной механизм трансформации если гетероатом содержит неподеленную пару электронов, возможны два пути метаболизма субстрата: прямое оксидирование гетероатома, как например в случае пиридинов и пиримидинов, с образованием N оксидов (путь I) или же релокализация радикала на атом углерода метильной группы (в общем случае алкильной) с последующим окислением атом углерода, что приводит к образованию соответствующего спирта и более метаболитически устойчивого вторичного амина (путь II). Субстратами Р 450 могут быть многие гидрофобные вещества как экзогенного (лекарственные препараты, ксенобиотики), так и эндогенного (стероиды, жирные кислоты и др. ) происхождения. Таким образом, в результате первой фазы обезвреживания с участием цитохромов Р 450 происходит модификация веществ с образованием функциональных групп, повышающих растворимость гидрофобного соединения. В результате таких превращений возможна потеря биологической активности молекулы или даже формирование более активного соединения, чем вещество, из которого оно образовалось ►К настоящему времени описано около несколько тысяч генов цитохромов Р 450, кодирующих различные изоформы фермента. Каждая из изоформ Р 450 (среди ферментов микросомального окисления насчитывается более 57 различных изоформ) имеет много субстратов
Для реакции дезалкилирования был предложен иной механизм трансформации если гетероатом содержит неподеленную пару электронов, возможны два пути метаболизма субстрата: прямое оксидирование гетероатома, как например в случае пиридинов и пиримидинов, с образованием N оксидов (путь I) или же релокализация радикала на атом углерода метильной группы (в общем случае алкильной) с последующим окислением атом углерода, что приводит к образованию соответствующего спирта и более метаболитически устойчивого вторичного амина (путь II). Субстратами Р 450 могут быть многие гидрофобные вещества как экзогенного (лекарственные препараты, ксенобиотики), так и эндогенного (стероиды, жирные кислоты и др. ) происхождения. Таким образом, в результате первой фазы обезвреживания с участием цитохромов Р 450 происходит модификация веществ с образованием функциональных групп, повышающих растворимость гидрофобного соединения. В результате таких превращений возможна потеря биологической активности молекулы или даже формирование более активного соединения, чем вещество, из которого оно образовалось ►К настоящему времени описано около несколько тысяч генов цитохромов Р 450, кодирующих различные изоформы фермента. Каждая из изоформ Р 450 (среди ферментов микросомального окисления насчитывается более 57 различных изоформ) имеет много субстратов
 Некоторые изоформы цитохрома Р 450 участвуют в метаболизме низкомолекулярных соединений, таких как этанол и ацетон. Среди всех изоформ цитохрома Р 450 три представителя, CYP 2 D 6, CYP 2 С 9 и CYP 3 А 4, наиболее задействованы в метаболизме ксенобиотиков в организме человека. Среди прочих значимых, но менее задействованных изоформ, можно перечислить CYP 1 А 2, CYP 2 С 19 и CYP 2 Е 1. ►В качестве субстратов для CYP 2 D 6 рассматриваются трициклические антидепрессанты, антагонисты адренорецепторов, представители класса антиаритмических ЛС. Анализ структурного разнообразия субстратов показал, что все они имеют общий топологический фармакофор: основный атом азота на расстоянии 5 7 Ǻ от сайта метаболизма, который включен в планарную ароматическую систему или находится в непосредственной близости от нее. Полагают, что Asp 310 в активном сайте фермента отвечает за связывание основного азота субстрата. Субстратная специфичность CYP 2 D 6 определяется в первую очередь именно этой схемой взаимодействия. ► несмотря на низкое содержание CYP 2 D 6 в клетках печени, взаимодействие его центра связывания с субстратами характеризуется высокими значениями Кb по сравнению с другими цитохромами, что может привести к быстрому насыщению фермента и нежелательным последствиям в случае излишних доз ЛС, как, например, в случае пропафенона, который под действием CYP 2 D 6 переходит в соответствующее 5 гидрокси производное
Некоторые изоформы цитохрома Р 450 участвуют в метаболизме низкомолекулярных соединений, таких как этанол и ацетон. Среди всех изоформ цитохрома Р 450 три представителя, CYP 2 D 6, CYP 2 С 9 и CYP 3 А 4, наиболее задействованы в метаболизме ксенобиотиков в организме человека. Среди прочих значимых, но менее задействованных изоформ, можно перечислить CYP 1 А 2, CYP 2 С 19 и CYP 2 Е 1. ►В качестве субстратов для CYP 2 D 6 рассматриваются трициклические антидепрессанты, антагонисты адренорецепторов, представители класса антиаритмических ЛС. Анализ структурного разнообразия субстратов показал, что все они имеют общий топологический фармакофор: основный атом азота на расстоянии 5 7 Ǻ от сайта метаболизма, который включен в планарную ароматическую систему или находится в непосредственной близости от нее. Полагают, что Asp 310 в активном сайте фермента отвечает за связывание основного азота субстрата. Субстратная специфичность CYP 2 D 6 определяется в первую очередь именно этой схемой взаимодействия. ► несмотря на низкое содержание CYP 2 D 6 в клетках печени, взаимодействие его центра связывания с субстратами характеризуется высокими значениями Кb по сравнению с другими цитохромами, что может привести к быстрому насыщению фермента и нежелательным последствиям в случае излишних доз ЛС, как, например, в случае пропафенона, который под действием CYP 2 D 6 переходит в соответствующее 5 гидрокси производное
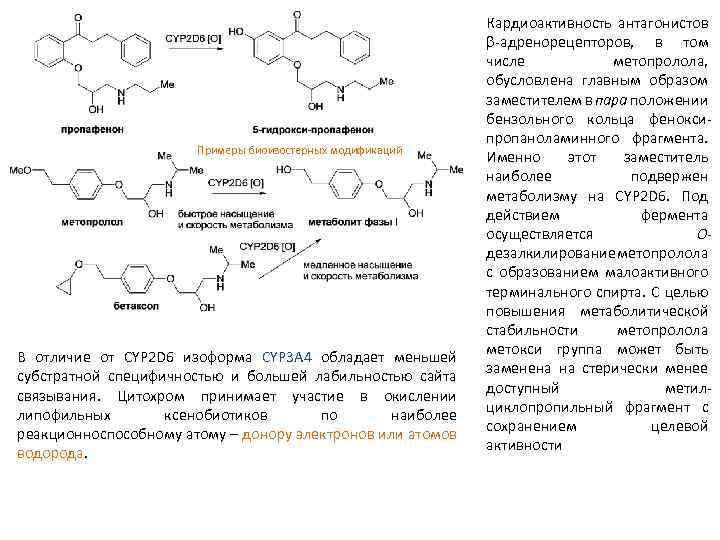 Примеры биоизостерных модификаций В отличие от CYP 2 D 6 изоформа CYP 3 А 4 обладает меньшей субстратной специфичностью и большей лабильностью сайта связывания. Цитохром принимает участие в окислении липофильных ксенобиотиков по наиболее реакционноспособному атому – донору электронов или атомов водорода. Кардиоактивность антагонистов адренорецепторов, в том числе метопролола, обусловлена главным образом заместителем в пара положении бензольного кольца фенокси пропаноламинного фрагмента. Именно этот заместитель наиболее подвержен метаболизму на CYP 2 D 6. Под действием фермента осуществляется O дезалкилирование метопролола с образованием малоактивного терминального спирта. С целью повышения метаболитической стабильности метопролола метокси группа может быть заменена на стерически менее доступный метил циклопропильный фрагмент с сохранением целевой активности
Примеры биоизостерных модификаций В отличие от CYP 2 D 6 изоформа CYP 3 А 4 обладает меньшей субстратной специфичностью и большей лабильностью сайта связывания. Цитохром принимает участие в окислении липофильных ксенобиотиков по наиболее реакционноспособному атому – донору электронов или атомов водорода. Кардиоактивность антагонистов адренорецепторов, в том числе метопролола, обусловлена главным образом заместителем в пара положении бензольного кольца фенокси пропаноламинного фрагмента. Именно этот заместитель наиболее подвержен метаболизму на CYP 2 D 6. Под действием фермента осуществляется O дезалкилирование метопролола с образованием малоактивного терминального спирта. С целью повышения метаболитической стабильности метопролола метокси группа может быть заменена на стерически менее доступный метил циклопропильный фрагмент с сохранением целевой активности
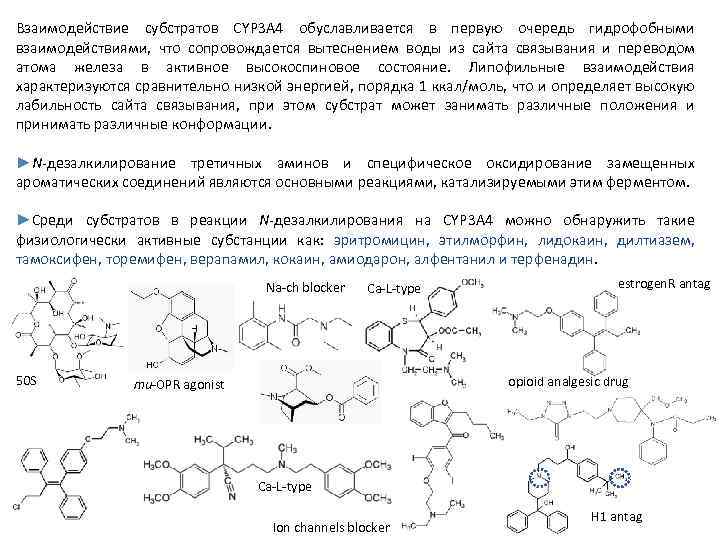 Взаимодействие субстратов CYP 3 А 4 обуславливается в первую очередь гидрофобными взаимодействиями, что сопровождается вытеснением воды из сайта связывания и переводом атома железа в активное высокоспиновое состояние. Липофильные взаимодействия характеризуются сравнительно низкой энергией, порядка 1 ккал/моль, что и определяет высокую лабильность сайта связывания, при этом субстрат может занимать различные положения и принимать различные конформации. ►N дезалкилирование третичных аминов и специфическое оксидирование замещенных ароматических соединений являются основными реакциями, катализируемыми этим ферментом. ►Среди субстратов в реакции N дезалкилирования на CYP 3 А 4 можно обнаружить такие физиологически активные субстанции как: эритромицин, этилморфин, лидокаин, дилтиазем, тамоксифен, торемифен, верапамил, кокаин, амиодарон, алфентанил и терфенадин. Na ch blocker 50 S Ca L type estrogen. R antag opioid analgesic drug mu OPR agonist Ca L type Ion channels blocker H 1 antag
Взаимодействие субстратов CYP 3 А 4 обуславливается в первую очередь гидрофобными взаимодействиями, что сопровождается вытеснением воды из сайта связывания и переводом атома железа в активное высокоспиновое состояние. Липофильные взаимодействия характеризуются сравнительно низкой энергией, порядка 1 ккал/моль, что и определяет высокую лабильность сайта связывания, при этом субстрат может занимать различные положения и принимать различные конформации. ►N дезалкилирование третичных аминов и специфическое оксидирование замещенных ароматических соединений являются основными реакциями, катализируемыми этим ферментом. ►Среди субстратов в реакции N дезалкилирования на CYP 3 А 4 можно обнаружить такие физиологически активные субстанции как: эритромицин, этилморфин, лидокаин, дилтиазем, тамоксифен, торемифен, верапамил, кокаин, амиодарон, алфентанил и терфенадин. Na ch blocker 50 S Ca L type estrogen. R antag opioid analgesic drug mu OPR agonist Ca L type Ion channels blocker H 1 antag
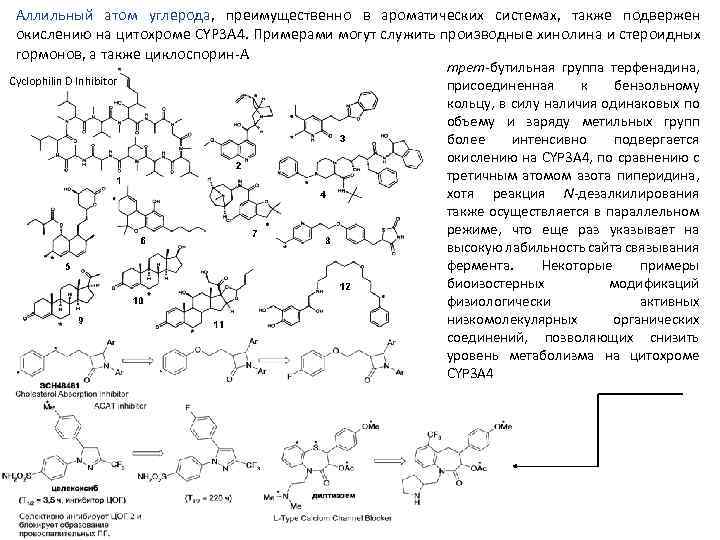 Аллильный атом углерода, преимущественно в ароматических системах, также подвержен окислению на цитохроме CYP 3 А 4. Примерами могут служить производные хинолина и стероидных гормонов, а также циклоспорин А Cyclophilin D Inhibitor трет бутильная группа терфенадина, присоединенная к бензольному кольцу, в силу наличия одинаковых по объему и заряду метильных групп более интенсивно подвергается окислению на CYP 3 А 4, по сравнению с третичным атомом азота пиперидина, хотя реакция N дезалкилирования также осуществляется в параллельном режиме, что еще раз указывает на высокую лабильность сайта связывания фермента. Некоторые примеры биоизостерных модификаций физиологически активных низкомолекулярных органических соединений, позволяющих снизить уровень метаболизма на цитохроме CYP 3 А 4
Аллильный атом углерода, преимущественно в ароматических системах, также подвержен окислению на цитохроме CYP 3 А 4. Примерами могут служить производные хинолина и стероидных гормонов, а также циклоспорин А Cyclophilin D Inhibitor трет бутильная группа терфенадина, присоединенная к бензольному кольцу, в силу наличия одинаковых по объему и заряду метильных групп более интенсивно подвергается окислению на CYP 3 А 4, по сравнению с третичным атомом азота пиперидина, хотя реакция N дезалкилирования также осуществляется в параллельном режиме, что еще раз указывает на высокую лабильность сайта связывания фермента. Некоторые примеры биоизостерных модификаций физиологически активных низкомолекулярных органических соединений, позволяющих снизить уровень метаболизма на цитохроме CYP 3 А 4
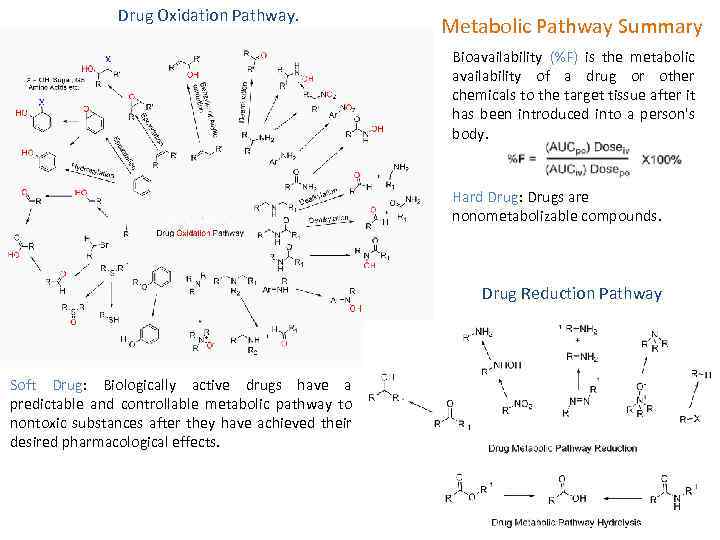 Drug Oxidation Pathway. Metabolic Pathway Summary Bioavailability (%F) is the metabolic availability of a drug or other chemicals to the target tissue after it has been introduced into a person's body. Hard Drug: Drugs are nonometabolizable compounds. Drug Reduction Pathway Soft Drug: Biologically active drugs have a predictable and controllable metabolic pathway to nontoxic substances after they have achieved their desired pharmacological effects.
Drug Oxidation Pathway. Metabolic Pathway Summary Bioavailability (%F) is the metabolic availability of a drug or other chemicals to the target tissue after it has been introduced into a person's body. Hard Drug: Drugs are nonometabolizable compounds. Drug Reduction Pathway Soft Drug: Biologically active drugs have a predictable and controllable metabolic pathway to nontoxic substances after they have achieved their desired pharmacological effects.
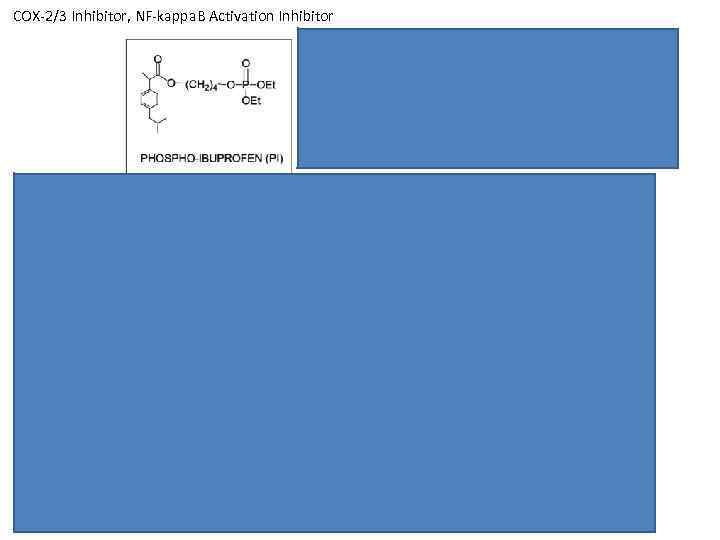 COX 2/3 Inhibitor, NF kappa. B Activation Inhibitor
COX 2/3 Inhibitor, NF kappa. B Activation Inhibitor
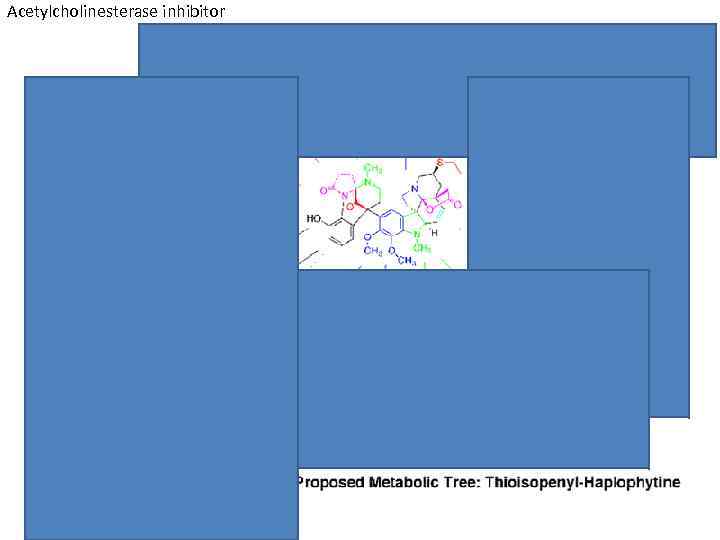 Acetylcholinesterase inhibitor
Acetylcholinesterase inhibitor
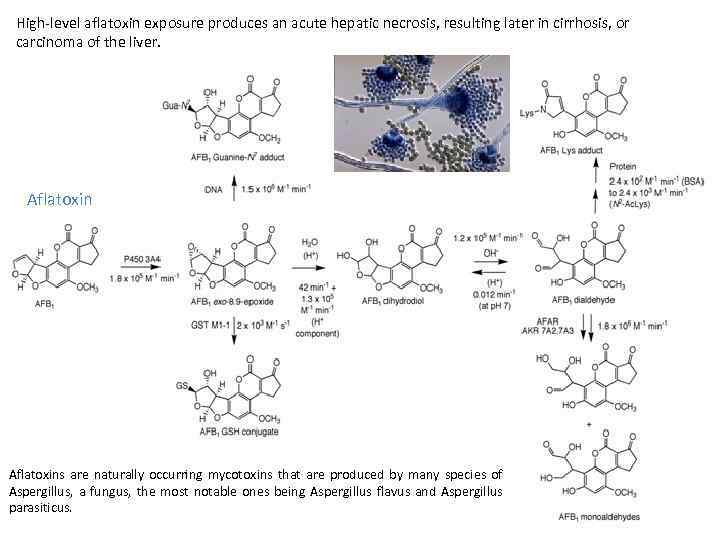 High level aflatoxin exposure produces an acute hepatic necrosis, resulting later in cirrhosis, or carcinoma of the liver. Aflatoxins are naturally occurring mycotoxins that are produced by many species of Aspergillus, a fungus, the most notable ones being Aspergillus flavus and Aspergillus parasiticus.
High level aflatoxin exposure produces an acute hepatic necrosis, resulting later in cirrhosis, or carcinoma of the liver. Aflatoxins are naturally occurring mycotoxins that are produced by many species of Aspergillus, a fungus, the most notable ones being Aspergillus flavus and Aspergillus parasiticus.
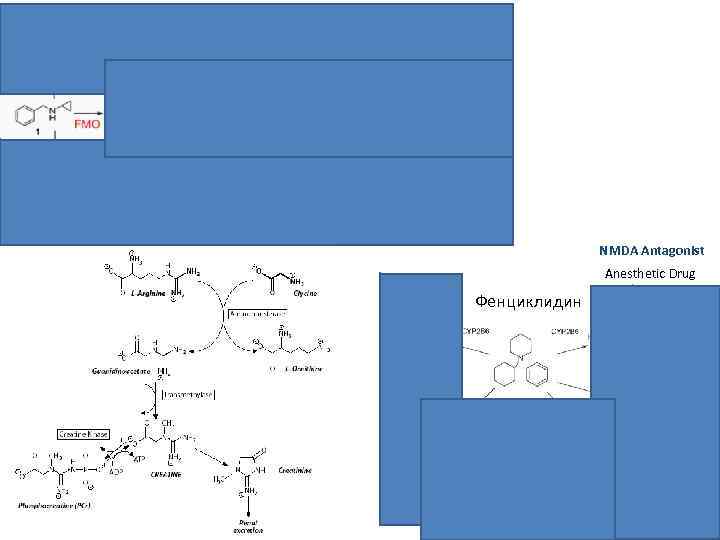 metabolic intermediate complex (MIC) flavin containing monooxygenase (FMO) NMDA Antagonist Anesthetic Drug Фенциклидин
metabolic intermediate complex (MIC) flavin containing monooxygenase (FMO) NMDA Antagonist Anesthetic Drug Фенциклидин
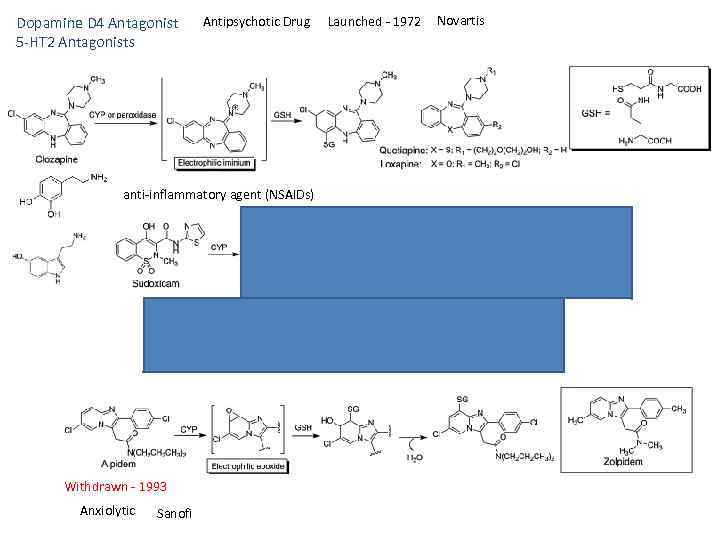 Dopamine D 4 Antagonist 5 HT 2 Antagonists Antipsychotic Drug anti inflammatory agent (NSAIDs) Withdrawn 1993 Anxiolytic Sanofi Launched 1972 Novartis
Dopamine D 4 Antagonist 5 HT 2 Antagonists Antipsychotic Drug anti inflammatory agent (NSAIDs) Withdrawn 1993 Anxiolytic Sanofi Launched 1972 Novartis
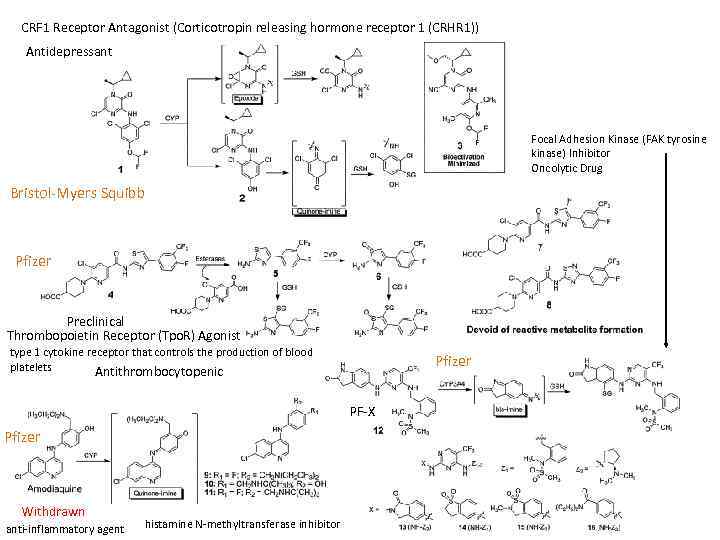 CRF 1 Receptor Antagonist (Corticotropin releasing hormone receptor 1 (CRHR 1)) Antidepressant Focal Adhesion Kinase (FAK tyrosine kinase) Inhibitor Oncolytic Drug Bristol Myers Squibb Pfizer Preclinical Thrombopoietin Receptor (Tpo. R) Agonist type 1 cytokine receptor that controls the production of blood platelets Antithrombocytopenic Pfizer PF X Pfizer Withdrawn anti inflammatory agent histamine N methyltransferase inhibitor
CRF 1 Receptor Antagonist (Corticotropin releasing hormone receptor 1 (CRHR 1)) Antidepressant Focal Adhesion Kinase (FAK tyrosine kinase) Inhibitor Oncolytic Drug Bristol Myers Squibb Pfizer Preclinical Thrombopoietin Receptor (Tpo. R) Agonist type 1 cytokine receptor that controls the production of blood platelets Antithrombocytopenic Pfizer PF X Pfizer Withdrawn anti inflammatory agent histamine N methyltransferase inhibitor
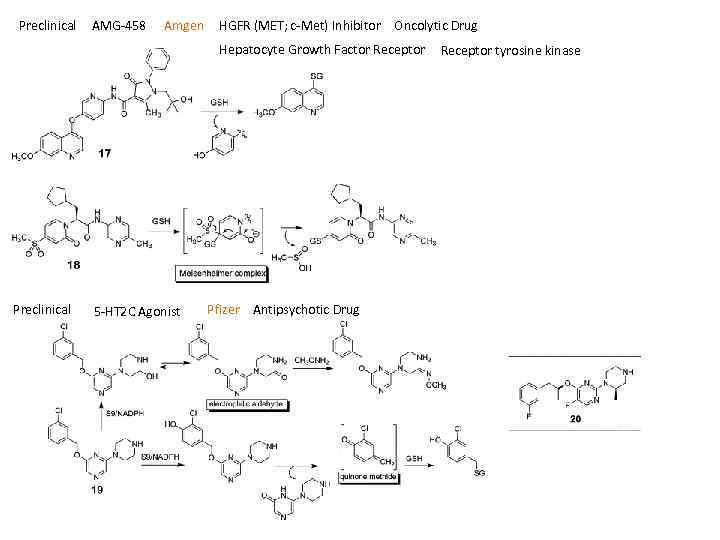 Preclinical AMG 458 Amgen HGFR (MET; c Met) Inhibitor Oncolytic Drug Hepatocyte Growth Factor Receptor Preclinical 5 HT 2 C Agonist Pfizer Antipsychotic Drug Receptor tyrosine kinase
Preclinical AMG 458 Amgen HGFR (MET; c Met) Inhibitor Oncolytic Drug Hepatocyte Growth Factor Receptor Preclinical 5 HT 2 C Agonist Pfizer Antipsychotic Drug Receptor tyrosine kinase
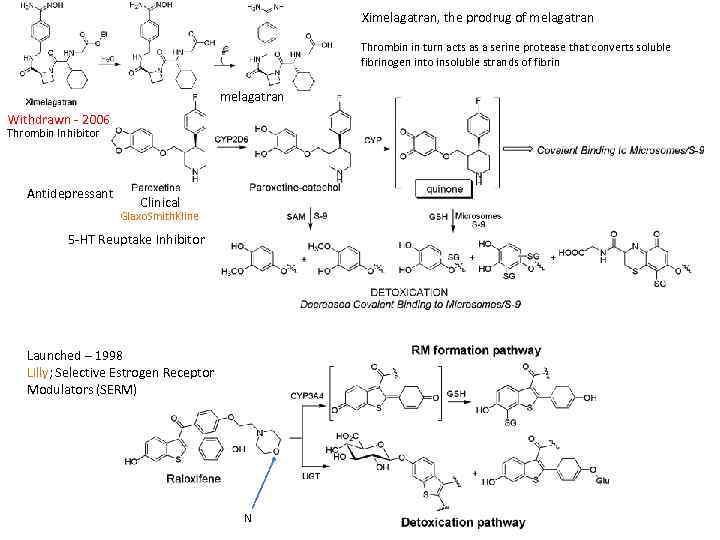 Ximelagatran, the prodrug of melagatran Thrombin in turn acts as a serine protease that converts soluble fibrinogen into insoluble strands of fibrin melagatran Withdrawn 2006 Thrombin Inhibitor Antidepressant Clinical Glaxo. Smith. Kline 5 HT Reuptake Inhibitor Launched – 1998 Lilly; Selective Estrogen Receptor Modulators (SERM) N
Ximelagatran, the prodrug of melagatran Thrombin in turn acts as a serine protease that converts soluble fibrinogen into insoluble strands of fibrin melagatran Withdrawn 2006 Thrombin Inhibitor Antidepressant Clinical Glaxo. Smith. Kline 5 HT Reuptake Inhibitor Launched – 1998 Lilly; Selective Estrogen Receptor Modulators (SERM) N
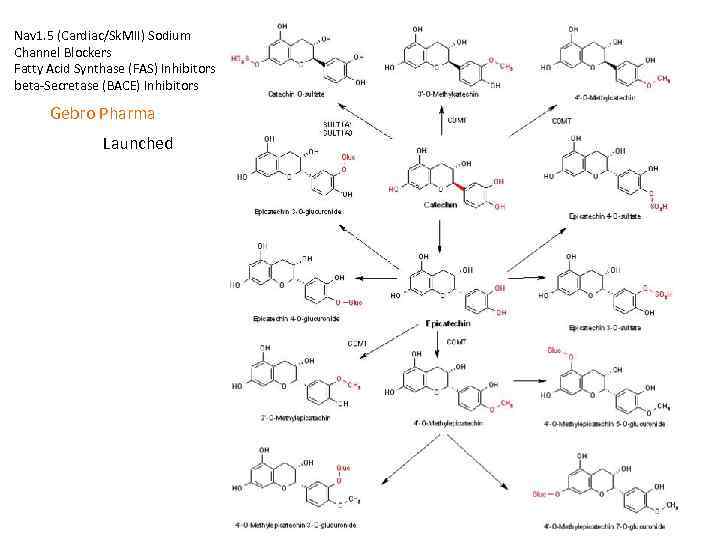 Nav 1. 5 (Cardiac/Sk. MII) Sodium Channel Blockers Fatty Acid Synthase (FAS) Inhibitors beta Secretase (BACE) Inhibitors Gebro Pharma Launched
Nav 1. 5 (Cardiac/Sk. MII) Sodium Channel Blockers Fatty Acid Synthase (FAS) Inhibitors beta Secretase (BACE) Inhibitors Gebro Pharma Launched
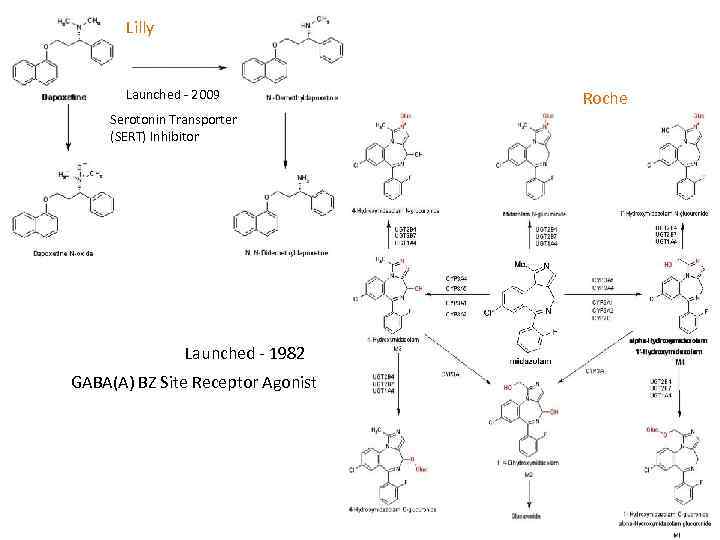 Lilly Launched 2009 Serotonin Transporter (SERT) Inhibitor Launched 1982 GABA(A) BZ Site Receptor Agonist Roche
Lilly Launched 2009 Serotonin Transporter (SERT) Inhibitor Launched 1982 GABA(A) BZ Site Receptor Agonist Roche
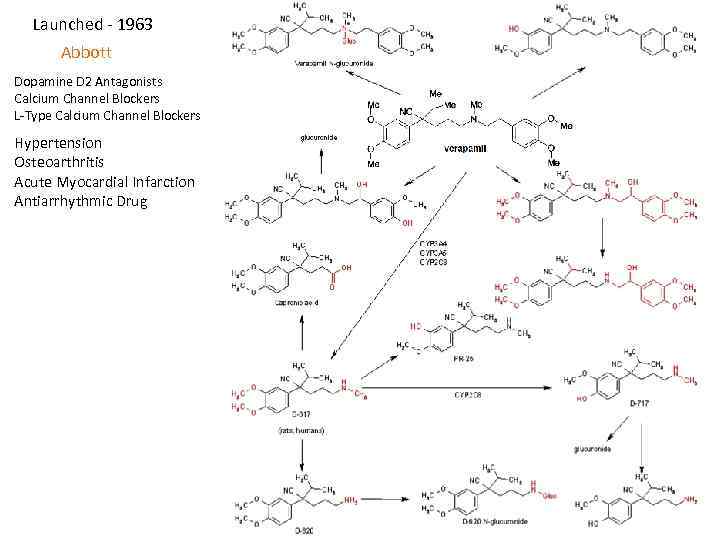 Launched 1963 Abbott Dopamine D 2 Antagonists Calcium Channel Blockers L Type Calcium Channel Blockers Hypertension Osteoarthritis Acute Myocardial Infarction Antiarrhythmic Drug
Launched 1963 Abbott Dopamine D 2 Antagonists Calcium Channel Blockers L Type Calcium Channel Blockers Hypertension Osteoarthritis Acute Myocardial Infarction Antiarrhythmic Drug


