Часть 2 соответствующая химическая чистота












































 Часть 2
Часть 2
 соответствующая химическая чистота соответствующая микробиологическая чистота отсутствие пирогенных веществ Регламентация фармакопейными статьями (ФС, ФСП, НД) с указанием «для инъекций» , «сорт для инъекций» , годен для инъекций» ДОПОЛНИТЕЛЬНАЯ ОЧИСТКА – только на этапе получения веществ или в регламентированных условиях
соответствующая химическая чистота соответствующая микробиологическая чистота отсутствие пирогенных веществ Регламентация фармакопейными статьями (ФС, ФСП, НД) с указанием «для инъекций» , «сорт для инъекций» , годен для инъекций» ДОПОЛНИТЕЛЬНАЯ ОЧИСТКА – только на этапе получения веществ или в регламентированных условиях
 1. Подбор материала упаковки (химическая устойчивое стекло, силиконирование, светозхащитные материалы) 2. Раздельное укупоривание ЛВ и растворителя (Мix-O-vial ) 3. Удаление кислорода из воды - кипячение, барботирование СО 2 (до 890 мгмл), N 2 (15 мг/мл), аргоном (56 мг/мл), гелием (8 мг/мл) 4. «Газовая защита» - остаточный О 2 0, 18 мг/л 1. Добавление антиоксидантов (1 -3 г/л) А) реагирующих со свободными радикалами (аскорбиновая и изоаскорбиновая кислоты, пропилгаллат, гидрохинон фенол, аминофенол, парааминофенол, нафтолы, фенил-алфа-нафтиламин), Б) разрушающих пероксиды (натрия сульфит, натрия метабисульфит, натрия бисульфит, натрия тиосульфат, тиоглицерол, тиосорбит, тиомочевина, тиогликолевая кислота, цистеина гидрохлорид, унитиол, ронгалит), В) Реагирующие с О 2 за счет низкого окислительно-восстановительного потенциала, (аскорбиновая и изоаскорбиновая кислоты, пропилгаллат, гидрохинон, хлорбутанол). Г) жирорастворимые А/О (лецитин, фенил-альфа-нафтиламин, пропилгаллат, кверцетин, производные альфа-токоферола, бутилокситолуол, бутилоксианизол, кислоту нордигидрогваятетовую и их синтетические смеси ) Д) комплексообразователиэтилендиаминтетрауксусная кислота, дигидроксиэтилглицин, лимонная и виннокаменная кислоты, тиомочевина, унитиол
1. Подбор материала упаковки (химическая устойчивое стекло, силиконирование, светозхащитные материалы) 2. Раздельное укупоривание ЛВ и растворителя (Мix-O-vial ) 3. Удаление кислорода из воды - кипячение, барботирование СО 2 (до 890 мгмл), N 2 (15 мг/мл), аргоном (56 мг/мл), гелием (8 мг/мл) 4. «Газовая защита» - остаточный О 2 0, 18 мг/л 1. Добавление антиоксидантов (1 -3 г/л) А) реагирующих со свободными радикалами (аскорбиновая и изоаскорбиновая кислоты, пропилгаллат, гидрохинон фенол, аминофенол, парааминофенол, нафтолы, фенил-алфа-нафтиламин), Б) разрушающих пероксиды (натрия сульфит, натрия метабисульфит, натрия бисульфит, натрия тиосульфат, тиоглицерол, тиосорбит, тиомочевина, тиогликолевая кислота, цистеина гидрохлорид, унитиол, ронгалит), В) Реагирующие с О 2 за счет низкого окислительно-восстановительного потенциала, (аскорбиновая и изоаскорбиновая кислоты, пропилгаллат, гидрохинон, хлорбутанол). Г) жирорастворимые А/О (лецитин, фенил-альфа-нафтиламин, пропилгаллат, кверцетин, производные альфа-токоферола, бутилокситолуол, бутилоксианизол, кислоту нордигидрогваятетовую и их синтетические смеси ) Д) комплексообразователиэтилендиаминтетрауксусная кислота, дигидроксиэтилглицин, лимонная и виннокаменная кислоты, тиомочевина, унитиол
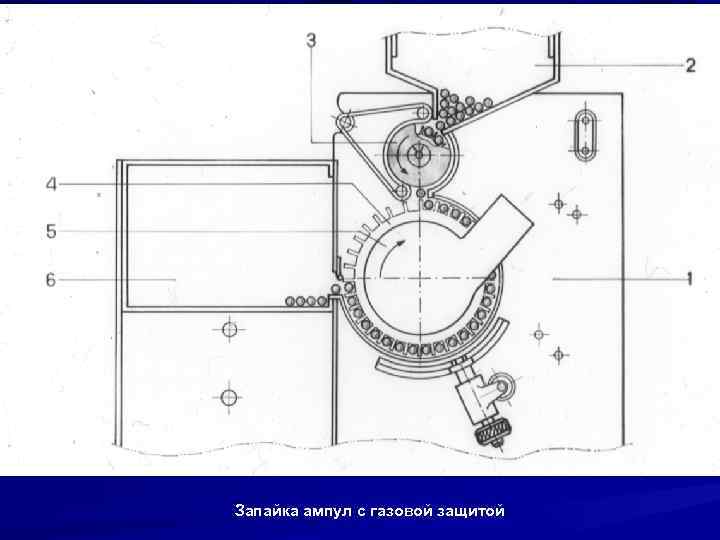
 Запайка ампул с газовой защитой
Запайка ампул с газовой защитой
 1. Добавление ПАВ (твин-80, аминопропиленгликоль, полиэтиленгликоль) - неионогенные и анионактивные ПАВ тормозят, а катионактивные ускоряют процесс гидролиза Механизм: образование мицелло-ассоциатов молекул ПАВ 2. Стабилизация растворов солей слабых кислот и сильных оснований - растворы натрия тиосульфата, никотиновой кислоты, кофеин-бензоата натрия, натрия нитрита. 3. Стабилизация растворов солей, образованных слабыми основаниями и сильными кислотами - растворы морфина гидрохлорида, новокаина, атропина сульфата, дибазола и др. 4. Стабилизация растворов глюкозы (реактив Вейбеля) 5. Добавление консервантов Требования к консервантам : ► фармакологическая индифферентность в используемой концентрации; ► широкий антимикробный спектр; ► отсутствие влияния на органолептические свойства ЛС; ► отсутствие химического взаимодействия с лекарственными и ЛВ; ► устойчивость при хранении; ► сохранение стерильности ЛС в течение длительного времени их применения
1. Добавление ПАВ (твин-80, аминопропиленгликоль, полиэтиленгликоль) - неионогенные и анионактивные ПАВ тормозят, а катионактивные ускоряют процесс гидролиза Механизм: образование мицелло-ассоциатов молекул ПАВ 2. Стабилизация растворов солей слабых кислот и сильных оснований - растворы натрия тиосульфата, никотиновой кислоты, кофеин-бензоата натрия, натрия нитрита. 3. Стабилизация растворов солей, образованных слабыми основаниями и сильными кислотами - растворы морфина гидрохлорида, новокаина, атропина сульфата, дибазола и др. 4. Стабилизация растворов глюкозы (реактив Вейбеля) 5. Добавление консервантов Требования к консервантам : ► фармакологическая индифферентность в используемой концентрации; ► широкий антимикробный спектр; ► отсутствие влияния на органолептические свойства ЛС; ► отсутствие химического взаимодействия с лекарственными и ЛВ; ► устойчивость при хранении; ► сохранение стерильности ЛС в течение длительного времени их применения
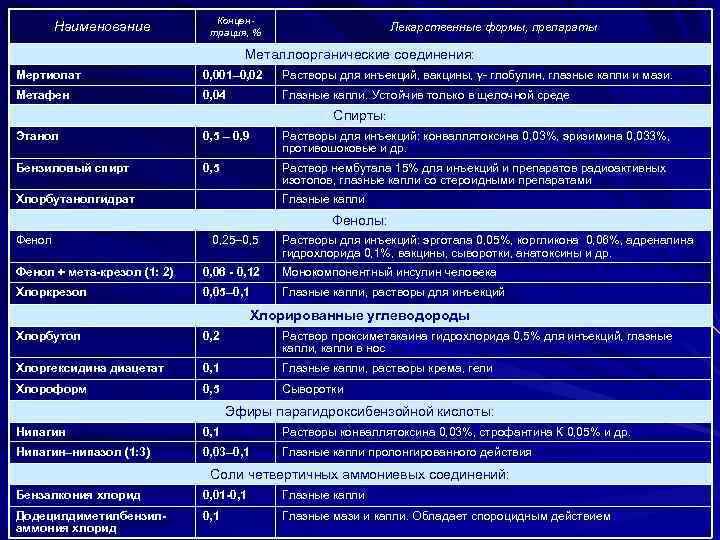
 Концен- Наименование трация, % Лекарственные формы, препараты Металлоорганические соединения: Мертиолат 0, 001– 0, 02 Растворы для инъекций, вакцины, γ- глобулин, глазные капли и мази. Метафен 0, 04 Глазные капли. Устойчив только в щелочной среде Спирты: Этанол 0, 5 – 0, 9 Растворы для инъекций: конваллятоксина 0, 03%, эризимина 0, 033%, противошоковые и др. Бензиловый спирт 0, 5 Раствор нембутала 15% для инъекций и препаратов радиоактивных изотопов, глазные капли со стероидными препаратами Хлорбутанолгидрат Глазные капли Фенолы: Фенол 0, 25– 0, 5 Растворы для инъекций: эрготала 0, 05%, коргликона 0, 06%, адреналина гидрохлорида 0, 1%, вакцины, сыворотки, анатоксины и др. Фенол + мета-крезол (1: 2) 0, 06 - 0, 12 Монокомпонентный инсулин человека Хлоркрезол 0, 05– 0, 1 Глазные капли, растворы для инъекций Хлорированные углеводороды Хлорбутол 0, 2 Раствор проксиметакаина гидрохлорида 0, 5% для инъекций, глазные капли, капли в нос Хлоргексидина диацетат 0, 1 Глазные капли, растворы крема, гели Хлороформ 0, 5 Сыворотки Эфиры парагидроксибензойной кислоты: Нипагин 0, 1 Растворы конваллятоксина 0, 03%, строфантина К 0, 05% и др. Нипагин–нипазол (1: 3) 0, 03– 0, 1 Глазные капли пролонгированного действия Соли четвертичных аммониевых соединений: Бензалкония хлорид 0, 01 -0, 1 Глазные капли Додецилдиметилбензил- 0, 1 Глазные мази и капли. Обладает спороцидным действием аммония хлорид
Концен- Наименование трация, % Лекарственные формы, препараты Металлоорганические соединения: Мертиолат 0, 001– 0, 02 Растворы для инъекций, вакцины, γ- глобулин, глазные капли и мази. Метафен 0, 04 Глазные капли. Устойчив только в щелочной среде Спирты: Этанол 0, 5 – 0, 9 Растворы для инъекций: конваллятоксина 0, 03%, эризимина 0, 033%, противошоковые и др. Бензиловый спирт 0, 5 Раствор нембутала 15% для инъекций и препаратов радиоактивных изотопов, глазные капли со стероидными препаратами Хлорбутанолгидрат Глазные капли Фенолы: Фенол 0, 25– 0, 5 Растворы для инъекций: эрготала 0, 05%, коргликона 0, 06%, адреналина гидрохлорида 0, 1%, вакцины, сыворотки, анатоксины и др. Фенол + мета-крезол (1: 2) 0, 06 - 0, 12 Монокомпонентный инсулин человека Хлоркрезол 0, 05– 0, 1 Глазные капли, растворы для инъекций Хлорированные углеводороды Хлорбутол 0, 2 Раствор проксиметакаина гидрохлорида 0, 5% для инъекций, глазные капли, капли в нос Хлоргексидина диацетат 0, 1 Глазные капли, растворы крема, гели Хлороформ 0, 5 Сыворотки Эфиры парагидроксибензойной кислоты: Нипагин 0, 1 Растворы конваллятоксина 0, 03%, строфантина К 0, 05% и др. Нипагин–нипазол (1: 3) 0, 03– 0, 1 Глазные капли пролонгированного действия Соли четвертичных аммониевых соединений: Бензалкония хлорид 0, 01 -0, 1 Глазные капли Додецилдиметилбензил- 0, 1 Глазные мази и капли. Обладает спороцидным действием аммония хлорид
 Осмотическая концентрация (более 50% постинънекционных осложнений) Гиперосмотические 1100 -3125 ммоль/л Пирогенные вещества р. Н (около 30% гнойно-воспалительных осложнений) ПОЛ (кислород) образование суперокид радикалов→разрушение мембран лизосом→выход гидролаз ОВП ─ окислительно-восстановительный потенциал. Оптимум -60 ─ -10 м. В, Осложнения: +10 ─ +50 м. В, ниже – 70 м. В
Осмотическая концентрация (более 50% постинънекционных осложнений) Гиперосмотические 1100 -3125 ммоль/л Пирогенные вещества р. Н (около 30% гнойно-воспалительных осложнений) ПОЛ (кислород) образование суперокид радикалов→разрушение мембран лизосом→выход гидролаз ОВП ─ окислительно-восстановительный потенциал. Оптимум -60 ─ -10 м. В, Осложнения: +10 ─ +50 м. В, ниже – 70 м. В
 ТРЕБОВАНИЯ 1. Материал и фильтр - максимальная защита раствора от контакта с воздухом 2. Эффективная задержка мелких частиц и микроорганизмов 3. Достаточная скорость фильтрации и приемлемый режим "забивания фильтров". 4. Высокая механическая прочность, противодействие гидравлическим ударам с сохранением функциональных характеристик 5. Индифферентнность к ЛВ и растворителю и способность материала фильтра выдерживать контакт с жидкой средой без изменений показателей его структуры; 6. Не изменять фильтрат (отсутствие выделения из мембраны в препараты токсичных веществ и веществ, способных изменить показатели препарата); 7. Стерилизуемость (вместе с оборудованием); 8. Безопасность для оператора, работающего с фильтром (например, отсутствие стекловолокнистых материалов) 9. Хорошие эргономические и экономические показатели.
ТРЕБОВАНИЯ 1. Материал и фильтр - максимальная защита раствора от контакта с воздухом 2. Эффективная задержка мелких частиц и микроорганизмов 3. Достаточная скорость фильтрации и приемлемый режим "забивания фильтров". 4. Высокая механическая прочность, противодействие гидравлическим ударам с сохранением функциональных характеристик 5. Индифферентнность к ЛВ и растворителю и способность материала фильтра выдерживать контакт с жидкой средой без изменений показателей его структуры; 6. Не изменять фильтрат (отсутствие выделения из мембраны в препараты токсичных веществ и веществ, способных изменить показатели препарата); 7. Стерилизуемость (вместе с оборудованием); 8. Безопасность для оператора, работающего с фильтром (например, отсутствие стекловолокнистых материалов) 9. Хорошие эргономические и экономические показатели.
 Q – объём вытекающей жидкости в м 3; F – поверхность фильтра, м 2; z – число капилляров на 1 м 2; r – средний радиус капилляров, м; P – разность давления по обе стороны фильтрующей перегородки в H/м 2; τ – время фильтрования, с; η – абсолютная вязкость фильтрата в Н/(с*м 2); l – средняя длина капилляров, м. Ресурс фильтра прямо пропорционален площади фильтрации прочих равных условиях пропорционален площади фильтрации (механизм забивания пор), пропорционален квадрату площади фильтрации (механизм накопления осадка без забивания пор). Ресурс комплекта глубинных фильтрующих элементов пропорционален квадрату площади фильтрации, т. е. при увеличении количества элементов в два раза ресурс комплекта увеличивается примерно в 4 раза.
Q – объём вытекающей жидкости в м 3; F – поверхность фильтра, м 2; z – число капилляров на 1 м 2; r – средний радиус капилляров, м; P – разность давления по обе стороны фильтрующей перегородки в H/м 2; τ – время фильтрования, с; η – абсолютная вязкость фильтрата в Н/(с*м 2); l – средняя длина капилляров, м. Ресурс фильтра прямо пропорционален площади фильтрации прочих равных условиях пропорционален площади фильтрации (механизм забивания пор), пропорционален квадрату площади фильтрации (механизм накопления осадка без забивания пор). Ресурс комплекта глубинных фильтрующих элементов пропорционален квадрату площади фильтрации, т. е. при увеличении количества элементов в два раза ресурс комплекта увеличивается примерно в 4 раза.
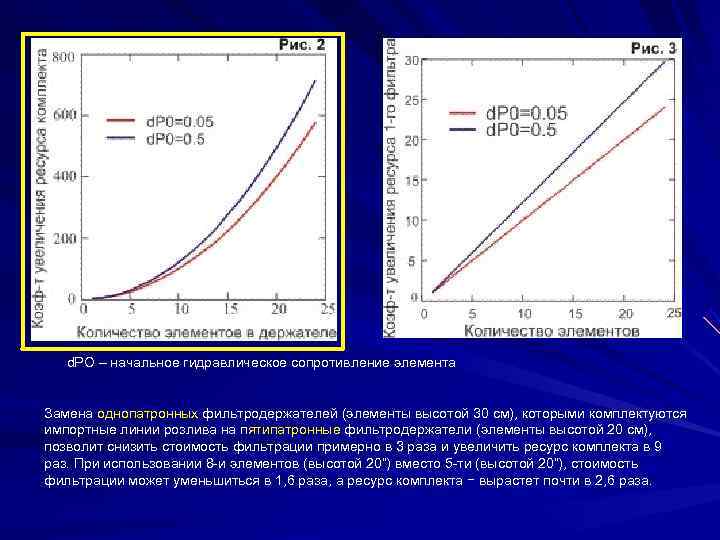
 d. PO – начальное гидравлическое сопротивление элемента Замена однопатронных фильтродержателей (элементы высотой 30 см), которыми комплектуются импортные линии розлива на пятипатронные фильтродержатели (элементы высотой 20 см), позволит снизить стоимость фильтрации примерно в 3 раза и увеличить ресурс комплекта в 9 раз. При использовании 8 -и элементов (высотой 20”) вместо 5 -ти (высотой 20”), стоимость фильтрации может уменьшиться в 1, 6 раза, а ресурс комплекта − вырастет почти в 2, 6 раза.
d. PO – начальное гидравлическое сопротивление элемента Замена однопатронных фильтродержателей (элементы высотой 30 см), которыми комплектуются импортные линии розлива на пятипатронные фильтродержатели (элементы высотой 20 см), позволит снизить стоимость фильтрации примерно в 3 раза и увеличить ресурс комплекта в 9 раз. При использовании 8 -и элементов (высотой 20”) вместо 5 -ти (высотой 20”), стоимость фильтрации может уменьшиться в 1, 6 раза, а ресурс комплекта − вырастет почти в 2, 6 раза.
 бумага, вата, ткани (марля, фланель, бязь, сукно, специальная фильтрующая ткань – бельтинг, шелк, капрон, ФПП, лавсан, миткаль), стеклянные и керамические плитки (Диатомит, перлит, фарфор), густые металлические сетки МФА (ацетат целлюлозы, диаметр пор 0, 22 мкм и 0, 45 мкм) - мембраны "Владипор" ММК (мембраны микропористые капроновые - алифатические полиамиды (nylon-6 и nylon-66)) диаметр пор 0, 1 мкм - 3 мкм), МФЦ - мембраны "Владипор" HAWP (смесь нитрата и ацетата целлюлозы, диаметр пор 0, 45 мкм), GSWP (смесь нитрата и ацетата целлюлозы, диаметр пор 0, 22 мкм), GVWP (поливинилиденфторид, диаметр пор 0, 22 мкм и 0, 45 мкм Фильтры ячейкового типа ФЯВ, ФЯП, ФЯРТУ 22 -3193 -75 Фильтры сухие рулонные типа ФРП, ФРУТУ РСФСР 17 -2803 -69 Фильтры ячейковые типа ЛАИК, ФЯЛ, 4 ФТУ 64 -1 -2123 -77 Фильтр АФА-ВП-10 ОСТ 9510052 -84
бумага, вата, ткани (марля, фланель, бязь, сукно, специальная фильтрующая ткань – бельтинг, шелк, капрон, ФПП, лавсан, миткаль), стеклянные и керамические плитки (Диатомит, перлит, фарфор), густые металлические сетки МФА (ацетат целлюлозы, диаметр пор 0, 22 мкм и 0, 45 мкм) - мембраны "Владипор" ММК (мембраны микропористые капроновые - алифатические полиамиды (nylon-6 и nylon-66)) диаметр пор 0, 1 мкм - 3 мкм), МФЦ - мембраны "Владипор" HAWP (смесь нитрата и ацетата целлюлозы, диаметр пор 0, 45 мкм), GSWP (смесь нитрата и ацетата целлюлозы, диаметр пор 0, 22 мкм), GVWP (поливинилиденфторид, диаметр пор 0, 22 мкм и 0, 45 мкм Фильтры ячейкового типа ФЯВ, ФЯП, ФЯРТУ 22 -3193 -75 Фильтры сухие рулонные типа ФРП, ФРУТУ РСФСР 17 -2803 -69 Фильтры ячейковые типа ЛАИК, ФЯЛ, 4 ФТУ 64 -1 -2123 -77 Фильтр АФА-ВП-10 ОСТ 9510052 -84
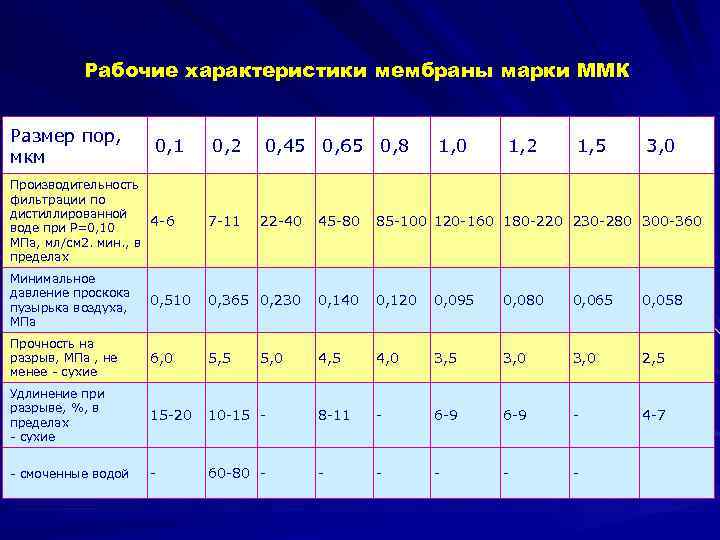
 Рабочие характеристики мембраны марки ММК Размер пор, 0, 1 0, 2 0, 45 0, 65 0, 8 1, 0 1, 2 1, 5 3, 0 мкм Производительность фильтрации по дистиллированной воде при Р=0, 10 4 -6 7 -11 22 -40 45 -80 85 -100 120 -160 180 -220 230 -280 300 -360 МПа, мл/см 2. мин. , в пределах Минимальное давление проскока пузырька воздуха, 0, 510 0, 365 0, 230 0, 140 0, 120 0, 095 0, 080 0, 065 0, 058 МПа Прочность на разрыв, МПа , не 6, 0 5, 5 5, 0 4, 5 4, 0 3, 5 3, 0 2, 5 менее - сухие Удлинение при разрыве, %, в пределах 15 -20 10 -15 - 8 -11 - 6 -9 - 4 -7 - сухие - смоченные водой - 60 -80 - - -
Рабочие характеристики мембраны марки ММК Размер пор, 0, 1 0, 2 0, 45 0, 65 0, 8 1, 0 1, 2 1, 5 3, 0 мкм Производительность фильтрации по дистиллированной воде при Р=0, 10 4 -6 7 -11 22 -40 45 -80 85 -100 120 -160 180 -220 230 -280 300 -360 МПа, мл/см 2. мин. , в пределах Минимальное давление проскока пузырька воздуха, 0, 510 0, 365 0, 230 0, 140 0, 120 0, 095 0, 080 0, 065 0, 058 МПа Прочность на разрыв, МПа , не 6, 0 5, 5 5, 0 4, 5 4, 0 3, 5 3, 0 2, 5 менее - сухие Удлинение при разрыве, %, в пределах 15 -20 10 -15 - 8 -11 - 6 -9 - 4 -7 - сухие - смоченные водой - 60 -80 - - -
 Механизм фильтрования: Механизм фильтрования: • ситовой, • ситовой • адсорбционный, • инерционный. Ø точный размер пор - абсолютная маркировка Ø меньшая склонность к забиванию, мембраны. особенно если размеры пор Ø задержка бактерий не зависит от скорости мембраны близки к размерам частиц потока фильтруемой жидкости и перепада фильтруемой жидкости. давления; Ø исключена возможность отслаивания Ø меньшая чувствительность к материала мембраны и попадания его в тепловому воздействию при фильтрат; стерилизации. Ø практически не удерживается фильтруемая Ø более высокая пропускная жидкость; способность, так что их приходится Ø могут подвергаться проверке на целостность заменять более часто. Более методом «точки пузырька» как до начала, так высокая эффективность задержки и после проведения процесса. частиц и м/о Ø как правило, не требуют промывки и выщелачивания.
Механизм фильтрования: Механизм фильтрования: • ситовой, • ситовой • адсорбционный, • инерционный. Ø точный размер пор - абсолютная маркировка Ø меньшая склонность к забиванию, мембраны. особенно если размеры пор Ø задержка бактерий не зависит от скорости мембраны близки к размерам частиц потока фильтруемой жидкости и перепада фильтруемой жидкости. давления; Ø исключена возможность отслаивания Ø меньшая чувствительность к материала мембраны и попадания его в тепловому воздействию при фильтрат; стерилизации. Ø практически не удерживается фильтруемая Ø более высокая пропускная жидкость; способность, так что их приходится Ø могут подвергаться проверке на целостность заменять более часто. Более методом «точки пузырька» как до начала, так высокая эффективность задержки и после проведения процесса. частиц и м/о Ø как правило, не требуют промывки и выщелачивания.
 1 - формование из раствора (фазоинверсионные методы) испарением растворителя (сухое формование); заменой растворителя на нерастворитель при диффузии последнего из паровой фазы. (политую пленку выдерживают в атмосфере паров растворителя и нерастворителя); заменой растворителя на нерастворитель при диффузии последнего из жидкой фазы -политую пленку погружают в жидкую фазу нерастворителя (мокрое формование). 2 - формование из расплава; 3 - вымывание наполнителя; 4 - выщелачивание (растворение) части полимера; 5 - получение новых свойств путем химической модификации готовых мембран; 6 - спекание порошков 7 - растягивания пленки (волокнистые)
1 - формование из раствора (фазоинверсионные методы) испарением растворителя (сухое формование); заменой растворителя на нерастворитель при диффузии последнего из паровой фазы. (политую пленку выдерживают в атмосфере паров растворителя и нерастворителя); заменой растворителя на нерастворитель при диффузии последнего из жидкой фазы -политую пленку погружают в жидкую фазу нерастворителя (мокрое формование). 2 - формование из расплава; 3 - вымывание наполнителя; 4 - выщелачивание (растворение) части полимера; 5 - получение новых свойств путем химической модификации готовых мембран; 6 - спекание порошков 7 - растягивания пленки (волокнистые)
 МФ-мембраны полученные сухим формованием: ацетат целлюлозы нитроцеллюлоза Тефлоновые мембраны, полученные растяжением пленки
МФ-мембраны полученные сухим формованием: ацетат целлюлозы нитроцеллюлоза Тефлоновые мембраны, полученные растяжением пленки
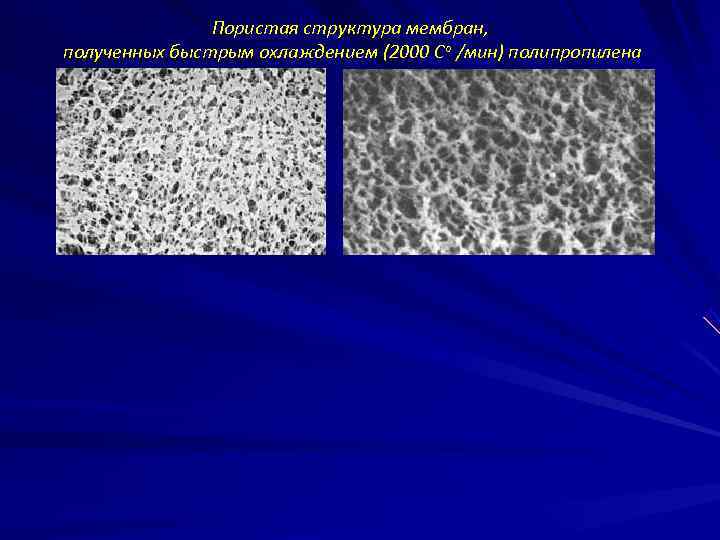
 Пористая структура мембран, полученных быстрым охлаждением (2000 Со /мин) полипропилена
Пористая структура мембран, полученных быстрым охлаждением (2000 Со /мин) полипропилена
 Влияние молекулярной массы полимера на свойства и структуру мембран полиэфирсульфон нейлон
Влияние молекулярной массы полимера на свойства и структуру мембран полиэфирсульфон нейлон
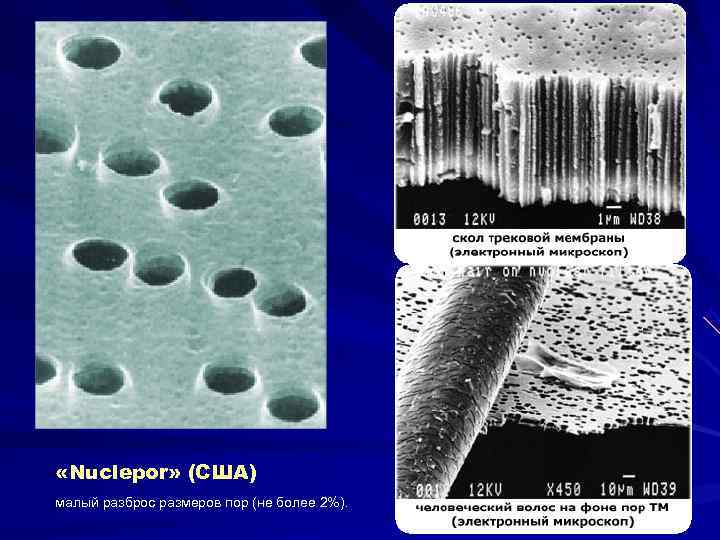
 трековые, ядерные мембраны ◙ облучения полимерных пленочных материалов ускоренными на циклотроне тяжелыми ионами или осколками деления (аргоном, криптоном, ксеноном) и последующая обработк а. УФ светом и травление в щелочи при заданной температуре. Сквозное отверстие – пора цилиндрической формы, диаметр которой прямо пропорционален времени травления (от сотых долей микрона до нескольких микрон (для сравнения: толщина человеческого волоса – 50 микрон). Диаметры всех пор оказываются совершенно одинаковыми. В зависимости от требуемого размера пор их плотность на мембране - от сотен тысяч до нескольких миллиардов на 1 см 2. 1 - источник ядерного излучения; 2 -бобины с пленкой; 3 -источник ультрафиолетового излучения; 4 - узел окисления; 5 -узел травления; 6 - аппарат для промывки; 7 -сушильное устройство; 8 - бобина с мембраной.
трековые, ядерные мембраны ◙ облучения полимерных пленочных материалов ускоренными на циклотроне тяжелыми ионами или осколками деления (аргоном, криптоном, ксеноном) и последующая обработк а. УФ светом и травление в щелочи при заданной температуре. Сквозное отверстие – пора цилиндрической формы, диаметр которой прямо пропорционален времени травления (от сотых долей микрона до нескольких микрон (для сравнения: толщина человеческого волоса – 50 микрон). Диаметры всех пор оказываются совершенно одинаковыми. В зависимости от требуемого размера пор их плотность на мембране - от сотен тысяч до нескольких миллиардов на 1 см 2. 1 - источник ядерного излучения; 2 -бобины с пленкой; 3 -источник ультрафиолетового излучения; 4 - узел окисления; 5 -узел травления; 6 - аппарат для промывки; 7 -сушильное устройство; 8 - бобина с мембраной.
 «Nuclepor» (США) малый разброс размеров пор (не более 2%).
«Nuclepor» (США) малый разброс размеров пор (не более 2%).
 Дисковые фильтры (мембраны)
Дисковые фильтры (мембраны)
 Ресурс и производительность фильтра ─ предотвращение образования осадка на мембране и забивания пор 1. Создание псевдоожиженного слоя над поверхностью фильтра (полистирольные или стеклянные шарики с диаметром 0, 3 -0, 7 мм) ─ проницаемость фильтра возрастает в 2 раза. 2. Создание тангенциального потока у поверхности фильтра ( за счёт вращения фильтрующего элемента). 3. Флокуляция микрочастиц (за счет наличия электрических зарядов на поверхности частиц) 4. Применение ультразвука. Методы очистки мембран 1. Промывка не менее 3 раз в умеренно кипящей воде, кипятят в 3% растворе HCl 5 -7 раз, трижды кипящей деминерализованной водой до отсутствия следов кислоты (индикатор бромкрезоловый синий). 2. Стерилизация Термическая стерилизация при 121 С, в количестве до 15 штук. Каждую мембрану рекомендуется положить между двумя кусками фильтровальной бумаги и обвернуть всю упаковку. Мембраны из тефлона ─ сухим воздухом при 180 С в течение 2 часов. Химическая стерилизация (окисью этилена). Стерилизация формальдегидом (24 часа в 2% растворе с последующим удалением его и промыванием водой для инъекций) Радиационная стерилизация УФ облучением. Проводится с обеих сторон стандартной бактерицидной лампой с расстояния 50 см в течение 30 минут.
Ресурс и производительность фильтра ─ предотвращение образования осадка на мембране и забивания пор 1. Создание псевдоожиженного слоя над поверхностью фильтра (полистирольные или стеклянные шарики с диаметром 0, 3 -0, 7 мм) ─ проницаемость фильтра возрастает в 2 раза. 2. Создание тангенциального потока у поверхности фильтра ( за счёт вращения фильтрующего элемента). 3. Флокуляция микрочастиц (за счет наличия электрических зарядов на поверхности частиц) 4. Применение ультразвука. Методы очистки мембран 1. Промывка не менее 3 раз в умеренно кипящей воде, кипятят в 3% растворе HCl 5 -7 раз, трижды кипящей деминерализованной водой до отсутствия следов кислоты (индикатор бромкрезоловый синий). 2. Стерилизация Термическая стерилизация при 121 С, в количестве до 15 штук. Каждую мембрану рекомендуется положить между двумя кусками фильтровальной бумаги и обвернуть всю упаковку. Мембраны из тефлона ─ сухим воздухом при 180 С в течение 2 часов. Химическая стерилизация (окисью этилена). Стерилизация формальдегидом (24 часа в 2% растворе с последующим удалением его и промыванием водой для инъекций) Радиационная стерилизация УФ облучением. Проводится с обеих сторон стандартной бактерицидной лампой с расстояния 50 см в течение 30 минут.
 Недостатки дисковых фильтродержателей: § Высокие эксплуатационные затраты; § Опасность внесения загрязнения внутрь фильтродержателя; § Отдельные мембраны не испытывают предварительно на целостность; § Требуют большого рабочего пространства, громоздкие в обращении; Достоинства капсульных фильтр-патронов: § Экономичность; § Отсутствие опасности загрязнений; § Компактность; § Не требуется автоклавирование; § Отсутствие деталей, требующих очистки; мембранные патронные элементы марки ЭПМ (НПП «Технофильтр» ) аналоги элементов Ultipor и Nylaflo фирмы Pall, Sartolon фирмы Sartorius AG
Недостатки дисковых фильтродержателей: § Высокие эксплуатационные затраты; § Опасность внесения загрязнения внутрь фильтродержателя; § Отдельные мембраны не испытывают предварительно на целостность; § Требуют большого рабочего пространства, громоздкие в обращении; Достоинства капсульных фильтр-патронов: § Экономичность; § Отсутствие опасности загрязнений; § Компактность; § Не требуется автоклавирование; § Отсутствие деталей, требующих очистки; мембранные патронные элементы марки ЭПМ (НПП «Технофильтр» ) аналоги элементов Ultipor и Nylaflo фирмы Pall, Sartolon фирмы Sartorius AG
 1. Гофрированная мембрана в один или два слоя, расположенная между двумя слоями нетканого полипропиленового волокна. Мембрана обеспечивает эффективную площадь фильтрации. 2. Адаптер "Д", диаметр=56, 0 мм ("А" или "B") байонетного типа с двумя уплотнительными кольцами из пищевой или силиконовой резины (для агрессивных сред - из фторкаучука). Адаптер обеспечивает герметичность установки фильтроэлемента в держатель. 3. Внутрений перфорированный опорный корпус обеспечивает механическую прочность. 4. Внешний перфорированный опорный корпус защищает от механических повреждений. 5. Заглушка хвостового (дискового) типа.
1. Гофрированная мембрана в один или два слоя, расположенная между двумя слоями нетканого полипропиленового волокна. Мембрана обеспечивает эффективную площадь фильтрации. 2. Адаптер "Д", диаметр=56, 0 мм ("А" или "B") байонетного типа с двумя уплотнительными кольцами из пищевой или силиконовой резины (для агрессивных сред - из фторкаучука). Адаптер обеспечивает герметичность установки фильтроэлемента в держатель. 3. Внутрений перфорированный опорный корпус обеспечивает механическую прочность. 4. Внешний перфорированный опорный корпус защищает от механических повреждений. 5. Заглушка хвостового (дискового) типа.
 Модификация микрофильтрационных мембран ММК (мембраны микропористые капроновые) - мембраны, обладающие положительным дзета -потенциалом (от 4 до 40 m. V) Задерживают до 100% колифагов и вирусов (вирус полиомиелита), бактерии, токсины, микоплазму и пирогены Стерильная фильтрация и депирогенизация парентеральных препаратов, фармацевтических жидкостей. Материал Фильтровальная мембрана ММК+ - "гидрофильная" мембрана из полиамида (Nylon-6) c положительным Дзета-потенциалом. Размер пор 0, 1; 0, 2; 0, 45
Модификация микрофильтрационных мембран ММК (мембраны микропористые капроновые) - мембраны, обладающие положительным дзета -потенциалом (от 4 до 40 m. V) Задерживают до 100% колифагов и вирусов (вирус полиомиелита), бактерии, токсины, микоплазму и пирогены Стерильная фильтрация и депирогенизация парентеральных препаратов, фармацевтических жидкостей. Материал Фильтровальная мембрана ММК+ - "гидрофильная" мембрана из полиамида (Nylon-6) c положительным Дзета-потенциалом. Размер пор 0, 1; 0, 2; 0, 45
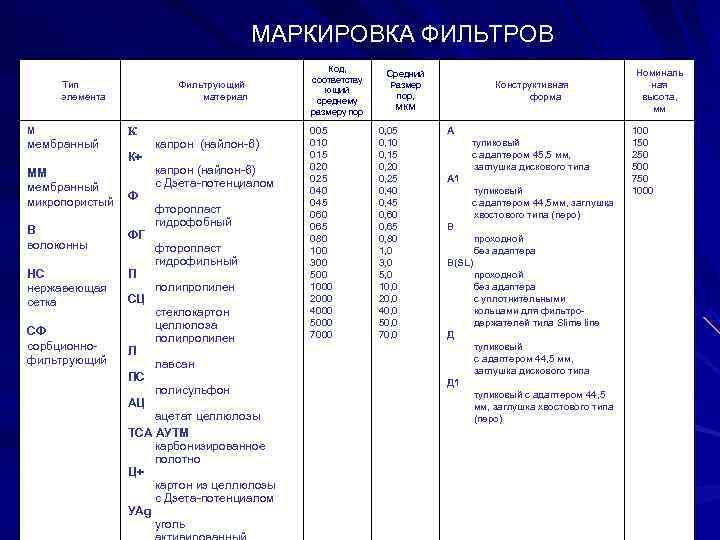
 МАРКИРОВКА ФИЛЬТРОВ Код, Номиналь Средний соответству Тип Фильтрующий Размер Конструктивная ющий элемента материал пор, форма высота, среднему МКМ мм размеру пор M К 005 0, 05 А 100 мембранный капрон (найлон-6) 010 0, 10 тупиковый 150 К+ 015 0, 15 с адаптером 45, 5 мм, 250 капрон (найлон-6) 020 0, 20 заглушка дискового типа 500 MM 025 0, 25 А 1 750 мембранный с Дзета-потенциалом 040 0, 40 тупиковый 1000 микропористый Ф 045 0, 45 с адаптером 44, 5 мм, заглушка фторопласт 060 0, 60 хвостового типа (перо) гидрофобный 065 0, 65 B B ФГ 080 0, 80 проходной волоконны фторопласт 100 1, 0 без адаптера гидрофильный 300 3, 0 B(SL) НС П 500 5, 0 проходной нержавеющая полипропилен 1000 10, 0 без адаптера сетка СЦ 2000 20, 0 с уплотнительными стеклокартон 4000 40, 0 кольцами для фильтро- 5000 50, 0 держателей типа Slime line СФ целлюлоза полипропилен 7000 70, 0 Д сорбционно- Л тупиковый фильтрующий с адаптером 44, 5 мм, лавсан заглушка дискового типа ПС Д 1 полисульфон тупиковый с адаптером 44, 5 АЦ мм, заглушка хвостового типа ацетат целлюлозы (перо) ТСА АУТМ карбонизированное полотно Ц+ картон из целлюлозы с Дзета-потенциалом УAg уголь
МАРКИРОВКА ФИЛЬТРОВ Код, Номиналь Средний соответству Тип Фильтрующий Размер Конструктивная ющий элемента материал пор, форма высота, среднему МКМ мм размеру пор M К 005 0, 05 А 100 мембранный капрон (найлон-6) 010 0, 10 тупиковый 150 К+ 015 0, 15 с адаптером 45, 5 мм, 250 капрон (найлон-6) 020 0, 20 заглушка дискового типа 500 MM 025 0, 25 А 1 750 мембранный с Дзета-потенциалом 040 0, 40 тупиковый 1000 микропористый Ф 045 0, 45 с адаптером 44, 5 мм, заглушка фторопласт 060 0, 60 хвостового типа (перо) гидрофобный 065 0, 65 B B ФГ 080 0, 80 проходной волоконны фторопласт 100 1, 0 без адаптера гидрофильный 300 3, 0 B(SL) НС П 500 5, 0 проходной нержавеющая полипропилен 1000 10, 0 без адаптера сетка СЦ 2000 20, 0 с уплотнительными стеклокартон 4000 40, 0 кольцами для фильтро- 5000 50, 0 держателей типа Slime line СФ целлюлоза полипропилен 7000 70, 0 Д сорбционно- Л тупиковый фильтрующий с адаптером 44, 5 мм, лавсан заглушка дискового типа ПС Д 1 полисульфон тупиковый с адаптером 44, 5 АЦ мм, заглушка хвостового типа ацетат целлюлозы (перо) ТСА АУТМ карбонизированное полотно Ц+ картон из целлюлозы с Дзета-потенциалом УAg уголь
 Наполнение ампул шприцевым методом
Наполнение ампул шприцевым методом
 Запайка ампул с газовой защитой
Запайка ампул с газовой защитой
 Наполнение и запайка ампул Наполнение: 1. Шприцевой 2. Вакуумный методы
Наполнение и запайка ампул Наполнение: 1. Шприцевой 2. Вакуумный методы
 Запайка ампул: 1. Оплавлением кончиков капилляров; 2. Оттяжкой кончиков капилляров; 3. Электрическим нагревом. Методы контроля запайки ампул: Вакуумный - помещение ампул на кассетах в камеру капиллярами вниз и откачка воздуха (вытекает раствор); С метиленовой синью или мыльным раствором - помещение ампул в кассетах в емкость с подкрашенной водой и на 20— 25 мин создания давление 100 20 к. Па (окрашивание или помутнение раствора; По свечению газовой среды внутри ампулы под действием высокочастотного электрического поля 20— 50 м. Гц. В зависимости от величины остаточного давления свечение будет разного цвета. Наблюдение проводится при 20 °С в диапазоне величины давления от 10 до 100 к. Па. (автоматическая линия 3060 -00 -00 ПС).
Запайка ампул: 1. Оплавлением кончиков капилляров; 2. Оттяжкой кончиков капилляров; 3. Электрическим нагревом. Методы контроля запайки ампул: Вакуумный - помещение ампул на кассетах в камеру капиллярами вниз и откачка воздуха (вытекает раствор); С метиленовой синью или мыльным раствором - помещение ампул в кассетах в емкость с подкрашенной водой и на 20— 25 мин создания давление 100 20 к. Па (окрашивание или помутнение раствора; По свечению газовой среды внутри ампулы под действием высокочастотного электрического поля 20— 50 м. Гц. В зависимости от величины остаточного давления свечение будет разного цвета. Наблюдение проводится при 20 °С в диапазоне величины давления от 10 до 100 к. Па. (автоматическая линия 3060 -00 -00 ПС).
 1. Надежность (эффективность) 2. Не изменять свойств объекта 3. Исключить вторичную контаминацию 4. Безопасность для персонала 5. Экономичность нагрев системы до 160 -170 0 С со скоростью 20 -40 0 С/с (на участке Т = 100 -110 0 С) и Влажным паром быстрого охлаждения, 0, 11 Мпа, 1200 С диаграмма "время - температура" показания независимого датчика температуры должны постоянно сверяться с данными диаграммы записывающего устройства (ГОСТ Р 52249 -2004). Химические индикаторы: 1. Смесь кислоты бензойной с фуксином (10: 1) - менее 119 -1210 С – цвет не изменяется 122 -1250 С – светло-синяя окраска выше 1250 С – интенсивно фиолетовый цвет 2. ИПС-120/45, ИПС-132/20, ИВС-180/60, ИВС -160/150
1. Надежность (эффективность) 2. Не изменять свойств объекта 3. Исключить вторичную контаминацию 4. Безопасность для персонала 5. Экономичность нагрев системы до 160 -170 0 С со скоростью 20 -40 0 С/с (на участке Т = 100 -110 0 С) и Влажным паром быстрого охлаждения, 0, 11 Мпа, 1200 С диаграмма "время - температура" показания независимого датчика температуры должны постоянно сверяться с данными диаграммы записывающего устройства (ГОСТ Р 52249 -2004). Химические индикаторы: 1. Смесь кислоты бензойной с фуксином (10: 1) - менее 119 -1210 С – цвет не изменяется 122 -1250 С – светло-синяя окраска выше 1250 С – интенсивно фиолетовый цвет 2. ИПС-120/45, ИПС-132/20, ИВС-180/60, ИВС -160/150
 После завершения высокотемпературной фазы цикла тепловой стерилизации следует принять меры против загрязнения загрузки в период охлаждения.
После завершения высокотемпературной фазы цикла тепловой стерилизации следует принять меры против загрязнения загрузки в период охлаждения.
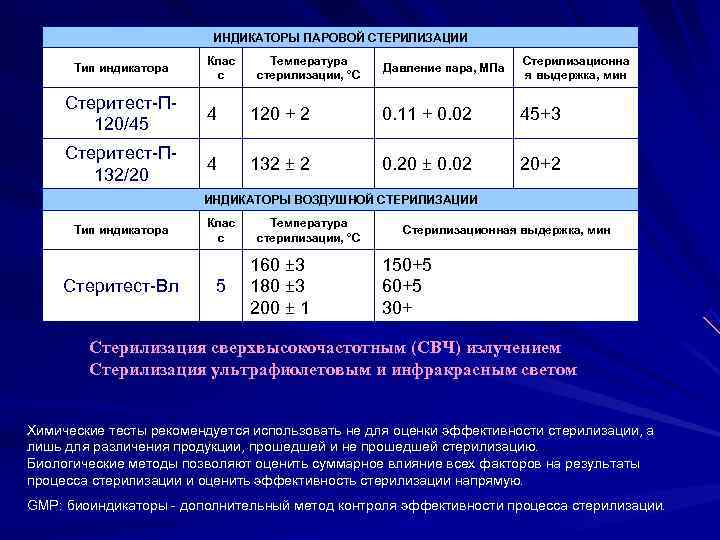
 ИНДИКАТОРЫ ПАРОВОЙ СТЕРИЛИЗАЦИИ Клас Температура Стерилизационна Тип индикатора Давление пара, МПа с стерилизации, °С я выдержка, мин Стеритест-П- 4 120 + 2 0. 11 + 0. 02 45+3 120/45 Стеритест-П- 4 132 ± 2 0. 20 ± 0. 02 20+2 132/20 ИНДИКАТОРЫ ВОЗДУШНОЙ СТЕРИЛИЗАЦИИ Клас Температура Тип индикатора Стерилизационная выдержка, мин с стерилизации, °С 160 ± 3 150+5 Стеритест-Вл 5 180 ± 3 60+5 200 ± 1 30+ Стерилизация сверхвысокочастотным (СВЧ) излучением Стерилизация ультрафиолетовым и инфракрасным светом Химические тесты рекомендуется использовать не для оценки эффективности стерилизации, а лишь для различения продукции, прошедшей и не прошедшей стерилизацию. Биологические методы позволяют оценить суммарное влияние всех факторов на результаты процесса стерилизации и оценить эффективность стерилизации напрямую. GMP: биоиндикаторы - дополнительный метод контроля эффективности процесса стерилизации.
ИНДИКАТОРЫ ПАРОВОЙ СТЕРИЛИЗАЦИИ Клас Температура Стерилизационна Тип индикатора Давление пара, МПа с стерилизации, °С я выдержка, мин Стеритест-П- 4 120 + 2 0. 11 + 0. 02 45+3 120/45 Стеритест-П- 4 132 ± 2 0. 20 ± 0. 02 20+2 132/20 ИНДИКАТОРЫ ВОЗДУШНОЙ СТЕРИЛИЗАЦИИ Клас Температура Тип индикатора Стерилизационная выдержка, мин с стерилизации, °С 160 ± 3 150+5 Стеритест-Вл 5 180 ± 3 60+5 200 ± 1 30+ Стерилизация сверхвысокочастотным (СВЧ) излучением Стерилизация ультрафиолетовым и инфракрасным светом Химические тесты рекомендуется использовать не для оценки эффективности стерилизации, а лишь для различения продукции, прошедшей и не прошедшей стерилизацию. Биологические методы позволяют оценить суммарное влияние всех факторов на результаты процесса стерилизации и оценить эффективность стерилизации напрямую. GMP: биоиндикаторы - дополнительный метод контроля эффективности процесса стерилизации.
 Биоиндикаторы - это стандартные препараты, в состав которых входят суспензия спор термоустойчивого микроорганизма в питательной среде и р. Н индикатор, помещенные на специальный носитель. При этом питательная среда служит для защиты спор от гибели в процессе нагревания, способствует росту переживших нагревание спор и выживанию спор во время хранения биоиндикаторов. В качестве р. Н -индикаторов используются индикаторы, у которых происходит изменение окраски в результате метаболизма микроорганизмов. Критерием оценки эффективности процесса стерилизации служат гибель или выживание спор в биоиндикаторе после окончания процесса стерилизации, что контролируется сохранением (в случае гибели спор) или изменением (в случае, если процесс стерилизации был неэффективным и тест- культура выжила) окраски биоиндикатора.
Биоиндикаторы - это стандартные препараты, в состав которых входят суспензия спор термоустойчивого микроорганизма в питательной среде и р. Н индикатор, помещенные на специальный носитель. При этом питательная среда служит для защиты спор от гибели в процессе нагревания, способствует росту переживших нагревание спор и выживанию спор во время хранения биоиндикаторов. В качестве р. Н -индикаторов используются индикаторы, у которых происходит изменение окраски в результате метаболизма микроорганизмов. Критерием оценки эффективности процесса стерилизации служат гибель или выживание спор в биоиндикаторе после окончания процесса стерилизации, что контролируется сохранением (в случае гибели спор) или изменением (в случае, если процесс стерилизации был неэффективным и тест- культура выжила) окраски биоиндикатора.
 Биологические индикаторы: Bacillus stearothermophilus Bacillus Subtilis (споровые формы)
Биологические индикаторы: Bacillus stearothermophilus Bacillus Subtilis (споровые формы)
 Прогрев стерилизуемых объектов происходит медленно из-за невысокой теплопроводности воздуха, и загружают стерилизаторы при температуре в них 60 °С и ниже. С момента нагрева воздуха в стерилизаторе до 180— 200 °С начинается отсчет времени стерилизации Толщина слоя порошков для достижения равномерного прогрева должна составлять 6— 7 см. Для надежной стерилизации масса стерилизуемого объекта не должна превышать 500 г.
Прогрев стерилизуемых объектов происходит медленно из-за невысокой теплопроводности воздуха, и загружают стерилизаторы при температуре в них 60 °С и ниже. С момента нагрева воздуха в стерилизаторе до 180— 200 °С начинается отсчет времени стерилизации Толщина слоя порошков для достижения равномерного прогрева должна составлять 6— 7 см. Для надежной стерилизации масса стерилизуемого объекта не должна превышать 500 г.
 Источники ионизирующего излучения: ускорители электронов прямого действия; 60 Со 27, 137 Cs 55 15− 25 к. Гр (до 50 линейные ускорители электронов; к. Гр) долгоживущие изотопы Со, Cs. 1. технологичность (включая возможность организации непрерывного автоматизированного процесса); 2. универсальность (возможность обеспечения высокой эффективности стерилизации практически для любого вида облучаемого материала при минимальной оптимизации условий облучения); 3. возможность достижения любой заданной надежности стерилизации; 4. простота контроля эффективности процесса за счет дозиметрии поглощенной энергии. должна измеряться поглощенная доза ионизирующего излучения (дозиметры, показания которых не зависят от используемой мощности дозы излучения), биологические индикаторы в качестве средства дополнительного контроля, использование чувствительных к излучению цветовых индикаторов на ОБЩИЕ ТРЕБОВАНИЯ каждой упаковке К ТЕХНОЛОГИЧЕСКОМУ РЕГЛАМЕНТУ РАДИАЦИОННОЙ СТЕРИЛИЗАЦИИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ РУКОВОДСТВО Р 2. 6. 4/3. 5. 4. 1040 -01
Источники ионизирующего излучения: ускорители электронов прямого действия; 60 Со 27, 137 Cs 55 15− 25 к. Гр (до 50 линейные ускорители электронов; к. Гр) долгоживущие изотопы Со, Cs. 1. технологичность (включая возможность организации непрерывного автоматизированного процесса); 2. универсальность (возможность обеспечения высокой эффективности стерилизации практически для любого вида облучаемого материала при минимальной оптимизации условий облучения); 3. возможность достижения любой заданной надежности стерилизации; 4. простота контроля эффективности процесса за счет дозиметрии поглощенной энергии. должна измеряться поглощенная доза ионизирующего излучения (дозиметры, показания которых не зависят от используемой мощности дозы излучения), биологические индикаторы в качестве средства дополнительного контроля, использование чувствительных к излучению цветовых индикаторов на ОБЩИЕ ТРЕБОВАНИЯ каждой упаковке К ТЕХНОЛОГИЧЕСКОМУ РЕГЛАМЕНТУ РАДИАЦИОННОЙ СТЕРИЛИЗАЦИИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ РУКОВОДСТВО Р 2. 6. 4/3. 5. 4. 1040 -01
 Радиолиз – деструкция веществ под влиянием радиации H 2 O®H 2 O+ + e-; H 2 O®H 2 O+ + H 2 O® H+ (H 2 O) + OH× H 2 O- + H 2 O® H× + OH-( H 2 O) Радикалы H+ и OH- образуются также при распаде H 2 O*® H× + OH× возбуждённых молекул Электрон может захватываться другой молекулой воды, образуя ион H 2 O-. Ионы во-ды могут гидратироваться, в результате чего получаются гидратированные ионы H+ и OH - и имеющие ненасыщенные химические связи (неспаренные электроны) радикалы H× и OH× Решение проблемы добавление стабилизаторов (акцепторов продуктов радиолиза); облучение предварительно замороженных растворов (программированная криорадиационная стерилизация); снижение доз стерилизации с 10— 25 к. Гр до 2, 5— 6 к. Гр, что возможно применении субстерилизации в малой дозе, выдерживании в течение 0, 5— 3 месяцев, а затем повторной стерилизации объекта в малой дозе. Эффективность радиационной стерилизации зависит и от внешних факторов (температура, наличие влаги и др. )
Радиолиз – деструкция веществ под влиянием радиации H 2 O®H 2 O+ + e-; H 2 O®H 2 O+ + H 2 O® H+ (H 2 O) + OH× H 2 O- + H 2 O® H× + OH-( H 2 O) Радикалы H+ и OH- образуются также при распаде H 2 O*® H× + OH× возбуждённых молекул Электрон может захватываться другой молекулой воды, образуя ион H 2 O-. Ионы во-ды могут гидратироваться, в результате чего получаются гидратированные ионы H+ и OH - и имеющие ненасыщенные химические связи (неспаренные электроны) радикалы H× и OH× Решение проблемы добавление стабилизаторов (акцепторов продуктов радиолиза); облучение предварительно замороженных растворов (программированная криорадиационная стерилизация); снижение доз стерилизации с 10— 25 к. Гр до 2, 5— 6 к. Гр, что возможно применении субстерилизации в малой дозе, выдерживании в течение 0, 5— 3 месяцев, а затем повторной стерилизации объекта в малой дозе. Эффективность радиационной стерилизации зависит и от внешних факторов (температура, наличие влаги и др. )
 смеси этиленоксида с флегманизаторами (углерода диоксидом (9: 1), бромистым метилом (1: 2, 5), фреоном) под давлением до 196133 Н/м 2 при +43 -45 о. С Наименование Концентрация С 2 Н 4 О 100% Параметры эффективности: CO 2+С 2 Н 4 О 6 -20 % С 2 Н 4 О стерилизующая доза газа; HCFC-124+С 2 Н 4 О 12% HCFC-124 температура в стерилизационной камере; отн. влажность в стерилизационной камере; время стерилизационной выдержки Особенности применения может использоваться только там, где нельзя применять другие методы стерилизации не допускать включения микроорганизмов в материал (например, в кристаллы или лиофилизированный белок). Учет влияния вида и количества упаковочного материала температуру и влажность загрузки - в соответствие с требованиями процесса контроль стерильности с использованием биологических индикаторов НЕДОСТАТКИ: ü ограниченный перечень форм, подлежащих обработке ü высокая токсичность смеси и продуктов ее взаимодействия с материалами ü длительная сохранность остаточных количеств реагента (выдержка в вентилируемом помещении от 1 до 14(21) суток
смеси этиленоксида с флегманизаторами (углерода диоксидом (9: 1), бромистым метилом (1: 2, 5), фреоном) под давлением до 196133 Н/м 2 при +43 -45 о. С Наименование Концентрация С 2 Н 4 О 100% Параметры эффективности: CO 2+С 2 Н 4 О 6 -20 % С 2 Н 4 О стерилизующая доза газа; HCFC-124+С 2 Н 4 О 12% HCFC-124 температура в стерилизационной камере; отн. влажность в стерилизационной камере; время стерилизационной выдержки Особенности применения может использоваться только там, где нельзя применять другие методы стерилизации не допускать включения микроорганизмов в материал (например, в кристаллы или лиофилизированный белок). Учет влияния вида и количества упаковочного материала температуру и влажность загрузки - в соответствие с требованиями процесса контроль стерильности с использованием биологических индикаторов НЕДОСТАТКИ: ü ограниченный перечень форм, подлежащих обработке ü высокая токсичность смеси и продуктов ее взаимодействия с материалами ü длительная сохранность остаточных количеств реагента (выдержка в вентилируемом помещении от 1 до 14(21) суток
 НЕДОСТАТКИ: ü меньшая надежность в стерильности, ü высокая стоимость процесса ( жесткие условия по микробной чистоте помещений); 0, 2 -0, 22 мкм (0, 1 мкм) ü трудности технического порядка (проницаемость мембран, Для стерильной фильтрации небольшой срок службы мембран), используются только ü сложность приготовления дисперсных лекарственных двухслойные конфигурации. форм; Проведение стерилизующей фильтрации не является достаточным условием стерилизации, если возможна стерилизация продукта в окончательной первичной упаковке. рекомендовать повторную фильтрацию продукта через дополнительный удерживающий микроорганизмы стерилизующий фильтр непосредственно перед наполнением
НЕДОСТАТКИ: ü меньшая надежность в стерильности, ü высокая стоимость процесса ( жесткие условия по микробной чистоте помещений); 0, 2 -0, 22 мкм (0, 1 мкм) ü трудности технического порядка (проницаемость мембран, Для стерильной фильтрации небольшой срок службы мембран), используются только ü сложность приготовления дисперсных лекарственных двухслойные конфигурации. форм; Проведение стерилизующей фильтрации не является достаточным условием стерилизации, если возможна стерилизация продукта в окончательной первичной упаковке. рекомендовать повторную фильтрацию продукта через дополнительный удерживающий микроорганизмы стерилизующий фильтр непосредственно перед наполнением
 Лекарственные формы для инъекций (растворы для инъекций) 1. Описание 2. Подлинность 3. Прозрачность 4. Цветность 5. р. Н или Кислотность или щелочность 6. Механические включения 7. Плотность 8. Вязкость 9. Посторонние примеси (родственные соединения) 10. Номинальный объем 11. Пирогенность или Бактериальные эндотоксины (ЛАЛ тест) 12. Токсичность 13. Содержание веществ гистаминоподобного действия 14. Стерильность 15. Количественное определение
Лекарственные формы для инъекций (растворы для инъекций) 1. Описание 2. Подлинность 3. Прозрачность 4. Цветность 5. р. Н или Кислотность или щелочность 6. Механические включения 7. Плотность 8. Вязкость 9. Посторонние примеси (родственные соединения) 10. Номинальный объем 11. Пирогенность или Бактериальные эндотоксины (ЛАЛ тест) 12. Токсичность 13. Содержание веществ гистаминоподобного действия 14. Стерильность 15. Количественное определение
 ИНСТРУКЦИЯ ПО КОНТРОЛЮ НА МЕХАНИЧЕСКИЕ ВКЛЮЧЕНИЯ ИНЪЕКЦИОННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ РД 42 -501 -98 Первичный − внутрицеховой сплошной (100 % емкостей). Номер просмотрщика вкладывается в упаковку продукции. вторичный – внутрицеховой выборочный (проба − 5% от партии до 2000 ампул, флаконов, бутылок и 250 штук от всех других партий) третий – выборочный контроль, осуществляемый контролёром ОКК (выборка в два этапа − 1 и 2 ступень.
ИНСТРУКЦИЯ ПО КОНТРОЛЮ НА МЕХАНИЧЕСКИЕ ВКЛЮЧЕНИЯ ИНЪЕКЦИОННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ РД 42 -501 -98 Первичный − внутрицеховой сплошной (100 % емкостей). Номер просмотрщика вкладывается в упаковку продукции. вторичный – внутрицеховой выборочный (проба − 5% от партии до 2000 ампул, флаконов, бутылок и 250 штук от всех других партий) третий – выборочный контроль, осуществляемый контролёром ОКК (выборка в два этапа − 1 и 2 ступень.
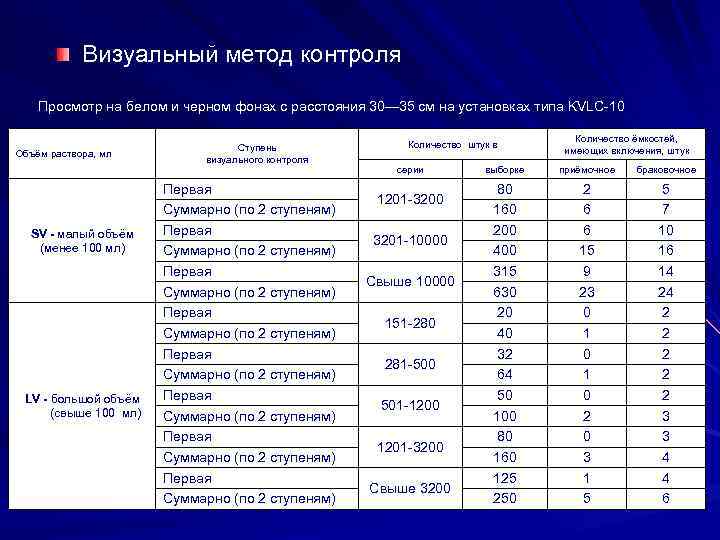
 Визуальный метод контроля Просмотр на белом и черном фонах с расстояния 30— 35 см на установках типа KVLC-10 Количество ёмкостей, Ступень Количество штук в Объём раствора, мл имеющих включения, штук визуального контроля серии выборке приёмочное браковочное Первая 80 2 5 1201 -3200 Суммарно (по 2 ступеням) 160 6 7 SV - малый объём Первая 200 6 10 3201 -10000 (менее 100 мл) Суммарно (по 2 ступеням) 400 15 16 Первая 315 9 14 Свыше 10000 Суммарно (по 2 ступеням) 630 23 24 Первая 20 2 151 -280 Суммарно (по 2 ступеням) 40 1 2 Первая 32 0 2 281 -500 Суммарно (по 2 ступеням) 64 1 2 LV - большой объём Первая 50 2 501 -1200 (свыше 100 мл) Суммарно (по 2 ступеням) 100 2 3 Первая 80 3 1201 -3200 Суммарно (по 2 ступеням) 160 3 4 Первая 125 1 4 Свыше 3200 Суммарно (по 2 ступеням) 250 5 6
Визуальный метод контроля Просмотр на белом и черном фонах с расстояния 30— 35 см на установках типа KVLC-10 Количество ёмкостей, Ступень Количество штук в Объём раствора, мл имеющих включения, штук визуального контроля серии выборке приёмочное браковочное Первая 80 2 5 1201 -3200 Суммарно (по 2 ступеням) 160 6 7 SV - малый объём Первая 200 6 10 3201 -10000 (менее 100 мл) Суммарно (по 2 ступеням) 400 15 16 Первая 315 9 14 Свыше 10000 Суммарно (по 2 ступеням) 630 23 24 Первая 20 2 151 -280 Суммарно (по 2 ступеням) 40 1 2 Первая 32 0 2 281 -500 Суммарно (по 2 ступеням) 64 1 2 LV - большой объём Первая 50 2 501 -1200 (свыше 100 мл) Суммарно (по 2 ступеням) 100 2 3 Первая 80 3 1201 -3200 Суммарно (по 2 ступеням) 160 3 4 Первая 125 1 4 Свыше 3200 Суммарно (по 2 ступеням) 250 5 6
 Счетно-фотометрический метод контроля анализаторы механических примесей фотометрически-счётные ФС-151, ФС-151 -1 или АОЗ-101. Количество механических Объём включений в 1 ёмкости, штук Параметры растворов, Выборка 1 и её объём оценки мл 5 мкм 25 мкм и более Растворитель, 50 мл 4 раза по 10 мл - Не более 2 8 штук (4 раза по 10 мл, SV (менее 100 мл) перемешивают Не более 6000 Не более 600 Если 2 минуты) количество частиц больше, 3 штуки (100 мл, то бракуют LV (менее 500 всю серию мл) удаляют воздух Не более 100 Не более 4 мешалкой) LV (500 мл и 2 штуки (4 раза более) по 10 или 25 мл) Не более 1 Не более 4
Счетно-фотометрический метод контроля анализаторы механических примесей фотометрически-счётные ФС-151, ФС-151 -1 или АОЗ-101. Количество механических Объём включений в 1 ёмкости, штук Параметры растворов, Выборка 1 и её объём оценки мл 5 мкм 25 мкм и более Растворитель, 50 мл 4 раза по 10 мл - Не более 2 8 штук (4 раза по 10 мл, SV (менее 100 мл) перемешивают Не более 6000 Не более 600 Если 2 минуты) количество частиц больше, 3 штуки (100 мл, то бракуют LV (менее 500 всю серию мл) удаляют воздух Не более 100 Не более 4 мешалкой) LV (500 мл и 2 штуки (4 раза более) по 10 или 25 мл) Не более 1 Не более 4
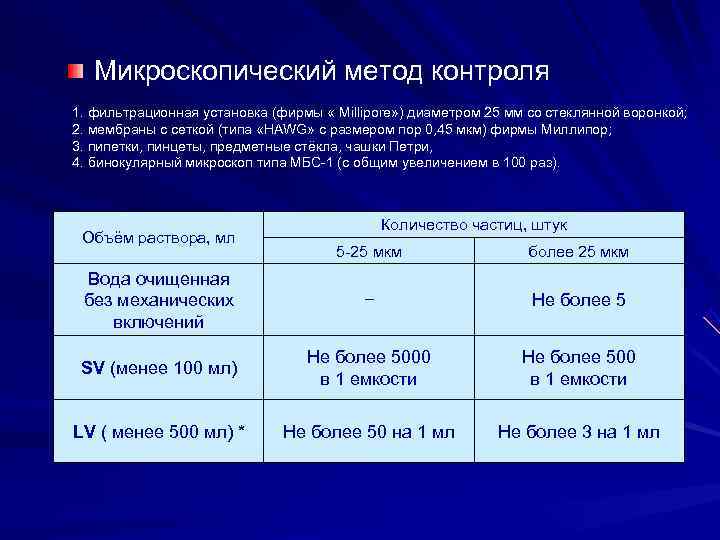
 Микроскопический метод контроля 1. фильтрационная установка (фирмы « Millipore» ) диаметром 25 мм со стеклянной воронкой; 2. мембраны с сеткой (типа «HAWG» с размером пор 0, 45 мкм) фирмы Миллипор; 3. пипетки, пинцеты, предметные стёкла, чашки Петри, 4. бинокулярный микроскоп типа МБС-1 (с общим увеличением в 100 раз). Количество частиц, штук Объём раствора, мл 5 -25 мкм более 25 мкм Вода очищенная без механических − Не более 5 включений Не более 5000 Не более 500 SV (менее 100 мл) в 1 емкости LV ( менее 500 мл) * Не более 50 на 1 мл Не более 3 на 1 мл
Микроскопический метод контроля 1. фильтрационная установка (фирмы « Millipore» ) диаметром 25 мм со стеклянной воронкой; 2. мембраны с сеткой (типа «HAWG» с размером пор 0, 45 мкм) фирмы Миллипор; 3. пипетки, пинцеты, предметные стёкла, чашки Петри, 4. бинокулярный микроскоп типа МБС-1 (с общим увеличением в 100 раз). Количество частиц, штук Объём раствора, мл 5 -25 мкм более 25 мкм Вода очищенная без механических − Не более 5 включений Не более 5000 Не более 500 SV (менее 100 мл) в 1 емкости LV ( менее 500 мл) * Не более 50 на 1 мл Не более 3 на 1 мл
 Испытание на стерильность При стерилизации паром под давлением – 10 единиц на анализ При стериллизации другим методом Оценка стерильности лекарств антимикробного действия ü с инактиватором (пара-аминобензойная кислота, пенициллаза) ü с изменением соотношения объемов посевного материала и питательной среды ü методом мембранной фильтрации 1. Метод прямого посева 2. Метод мембранной фильтрации Питательные среды : тиогликолевая, Сабуро Инкубация – до 14 суток
Испытание на стерильность При стерилизации паром под давлением – 10 единиц на анализ При стериллизации другим методом Оценка стерильности лекарств антимикробного действия ü с инактиватором (пара-аминобензойная кислота, пенициллаза) ü с изменением соотношения объемов посевного материала и питательной среды ü методом мембранной фильтрации 1. Метод прямого посева 2. Метод мембранной фильтрации Питательные среды : тиогликолевая, Сабуро Инкубация – до 14 суток
 Погибшие м/о, остаки м/о, бактериальные эндотоксины (липополисахарид, ы) длинная цепь жирной кислоты (липид А), + сахарная цепь + вариабельная углеводная цепочка (О-антиген). Экзогенны е Эндогенные (нейтрофильные лейкоциты, моноциты и другие подвижные и фиксированные макрофаги ) Источники эндотоксинов вода, (растворитель или для обработки); ампулы и флаконы; химические вещества и специально необработанные материалы; воздух; персонал Легкая степень – температура тела повышается в пределах 1 0 С, возникают головная боль, боли в мышцах. Средняя тяжесть – озноб, повышение температуры тела на 1, 5 -2 0 С, учащение пульса и дыхания. Тяжелая реакция – потрясающий озноб, температура повышается более чем на 2 0 С, достигая 40 0 С и более, выраженная головная боль, боли в мышцах, костях, одышка, цианоз губ, тахикардия.
Погибшие м/о, остаки м/о, бактериальные эндотоксины (липополисахарид, ы) длинная цепь жирной кислоты (липид А), + сахарная цепь + вариабельная углеводная цепочка (О-антиген). Экзогенны е Эндогенные (нейтрофильные лейкоциты, моноциты и другие подвижные и фиксированные макрофаги ) Источники эндотоксинов вода, (растворитель или для обработки); ампулы и флаконы; химические вещества и специально необработанные материалы; воздух; персонал Легкая степень – температура тела повышается в пределах 1 0 С, возникают головная боль, боли в мышцах. Средняя тяжесть – озноб, повышение температуры тела на 1, 5 -2 0 С, учащение пульса и дыхания. Тяжелая реакция – потрясающий озноб, температура повышается более чем на 2 0 С, достигая 40 0 С и более, выраженная головная боль, боли в мышцах, костях, одышка, цианоз губ, тахикардия.
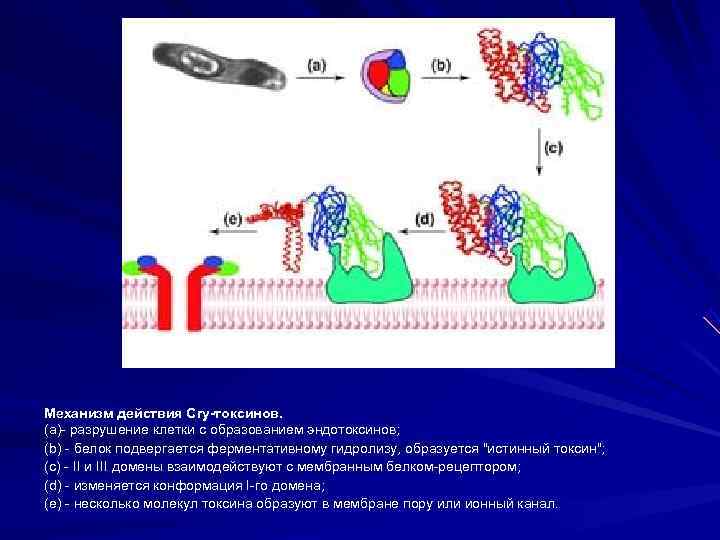
 Механизм действия Cry-токсинов. (a)- разрушение клетки с образованием эндотоксинов; (b) - белок подвергается ферментативному гидролизу, образуется "истинный токсин"; (с) - II и III домены взаимодействуют с мембранным белком-рецептором; (d) - изменяется конформация I-го домена; (e) - несколько молекул токсина образуют в мембране пору или ионный канал.
Механизм действия Cry-токсинов. (a)- разрушение клетки с образованием эндотоксинов; (b) - белок подвергается ферментативному гидролизу, образуется "истинный токсин"; (с) - II и III домены взаимодействуют с мембранным белком-рецептором; (d) - изменяется конформация I-го домена; (e) - несколько молекул токсина образуют в мембране пору или ионный канал.
 Пироген связывается с белками к СD 14 -рецепторам лейкоцитов (особенно моноцитов и макрофагов), эндотелиальными и другими типами клеток (липополисахарид-связывающий белковый комплекс). Активированные липополисахарид-связывающим белковым комплексом, мононуклеарные фагоциты продуцируют фактор некроза опухоли, который в свою очередь индуцирует синтез интерлейкина-1 → действие на эндотелиальные клетки, продуцирующие интерлейкин-6, интерлейкин-8 и адгезивные молекулы. Первичное высвобождение эндотоксина приводит к ЦИТОКИНОВОМУ КАСКАДУ, который активирует высвобождение провоспалительных цитокинов макрофагов и повышает эндотелиальную адгезию молекул для лейкоцитов, усиливая комплемент-опосредованную реакцию нейтрофилов Высокие уровни липополисахарида приводят к повреждению эндотелиальных клеток, которое даёт начало коагуляционному каскаду При длительном избытке эндотоксина цитокиновый каскад усиливает синтез вторичных эффекторов - оксида азота (NO) и фактора активации тромбоцитов. Эндокринные и паракринные эффекты цитокинов и вторичных медиаторов приводят к системной вазодилатации и гипотензии, снижению сердечной сократимости, гиперактивации системы коагуляции, повреждению и активации эндотелия, системной адгезии лейкоцитов. Системная вазодилатация и снижение сердечной сократимости - снижение перфузии и гипоксия. На фоне повреждение эндотелия, прогрессирование активации системы коагуляции и повышение проницаемости капилляров реализуются в : - септический шок; - полиорганная недостаточность; - ДВС-синдром; - респираторный дистресс синдром взрослых. ДВС-синдром ( тромбогеморрагический синдром, коагулопатия потребления) - Диссеминированное внутрисосудистое свертывание опасное для жизни нарушение свертываемости крови вследствие массивного высвобождения из тканей тромбопластических веществ.
Пироген связывается с белками к СD 14 -рецепторам лейкоцитов (особенно моноцитов и макрофагов), эндотелиальными и другими типами клеток (липополисахарид-связывающий белковый комплекс). Активированные липополисахарид-связывающим белковым комплексом, мононуклеарные фагоциты продуцируют фактор некроза опухоли, который в свою очередь индуцирует синтез интерлейкина-1 → действие на эндотелиальные клетки, продуцирующие интерлейкин-6, интерлейкин-8 и адгезивные молекулы. Первичное высвобождение эндотоксина приводит к ЦИТОКИНОВОМУ КАСКАДУ, который активирует высвобождение провоспалительных цитокинов макрофагов и повышает эндотелиальную адгезию молекул для лейкоцитов, усиливая комплемент-опосредованную реакцию нейтрофилов Высокие уровни липополисахарида приводят к повреждению эндотелиальных клеток, которое даёт начало коагуляционному каскаду При длительном избытке эндотоксина цитокиновый каскад усиливает синтез вторичных эффекторов - оксида азота (NO) и фактора активации тромбоцитов. Эндокринные и паракринные эффекты цитокинов и вторичных медиаторов приводят к системной вазодилатации и гипотензии, снижению сердечной сократимости, гиперактивации системы коагуляции, повреждению и активации эндотелия, системной адгезии лейкоцитов. Системная вазодилатация и снижение сердечной сократимости - снижение перфузии и гипоксия. На фоне повреждение эндотелия, прогрессирование активации системы коагуляции и повышение проницаемости капилляров реализуются в : - септический шок; - полиорганная недостаточность; - ДВС-синдром; - респираторный дистресс синдром взрослых. ДВС-синдром ( тромбогеморрагический синдром, коагулопатия потребления) - Диссеминированное внутрисосудистое свертывание опасное для жизни нарушение свертываемости крови вследствие массивного высвобождения из тканей тромбопластических веществ.
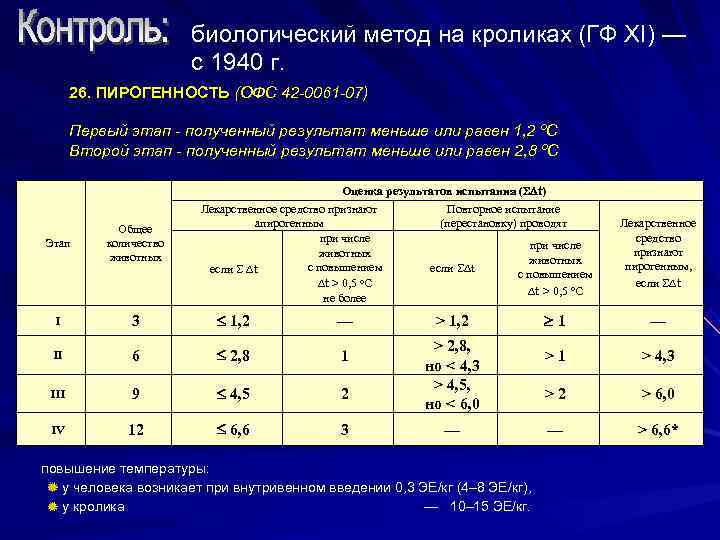
 биологический метод на кроликах (ГФ XI) — с 1940 г. 26. ПИРОГЕННОСТЬ (ОФС 42 -0061 -07) Первый этап - полученный результат меньше или равен 1, 2 ºС Второй этап - полученный результат меньше или равен 2, 8 ºС Оценка результатов испытания ( t) Лекарственное средство признают Повторное испытание Общее апирогенным (перестановку) проводят Лекарственное Этап количество при числе средство при числе животных признают животных если t с повышением если t пирогенным, с повышением t > 0, 5 о. С если t t > 0, 5 о. С не более I 3 1, 2 — > 1, 2 1 — > 2, 8, II 6 2, 8 1 >1 > 4, 3 но < 4, 3 > 4, 5, III 9 4, 5 2 >2 > 6, 0 но < 6, 0 IV 12 6, 6 3 — > 6, 6* повышение температуры: у человека возникает при внутривенном введении 0, 3 ЭЕ/кг (4– 8 ЭЕ/кг), у кролика — 10– 15 ЭЕ/кг.
биологический метод на кроликах (ГФ XI) — с 1940 г. 26. ПИРОГЕННОСТЬ (ОФС 42 -0061 -07) Первый этап - полученный результат меньше или равен 1, 2 ºС Второй этап - полученный результат меньше или равен 2, 8 ºС Оценка результатов испытания ( t) Лекарственное средство признают Повторное испытание Общее апирогенным (перестановку) проводят Лекарственное Этап количество при числе средство при числе животных признают животных если t с повышением если t пирогенным, с повышением t > 0, 5 о. С если t t > 0, 5 о. С не более I 3 1, 2 — > 1, 2 1 — > 2, 8, II 6 2, 8 1 >1 > 4, 3 но < 4, 3 > 4, 5, III 9 4, 5 2 >2 > 6, 0 но < 6, 0 IV 12 6, 6 3 — > 6, 6* повышение температуры: у человека возникает при внутривенном введении 0, 3 ЭЕ/кг (4– 8 ЭЕ/кг), у кролика — 10– 15 ЭЕ/кг.
 Мечехвост (Limulus) - род суставчатоногих, семейство Limulidae, отряд Xiphosura s. Poecilopoda. Американский мечехвост (Limulus polyphemus) 1956 г. - американский ученый Bang Frederick. «Кровь» - гемолимфа, голубая окраска, содержит только один тип клеток - амебоциты.
Мечехвост (Limulus) - род суставчатоногих, семейство Limulidae, отряд Xiphosura s. Poecilopoda. Американский мечехвост (Limulus polyphemus) 1956 г. - американский ученый Bang Frederick. «Кровь» - гемолимфа, голубая окраска, содержит только один тип клеток - амебоциты.
 Свертывающий фермент перерабатывает субстрат: коагулоген. Молекула коагулогена разрезается на несколько полипептидных цепей, между которыми затем образуются связи, в результате чего получается пространственная структура геля
Свертывающий фермент перерабатывает субстрат: коагулоген. Молекула коагулогена разрезается на несколько полипептидных цепей, между которыми затем образуются связи, в результате чего получается пространственная структура геля
 27. БАКТЕРИАЛЬНЫЕ ЭНДОТОКСИНЫ (ОФС 42 -0062 -07) Реакция лизата амебоцитов с эндотоксином открыта в США в 1964 году LAL-тест «Limulus Amebocite Lisate» - лизат амебоцитов мечехвоста с 1980 г. , в РФ ВФС 42 -2960 -97, ОФС 42 -0062 -07 Пирогены (эндотоксины) активируют в лизате амебоцитов комплекс ферментов, изменяющий физико-химические свойства смеси ТАL-тест Tachypleus tridentatus (тахиплеус тризубый)
27. БАКТЕРИАЛЬНЫЕ ЭНДОТОКСИНЫ (ОФС 42 -0062 -07) Реакция лизата амебоцитов с эндотоксином открыта в США в 1964 году LAL-тест «Limulus Amebocite Lisate» - лизат амебоцитов мечехвоста с 1980 г. , в РФ ВФС 42 -2960 -97, ОФС 42 -0062 -07 Пирогены (эндотоксины) активируют в лизате амебоцитов комплекс ферментов, изменяющий физико-химические свойства смеси ТАL-тест Tachypleus tridentatus (тахиплеус тризубый)
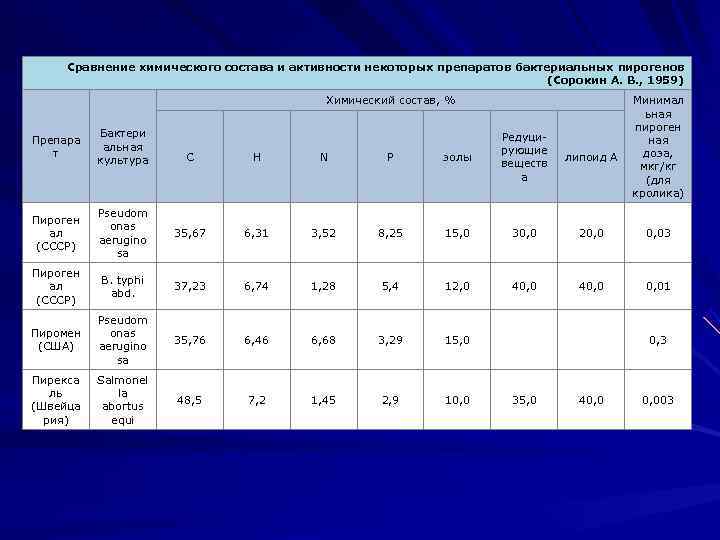
 Сравнение химического состава и активности некоторых препаратов бактериальных пирогенов (Сорокин А. В. , 1959) Химический состав, % Минимал ьная пироген Бактери Редуци- Препара ная альная рующие т С H N Р золы липоид А доза, культура веществ мкг/кг а (для кролика) Pseudom Пироген onas ал 35, 67 6, 31 3, 52 8, 25 15, 0 30, 0 20, 0 0, 03 aerugino (СССР) sa Пироген В. typhi ал 37, 23 6, 74 1, 28 5, 4 12, 0 40, 0 0, 01 abd. (СССР) Pseudom Пиромен onas 35, 76 6, 46 6, 68 3, 29 15, 0 0, 3 (США) aerugino sa Пирекса Salmonel ль la 48, 5 7, 2 1, 45 2, 9 10, 0 35, 0 40, 003 (Швейца abortus рия) equi
Сравнение химического состава и активности некоторых препаратов бактериальных пирогенов (Сорокин А. В. , 1959) Химический состав, % Минимал ьная пироген Бактери Редуци- Препара ная альная рующие т С H N Р золы липоид А доза, культура веществ мкг/кг а (для кролика) Pseudom Пироген onas ал 35, 67 6, 31 3, 52 8, 25 15, 0 30, 0 20, 0 0, 03 aerugino (СССР) sa Пироген В. typhi ал 37, 23 6, 74 1, 28 5, 4 12, 0 40, 0 0, 01 abd. (СССР) Pseudom Пиромен onas 35, 76 6, 46 6, 68 3, 29 15, 0 0, 3 (США) aerugino sa Пирекса Salmonel ль la 48, 5 7, 2 1, 45 2, 9 10, 0 35, 0 40, 003 (Швейца abortus рия) equi
 Возможности использования ЛАЛ-теста ненаркотические анальгетики, транквилизаторы, нейролептики, кортикостероиды и некоторые анестетики (т. е. препараты-антипиретики, вызывающие понижение температуры тела, и, следовательно, способные маскировать наличие пирогенов); препараты плаценты, вакцины, новокаин (т. е. препараты, вызывающие повышение температуры, обусловленное их фармакологическими свойствами); средства для наркоза, сердечные гликозиды, наркотические анальгетики, инсулин, адреналин, снотворные средства, деполяризующие миорелаксанты (т. е. препараты, которые в силу своих фармакологических свойств вызывают изменения физиологического состояния животных); инфузионные препараты, суточный объем введения которых превышает 700 мл; радиофармацевтические препараты; антибиотики, воздействуя на микрофлору, вызывают у кроликов дисбактериоз или, как в случае линкомицина гидрохлорида — кандидомикоз. постадийный контроль производства: контроль сырья; контроль воды для инъекций; проверка оборудования элементов фильтра на вымывание из них пирогенов; контроль растворов перед стерилизующим фильтрованием; контроль чистоты ампул, флаконов.
Возможности использования ЛАЛ-теста ненаркотические анальгетики, транквилизаторы, нейролептики, кортикостероиды и некоторые анестетики (т. е. препараты-антипиретики, вызывающие понижение температуры тела, и, следовательно, способные маскировать наличие пирогенов); препараты плаценты, вакцины, новокаин (т. е. препараты, вызывающие повышение температуры, обусловленное их фармакологическими свойствами); средства для наркоза, сердечные гликозиды, наркотические анальгетики, инсулин, адреналин, снотворные средства, деполяризующие миорелаксанты (т. е. препараты, которые в силу своих фармакологических свойств вызывают изменения физиологического состояния животных); инфузионные препараты, суточный объем введения которых превышает 700 мл; радиофармацевтические препараты; антибиотики, воздействуя на микрофлору, вызывают у кроликов дисбактериоз или, как в случае линкомицина гидрохлорида — кандидомикоз. постадийный контроль производства: контроль сырья; контроль воды для инъекций; проверка оборудования элементов фильтра на вымывание из них пирогенов; контроль растворов перед стерилизующим фильтрованием; контроль чистоты ампул, флаконов.
 Реализация LAL-теста Гель-тромб тест (GLAL) (Pyrotell. R - Associates of Cape Cod, Inc) образование плотного геля на дне пробирки - контроль по переворачиванию Турбидиметрический LAL-тест (Pyrotell-TR - Associates of Cape Cod, Inc) чувствительность считывающего устройства (спектрофотометр Bio-Tek ELx 808 или аналогичный) − от 0, 001 ЕДэ/мл. Хромогенный LAL-тест (CLAL) (Pyrochrome. R - Associates of Cape Cod, Inc) Максимальная чувствительность - 0, 005 ЕДэ/мл. (добавление хромогенного субстрата BOC-Leu-Gly-Arg-CONH- -NO 2 - простой полипептид с хромофором на конце , как более чувствительного индикатора эндотоксина, в присутствии которого LAL приобретает жёлтый цвет – р- нитроанлин, ) Апирогенная вода для LAL-теста - LAL-вода, предназначена для растворения LAL-реактива, приготовления растворов эндотоксина в разных концентрациях, разведения образцов, а также используется в качестве отрицательного контроля необходимо развести исходный препарат равным объемом раствора эндотоксина с концентрацией 4.
Реализация LAL-теста Гель-тромб тест (GLAL) (Pyrotell. R - Associates of Cape Cod, Inc) образование плотного геля на дне пробирки - контроль по переворачиванию Турбидиметрический LAL-тест (Pyrotell-TR - Associates of Cape Cod, Inc) чувствительность считывающего устройства (спектрофотометр Bio-Tek ELx 808 или аналогичный) − от 0, 001 ЕДэ/мл. Хромогенный LAL-тест (CLAL) (Pyrochrome. R - Associates of Cape Cod, Inc) Максимальная чувствительность - 0, 005 ЕДэ/мл. (добавление хромогенного субстрата BOC-Leu-Gly-Arg-CONH- -NO 2 - простой полипептид с хромофором на конце , как более чувствительного индикатора эндотоксина, в присутствии которого LAL приобретает жёлтый цвет – р- нитроанлин, ) Апирогенная вода для LAL-теста - LAL-вода, предназначена для растворения LAL-реактива, приготовления растворов эндотоксина в разных концентрациях, разведения образцов, а также используется в качестве отрицательного контроля необходимо развести исходный препарат равным объемом раствора эндотоксина с концентрацией 4.
 Метод А. Качественный гель-тромб тест Метод В. Количественный гель-тромб тест (разведение препарата водой) Метод С. Кинетический турбидиметрический тест (скорость изменения оптической плотности реакционной смеси) Метод D. Кинетический хромогенный тест Метод Е. Хромогенный тест по конечной точке Метод F. Турбидиметрический тест по конечной точке.
Метод А. Качественный гель-тромб тест Метод В. Количественный гель-тромб тест (разведение препарата водой) Метод С. Кинетический турбидиметрический тест (скорость изменения оптической плотности реакционной смеси) Метод D. Кинетический хромогенный тест Метод Е. Хромогенный тест по конечной точке Метод F. Турбидиметрический тест по конечной точке.
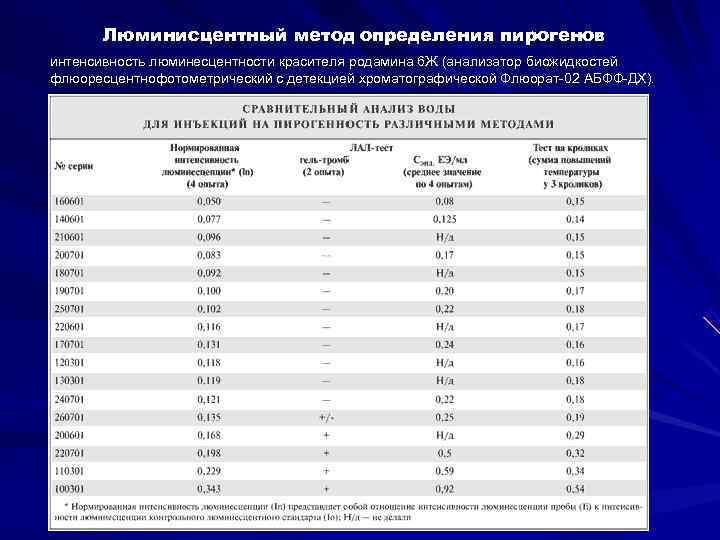
 Люминисцентный метод определения пирогенов интенсивность люминесцентности красителя родамина 6 Ж (анализатор биожидкостей флюоресцентнофотометрический с детекцией хроматографической Флюорат-02 АБФФ-ДХ).
Люминисцентный метод определения пирогенов интенсивность люминесцентности красителя родамина 6 Ж (анализатор биожидкостей флюоресцентнофотометрический с детекцией хроматографической Флюорат-02 АБФФ-ДХ).

