Органика Зейфмана.ppt
- Количество слайдов: 127
 Часть 1 Основные интермедиаты в органических реакциях
Часть 1 Основные интермедиаты в органических реакциях
 • Многие органические реакции проходят через образование промежуточных малостабильных частиц – карбокатионов, карбоанионов, радикалов… • Стабилизация частиц достигается в первую очередь за счет резонансных структур, а не индуктивных эффектов
• Многие органические реакции проходят через образование промежуточных малостабильных частиц – карбокатионов, карбоанионов, радикалов… • Стабилизация частиц достигается в первую очередь за счет резонансных структур, а не индуктивных эффектов
 Карбокатионы • Карбокатионы – неустойчивые частицы, в которых атом углерода имеет три заместителя и несет положительный заряд • Как правило плоские -> ахиральны
Карбокатионы • Карбокатионы – неустойчивые частицы, в которых атом углерода имеет три заместителя и несет положительный заряд • Как правило плоские -> ахиральны
 Устойчивость • Наличие донорных групп стабилизирует карбокатион. Например, устойчивость возрастает в ряду CH 3+>CH 3 CH 2+>CH(CH 3)2+>C(CH 3)3+ • Наличие в α-положении двойной связи стабилизирует карбокатион (Ph. CH 2+ и CH 2=CHCH 2+ стабильнее CH 3+)
Устойчивость • Наличие донорных групп стабилизирует карбокатион. Например, устойчивость возрастает в ряду CH 3+>CH 3 CH 2+>CH(CH 3)2+>C(CH 3)3+ • Наличие в α-положении двойной связи стабилизирует карбокатион (Ph. CH 2+ и CH 2=CHCH 2+ стабильнее CH 3+)
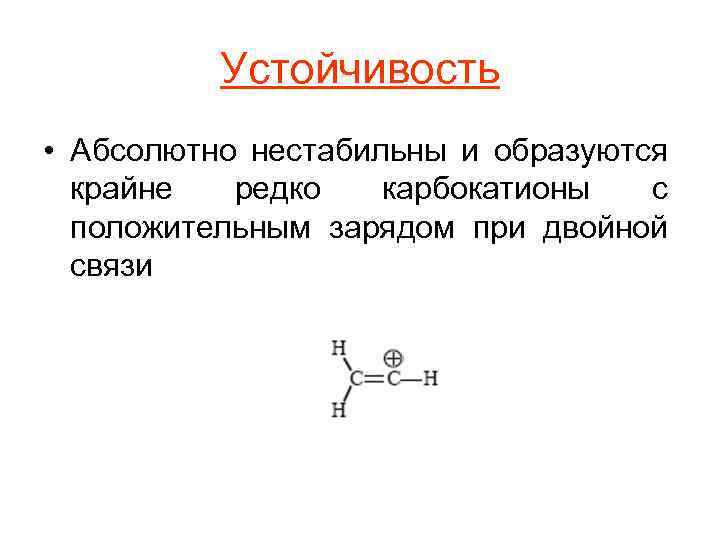 Устойчивость • Абсолютно нестабильны и образуются крайне редко карбокатионы с положительным зарядом при двойной связи
Устойчивость • Абсолютно нестабильны и образуются крайне редко карбокатионы с положительным зарядом при двойной связи
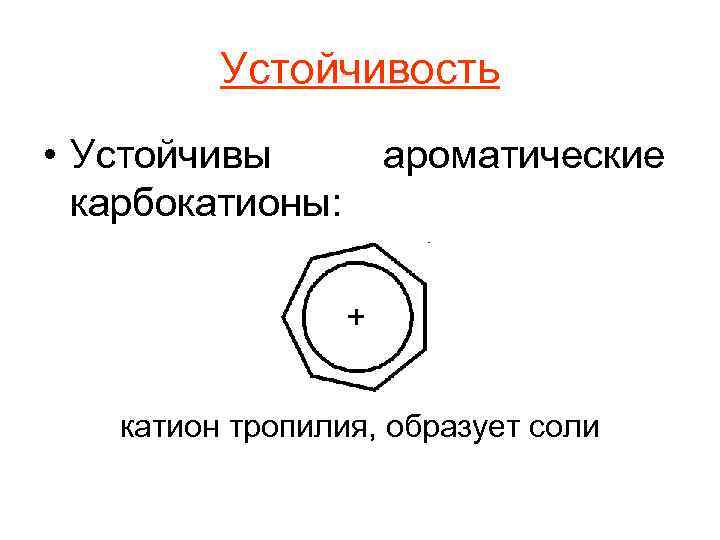 Устойчивость • Устойчивы карбокатионы: ароматические катион тропилия, образует соли
Устойчивость • Устойчивы карбокатионы: ароматические катион тропилия, образует соли
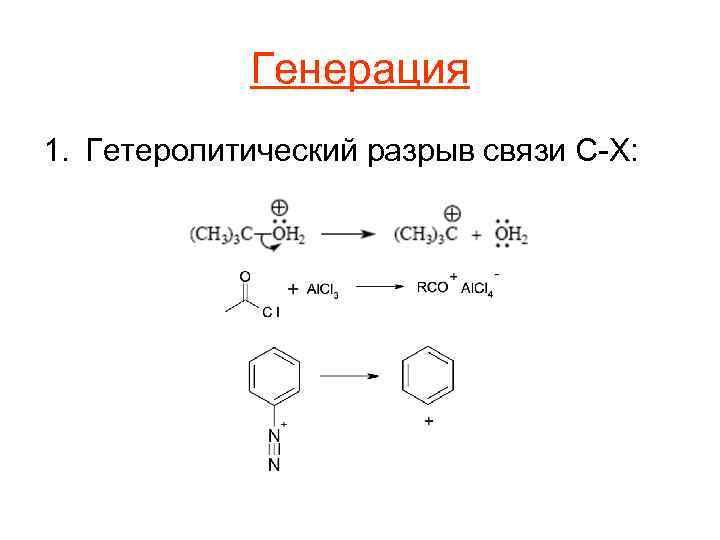 Генерация 1. Гетеролитический разрыв связи C-X:
Генерация 1. Гетеролитический разрыв связи C-X:
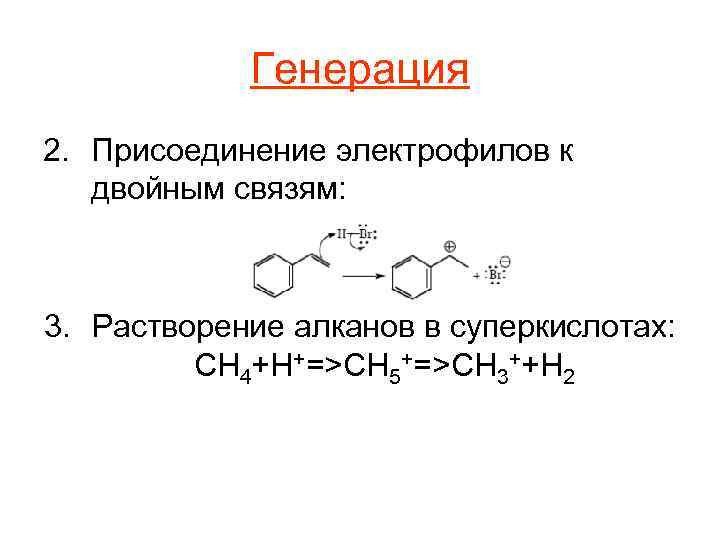 Генерация 2. Присоединение электрофилов к двойным связям: 3. Растворение алканов в суперкислотах: CH 4+H+=>CH 5+=>CH 3++H 2
Генерация 2. Присоединение электрофилов к двойным связям: 3. Растворение алканов в суперкислотах: CH 4+H+=>CH 5+=>CH 3++H 2
 Реакции 1. Выброс протона – приводит образованию двойной связи: Необходимо содействие основания (даже слабого) к
Реакции 1. Выброс протона – приводит образованию двойной связи: Необходимо содействие основания (даже слабого) к
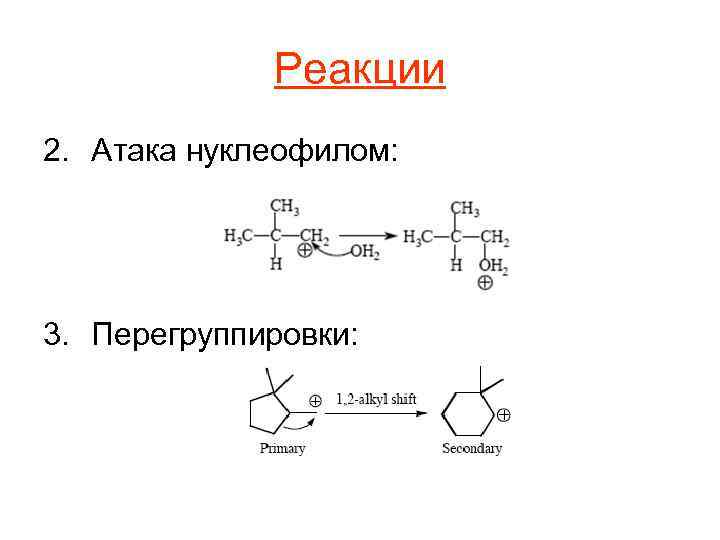 Реакции 2. Атака нуклеофилом: 3. Перегруппировки:
Реакции 2. Атака нуклеофилом: 3. Перегруппировки:
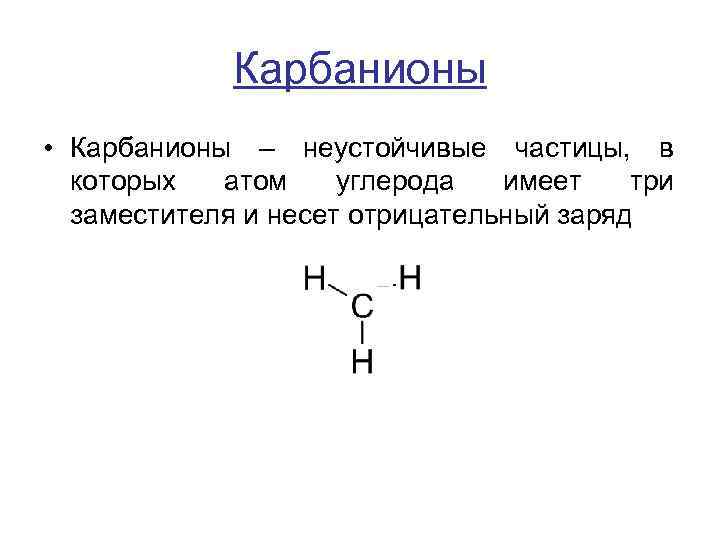 Карбанионы • Карбанионы – неустойчивые частицы, в которых атом углерода имеет три заместителя и несет отрицательный заряд
Карбанионы • Карбанионы – неустойчивые частицы, в которых атом углерода имеет три заместителя и несет отрицательный заряд
 Устойчивость • Наличие акцепторных групп стабилизирует карбанион: p. Ka для кетонов ~25, а для алканов ~50 • Относительно более стабильны анионы аллильного и бензильного типа • Стабильны ароматические карбанионы:
Устойчивость • Наличие акцепторных групп стабилизирует карбанион: p. Ka для кетонов ~25, а для алканов ~50 • Относительно более стабильны анионы аллильного и бензильного типа • Стабильны ароматические карбанионы:
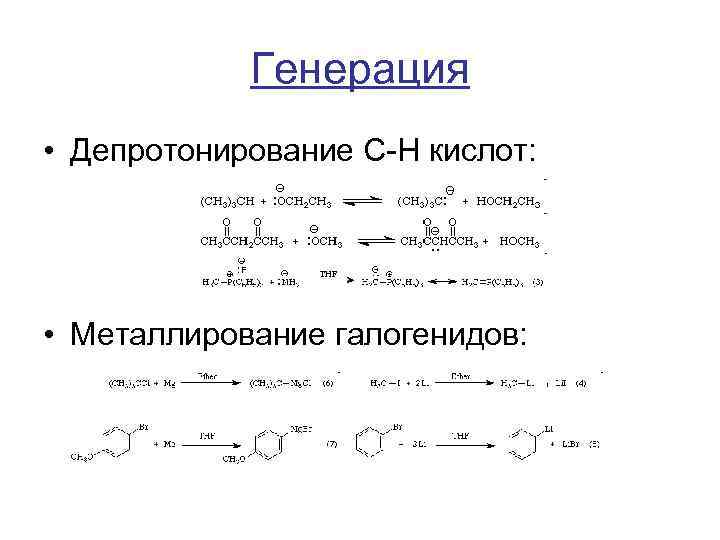 Генерация • Депротонирование C-H кислот: • Металлирование галогенидов:
Генерация • Депротонирование C-H кислот: • Металлирование галогенидов:
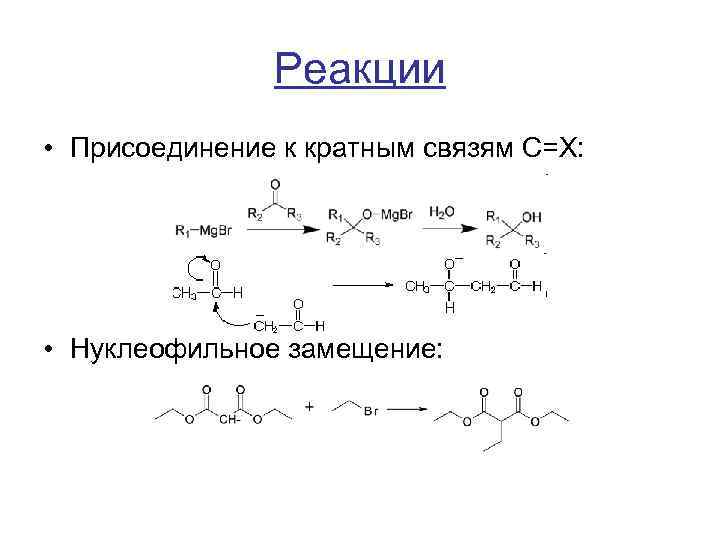 Реакции • Присоединение к кратным связям C=X: • Нуклеофильное замещение:
Реакции • Присоединение к кратным связям C=X: • Нуклеофильное замещение:
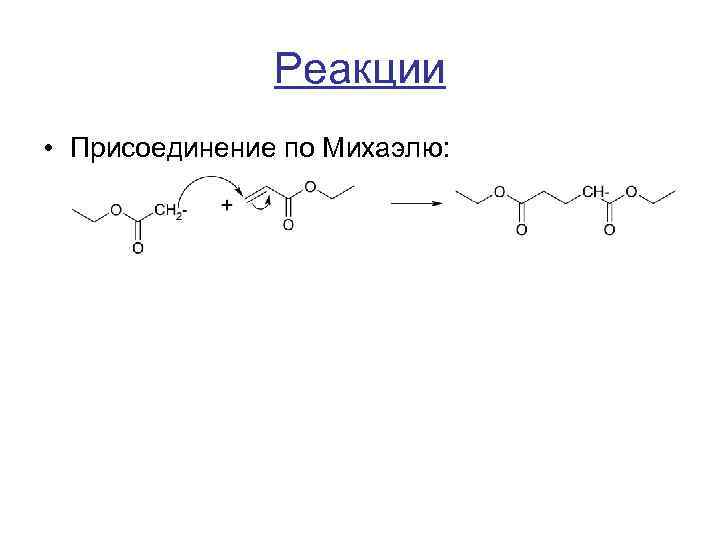 Реакции • Присоединение по Михаэлю:
Реакции • Присоединение по Михаэлю:
 Радикалы • В общем случае – частицы с неспаренными электронами • В общем случае не обязательно плоские
Радикалы • В общем случае – частицы с неспаренными электронами • В общем случае не обязательно плоские
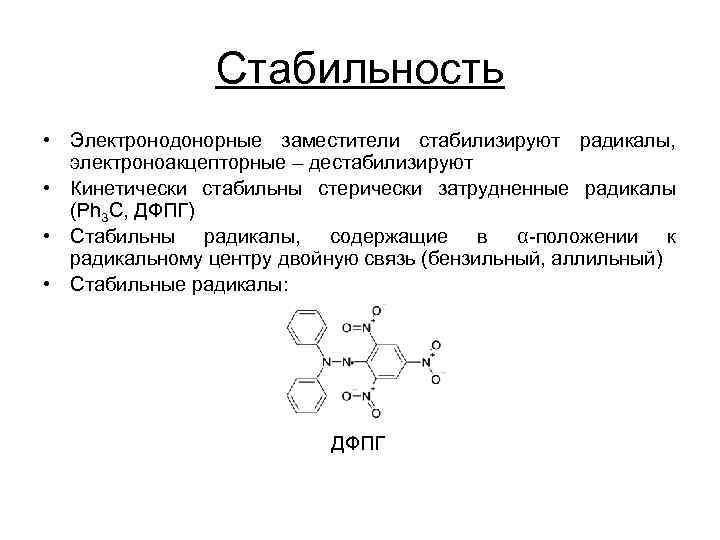 Стабильность • Электронодонорные заместители стабилизируют радикалы, электроноакцепторные – дестабилизируют • Кинетически стабильны стерически затрудненные радикалы (Ph 3 C, ДФПГ) • Стабильны радикалы, содержащие в α-положении к радикальному центру двойную связь (бензильный, аллильный) • Стабильные радикалы: ДФПГ
Стабильность • Электронодонорные заместители стабилизируют радикалы, электроноакцепторные – дестабилизируют • Кинетически стабильны стерически затрудненные радикалы (Ph 3 C, ДФПГ) • Стабильны радикалы, содержащие в α-положении к радикальному центру двойную связь (бензильный, аллильный) • Стабильные радикалы: ДФПГ
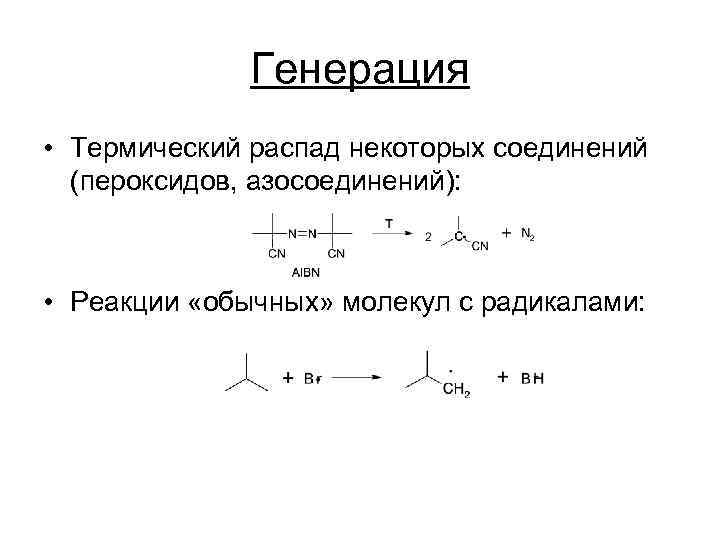 Генерация • Термический распад некоторых соединений (пероксидов, азосоединений): • Реакции «обычных» молекул с радикалами:
Генерация • Термический распад некоторых соединений (пероксидов, азосоединений): • Реакции «обычных» молекул с радикалами:
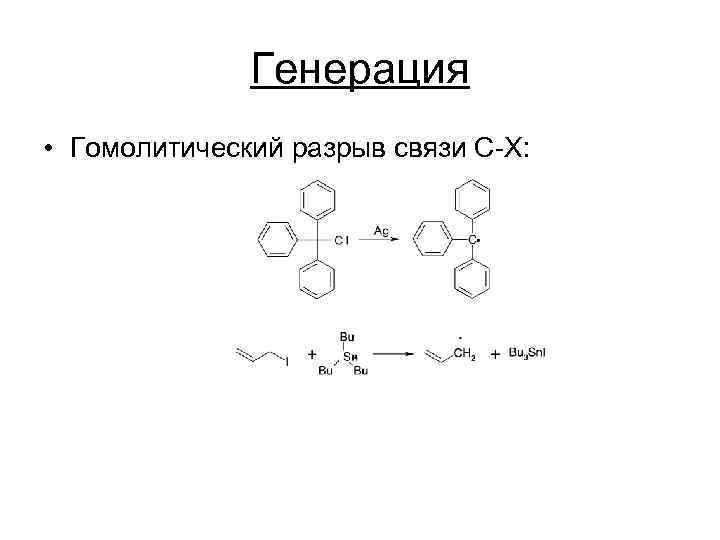 Генерация • Гомолитический разрыв связи C-X:
Генерация • Гомолитический разрыв связи C-X:
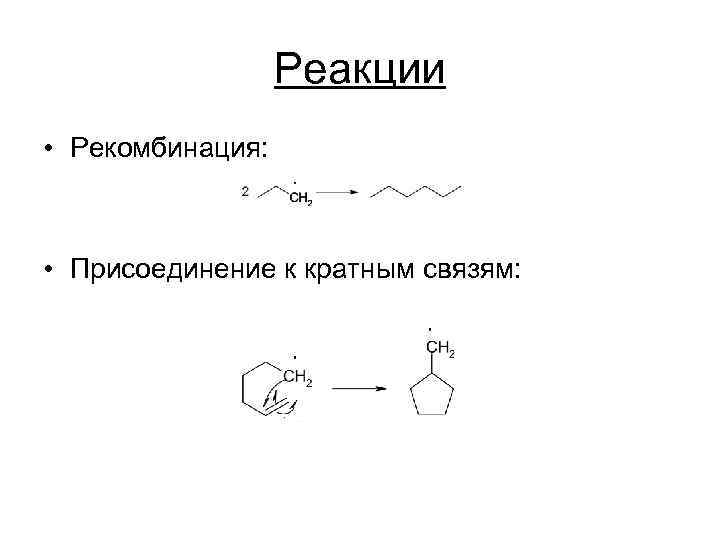 Реакции • Рекомбинация: • Присоединение к кратным связям:
Реакции • Рекомбинация: • Присоединение к кратным связям:
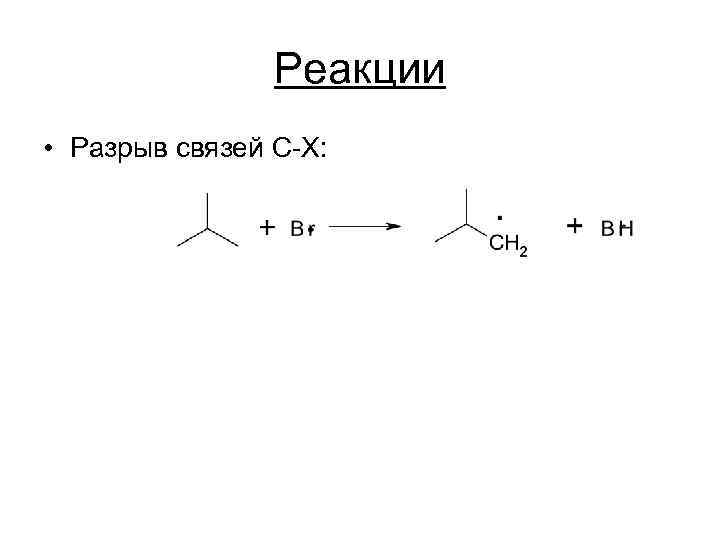 Реакции • Разрыв связей C-X:
Реакции • Разрыв связей C-X:
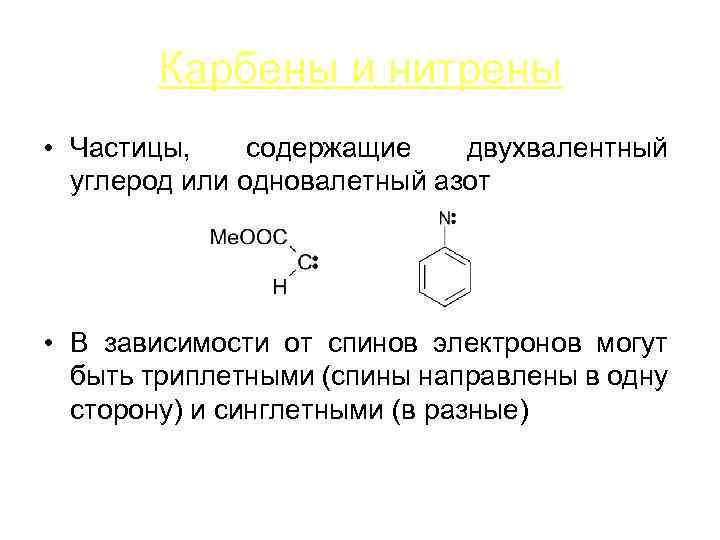 Карбены и нитрены • Частицы, содержащие двухвалентный углерод или одновалетный азот • В зависимости от спинов электронов могут быть триплетными (спины направлены в одну сторону) и синглетными (в разные)
Карбены и нитрены • Частицы, содержащие двухвалентный углерод или одновалетный азот • В зависимости от спинов электронов могут быть триплетными (спины направлены в одну сторону) и синглетными (в разные)
 Устойчивость • Все карбены крайне неустойчивы • Возможна стабилизация за счет резонанса (опять же арильные и винильные заместители)
Устойчивость • Все карбены крайне неустойчивы • Возможна стабилизация за счет резонанса (опять же арильные и винильные заместители)
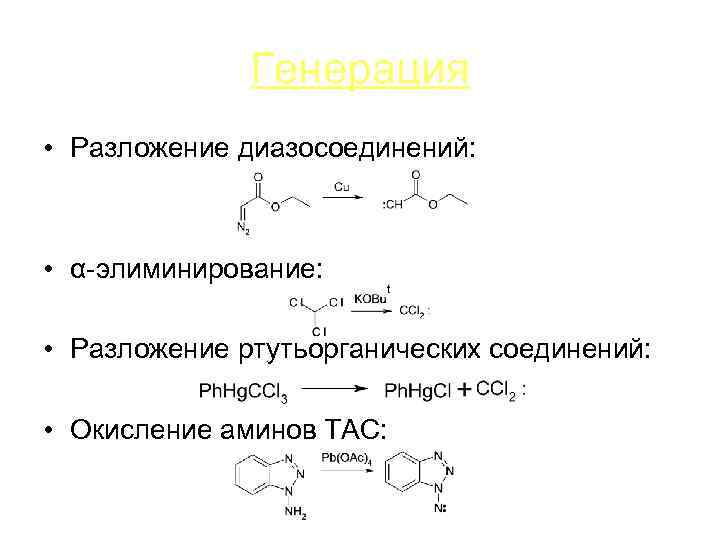 Генерация • Разложение диазосоединений: • α-элиминирование: • Разложение ртутьорганических соединений: • Окисление аминов ТАС:
Генерация • Разложение диазосоединений: • α-элиминирование: • Разложение ртутьорганических соединений: • Окисление аминов ТАС:
 Реакции • Встраивание в связь C-X: • Циклоприсоединение к кратным связям:
Реакции • Встраивание в связь C-X: • Циклоприсоединение к кратным связям:
 Помимо описанных выше частиц существует много других (ионрадикалы, арины, металлоорганические соединения). Они встречаются реже и будут рассмотрены в соответствующих реакциях
Помимо описанных выше частиц существует много других (ионрадикалы, арины, металлоорганические соединения). Они встречаются реже и будут рассмотрены в соответствующих реакциях
 Часть 2 Основные механизмы органических реакций
Часть 2 Основные механизмы органических реакций
 Нуклеофильное замещение R-X+Nu: ->R-Nu+X: • Нуклеофил – частица (ион, молекула), имеющая электронную пару • Нуклеофильное замещение может проходить по механизмам SN 1, SN 2, SNAr, SNi
Нуклеофильное замещение R-X+Nu: ->R-Nu+X: • Нуклеофил – частица (ион, молекула), имеющая электронную пару • Нуклеофильное замещение может проходить по механизмам SN 1, SN 2, SNAr, SNi
 S N 1 • Мономолекулярное нуклеофильное замещение при четырехкоординированном углероде (скорость реакции пропорциональна концентрации субстрата и не зависит от концентрации нуклеофила): • Промежуточно образуется карбокатион
S N 1 • Мономолекулярное нуклеофильное замещение при четырехкоординированном углероде (скорость реакции пропорциональна концентрации субстрата и не зависит от концентрации нуклеофила): • Промежуточно образуется карбокатион
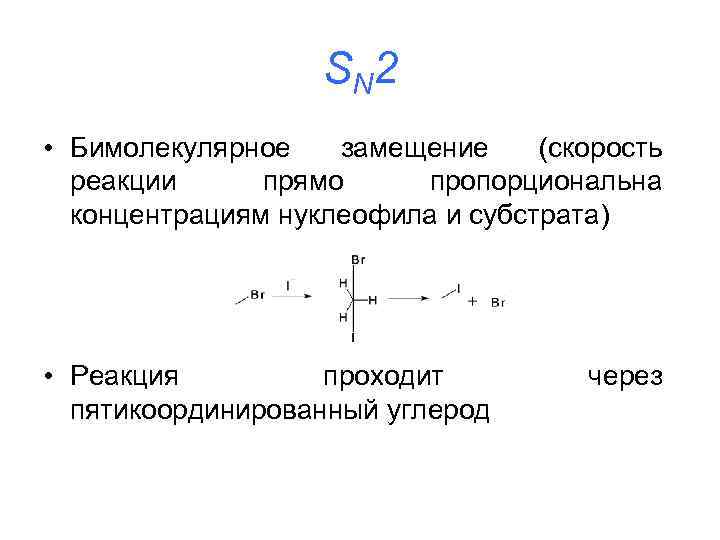 S N 2 • Бимолекулярное замещение (скорость реакции прямо пропорциональна концентрациям нуклеофила и субстрата) • Реакция проходит пятикоординированный углерод через
S N 2 • Бимолекулярное замещение (скорость реакции прямо пропорциональна концентрациям нуклеофила и субстрата) • Реакция проходит пятикоординированный углерод через
 Сравнение SN 1 и SN 2 • SN 2 приводит к полному обращению конфигурации, SN 1 – к полной (частичной) рацемизации • SN 2 не проходит для субстратов, содержащих объемные группы при атакуемом атоме углерода (например (CH 3)3 CCI) • Оптимальный растворитель для SN 1 – достаточно кислый протонный (CH 3 COOH), а для SN 2 – биполярный апротонный (ДМФА, ацетон)
Сравнение SN 1 и SN 2 • SN 2 приводит к полному обращению конфигурации, SN 1 – к полной (частичной) рацемизации • SN 2 не проходит для субстратов, содержащих объемные группы при атакуемом атоме углерода (например (CH 3)3 CCI) • Оптимальный растворитель для SN 1 – достаточно кислый протонный (CH 3 COOH), а для SN 2 – биполярный апротонный (ДМФА, ацетон)
 SNAr • Нуклеофильное замещение в ароматических соединениях • Может проходить через комплекс Мейзенхеймера, арины, по радикальному механизму и механизму ANRORC
SNAr • Нуклеофильное замещение в ароматических соединениях • Может проходить через комплекс Мейзенхеймера, арины, по радикальному механизму и механизму ANRORC
 SNAr через комплекс Мейзенхеймера • Характерно для активированных субстратов (содержащих электроноакцепторные группы) • Для неактивированных субстратов проходит с очень большим трудом (реакция хлорбензола с Na. OH проходит при 350 o. С и под давлением)
SNAr через комплекс Мейзенхеймера • Характерно для активированных субстратов (содержащих электроноакцепторные группы) • Для неактивированных субстратов проходит с очень большим трудом (реакция хлорбензола с Na. OH проходит при 350 o. С и под давлением)
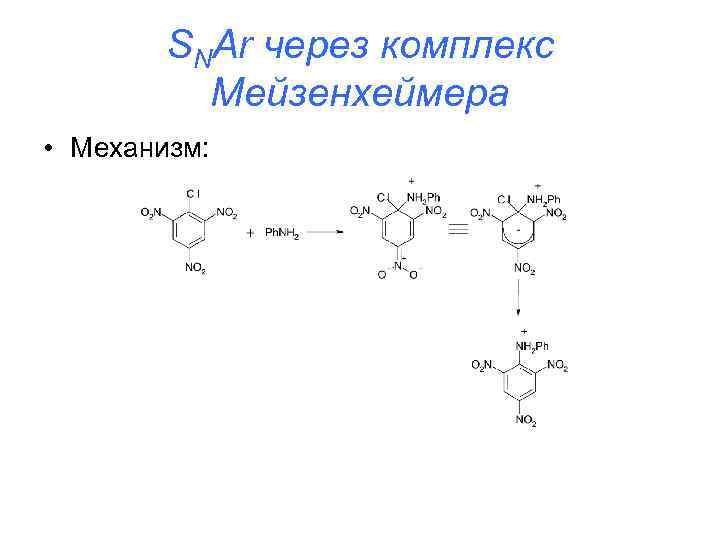 SNAr через комплекс Мейзенхеймера • Механизм:
SNAr через комплекс Мейзенхеймера • Механизм:
 SNAr через образование аринов • Протекает под действием сильных оснований • Приводит к образованию смеси продуктов
SNAr через образование аринов • Протекает под действием сильных оснований • Приводит к образованию смеси продуктов
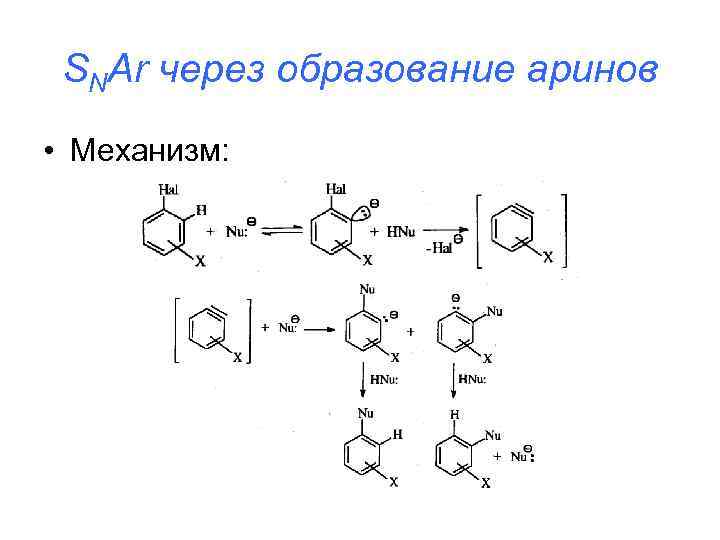 SNAr через образование аринов • Механизм:
SNAr через образование аринов • Механизм:
 ANRORC • Addition of Nucleofile, Ring Opening, Ring Cloisure (присоединение нуклеофила, раскрытие цикла, закрытие цикла)
ANRORC • Addition of Nucleofile, Ring Opening, Ring Cloisure (присоединение нуклеофила, раскрытие цикла, закрытие цикла)
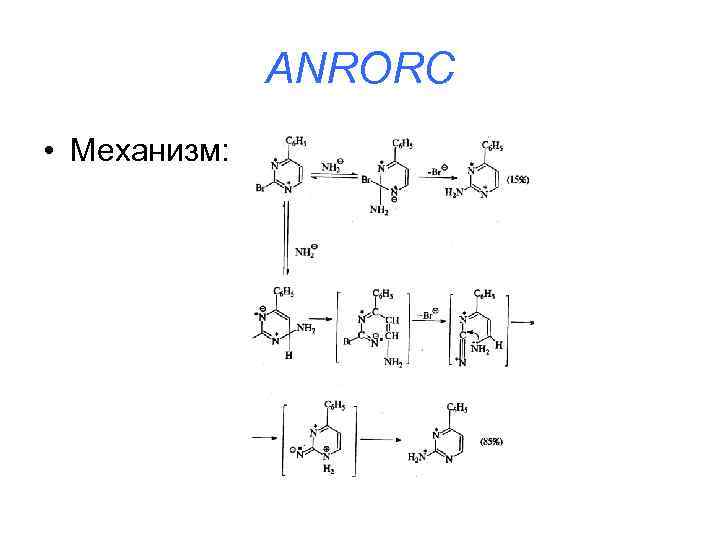 ANRORC • Механизм:
ANRORC • Механизм:
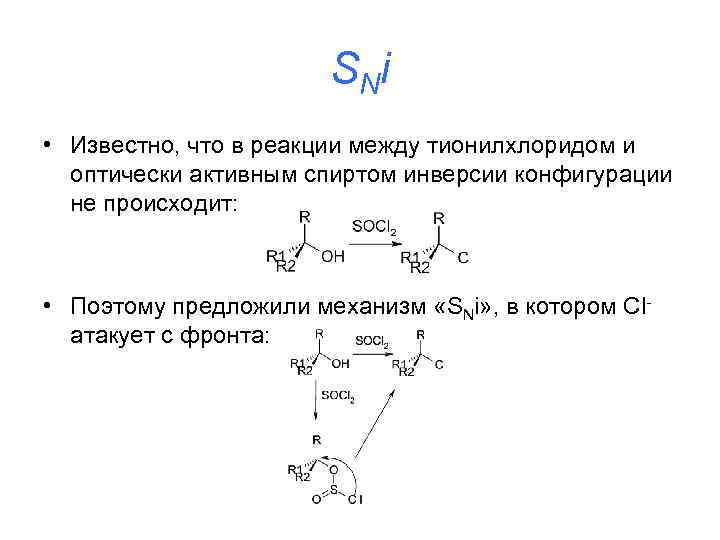 S Ni • Известно, что в реакции между тионилхлоридом и оптически активным спиртом инверсии конфигурации не происходит: • Поэтому предложили механизм «SNi» , в котором Clатакует с фронта:
S Ni • Известно, что в реакции между тионилхлоридом и оптически активным спиртом инверсии конфигурации не происходит: • Поэтому предложили механизм «SNi» , в котором Clатакует с фронта:
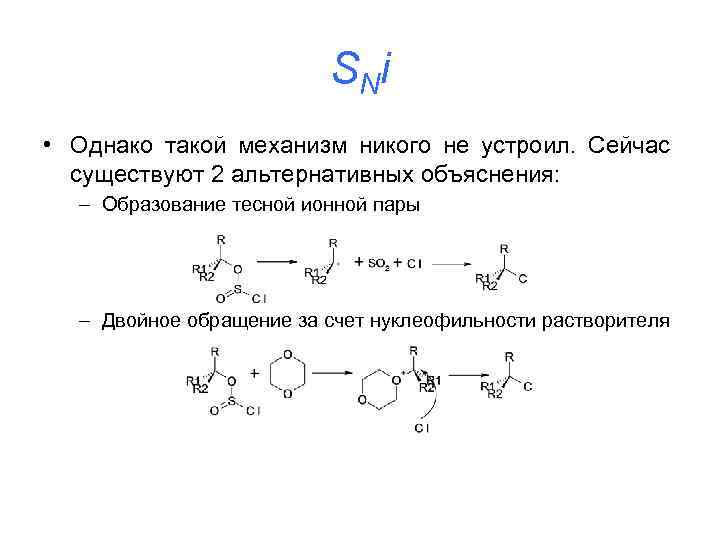 S Ni • Однако такой механизм никого не устроил. Сейчас существуют 2 альтернативных объяснения: – Образование тесной ионной пары – Двойное обращение за счет нуклеофильности растворителя
S Ni • Однако такой механизм никого не устроил. Сейчас существуют 2 альтернативных объяснения: – Образование тесной ионной пары – Двойное обращение за счет нуклеофильности растворителя
 Нуклеофильное присоединение • Присоединение нуклеофильных реагентов к кратной связи (в основном к связям C=X, где X=O, N) • Реакция обратима!
Нуклеофильное присоединение • Присоединение нуклеофильных реагентов к кратной связи (в основном к связям C=X, где X=O, N) • Реакция обратима!
 Электрофильное замещение • Характерно для ароматических субстратов (SEAr) • Механизм: • Правила ориентации (школьная программа)
Электрофильное замещение • Характерно для ароматических субстратов (SEAr) • Механизм: • Правила ориентации (школьная программа)
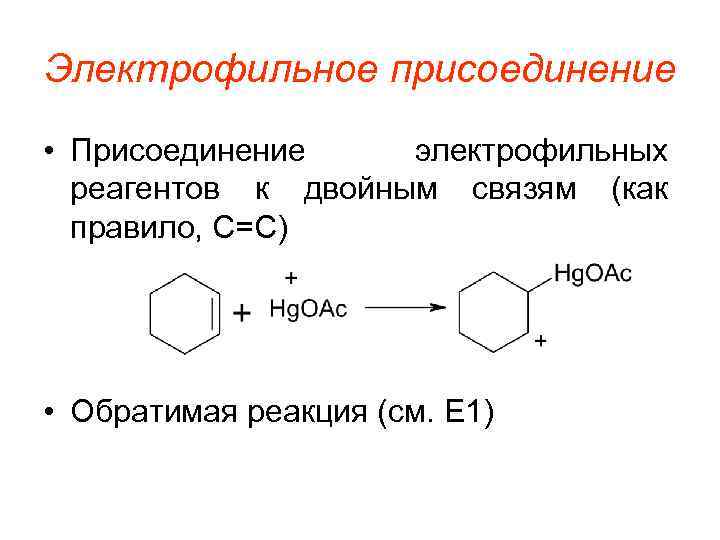 Электрофильное присоединение • Присоединение электрофильных реагентов к двойным связям (как правило, C=C) • Обратимая реакция (см. E 1)
Электрофильное присоединение • Присоединение электрофильных реагентов к двойным связям (как правило, C=C) • Обратимая реакция (см. E 1)
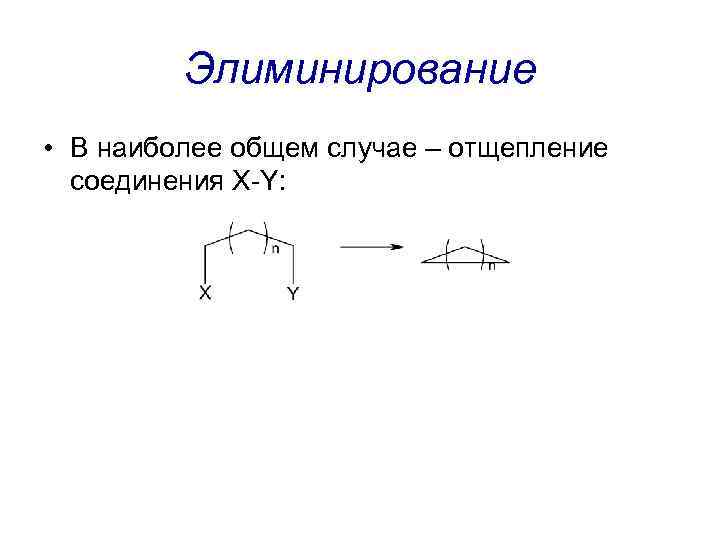 Элиминирование • В наиболее общем случае – отщепление соединения X-Y:
Элиминирование • В наиболее общем случае – отщепление соединения X-Y:
 Элиминирование • α-элиминирование: • β-элиминирование: • γ-элиминирование:
Элиминирование • α-элиминирование: • β-элиминирование: • γ-элиминирование:
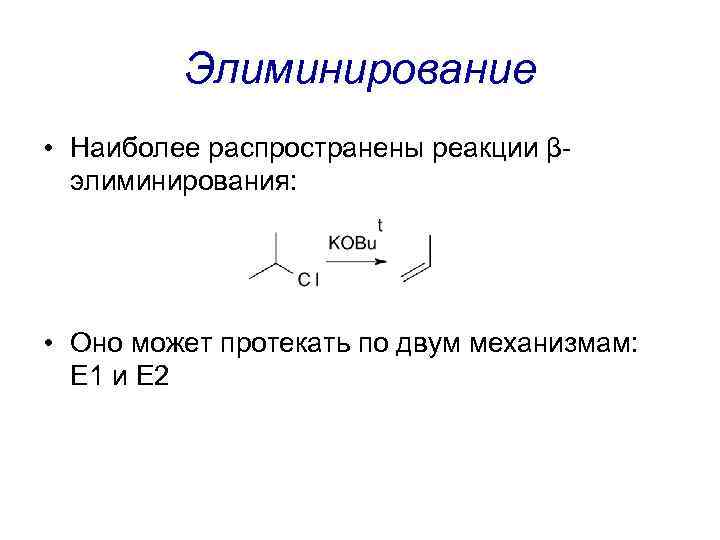 Элиминирование • Наиболее распространены реакции βэлиминирования: • Оно может протекать по двум механизмам: E 1 и E 2
Элиминирование • Наиболее распространены реакции βэлиминирования: • Оно может протекать по двум механизмам: E 1 и E 2
 Элиминирование • E 1: мономолекулярное элиминирование; проходит через образование карбокатиона в достаточно кислых средах • E 2: бимолекулярное элиминирование; антиперипланарного расположения H и X требует
Элиминирование • E 1: мономолекулярное элиминирование; проходит через образование карбокатиона в достаточно кислых средах • E 2: бимолекулярное элиминирование; антиперипланарного расположения H и X требует
 Элиминирование • При β-элиминировании как правило образуется наиболее замещенный и транс-алкен (правило Зайцева) • Исключение из правила Зайцева – разложение гидроксидов четвертичных аминов (реакция Гофмана): • Как правило, элиминирование конкурирует с нуклеофильным замещением; при этом элиминированию способствует нагревание и использование сильных оснований
Элиминирование • При β-элиминировании как правило образуется наиболее замещенный и транс-алкен (правило Зайцева) • Исключение из правила Зайцева – разложение гидроксидов четвертичных аминов (реакция Гофмана): • Как правило, элиминирование конкурирует с нуклеофильным замещением; при этом элиминированию способствует нагревание и использование сильных оснований
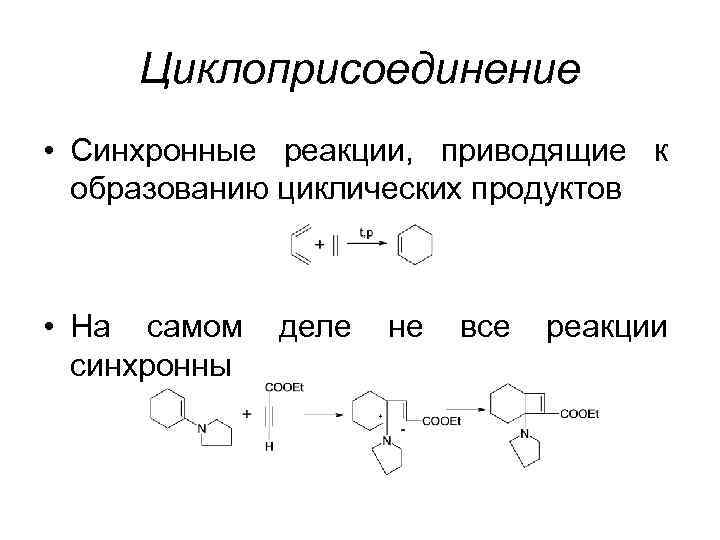 Циклоприсоединение • Синхронные реакции, приводящие к образованию циклических продуктов • На самом синхронны деле не все реакции
Циклоприсоединение • Синхронные реакции, приводящие к образованию циклических продуктов • На самом синхронны деле не все реакции
![[1, n]-сдвиги • Сдвиги заместителей (характерны для карбокатионов и карбанинов) • [1, 2]-гидридный сдвиг: [1, n]-сдвиги • Сдвиги заместителей (характерны для карбокатионов и карбанинов) • [1, 2]-гидридный сдвиг:](https://present5.com/presentation/3/-19759704_126575846.pdf-img/-19759704_126575846.pdf-50.jpg) [1, n]-сдвиги • Сдвиги заместителей (характерны для карбокатионов и карбанинов) • [1, 2]-гидридный сдвиг: • [1, 2]-алкильный сдвиг:
[1, n]-сдвиги • Сдвиги заместителей (характерны для карбокатионов и карбанинов) • [1, 2]-гидридный сдвиг: • [1, 2]-алкильный сдвиг:
 Часть 3 Именные и безымянные органические реакции
Часть 3 Именные и безымянные органические реакции
 Конденсации • Реакции образования C-C связей, протекающие с отщеплением небольших молекул • В большинстве реакций участвуют карбонильные соединения • Мощный метод построения углеродного скелета
Конденсации • Реакции образования C-C связей, протекающие с отщеплением небольших молекул • В большинстве реакций участвуют карбонильные соединения • Мощный метод построения углеродного скелета
 Альдольно-кротоновая конденсация • Конденсация двух молекул кетона, проходящая под действием основания или кислоты • В зависимости от условий может получиться гидроксикетон (альдоль) или непредельный кетон (кротон) • Возможны асимметрические варианты • Можно вводить в реакцию 2 разных кетона (важен порядок прибавления реагентов)
Альдольно-кротоновая конденсация • Конденсация двух молекул кетона, проходящая под действием основания или кислоты • В зависимости от условий может получиться гидроксикетон (альдоль) или непредельный кетон (кротон) • Возможны асимметрические варианты • Можно вводить в реакцию 2 разных кетона (важен порядок прибавления реагентов)
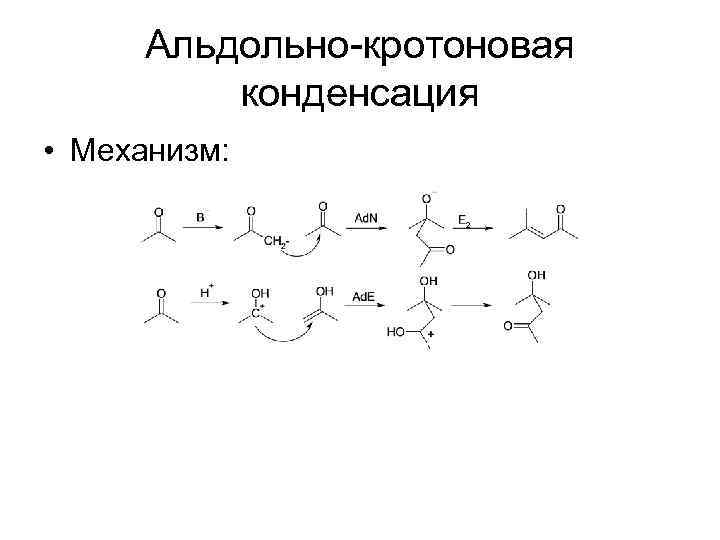 Альдольно-кротоновая конденсация • Механизм:
Альдольно-кротоновая конденсация • Механизм:
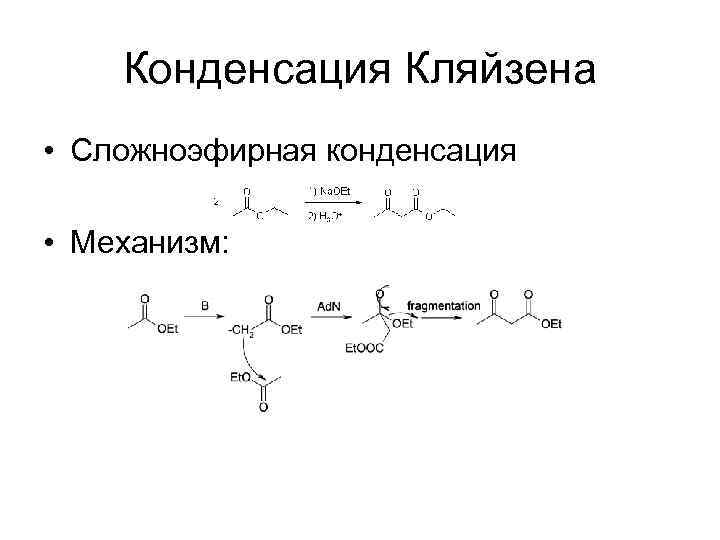 Конденсация Кляйзена • Сложноэфирная конденсация • Механизм:
Конденсация Кляйзена • Сложноэфирная конденсация • Механизм:
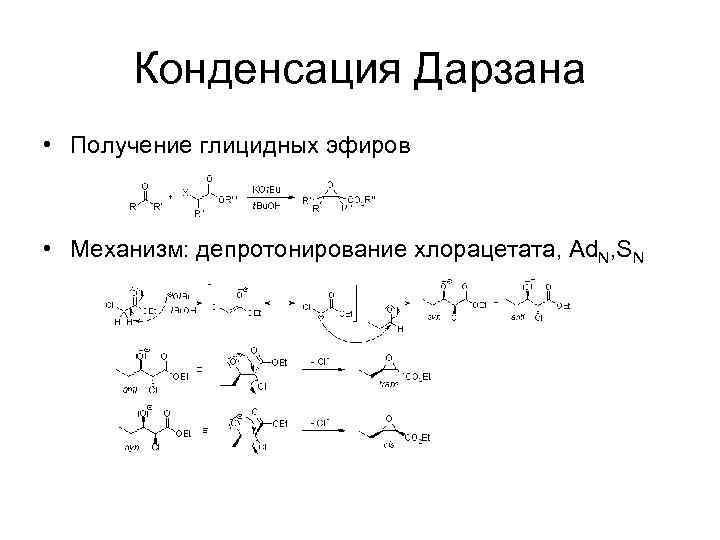 Конденсация Дарзана • Получение глицидных эфиров • Механизм: депротонирование хлорацетата, Ad. N, SN
Конденсация Дарзана • Получение глицидных эфиров • Механизм: депротонирование хлорацетата, Ad. N, SN
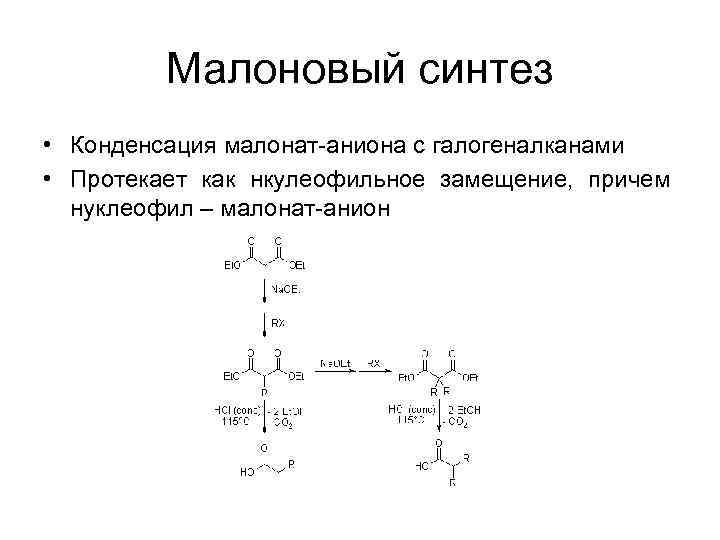 Малоновый синтез • Конденсация малонат-аниона с галогеналканами • Протекает как нкулеофильное замещение, причем нуклеофил – малонат-анион
Малоновый синтез • Конденсация малонат-аниона с галогеналканами • Протекает как нкулеофильное замещение, причем нуклеофил – малонат-анион
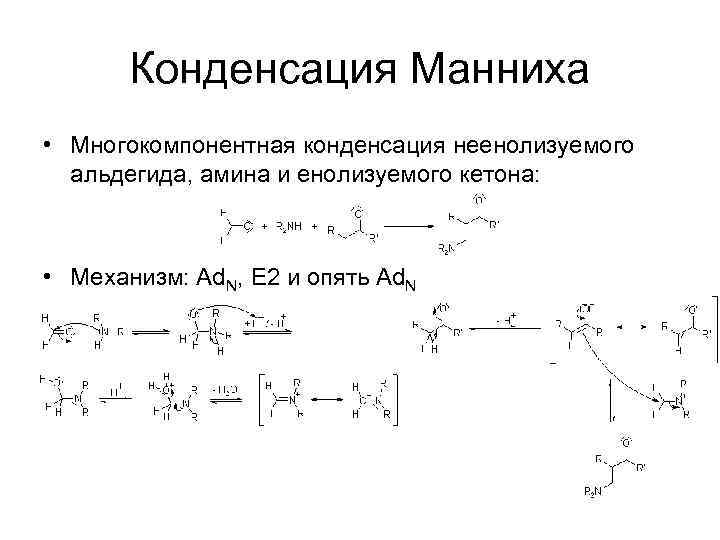 Конденсация Манниха • Многокомпонентная конденсация неенолизуемого альдегида, амина и енолизуемого кетона: • Механизм: Ad. N, E 2 и опять Ad. N
Конденсация Манниха • Многокомпонентная конденсация неенолизуемого альдегида, амина и енолизуемого кетона: • Механизм: Ad. N, E 2 и опять Ad. N
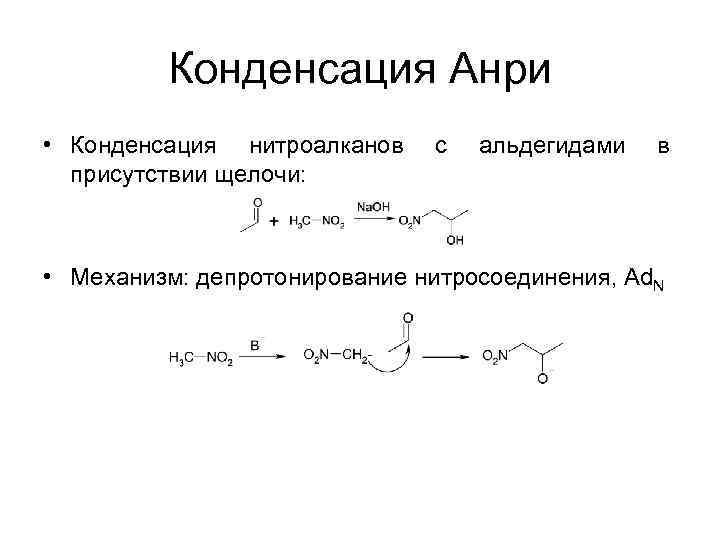 Конденсация Анри • Конденсация нитроалканов присутствии щелочи: с альдегидами в • Механизм: депротонирование нитросоединения, Ad. N
Конденсация Анри • Конденсация нитроалканов присутствии щелочи: с альдегидами в • Механизм: депротонирование нитросоединения, Ad. N
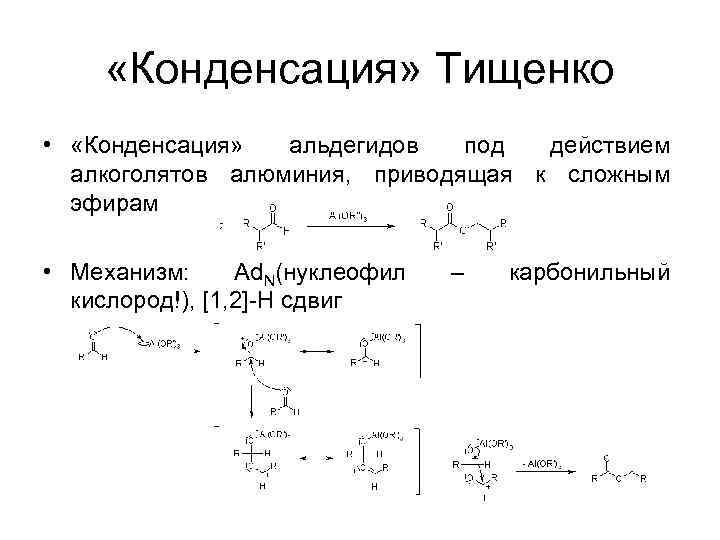 «Конденсация» Тищенко • «Конденсация» альдегидов под действием алкоголятов алюминия, приводящая к сложным эфирам • Механизм: Ad. N(нуклеофил кислород!), [1, 2]-H сдвиг – карбонильный
«Конденсация» Тищенко • «Конденсация» альдегидов под действием алкоголятов алюминия, приводящая к сложным эфирам • Механизм: Ad. N(нуклеофил кислород!), [1, 2]-H сдвиг – карбонильный
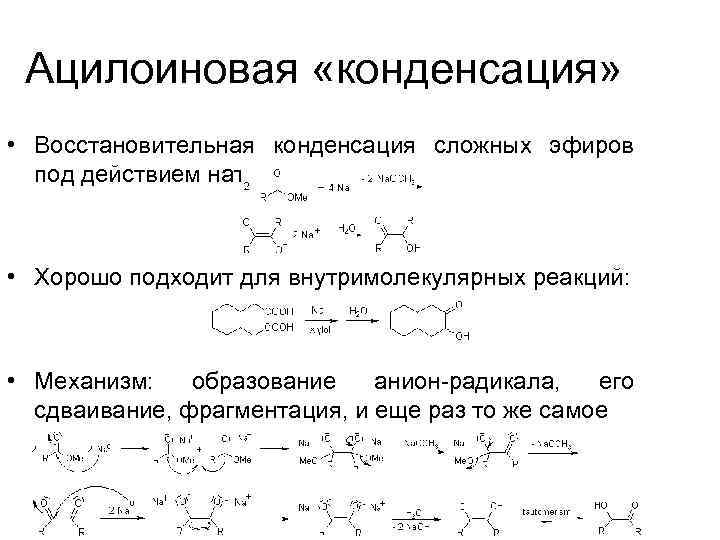 Ацилоиновая «конденсация» • Восстановительная конденсация сложных эфиров под действием натрия: • Хорошо подходит для внутримолекулярных реакций: • Механизм: образование анион-радикала, его сдваивание, фрагментация, и еще раз то же самое
Ацилоиновая «конденсация» • Восстановительная конденсация сложных эфиров под действием натрия: • Хорошо подходит для внутримолекулярных реакций: • Механизм: образование анион-радикала, его сдваивание, фрагментация, и еще раз то же самое
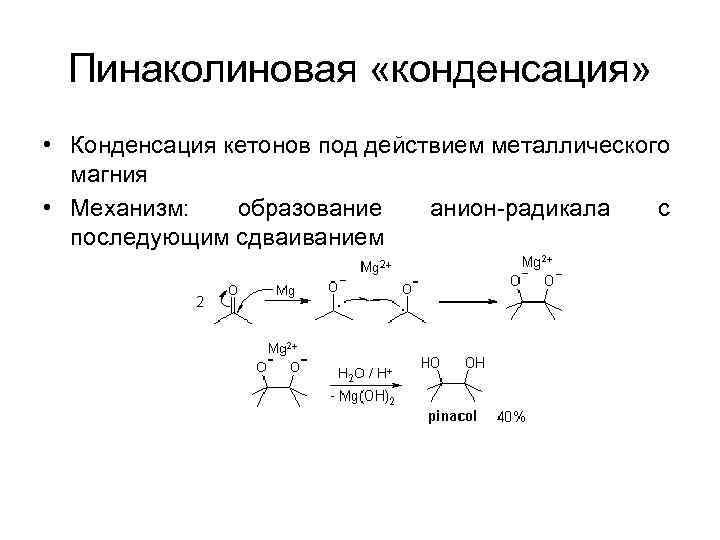 Пинаколиновая «конденсация» • Конденсация кетонов под действием металлического магния • Механизм: образование анион-радикала с последующим сдваиванием
Пинаколиновая «конденсация» • Конденсация кетонов под действием металлического магния • Механизм: образование анион-радикала с последующим сдваиванием
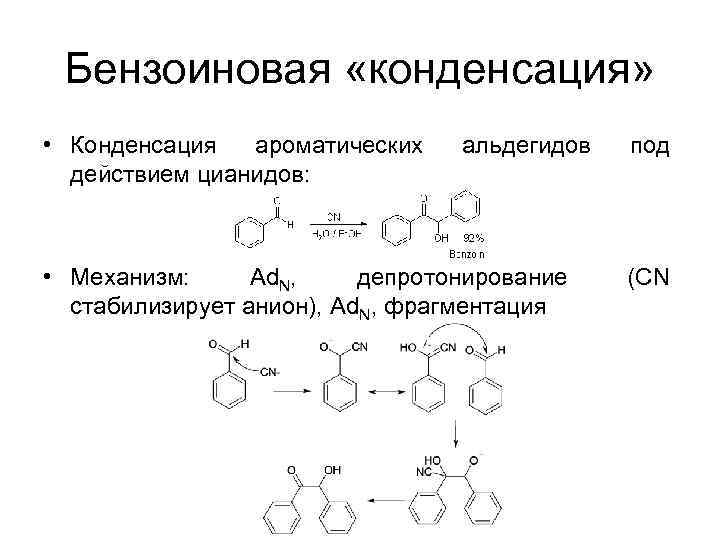 Бензоиновая «конденсация» • Конденсация ароматических действием цианидов: альдегидов • Механизм: Ad. N, депротонирование стабилизирует анион), Ad. N, фрагментация под (CN
Бензоиновая «конденсация» • Конденсация ароматических действием цианидов: альдегидов • Механизм: Ad. N, депротонирование стабилизирует анион), Ad. N, фрагментация под (CN
 Реакции окисления и восстановления • Формально очень многие органические реакции относятся к ОВ-реакциям (например, SEAr), но мы не будем их рассматривать с такой точки зрения
Реакции окисления и восстановления • Формально очень многие органические реакции относятся к ОВ-реакциям (например, SEAr), но мы не будем их рассматривать с такой точки зрения
 Восстановление карбонильных соединений • Реакционная способность падает RCHO>RCOR’>RCOO • Наиболее мощный восстановитель Восстанавливает все до спиртов: в – ряду Li. Al. H 4. • Боргидрид натрия Na. BH 4 восстанавливает альдегиды и кетоны (с трудом) • Вариации на тему боргидрида натрия – ацетоксиборгидрид натрия Na. BH(OAc)3, цианоборгидрид натрия Na. BH 3 CN, L-селектрид K[BH(CH(CH 3)C(CH)3)3] – более селективны
Восстановление карбонильных соединений • Реакционная способность падает RCHO>RCOR’>RCOO • Наиболее мощный восстановитель Восстанавливает все до спиртов: в – ряду Li. Al. H 4. • Боргидрид натрия Na. BH 4 восстанавливает альдегиды и кетоны (с трудом) • Вариации на тему боргидрида натрия – ацетоксиборгидрид натрия Na. BH(OAc)3, цианоборгидрид натрия Na. BH 3 CN, L-селектрид K[BH(CH(CH 3)C(CH)3)3] – более селективны
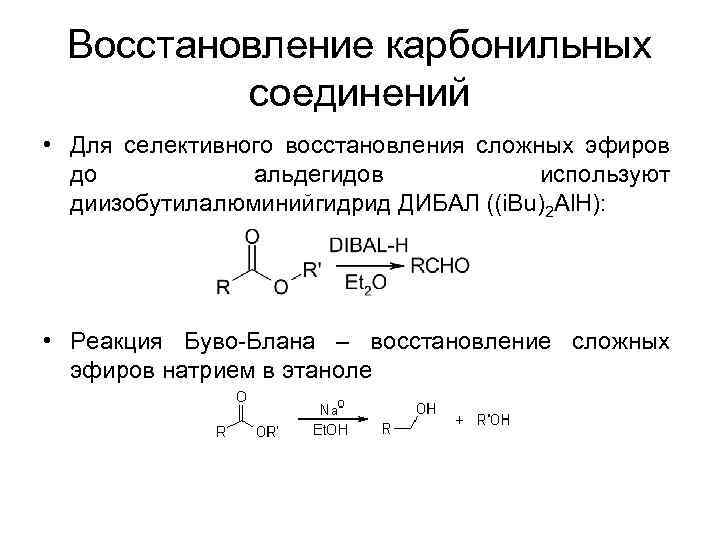 Восстановление карбонильных соединений • Для селективного восстановления сложных эфиров до альдегидов используют диизобутилалюминийгидрид ДИБАЛ ((i. Bu)2 Al. H): • Реакция Буво-Блана – восстановление сложных эфиров натрием в этаноле
Восстановление карбонильных соединений • Для селективного восстановления сложных эфиров до альдегидов используют диизобутилалюминийгидрид ДИБАЛ ((i. Bu)2 Al. H): • Реакция Буво-Блана – восстановление сложных эфиров натрием в этаноле
 Реакция Вольфа-Кижнера • Превращение кетонов в гидразоны с последующим нагреванием со щелочью в высококипящем растворителе (этиленгликоле): • Механизм: присоединение – фрагментация, депротонирование гидразона и отщепление N 2
Реакция Вольфа-Кижнера • Превращение кетонов в гидразоны с последующим нагреванием со щелочью в высококипящем растворителе (этиленгликоле): • Механизм: присоединение – фрагментация, депротонирование гидразона и отщепление N 2
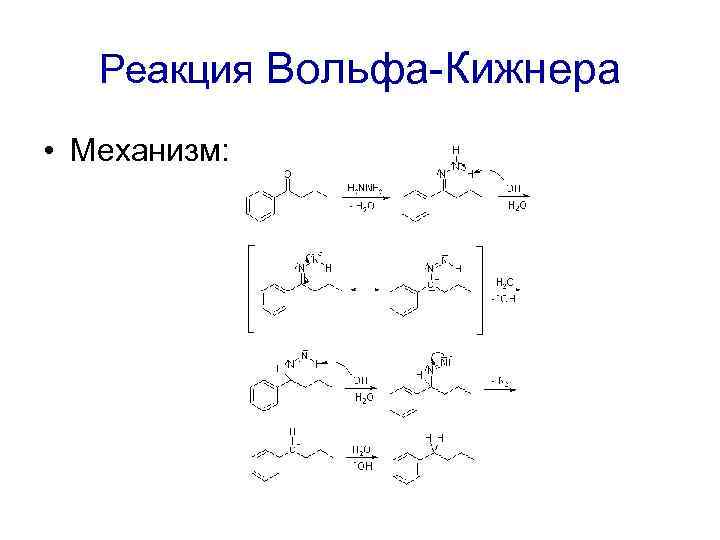 Реакция Вольфа-Кижнера • Механизм:
Реакция Вольфа-Кижнера • Механизм:
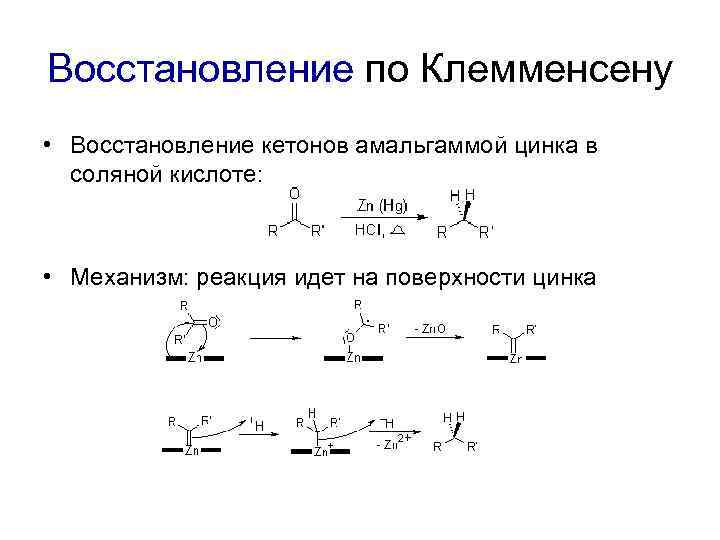 Восстановление по Клемменсену • Восстановление кетонов амальгаммой цинка в соляной кислоте: • Механизм: реакция идет на поверхности цинка
Восстановление по Клемменсену • Восстановление кетонов амальгаммой цинка в соляной кислоте: • Механизм: реакция идет на поверхности цинка
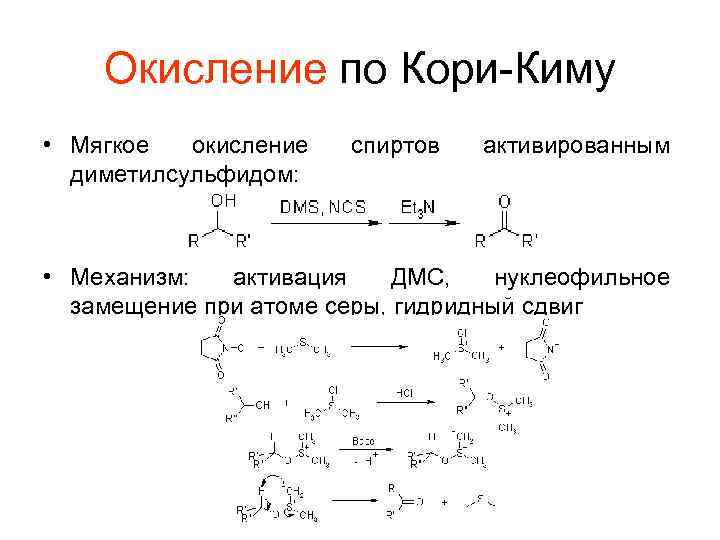 Окисление по Кори-Киму • Мягкое окисление диметилсульфидом: спиртов активированным • Механизм: активация ДМС, нуклеофильное замещение при атоме серы, гидридный сдвиг
Окисление по Кори-Киму • Мягкое окисление диметилсульфидом: спиртов активированным • Механизм: активация ДМС, нуклеофильное замещение при атоме серы, гидридный сдвиг
 Окисление по Сверну • Мягкое окисление спиртов в альдегиды смесью ДМСО с оксалилхлоридом: • Механизм: такой же, как у Кори-Кима …
Окисление по Сверну • Мягкое окисление спиртов в альдегиды смесью ДМСО с оксалилхлоридом: • Механизм: такой же, как у Кори-Кима …
 Восстановление по Берчу • Восстановление бензольного кольца натрием: • Механизм: две восстановления стадии одноэлектронного • Очевидно, для замещенного бензола будет 2 варианта; какой из них получится – зависит от заместителя
Восстановление по Берчу • Восстановление бензольного кольца натрием: • Механизм: две восстановления стадии одноэлектронного • Очевидно, для замещенного бензола будет 2 варианта; какой из них получится – зависит от заместителя
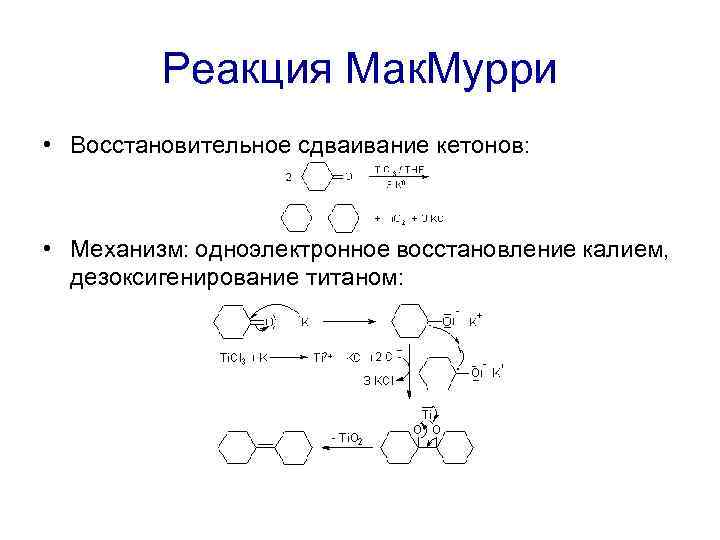 Реакция Мак. Мурри • Восстановительное сдваивание кетонов: • Механизм: одноэлектронное восстановление калием, дезоксигенирование титаном:
Реакция Мак. Мурри • Восстановительное сдваивание кетонов: • Механизм: одноэлектронное восстановление калием, дезоксигенирование титаном:
 Реакция Глязера • Окислительное сдваивание терминальных ацетиленов под действием одновалентной меди: • Реакция видимо идет через радикалы
Реакция Глязера • Окислительное сдваивание терминальных ацетиленов под действием одновалентной меди: • Реакция видимо идет через радикалы
 Реакция Нефа • Гидролиз нитросоединений до карбонильных соединений: • Механизм: депротонирование, Ad. N, фрагментация:
Реакция Нефа • Гидролиз нитросоединений до карбонильных соединений: • Механизм: депротонирование, Ad. N, фрагментация:
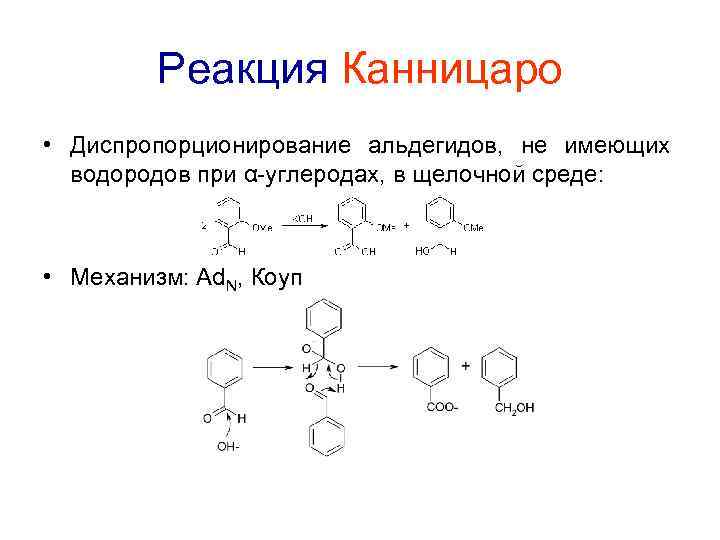 Реакция Канницаро • Диспропорционирование альдегидов, не имеющих водородов при α-углеродах, в щелочной среде: • Механизм: Ad. N, Коуп
Реакция Канницаро • Диспропорционирование альдегидов, не имеющих водородов при α-углеродах, в щелочной среде: • Механизм: Ad. N, Коуп
 Реакция Канницаро • Если целевым продуктом является спирт, используют кросс-Каницарро с формальдегидом:
Реакция Канницаро • Если целевым продуктом является спирт, используют кросс-Каницарро с формальдегидом:
 Реакции с участием фосфорорганических соединений
Реакции с участием фосфорорганических соединений
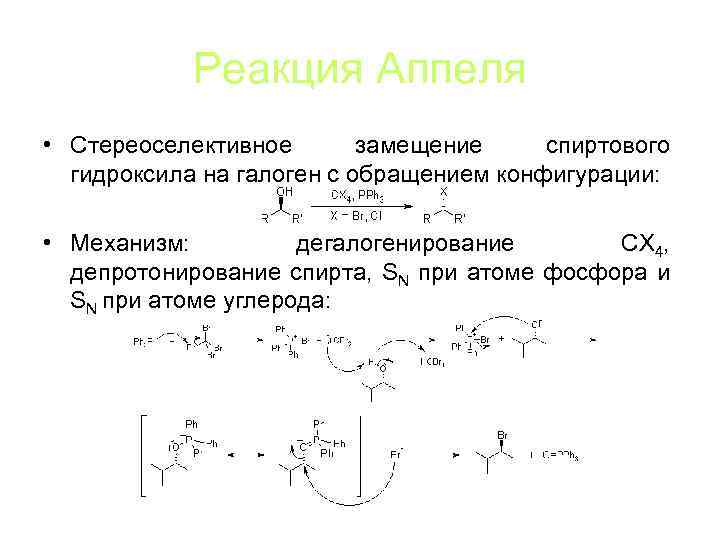 Реакция Аппеля • Стереоселективное замещение спиртового гидроксила на галоген с обращением конфигурации: • Механизм: дегалогенирование CX 4, депротонирование спирта, SN при атоме фосфора и SN при атоме углерода:
Реакция Аппеля • Стереоселективное замещение спиртового гидроксила на галоген с обращением конфигурации: • Механизм: дегалогенирование CX 4, депротонирование спирта, SN при атоме фосфора и SN при атоме углерода:
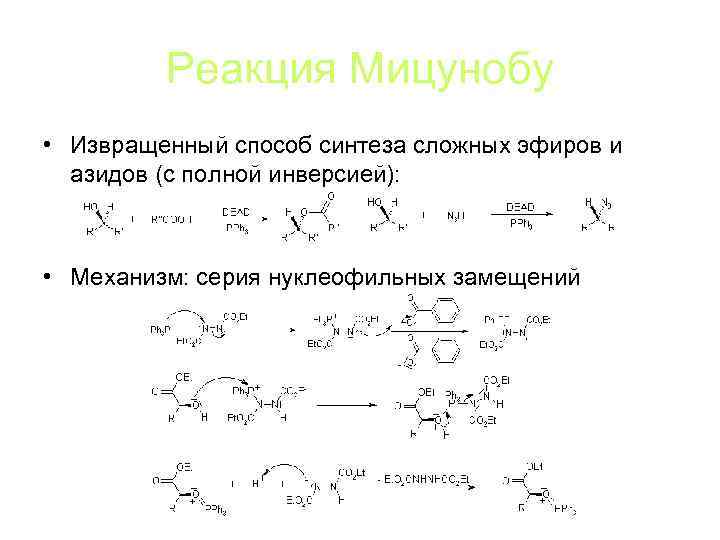 Реакция Мицунобу • Извращенный способ синтеза сложных эфиров и азидов (с полной инверсией): • Механизм: серия нуклеофильных замещений
Реакция Мицунобу • Извращенный способ синтеза сложных эфиров и азидов (с полной инверсией): • Механизм: серия нуклеофильных замещений
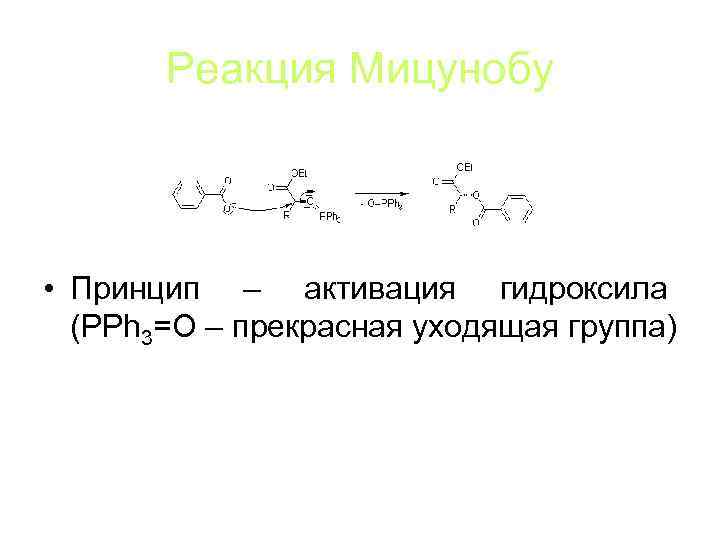 Реакция Мицунобу • Принцип – активация гидроксила (PPh 3=O – прекрасная уходящая группа)
Реакция Мицунобу • Принцип – активация гидроксила (PPh 3=O – прекрасная уходящая группа)
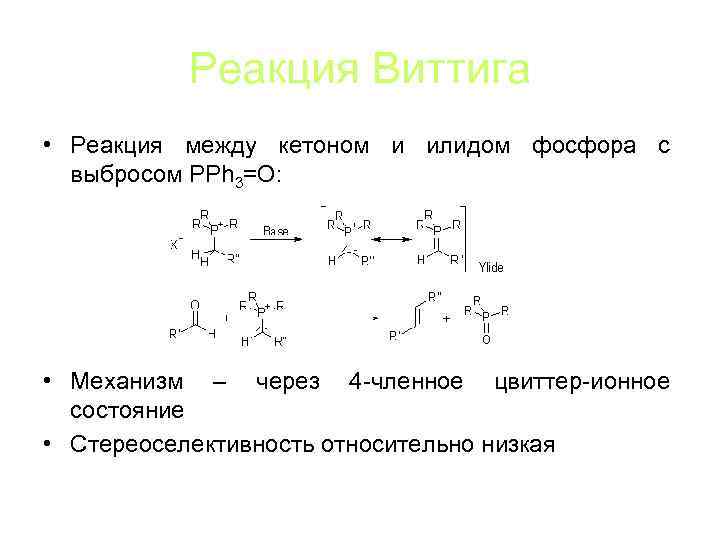 Реакция Виттига • Реакция между кетоном и илидом фосфора с выбросом PPh 3=O: • Механизм – через 4 -членное цвиттер-ионное состояние • Стереоселективность относительно низкая
Реакция Виттига • Реакция между кетоном и илидом фосфора с выбросом PPh 3=O: • Механизм – через 4 -членное цвиттер-ионное состояние • Стереоселективность относительно низкая
 Реакция Хорнера-Виттига • Реакция между кетоном и илидом фосфора с выбросом соли фосфоновой кислоты: • Механизм: депротонирование эфира, Ad. N к атомому фосфора, выброс соли
Реакция Хорнера-Виттига • Реакция между кетоном и илидом фосфора с выбросом соли фосфоновой кислоты: • Механизм: депротонирование эфира, Ad. N к атомому фосфора, выброс соли
 Реакция Хорнера-Виттига
Реакция Хорнера-Виттига
 Перегруппировки
Перегруппировки
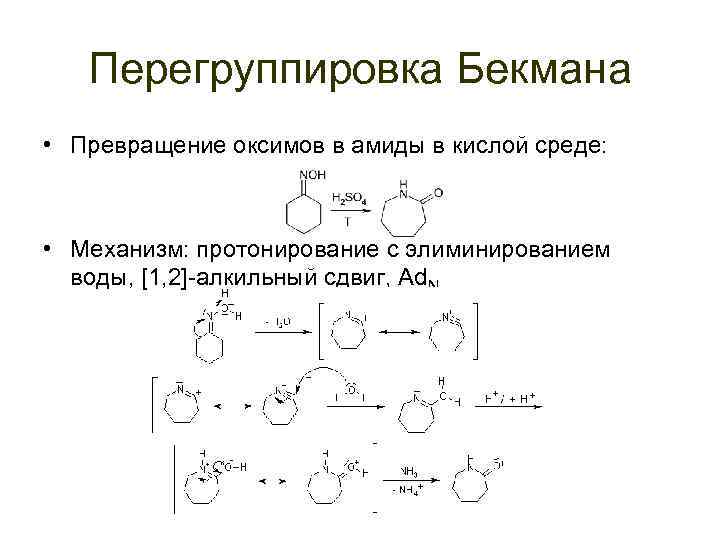 Перегруппировка Бекмана • Превращение оксимов в амиды в кислой среде: • Механизм: протонирование с элиминированием воды, [1, 2]-алкильный сдвиг, Ad. N
Перегруппировка Бекмана • Превращение оксимов в амиды в кислой среде: • Механизм: протонирование с элиминированием воды, [1, 2]-алкильный сдвиг, Ad. N
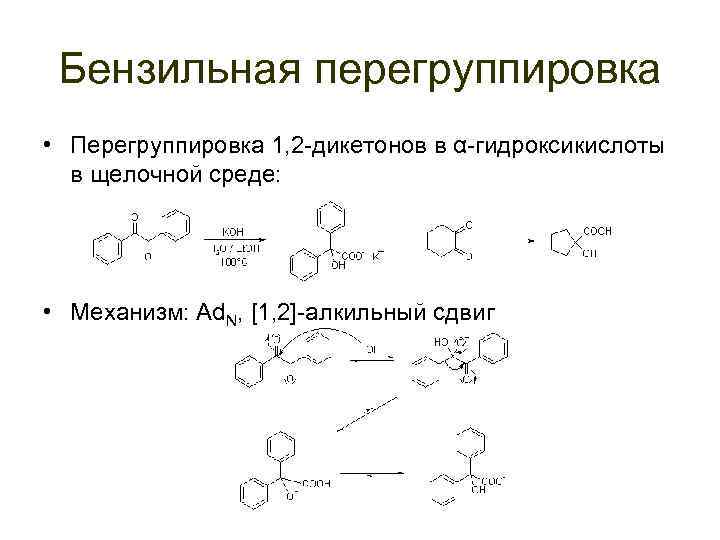 Бензильная перегруппировка • Перегруппировка 1, 2 -дикетонов в α-гидроксикислоты в щелочной среде: • Механизм: Ad. N, [1, 2]-алкильный сдвиг
Бензильная перегруппировка • Перегруппировка 1, 2 -дикетонов в α-гидроксикислоты в щелочной среде: • Механизм: Ad. N, [1, 2]-алкильный сдвиг
 Пинаколиновая перегруппировка • Перегруппировка пинаконов в пинаколины в кислой среде: • Механизм: протонирование, отщепление воды, [1, 2]алкильный сдвиг
Пинаколиновая перегруппировка • Перегруппировка пинаконов в пинаколины в кислой среде: • Механизм: протонирование, отщепление воды, [1, 2]алкильный сдвиг
 Перегруппировка Курциуса • Превращение ацилазидов в изоцианаты, которые затем могут дать карбаматы или уретаны: • Механизм: отщепление нитрена, Ad. N азота, перегруппировка
Перегруппировка Курциуса • Превращение ацилазидов в изоцианаты, которые затем могут дать карбаматы или уретаны: • Механизм: отщепление нитрена, Ad. N азота, перегруппировка
![Перегруппировка Коупа • [3, 3]-сигматропная перегруппировка • Проходит по синхронному механизму: Перегруппировка Коупа • [3, 3]-сигматропная перегруппировка • Проходит по синхронному механизму:](https://present5.com/presentation/3/-19759704_126575846.pdf-img/-19759704_126575846.pdf-90.jpg) Перегруппировка Коупа • [3, 3]-сигматропная перегруппировка • Проходит по синхронному механизму:
Перегруппировка Коупа • [3, 3]-сигматропная перегруппировка • Проходит по синхронному механизму:
![Перегруппировка Кляйзена • [3, 3]-сигматропная перегруппировка аллилвиниловых и аллилфениловых эфиров: • Механизм: синхронный, через Перегруппировка Кляйзена • [3, 3]-сигматропная перегруппировка аллилвиниловых и аллилфениловых эфиров: • Механизм: синхронный, через](https://present5.com/presentation/3/-19759704_126575846.pdf-img/-19759704_126575846.pdf-91.jpg) Перегруппировка Кляйзена • [3, 3]-сигматропная перегруппировка аллилвиниловых и аллилфениловых эфиров: • Механизм: синхронный, через шестичленное ПС
Перегруппировка Кляйзена • [3, 3]-сигматропная перегруппировка аллилвиниловых и аллилфениловых эфиров: • Механизм: синхронный, через шестичленное ПС
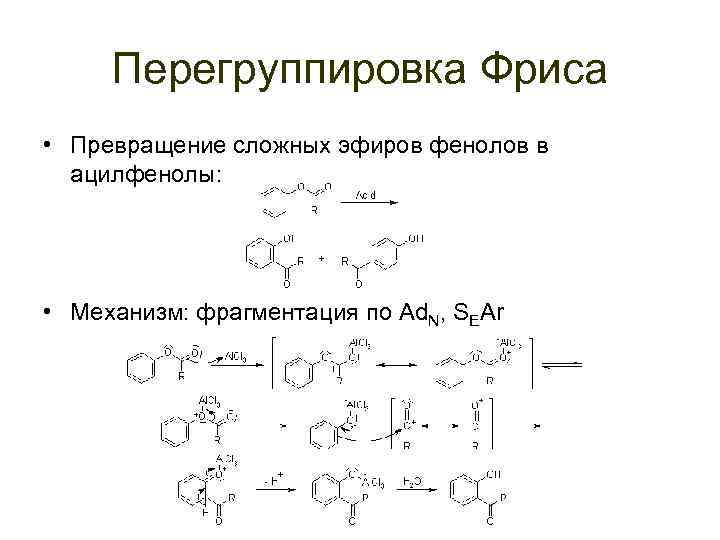 Перегруппировка Фриса • Превращение сложных эфиров фенолов в ацилфенолы: • Механизм: фрагментация по Ad. N, SEAr
Перегруппировка Фриса • Превращение сложных эфиров фенолов в ацилфенолы: • Механизм: фрагментация по Ad. N, SEAr
![Перегруппировка Фаворского • Раскрытие циклопропанонов под действием щелочи: • Механизм: Ad. N, [1, 2]-гидридный Перегруппировка Фаворского • Раскрытие циклопропанонов под действием щелочи: • Механизм: Ad. N, [1, 2]-гидридный](https://present5.com/presentation/3/-19759704_126575846.pdf-img/-19759704_126575846.pdf-93.jpg) Перегруппировка Фаворского • Раскрытие циклопропанонов под действием щелочи: • Механизм: Ad. N, [1, 2]-гидридный сдвиг • Общеизвестный вариант – гидролиз α-хлоркетонов:
Перегруппировка Фаворского • Раскрытие циклопропанонов под действием щелочи: • Механизм: Ad. N, [1, 2]-гидридный сдвиг • Общеизвестный вариант – гидролиз α-хлоркетонов:
 Часто используемые препаративные реакции
Часто используемые препаративные реакции
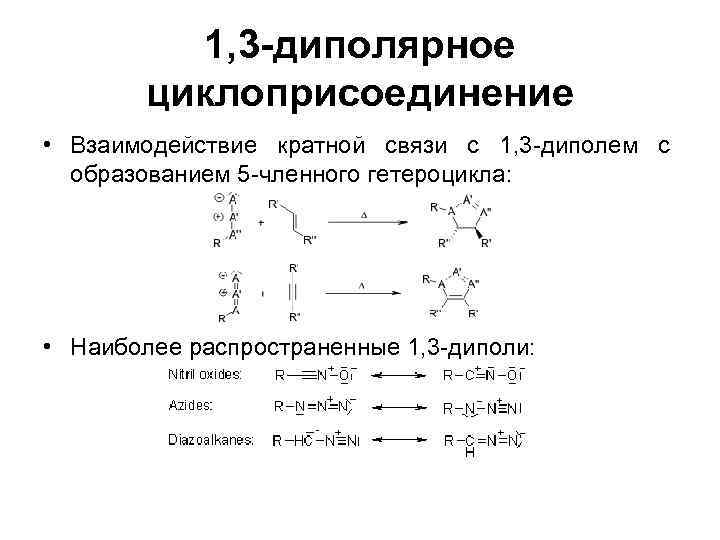 1, 3 -диполярное циклоприсоединение • Взаимодействие кратной связи с 1, 3 -диполем с образованием 5 -членного гетероцикла: • Наиболее распространенные 1, 3 -диполи:
1, 3 -диполярное циклоприсоединение • Взаимодействие кратной связи с 1, 3 -диполем с образованием 5 -членного гетероцикла: • Наиболее распространенные 1, 3 -диполи:
 Направленное ортометаллирование • Взаимодействие алкиллитиевого соединения с ароматическим соединением, содержащим направляющую (координирующую) группу
Направленное ортометаллирование • Взаимодействие алкиллитиевого соединения с ароматическим соединением, содержащим направляющую (координирующую) группу
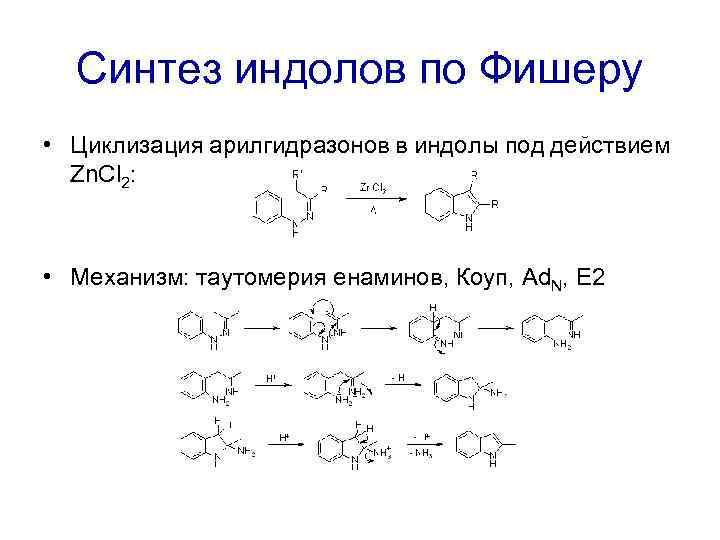 Синтез индолов по Фишеру • Циклизация арилгидразонов в индолы под действием Zn. Cl 2: • Механизм: таутомерия енаминов, Коуп, Ad. N, E 2
Синтез индолов по Фишеру • Циклизация арилгидразонов в индолы под действием Zn. Cl 2: • Механизм: таутомерия енаминов, Коуп, Ad. N, E 2
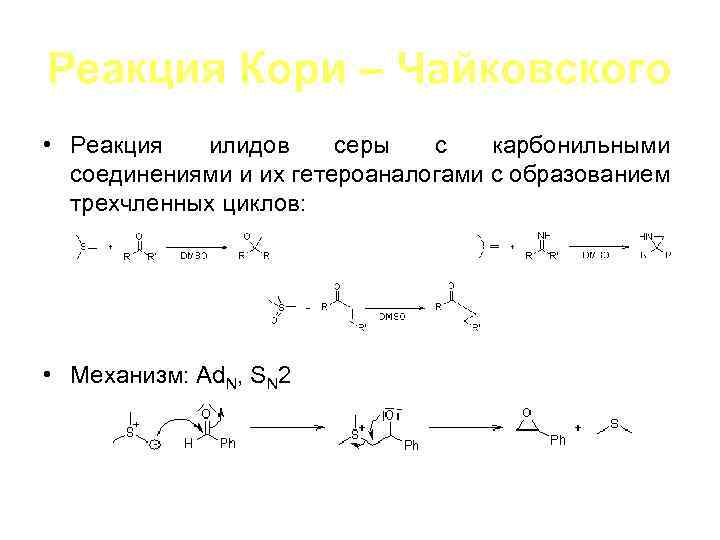 Реакция Кори – Чайковского • Реакция илидов серы с карбонильными соединениями и их гетероаналогами с образованием трехчленных циклов: • Механизм: Ad. N, SN 2
Реакция Кори – Чайковского • Реакция илидов серы с карбонильными соединениями и их гетероаналогами с образованием трехчленных циклов: • Механизм: Ad. N, SN 2
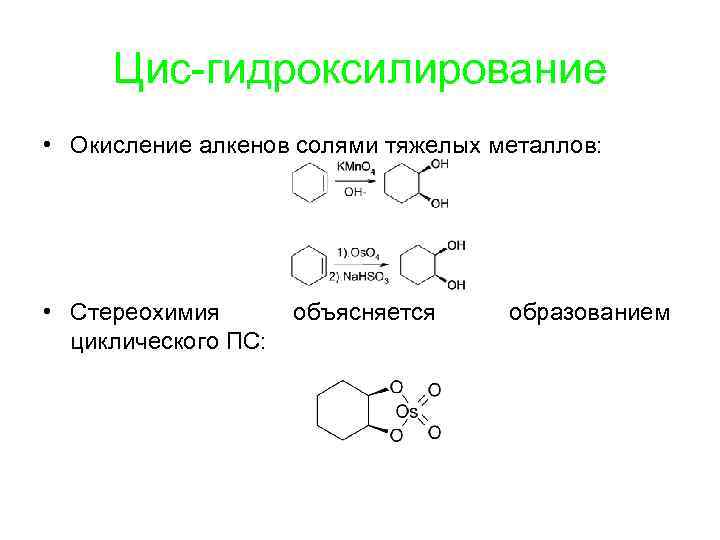 Цис-гидроксилирование • Окисление алкенов солями тяжелых металлов: • Стереохимия циклического ПС: объясняется образованием
Цис-гидроксилирование • Окисление алкенов солями тяжелых металлов: • Стереохимия циклического ПС: объясняется образованием
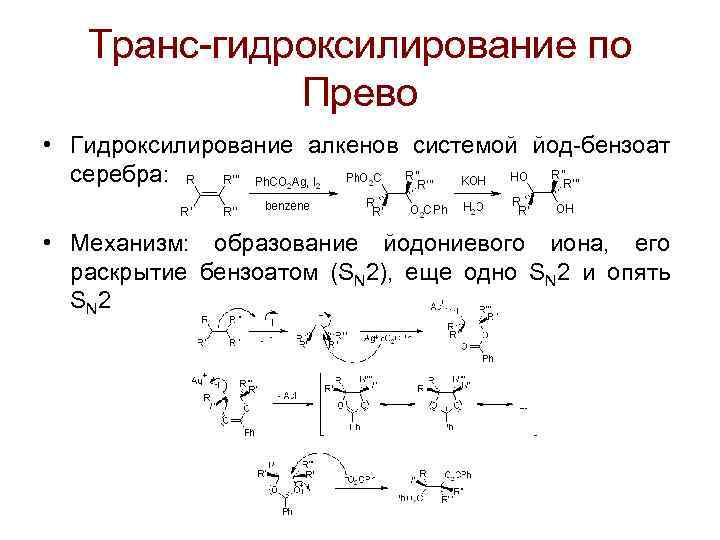 Транс-гидроксилирование по Прево • Гидроксилирование алкенов системой йод-бензоат серебра: • Механизм: образование йодониевого иона, его раскрытие бензоатом (SN 2), еще одно SN 2 и опять S N 2
Транс-гидроксилирование по Прево • Гидроксилирование алкенов системой йод-бензоат серебра: • Механизм: образование йодониевого иона, его раскрытие бензоатом (SN 2), еще одно SN 2 и опять S N 2
 Реакция Риттера • Образование амидов из нитрилов (спиртов) в сильнокислой среде: и • Механизм: Ad. N (Nu = RCN), Ad. N (Nu = H 2 O) алкенов
Реакция Риттера • Образование амидов из нитрилов (спиртов) в сильнокислой среде: и • Механизм: Ad. N (Nu = RCN), Ad. N (Nu = H 2 O) алкенов
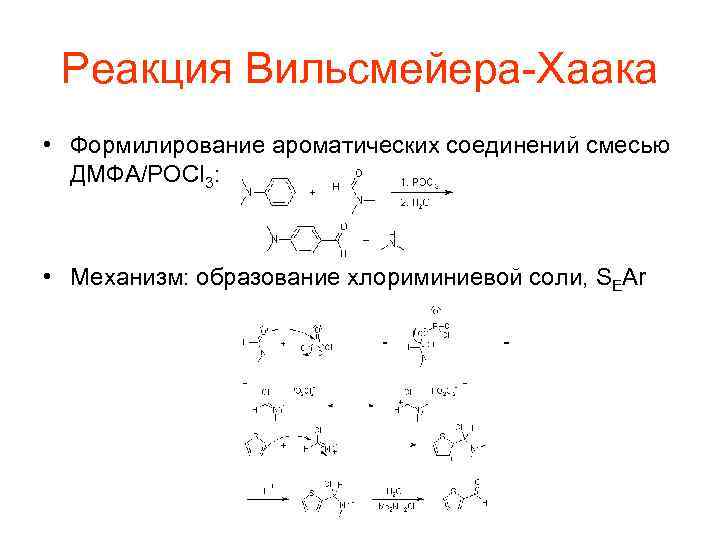 Реакция Вильсмейера-Хаака • Формилирование ароматических соединений смесью ДМФА/POCl 3: • Механизм: образование хлориминиевой соли, SEAr
Реакция Вильсмейера-Хаака • Формилирование ароматических соединений смесью ДМФА/POCl 3: • Механизм: образование хлориминиевой соли, SEAr
 Реакция Воля-Циглера • Аллильное бромирование алкенов: • Механизм: образование радикала Br. , радикальные реакции
Реакция Воля-Циглера • Аллильное бромирование алкенов: • Механизм: образование радикала Br. , радикальные реакции
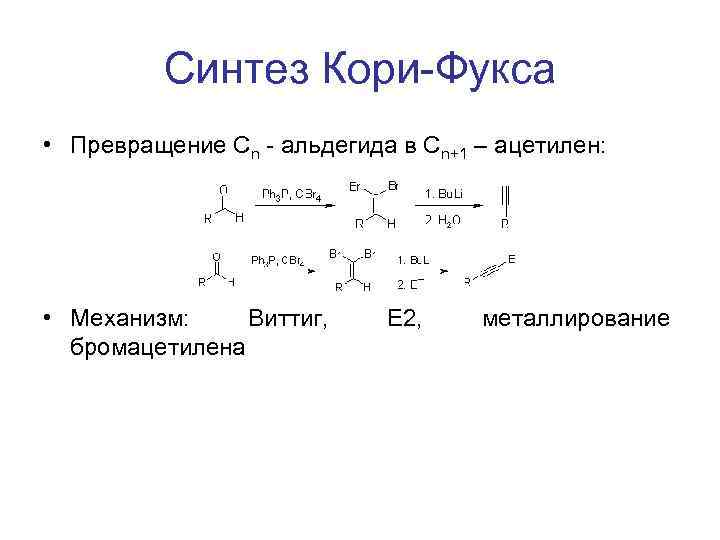 Синтез Кори-Фукса • Превращение Cn - альдегида в Сn+1 – ацетилен: • Механизм: Виттиг, бромацетилена E 2, металлирование
Синтез Кори-Фукса • Превращение Cn - альдегида в Сn+1 – ацетилен: • Механизм: Виттиг, бромацетилена E 2, металлирование
 Синтез Арндта-Айстерта • Удлинение углеродной цепи карбоновой кислоты на 1 атом углерода: • Механизм: Ad. N, фрагментация нуклеофила, распад диазосоединения, [1, 2]-алкильный сдвиг, Ad. N
Синтез Арндта-Айстерта • Удлинение углеродной цепи карбоновой кислоты на 1 атом углерода: • Механизм: Ad. N, фрагментация нуклеофила, распад диазосоединения, [1, 2]-алкильный сдвиг, Ad. N
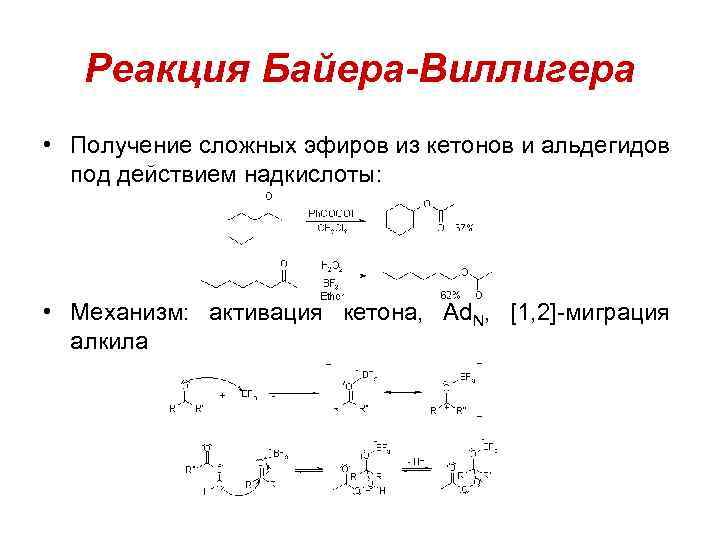 Реакция Байера-Виллигера • Получение сложных эфиров из кетонов и альдегидов под действием надкислоты: • Механизм: активация кетона, Ad. N, [1, 2]-миграция алкила
Реакция Байера-Виллигера • Получение сложных эфиров из кетонов и альдегидов под действием надкислоты: • Механизм: активация кетона, Ad. N, [1, 2]-миграция алкила
 Реакция Байера-Виллигера • Лучше мигрируют заместители, образующие более стабильные карбокатионы
Реакция Байера-Виллигера • Лучше мигрируют заместители, образующие более стабильные карбокатионы
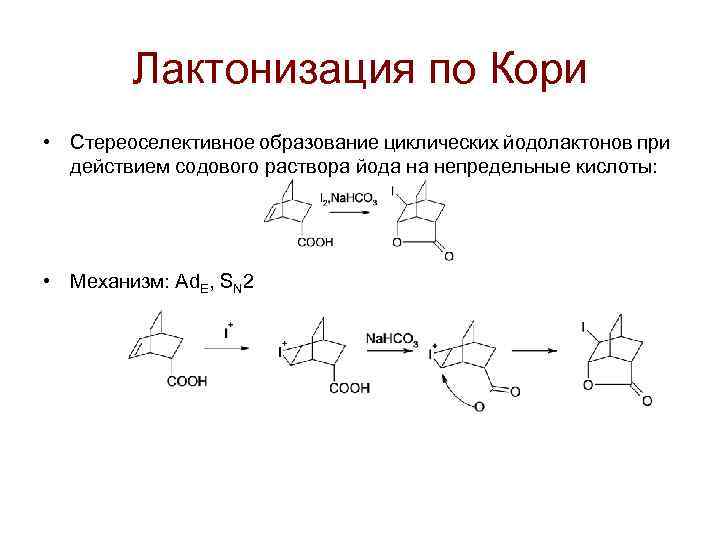 Лактонизация по Кори • Стереоселективное образование циклических йодолактонов при действием содового раствора йода на непредельные кислоты: • Механизм: Ad. E, SN 2
Лактонизация по Кори • Стереоселективное образование циклических йодолактонов при действием содового раствора йода на непредельные кислоты: • Механизм: Ad. E, SN 2
 Часть 4 Задачи
Часть 4 Задачи
 Расчетная задача на сообразительность Пары циклогексена пропустили через нагретую до температуры красного каления железную трубку. После пропускания объем смеси увеличился на 10%, а количество бромной воды на обесцвечивание продуктов реакции не изменилось по сравнению с количеством воды на обесцвечивание исходного циклогексена. Расчитать степень превращения циклогексена и состав продуктов на выходе.
Расчетная задача на сообразительность Пары циклогексена пропустили через нагретую до температуры красного каления железную трубку. После пропускания объем смеси увеличился на 10%, а количество бромной воды на обесцвечивание продуктов реакции не изменилось по сравнению с количеством воды на обесцвечивание исходного циклогексена. Расчитать степень превращения циклогексена и состав продуктов на выходе.
 Задачи 1. При жестком окислении кетона Х получены равные количества CH 3 COOH, C 2 H 5 COOH и C 5 H 11 COOH. Найти кетон. 2. Из циклопентанона можно синтезировать циклобутанкарбоновую кислоту следующим образом: C 5 H 8 O + Bu. ONO A A + NH 2 Cl B B (hv) C C + H 2 O C 4 H 7 COOH Какие вещества получаются на каждой стадии?
Задачи 1. При жестком окислении кетона Х получены равные количества CH 3 COOH, C 2 H 5 COOH и C 5 H 11 COOH. Найти кетон. 2. Из циклопентанона можно синтезировать циклобутанкарбоновую кислоту следующим образом: C 5 H 8 O + Bu. ONO A A + NH 2 Cl B B (hv) C C + H 2 O C 4 H 7 COOH Какие вещества получаются на каждой стадии?
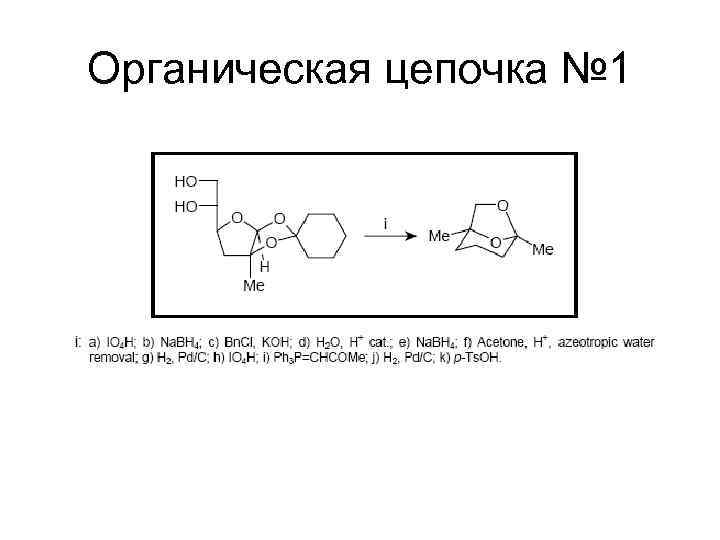 Органическая цепочка № 1
Органическая цепочка № 1
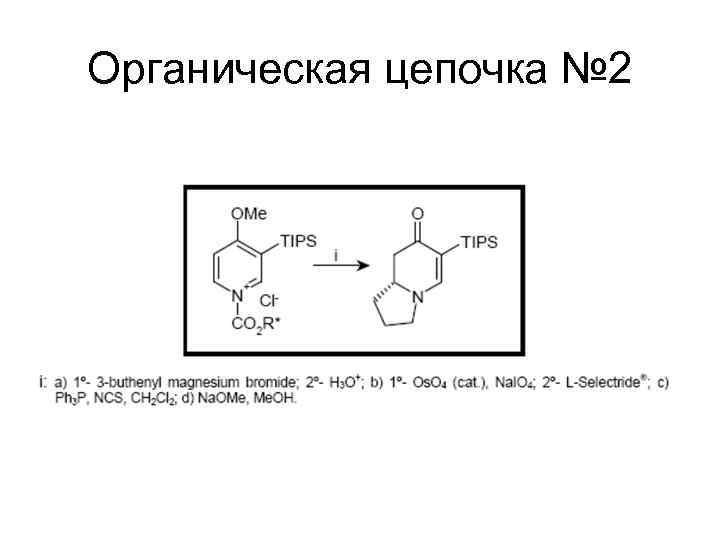 Органическая цепочка № 2
Органическая цепочка № 2
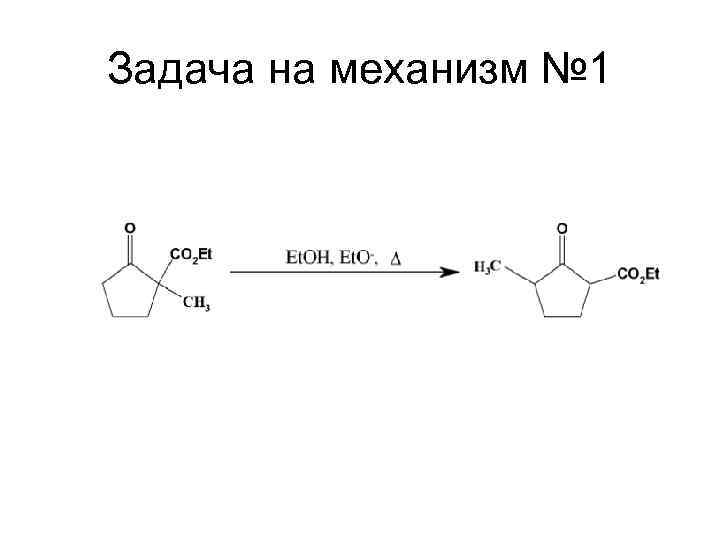 Задача на механизм № 1
Задача на механизм № 1
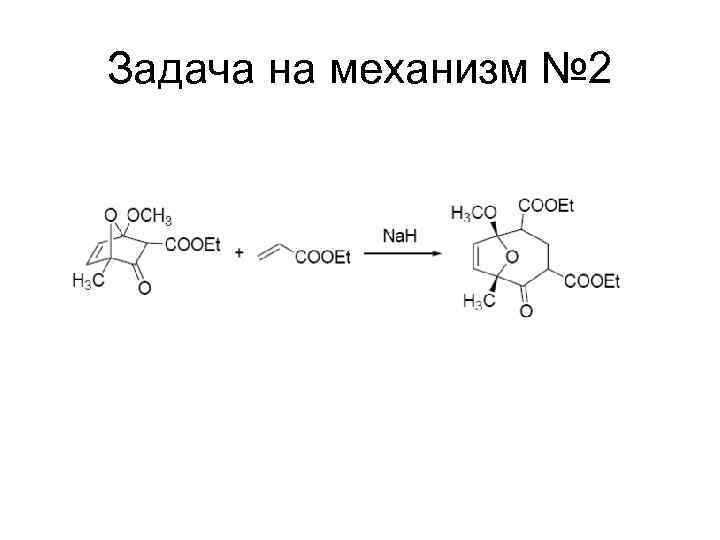 Задача на механизм № 2
Задача на механизм № 2
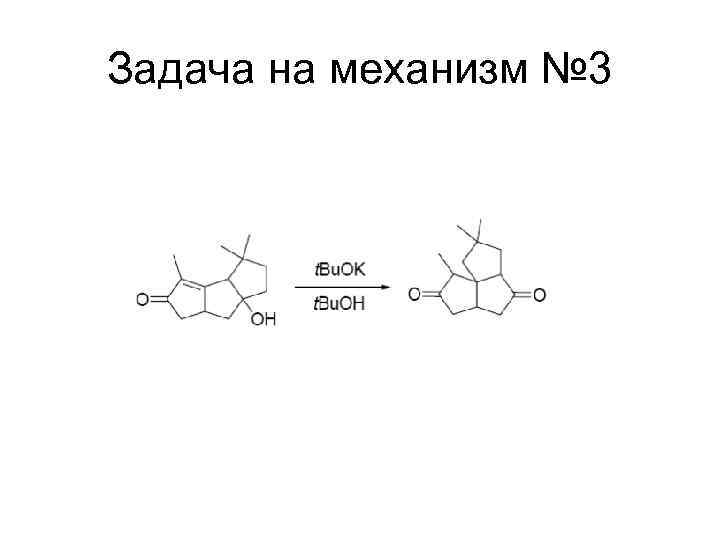 Задача на механизм № 3
Задача на механизм № 3
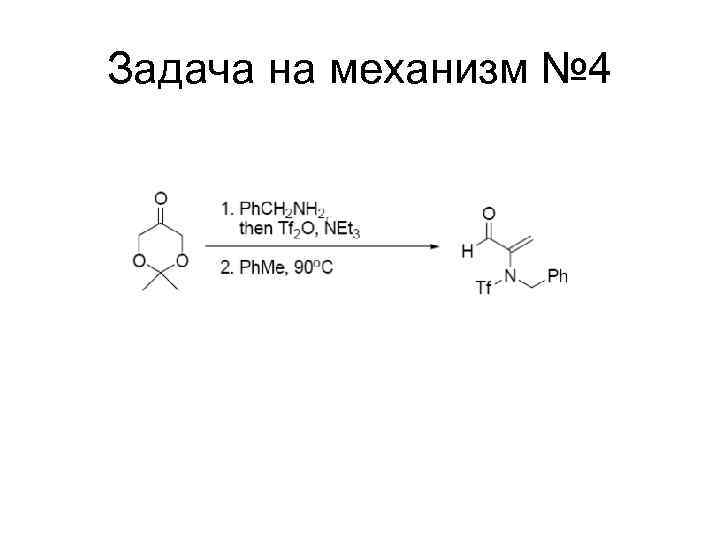 Задача на механизм № 4
Задача на механизм № 4
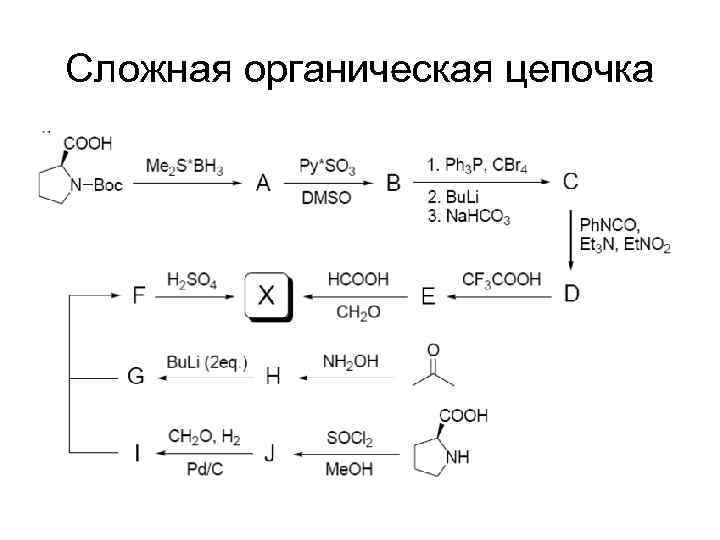 Сложная органическая цепочка
Сложная органическая цепочка
 ТАС Интересное с теоретической точки зрения соединение Х можно получить исходя из фталимида (А) следующим образом (ТАС - тетраацетат свинца): A + NH 2 Cl (Na. HCO 3) Б Б + С 2 Н 4 + ТАС B B + N 2 H 4 Г + Д (изомер Б) Г + ТАС + C 2 H 4 X (C 4 H 8 N 2) Нагревание Х приводит к его изомеризации в гидразид ацетальдегида. Напишите уравнения реакций. Рассмотрите эту схему синтеза, используя вместо этилена пропилен. Какие изомеры будут существовать для аналога Х в этом случае?
ТАС Интересное с теоретической точки зрения соединение Х можно получить исходя из фталимида (А) следующим образом (ТАС - тетраацетат свинца): A + NH 2 Cl (Na. HCO 3) Б Б + С 2 Н 4 + ТАС B B + N 2 H 4 Г + Д (изомер Б) Г + ТАС + C 2 H 4 X (C 4 H 8 N 2) Нагревание Х приводит к его изомеризации в гидразид ацетальдегида. Напишите уравнения реакций. Рассмотрите эту схему синтеза, используя вместо этилена пропилен. Какие изомеры будут существовать для аналога Х в этом случае?
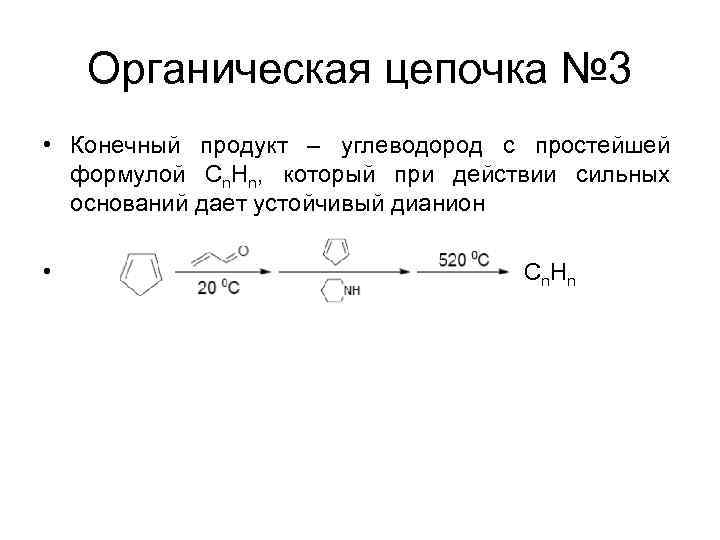 Органическая цепочка № 3 • Конечный продукт – углеводород с простейшей формулой Cn. Hn, который при действии сильных оснований дает устойчивый дианион • C n. H n
Органическая цепочка № 3 • Конечный продукт – углеводород с простейшей формулой Cn. Hn, который при действии сильных оснований дает устойчивый дианион • C n. H n
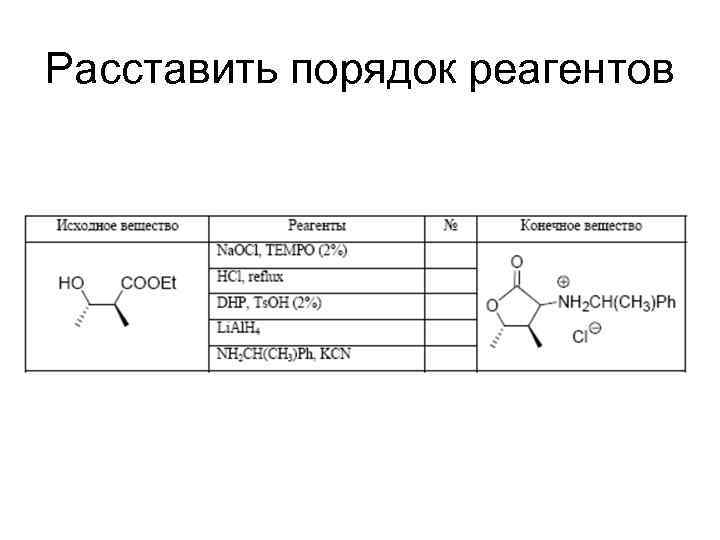 Расставить порядок реагентов
Расставить порядок реагентов
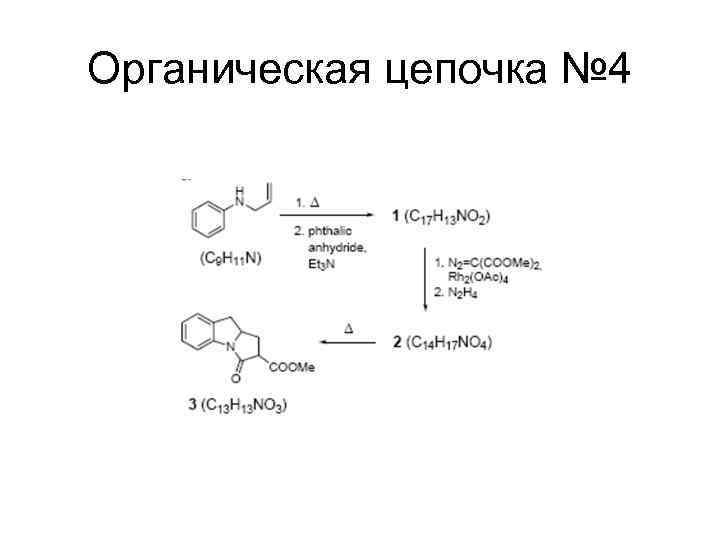 Органическая цепочка № 4
Органическая цепочка № 4
 Органическая цепочка № 5
Органическая цепочка № 5
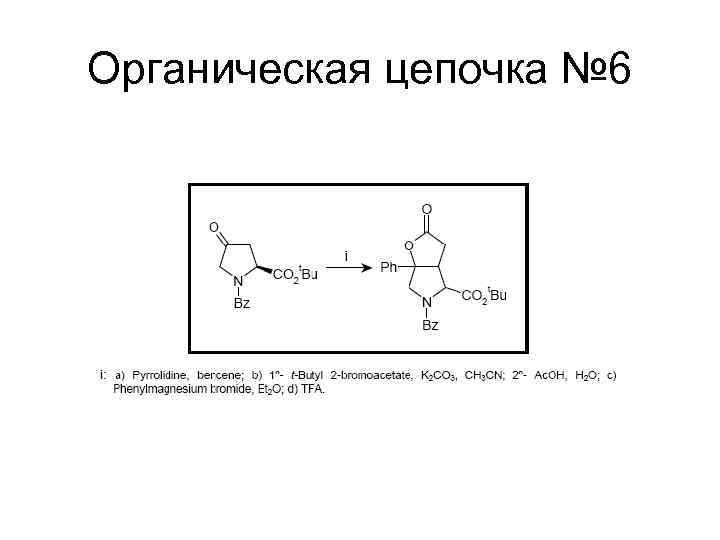 Органическая цепочка № 6
Органическая цепочка № 6
 Изомерные углеводороды • Два изомерных углеводорода, не обесцвечивающие бромную воду и имеющие соотношение атомов углерода и водорода в них 1: 2, образуют только по 1 монохлорпроизводному. Один из них образует 6, а другой - 7 дихлорпроизводных (без учета оптических изомеров). Найти углеводороды.
Изомерные углеводороды • Два изомерных углеводорода, не обесцвечивающие бромную воду и имеющие соотношение атомов углерода и водорода в них 1: 2, образуют только по 1 монохлорпроизводному. Один из них образует 6, а другой - 7 дихлорпроизводных (без учета оптических изомеров). Найти углеводороды.
 Задача на механизм № 5 • Аминокетоны – важный класс органических соединений, так как на их основе можно синтезировать различные гетероциклы. Также многие из них обладают физиологической активностью. Один из общих методов получения α-аминокетонов – синтез Небера. Расшифруйте промежуточные продукты, приведите механизм превращения B в C
Задача на механизм № 5 • Аминокетоны – важный класс органических соединений, так как на их основе можно синтезировать различные гетероциклы. Также многие из них обладают физиологической активностью. Один из общих методов получения α-аминокетонов – синтез Небера. Расшифруйте промежуточные продукты, приведите механизм превращения B в C
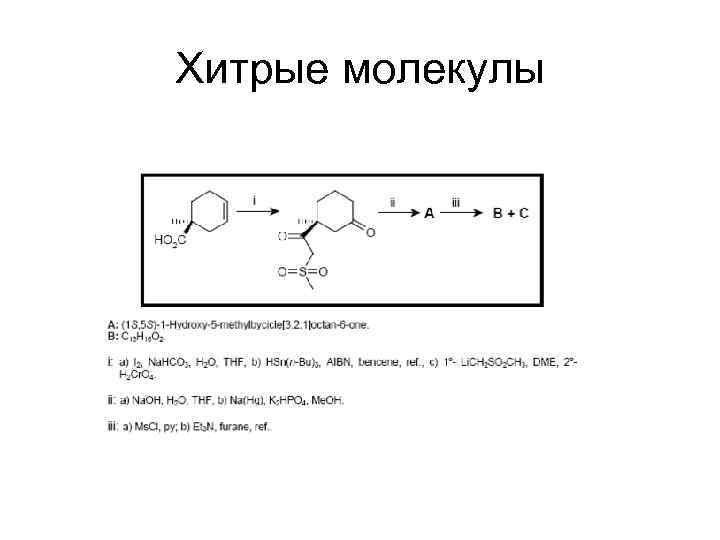 Хитрые молекулы
Хитрые молекулы


