Лучевая диагностика инсульта.pptx
- Количество слайдов: 139

Церебральный инсульт Современные возможности инструментальной диагностики острых нарушений мозгового кровообращения. ОКБ 1. ГКБ 40. Кафедра лучевой диагностики УГМА. Екатеринбург, 2009 -2014

Эпидемиология и экономика • Прямой и косвенный ущерб - 500 -700 млрд рублей в год • ~5% - субарахноидальное кровоизлияние • ~10 -20% - первичное внутримозговое кровоизлияние • ~75 -80% - ишемический инсульт

Задачи нейрорадиолога при инсульте • Установить, ишемический или геморрагический инсульт • Оценка морфологического состояния мозговой паренхимы • Оценка функционального состояния мозговой паренхимы • Оценка состояния экстра- и интракраниальных сосудов • Оценка причинной связи между состоянием сосудов и инсультом • Выяснить, есть ли признаки других сосудистых изменений • Установить, экстра-, или интракраниально расположена причина, вызвавшая инсульт

Подтипы ишемического инсульта TOAST and Baltimore-Washington Cooperative Young Stroke Study criteria 1993 -1995 • атеротромботический – 34 % • кардиоэмболические – 22 % • гемодинамические – 15 % • лакунарные – 22 % • гемореологическая микроокклюзия – 7 % • Large artery atherosclerosis - 14 -66% • Cardioembolic Infarction - ~20% • Small-Artery Occlusion (Lacunae) - 10 -29% • Acute Stroke of Other Determined Etiology - 616% • Stroke of Undetermined Etiology - 1 -8% - 2940%



Стадии ишемического инсульта (по RG Gonzalez) 1. Острейшая (до 6 часов) возможны интервенции 2. Острая (6 -24 часа) инфаркт может быть не видим на КТ/МРТ 3. Подострая (24 часа-6 недель) стадия накопления КВ и «затуманивания» 4. Хроническая (после 6 недель) резорбция и рубцевание

Стадии ишемического инсульта (Allen et all, 2012) • • • Ранняя острейшая (0 -6 ч) Поздняя острейшая (6 -24 часа) Острая (1 -7 дней) Подострая (1 -3 нед) Хроническая (>3 нед)

Преимущества и недостатки КТ ПРЕИМУЩЕСТВА НЕДОСТАТКИ • Широко доступна и относительно дешева Ионизирующее излучение • Неинвазивна • • • Низкая чувствительность в острейшей стадии Чувствительна к геморрагии, метод выбора Сложно дифференцировать острый инфаркт и его исход Хорошо видно костные структуры Плохо видно структуры ЗЧЯ Хороший доступ к пациенту во время исследования Быстрое получение данных Можно проводить КТА и КТ-перфузию изменений Низкий рейтинг согласия между разными врачами в оценке ишемических Невозможно различать жизнеспособную ткань в участках гипоперфузии
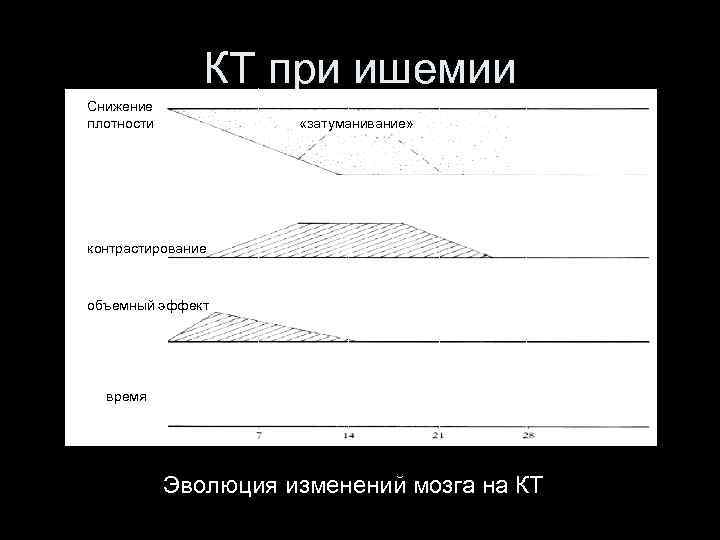
КТ при ишемии Снижение плотности «затуманивание» контрастирование объемный эффект время Эволюция изменений мозга на КТ
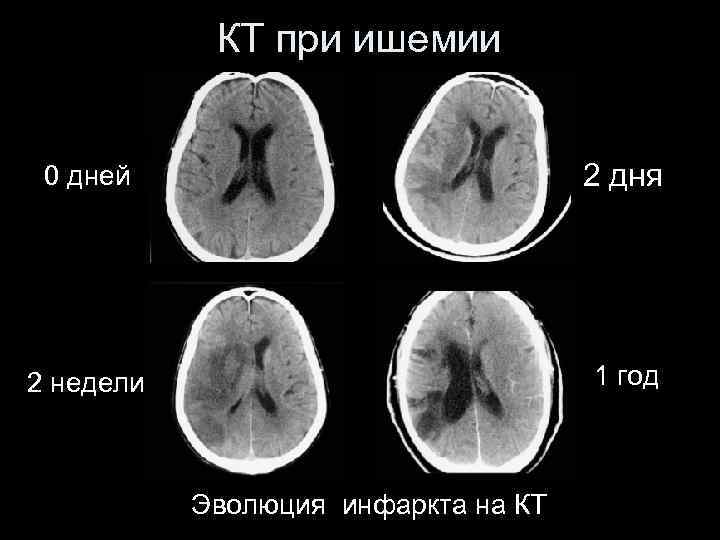
КТ при ишемии 0 дней 2 дня 2 недели 1 год Эволюция инфаркта на КТ
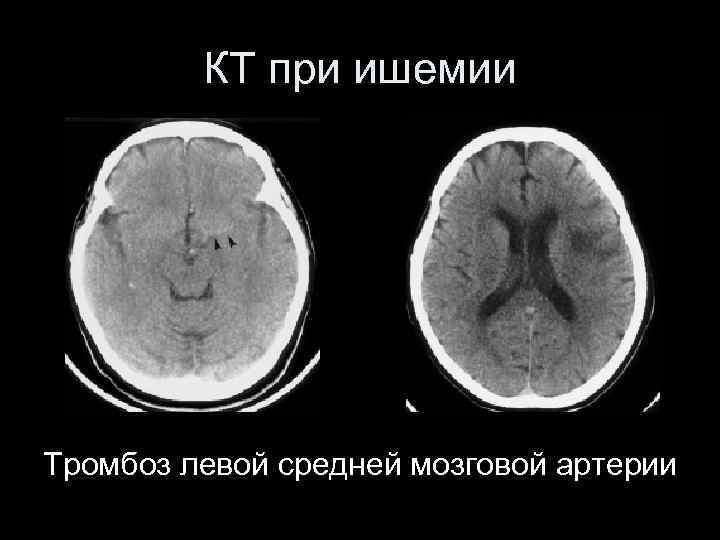
КТ при ишемии Тромбоз левой средней мозговой артерии
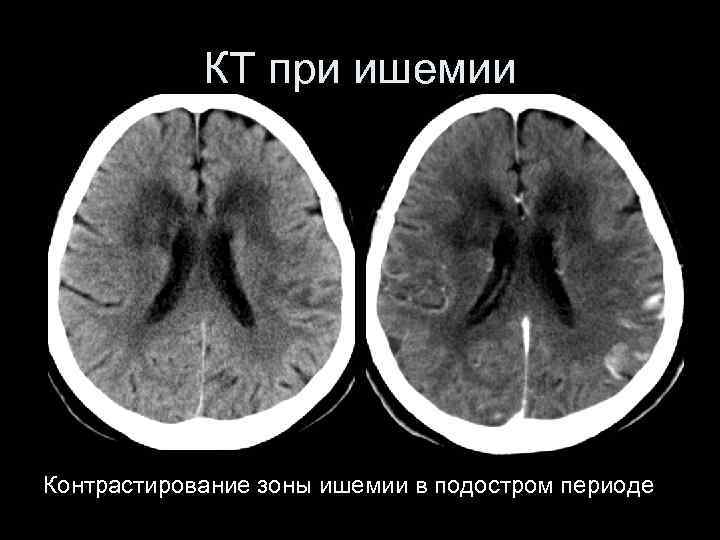
КТ при ишемии Контрастирование зоны ишемии в подостром периоде
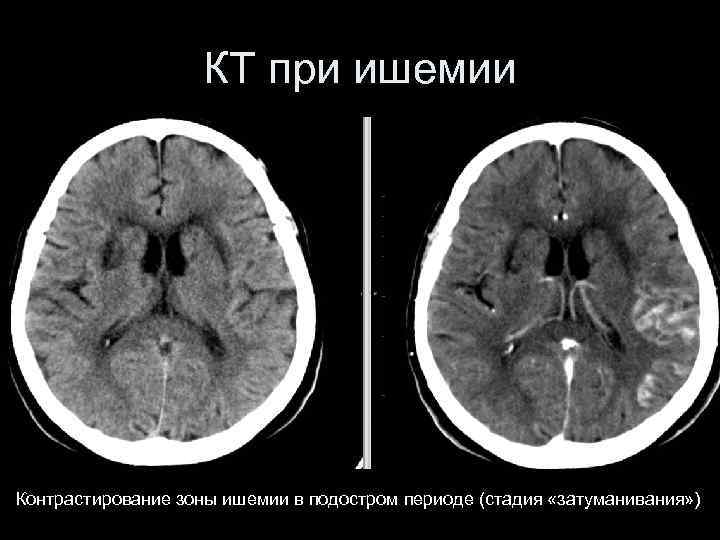
КТ при ишемии Контрастирование зоны ишемии в подостром периоде (стадия «затуманивания» )
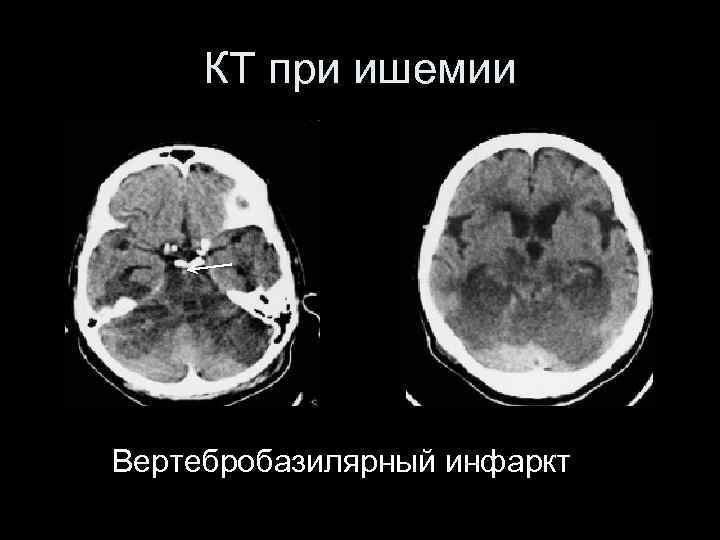
КТ при ишемии Вертебробазилярный инфаркт
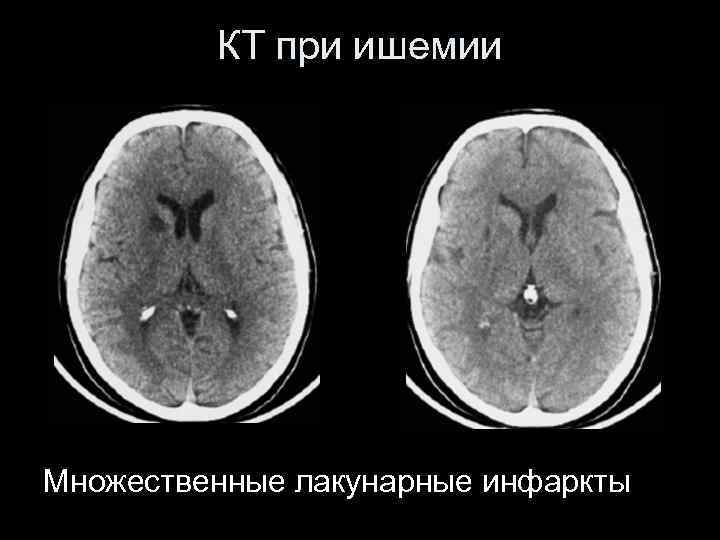
КТ при ишемии Множественные лакунарные инфаркты
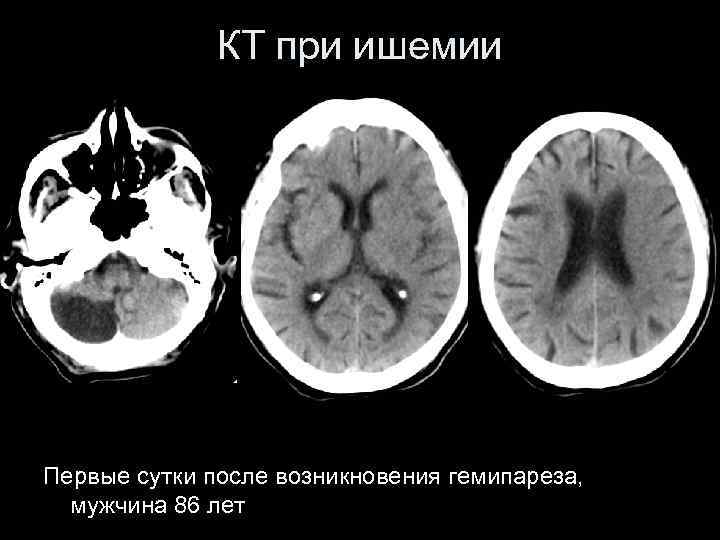
КТ при ишемии Первые сутки после возникновения гемипареза, мужчина 86 лет
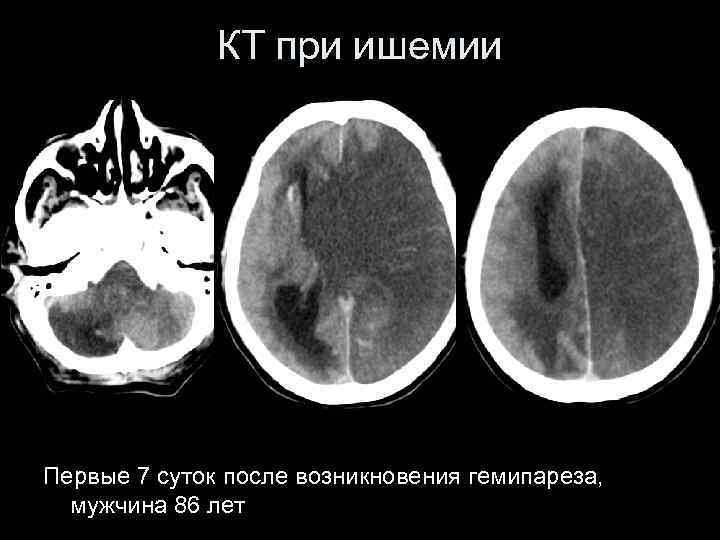
КТ при ишемии Первые 7 суток после возникновения гемипареза, мужчина 86 лет
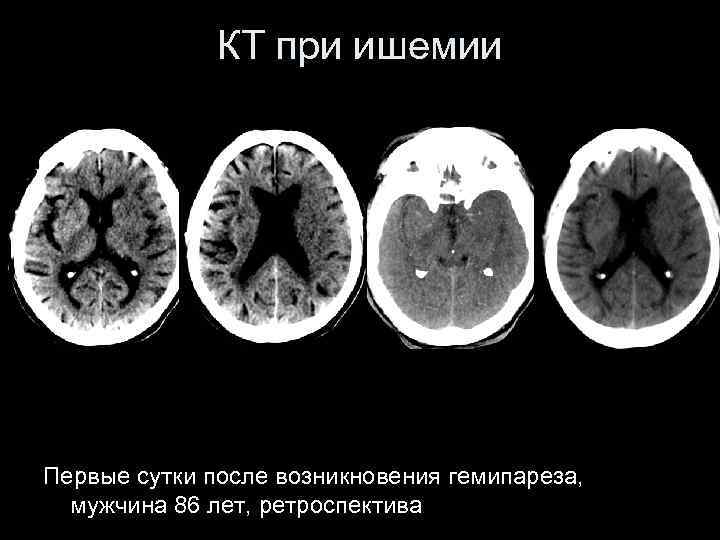
КТ при ишемии Первые сутки после возникновения гемипареза, мужчина 86 лет, ретроспектива
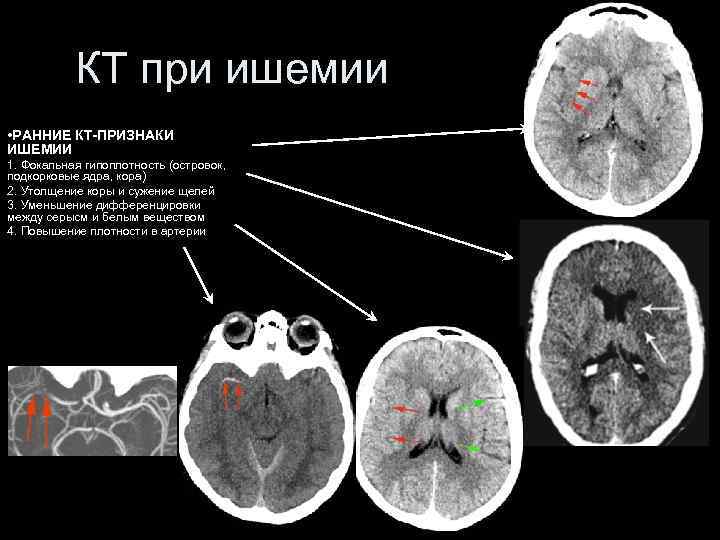
КТ при ишемии • РАННИЕ КТ-ПРИЗНАКИ ИШЕМИИ 1. Фокальная гипоплотность (островок, подкорковые ядра, кора) 2. Утолщение коры и сужение щелей 3. Уменьшение дифференцировки между серысм и белым веществом 4. Повышение плотности в артерии

Современная КТ: КТ-перфузия Серое в-во Белое в-во CBF* 60 25 * мл/100 г/мин ** мл/100 г CBV** 4 2 MTT 4 4. 8 • Интерпретация КТП • CBV, CBF совпадают: • Тромболизис не нужен вне зависимости от размера очага • Крупная зона CBV, еще более крупная CBF • Возможен тромболизис в зависимости от времени и размера очага • При CBV >100 мл лечение, скорее всего, не показано • Малая зона CBV, большая зона CBF • В типичных случая – хороший кандидат для тромболизиса. Осторожно, если время после инсульта более 3 часов.
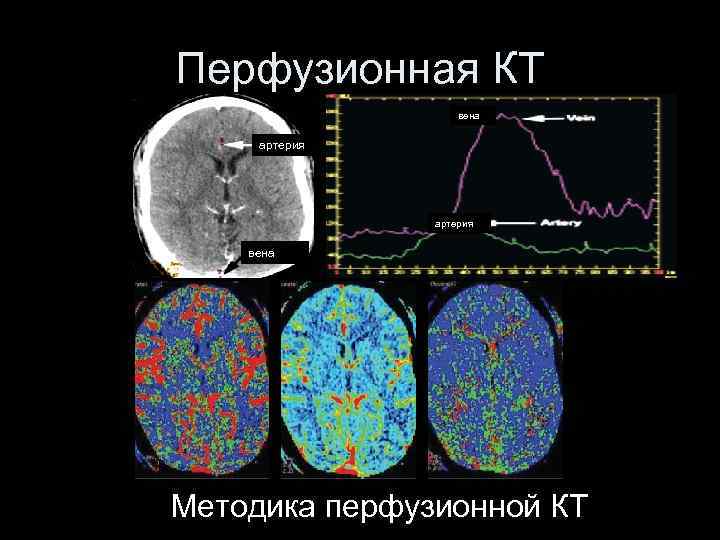
Перфузионная КТ вена артерия вена Методика перфузионной КТ
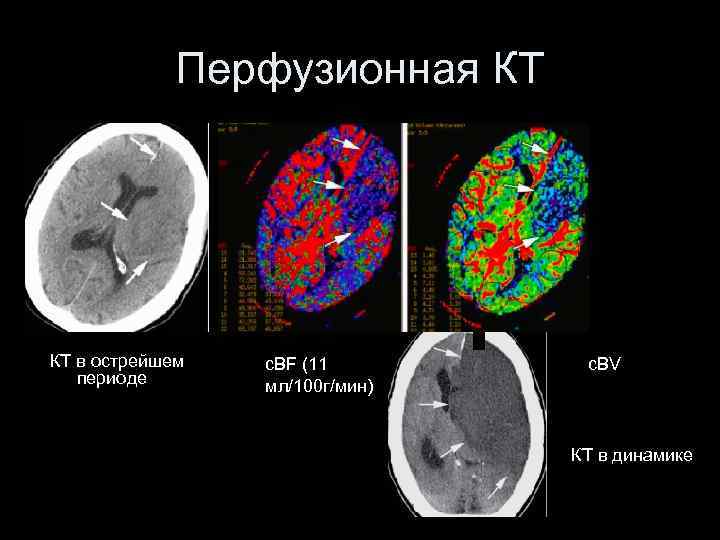
Перфузионная КТ КТ в острейшем периоде c. BF (11 мл/100 г/мин) c. BV КТ в динамике
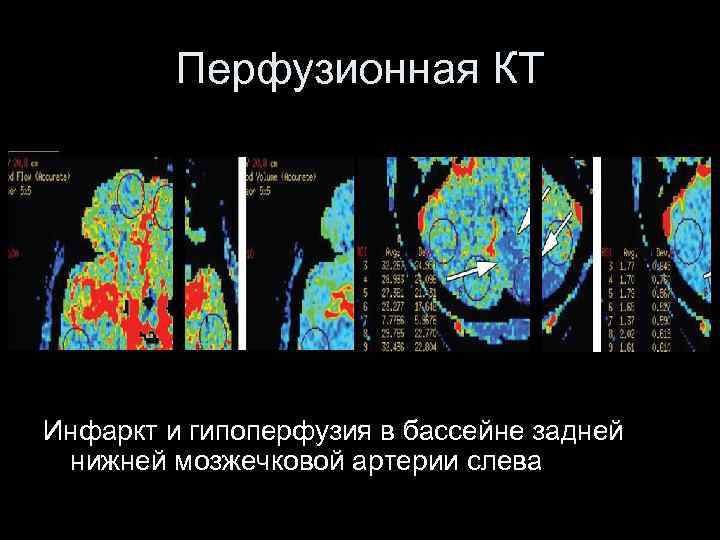
Перфузионная КТ Инфаркт и гипоперфузия в бассейне задней нижней мозжечковой артерии слева
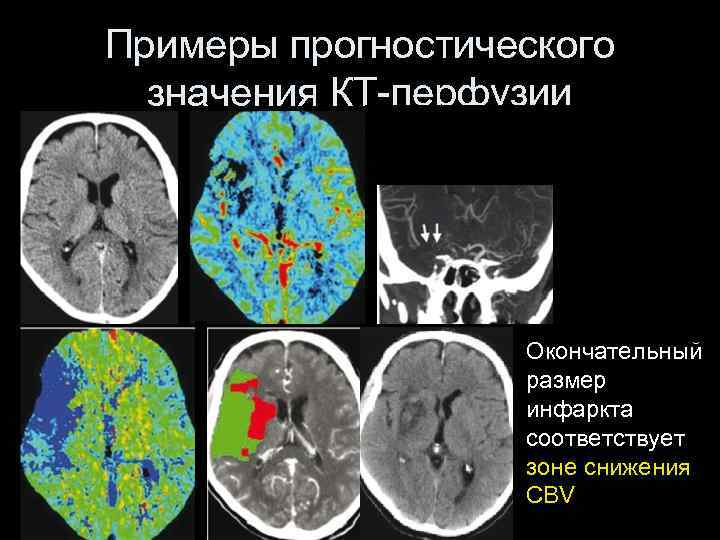
Примеры прогностического значения КТ-перфузии Окончательный размер инфаркта соответствует зоне снижения CBV
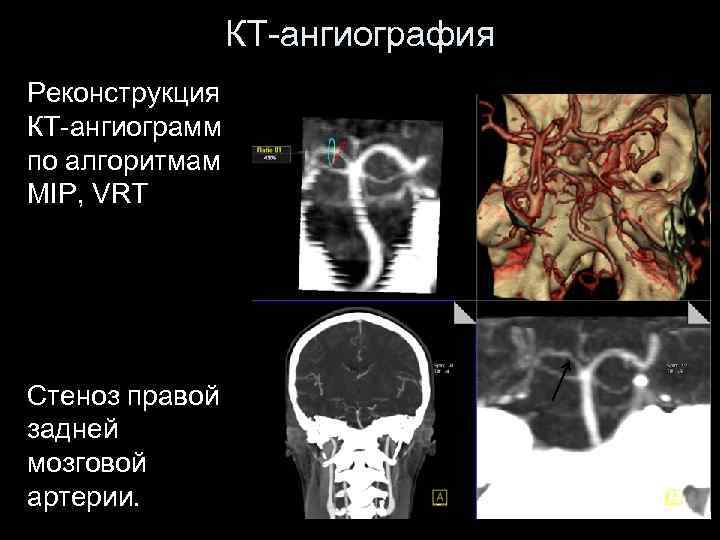
КТ-ангиография Реконструкция КТ-ангиограмм по алгоритмам MIP, VRT Стеноз правой задней мозговой артерии.
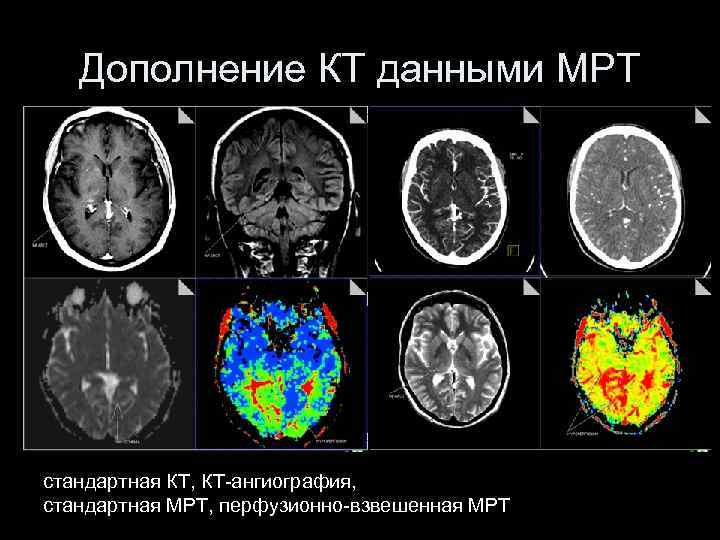
Дополнение КТ данными МРТ стандартная КТ, КТ-ангиография, стандартная МРТ, перфузионно-взвешенная МРТ

Недостатки КТ и особенности ее проведения Методика Недостатки и особенности Неусиленная КТ Ключевой фактор – отсутствие геморрагии Незначительные гипоплотные участки значения не имеют Наличие признаков инфаркта на территории от 1/3 бассейна СМА и более – противопоказание к тромболизису Гиперплотная СМА не всегда указывает на тромбоз, лучше сделать КТАГ Необходим тщательный поиск крови в субарахноидальных пространствах и желудочках КТ перфузия Ограниченность покрытия Неинформативность при движениях, оценка цветных карт перфузии при двигательных артефактах – ошибочна. Лучше применять контралатеральные сосуды для измерения фракции притока/оттока Легче сначала оценить МТТ, а потом сравнивать соотношение CBF/CBV КТ-ангиография Следует использовать предустановленные прицельные MIP для быстрого анализа Внимательно оценить основную артерию и кавернозную часть ВСА Исходные срезы позволяют судить о перфузии Оценивать данные вместе с клиникой

Роль МРТ при инсульте • Визуализация в острейшей стадии для раннего выявления ишемического очага (диффузионно-взвешенная МРТ) • Обнаружение потенциально восстановимой мозговой паренхимы (перфузионно-диффузионное несоответствие)

Преимущества и недостатки традиционной МРТ при инсульте ПРЕИМУЩЕСТВА НЕДОСТАТКИ Неинвазивность Недостаточная доступность, высокая стоимость Отсутствие лучевой нагрузки Наличие противопоказаний Высокое разрешение, высокий тканевой контраст Низкая чувствительность в острейшую стадию Чувствительность к изменениям Сложно оценить степень ствола, структур задней ямки ишемического поражения Возможность манипулирования тканевым контрастом Разные последовательности позволяют получать дополнительную информацию Невозможность отличить жизнеспособную ткань
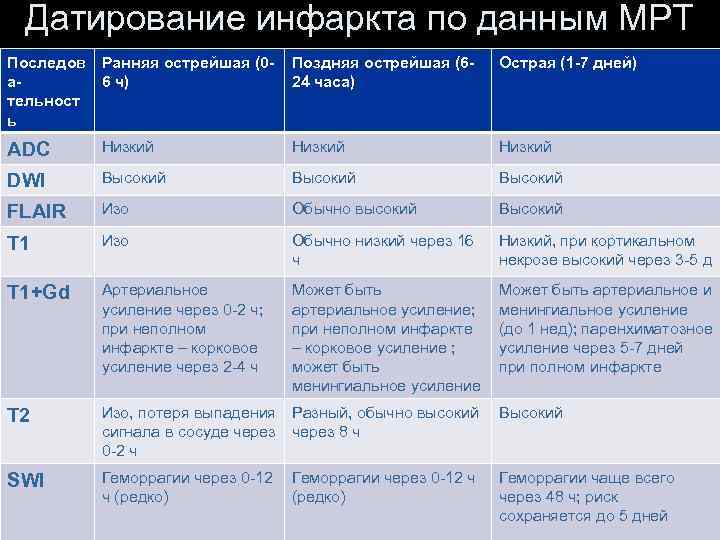
Датирование инфаркта по данным МРТ Последов Ранняя острейшая (0 а 6 ч) тельност ь Поздняя острейшая (624 часа) Острая (1 -7 дней) ADC Низкий DWI Высокий FLAIR Изо Обычно высокий Высокий T 1 Изо Обычно низкий через 16 ч Низкий, при кортикальном некрозе высокий через 3 -5 д T 1+Gd Артериальное усиление через 0 -2 ч; при неполном инфаркте – корковое усиление через 2 -4 ч Может быть артериальное усиление; при неполном инфаркте – корковое усиление ; может быть менингиальное усиление Может быть артериальное и менингиальное усиление (до 1 нед); паренхиматозное усиление через 5 -7 дней при полном инфаркте T 2 Изо, потеря выпадения Разный, обычно высокий Высокий сигнала в сосуде через 8 ч 0 -2 ч SWI Геморрагии через 0 -12 ч ч (редко) Геморрагии чаще всего через 48 ч; риск сохраняется до 5 дней

Датирование инфаркта по данным МРТ Последов Подострый (1 -3 нед) ательност ь Хронический (>3 нед) ADC Низкий 7 -10 д; может стать изо через 10 -15 д; потом высокий Высокий DWI Высокий 10 -14 д; затем изо или низкий; высокий при Т 2 просвечивании Разный; м. б. изо; высокий при Т 2 просвечивании; низкий в кистах FLAIR Высокий Низкий в кистах T 1 Низкий; часто высокий в корковом некрозе после 2 недель Низкий; может быть высокий при корковом некрозе (проходит через 3 мес. , редко виден до года) T 1+Gd Паренхиматозное усиление при полном инфаркте 1 -8 нед инфаркте может сохраняться 8 нед – 4 мес T 2 Высокий; через 2 -3 нед - затуманивание Высокий
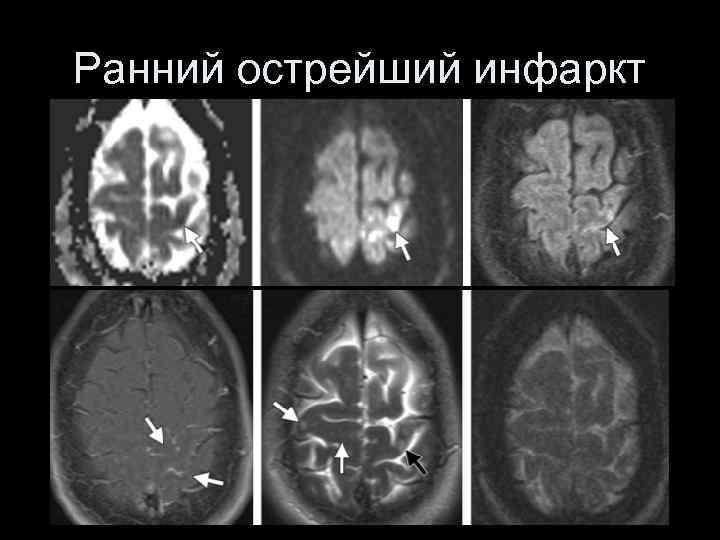
Ранний острейший инфаркт
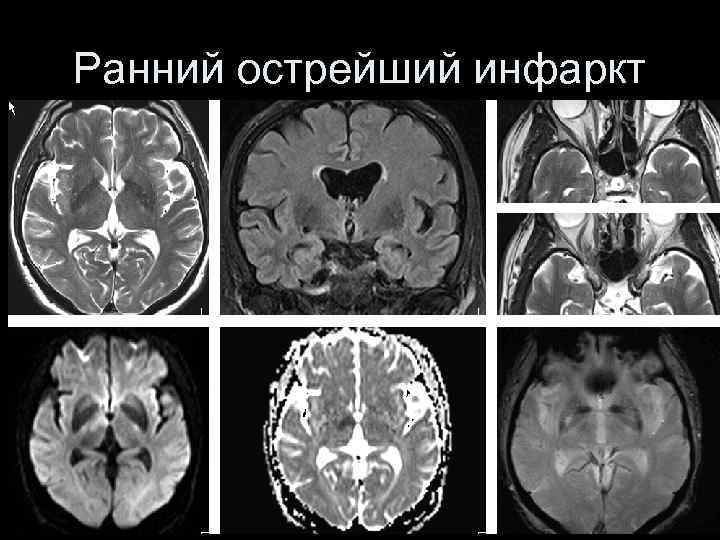
Ранний острейший инфаркт
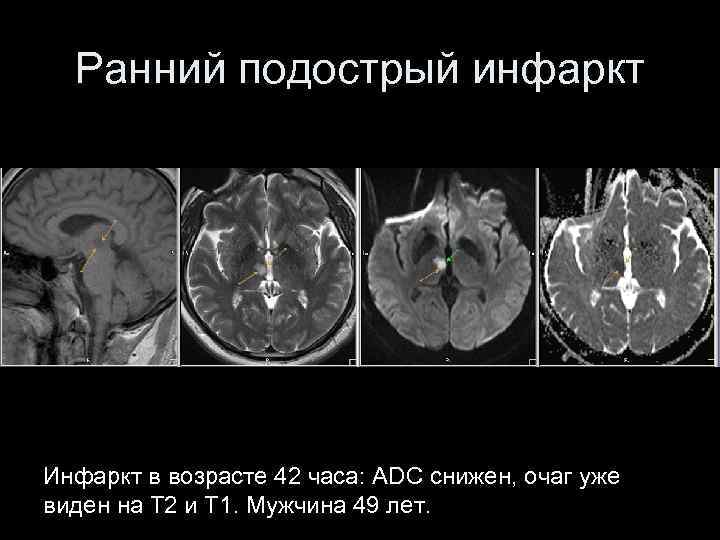
Ранний подострый инфаркт Инфаркт в возрасте 42 часа: ADC снижен, очаг уже виден на Т 2 и Т 1. Мужчина 49 лет.
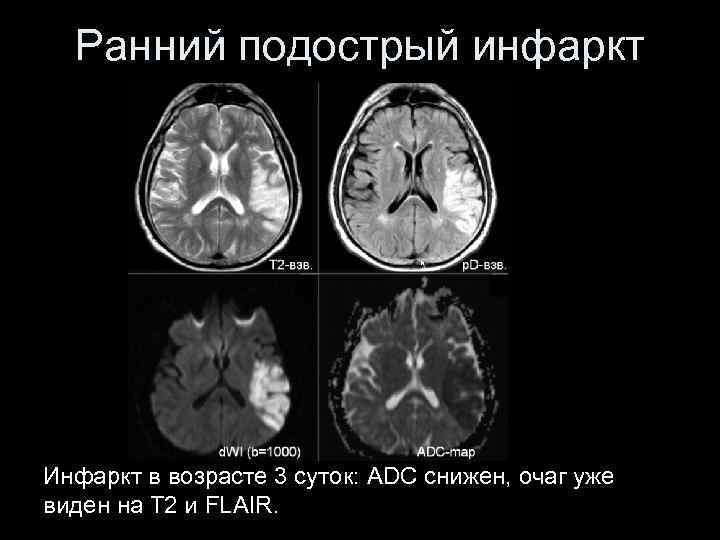
Ранний подострый инфаркт Инфаркт в возрасте 3 суток: ADC снижен, очаг уже виден на Т 2 и FLAIR.
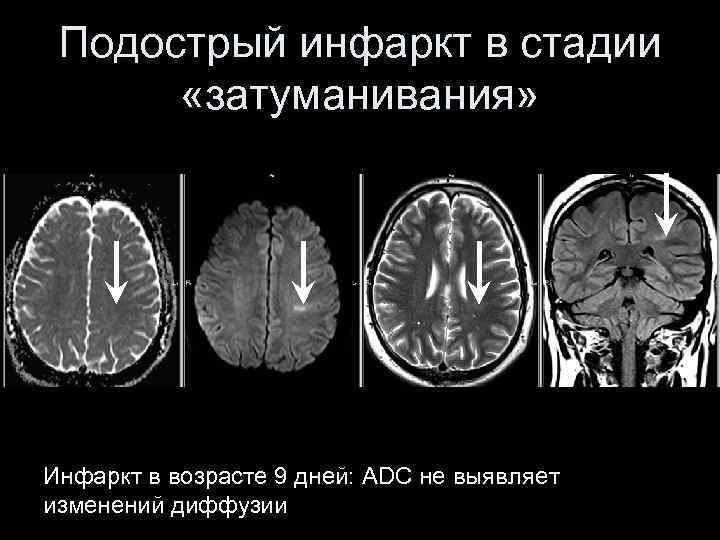
Подострый инфаркт в стадии «затуманивания» Инфаркт в возрасте 9 дней: ADC не выявляет изменений диффузии
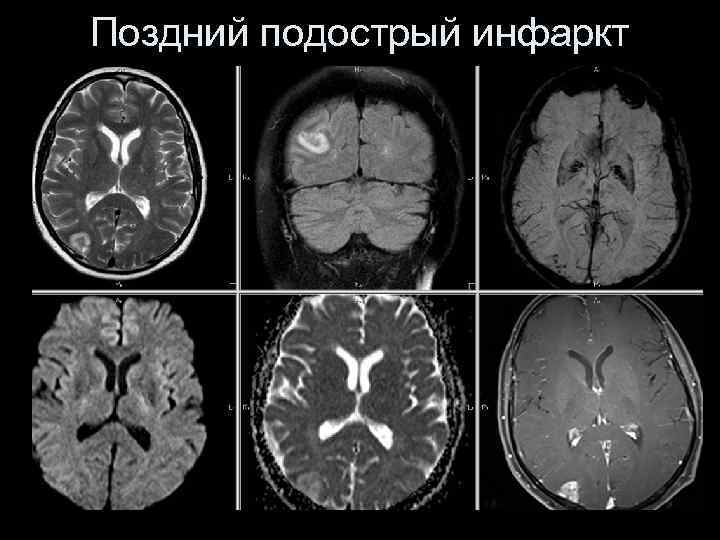
Поздний подострый инфаркт
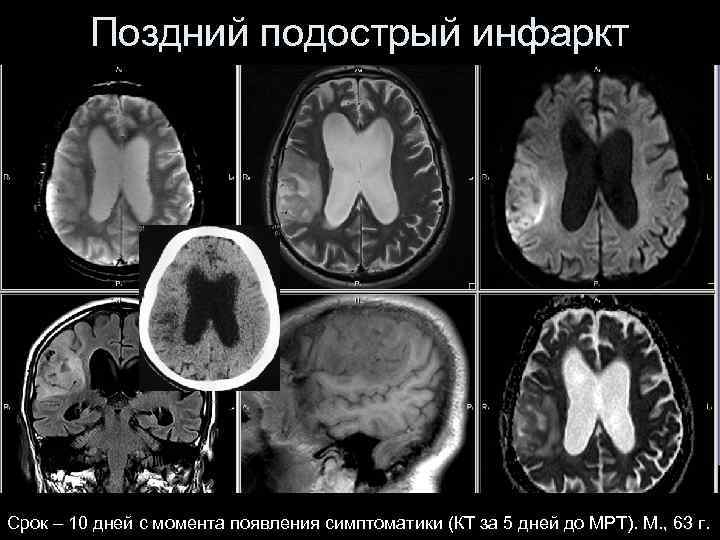
Поздний подострый инфаркт Срок – 10 дней с момента появления симптоматики (КТ за 5 дней до МРТ). М. , 63 г.
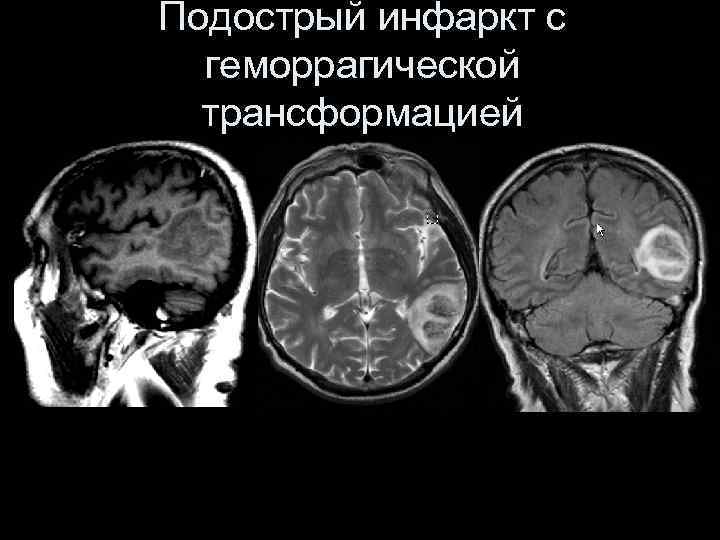
Подострый инфаркт с геморрагической трансформацией
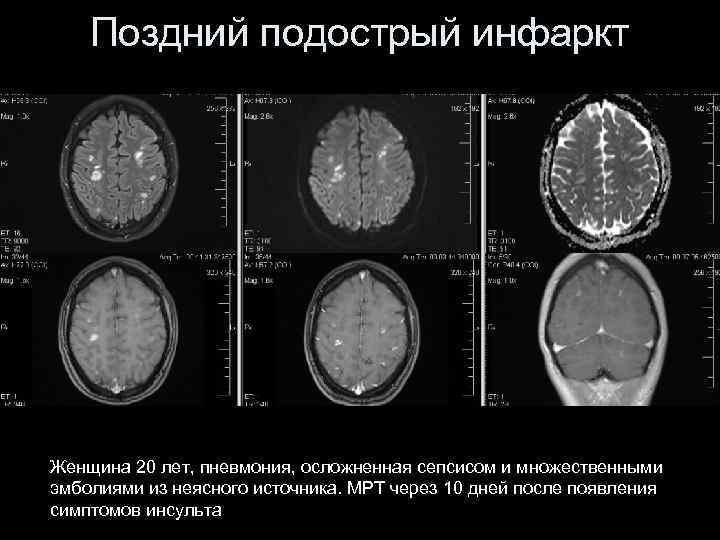
Поздний подострый инфаркт Женщина 20 лет, пневмония, осложненная сепсисом и множественными эмболиями из неясного источника. МРТ через 10 дней после появления симптомов инсульта
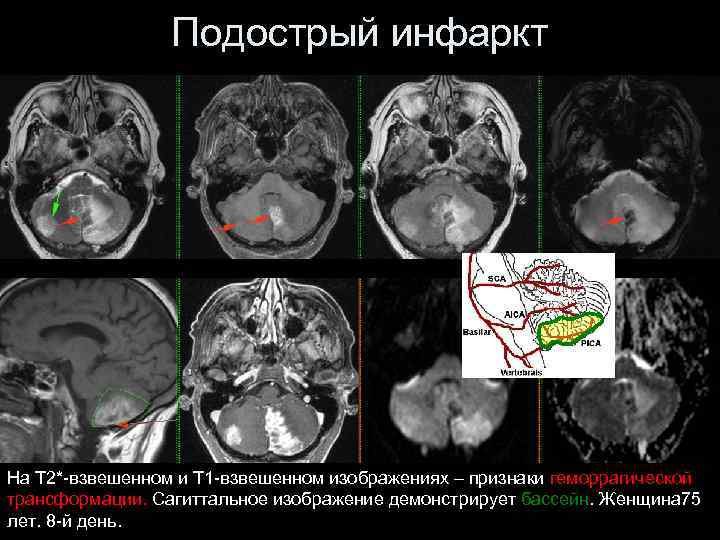
Подострый инфаркт На Т 2*-взвешенном и Т 1 -взвешенном изображениях – признаки геморрагической трансформации. Сагиттальное изображение демонстрирует бассейн. Женщина 75 лет. 8 -й день.
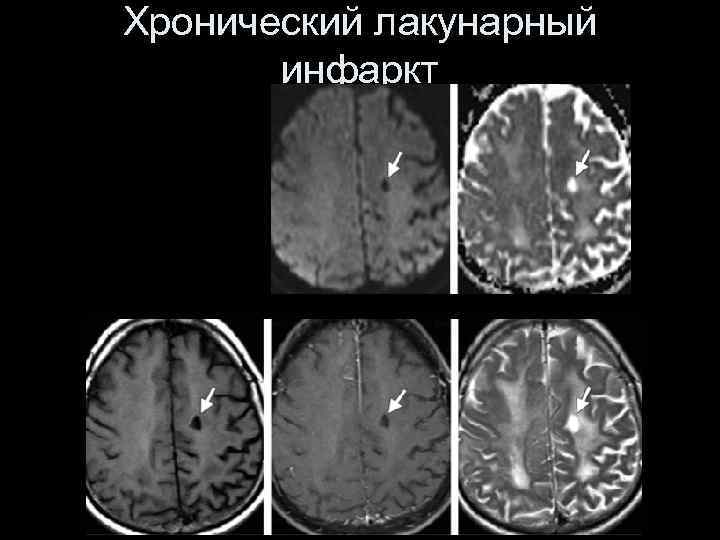
Хронический лакунарный инфаркт
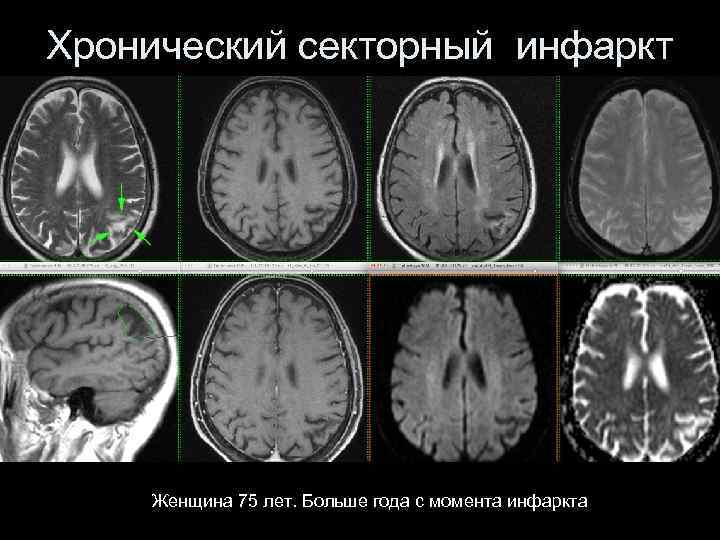
Хронический секторный инфаркт Женщина 75 лет. Больше года с момента инфаркта
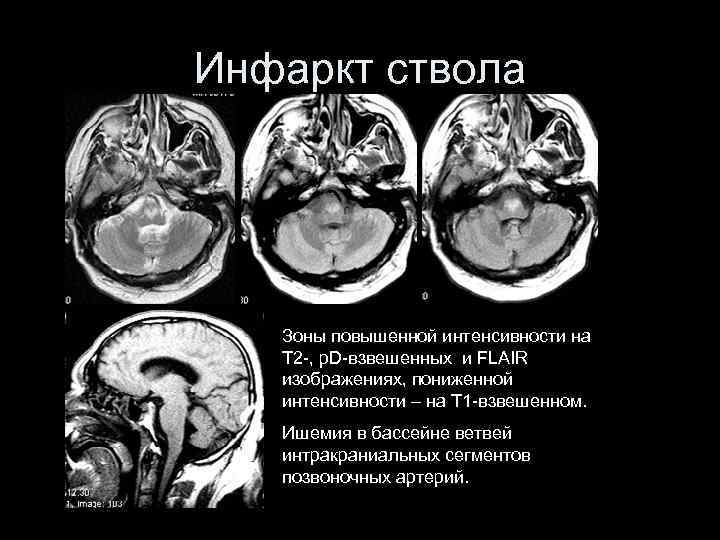
Инфаркт ствола Зоны повышенной интенсивности на T 2 -, p. D-взвешенных и FLAIR изображениях, пониженной интенсивности – на T 1 -взвешенном. Ишемия в бассейне ветвей интракраниальных сегментов позвоночных артерий.
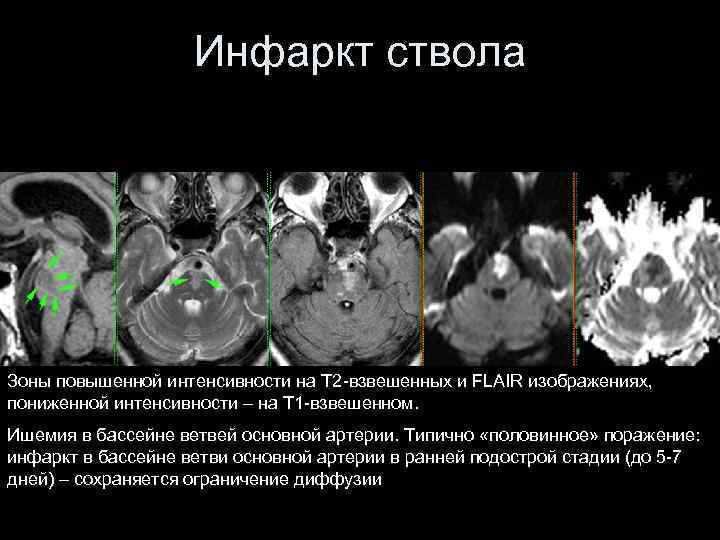
Инфаркт ствола Зоны повышенной интенсивности на T 2 -взвешенных и FLAIR изображениях, пониженной интенсивности – на T 1 -взвешенном. Ишемия в бассейне ветвей основной артерии. Типично «половинное» поражение: инфаркт в бассейне ветви основной артерии в ранней подострой стадии (до 5 -7 дней) – сохраняется ограничение диффузии
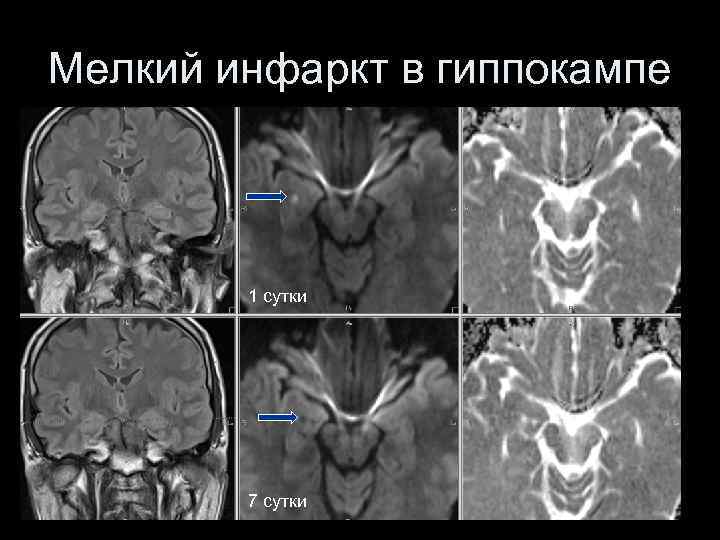
Мелкий инфаркт в гиппокампе 1 сутки 7 сутки
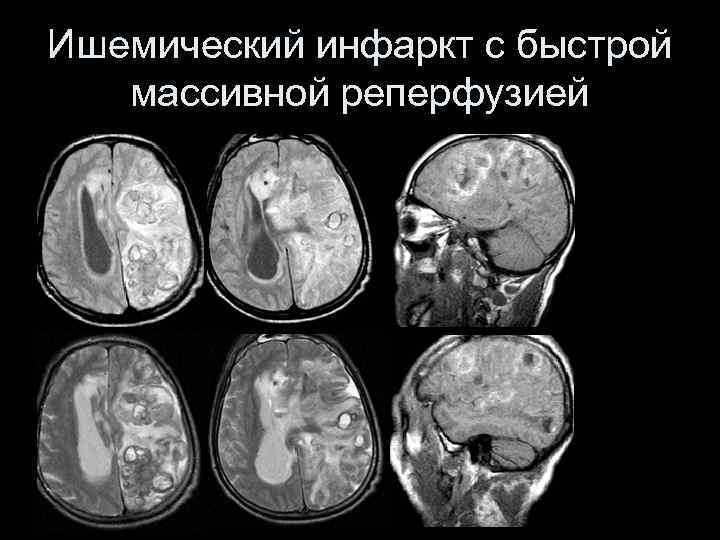
Ишемический инфаркт с быстрой массивной реперфузией
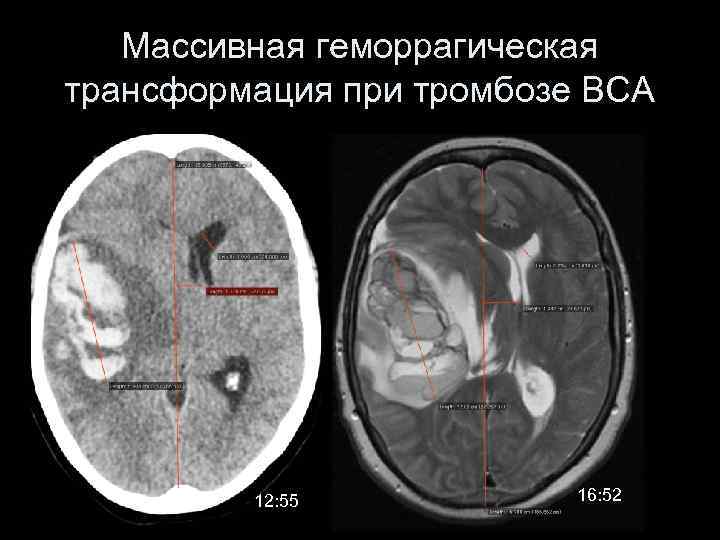
Массивная геморрагическая трансформация при тромбозе ВСА 12: 55 16: 52
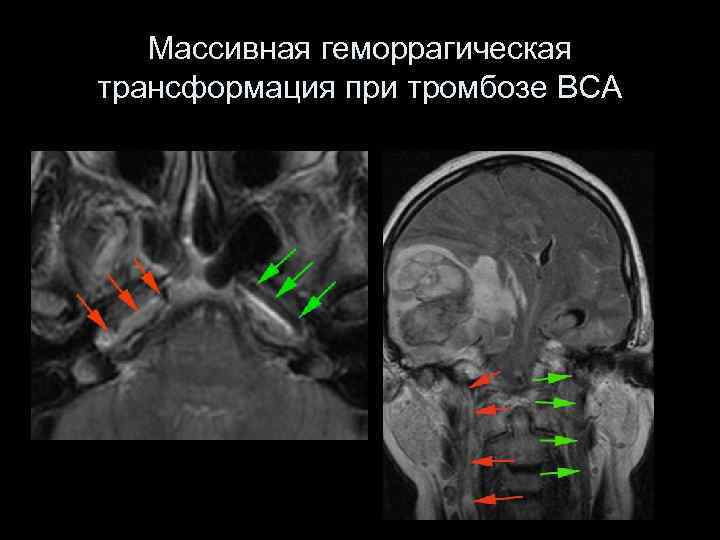
Массивная геморрагическая трансформация при тромбозе ВСА
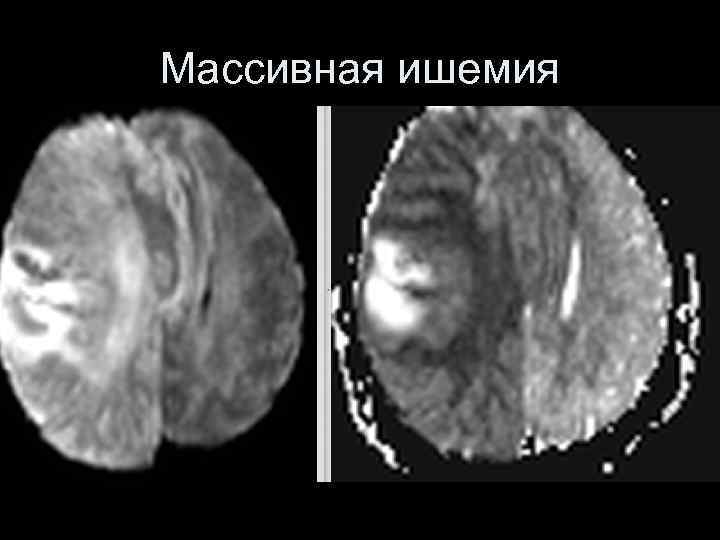
Массивная ишемия
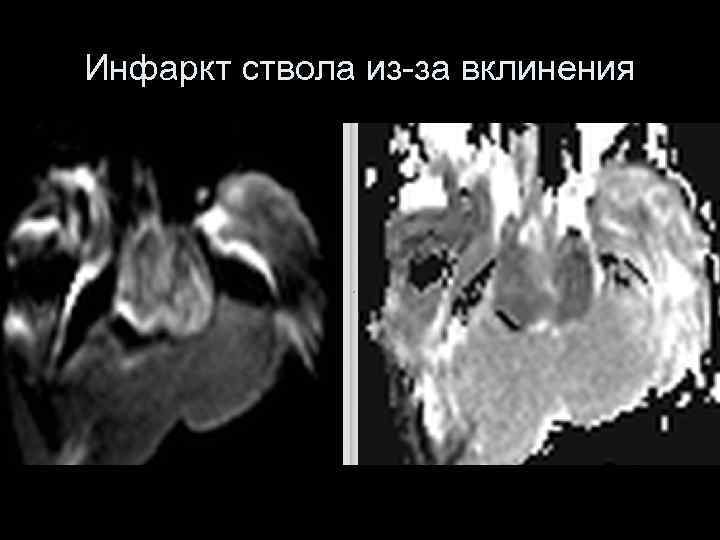
Инфаркт ствола из-за вклинения
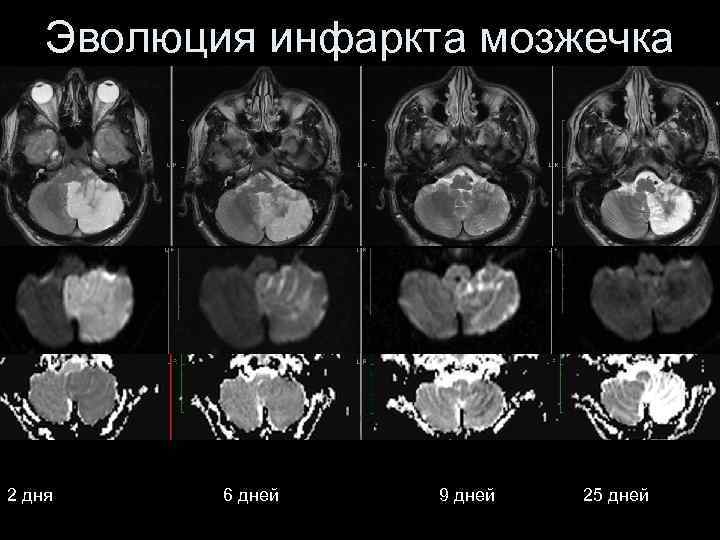
Эволюция инфаркта мозжечка 2 дня 6 дней 9 дней 25 дней
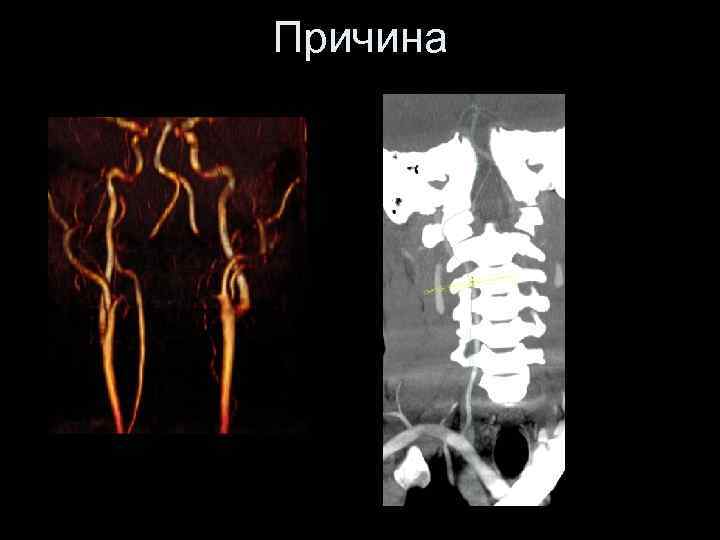
Причина
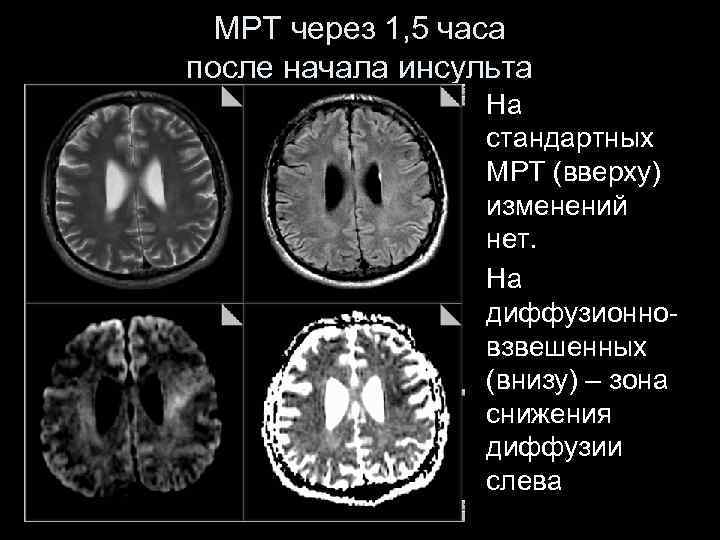
МРТ через 1, 5 часа после начала инсульта На стандартных МРТ (вверху) изменений нет. На диффузионновзвешенных (внизу) – зона снижения диффузии слева
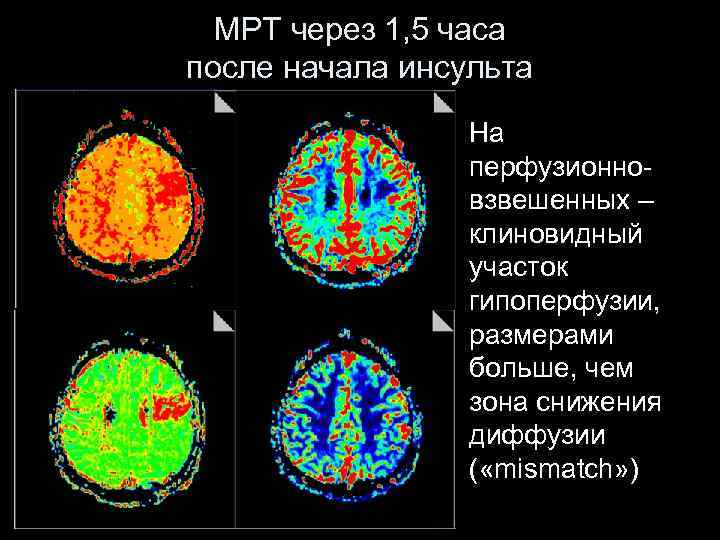
МРТ через 1, 5 часа после начала инсульта На перфузионновзвешенных – клиновидный участок гипоперфузии, размерами больше, чем зона снижения диффузии ( «mismatch» )
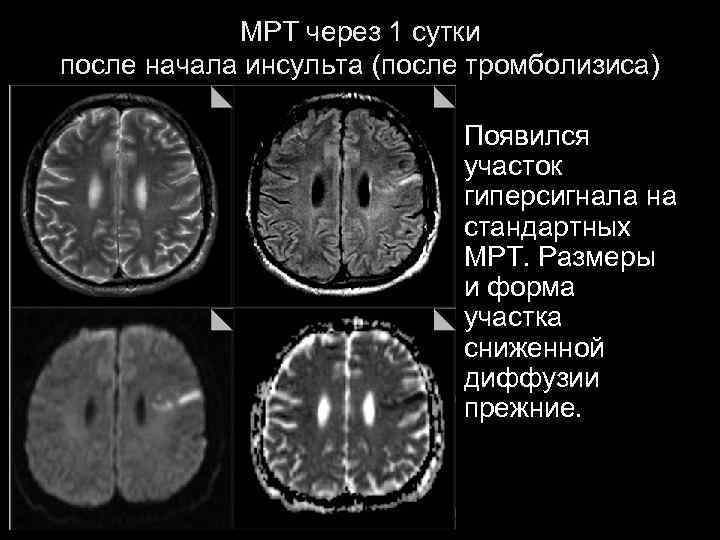
МРТ через 1 сутки после начала инсульта (после тромболизиса) Появился участок гиперсигнала на стандартных МРТ. Размеры и форма участка сниженной диффузии прежние.
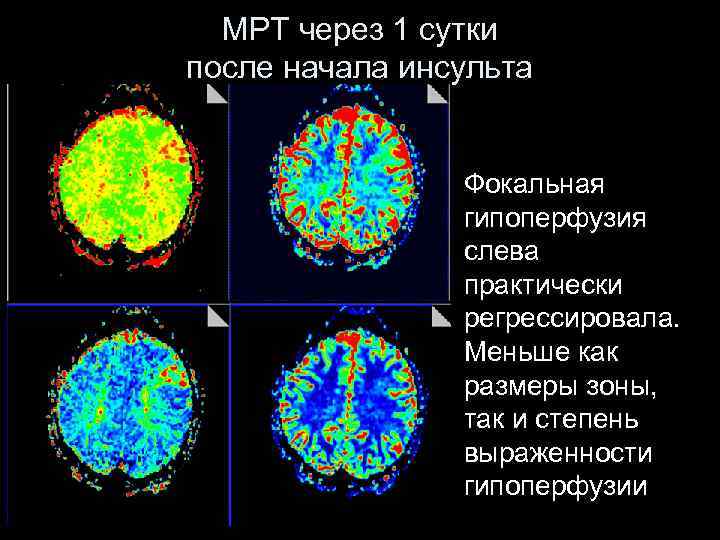
МРТ через 1 сутки после начала инсульта Фокальная гипоперфузия слева практически регрессировала. Меньше как размеры зоны, так и степень выраженности гипоперфузии
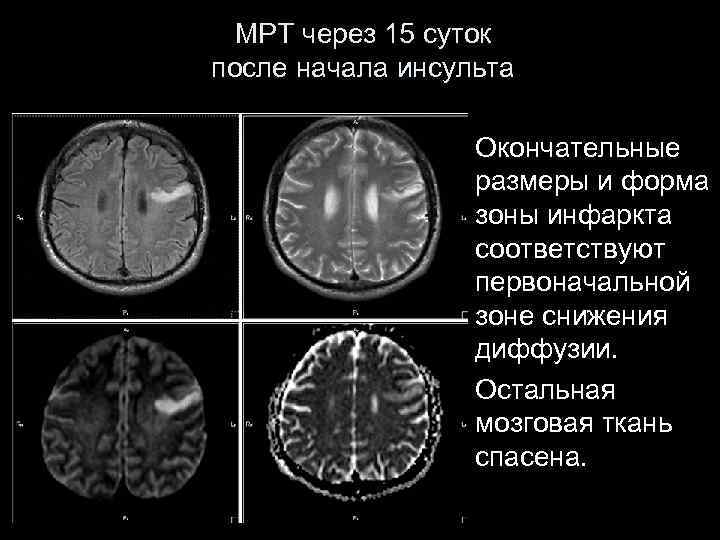
МРТ через 15 суток после начала инсульта Окончательные размеры и форма зоны инфаркта соответствуют первоначальной зоне снижения диффузии. Остальная мозговая ткань спасена.
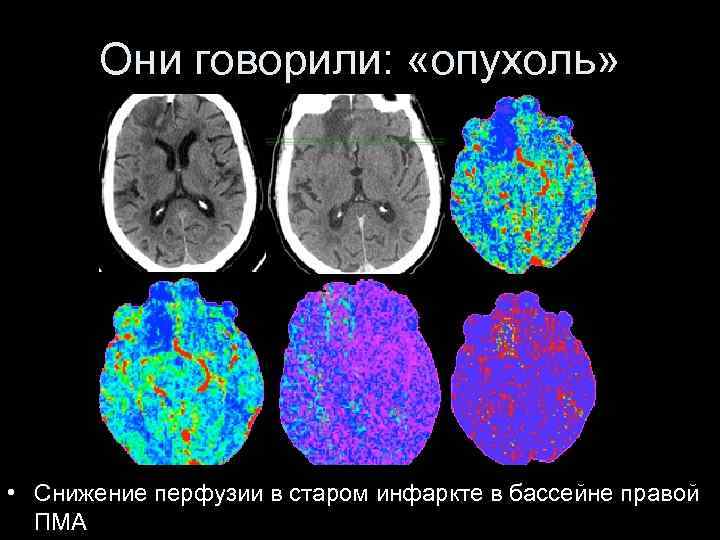
Они говорили: «опухоль» • Снижение перфузии в старом инфаркте в бассейне правой ПМА

Визуализация перфузии

Последние рекомендации по МР-диффузии и МРперфузии • • RECOMMENDATIONS DWI should be considered superior to noncon- trast CT scan for the diagnosis of acute ischemic stroke in patients presenting within 12 hours of symptom onset (Level A). There is insufficient evidence to support or refute the value of PWI in diagnosing acute ischemic stroke (Level U). Baseline DWI volume should be considered use- ful in predicting baseline clinical stroke severity and final lesion volume in anterior-circulation stroke syndromes (Level B). Baseline DWI volume may be considered not use-ful in predicting baseline NIHSS score in posterior-circulation stroke syndromes (Level C). Baseline DWI volume may be considered useful in predicting clinical outcome as measured by the NIHSS and Barthel Index (Level C). Baseline PWI volume may be considered useful in predicting baseline clinical stroke severity (Level C). • DWI превосходит КТ без контраста в диагностике острого ишемического инсульта в первые 12 часов после появления симптомов (Уровень А) • Нет достаточных тельносттельств рекомендации выполнять или не выполнять • • PWI при диагностике ОИИ (Уровень У) Базовый объем инфаркта на DWI полезен для предсказания тяжести инфаркта и окончательных его размеров при инсульте в передней циркуляции (Уровень Б) Базовый объем инфаркта на DWI может считать бесполезным в предсказании тяжести по шкале NIHSS при инсульте в задней циркуляции (Уровень С) Базовый объем инфаркта на DWI может считаться полезным в предсказании клинического исхода по шкале NIHSS и индексу Barthel (Уровень С) Базовый объем инфаркта на PWI может считаться полезным в предсказании базовой клинической тяжести инфаркта (Уровень С)

Перфузионная визуализация - ишемия • Несмотря на широкое применение в клинической практике, диагностическая и клиническая полезность перфузионной МРТ не доказана в контролируемых, адекватного дизайна исследованиях • Не существует, определения того, какой метод определения перфузии наиболее точен. • Дополнительную сумятицу в отсутствующий консенсус вносят различные определения того, что представляют из себя ядро инфаркта, регион полутени и окончательный его размер, а также клинический исход • крайне важно проведение многоцентровых, проспективных, систематических исследований для полной оценки этого многообещающего диагностического инструмента

Перфузионная визуализация - ишемия • 1. Объемы ядра инфаркта и ишемической полутени при поступлении могут явиться значимыми предсказательными факторами для оценки клинического исхода, с возможностями, потенциально превышающими таковые у используемых клинических шкал (NIHSS) (Класс рекомендации IIb, уровень доказательности: B). • 2. Имеется все большее число косвенных данных, что даже относительно неточное измерение несовпадение объема инфарктного ядра и ишемической полутени может быть использовано для отбора пациентов для проведения внутривенного тромболитического лечения за пределами трехчасового промежутка. При совместном применении с методиками сосудистой визуализации, такой подход может потенциально помочь в оценке уместности других способов лечения, таких, как механическое разрушение тромба и внутриартериальный тромболизис, а также предоставить суррогатный способ оценки эффективности лечения (Класс рекомендации IIb, уровень доказательности: B).

ПЕРФУЗИЯ • Клиническая полезность адекватно не доказана • DIAS-II – нет преимущества в отборе пациентов для ТЛ на основе PWI • DEFUSE, DEFUSE-2, EPITHET – получили + результаты при отборе пациентов на ТЛ после 3 часов • MR RESCUE – не выявило разницы • Уровень 2 B

ПЕРФУЗИЯ • Имеет значение не только для выявления полутени • Повышает точность диагностики инфаркта при отрицательной НУКТ • Позволяет увидеть окклюзию мелкого сосуда благодаря гипоперфузии снабжаемого им сектора • Исключает имитаторы инсульта • Лучше оценивает ядро и коллатеральный поток • Предсказывает риск кровоизлияния

Геморрагический инсульт

Эпидемиология и экономика • • • 10 -20% всех инсультов 24, 4 на 100 000 населения в год в России смертность в остром периоде - 40 -50% инвалидизация - 75% тенденция к увеличению частоты церебральной геморрагии из-за неконтролируемой АГ • расчетная сумма затрат на проблему геморрагического инсульта в России - от 2, 4 до 3, 6 млрд долларов в год

Причины нетравматичекой церебральной геморрагии • • • Артериальная гипертензия Сосудистая мальформация, аневризма Амилодная ангиопатия Коагулопатии Венозный тромбоз Геморрагическая трансформация ишемического инфаркта • Кровоизлияние в опухоль

Лучевая диагностика • • УЗИ Стандартная рентгенография Традиционная ангиография Компьютерная томография с КТангиографией • Магнитно-резонансная томография с МРангиографией • Методы выбора: КТ и АГ.

КТ при первичном паренхиматозном кровоизлияинии

Роль КТ при ППК • Установить наличие гематомы (только в 50% при гематомах есть кровь в ликворе) и ее особенности • Выявить внутрижелудочковое кровоизлияние (прогноз!) • Дифференцировать первичные и вторичные гематомы (опухоли, метастазы, сосудистые мальформации) • Отследить динамику при неясной клинической картине • Установить наличие осложнений • Послеоперационный контроль
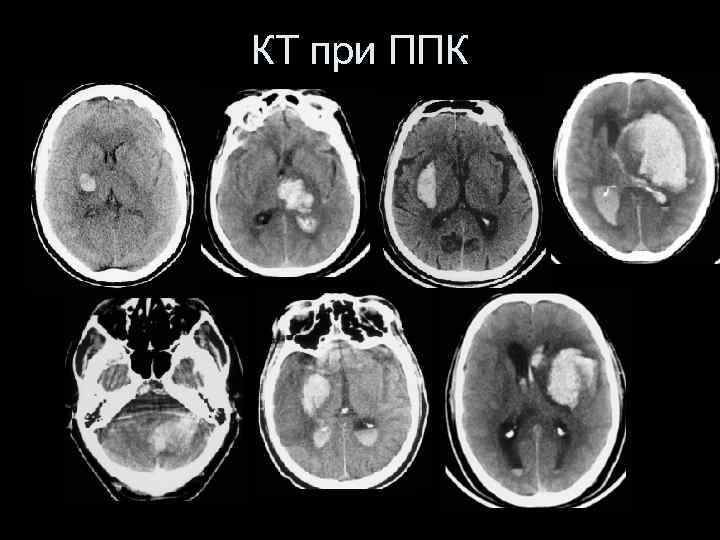
КТ при ППК

Амилоидная ангиопатия • Самая частая причина негипертензионного кровоизлияния у пожилых • Имеется у 33% на аутопсии в возрасте 60 -70, с увеличением частоты до 75% после 90 лет. • β-амилоид откладывается в медии и адвентиции мелких и среднего калибра сосудов коры, субкортикального вещества, мягкой оболочки • В 25 -40% кровоизлияние наступает на фоне деменции • Сочетается с выраженной атрофией и лейкоэнцефалопатией
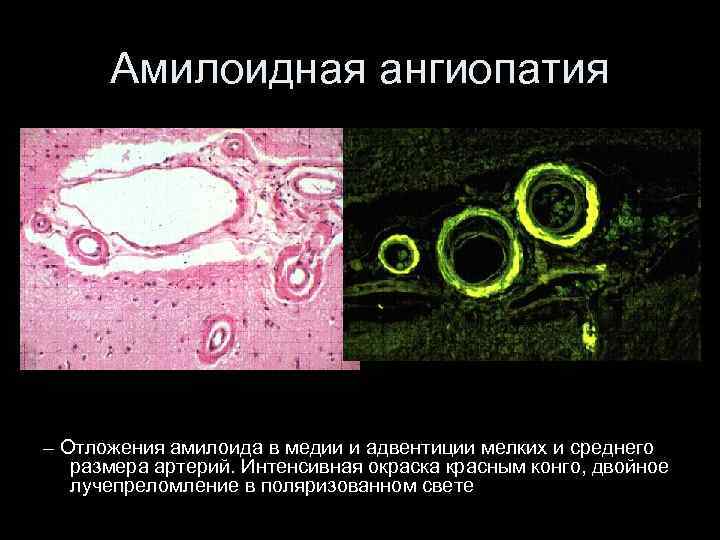
Амилоидная ангиопатия – Отложения амилоида в медии и адвентиции мелких и среднего размера артерий. Интенсивная окраска красным конго, двойное лучепреломление в поляризованном свете
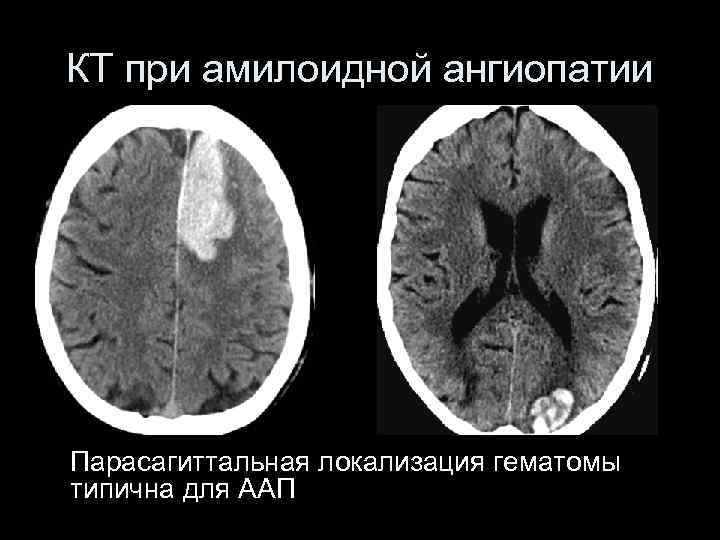
КТ при амилоидной ангиопатии Парасагиттальная локализация гематомы типична для ААП
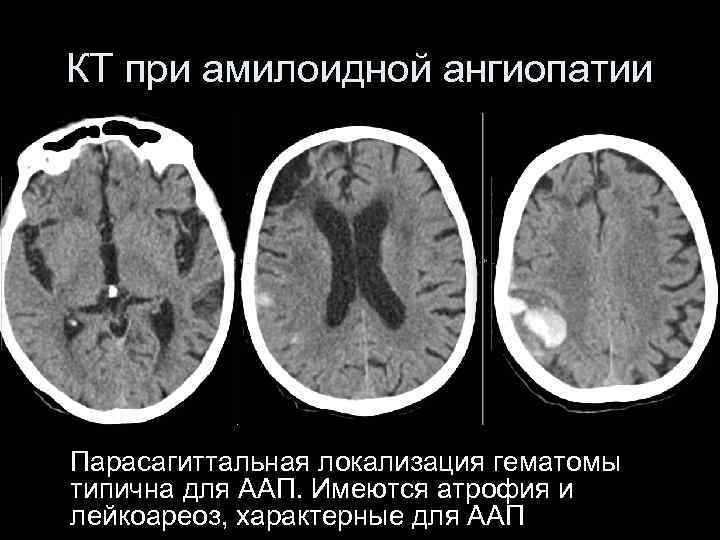
КТ при амилоидной ангиопатии Парасагиттальная локализация гематомы типична для ААП. Имеются атрофия и лейкоареоз, характерные для ААП
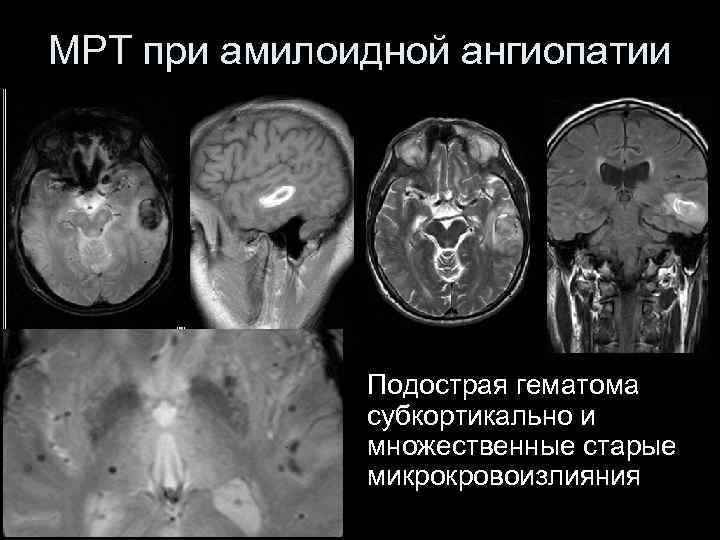
МРТ при амилоидной ангиопатии Подострая гематома субкортикально и множественные старые микрокровоизлияния
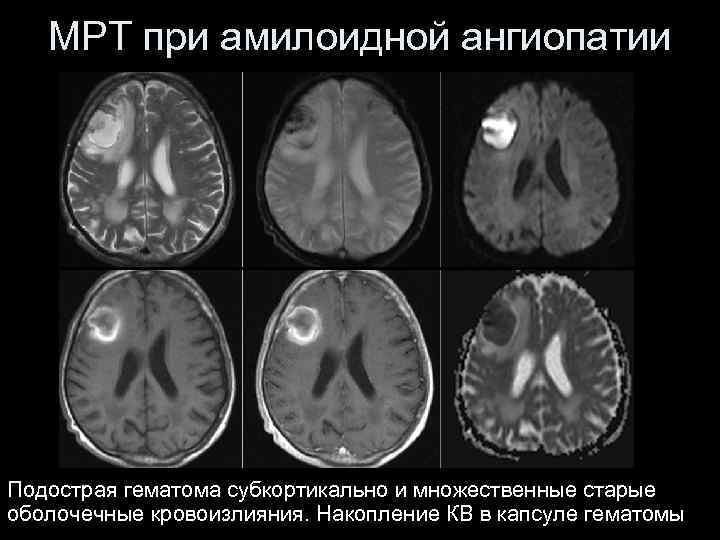
МРТ при амилоидной ангиопатии Подострая гематома субкортикально и множественные старые оболочечные кровоизлияния. Накопление КВ в капсуле гематомы
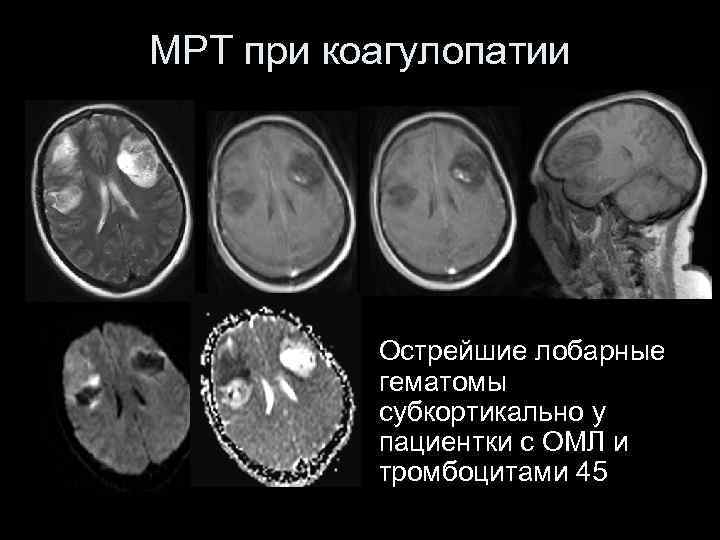
МРТ при коагулопатии Острейшие лобарные гематомы субкортикально у пациентки с ОМЛ и тромбоцитами 45
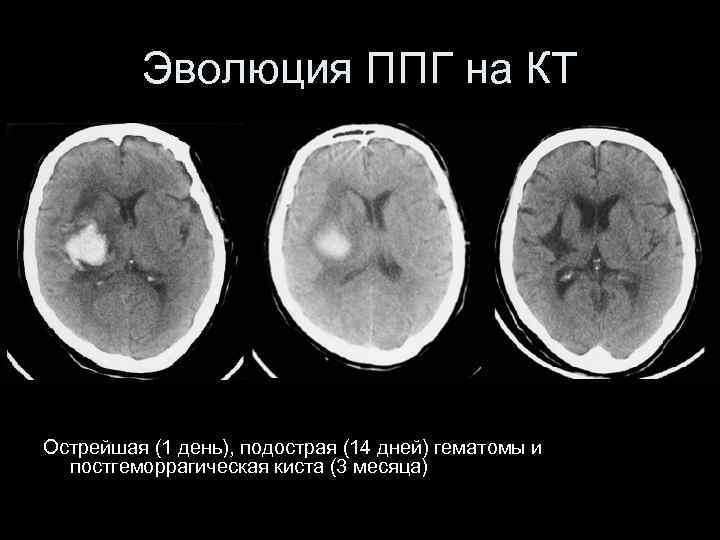
Эволюция ППГ на КТ Острейшая (1 день), подострая (14 дней) гематомы и постгеморрагическая киста (3 месяца)
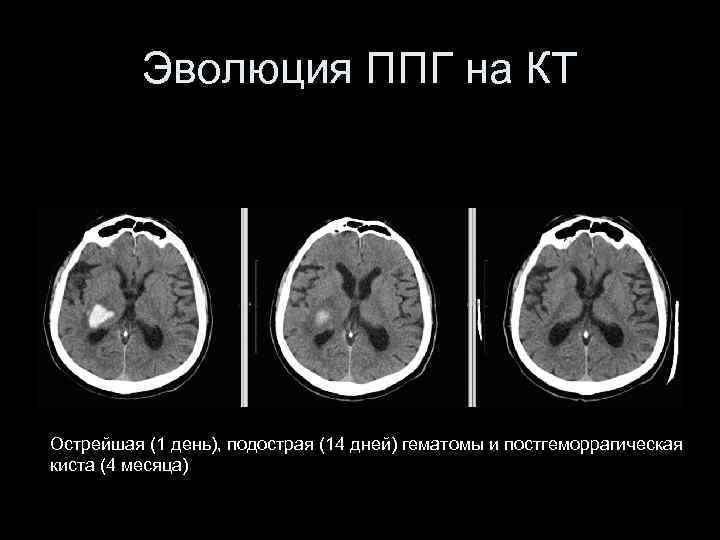
Эволюция ППГ на КТ Острейшая (1 день), подострая (14 дней) гематомы и постгеморрагическая киста (4 месяца)
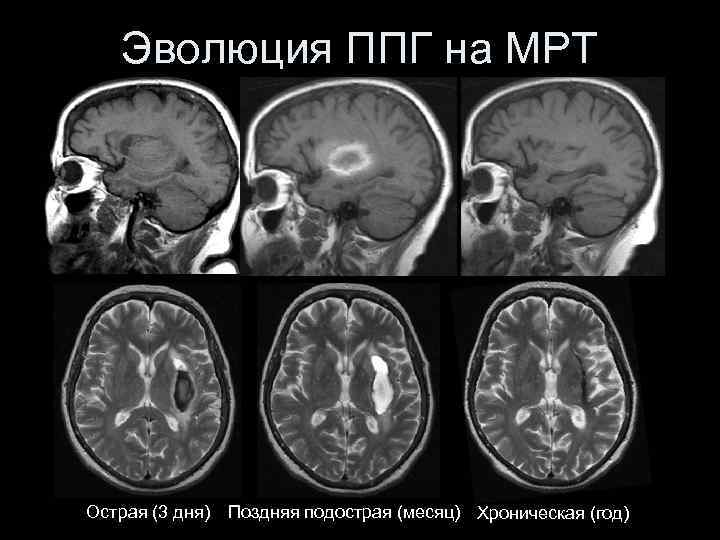
Эволюция ППГ на МРТ а Острая (3 дня) Поздняя подострая (месяц) Хроническая (год)
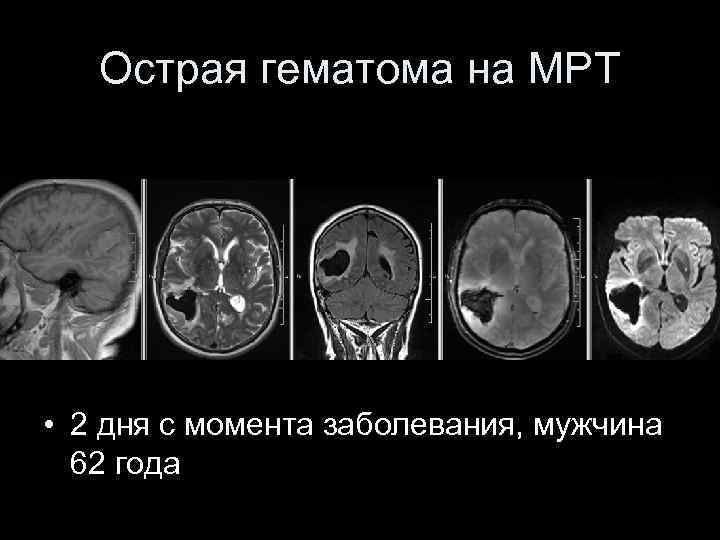
Острая гематома на МРТ • 2 дня с момента заболевания, мужчина 62 года

Применение контраста на КТ при ППГ • a) пациент до 40 лет; • b) нет АГ в анамнезе; • c) прогрессирование неврологическолго дефицита на протяжении более, чем 4 часов; • d) преходящий дефицит в анамнезе; • e) атипичный вид на КТ и диспропорция между субурахноидальной, субдуральной кровью; • f) наличие предполагаемой сопутствующей патологии, такой как онкологическая, бактериальный эндокардит, артериит.
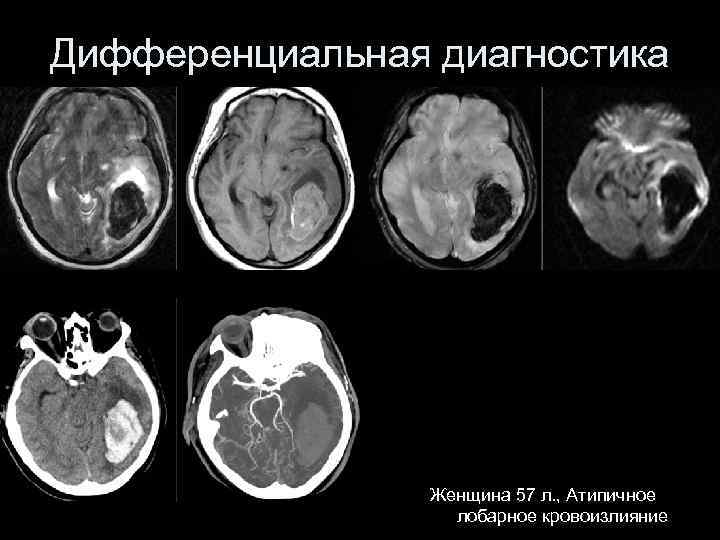
Дифференциальная диагностика Женщина 57 л. , Атипичное лобарное кровоизлияние
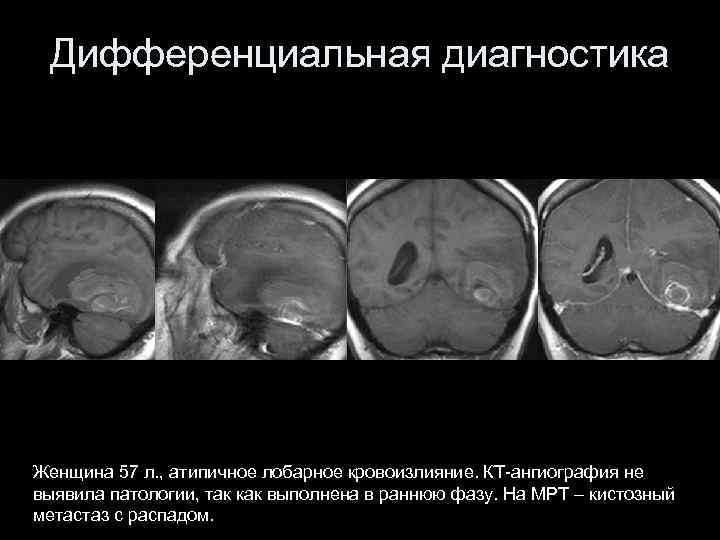
Дифференциальная диагностика Женщина 57 л. , атипичное лобарное кровоизлияние. КТ-ангиография не выявила патологии, так как выполнена в раннюю фазу. На МРТ – кистозный метастаз с распадом.
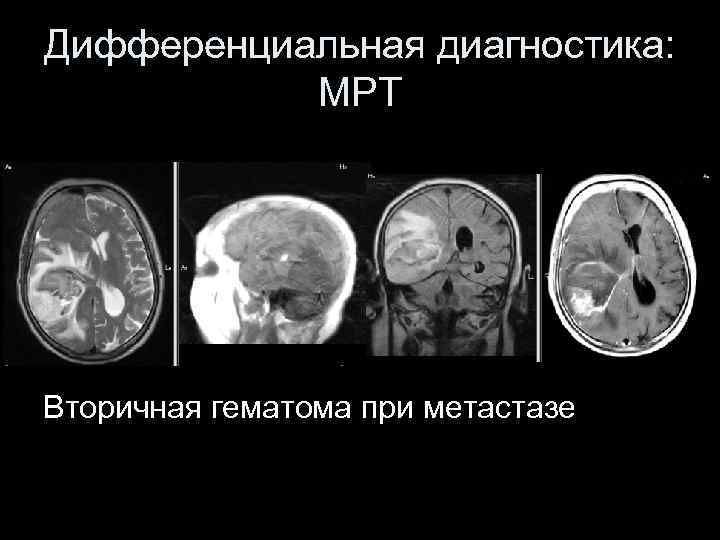
Дифференциальная диагностика: МРТ Вторичная гематома при метастазе
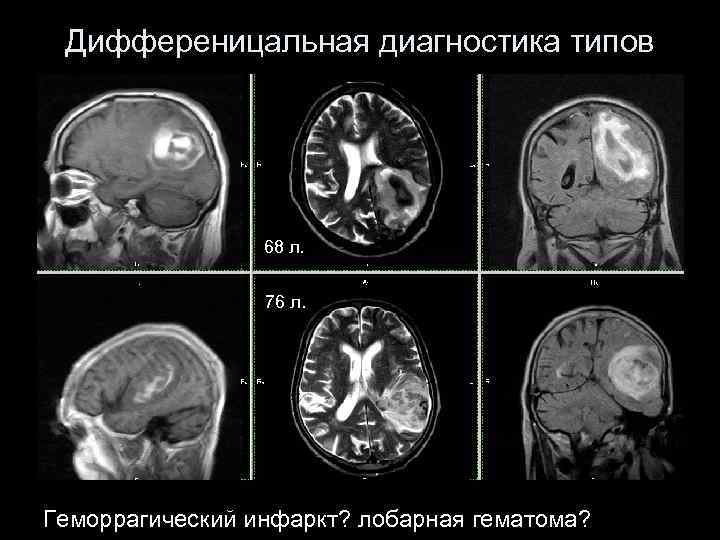
Дифференицальная диагностика типов 68 л. 76 л. Геморрагический инфаркт? лобарная гематома?

КТ при субарахноидальном кровоизлиянии • • 8% всех инсультов 75% всех САК – аневризматические 11 случаев на 100 000 в популяции 25% смертей – на 1 день, 50% - в течении первых 5 -ти дней • Чувствительность КТ – 93 -100% в течение первых 12 часов
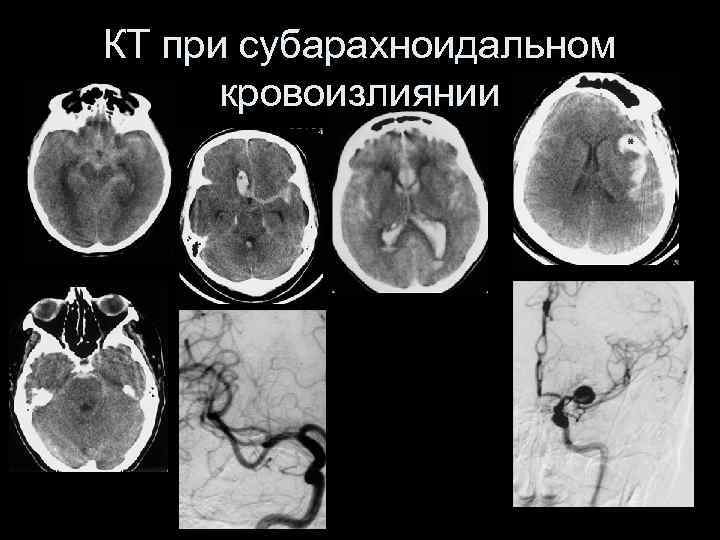
КТ при субарахноидальном кровоизлиянии
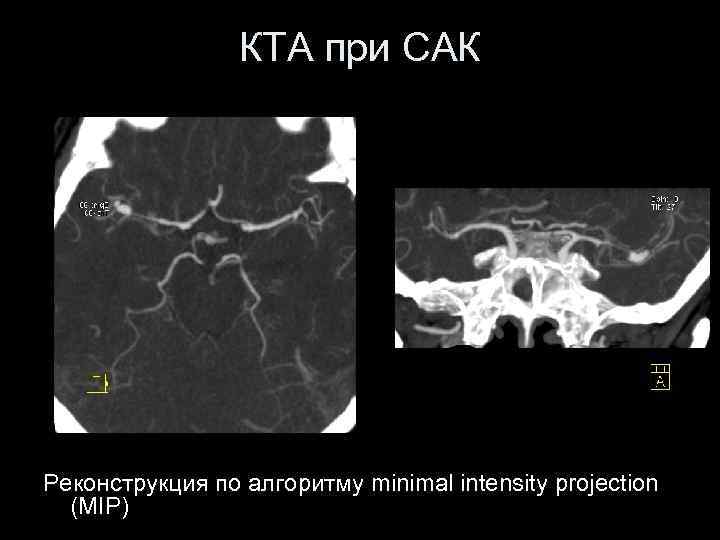
КТА при САК Реконструкция по алгоритму minimal intensity projection (MIP)
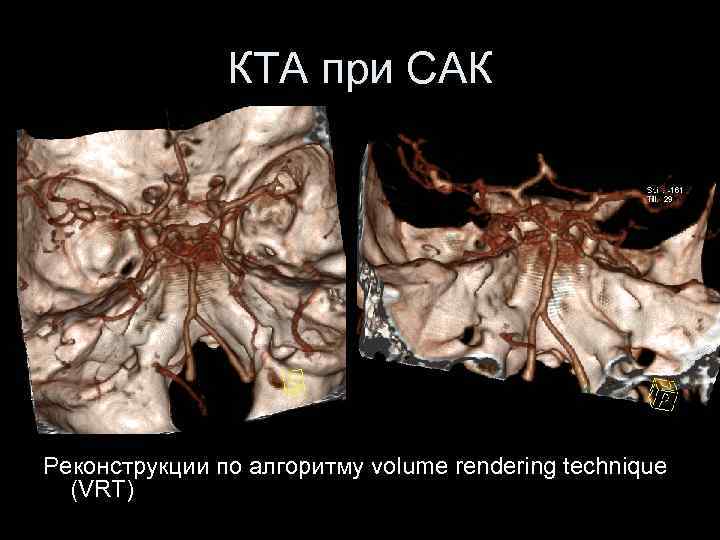
КТА при САК Реконструкции по алгоритму volume rendering technique (VRT)
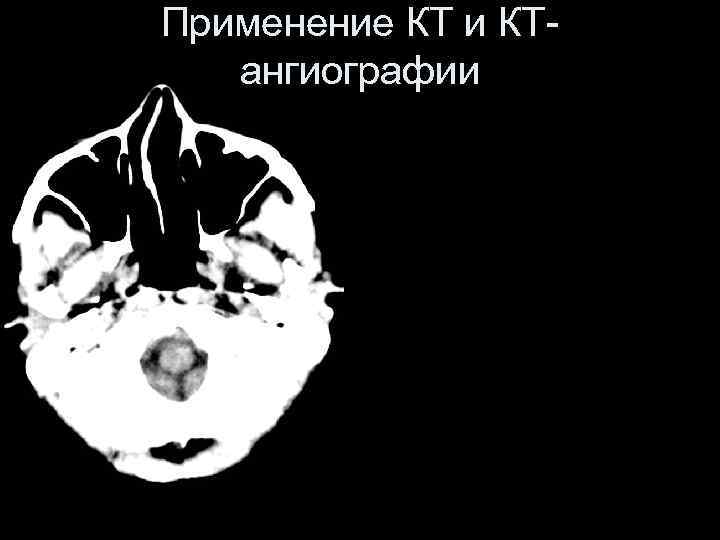
Применение КТ и КТангиографии
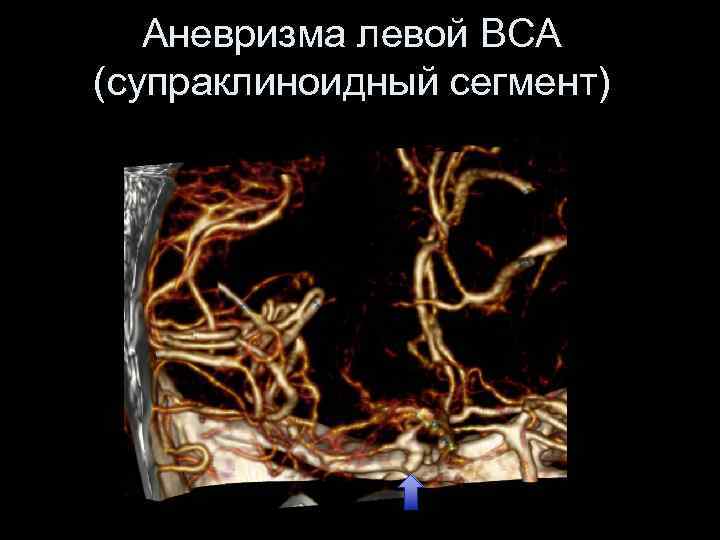
Аневризма левой ВСА (супраклиноидный сегмент)
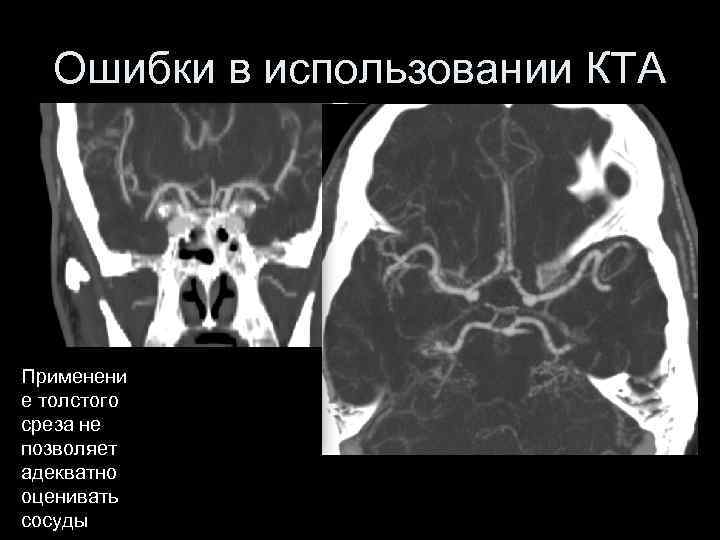
Ошибки в использовании КТА Применени е толстого среза не позволяет адекватно оценивать сосуды

Ошибки в использовании КТА
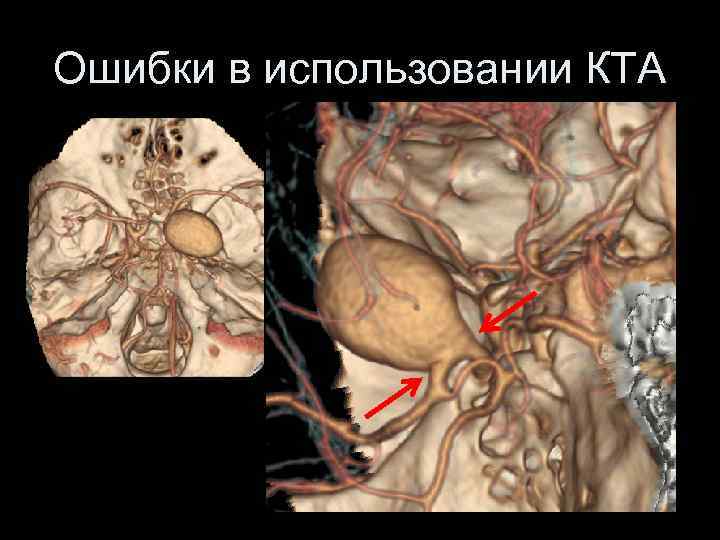
Ошибки в использовании КТА
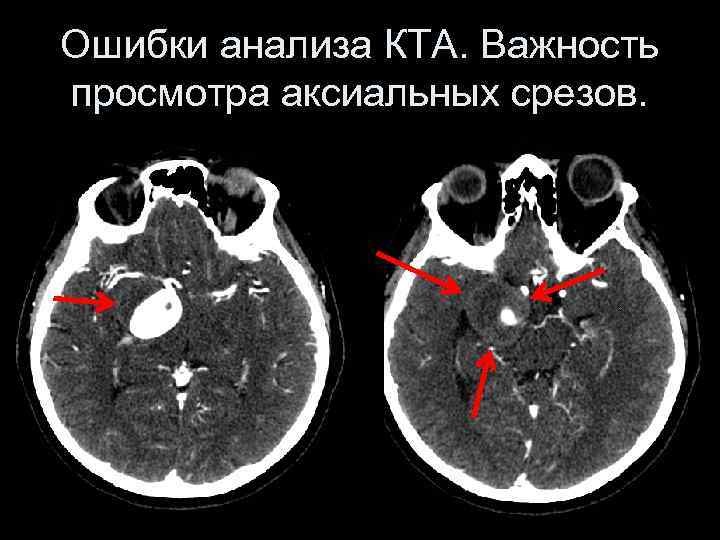
Ошибки анализа КТА. Важность просмотра аксиальных срезов.

Роль КТ при субарахноидальном кровоизлиянии • • Подтвердить САК Установить локализацию и объем (прогноз!) Выявить повторное кровоизлияние Осложнения: – – – Прорыв в желудочки Паренхиматозная гематома Субдуральная гематома Ишемия при вазоспазме Гидроцефалия • Послеоперационный контроль • КТ-ангиография для поиска аневризмы (чувствительность и специфичность более 92 -95%) • Чем тоньше коллимация луча у томографа – тем выше точность КТА!

МРТ при субарахноидальном кровоизлиянии • Неинвазивное выявление сосудистых мальформаций при невозможности провести ангиографию, либо при негативной АГ • Оценка мозговой паренхимы при наличии неврологических выпадений • Выявление и количественная оценка гидроцефалии (фазовый контраст) • Выявление сосудистого спазма и его последствий (МР-ангиография, перфузионная МРТ)

Зависимость сигнала геморрагии на МРТ от времени Т 1 -взвешенное Т 2 -взвешенное -острейшая (внутриклеточный оксигемиоглобин) 0 или + + -собственно острая (внутриклеточный деоксигемиоглобин) 0 - -начало стадии (внутриклеточный метгемиоглобин) + - -конец стадии (внеклеточный метгемиоглобин) + + - + Острая (0 -2 дня) Подострая(3 -14 дней) Хроническая (>14 дней) -начало стадии (внутриклеточные гемохромы) + появление гипоинтенсивного ободка (гемосидерина) -конец стадии
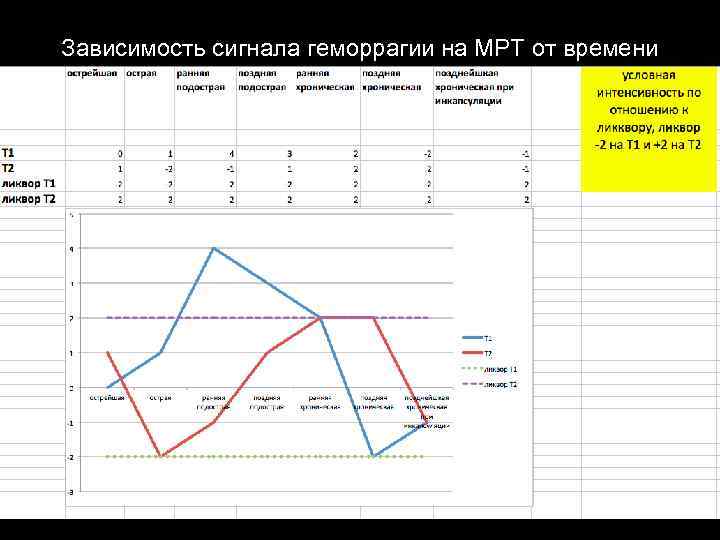
Зависимость сигнала геморрагии на МРТ от времени
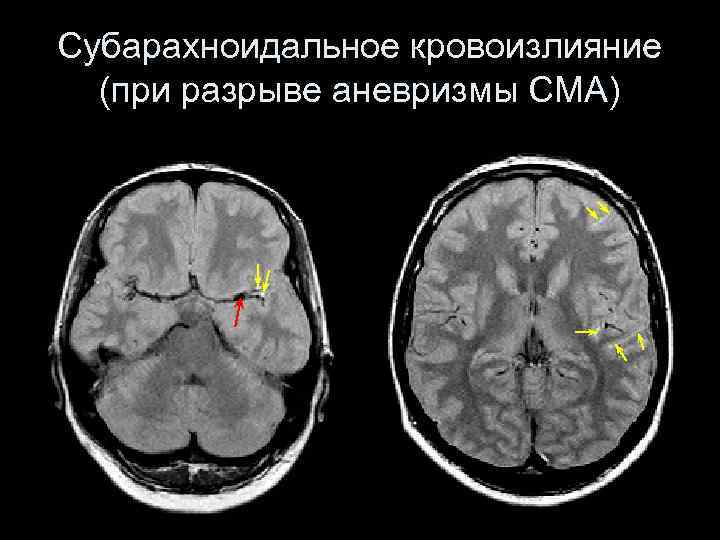
Субарахноидальное кровоизлияние (при разрыве аневризмы СМА)
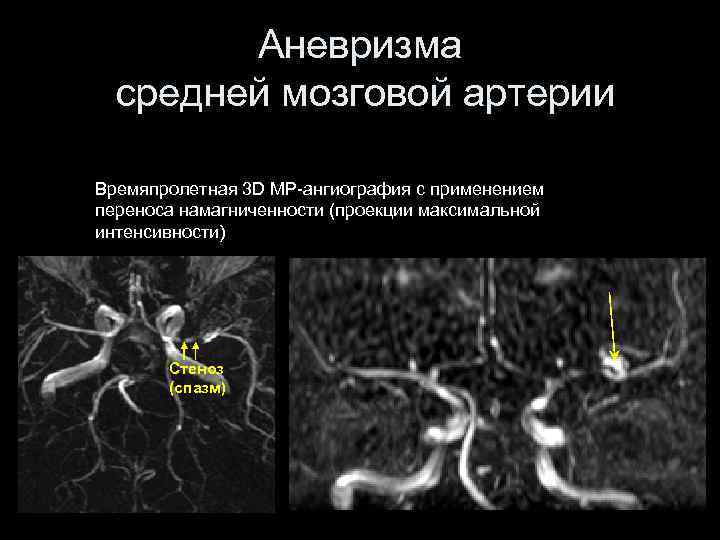
Аневризма средней мозговой артерии Времяпролетная 3 D МР-ангиография с применением переноса намагниченности (проекции максимальной интенсивности) Стеноз (спазм)
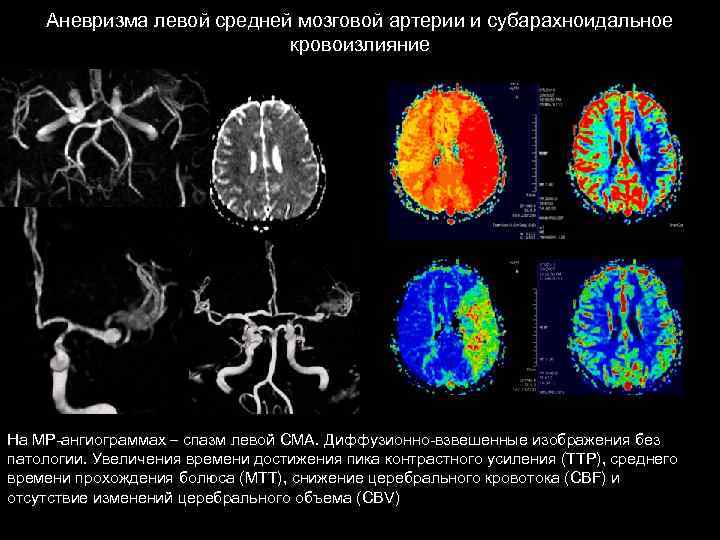
Аневризма левой средней мозговой артерии и субарахноидальное кровоизлияние TTP MTT CBF CBV На МР-ангиограммах – спазм левой СМА. Диффузионно-взвешенные изображения без патологии. Увеличения времени достижения пика контрастного усиления (ТТР), среднего времени прохождения болюса (MTT), снижение церебрального кровотока (CBF) и отсутствие изменений церебрального объема (CBV)

Применение КТ- и МР-перфузии при САК • • КТ и МР перфузия имеют потенциал прогнозирования течения отсроченной церебральной ишемии при спазме и могут способствовать объективному уточнения лечебной тактики Невозможность получения количественных данных, а также влияние множества факторов на качество МР-перфузионных изображений, различия в картах перфузии между разными производителями аппаратных и программных комплексов делают необходимым дождаться проверки достоверности и воспроизводимости методики до начала ее рутинного применения. Большой перехлест в показателях перфузии на КТ у групп пациентов без клиники ишемии и с таковой затрудняют ее использование в качестве основы для изменения тактики ведения пациента. Значительная лучевая нагрузка и потенциальная нефротоксичность контрастных препаратов ограничивают применение методики КТперфузии, особенно для целей контроля.

Перфузионная визуализация - САК • Применение перфузионных методик для корректировки тактики ведения пациентов с отсроченной церебральной ишемией, вызванной ангиоспазмом на фоне субарахноидального кровоизлияния остаётся прерогативой исследовательских центров, так корреляция показателей перфузии при ишемии с клиническими проявлениями неоднозначна, а конкретных рекомендаций по изменению тактики лечения на основе данных перфузионных исследований не данный момент не существует.
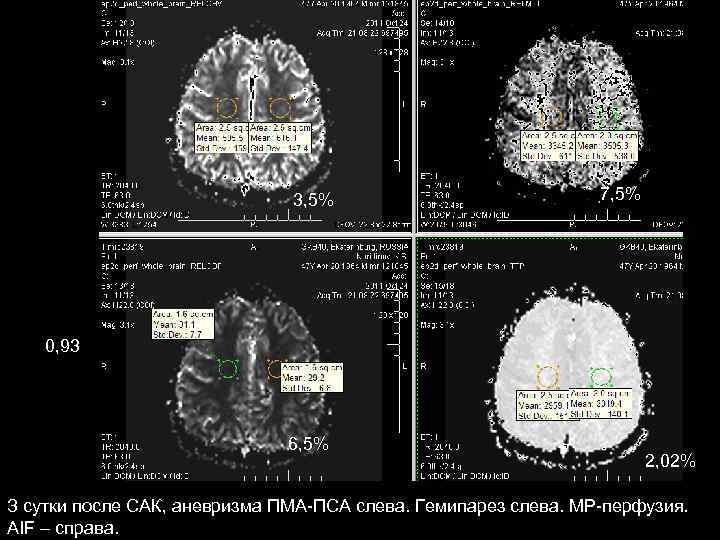
3, 5% 7, 5% 0, 93 6, 5% 2, 02% З сутки после САК, аневризма ПМА-ПСА слева. Гемипарез слева. МР-перфузия. AIF – справа.
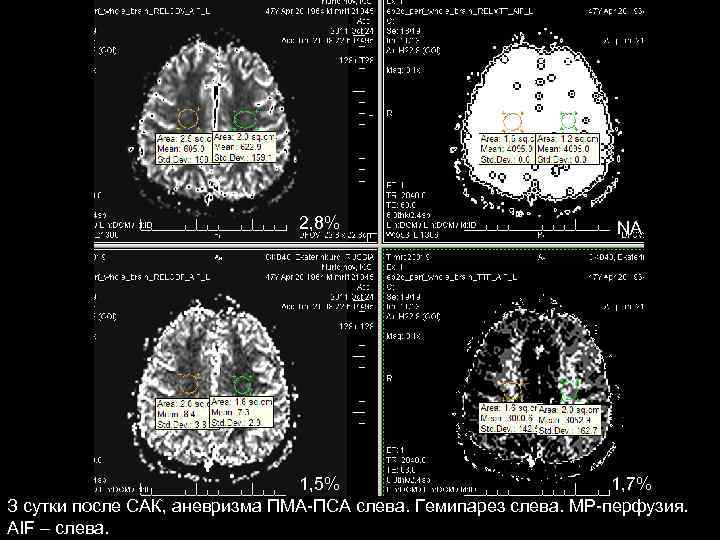
2, 8% NA 1, 5% 1, 7% З сутки после САК, аневризма ПМА-ПСА слева. Гемипарез слева. МР-перфузия. AIF – слева.
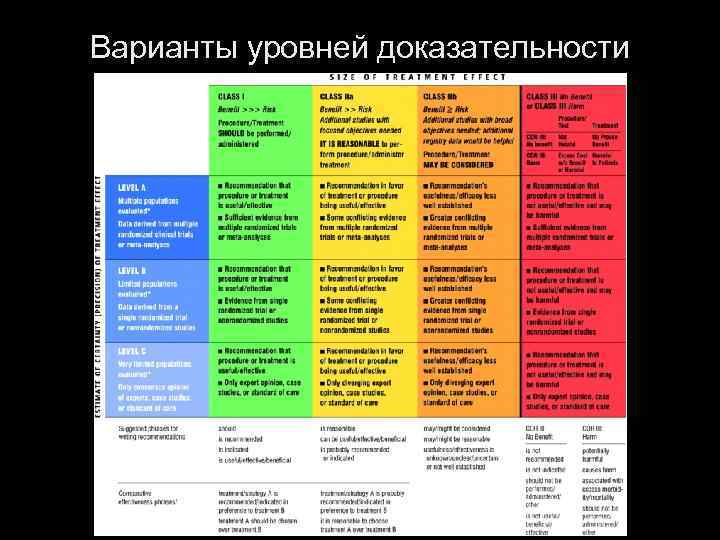
Варианты уровней доказательности

Существующие рекомендации • "Recommendations for Imaging of Acute Ischemic Stroke" - 2009 AHA • Summary • Although widely accepted and used in practice, the diagnostic and clinical utility of perfusion MRI has not been proven in controlled, adequately powered studies. Descriptive case series and studies of the relationship of MRP parameters to other clinical, imaging, and therapeutic variables have shaped the concepts and hypotheses about its potential utility (LOE: B, C). The identification and response to treatment of the ischemic penumbra pattern when defined as a simple diffusion/perfusion mismatch may be the most useful application of perfusion MR, both for patient selection and as an outcome measure in clinical trials. Individual centers have demonstrated that different MRP parameters are generally predictive of tissue fate and clinical outcome; however, despite these different methods already being applied, there has been no determination of which technique is most accurate. Contributing to the lack of consensus is the variability in definitions of what represents ischemic core, penumbra, final infarct size, and clinical outcome on which the measures of accuracy are based. Furthermore, time to reperfusion affects these parameters and is an integral component in the evaluation of all MRP methods, yet it often is not taken into account. To progress toward a consensus on the optimal perfusion MR technique to use in the diagnosis and management of acute ischemic stroke, it is imperative that multicenter, prospective, systematic trials be conducted to fully evaluate this promising tool.

Обновленные рекомендации 2013 • При перстистирующем дефиците: – Перед началом лечения острого ИИ необходима визуализация, в большинстве случаев достаточно НУКТ (Класс 1: УД А) – Перед внутривенным тромболизисом рекомендуется НУКТ или МРТ для исключения геморрагии и оценки ранних КТ признаков ишемии (Класс 1: УД А) – Внутривенный тромболизис при наличии ранних КТ-признаков ишемии рекомендуется (если нет явной гипоплотности), вне зависимости от их распространенности (изменение в сравнении с 2009) (Класс 1: УД А) – Неинвазивная визуализация сосудов строго показана при первичной оценке пациента с инсультом, если предполагается внутриартериальный тромболизис лио механическое разрушение тромба, но это не должно препятствовать своевременному внутривенному тромолизису (Класс 1: УД А) – У кандидата на в/в ТЛ визуализация должна выполняться в течение 45 минут в момента поступления в приемное отделение врачом, специализированным по КТ и МРТ мозга (Класс 1: УД С) – КТ-П и МР-П и DWI с измерением ядра и полутени, могут быть рассмотрены для отбора пациентов для реперфузионной терапии за пределами разрешенных временных промежутков для в/в ТЛ. Эти методики несут информацию для уточнения диагноза, механизма и тяжести инфаркта и способствуют принятию информированного решения (Класс Iiб: УД Б) – Явный участок сниженной плотности на НУКТ может говорить об увеличенном риске кровоизлияния при ТЛ и должен учитываться. Если он занимает более трети бассейна СМА, ТЛ противопоказан (Класс III: УД А)

Существующие рекомендации • "Guidelines for the Management of Aneurysmal Subarachnoid Hemorrhage" - 2009 Absolute values of TCD readings can be misleading, but the Lindegaard ratios (ratio of the velocity in the brain vessel of choice to the velocity in the ipsilateral extracranial internal carotid artery) have been shown to be helpful in following trends. Ratios in the range of 5 to 6 for the supraclinoid internal carotid, anterior cerebral artery, middle cerebral artery, and vertebrobasilar system have been demonstrated to indicate severe spasm and should be treated on the basis of the clinical situation. These trends have been shown to be useful in guiding therapy; however, other modalities such as diffusion perfusion, MRI, and xenon-CT cerebral perfusion studies have been advantageous in guiding management and may be complementary. Whether the use of TCD to treat SAH improves outcome has not been adequately demonstrated. Many centers continue to rely on cerebral angiography for the diagnosis of vasospasm, especially since the development of new interventional radiological treatment(see below). However, the American Academy of Neurology Expert Committee believes that the literature provides Type A, Class II level evidence supporting the use of TCD on the basis of the fact that although sensitivity and specificity are quite variable and depend on the vessel of interest, severe spasm can be identified with fairly high reliability.
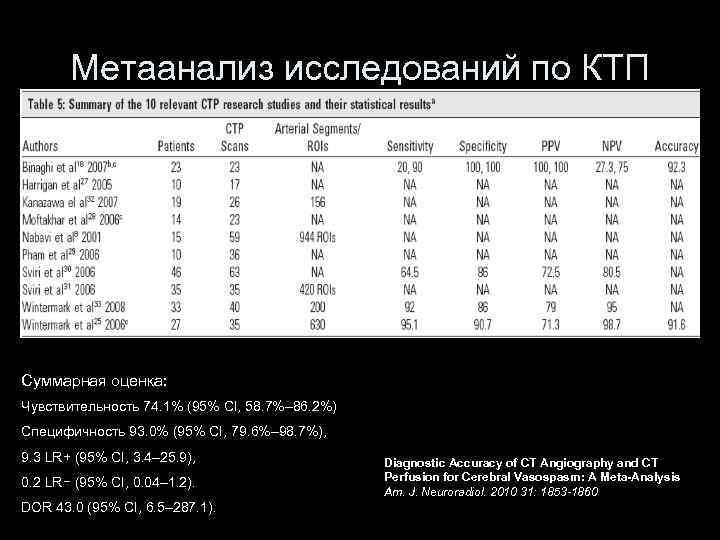
Метаанализ исследований по КТП Суммарная оценка: Чувствительность 74. 1% (95% CI, 58. 7%– 86. 2%) Специфичность 93. 0% (95% CI, 79. 6%– 98. 7%), 9. 3 LR+ (95% CI, 3. 4– 25. 9), 0. 2 LR− (95% CI, 0. 04– 1. 2). DOR 43. 0 (95% CI, 6. 5– 287. 1). Diagnostic Accuracy of CT Angiography and CT Perfusion for Cerebral Vasospasm: A Meta-Analysis Am. J. Neuroradiol. 2010 31: 1853 -1860

Обновленные рекомендации AHA 2012 года • • • Включены 5 новых рекомендаций класса I (уровень Б) После любого лечения аневризмы обычно требуется цереброваскулярная визуализация для обнаружения остаточной полости или рецидива аневризмы, требующих повторного вмешательства. Цифровая субтракционная ангиография с трехмерной ротационной показаны для выявления аневризм у пациентов с САК (кроме тех случаев, когда она уже выявлена неинвазивными методами) и для планирования вмешательства (следует ли провести перкутанную эмболизацию или открытое микрохирургическое вмешательство). В промежутке времени между возникновением САК и лечением аневризмы необходим контроль артериального давления при помощи титруемого препарата, чтобы сбалансировать риск инсульта, кровоизлияния из-за гипертензии и обеспечить церебральную перфузию. При отсутствии убедительных противопоказаний необходима отсроченная визуализация после клипирования или перкутанной эмболизации аневризмы для выявления рецидива или остаточной полости, а при обнаружении значимой (увеличивающейся) полости – всерьез должна быть рассмотрена возможность повторного вмешательства для ее ликвидации. Тромбоцитопения, связанная с гепарином, и тромбоз глубоких вен – нечастые, но и не редкие ситуации у пациентов с САК. Рекомендуется их раннее выявление и специальное лечение, однако идеальный алгоритм их скрининга еще предстоит выработать. Stroke. 2012; 43: 1711 -1737 Published online before print May 3, 2012

Нормативные документы • Приказ Министерства здравоохранения и социального развития Российской Федерации от 6 июля 2009 г. № 389 н «Об утверждении Порядка оказания медицинской помощи больным с острыми нарушениями мозгового кровообращения» • Приказ Минздравсоцразвития России № 357 н от 27 апреля 2011 г. «О внесении изменений в приказ Министерства здравоохранения и социального развития Российской Федерации от 6 июля 2009 г. № 389 н «Об утверждении Порядка оказания медицинской помощи больным с острыми нарушениями мозгового кровообращения»

Визуализация, порядок и результаты • • Больные с признаками ОНМК при поступлении в Отделение в экстренном порядке осматриваются дежурным врачом, который: оценивает жизненно важные функции (при наличии медицинских показаний осуществляет их коррекцию), общее состояние больного и неврологический статус в специально выделенном помещении; организует выполнение электрокардиографии (далее - ЭКГ), забор крови для определения количества тромбоцитов, содержания глюкозы в периферической крови, международного нормализованного отношения (далее - МНО), активированного частичного тромбопластинового времени (далее - АЧТВ). 6. Определение содержания тромбоцитов, глюкозы в периферической крови, МНО, АЧТВ производится в течение 20 минут от момента забора крови, после чего результат передается дежурному врачу Отделения. После осмотра 7. больные с признаками ОНМК направляются в отделение лучевой диагностики (кабинет компьютерной томографии), где осуществляется проведение компьютерной томографии (далее - КТ) или высокопольной магнитно-резонансной томографии (далее - МРТ) головного мозга для уточнения диагноза. … 8. Время от момента поступления больного с признаками ОНМК в Отделение до получения врачом Отделения результатов КТ или МРТ головного мозга и исследования крови составляет минут. • • не более 40 9. При подтверждении диагноза ОНМК больные госпитализируются в блок интенсивной терапии и реанимации Отделения (далее - БИТР). 10. Больным, у которых по данным КТ установлены признаки геморрагического инсульта, проводится консультация нейрохирурга, после чего принимается решение о тактике лечения.

Заключение • Основным методом неотложной нейровизуализации инсульта является КТ • Стандартные КТ без контрастирования позволяют решить вопрос о целесообразности тромболизиса, при условии опытности лучевого диагноста • Современные методики КТ теоретически могут позволить «расширить» либо «сузить» терапевтическое окно • МРТ пока является вспомогательным методом, но имеет потенциал заменить КТ, особенно это касается DWI. • МРТ более эффективна в дифференциальной диагностике инсульта и заболеваний с инсультоподобной клиникой. • Стандартная ангиография, оставаясь золотым стандартом в диагностике стенозов, аневризм, диссекций сейчас применяется чаще с терапевтической целью, как первый этап интервенционного лечения

Приложение • Критерии Уместности Американской Коллегии Радиологии • ACR® Appropriateness Criteria • Цереброваскулярное заболевание

Клинические ситуации 1. Бессимптомное. Структурное поражение клинически (сосудистый шум при аускультации) и/или наличие факторов риска 2. ТИА в каротидном или вертебробазилярном бассейнах, начальный скрининг. (ТИА – сообщенный пациентом, либо другим человеком, преходящий эпизод. Острый неврологический дефицит в ходу должен вестись как острый инсульт, и может считаться ТИА только ретроспективно, если дефицит регрессировал без вмешательства) 3. Вновь появившийся фокальный неврологический дефицит, стабильный или с ухудшением. Менее 3 часов 4. Вновь появившийся фокальный неврологический дефицит, стабильный или с ухудшением. 3 -24 часа. 5. Вновь появившийся фокальный неврологический дефицит, стабильный или с ухудшением. Более 24 часов. 6. Риск наличия неразорвавшейся аневризмы. Семейный анамнез интракраниальной аневризмы. 7. Клинически заподозренное острое САК, не подтвержденное. 8. САК, подтвержденное люмбальной пункцией или визуализацией 9. Доказанное САК, отрицательная ангиография, исследование в динамике 10. Клинически подозреваемая внутримозговая гематома, не подтвержденная. 11. Подтвержденная внутримозговая гематома
















Благодарю за внимание
![Последние исследования Let me start with primary prevention. Results from the ARUBA trial[1] were Последние исследования Let me start with primary prevention. Results from the ARUBA trial[1] were](https://present5.com/presentation/1/263111743_401614881.pdf-img/263111743_401614881.pdf-139.jpg)
Последние исследования Let me start with primary prevention. Results from the ARUBA trial[1] were reported. This is a trial in which patients with asymptomatic arteriovenous malformations were randomized into 2 groups. One group received interventional radiology surgery or radiation and the other group of patients was treated medically. This trial was terminated early by the Data and Safety Monitoring Board (DSMB) due to the very high complication rate of surgery or therapy with radiation. The relative risk in favor of medical or conservative therapy was 0. 29, showing a risk increase of 70%. The next trial was NEST 3. [2] This was a laser treatment trial in which patients with National Institutes of Health Stroke Scale (NIHSS) scores of 7 -17 were enrolled. Patients were not supposed to receive tissue plasminogen activator. The study was terminated prematurely by the DSMB for futility. So, this trial for neuroprotective therapy failed. A positive trial was DESTINY II. [3] This trial investigated hemicraniectomy in patients with a malignant infarct of the middle cerebral artery who were older than 60 years of age. DESTINY I had already shown that younger patients have a clear benefit from hemicraniectomy. In this trial, the outcome was modified Rankin Scale (m. RS) scores, 0 -4 vs 5 or 6. The trial was stopped by the DSMB, in this case due to efficacy findings. The primary endpoint indicating a good outcome -- an m. RS score from 0 to 4 -- occurred in 39% of the surgery group compared with 17% of the conservatively treated group. This was highly statistically significant. The number needed to treat is 5 for the benefit of hemicraniectomy over optimal medical treatment, so this treatment should also be offered to patients above the age of 60. The next trial that was reported was ARCH. [4] ARCH randomized patients with transient ischemic attack (TIA) or minor stroke who had significant aortic plaques. Patients were randomized to either warfarin or the combination of aspirin and clopidogrel. This trial was stopped because it turned out that the trial would never reach the power for a definite result. The outcome was that there was a small benefit in favor of aspirin plus clopidogrel vs warfarin, which was not statistically significant. Unfortunately, we still don't know what the best treatment is for patients who have aortic plaques with TIA or minor stroke. The next trial was SPS 3. [5] SPS 3 randomized patients who had lacunar stroke to either aggressive antihypertensive therapy (target systolic blood pressure < 130 mm Hg) or a more conservative therapy (target systolic blood pressure 131 -149 mm Hg). The endpoint was stroke. The trial showed a relative risk reduction of 19% with the more aggressive approach, which just failed statistical significance. Nevertheless, I think that it is very important to treat patients with lacunar stroke aggressively when it comes to long-term blood pressure control. INTERACT 2[6] was a study that randomized 2839 patients within 6 hours of having cerebral bleeding. Half of the patients achieved systolic blood pressure of < 140 mm Hg, which was achieved by IV treatment with antihypertensive drugs. The control group received standard care. The endpoint was death or major disability. There was an odds ratio of 0. 87 in favor of a more aggressive immediate lowering of blood pressure in patients with cerebral bleeds, which just failed significance. The last important trial was STICHII. [7] This trial investigated immediate hematoma evacuation in patients with a cerebral bleed with medical treatment within 12 hours. The trial had 601 patients. The odds ratio in favor of surgical therapy was not statistically significant. An unfavorable outcome was seen in 59% of patients who received medical therapy and 62% of patients who were operated. This clearly shows that surgery has no benefit for these kinds of patients, with one exception: People who had superficial hemorrhages and no intraventricular hemorrhages had a benefit from surgery.
Лучевая диагностика инсульта.pptx