Цепные и сопряженные реакции.ppt
- Количество слайдов: 30
 Цепные реакции. Цепной и тепловой взрывы Лекция 11
Цепные реакции. Цепной и тепловой взрывы Лекция 11
 Особенности цепных реакций • Это реакции, развивающиеся в условиях взаимовлияния элементарных актов, поэтому наблюдаемая скорость не является результатом простого суммирования. • В цепных и сопряженных реакциях, нарушается принцип независимости, являющийся одним из постулатов химической кинетики. • Скорость рассматриваемых реакций характеризуется большой чувствительностью к примесям, которые могут как инициировать и ускорять реакции, так и тормозить их.
Особенности цепных реакций • Это реакции, развивающиеся в условиях взаимовлияния элементарных актов, поэтому наблюдаемая скорость не является результатом простого суммирования. • В цепных и сопряженных реакциях, нарушается принцип независимости, являющийся одним из постулатов химической кинетики. • Скорость рассматриваемых реакций характеризуется большой чувствительностью к примесям, которые могут как инициировать и ускорять реакции, так и тормозить их.
 Определение цепных реакций • Цепные реакции 1– это химические реакции, в которых появление активной частицы вызывает большое число превращений неактивных частиц вследствие регенерации активной частицы в каждом элементарном акте реакции. При этом в ходе реакции активирование одной частицы приводит к тому, что не только данная частица, но последовательно целый ряд других частиц вступает в реакцию, в результате чего кроме продуктов возникают новые активные частицы. • Активными частицами являются атомы, обладающие неспаренными электронами, свободные радикалы, несольватированные ионы, возбужденные молекулы, т. е. частицы с некомпенсированной валентностью.
Определение цепных реакций • Цепные реакции 1– это химические реакции, в которых появление активной частицы вызывает большое число превращений неактивных частиц вследствие регенерации активной частицы в каждом элементарном акте реакции. При этом в ходе реакции активирование одной частицы приводит к тому, что не только данная частица, но последовательно целый ряд других частиц вступает в реакцию, в результате чего кроме продуктов возникают новые активные частицы. • Активными частицами являются атомы, обладающие неспаренными электронами, свободные радикалы, несольватированные ионы, возбужденные молекулы, т. е. частицы с некомпенсированной валентностью.
 Типичные цепные реакции • • • галогенирование, окисление, полимеризация, ядерные процессы. Цепными являются также многие процессы, связанные с пищевой промышленностью, а именно: прогоркание жиров, окисление красящих веществ в процессе созревания красных вин и ряд других. • Начало развитию теории цепных процессов было положено в 1913 г. , когда Боденштейн ввел понятие «цепная реакция» .
Типичные цепные реакции • • • галогенирование, окисление, полимеризация, ядерные процессы. Цепными являются также многие процессы, связанные с пищевой промышленностью, а именно: прогоркание жиров, окисление красящих веществ в процессе созревания красных вин и ряд других. • Начало развитию теории цепных процессов было положено в 1913 г. , когда Боденштейн ввел понятие «цепная реакция» .
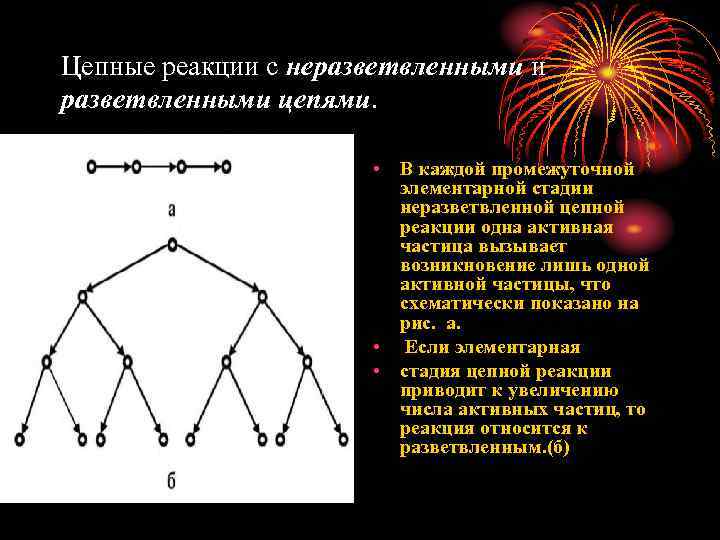 Цепные реакции с неразветвленными и разветвленными цепями. • В каждой промежуточной элементарной стадии неразветвленной цепной реакции одна активная частица вызывает возникновение лишь одной активной частицы, что схематически показано на рис. а. • Если элементарная • стадия цепной реакции приводит к увеличению числа активных частиц, то реакция относится к разветвленным. (б)
Цепные реакции с неразветвленными и разветвленными цепями. • В каждой промежуточной элементарной стадии неразветвленной цепной реакции одна активная частица вызывает возникновение лишь одной активной частицы, что схематически показано на рис. а. • Если элементарная • стадия цепной реакции приводит к увеличению числа активных частиц, то реакция относится к разветвленным. (б)
 Стадии цепных реакций • Любая цепная реакция состоит из трех основных стадий: • зарождения, • продолжения и • обрыва цепи
Стадии цепных реакций • Любая цепная реакция состоит из трех основных стадий: • зарождения, • продолжения и • обрыва цепи
 Причины, вызывающие зарождение цепи • В стадии зарождения (инициирования) цепи образуются активные частицы. • Зарождение цепи может быть вызвано различными причинами: • Распадом молекулы (молекул) на радикалы; • гетерогенными условиями протекания реакции, в частности за счет участия стенок сосуда; • инициированием извне, в том числе под действием света и ионизирующего излучения; • добавками специальных веществ – инициаторов образования свободных радикалов.
Причины, вызывающие зарождение цепи • В стадии зарождения (инициирования) цепи образуются активные частицы. • Зарождение цепи может быть вызвано различными причинами: • Распадом молекулы (молекул) на радикалы; • гетерогенными условиями протекания реакции, в частности за счет участия стенок сосуда; • инициированием извне, в том числе под действием света и ионизирующего излучения; • добавками специальных веществ – инициаторов образования свободных радикалов.

 Стадия продолжения цепи • Данная стадия состоит из большого числа повторяющихся элементарных реакций взаимодействия активных частиц с реагентами. • В результате возникает «цепь» реакций, которая при благоприятных условиях, может достичь многих тысяч звеньев. • Звеном цепи называют повторяющуюся совокупность элементарных стадий (реакций), которые начинаются образованием активной частицы и заканчиваются ее регенерацией. • Звено цепи - это цикл радикальных превращений с сохранением свободной (некомпенсированной) валентности и регенерацией исходной частицы.
Стадия продолжения цепи • Данная стадия состоит из большого числа повторяющихся элементарных реакций взаимодействия активных частиц с реагентами. • В результате возникает «цепь» реакций, которая при благоприятных условиях, может достичь многих тысяч звеньев. • Звеном цепи называют повторяющуюся совокупность элементарных стадий (реакций), которые начинаются образованием активной частицы и заканчиваются ее регенерацией. • Звено цепи - это цикл радикальных превращений с сохранением свободной (некомпенсированной) валентности и регенерацией исходной частицы.
 Обрыв цепи • обрывом цепи ( «гибель» активных частиц) называется стадия, на которой активные валентно-ненасыщенные частицы превращаются в валентно-насыщенные или в частицы, не способные к продолжению цепи. Обрыв цепи происходит путем: • захвата активных частиц стенками реакционных сосудов, • третьими частицами, • а также другими путями, в частности при взаимодействии (рекомбинации) активных частиц.
Обрыв цепи • обрывом цепи ( «гибель» активных частиц) называется стадия, на которой активные валентно-ненасыщенные частицы превращаются в валентно-насыщенные или в частицы, не способные к продолжению цепи. Обрыв цепи происходит путем: • захвата активных частиц стенками реакционных сосудов, • третьими частицами, • а также другими путями, в частности при взаимодействии (рекомбинации) активных частиц.
 • H +H +M→H 2 +M; где M и S обозначают третью частицу или стенку сосуда отличие от неразветвленных цепных реакций, где в процессах продолжения цепи на одну вступающую в реакцию частицу возникает также единственная частица другого сорта, в разветвленных цепях имеет место увеличение числа активных частиц.
• H +H +M→H 2 +M; где M и S обозначают третью частицу или стенку сосуда отличие от неразветвленных цепных реакций, где в процессах продолжения цепи на одну вступающую в реакцию частицу возникает также единственная частица другого сорта, в разветвленных цепях имеет место увеличение числа активных частиц.
 Лавинообразное развитие разветвленной цепной реакции • При частых разветвлениях развитие химической реакции может носить лавинообразный характер. • В этом случае скорость реакции, даже при малом первоначальном числе активных частиц, или первичных цепей, может быстро возрасти и процесс завершится самовоспламенением или взрывом
Лавинообразное развитие разветвленной цепной реакции • При частых разветвлениях развитие химической реакции может носить лавинообразный характер. • В этом случае скорость реакции, даже при малом первоначальном числе активных частиц, или первичных цепей, может быстро возрасти и процесс завершится самовоспламенением или взрывом
 Длина цепи • В результате существования обрыва цепей число звеньев в каждой цепи, называемое длиной цепи, конечно. • в ходе реакции в системе развиваются цепи различной длины – от очень коротких до очень длинных. • Тем не менее при данных условиях реакцию можно охарактеризовать средней длиной цепи L, зависящей от очень многих факторов – температуры, давления, примесей, формы сосуда и состояния его стенок и т. д. • Средняя длины цепи L – это среднее число звеньев цепи, вызываемым одной активной частицей (атомом или радикалом), возникшей первоначально каким-либо независимым путем
Длина цепи • В результате существования обрыва цепей число звеньев в каждой цепи, называемое длиной цепи, конечно. • в ходе реакции в системе развиваются цепи различной длины – от очень коротких до очень длинных. • Тем не менее при данных условиях реакцию можно охарактеризовать средней длиной цепи L, зависящей от очень многих факторов – температуры, давления, примесей, формы сосуда и состояния его стенок и т. д. • Средняя длины цепи L – это среднее число звеньев цепи, вызываемым одной активной частицей (атомом или радикалом), возникшей первоначально каким-либо независимым путем
 Уравнение длины цепи • Пусть число таких независимо возникающих в единицу времени в единице объема частиц равно V 0. , • V 0 - это скорость зарождения цепей. • Скорость цепных реакций зависит от длины цепи, которая, в свою очередь, определяется соотношением скоростей обрыва и продолжения цепи. • Обрыв цепи в одном из ее звеньев характеризуется вероятностью обрыва цепи β– величиной обратной средней длине цепи. • Тогда вероятность продолжения цепи будет равна 1 − β. • Для цепной неразветвленной реакции длина цепи равна • L = (1− β)/β, • т. е. длина цепи равна отношению вероятностей продолжения и обрыва цепи
Уравнение длины цепи • Пусть число таких независимо возникающих в единицу времени в единице объема частиц равно V 0. , • V 0 - это скорость зарождения цепей. • Скорость цепных реакций зависит от длины цепи, которая, в свою очередь, определяется соотношением скоростей обрыва и продолжения цепи. • Обрыв цепи в одном из ее звеньев характеризуется вероятностью обрыва цепи β– величиной обратной средней длине цепи. • Тогда вероятность продолжения цепи будет равна 1 − β. • Для цепной неразветвленной реакции длина цепи равна • L = (1− β)/β, • т. е. длина цепи равна отношению вероятностей продолжения и обрыва цепи
 • Если вероятность обрыва цепи мала (β <<1), то вместо уравнения можно записать: L =1/β. • Следовательно, вероятность обрыва цепи : β =1/L. • Собственно скорость неразветвленной цепной реакции равна произведению скорости зарождения цепи на длину цепи: v = ν 0 L. • Отсюда следует, что на каждый акт зарождения цепи приходится L звеньев цепной реакции. • Скорость неразветвленной цепной реакции определяется течением всех ее трех стадий и зависит от скорости зарождения цепи и длины цепи. Последняя связана с условиями продолжения и обрыва цепи. • Скорость разветвленной цепной реакции определяется увеличением во времени концентрации активных частиц ν , т. е. их числа N в единице объема V. • Она может быть представлена следующим кинетическим уравнением: V = dν/dτ = ν 0 + kэ ׳ ν+ kэ ״ ν • где ν 0 – скорость зарождения цепи; kэ′ и kэ′′ – эффективные константы скорости стадий продолжения и обрыва цепи соответственно; ν – частичная концентра-ция 1 активных частиц. • В СИ единица измерения частичной концентрации ν =N/V – один м− 3 ( частица/м 3 ).
• Если вероятность обрыва цепи мала (β <<1), то вместо уравнения можно записать: L =1/β. • Следовательно, вероятность обрыва цепи : β =1/L. • Собственно скорость неразветвленной цепной реакции равна произведению скорости зарождения цепи на длину цепи: v = ν 0 L. • Отсюда следует, что на каждый акт зарождения цепи приходится L звеньев цепной реакции. • Скорость неразветвленной цепной реакции определяется течением всех ее трех стадий и зависит от скорости зарождения цепи и длины цепи. Последняя связана с условиями продолжения и обрыва цепи. • Скорость разветвленной цепной реакции определяется увеличением во времени концентрации активных частиц ν , т. е. их числа N в единице объема V. • Она может быть представлена следующим кинетическим уравнением: V = dν/dτ = ν 0 + kэ ׳ ν+ kэ ״ ν • где ν 0 – скорость зарождения цепи; kэ′ и kэ′′ – эффективные константы скорости стадий продолжения и обрыва цепи соответственно; ν – частичная концентра-ция 1 активных частиц. • В СИ единица измерения частичной концентрации ν =N/V – один м− 3 ( частица/м 3 ).
 Цепной взрыв • Взрыв – это процесс быстрого выделения энергии, связанного с внезапным изменением состояния вещества, в результате чего в среде образуется ударная или взрывная волна. Возникновение цепного воспламенения или взрыва, • Взрыв есть результат лавинообразного нарастания числа активных частиц (свободных радикалов) при постоянной температуре вследствие протекания разветвленной цепной реакции. • Цепной взрыв следует отличать от теплового взрыва, который возникает при обычной (не цепной) экзотермической реакции, когда выделение теплоты при химической реакции становится больше теплоотдачи.
Цепной взрыв • Взрыв – это процесс быстрого выделения энергии, связанного с внезапным изменением состояния вещества, в результате чего в среде образуется ударная или взрывная волна. Возникновение цепного воспламенения или взрыва, • Взрыв есть результат лавинообразного нарастания числа активных частиц (свободных радикалов) при постоянной температуре вследствие протекания разветвленной цепной реакции. • Цепной взрыв следует отличать от теплового взрыва, который возникает при обычной (не цепной) экзотермической реакции, когда выделение теплоты при химической реакции становится больше теплоотдачи.
 Индукционный период • время, в течение которого скорость реакции возрастает в e раз; • V = A (e- ϕ τ -1) • где A и ϕ– постоянные, характеризующие реакцию и зависящие от ряда условий. • экспериментальное определение продолжительности индукционного периода фактически зависит от чувствительности прибора.
Индукционный период • время, в течение которого скорость реакции возрастает в e раз; • V = A (e- ϕ τ -1) • где A и ϕ– постоянные, характеризующие реакцию и зависящие от ряда условий. • экспериментальное определение продолжительности индукционного периода фактически зависит от чувствительности прибора.
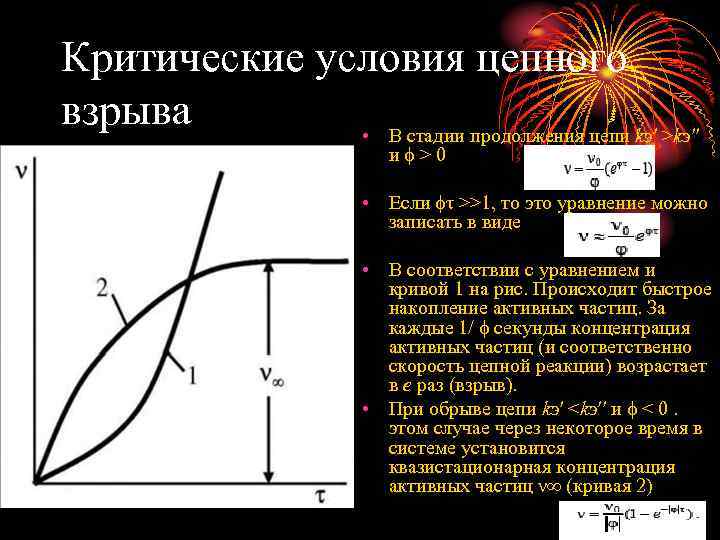 Критические условия цепного взрыва • В стадии продолжения цепи kэ′ >kэ′′ и ϕ > 0 • Если ϕτ >>1, то это уравнение можно записать в виде • В соответствии с уравнением и кривой 1 на рис. Происходит быстрое накопление активных частиц. За каждые 1/ ϕ секунды концентрация активных частиц (и соответственно скорость цепной реакции) возрастает в e раз (взрыв). • При обрыве цепи kэ′
Критические условия цепного взрыва • В стадии продолжения цепи kэ′ >kэ′′ и ϕ > 0 • Если ϕτ >>1, то это уравнение можно записать в виде • В соответствии с уравнением и кривой 1 на рис. Происходит быстрое накопление активных частиц. За каждые 1/ ϕ секунды концентрация активных частиц (и соответственно скорость цепной реакции) возрастает в e раз (взрыв). • При обрыве цепи kэ′
 Термическая активация • • • Повышение реакционной способности путём нагрева реакционной системы называется термической активацией. На молекулярном уровне повышению температуры соответствует увеличение поступательной энергии движения молекул. Столкновения молекул приобретают большую энергию, и в результате доля молекул, способных преодолеть потенциальный барьер, возрастает. Термическая активация включает не только увеличение энергии столкновения молекул, но и возрастание их вращательной и колебательной (а при высоких температурах и электронной) энергии. Протекание некоторых реакций (реакции распада) можно упрощенно представить как увеличение амплитуды колебаний одной из связей, приводящее к её разрыву. При повышении температуры увеличивается скорость тех реакций, протекание которых связано с преодолением потенциального барьера
Термическая активация • • • Повышение реакционной способности путём нагрева реакционной системы называется термической активацией. На молекулярном уровне повышению температуры соответствует увеличение поступательной энергии движения молекул. Столкновения молекул приобретают большую энергию, и в результате доля молекул, способных преодолеть потенциальный барьер, возрастает. Термическая активация включает не только увеличение энергии столкновения молекул, но и возрастание их вращательной и колебательной (а при высоких температурах и электронной) энергии. Протекание некоторых реакций (реакции распада) можно упрощенно представить как увеличение амплитуды колебаний одной из связей, приводящее к её разрыву. При повышении температуры увеличивается скорость тех реакций, протекание которых связано с преодолением потенциального барьера
 Тепловое воспламенение (взрыв) или самовоспламенение • равновесный нагрев смеси до температуры, выше которой смесь самостоятельно, без дальнейшего внешнего нагрева, воспламеняется. • Пусть Q+ - скорость тепловыделения в сосуде • Где -q - тепловой эффект реакции (Дж/моль) • ώ – скорость тепловой реакции (моль/с м 3)
Тепловое воспламенение (взрыв) или самовоспламенение • равновесный нагрев смеси до температуры, выше которой смесь самостоятельно, без дальнейшего внешнего нагрева, воспламеняется. • Пусть Q+ - скорость тепловыделения в сосуде • Где -q - тепловой эффект реакции (Дж/моль) • ώ – скорость тепловой реакции (моль/с м 3)
 Теплопотери в сосуде • Q- - скорость теплопотерь за счет теплообмена газа со стенкой сосуда ά - коэффициент теплоотдачи от газа к стенке, -S - общая площадь стенки сосуда -Пусть некоторый объем газа V заключен в сосуд, стенки которого поддерживаются при постоянной температуре Т 0. - Предположим, что при возникновении химической реакции температура Т горючей смеси внутри сосуда везде растет одинаково. Весь объем горючей смеси реагирует одинаково во всех точках, т. к. концентрация реагирующих веществ в любой точке сосуда одна и та же.
Теплопотери в сосуде • Q- - скорость теплопотерь за счет теплообмена газа со стенкой сосуда ά - коэффициент теплоотдачи от газа к стенке, -S - общая площадь стенки сосуда -Пусть некоторый объем газа V заключен в сосуд, стенки которого поддерживаются при постоянной температуре Т 0. - Предположим, что при возникновении химической реакции температура Т горючей смеси внутри сосуда везде растет одинаково. Весь объем горючей смеси реагирует одинаково во всех точках, т. к. концентрация реагирующих веществ в любой точке сосуда одна и та же.
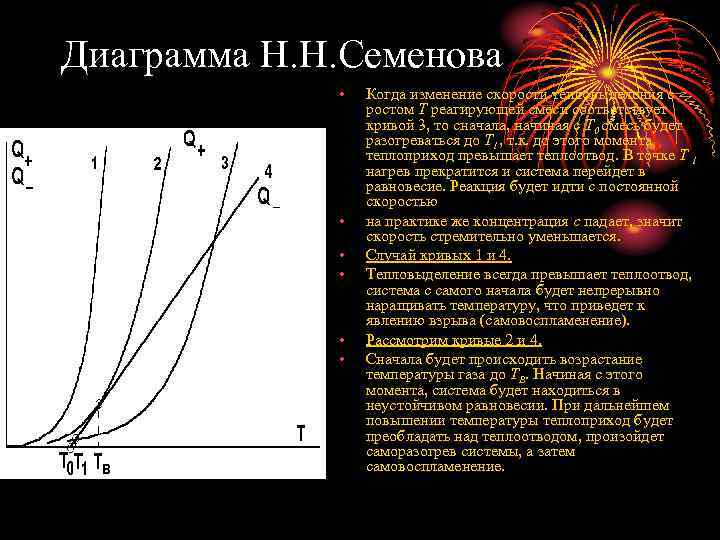 Диаграмма Н. Н. Семенова • • • Когда изменение скорости тепловыделения с ростом Т реагирующей смеси соответствует кривой 3, то сначала, начиная с Т 0 смесь будет разогреваться до Т 1, т. к. до этого момента теплоприход превышает теплоотвод. В точке Т 1 нагрев прекратится и система перейдет в равновесие. Реакция будет идти с постоянной скоростью на практике же концентрация с падает, значит скорость стремительно уменьшается. Случай кривых 1 и 4. Тепловыделение всегда превышает теплоотвод, система с самого начала будет непрерывно наращивать температуру, что приведет к явлению взрыва (самовоспламенение). Рассмотрим кривые 2 и 4. Сначала будет происходить возрастание температуры газа до ТВ. Начиная с этого момента, система будет находиться в неустойчивом равновесии. При дальнейшем повышении температуры теплоприход будет преобладать над теплоотводом, произойдет саморазогрев системы, а затем самовоспламенение.
Диаграмма Н. Н. Семенова • • • Когда изменение скорости тепловыделения с ростом Т реагирующей смеси соответствует кривой 3, то сначала, начиная с Т 0 смесь будет разогреваться до Т 1, т. к. до этого момента теплоприход превышает теплоотвод. В точке Т 1 нагрев прекратится и система перейдет в равновесие. Реакция будет идти с постоянной скоростью на практике же концентрация с падает, значит скорость стремительно уменьшается. Случай кривых 1 и 4. Тепловыделение всегда превышает теплоотвод, система с самого начала будет непрерывно наращивать температуру, что приведет к явлению взрыва (самовоспламенение). Рассмотрим кривые 2 и 4. Сначала будет происходить возрастание температуры газа до ТВ. Начиная с этого момента, система будет находиться в неустойчивом равновесии. При дальнейшем повышении температуры теплоприход будет преобладать над теплоотводом, произойдет саморазогрев системы, а затем самовоспламенение.
 Температура самовоспламенения • В точке ТВ наблюдается равенство скоростей изменение тепловыделения и теплоотвода : При постоянном повышении температуры стенки ТS соответствующая прямая теплоотдачи перемещается вправо параллельно самой себе при a=const. До тех пор пока прямая Q- пересекает Q+ разогрев системы стационарен Выше температуры TS теплоприход превышает теплоотвод: система прогрессивно разогревается, реагирует, происходит воспламенение. TS является нижней границей температуры самовоспламенения.
Температура самовоспламенения • В точке ТВ наблюдается равенство скоростей изменение тепловыделения и теплоотвода : При постоянном повышении температуры стенки ТS соответствующая прямая теплоотдачи перемещается вправо параллельно самой себе при a=const. До тех пор пока прямая Q- пересекает Q+ разогрев системы стационарен Выше температуры TS теплоприход превышает теплоотвод: система прогрессивно разогревается, реагирует, происходит воспламенение. TS является нижней границей температуры самовоспламенения.
 Необходимые и достаточные условия теплового самовоспламенения • Необходимые • Скорость тепловой реакции соизмерима с температурой • Химическая реакция экзотермическая • Достаточные • Скорость тепловой реакции соизмерима с температурой • Химическая реакция экзотермическая • Q+ > Q-.
Необходимые и достаточные условия теплового самовоспламенения • Необходимые • Скорость тепловой реакции соизмерима с температурой • Химическая реакция экзотермическая • Достаточные • Скорость тепловой реакции соизмерима с температурой • Химическая реакция экзотермическая • Q+ > Q-.
 Индукционный период самовоспламенения С • • • температурой самовоспламенения TS всегда связана величина ti индукционный период или задержка воспламенения, поскольку переход от. TS к TB всегда связан с некоторым временем развития реакций и накопления тепла Три вида кривых изменения Т смеси от времени и определение времени индукции как времени, соответствующего точке перегиба. Нижняя кривая соответствует случаю стационарного разогрева до Т 1. Пунктирная линия отражает более реальный случай, когда учитывается расход горючего. Верхняя кривая соответствует самовоспламенению
Индукционный период самовоспламенения С • • • температурой самовоспламенения TS всегда связана величина ti индукционный период или задержка воспламенения, поскольку переход от. TS к TB всегда связан с некоторым временем развития реакций и накопления тепла Три вида кривых изменения Т смеси от времени и определение времени индукции как времени, соответствующего точке перегиба. Нижняя кривая соответствует случаю стационарного разогрева до Т 1. Пунктирная линия отражает более реальный случай, когда учитывается расход горючего. Верхняя кривая соответствует самовоспламенению
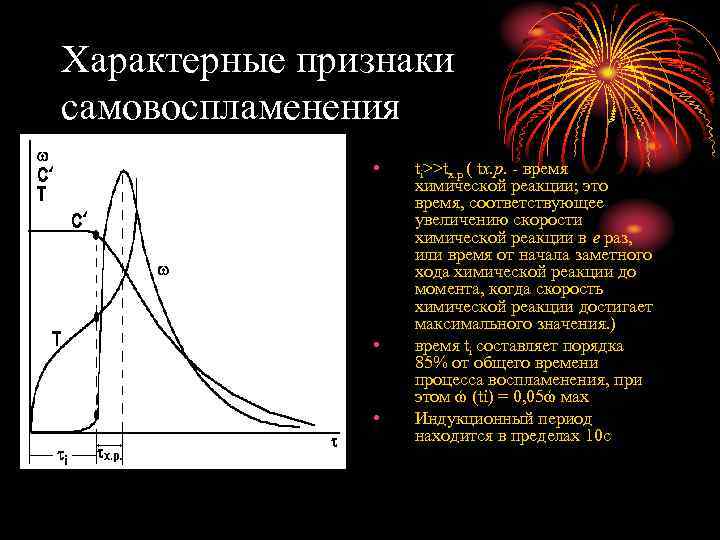 Характерные признаки самовоспламенения • • • ti>>tх. р ( tx. p. - время химической реакции; это время, соответствующее увеличению скорости химической реакции в е раз, или время от начала заметного хода химической реакции до момента, когда скорость химической реакции достигает максимального значения. ) время ti составляет порядка 85% от общего времени процесса воспламенения, при этом ώ (ti) = 0, 05ώ мах Индукционный период находится в пределах 10 с
Характерные признаки самовоспламенения • • • ti>>tх. р ( tx. p. - время химической реакции; это время, соответствующее увеличению скорости химической реакции в е раз, или время от начала заметного хода химической реакции до момента, когда скорость химической реакции достигает максимального значения. ) время ti составляет порядка 85% от общего времени процесса воспламенения, при этом ώ (ti) = 0, 05ώ мах Индукционный период находится в пределах 10 с
 Факторы, определяющие температуру самовоспламенения • химический состав; • физические свойства состава горючей смеси (теплоемкость, теплопроводность); • время индукции ti; • давление в сосуде Р; • материалы стенок сосуда; • начальная температуры стенок TS; • метод определения температуры самовоспламенения
Факторы, определяющие температуру самовоспламенения • химический состав; • физические свойства состава горючей смеси (теплоемкость, теплопроводность); • время индукции ti; • давление в сосуде Р; • материалы стенок сосуда; • начальная температуры стенок TS; • метод определения температуры самовоспламенения
 Экспериментальные методы определения температуры самовоспламенения газовых смесей • метод впуска заранее заготовленной холодной смеси в эвакуированный нагретый сосуд; • метод нагревания компонентов смеси раздельно и затем смешивание в потоке нагретого сосуда (метод концентрических трубок). • метод адиабатического сжатия заранее заготовленной смеси
Экспериментальные методы определения температуры самовоспламенения газовых смесей • метод впуска заранее заготовленной холодной смеси в эвакуированный нагретый сосуд; • метод нагревания компонентов смеси раздельно и затем смешивание в потоке нагретого сосуда (метод концентрических трубок). • метод адиабатического сжатия заранее заготовленной смеси
 Особенности самовоспламенения • • Наличие периода индукции. Наличие критических условий границы самовоспламенения
Особенности самовоспламенения • • Наличие периода индукции. Наличие критических условий границы самовоспламенения
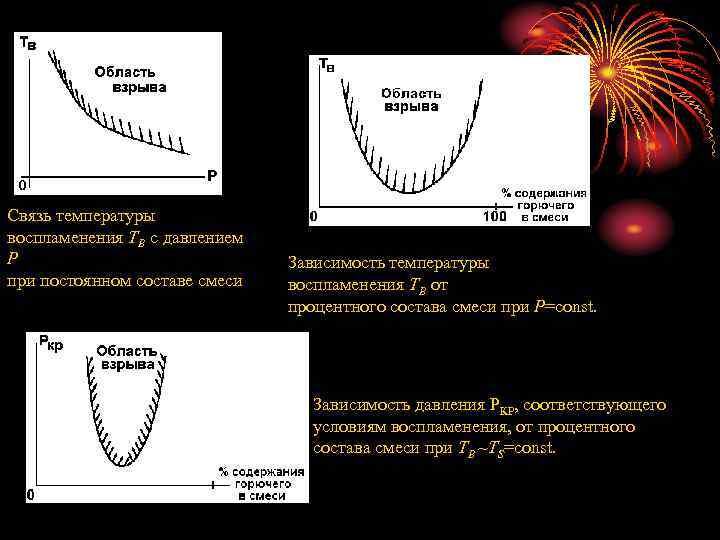 Связь температуры воспламенения ТB с давлением Р при постоянном составе смеси Зависимость температуры воспламенения ТВ от процентного состава смеси при Р=const. Зависимость давления РКР, соответствующего условиям воспламенения, от процентного состава смеси при ТВ ~TS=const.
Связь температуры воспламенения ТB с давлением Р при постоянном составе смеси Зависимость температуры воспламенения ТВ от процентного состава смеси при Р=const. Зависимость давления РКР, соответствующего условиям воспламенения, от процентного состава смеси при ТВ ~TS=const.


