prezentatsiya_po_teme_spirty.ppt
- Количество слайдов: 48

 Цели и задачи : • узнать о представителях класса спиртов, их классификации • изучить изомерию и номенклатуру класса. • Научиться решать тестовые задания по теме.
Цели и задачи : • узнать о представителях класса спиртов, их классификации • изучить изомерию и номенклатуру класса. • Научиться решать тестовые задания по теме.
 Спирты: классификация, изомерия, номенклатура • Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильные группы -ОН. Общая формула спиртов R-(OH)n
Спирты: классификация, изомерия, номенклатура • Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильные группы -ОН. Общая формула спиртов R-(OH)n
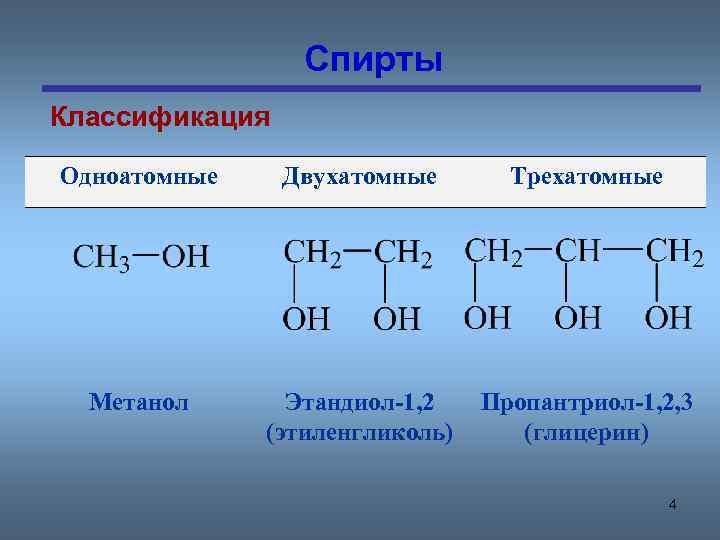 Спирты Классификация Одноатомные Двухатомные Трехатомные Метанол Этандиол-1, 2 (этиленгликоль) Пропантриол-1, 2, 3 (глицерин) 4
Спирты Классификация Одноатомные Двухатомные Трехатомные Метанол Этандиол-1, 2 (этиленгликоль) Пропантриол-1, 2, 3 (глицерин) 4
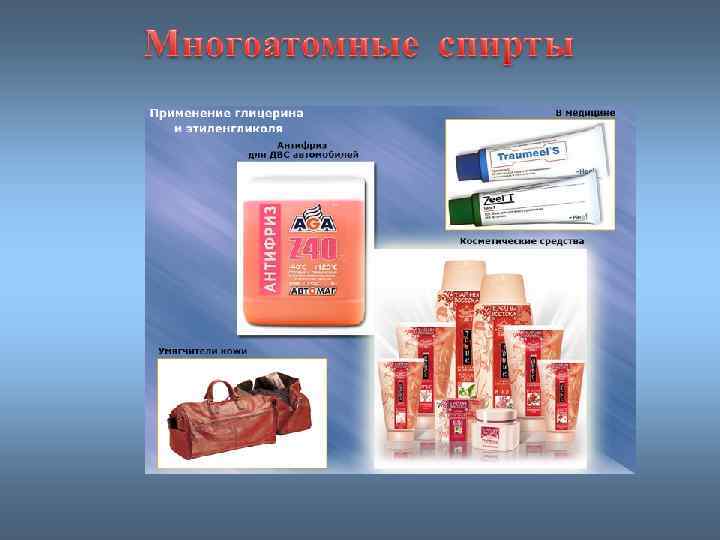
 классификация • По количеству функциональных групп –ОН Одноатомные и многоатомные.
классификация • По количеству функциональных групп –ОН Одноатомные и многоатомные.
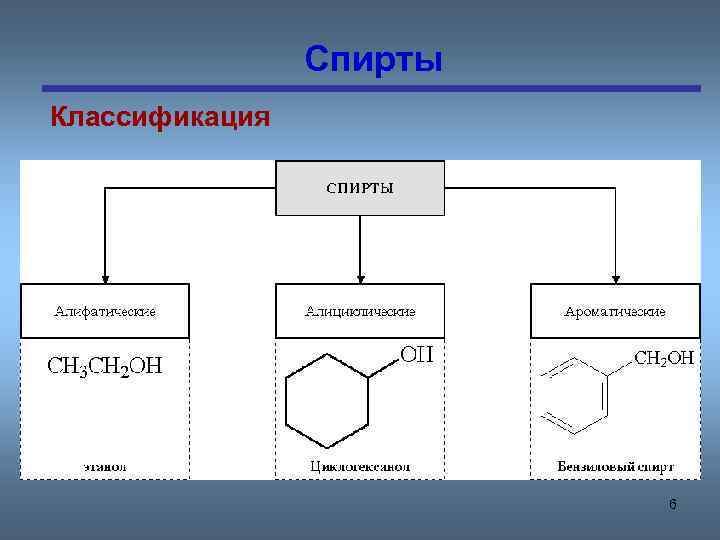 Спирты Классификация 6
Спирты Классификация 6
 Классификация • По характеру углеводородного радикала: спирты предельные Сn. H 2 n+1 OH непредельные ароматические Cn. H 2 n-7 OH Cn. H 2 n-1 OH
Классификация • По характеру углеводородного радикала: спирты предельные Сn. H 2 n+1 OH непредельные ароматические Cn. H 2 n-7 OH Cn. H 2 n-1 OH
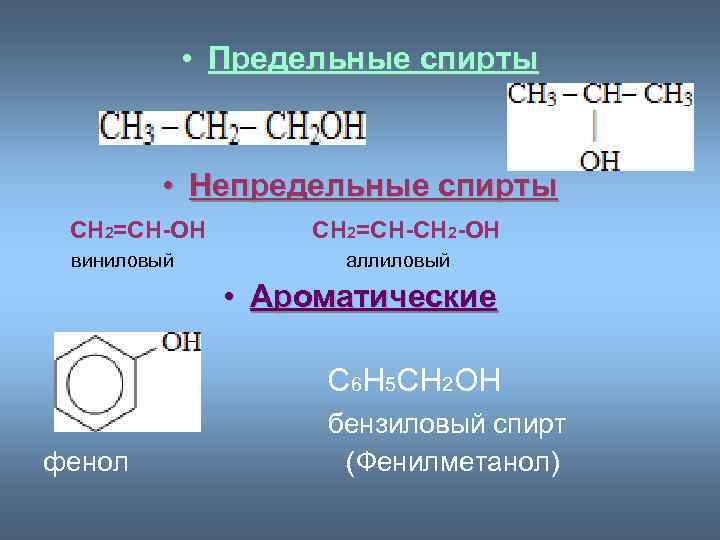 • Предельные спирты • Непредельные спирты СН 2=СН-ОН виниловый СН 2=СН-СН 2 -ОН аллиловый • Ароматические С 6 Н 5 СН 2 ОН фенол бензиловый спирт (Фенилметанол)
• Предельные спирты • Непредельные спирты СН 2=СН-ОН виниловый СН 2=СН-СН 2 -ОН аллиловый • Ароматические С 6 Н 5 СН 2 ОН фенол бензиловый спирт (Фенилметанол)
 • Непредельным одноатомным спиртом является витамин А, важнейшая биологическая функция которого – участие в зрительном процессе. • А вот его формула:
• Непредельным одноатомным спиртом является витамин А, важнейшая биологическая функция которого – участие в зрительном процессе. • А вот его формула:
 Классификация • По типу связывания гидроксильной группы с атомом углерода: спирты первичные вторичные третичные
Классификация • По типу связывания гидроксильной группы с атомом углерода: спирты первичные вторичные третичные
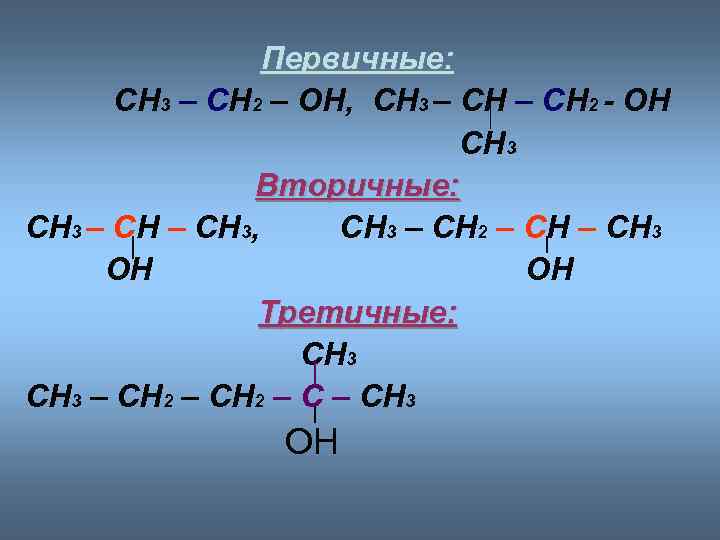 Первичные: СН 3 – СН 2 – ОН, СН 3 – СН 2 - ОН СН 3 Вторичные: СН 3 – СН 3, СН 3 – СН 2 – СН 3 ОН ОН Третичные: СН 3 – СН 2 – СН 3 ОН
Первичные: СН 3 – СН 2 – ОН, СН 3 – СН 2 - ОН СН 3 Вторичные: СН 3 – СН 3, СН 3 – СН 2 – СН 3 ОН ОН Третичные: СН 3 – СН 2 – СН 3 ОН
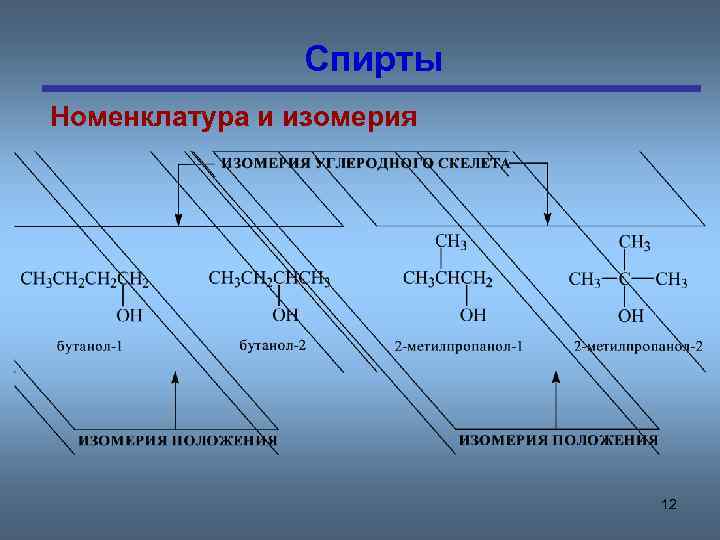 Спирты Номенклатура и изомерия 12
Спирты Номенклатура и изомерия 12
 изомерия • Межклассовая изомерия этанол CH 3 -CH 2 -OH и диметиловый эфир CH 3 – О – CH 3
изомерия • Межклассовая изомерия этанол CH 3 -CH 2 -OH и диметиловый эфир CH 3 – О – CH 3
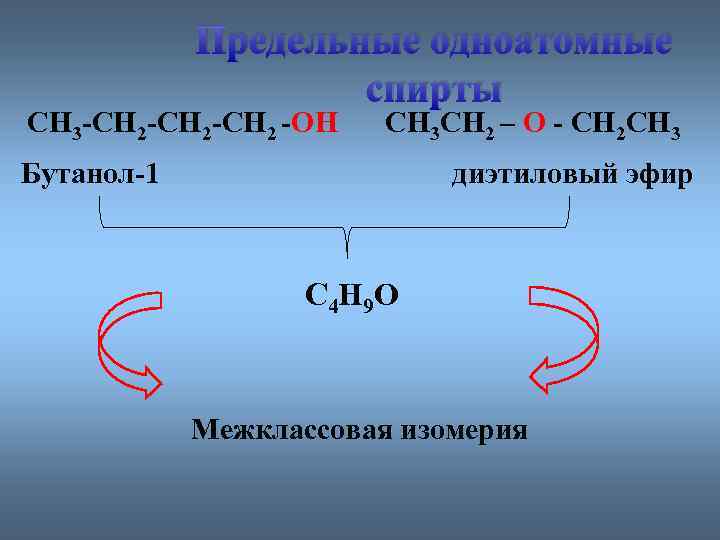 Предельные одноатомные cпирты СН 3 -СН 2 -СН 2 -ОН СН 3 СН 2 – О - СН 2 СН 3 Бутанол-1 диэтиловый эфир С 4 Н 9 О Межклассовая изомерия
Предельные одноатомные cпирты СН 3 -СН 2 -СН 2 -ОН СН 3 СН 2 – О - СН 2 СН 3 Бутанол-1 диэтиловый эфир С 4 Н 9 О Межклассовая изомерия
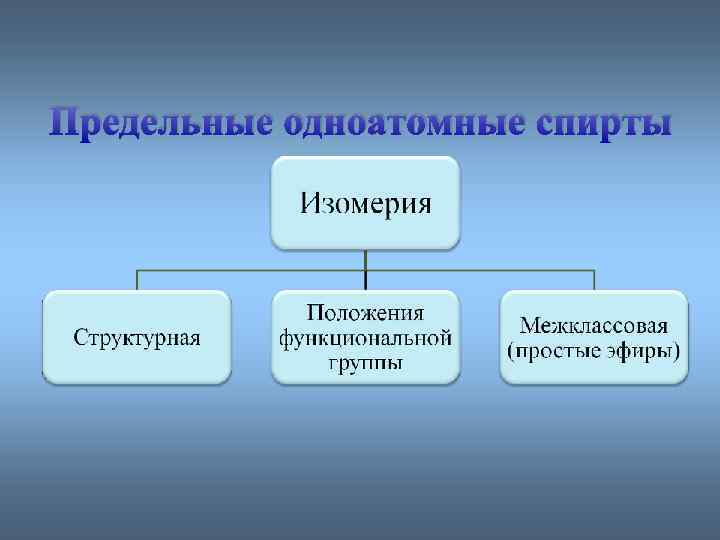 Предельные одноатомные cпирты
Предельные одноатомные cпирты
 • Найдите формулу изомера бутанола-1: • Найдите формулы изомеров и гомологов:
• Найдите формулу изомера бутанола-1: • Найдите формулы изомеров и гомологов:
 номенклатура • Обратите внимание на особенности номенклатуры спиртов: • Самая длинная цепочка атомов углерода номеруется с того конца, к которому ближе гидроксильная группа ОН 6 5 4 I 3 2 1 СНз – СН 2 – СН 3 • Основой названия спирта является название соответствующего углеводорода с добавлением суффикса – ол Метанол, этанол, пропанол, бутанол…
номенклатура • Обратите внимание на особенности номенклатуры спиртов: • Самая длинная цепочка атомов углерода номеруется с того конца, к которому ближе гидроксильная группа ОН 6 5 4 I 3 2 1 СНз – СН 2 – СН 3 • Основой названия спирта является название соответствующего углеводорода с добавлением суффикса – ол Метанол, этанол, пропанол, бутанол…
 • После суффикса ставится цифра, указывающая на положение гидроксильной группы. пропанол – 1, пропанол – 2… • Вместе с тем для названий некоторых спиртов используется и рациональная номенклатура – метиловый спирт, этиловый, амиловый…
• После суффикса ставится цифра, указывающая на положение гидроксильной группы. пропанол – 1, пропанол – 2… • Вместе с тем для названий некоторых спиртов используется и рациональная номенклатура – метиловый спирт, этиловый, амиловый…
 • Формула 3 -метилбутанола-2: 3 -метилбутанола-2 1 3 2 4
• Формула 3 -метилбутанола-2: 3 -метилбутанола-2 1 3 2 4
 Тест. • Даны вещества: 2 -метилбутанол-2, пентанол-2, пропилэтиловый эфир, 2 -метилбутанол-1, 2, 2 -диметилпропанол-1. Найти изомеры пентанола-1 и составить структурные формулы.
Тест. • Даны вещества: 2 -метилбутанол-2, пентанол-2, пропилэтиловый эфир, 2 -метилбутанол-1, 2, 2 -диметилпропанол-1. Найти изомеры пентанола-1 и составить структурные формулы.
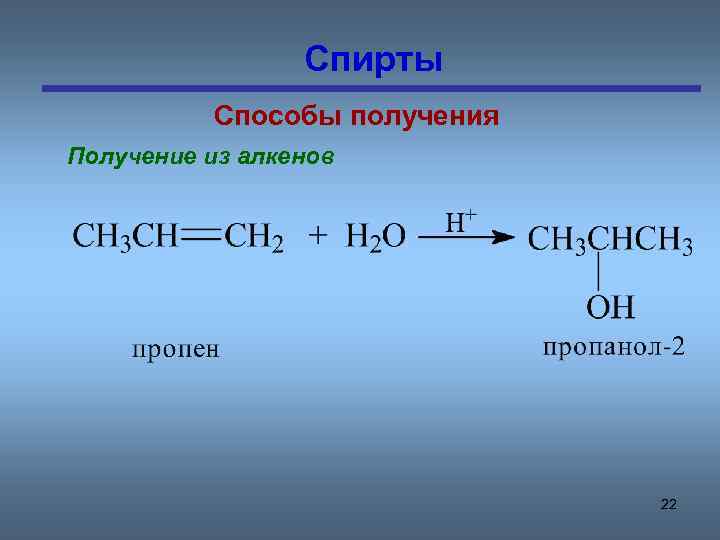 Спирты Способы получения Получение из алкенов 22
Спирты Способы получения Получение из алкенов 22
 Спирты Способы получения Получение из галогенпроизводных 23
Спирты Способы получения Получение из галогенпроизводных 23
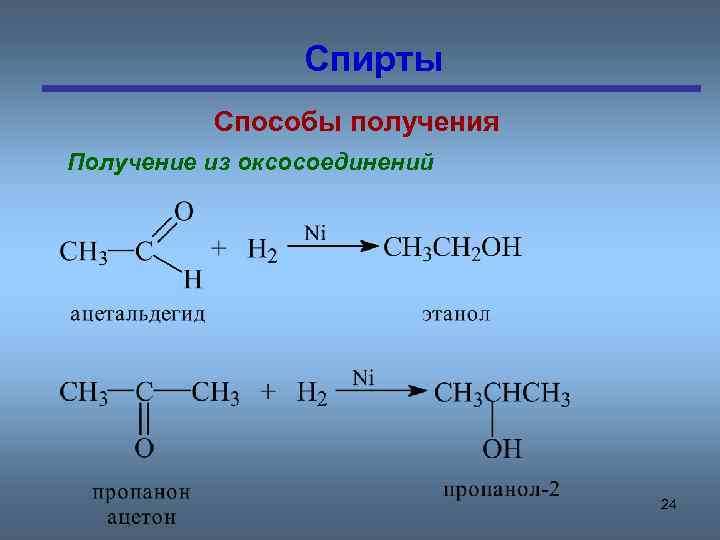 Спирты Способы получения Получение из оксосоединений 24
Спирты Способы получения Получение из оксосоединений 24
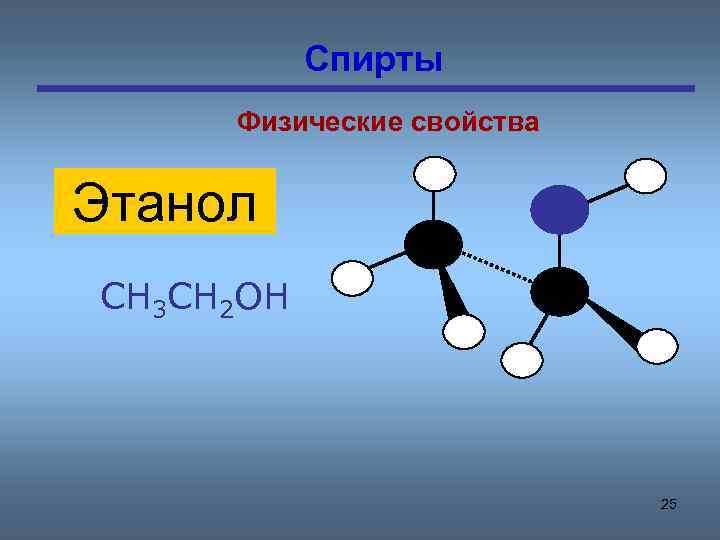 Спирты Физические свойства Этанол CH 3 CH 2 OH 25
Спирты Физические свойства Этанол CH 3 CH 2 OH 25
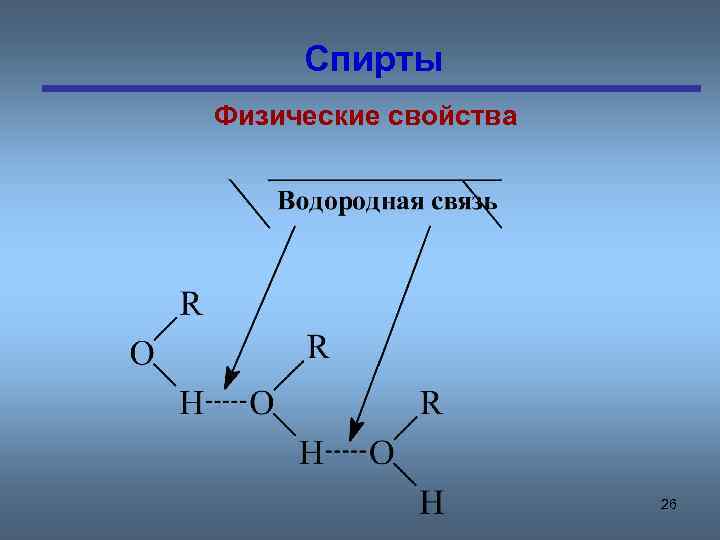 Спирты Физические свойства 26
Спирты Физические свойства 26
 Предельные одноатомные cпирты …О - Н …О - Н …О – Н … R R R Первые члены гомологического ряда спиртов по сравнению с соответствующими алканами являются жидкостями. Это объясняется наличием водородных связей между молекулами спиртов Связь между атомом водорода одной молекулы и атомом сильно электроотрицательных элементов ( кислород) другой молекулы называют водородной
Предельные одноатомные cпирты …О - Н …О - Н …О – Н … R R R Первые члены гомологического ряда спиртов по сравнению с соответствующими алканами являются жидкостями. Это объясняется наличием водородных связей между молекулами спиртов Связь между атомом водорода одной молекулы и атомом сильно электроотрицательных элементов ( кислород) другой молекулы называют водородной
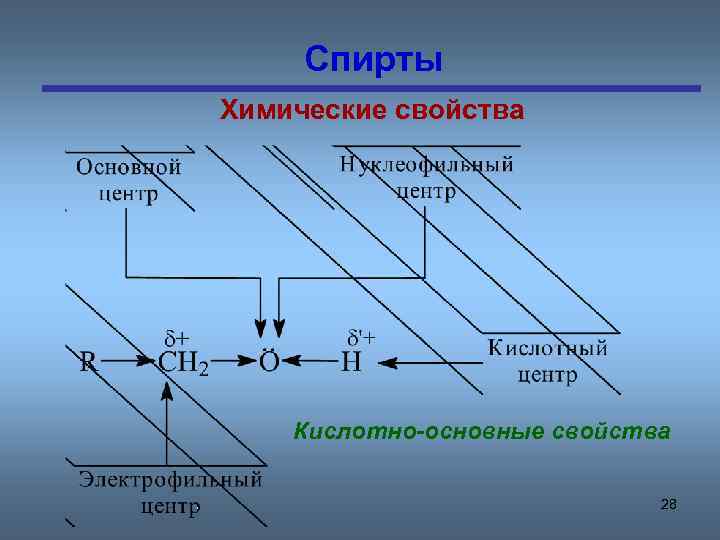 Спирты Химические свойства Кислотно-основные свойства 28
Спирты Химические свойства Кислотно-основные свойства 28
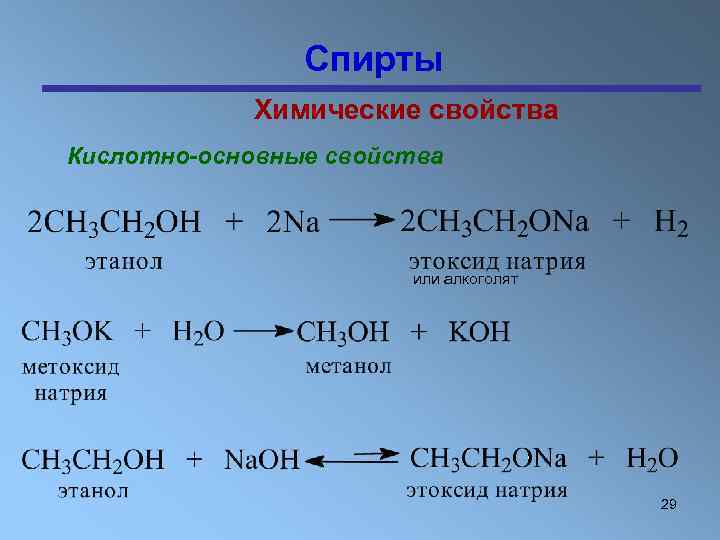 Спирты Химические свойства Кислотно-основные свойства или алкоголят 29
Спирты Химические свойства Кислотно-основные свойства или алкоголят 29
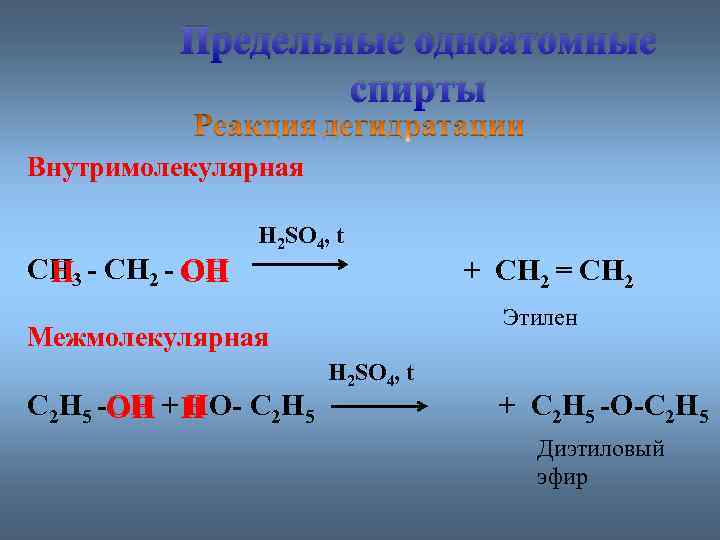 Предельные одноатомные cпирты Внутримолекулярная СН 3 - СН 2 - ОН Н H 2 SO 4, t + СН 2 = СН 2 Этилен Межмолекулярная С 2 Н 5 -ОН + Н С 2 Н 5 ОН НО- H 2 SO 4, t + С 2 Н 5 -О-С 2 Н 5 Диэтиловый эфир
Предельные одноатомные cпирты Внутримолекулярная СН 3 - СН 2 - ОН Н H 2 SO 4, t + СН 2 = СН 2 Этилен Межмолекулярная С 2 Н 5 -ОН + Н С 2 Н 5 ОН НО- H 2 SO 4, t + С 2 Н 5 -О-С 2 Н 5 Диэтиловый эфир
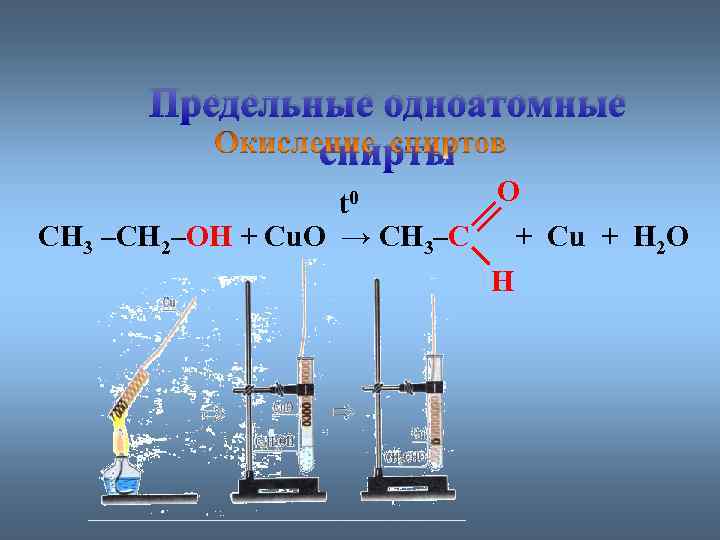 Предельные одноатомные cпирты O t 0 CH 3 –CH 2–OH + Cu. O → CH 3–C + Cu + H 2 O H
Предельные одноатомные cпирты O t 0 CH 3 –CH 2–OH + Cu. O → CH 3–C + Cu + H 2 O H
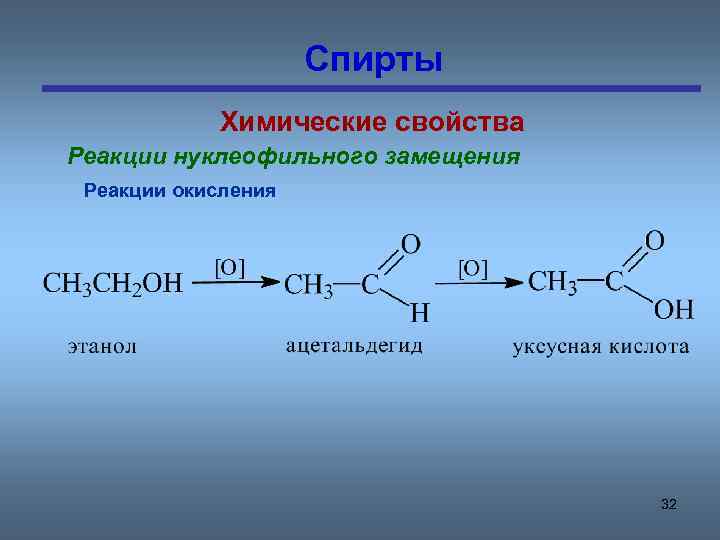 Спирты Химические свойства Реакции нуклеофильного замещения Реакции окисления 32
Спирты Химические свойства Реакции нуклеофильного замещения Реакции окисления 32
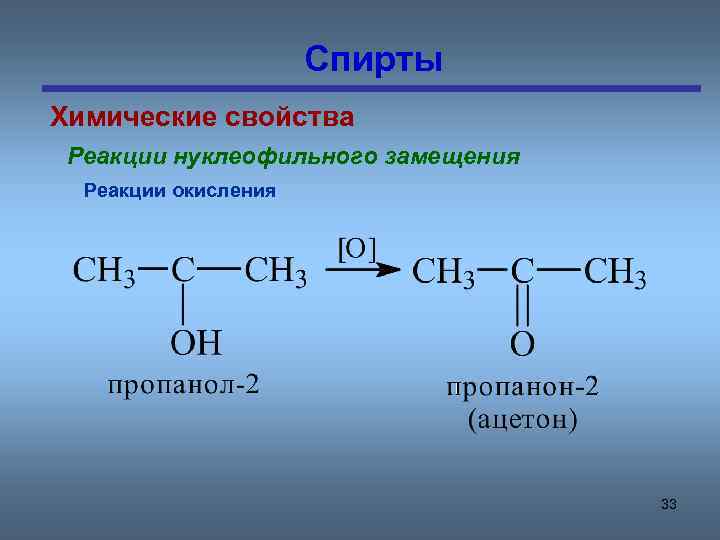 Спирты Химические свойства Реакции нуклеофильного замещения Реакции окисления 33
Спирты Химические свойства Реакции нуклеофильного замещения Реакции окисления 33
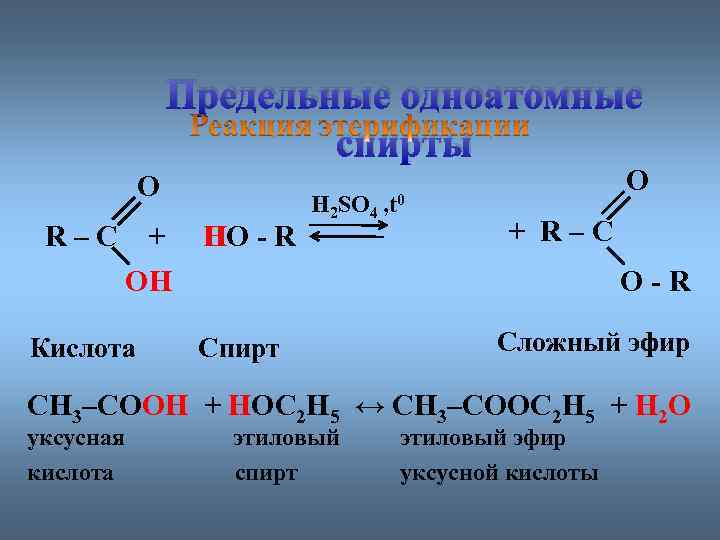 Предельные одноатомные cпирты O R–C + OH ОH Кислота HO - R H H 2 SO 4 , t 0 O + R–C О-R Спирт Сложный эфир CH 3–CОOH + HОC 2 H 5 ↔ CH 3–СООC 2 H 5 + H 2 О уксусная кислота этиловый спирт этиловый эфир уксусной кислоты
Предельные одноатомные cпирты O R–C + OH ОH Кислота HO - R H H 2 SO 4 , t 0 O + R–C О-R Спирт Сложный эфир CH 3–CОOH + HОC 2 H 5 ↔ CH 3–СООC 2 H 5 + H 2 О уксусная кислота этиловый спирт этиловый эфир уксусной кислоты
 Спирты Химические свойства Реакции замещения Взаимодействии спиртов с галогенопроизводными 35
Спирты Химические свойства Реакции замещения Взаимодействии спиртов с галогенопроизводными 35
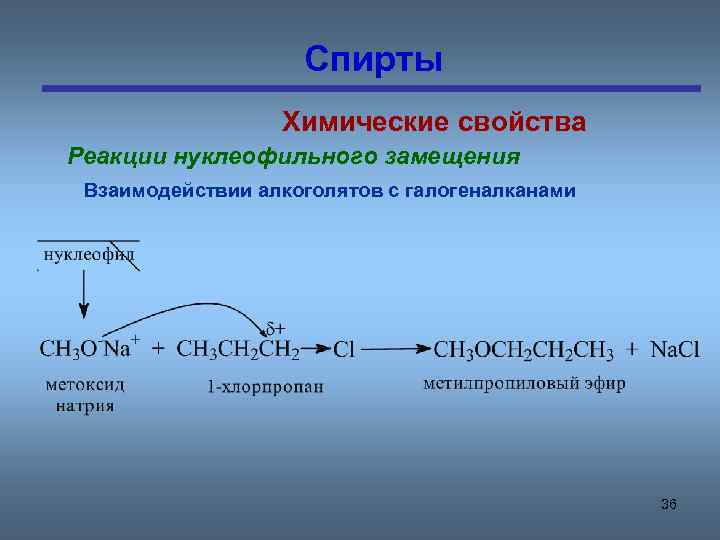 Спирты Химические свойства Реакции нуклеофильного замещения Взаимодействии алкоголятов с галогеналканами 36
Спирты Химические свойства Реакции нуклеофильного замещения Взаимодействии алкоголятов с галогеналканами 36
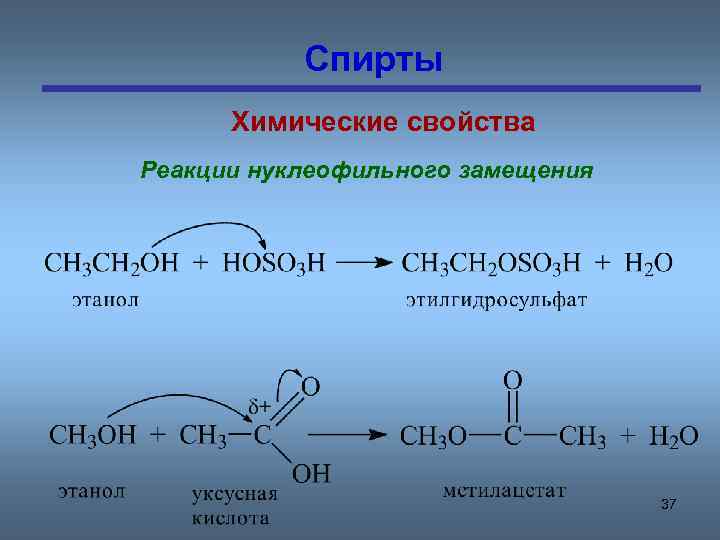 Спирты Химические свойства Реакции нуклеофильного замещения 37
Спирты Химические свойства Реакции нуклеофильного замещения 37
 Предельные одноатомные cпирты
Предельные одноатомные cпирты
 Предельные одноатомные cпирты
Предельные одноатомные cпирты

 Предельные одноатомные cпирты
Предельные одноатомные cпирты
 СН 2 - СН 2 – СН - СН 2 ОН ОН ОН этиленгликоль ОН ОН глицерин Качественная реакция на многоатомность спиртов – взаимодействие со свежеприготовленным голубым осадком гидроксида меди (+2) при обычных условиях Cu(OH)2 глицерин
СН 2 - СН 2 – СН - СН 2 ОН ОН ОН этиленгликоль ОН ОН глицерин Качественная реакция на многоатомность спиртов – взаимодействие со свежеприготовленным голубым осадком гидроксида меди (+2) при обычных условиях Cu(OH)2 глицерин
 1. С ЩЕЛОЧНЫМИ МЕТАЛЛАМИ ГЛИКОЛИ ОБРАЗУЮТ ПОЛНЫЙ И НЕПОЛНЫЙ ГЛИКОЛЯТЫ: CH 2 OH 2 +2 NA CH 2 OH CH 2 ONA 2 CH 2 ONA
1. С ЩЕЛОЧНЫМИ МЕТАЛЛАМИ ГЛИКОЛИ ОБРАЗУЮТ ПОЛНЫЙ И НЕПОЛНЫЙ ГЛИКОЛЯТЫ: CH 2 OH 2 +2 NA CH 2 OH CH 2 ONA 2 CH 2 ONA
 ЭТИЛЕНГЛИКОЛЬ РЕАГИРУЕТ С ЕДКИМИ ЩЕЛОЧАМИ: CH 2 OH CH 2 ONA +2 NAOH = +2 H 2 O CH 2 OH CH 2 ONA
ЭТИЛЕНГЛИКОЛЬ РЕАГИРУЕТ С ЕДКИМИ ЩЕЛОЧАМИ: CH 2 OH CH 2 ONA +2 NAOH = +2 H 2 O CH 2 OH CH 2 ONA
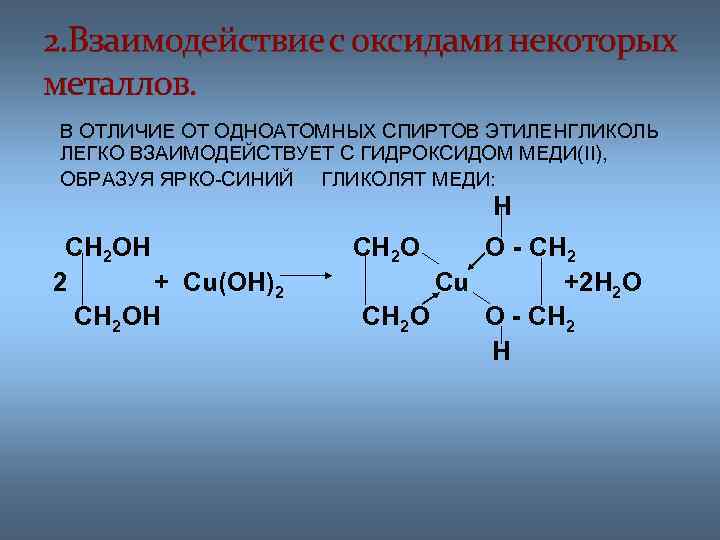 В ОТЛИЧИЕ ОТ ОДНОАТОМНЫХ СПИРТОВ ЭТИЛЕНГЛИКОЛЬ ЛЕГКО ВЗАИМОДЕЙСТВУЕТ С ГИДРОКСИДОМ МЕДИ(II), ОБРАЗУЯ ЯРКО-СИНИЙ ГЛИКОЛЯТ МЕДИ: H CH 2 OH 2 + Cu(OH)2 CH 2 OH CH 2 O O - CH 2 Cu +2 H 2 O CH 2 O O - CH 2 H
В ОТЛИЧИЕ ОТ ОДНОАТОМНЫХ СПИРТОВ ЭТИЛЕНГЛИКОЛЬ ЛЕГКО ВЗАИМОДЕЙСТВУЕТ С ГИДРОКСИДОМ МЕДИ(II), ОБРАЗУЯ ЯРКО-СИНИЙ ГЛИКОЛЯТ МЕДИ: H CH 2 OH 2 + Cu(OH)2 CH 2 OH CH 2 O O - CH 2 Cu +2 H 2 O CH 2 O O - CH 2 H
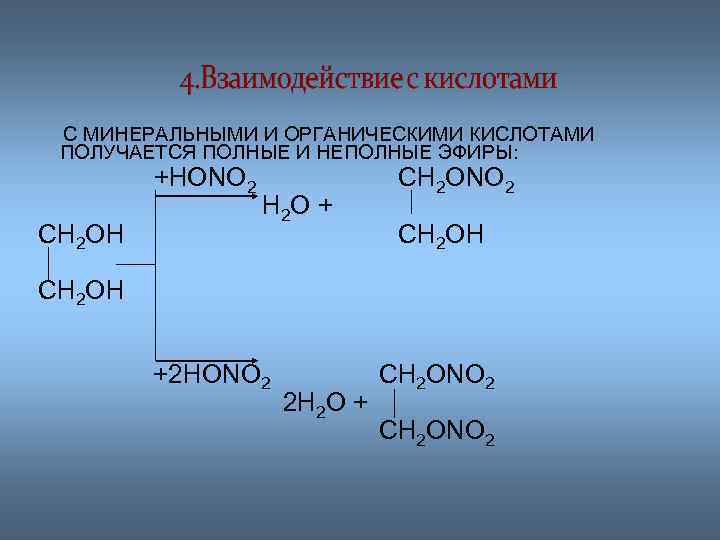 С МИНЕРАЛЬНЫМИ И ОРГАНИЧЕСКИМИ КИСЛОТАМИ ПОЛУЧАЕТСЯ ПОЛНЫЕ И НЕПОЛНЫЕ ЭФИРЫ: +HONO 2 CH 2 OH H 2 O + CH 2 ONO 2 CH 2 OH +2 HONO 2 2 H 2 O + CH 2 ONO 2
С МИНЕРАЛЬНЫМИ И ОРГАНИЧЕСКИМИ КИСЛОТАМИ ПОЛУЧАЕТСЯ ПОЛНЫЕ И НЕПОЛНЫЕ ЭФИРЫ: +HONO 2 CH 2 OH H 2 O + CH 2 ONO 2 CH 2 OH +2 HONO 2 2 H 2 O + CH 2 ONO 2
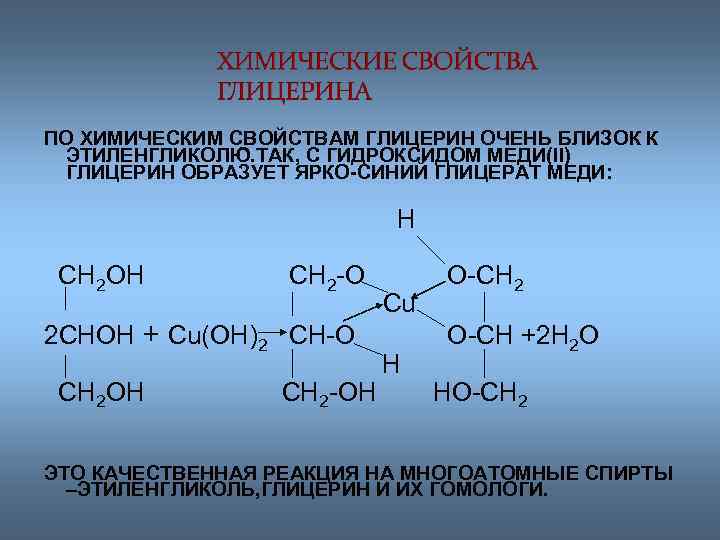 ПО ХИМИЧЕСКИМ СВОЙСТВАМ ГЛИЦЕРИН ОЧЕНЬ БЛИЗОК К ЭТИЛЕНГЛИКОЛЮ. ТАК, С ГИДРОКСИДОМ МЕДИ(II) ГЛИЦЕРИН ОБРАЗУЕТ ЯРКО-СИНИЙ ГЛИЦЕРАТ МЕДИ: H CH 2 OH CH 2 -O 2 CHOH + Cu(OH)2 CH-O CH 2 OH CH 2 -OH Сu H O-CH 2 O-CH +2 H 2 O HO-CH 2 ЭТО КАЧЕСТВЕННАЯ РЕАКЦИЯ НА МНОГОАТОМНЫЕ СПИРТЫ –ЭТИЛЕНГЛИКОЛЬ, ГЛИЦЕРИН И ИХ ГОМОЛОГИ.
ПО ХИМИЧЕСКИМ СВОЙСТВАМ ГЛИЦЕРИН ОЧЕНЬ БЛИЗОК К ЭТИЛЕНГЛИКОЛЮ. ТАК, С ГИДРОКСИДОМ МЕДИ(II) ГЛИЦЕРИН ОБРАЗУЕТ ЯРКО-СИНИЙ ГЛИЦЕРАТ МЕДИ: H CH 2 OH CH 2 -O 2 CHOH + Cu(OH)2 CH-O CH 2 OH CH 2 -OH Сu H O-CH 2 O-CH +2 H 2 O HO-CH 2 ЭТО КАЧЕСТВЕННАЯ РЕАКЦИЯ НА МНОГОАТОМНЫЕ СПИРТЫ –ЭТИЛЕНГЛИКОЛЬ, ГЛИЦЕРИН И ИХ ГОМОЛОГИ.
 При взаимодействии глицерина с неорганическими и органическими кислотами получаются полные и неполные сложные эфиры. CH 2 OH CH 2 ONO 2 H 2 SO 4 2 CHOH + 3 HNO 3 CH 2 OH CHONO 2 +3 H 2 O CH 2 ONO 2 НИТРОГЛИЦЕРИН –ТЯЖЕЛАЯ МАСЛЯНИСТАЯ ЖИДКОСТЬ, ВЗРЫВЧАТОЕ ВЕЩЕСТВО(ВЗРЫВАЕТСЯ ОТ ЛЕГКОГО СОТРЯСЕНИЯ И НАГРЕВАНИЯ).
При взаимодействии глицерина с неорганическими и органическими кислотами получаются полные и неполные сложные эфиры. CH 2 OH CH 2 ONO 2 H 2 SO 4 2 CHOH + 3 HNO 3 CH 2 OH CHONO 2 +3 H 2 O CH 2 ONO 2 НИТРОГЛИЦЕРИН –ТЯЖЕЛАЯ МАСЛЯНИСТАЯ ЖИДКОСТЬ, ВЗРЫВЧАТОЕ ВЕЩЕСТВО(ВЗРЫВАЕТСЯ ОТ ЛЕГКОГО СОТРЯСЕНИЯ И НАГРЕВАНИЯ).