818e16fd8152255bbb8a86db1169191d.ppt
- Количество слайдов: 74

CAT: Anti-tissue transglutaminase: belang bij de diagnose en follow-up van coeliakie Britt Van Meensel Coördinator: Prof. Dr. X. Bossuyt

Indeling Diagnostic scenario: 1. definitie 2. symptomen 3. prevalentie 4. diagnose 5. pathogenese Critical appraisal: A. Diagnose bij patiënten zonder Ig. A deficiëntie B. Follow-up bij patiënten zonder Ig. A deficiëntie C. Diagnose bij Ig. A deficiënte patiënten D. Follow-up bij Ig. A deficiënte patiënten E. Screening van risicogroepen F. Screening van de algemene populatie

Diagnostic scenario

Coeliakie: definitie Coeliakie = glutenovergevoeligheid Een afwijkende dunnedarmmucosa, veroorzaakt door de gliadinefractie van tarwegluten en gelijkaardige alcohol oplosbare eiwitten in rogge, gerst en waarschijnlijk ook haver - therapie: glutenvrij dieet - kan ontstaan op elke leeftijd - genetische factoren: • associatie met bepaalde HLA-genen • eerstegraadsverwanten: 10%

Coeliakie: symptomen Ø KLASSIEKE SYMPTOMEN 4 -24 maanden: diarree, groeivertraging, abdominale distentie APO afwijkend Ø ATYPISCHE SYMPTOMEN anemie, kleine gestalte, vage abdominale klachten, dermatitis herpetiformis, neurologische klachten, infertiliteit, … Ø ASYMPTOMATISCH = SILENT COELIAKIE APO normaal of minimale afwijkingen Ø POTENTIELE COELIAKIE bioptie normaal, antistoffen positief

Coeliakie: symptomen Ø Geassocieerde aandoeningen DM type I, autoimmune thyroiditis/hepatitis, Sjogren, Addison, Down/Turner syndroom, congenitale hartafwijkingen, Ig. A deficiëntie, … Ø Complicaties maligniteiten, osteoporose

Coeliakie: prevalentie Current approaches to diagnosis and treatment of celiac disease: an evolving spectrum. Gastroenterology 2001; 120: 636 -651 Prevalentie in Europa en Noord-Amerika: 1/300
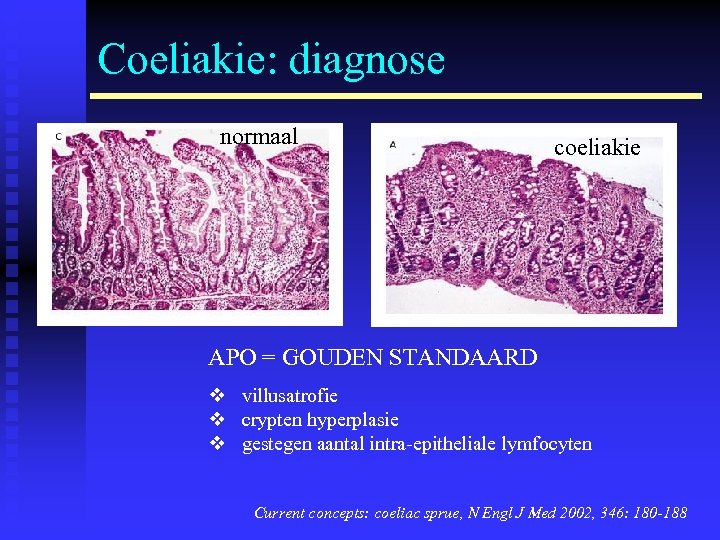
Coeliakie: diagnose normaal coeliakie APO = GOUDEN STANDAARD v villusatrofie v crypten hyperplasie v gestegen aantal intra-epitheliale lymfocyten Current concepts: coeliac sprue, N Engl J Med 2002, 346: 180 -188

Coeliakie: diagnose SEROLOGIE: v Extra hulp bij stellen van de diagnose v Respons op glutenvrij dieet v Therapietrouw v Screenen naar coeliakie v Tijdstip van bioptiename bij gluten challenge
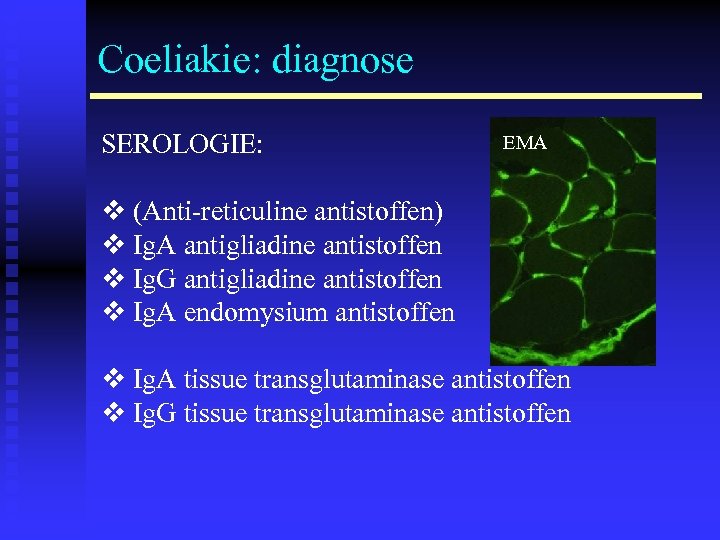
Coeliakie: diagnose SEROLOGIE: EMA v (Anti-reticuline antistoffen) v Ig. A antigliadine antistoffen v Ig. G antigliadine antistoffen v Ig. A endomysium antistoffen v Ig. A tissue transglutaminase antistoffen v Ig. G tissue transglutaminase antistoffen

Coeliakie: diagnose v Gliadine = een ethanol oplosbare fractie van gluten. v Endomysium = een ondersteunende structuur die afzonderlijke spiervezels omringt. Het bevat collageen, reticuline en tissue transglutaminase. v Tissue-transglutaminase: Dieterich et al. toonden in 1997 aan dat tissue-transglutaminase het belangrijkste auto-antigen is dat door EMA herkend wordt.
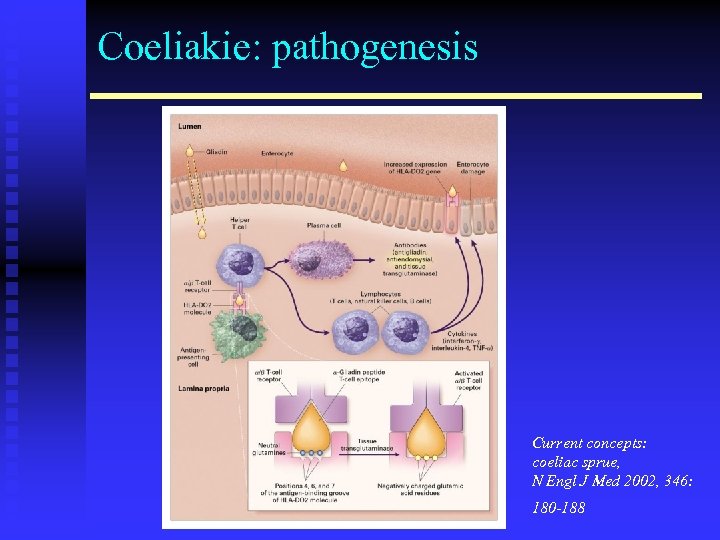
Coeliakie: pathogenesis Current concepts: coeliac sprue, N Engl J Med 2002, 346: 180 -188

Critical appraisal

Evidence-based laboratory medicine: supporting decision -making. Christopher P. Price. Clinical chemistry 46: 8 10411050 (2000) Patient: - diagnose van coeliakie (met/zonder Ig. A deficiëntie) - follow-up van coeliakie (met/zonder Ig. A deficiëntie) Intervention: hu Ig. A/Ig. G tissue transglutaminase (t. TG) Comparison: anti-gliadine AS (AGA), anti-endomysium AS (EMA), bioptie Outcome: is het opsporen van AS tegen t. TG een goede test voor de diagnose/follow-up van coeliakie ?

Critical appraisal: bronnen 1. Literatuurstudie 2. Eigen studie: - 75 diagnostische stalen van onbehandelde coeliakie-patiënten - 70 controlestalen - 32 follow-up stalen Ig. A/Ig. G t. TG kits van 10 firma’s: uitvoering op Ph. D (Biorad)

A. Ig. A t. TG bij de diagnose van coeliakie bij patiënten zonder Ig. A -deficiëntie

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 1. PRE-ANALYTISCHE FACTOREN: - serumstalen - bewaren op 2 -8°C gedurende enkele dagen of op -20°C gedurende een langere periode - vermijd microbieel gecontamineerde stalen, aan hitte blootgestelde stalen of stalen met zichtbare partikels - interferenties door bilirubine, haemoglobine en triglyceriden konden niet worden aangetoond
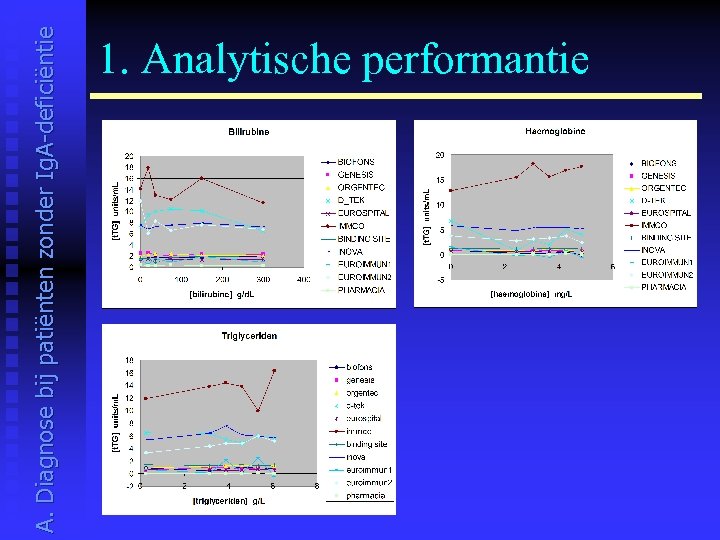
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: a) Meetbereik - absorbanties worden afgelezen - omrekening naar units/m. L (binnen een bepaalde range) - positief vanaf een bepaalde cut-off b) Calibratoren 1 tot 5 (verschillend van firma tot firma) c) Controles bij elke run: positieve en negatieve controle
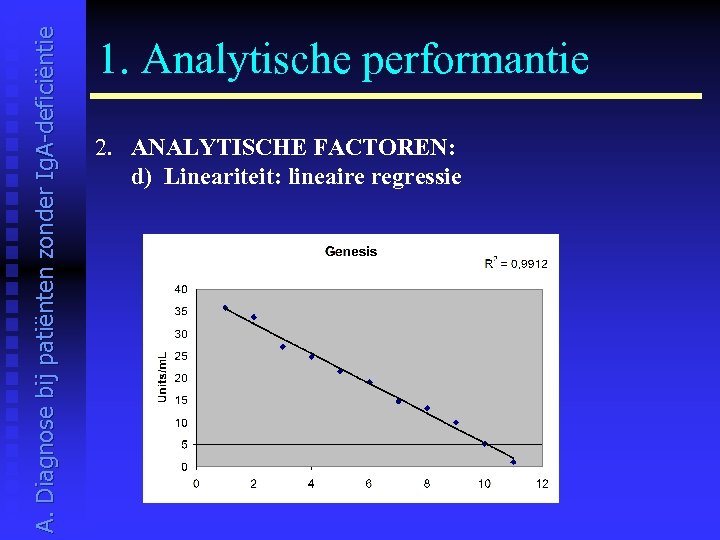
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: d) Lineariteit: lineaire regressie

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: d) Lineariteit goede lineariteit (R²: 0. 844 – 0. 996) B I O F O N S R² G E N E S I S O R G E N T E C 0. 974 0. 991 0. 995 D T E K E U R O S P I T A L I M M C O B I N D I N G S I T E 0. 918 0. 844 0. 976 0. 986 I N O V A E U R O I M M U N 1 E U R O I M M U N 2 P H A R M A C I A 0. 603 0. 996 0. 950 Opm. Bij Inova was er één outlyer aanwezig. Als we dit punt buiten beschouwing laten, bekomen we een resultaat van 0. 9485

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: 3. e) Intra- en inter-run variabiliteit Intra-run variabiliteit: - bijsluiters firma: 1. 3 -10. 4% - eigen studie: 5 -15% G E N E S I S O R G E N T E C D T E K E U R O S P I T A L I M M C O B I N D I N G S I T E I N O V A E U R O I M M U N 1 E U R O I M M U N 2 P H A R M A C I A Waarde staal Gemiddelde B I O F O N S laag CV INTRA 5. 8 4. 6 8. 1 15 5 11. 9 6. 1 6. 4 7. 5 10. 2 8. 8 hoog CV INTRA 15 6. 1 6 21. 1 4. 2 12. 4 5. 9 5. 1 7. 3 6. 4 5. 2 CV (%) = Stdev x 100 _____ Inter-run variabiliteit: - bijsluiters firma: 1. 8 -12%
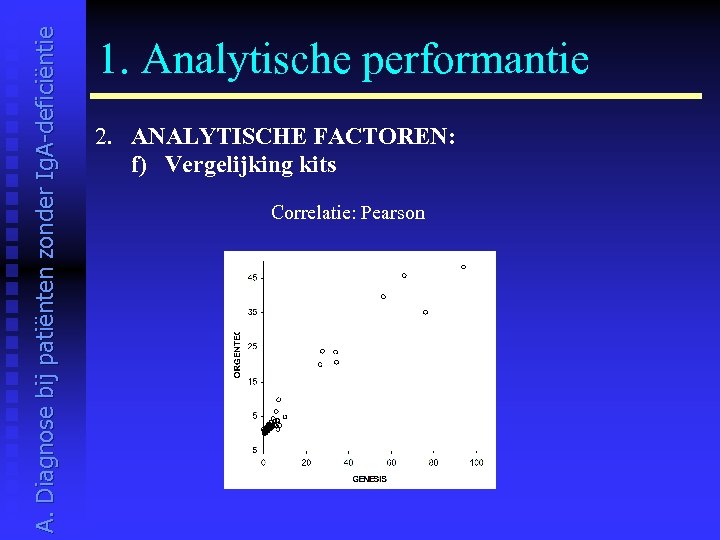
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: f) Vergelijking kits Correlatie: Pearson
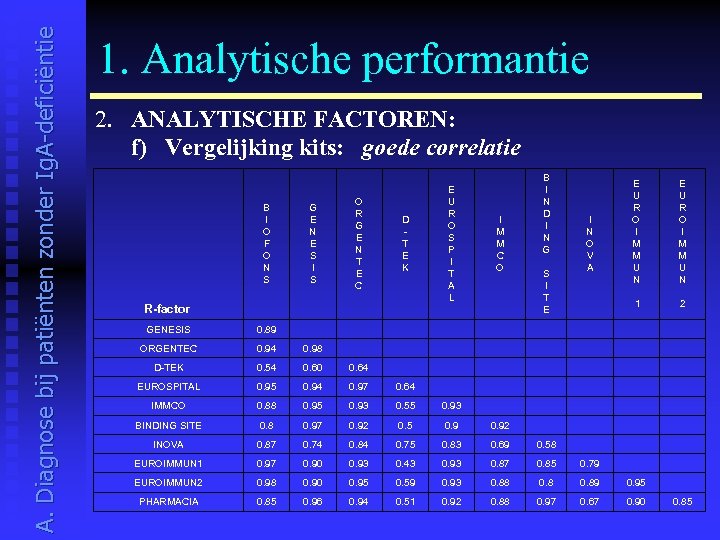
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: f) Vergelijking kits: goede correlatie B I O F O N S G E N E S I S O R G E N T E C D T E K R-factor E U R O S P I T A L I M M C O B I N D I N G S I T E I N O V A E U R O I M M U N 1 E U R O I M M U N 2 GENESIS 0. 89 ORGENTEC 0. 94 0. 98 D-TEK 0. 54 0. 60 0. 64 EUROSPITAL 0. 95 0. 94 0. 97 0. 64 IMMCO 0. 88 0. 95 0. 93 0. 55 0. 93 BINDING SITE 0. 8 0. 97 0. 92 0. 5 0. 92 INOVA 0. 87 0. 74 0. 84 0. 75 0. 83 0. 69 0. 58 EUROIMMUN 1 0. 97 0. 90 0. 93 0. 43 0. 93 0. 87 0. 85 0. 79 EUROIMMUN 2 0. 98 0. 90 0. 95 0. 59 0. 93 0. 88 0. 89 0. 95 PHARMACIA 0. 85 0. 96 0. 94 0. 51 0. 92 0. 88 0. 97 0. 67 0. 90 0. 85
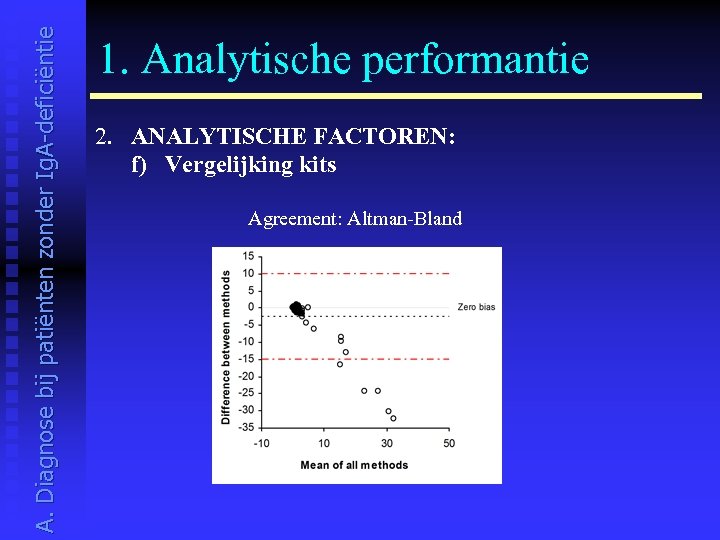
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: f) Vergelijking kits Agreement: Altman-Bland
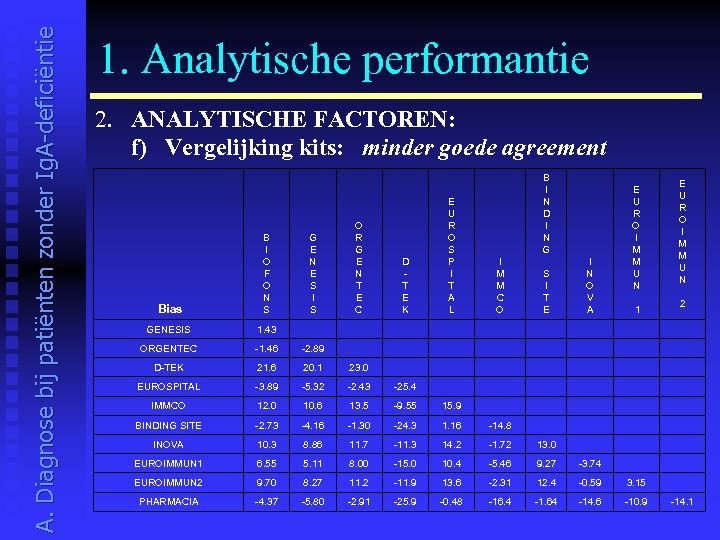
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie 2. ANALYTISCHE FACTOREN: f) Vergelijking kits: minder goede agreement I M M C O B I N D I N G S I T E E U R O I M M U N 2 Bias B I O F O N S G E N E S I S O R G E N T E C D T E K E U R O S P I T A L GENESIS 1. 43 ORGENTEC -1. 46 -2. 89 D-TEK 21. 6 20. 1 23. 0 EUROSPITAL -3. 89 -5. 32 -2. 43 -25. 4 IMMCO 12. 0 10. 6 13. 5 -9. 55 15. 9 BINDING SITE -2. 73 -4. 16 -1. 30 -24. 3 1. 16 -14. 8 INOVA 10. 3 8. 86 11. 7 -11. 3 14. 2 -1. 72 13. 0 EUROIMMUN 1 6. 55 5. 11 8. 00 -15. 0 10. 4 -5. 46 9. 27 -3. 74 EUROIMMUN 2 9. 70 8. 27 11. 2 -11. 9 13. 6 -2. 31 12. 4 -0. 59 3. 15 PHARMACIA -4. 37 -5. 80 -2. 91 -25. 9 -0. 48 -16. 4 -1. 64 -14. 6 -10. 9 -14. 1 I N O V A 1
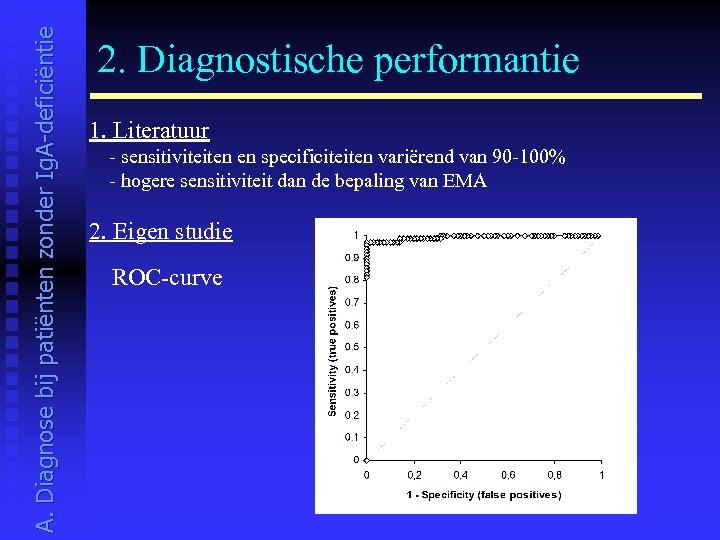
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie 1. Literatuur - sensitiviteiten en specificiteiten variërend van 90 -100% - hogere sensitiviteit dan de bepaling van EMA 2. Eigen studie ROC-curve

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie B I O F O N S AUC G E N E S I S O R G E N T E C 0. 991 0. 993 0. 989 D T E K E U R O S P I T A L 0. 986 0. 993 I M M C O B I N D I N G S I T E 0. 980 AUC: 0. 986 - 0. 997 I N O V A E U R O I M M U N 1 E U R O I M M U N 2 P H A R M A C I A 0. 997 0. 991 0. 993 0. 996

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Diagnostische parameters: - sensitiviteit: SENS = TP/(TP+FN) - specificiteit: SPEC = TN/(TN+FP) - positief predictieve waarde: PPW = TP/(TP+FP) - negatief predictieve waarde: NPW = TN/(TN+FN) - positieve likelihood ratio: +LR = sens/(1 - spec) - negatieve likelihood ratio: -LR = (1 - sens)/spec - number needed to diagnose: NND = 1/(sens - (1 - spec)) = het aantal testen dat we moeten uitvoeren om één correct positief of één correct negatief resultaat te bekomen
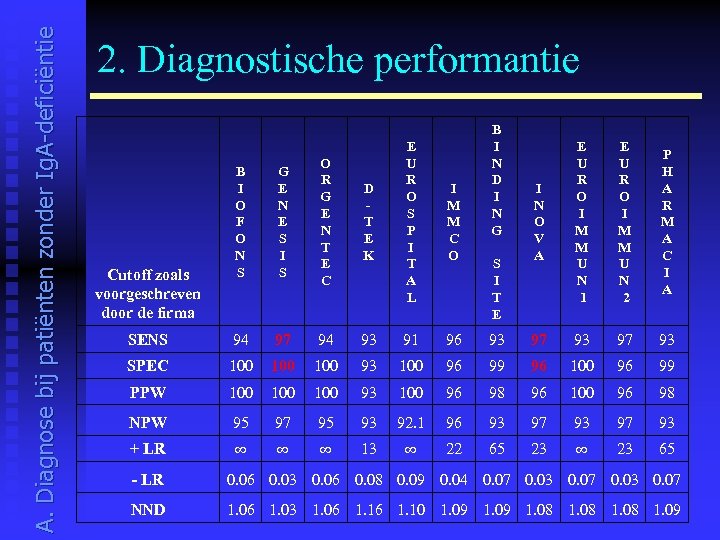
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie D T E K E U R O S P I T A L I M M C O B I N D I N G S I T E I N O V A E U R O I M M U N 1 E U R O I M M U N 2 P H A R M A C I A B I O F O N S G E N E S I S O R G E N T E C SENS 94 97 94 93 91 96 93 97 93 SPEC 100 100 93 100 96 99 96 100 96 99 PPW 100 100 93 100 96 98 96 100 96 98 NPW 95 97 95 93 92. 1 96 93 97 93 + LR ∞ ∞ ∞ 13 ∞ 22 65 23 ∞ 23 65 Cutoff zoals voorgeschreven door de firma - LR 0. 06 0. 03 0. 06 0. 08 0. 09 0. 04 0. 07 0. 03 0. 07 NND 1. 06 1. 03 1. 06 1. 10 1. 09 1. 08 1. 09
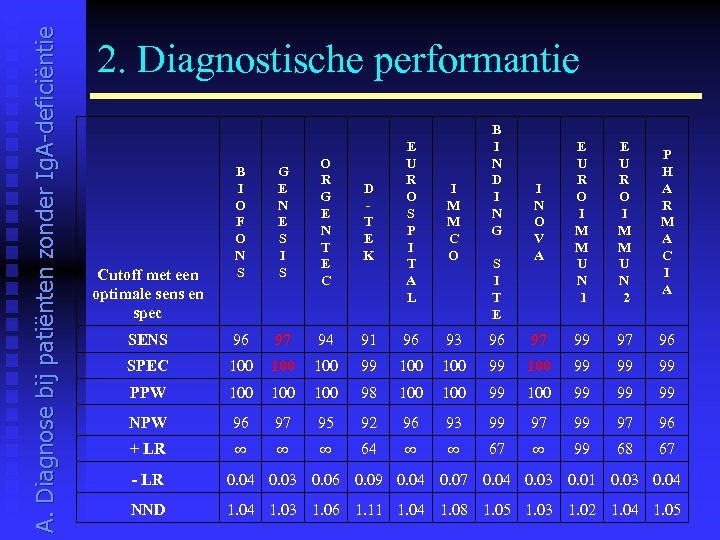
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie D T E K E U R O S P I T A L I M M C O B I N D I N G S I T E I N O V A E U R O I M M U N 1 E U R O I M M U N 2 P H A R M A C I A B I O F O N S G E N E S I S O R G E N T E C SENS 96 97 94 91 96 93 96 97 99 97 96 SPEC 100 100 99 99 99 PPW 100 100 98 100 99 99 99 NPW 96 97 95 92 96 93 99 97 96 + LR ∞ ∞ ∞ 64 ∞ ∞ 67 ∞ 99 68 67 Cutoff met een optimale sens en spec - LR 0. 04 0. 03 0. 06 0. 09 0. 04 0. 07 0. 04 0. 03 0. 01 0. 03 0. 04 NND 1. 04 1. 03 1. 06 1. 11 1. 04 1. 08 1. 05 1. 03 1. 02 1. 04 1. 05
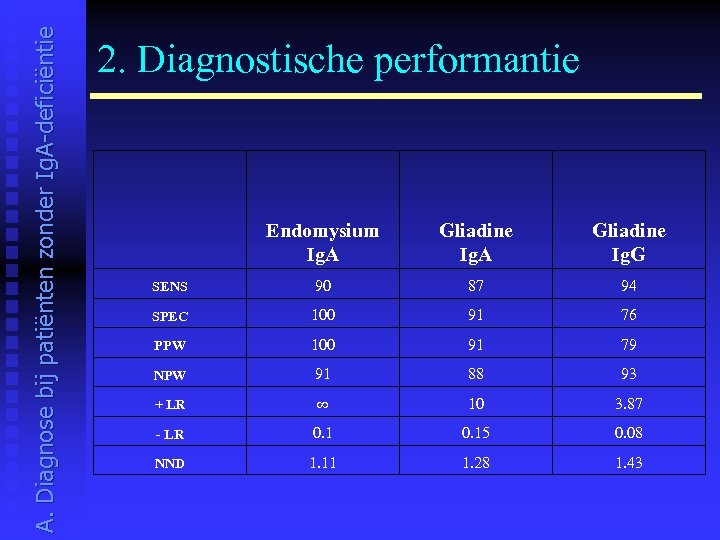
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Endomysium Ig. A Gliadine Ig. G SENS 90 87 94 SPEC 100 91 76 PPW 100 91 79 NPW 91 88 93 + LR ∞ 10 3. 87 - LR 0. 15 0. 08 NND 1. 11 1. 28 1. 43
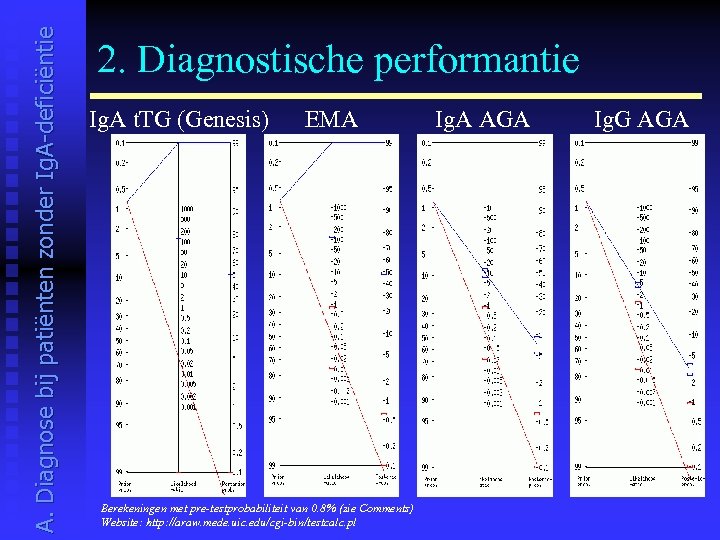
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Ig. A t. TG (Genesis) EMA Berekeningen met pre-testprobabiliteit van 0. 8% (zie Comments) Website: http: //araw. mede. uic. edu/cgi-bin/testcalc. pl Ig. A AGA Ig. G AGA

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Genesis en Inova: 2 op 70 stalen negatief - De kits van andere firma’s konden evenmin t. TG antistoffen aantonen - EMA waren negatief - Ig. A AGA waren bij deze 2 stalen wel positief - Stalen met negatieve Ig. A t. TG antistoffen en negatieve EMA werden ook reeds in de literatuur vermeld Er bestaan coeliakiepatiënten die negatief zijn voor Ig. A t. TG en endomysium antistoffen. Bij deze patiënten vormen de Ig. A AGA een alternatief
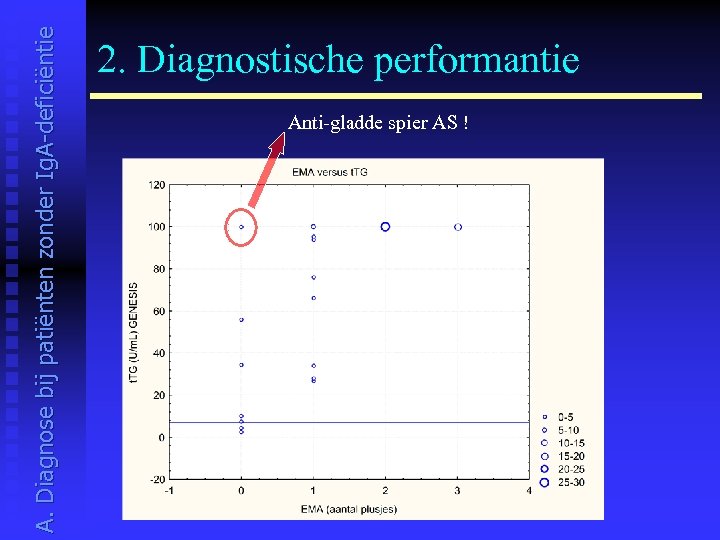
A. Diagnose bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Anti-gladde spier AS !

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 3. Klinische impact 1. Diagnostisch: Kunnen andere testen vermeden/vervangen worden ? - vervanging van de Ig. A EMA-test door de Ig. A t. TG-test - Ig. A AGA-test voor t. TG negatieve patiënten - is bioptie nog een noodzaak ? Rapport van het eerste wereldcongres van pediatrische gastroenterologie, hepatologie en nutritie: typische kliniek positieve serologie positieve HLA-typering verdwijnen klachten onder glutenvrij dieet Wanneer aanwezig bij een patiënt kan dit in bepaalde gevallen voldoende zijn om de diagnose te stellen. Momenteel nog niet aanbevolen (ontbreken van studies).

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 3. Klinische impact 2. Therapeutisch: a) Patiënten met een typische kliniek Bij deze patiënten wordt meestal een bioptie gedaan. Het al dan niet starten van een therapie zal dan voornamelijk afhangen van het resultaat van de histologie en minder van het resultaat van de serologie. b) Screening Cf. later

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 4. Organisatorische en financiële impact: cf. C 3

A. Diagnose bij patiënten zonder Ig. A-deficiëntie 5. Decision Vervangen van de bepaling van Ig. A EMA door de bepaling van Ig. A t. TG in het kader van de diagnosestelling van coeliakie bij patiënten zonder Ig. A deficiëntie. De bepaling van Ig. A AGA reserveren we voor coeliakie patiënten die negatief zijn voor de bepaling van Ig. A t. TGAS.

B. Ig. A t. TG bij follow-up patiënten zonder Ig. A-deficiëntie

B. Follow-up bij patiënten zonder Ig. A-deficiëntie 1. Analytische performantie: cf. punt 1 2. Diagnostische performantie 1. Literatuur - persisteren EMA/Ig. A AGA = persisteren histologische letsels - EMA/Ig. A AGA dalen tijdens glutenvrij dieet maar seroconversie ≠ normaliseren dunnedarmmucosa - Ig. G AGA: immunologisch geheugen - Ig. A t. TG antistoffen: dalen tijdens dieet en stijgen tijdens gluten challenge - Correlatie tussen Ig. A t. TG antistoffen en APO: 14 - 76% 2. Eigen studie
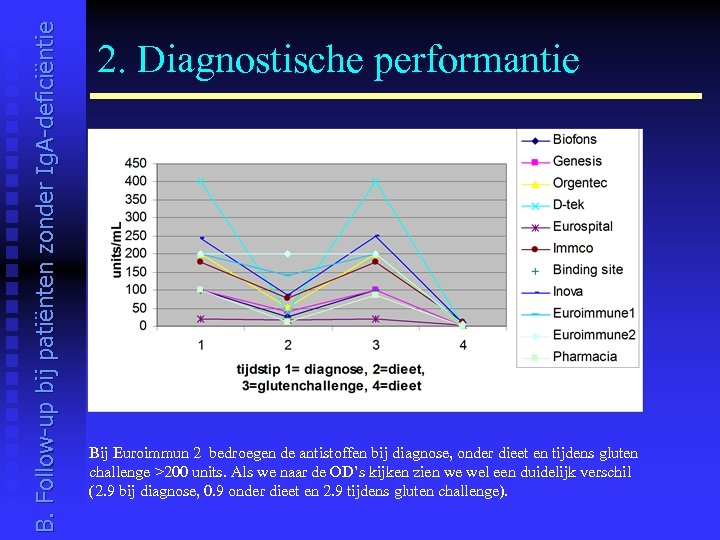
B. Follow-up bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie Bij Euroimmun 2 bedroegen de antistoffen bij diagnose, onder dieet en tijdens gluten challenge >200 units. Als we naar de OD’s kijken zien we wel een duidelijk verschil (2. 9 bij diagnose, 0. 9 onder dieet en 2. 9 tijdens gluten challenge).

B. Follow-up bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie t. TG: aantal pos APO positief: 24 stalen APO negatief: 4 stalen Biofons 16 (67%) 0 Genesis 19 (79%) 1 Orgentec 16 (67%) 0 D-tek 19 (79%) 0 Eurospital 17 (71%) 0 Immco 17 (71%) 0 Binding Site 17 (71%) 0 Inova 19 (79%) 1 Euroimmun 1 17 (71%) 0 Euroimmun 2 17 (71%) 1 Pharmacia 16 (67%) 0
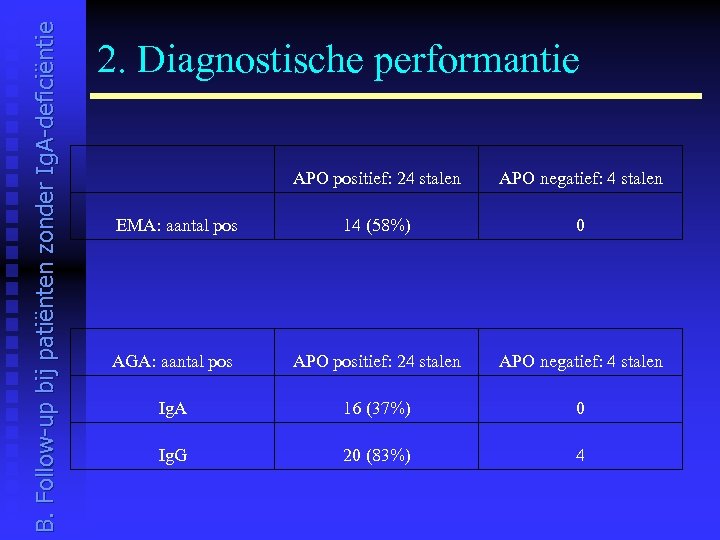
B. Follow-up bij patiënten zonder Ig. A-deficiëntie 2. Diagnostische performantie APO positief: 24 stalen APO negatief: 4 stalen EMA: aantal pos 14 (58%) 0 AGA: aantal pos APO positief: 24 stalen APO negatief: 4 stalen Ig. A 16 (37%) 0 Ig. G 20 (83%) 4

B. Follow-up bij patiënten zonder Ig. A-deficiëntie 3. Klinische impact 1. Diagnostisch: Kunnen andere testen vermeden/vervangen worden ? - Vervanging van de Ig. A EMA-test door de Ig. A t. TG-test (betere correlatie met histologisch onderzoek) - De enige manier om histologisch herstel met zekerheid aan te tonen is dunnedarmbioptie 2. Outcome: Een stijging/persisteren van antistoffen kan wijzen op slechte dieet compliance. Wanneer een patiënt zich niet houdt aan het glutenvrij dieet kan dat het risico op complicaties verhogen.

B. Follow-up bij patiënten zonder Ig. A-deficiëntie 4. Financiële impact: cf. punt 1 5. Decision Vervangen van de bepaling van Ig. A EMA door de bepaling van Ig. A t. TG in het kader van de follow-up van coeliakie bij patiënten zonder Ig. A deficiëntie. De Ig. A AGA-test voeren we enkel uit bij patiënten die bij diagnose negatief waren voor de Ig. A t. TG-test.

C. Ig. G t. TG bij de diagnose van coeliakie bij Ig. A-deficiënte patiënten

1. Analytische performantie: cf. punt 1 C. Diagnose bij Ig. A-deficiënte patiënten 2. Diagnostische performantie 1. Literatuur A. Ig. A deficiëntie: - 2 tot 10 % van de coeliakiepatiënten is Ig. A deficiënt - deze patiënten zijn negatief voor de Ig. A gebaseerde testen - guidelines bevelen aan steeds totaal [Ig. A] te bepalen bij vermoeden van coeliakie B. serologie: - Ig. G AGA: goede sensitiviteit, lage specificiteit - Ig. G t. TG: sensitiviteit: 98. 7%, specificiteit: 98. 6%

C. Diagnose bij Ig. A-deficiënte patiënten 2. Diagnostische performantie 2. Eigen studie: 5 Ig. A deficiënte coeliakie patiënten, 69 controlestalen Ig. G AGA - goede sensitiviteit (alle 5 patiënten: positief) - minder goede specificiteit (75%) Ig. G t. TG - goede specificiteit (88 -100%) - slechtere sensitiviteit: bij de meeste kits waren slechts 3 van de 5 patiënten positief

C. Diagnose bij Ig. A-deficiënte patiënten 3. Klinische impact 1. Diagnostisch: - de Ig. G t. TG kan de Ig. G AGA-test momenteel niet vervangen - steeds bioptie nodig om diagnose te bevestigen (cf. lage specificiteit van de Ig. G AGA-test) 2. Therapeutisch: cf. punt 1 Therapeutisch:
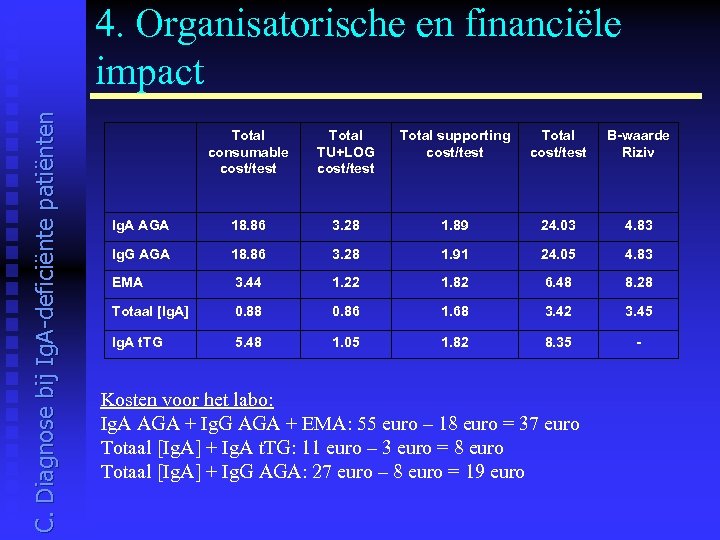
C. Diagnose bij Ig. A-deficiënte patiënten 4. Organisatorische en financiële impact Total consumable cost/test Total TU+LOG cost/test Total supporting cost/test Total cost/test B-waarde Riziv Ig. A AGA 18. 86 3. 28 1. 89 24. 03 4. 83 Ig. G AGA 18. 86 3. 28 1. 91 24. 05 4. 83 EMA 3. 44 1. 22 1. 82 6. 48 8. 28 Totaal [Ig. A] 0. 88 0. 86 1. 68 3. 42 3. 45 Ig. A t. TG 5. 48 1. 05 1. 82 8. 35 - Kosten voor het labo: Ig. A AGA + Ig. G AGA + EMA: 55 euro – 18 euro = 37 euro Totaal [Ig. A] + Ig. A t. TG: 11 euro – 3 euro = 8 euro Totaal [Ig. A] + Ig. G AGA: 27 euro – 8 euro = 19 euro
![C. Diagnose bij Ig. A-deficiënte patiënten 5. Decision A. Totaal [Ig. A] Bij een C. Diagnose bij Ig. A-deficiënte patiënten 5. Decision A. Totaal [Ig. A] Bij een](https://present5.com/presentation/818e16fd8152255bbb8a86db1169191d/image-52.jpg)
C. Diagnose bij Ig. A-deficiënte patiënten 5. Decision A. Totaal [Ig. A] Bij een serologie-aanvraag voor coeliakie wordt eerst totaal [Ig. A] bepaald. Is de patiënt niet-Ig. A deficiënt, dan voeren we een bepaling van Ig. A t. TG (en evt. Ig. A AGA) uit. Is de patiënt wel Ig. A deficiënt, dan beperken we ons tot de Ig. G AGA-test. B. Ig. G t. TG Omdat in onze eigen studie de Ig. G t. TG ELISA een lagere sensitiviteit vertoont ten opzichte van de Ig. G AGA ELISA, behouden we de Ig. G AGA test voor diagnose-stelling bij Ig. A deficiënte patiënten.

D. Ig. G t. TG bij Ig. A-deficiënte follow-up patiënten

1. Analytische performantie: cf. punt 1 D. Follow-up bij Ig. A-deficiënte patiënten 2. Diagnostische performantie 1. Literatuur - Cataldo et al. : Ig. G AGA antistoffen negativeerden bij 34 patiënten die sinds meer dan een jaar op een glutenvrij dieet staan en bleven positief bij 10 patiënten die hun dieet niet strikt opvolgden - Korponay-Szabo et al. : Ig. G t. TG antistoffen negativeren slechts zeer traag en kunnen zelfs positief blijven wanneer de dunnedarmmucosa reeds genormaliseerd is

D. Follow-up bij Ig. A-deficiënte patiënten 2. Diagnostische performantie 2. Eigen studie 3. 2 Ig. A deficiënte coeliakiepatiënten tijdens follow-up, 4. 1 met normale histologie, 1 met afwijkende histologie Ig. G AGA - patiënt met afwijkende histologie: positieve AS - patiënt met normale histologie: negatieve AS Ig. G t. TG - patiënt met afwijkende histologie: positieve AS - patiënt met normale histologie: positieve AS

D. Follow-up bij Ig. A-deficiënte patiënten 3. Klinische impact 1. Diagnostisch: - de Ig. G t. TG-test is geen goede test voor de FU van Ig. A deficiënte coeliakiepatiënten - de Ig. G AGA-test = alternatief 2. Outcome: De Ig. G t. TG AS kunnen nog positief zijn op het moment dat de bioptie reeds genormaliseerd is (een persisteren van AS wordt geïnterpreteerd als een slechte dieet compliance)

D. Follow-up bij Ig. A-deficiënte patiënten 4. Financiële impact: cf. punt 3 5. Decision Omdat de Ig. G t. TG geen goede test blijkt te zijn voor de follow-up van Ig. A deficiënte coeliakie-patiënten, behouden we voorlopig de Ig. G AGA-test.

E. Screening van risicogroepen

1. Analytische performantie: cf. punt 1 2. Diagnostische performantie E. Screening van risicogroepen DM type I: Prevalentie: 0. 97 tot 16. 4% De diagnose diabetes wordt meestal gesteld vóór de diagnose coeliakie Symptomen: - malabsorptie - groeiretardatie - instabiele diabetes - soms subtieler

2. Diagnostische performantie E. Screening van risicogroepen Waarmee screenen? - Steeds een bepaling van totaal [Ig. A] includeren (cf. punt C) - Bij niet-Ig. A deficiënte patiënten screenen we met de Ig. A t. TG-test (cf. punt A) - Een bepaling van Ig. A AGA bij een negatief Ig. A t. TG resultaat is niet zinvol. Theorema van Bayes: Stel: coeliakieprevalentie bij diabetes-patiënten = 5% → de kans dat een negatief t. TG-resultaat afkomstig is van een coeliakiepatiënt = 0. 16% → de kans dat een negatief t. TG-resultaat gecombineerd met een positief Ig. A AGA-resultaat afkomstig is van een coeliakiepatiënt = 1. 7%
![3. Klinische impact E. Screening van risicogroepen 1. Diagnostisch: Als totaal [Ig. A] normaal 3. Klinische impact E. Screening van risicogroepen 1. Diagnostisch: Als totaal [Ig. A] normaal](https://present5.com/presentation/818e16fd8152255bbb8a86db1169191d/image-61.jpg)
3. Klinische impact E. Screening van risicogroepen 1. Diagnostisch: Als totaal [Ig. A] normaal is, screenen we met de Ig. A t. TG-test (hogere sensitiviteit dan de Ig. A EMA-test) Positieve serologie moet steeds bevestigd worden op bioptie 2. Therapeutisch: Wanneer men een test gebruikt als screeningstest is het belangrijk dat deze test een zo hoog mogelijke sensitiviteit heeft. Indien de test vals negatief is zal men immers niet overgaan tot bioptie en loopt men het risico de diagnose te missen. 3. Outcome: Subjectieve klachten, groei, biochemische en hematologische parameters en diabetes-controle kunnen verbeteren na starten van het glutenvrij dieet.

E. Screening van risicogroepen 4. Financiële impact: cf. punt 1, 3 5. Decision In het kader van screening naar coeliakie bepalen we steeds totaal [Ig. A]. Is deze waarde normaal dan gaan we over tot het uitvoeren van de Ig. A t. TG-test. Bij Ig. A-deficiënte patiënten voeren we een bepaling van Ig. G AGA uit.

F. Screening van de algemene populatie

F. Screening van de algemene populatie Criteria WHO (1) vroegtijdige detectie is moeilijk op basis van de kliniek; (2) de aandoening is frequent en veroorzaakt significante morbiditeit; (3) er bestaat een gevoelige en specifieke screeningstest; (4) er is een efficiënte behandeling beschikbaar; (5) indien niet herkend, kan de ziekte aanleiding geven tot ernstige complicaties ? Rapport van het eerste wereldcongres van pediatrische gastroenterologie, hepatologie en nutritie: screening van de volledige populatie wordt momenteel NIET aanbevolen

Samenvatting van de bevindingen • De bepaling van Ig. A t. TG-antistoffen is superieur aan de bepaling van EMA of AGA bij de diagnose van coeliakie bij patiënten zonder Ig. A-deficiëntie. • Ig. A t. TG-antistoffen dalen onder een glutenvrij dieet en stijgen bij het maken van ernstige dieetfouten. Het negativeren van de Ig. A t. TG antistoffen is echter geen goede indicator voor het histologische herstel van de ziekte. De enige goede test om dit aan te tonen is bioptie. • Totaal [Ig. A] zou steeds moeten bepaald worden bij serologie-aanvraag voor coeliakie. • Zowel voor de diagnose als voor de follow up van Ig. A deficiënte coeliakie patiënten behouden we voorlopig de Ig. G AGA test.

Comments: huidige situatie in GHB

Huidige situatie in GHB Pediatrie: - diagnose coeliakie: originele ESPGHAN-criteria (3 biopties) - bij serologieaanvraag wordt standaard ook totaal [Ig. A] aangevraagd - DM type I: jaarlijkse screening naar coeliakie (bioptie indien EMA positief) Volwassenen: - diagnose coeliakie: herziene ESPGHAN-criteria (1 bioptie) - totaal [Ig. A] wordt niet standaard aangevraagd

Huidige situatie in GHB Aanvragen serologie: - Ig. A AGA, Ig. G AGA, Ig. A EMA - wekelijks: 70 aanvragen voor bepalen van EMA, bij 60% van deze stalen zijn ook Ig. A en Ig. G AGA aangevraagd - de helft van de stalen: afkomstig van de periferie - 40% pediatrische stalen - aanvragen binnen het ziekenhuis: jaarlijks zijn er 13 stalen afkomstig van nieuw gediagnosticeerde coeliakie patiënten (= 0. 8% van de stalen of 1/125 stalen)

To do

To do 1: Implementatie van de Ig. A t. TG-test Genesis - Genesis en Inova: beste diagnostische performantie - Genesis: betere technische perfomantie
![To do 2: Aanvraagformulier □ serologie coeliakie Diagnose coeliakie [Ig. A] normaal [Ig. A] To do 2: Aanvraagformulier □ serologie coeliakie Diagnose coeliakie [Ig. A] normaal [Ig. A]](https://present5.com/presentation/818e16fd8152255bbb8a86db1169191d/image-71.jpg)
To do 2: Aanvraagformulier □ serologie coeliakie Diagnose coeliakie [Ig. A] normaal [Ig. A] gedaald Ig. A t. TG Ig. G AGA

To do 2: Aanvraagformulier Probleem 1: we missen coeliakie-patiënten die niet Ig. A deficiënt zijn en toch negatief zijn voor de Ig. A t. TG-test. Wanneer moeten we een bepaling van Ig. A AGA doen? Screening: bepaling van Ig. A AGA is zinloos Bewezen coeliakie op bioptie en negatieve Ig. A t. TG AS: - Uitvoeren van de Ig. A AGA-test * Uitbesteden van de test * Identificatie van de patiënten: Toegang tot de resultaten van APO? Op specifieke aanvraag? - Volledig afschaffen van de Ig. A AGA-test

To do 2: Aanvraagformulier Probleem 2: uitvoerfrequentie van de Ig. G AGA-test → Stalen voor de Ig. G AGA-test doorsturen naar een labo met hogere uitvoerfrequentie; → Voorstel indienen bij het RIZIV om de Ig. G AGA-test enkel terugbetaalbaar te maken bij Ig. A-deficiënte patiënten. In dit geval zal er één referentielabo moeten komen voor het uitvoeren van de Ig. G AGA-test.

To do 3: Nomenclatuuraanvraag Twee testen te kiezen uit t. TG, EMA en AGA zijn terugbetaalbaar Ig. G AGA enkel terugbetaalbaar bij bewezen Ig. A deficiëntie
818e16fd8152255bbb8a86db1169191d.ppt