420af7bc9cf57958486d2ebf530bbcc8.ppt
- Количество слайдов: 25
 CAPÍTULO 20. LA SELECCIÓN NATURAL (II) - Selección contra alelos recesivos - Polimorfismo balanceado - Selección contra alelos del cromosoma X
CAPÍTULO 20. LA SELECCIÓN NATURAL (II) - Selección contra alelos recesivos - Polimorfismo balanceado - Selección contra alelos del cromosoma X
 Bibliografía complementaria Lao et al (2003) Spatial patterns of cystic fibrosis mutation spectra in European populations European Journal of Human Genetics 11, 385 – 394 (JAP 1333) Snow et al. (2005) The global distribution of clinical episodes of Plasmodium falciparum malaria. Nature 434: 214 -217 Woolf CM (2005) Albinism (OCA 2) in Amerindians YEARBOOK OF PHYSICAL ANTHROPOLOGY 48: 118– 140 (JAP 1332)
Bibliografía complementaria Lao et al (2003) Spatial patterns of cystic fibrosis mutation spectra in European populations European Journal of Human Genetics 11, 385 – 394 (JAP 1333) Snow et al. (2005) The global distribution of clinical episodes of Plasmodium falciparum malaria. Nature 434: 214 -217 Woolf CM (2005) Albinism (OCA 2) in Amerindians YEARBOOK OF PHYSICAL ANTHROPOLOGY 48: 118– 140 (JAP 1332)
 Selección contra alelos recesivos Si consideramos un locus dialélico, donde A es el alelo dominante, de frecuencia p, a el alelo recesivo, de frecuencia q, s es la desventaja selectiva de los homocigotos y µ la tasa de mutación, las frecuencias genotípicas antes y después de la acción de la selección en una generación dada serán: GENOTIPO EFICACIA BIOLÓGICA FRECUENCIA ANTES DESPUÉS AA 1 p 2 Aa 1 2. p. q aa 1 -s q 2 Pérdida de individuos aa por generación: s. q 2 Equilibrio mutación-selección: s. q 2 = µ. (1 -q)≈µ
Selección contra alelos recesivos Si consideramos un locus dialélico, donde A es el alelo dominante, de frecuencia p, a el alelo recesivo, de frecuencia q, s es la desventaja selectiva de los homocigotos y µ la tasa de mutación, las frecuencias genotípicas antes y después de la acción de la selección en una generación dada serán: GENOTIPO EFICACIA BIOLÓGICA FRECUENCIA ANTES DESPUÉS AA 1 p 2 Aa 1 2. p. q aa 1 -s q 2 Pérdida de individuos aa por generación: s. q 2 Equilibrio mutación-selección: s. q 2 = µ. (1 -q)≈µ
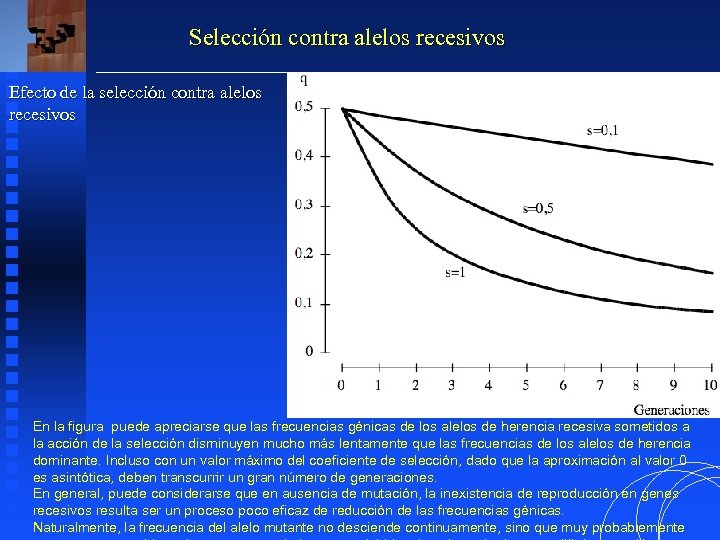 Selección contra alelos recesivos Efecto de la selección contra alelos recesivos En la figura puede apreciarse que las frecuencias génicas de los alelos de herencia recesiva sometidos a la acción de la selección disminuyen mucho más lentamente que las frecuencias de los alelos de herencia dominante. Incluso con un valor máximo del coeficiente de selección, dado que la aproximación al valor 0 es asintótica, deben transcurrir un gran número de generaciones. En general, puede considerarse que en ausencia de mutación, la inexistencia de reproducción en genes recesivos resulta ser un proceso poco eficaz de reducción de las frecuencias génicas. Naturalmente, la frecuencia del alelo mutante no desciende continuamente, sino que muy probablemente
Selección contra alelos recesivos Efecto de la selección contra alelos recesivos En la figura puede apreciarse que las frecuencias génicas de los alelos de herencia recesiva sometidos a la acción de la selección disminuyen mucho más lentamente que las frecuencias de los alelos de herencia dominante. Incluso con un valor máximo del coeficiente de selección, dado que la aproximación al valor 0 es asintótica, deben transcurrir un gran número de generaciones. En general, puede considerarse que en ausencia de mutación, la inexistencia de reproducción en genes recesivos resulta ser un proceso poco eficaz de reducción de las frecuencias génicas. Naturalmente, la frecuencia del alelo mutante no desciende continuamente, sino que muy probablemente
 Selección contra alelos recesivos Albinismo Ausencia de pigmento en los ojos piel, y cabello. Su incidencia es de alrededor de 1 de cada 15. 000. Puede ser ocular u oculocutáneo. El segundo caso es el más frecuente. Su origen se encuentra en el gen OCA 2 (15 q 11. 2 -q 12).
Selección contra alelos recesivos Albinismo Ausencia de pigmento en los ojos piel, y cabello. Su incidencia es de alrededor de 1 de cada 15. 000. Puede ser ocular u oculocutáneo. El segundo caso es el más frecuente. Su origen se encuentra en el gen OCA 2 (15 q 11. 2 -q 12).
 Selección contra alelos recesivos Albinismo Woolf (2005) Siendo un carácter de herencia recesiva, la elevada endogamia y la consanguinidad favorecen su aparición. Este hecho, unido a la deriva genética en poblaciones aisladas de pequeño tamaño puede dar lugar a una notable incidencia, teniendo en cuenta además que no es altamente deletereo. Es el caso de las poblaciones de la tabla. Se suele citar también la localidad de Aicuña en Argentina, con 3 individuos albinos en una población de 221 habitantes. http: //www. letraslibres. com/revista/convivio/aicun a-no-es-un-pueblo-de-albinos? page=full
Selección contra alelos recesivos Albinismo Woolf (2005) Siendo un carácter de herencia recesiva, la elevada endogamia y la consanguinidad favorecen su aparición. Este hecho, unido a la deriva genética en poblaciones aisladas de pequeño tamaño puede dar lugar a una notable incidencia, teniendo en cuenta además que no es altamente deletereo. Es el caso de las poblaciones de la tabla. Se suele citar también la localidad de Aicuña en Argentina, con 3 individuos albinos en una población de 221 habitantes. http: //www. letraslibres. com/revista/convivio/aicun a-no-es-un-pueblo-de-albinos? page=full
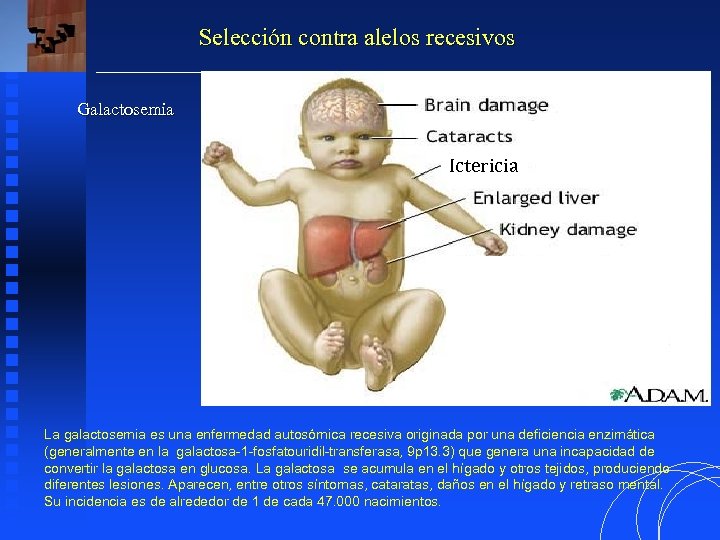 Selección contra alelos recesivos Galactosemia Ictericia La galactosemia es una enfermedad autosómica recesiva originada por una deficiencia enzimática (generalmente en la galactosa-1 -fosfatouridil-transferasa, 9 p 13. 3) que genera una incapacidad de convertir la galactosa en glucosa. La galactosa se acumula en el hígado y otros tejidos, produciendo diferentes lesiones. Aparecen, entre otros síntomas, cataratas, daños en el hígado y retraso mental. Su incidencia es de alrededor de 1 de cada 47. 000 nacimientos.
Selección contra alelos recesivos Galactosemia Ictericia La galactosemia es una enfermedad autosómica recesiva originada por una deficiencia enzimática (generalmente en la galactosa-1 -fosfatouridil-transferasa, 9 p 13. 3) que genera una incapacidad de convertir la galactosa en glucosa. La galactosa se acumula en el hígado y otros tejidos, produciendo diferentes lesiones. Aparecen, entre otros síntomas, cataratas, daños en el hígado y retraso mental. Su incidencia es de alrededor de 1 de cada 47. 000 nacimientos.
 Selección contra alelos recesivos Fenilcetonuria La causa de la enfermedad generalmente es la carencia de la enzima fenilalanina hidroxilasa (12 q 23. 2), responsable de la hidroxilación del aminoácido fenilalanina en la reacción que produce tirosina. Por ello, su defecto determina un incremento de la concentración sanguínea de fenilalanina. También se aumenta la transaminación de la fenilalanina como vía metabólica alternativa, y asimismo se acumulan los metabolitos fenilpiruvato, fenilactato y fenilacetato. El fenilpiruvato es un neurotóxico que afecta gravemente al cerebro durante el crecimiento y el desarrollo. Los efectos de la acumulación de este neurotóxico causan oligofrenia fenilpirúvica, caracterizada por un cociente intelectual inferior a 20. Los primeros meses de vida, los niños que padecen esta enfermedad parecen estar sanos. Entre los tres y los seis meses pierden el interés por el entorno, y al año se evidencia un retraso importante en su desarrollo. Los síntomas suelen ser retraso psicomotor, cuadros psicóticos de tipo autista, convulsiones, síndrome de West, convulsiones generalizadas y un eczema facial muy rebelde. Por lo general su desarrollo físico es bueno, tienden a tener el cabello más claro que sus hermanos, piel clara, y presentan un olor característico a paja mojada. Los datos sobre la frecuencia de la fenilcetonuria en la población total de Europa y Norteamérica son de
Selección contra alelos recesivos Fenilcetonuria La causa de la enfermedad generalmente es la carencia de la enzima fenilalanina hidroxilasa (12 q 23. 2), responsable de la hidroxilación del aminoácido fenilalanina en la reacción que produce tirosina. Por ello, su defecto determina un incremento de la concentración sanguínea de fenilalanina. También se aumenta la transaminación de la fenilalanina como vía metabólica alternativa, y asimismo se acumulan los metabolitos fenilpiruvato, fenilactato y fenilacetato. El fenilpiruvato es un neurotóxico que afecta gravemente al cerebro durante el crecimiento y el desarrollo. Los efectos de la acumulación de este neurotóxico causan oligofrenia fenilpirúvica, caracterizada por un cociente intelectual inferior a 20. Los primeros meses de vida, los niños que padecen esta enfermedad parecen estar sanos. Entre los tres y los seis meses pierden el interés por el entorno, y al año se evidencia un retraso importante en su desarrollo. Los síntomas suelen ser retraso psicomotor, cuadros psicóticos de tipo autista, convulsiones, síndrome de West, convulsiones generalizadas y un eczema facial muy rebelde. Por lo general su desarrollo físico es bueno, tienden a tener el cabello más claro que sus hermanos, piel clara, y presentan un olor característico a paja mojada. Los datos sobre la frecuencia de la fenilcetonuria en la población total de Europa y Norteamérica son de
 Polimorfismo balanceado Hasta aquí se ha visto la selección como un proceso que tiende a aumentar una frecuencia génica a expensas de otra. En estos casos, sólo es posible alcanzar el equilibrio cuando las tasas de mutación recurrente aportan un suficiente número de alelos, para compensar los alelos perdidos por selección. Existen algunos casos, sin embargo, en los que el modo de acción de la selección, por sí mismo, determina un equilibrio. Es el modelo de la selección natural a favor del heterocigoto, que origina los denominados polimorfismos balanceados. El polimorfismo balanceado es un caso particular de la selección natural diversificadora, Al propiciar el mantenimiento de diferentes genotipos dentro de la población, la acción de la selección natural ayuda a conservar la diversidad genética.
Polimorfismo balanceado Hasta aquí se ha visto la selección como un proceso que tiende a aumentar una frecuencia génica a expensas de otra. En estos casos, sólo es posible alcanzar el equilibrio cuando las tasas de mutación recurrente aportan un suficiente número de alelos, para compensar los alelos perdidos por selección. Existen algunos casos, sin embargo, en los que el modo de acción de la selección, por sí mismo, determina un equilibrio. Es el modelo de la selección natural a favor del heterocigoto, que origina los denominados polimorfismos balanceados. El polimorfismo balanceado es un caso particular de la selección natural diversificadora, Al propiciar el mantenimiento de diferentes genotipos dentro de la población, la acción de la selección natural ayuda a conservar la diversidad genética.
 Polimorfismo balanceado Si consideramos un locus dialélico, donde A aparece con una frecuencia p, a con una frecuencia q, s 1 es la desventaja selectiva del homocigoto AA y s 2 la desventaja selectiva del homocigoto aa, las frecuencias genotípicas antes y después de la acción de la selección en una generación dada serán: GENOTIPO EFICACIA BIOLÓGICA FRECUENCIA ANTES DESPUÉS AA 1 -s 1 p 2 Aa 1 2. p. q aa 1 - s 2 q 2 Pérdida de individuos homocigotos por generación: s 1. p 2 + s 2. q 2
Polimorfismo balanceado Si consideramos un locus dialélico, donde A aparece con una frecuencia p, a con una frecuencia q, s 1 es la desventaja selectiva del homocigoto AA y s 2 la desventaja selectiva del homocigoto aa, las frecuencias genotípicas antes y después de la acción de la selección en una generación dada serán: GENOTIPO EFICACIA BIOLÓGICA FRECUENCIA ANTES DESPUÉS AA 1 -s 1 p 2 Aa 1 2. p. q aa 1 - s 2 q 2 Pérdida de individuos homocigotos por generación: s 1. p 2 + s 2. q 2
 Polimorfismo balanceado La frecuencia del alelo a en la siguiente generación será: Puesto que pq + q 2 = q. (p + q) = q, entonces será La variación de una generación a la siguiente será: El equilibrio se alcanzará cuando
Polimorfismo balanceado La frecuencia del alelo a en la siguiente generación será: Puesto que pq + q 2 = q. (p + q) = q, entonces será La variación de una generación a la siguiente será: El equilibrio se alcanzará cuando
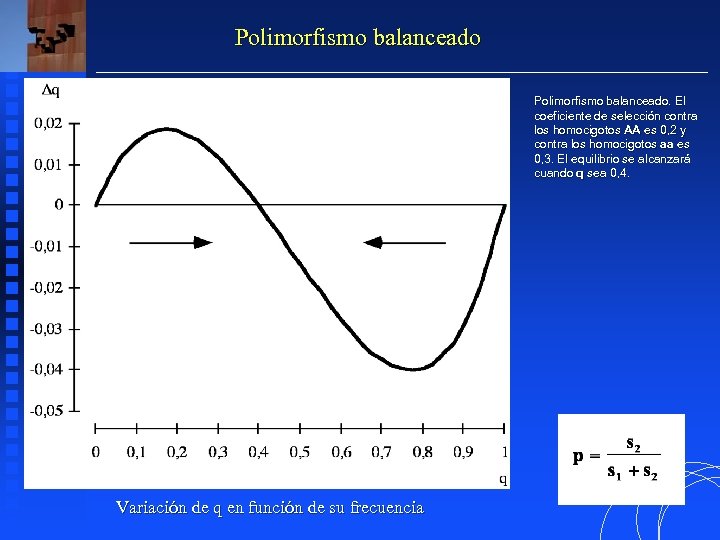 Polimorfismo balanceado. El balanceado. coeficiente de selección contra los homocigotos AA es 0, 2 y contra los homocigotos aa es 0, 3. El equilibrio se alcanzará cuando q sea 0, 4. Variación de q en función de su frecuencia
Polimorfismo balanceado. El balanceado. coeficiente de selección contra los homocigotos AA es 0, 2 y contra los homocigotos aa es 0, 3. El equilibrio se alcanzará cuando q sea 0, 4. Variación de q en función de su frecuencia
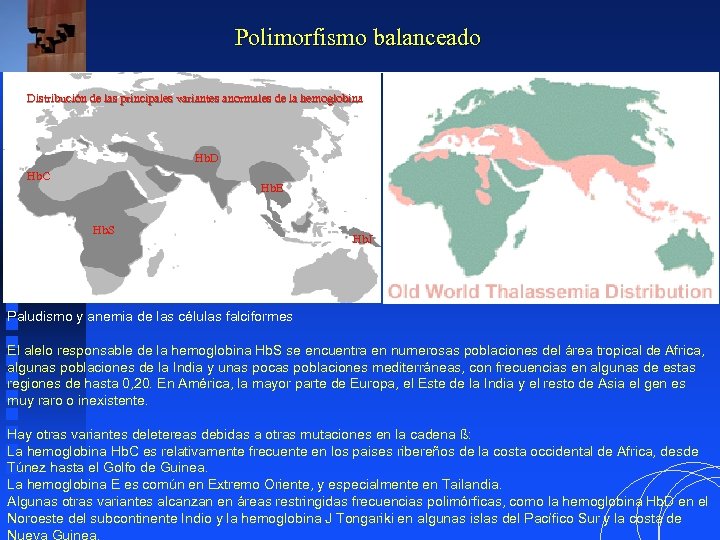 Polimorfismo balanceado Distribución de las principales variantes anormales de la hemoglobina Hb. D Hb. C Hb. E Hb. S Hb. J Paludismo y anemia de las células falciformes El alelo responsable de la hemoglobina Hb. S se encuentra en numerosas poblaciones del área tropical de Africa, algunas poblaciones de la India y unas pocas poblaciones mediterráneas, con frecuencias en algunas de estas regiones de hasta 0, 20. En América, la mayor parte de Europa, el Este de la India y el resto de Asia el gen es muy raro o inexistente. Hay otras variantes deletereas debidas a otras mutaciones en la cadena ß: La hemoglobina Hb. C es relativamente frecuente en los paises ribereños de la costa occidental de Africa, desde Túnez hasta el Golfo de Guinea. La hemoglobina E es común en Extremo Oriente, y especialmente en Tailandia. Algunas otras variantes alcanzan en áreas restringidas frecuencias polimórficas, como la hemoglobina Hb. D en el Noroeste del subcontinente Indio y la hemoglobina J Tongariki en algunas islas del Pacífico Sur y la costa de Nueva Guinea.
Polimorfismo balanceado Distribución de las principales variantes anormales de la hemoglobina Hb. D Hb. C Hb. E Hb. S Hb. J Paludismo y anemia de las células falciformes El alelo responsable de la hemoglobina Hb. S se encuentra en numerosas poblaciones del área tropical de Africa, algunas poblaciones de la India y unas pocas poblaciones mediterráneas, con frecuencias en algunas de estas regiones de hasta 0, 20. En América, la mayor parte de Europa, el Este de la India y el resto de Asia el gen es muy raro o inexistente. Hay otras variantes deletereas debidas a otras mutaciones en la cadena ß: La hemoglobina Hb. C es relativamente frecuente en los paises ribereños de la costa occidental de Africa, desde Túnez hasta el Golfo de Guinea. La hemoglobina E es común en Extremo Oriente, y especialmente en Tailandia. Algunas otras variantes alcanzan en áreas restringidas frecuencias polimórficas, como la hemoglobina Hb. D en el Noroeste del subcontinente Indio y la hemoglobina J Tongariki en algunas islas del Pacífico Sur y la costa de Nueva Guinea.
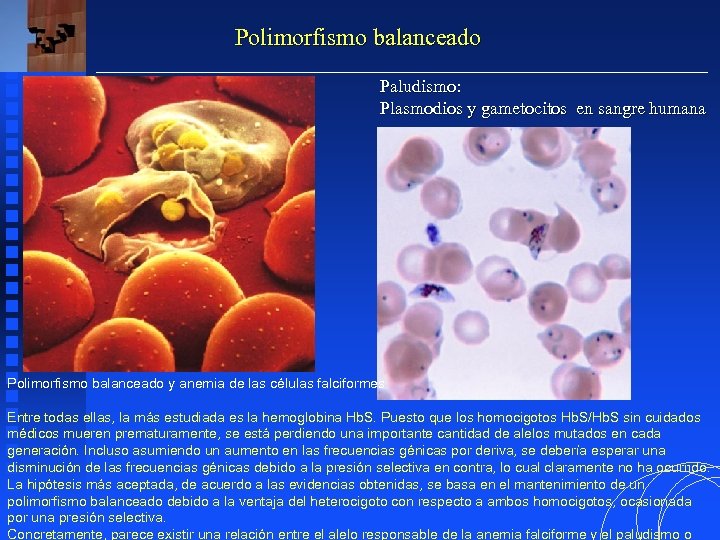 Polimorfismo balanceado Paludismo: Plasmodios y gametocitos en sangre humana Polimorfismo balanceado y anemia de las células falciformes Entre todas ellas, la más estudiada es la hemoglobina Hb. S. Puesto que los homocigotos Hb. S/Hb. S sin cuidados médicos mueren prematuramente, se está perdiendo una importante cantidad de alelos mutados en cada generación. Incluso asumiendo un aumento en las frecuencias génicas por deriva, se debería esperar una disminución de las frecuencias génicas debido a la presión selectiva en contra, lo cual claramente no ha ocurrido. La hipótesis más aceptada, de acuerdo a las evidencias obtenidas, se basa en el mantenimiento de un polimorfismo balanceado debido a la ventaja del heterocigoto con respecto a ambos homocigotos, ocasionada por una presión selectiva. Concretamente, parece existir una relación entre el alelo responsable de la anemia falciforme y el paludismo o
Polimorfismo balanceado Paludismo: Plasmodios y gametocitos en sangre humana Polimorfismo balanceado y anemia de las células falciformes Entre todas ellas, la más estudiada es la hemoglobina Hb. S. Puesto que los homocigotos Hb. S/Hb. S sin cuidados médicos mueren prematuramente, se está perdiendo una importante cantidad de alelos mutados en cada generación. Incluso asumiendo un aumento en las frecuencias génicas por deriva, se debería esperar una disminución de las frecuencias génicas debido a la presión selectiva en contra, lo cual claramente no ha ocurrido. La hipótesis más aceptada, de acuerdo a las evidencias obtenidas, se basa en el mantenimiento de un polimorfismo balanceado debido a la ventaja del heterocigoto con respecto a ambos homocigotos, ocasionada por una presión selectiva. Concretamente, parece existir una relación entre el alelo responsable de la anemia falciforme y el paludismo o
 Polimorfismo balanceado Mosquito Anopheles Ciclo del plasmodio Polimorfismo balanceado y anemia de las células falciformes Plasmodium falciparum, transmitido por el mosquito Anopheles, produce la forma más maligna y común de esta enfermedad. Hay otras especies de parásito que producen variantes menos agresivas. Donde el paludismo se encuentra presente de forma continuada, prácticamente todos los niños se encuentran infectados a los dos años de edad. El número de parásitos desciende con la edad, en la medida que las defensas inmunológicas del organismo van adquiriendo efectividad, pero en algunas
Polimorfismo balanceado Mosquito Anopheles Ciclo del plasmodio Polimorfismo balanceado y anemia de las células falciformes Plasmodium falciparum, transmitido por el mosquito Anopheles, produce la forma más maligna y común de esta enfermedad. Hay otras especies de parásito que producen variantes menos agresivas. Donde el paludismo se encuentra presente de forma continuada, prácticamente todos los niños se encuentran infectados a los dos años de edad. El número de parásitos desciende con la edad, en la medida que las defensas inmunológicas del organismo van adquiriendo efectividad, pero en algunas
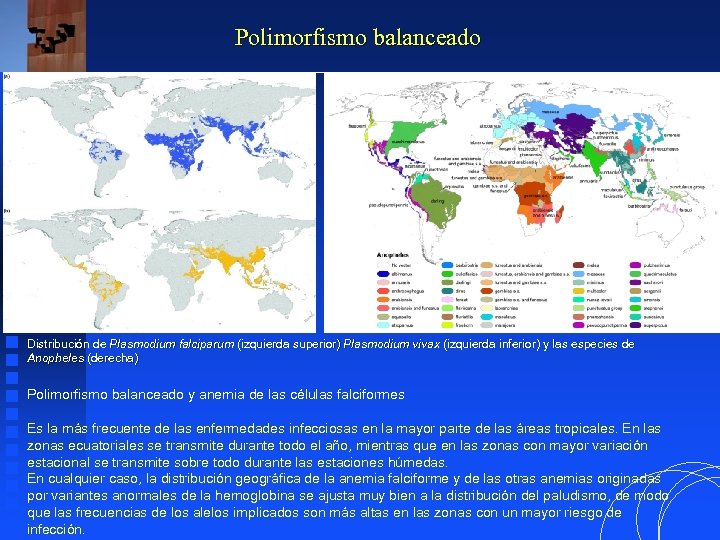 Polimorfismo balanceado Distribución de Plasmodium falciparum (izquierda superior) Plasmodium vivax (izquierda inferior) y las especies de Anopheles (derecha) Polimorfismo balanceado y anemia de las células falciformes Es la más frecuente de las enfermedades infecciosas en la mayor parte de las áreas tropicales. En las zonas ecuatoriales se transmite durante todo el año, mientras que en las zonas con mayor variación estacional se transmite sobre todo durante las estaciones húmedas. En cualquier caso, la distribución geográfica de la anemia falciforme y de las otras anemias originadas por variantes anormales de la hemoglobina se ajusta muy bien a la distribución del paludismo, de modo que las frecuencias de los alelos implicados son más altas en las zonas con un mayor riesgo de infección.
Polimorfismo balanceado Distribución de Plasmodium falciparum (izquierda superior) Plasmodium vivax (izquierda inferior) y las especies de Anopheles (derecha) Polimorfismo balanceado y anemia de las células falciformes Es la más frecuente de las enfermedades infecciosas en la mayor parte de las áreas tropicales. En las zonas ecuatoriales se transmite durante todo el año, mientras que en las zonas con mayor variación estacional se transmite sobre todo durante las estaciones húmedas. En cualquier caso, la distribución geográfica de la anemia falciforme y de las otras anemias originadas por variantes anormales de la hemoglobina se ajusta muy bien a la distribución del paludismo, de modo que las frecuencias de los alelos implicados son más altas en las zonas con un mayor riesgo de infección.
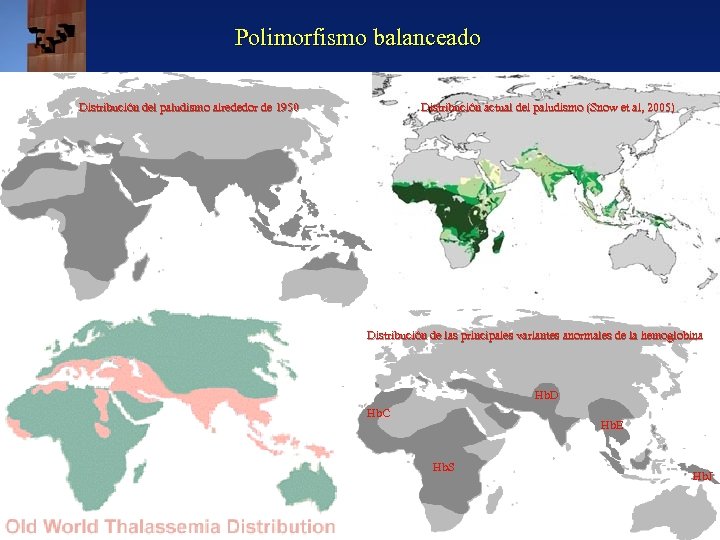 Polimorfismo balanceado Distribución del paludismo alrededor de 1950 Distribución actual del paludismo (Snow et al, 2005) Distribución de las principales variantes anormales de la hemoglobina Hb. D Hb. C Hb. E Hb. S Hb. J
Polimorfismo balanceado Distribución del paludismo alrededor de 1950 Distribución actual del paludismo (Snow et al, 2005) Distribución de las principales variantes anormales de la hemoglobina Hb. D Hb. C Hb. E Hb. S Hb. J
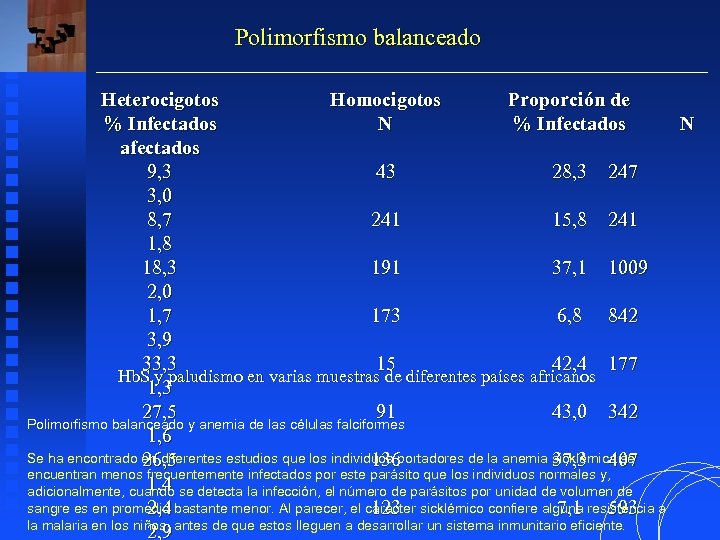 Polimorfismo balanceado Heterocigotos Homocigotos Proporción de % Infectados N afectados 9, 3 43 28, 3 247 3, 0 8, 7 241 15, 8 241 1, 8 18, 3 191 37, 1 1009 2, 0 1, 7 173 6, 8 842 3, 9 33, 3 15 42, 4 177 Hb. S y paludismo en varias muestras de diferentes países africanos 1, 3 27, 5 91 43, 0 342 Polimorfismo balanceado y anemia de las células falciformes 1, 6 Se ha encontrado en diferentes estudios que los individuos portadores de la anemia 37, 3 sicklémica se 26, 5 136 407 encuentran menos frecuentemente infectados por este parásito que los individuos normales y, 1, 4 adicionalmente, cuando se detecta la infección, el número de parásitos por unidad de volumen de sangre es en promedio bastante menor. Al parecer, el carácter sicklémico confiere alguna resistencia a 2, 4 123 7, 1 593 la malaria en los niños, antes de que estos lleguen a desarrollar un sistema inmunitario eficiente. 2, 9
Polimorfismo balanceado Heterocigotos Homocigotos Proporción de % Infectados N afectados 9, 3 43 28, 3 247 3, 0 8, 7 241 15, 8 241 1, 8 18, 3 191 37, 1 1009 2, 0 1, 7 173 6, 8 842 3, 9 33, 3 15 42, 4 177 Hb. S y paludismo en varias muestras de diferentes países africanos 1, 3 27, 5 91 43, 0 342 Polimorfismo balanceado y anemia de las células falciformes 1, 6 Se ha encontrado en diferentes estudios que los individuos portadores de la anemia 37, 3 sicklémica se 26, 5 136 407 encuentran menos frecuentemente infectados por este parásito que los individuos normales y, 1, 4 adicionalmente, cuando se detecta la infección, el número de parásitos por unidad de volumen de sangre es en promedio bastante menor. Al parecer, el carácter sicklémico confiere alguna resistencia a 2, 4 123 7, 1 593 la malaria en los niños, antes de que estos lleguen a desarrollar un sistema inmunitario eficiente. 2, 9
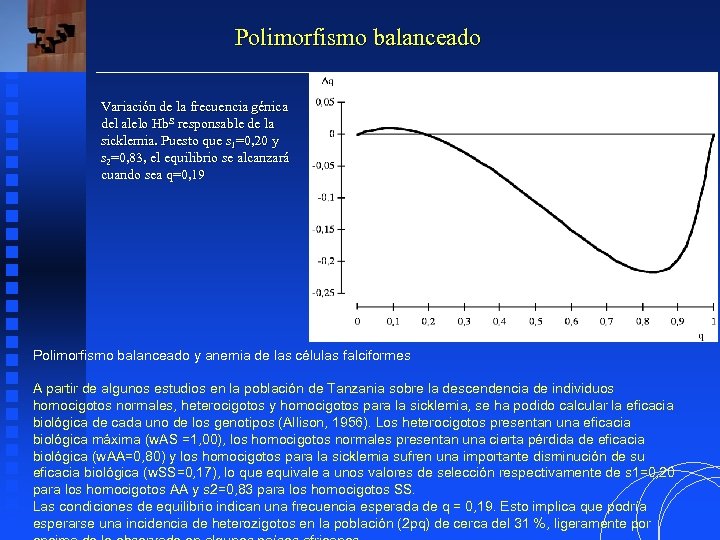 Polimorfismo balanceado Variación de la frecuencia génica del alelo Hb. S responsable de la sicklemia. Puesto que s 1=0, 20 y s 2=0, 83, el equilibrio se alcanzará cuando sea q=0, 19 Polimorfismo balanceado y anemia de las células falciformes A partir de algunos estudios en la población de Tanzania sobre la descendencia de individuos homocigotos normales, heterocigotos y homocigotos para la sicklemia, se ha podido calcular la eficacia biológica de cada uno de los genotipos (Allison, 1956). Los heterocigotos presentan una eficacia biológica máxima (w. AS =1, 00), los homocigotos normales presentan una cierta pérdida de eficacia biológica (w. AA=0, 80) y los homocigotos para la sicklemia sufren una importante disminución de su eficacia biológica (w. SS=0, 17), lo que equivale a unos valores de selección respectivamente de s 1=0, 20 para los homocigotos AA y s 2=0, 83 para los homocigotos SS. Las condiciones de equilibrio indican una frecuencia esperada de q = 0, 19. Esto implica que podría esperarse una incidencia de heterozigotos en la población (2 pq) de cerca del 31 %, ligeramente por
Polimorfismo balanceado Variación de la frecuencia génica del alelo Hb. S responsable de la sicklemia. Puesto que s 1=0, 20 y s 2=0, 83, el equilibrio se alcanzará cuando sea q=0, 19 Polimorfismo balanceado y anemia de las células falciformes A partir de algunos estudios en la población de Tanzania sobre la descendencia de individuos homocigotos normales, heterocigotos y homocigotos para la sicklemia, se ha podido calcular la eficacia biológica de cada uno de los genotipos (Allison, 1956). Los heterocigotos presentan una eficacia biológica máxima (w. AS =1, 00), los homocigotos normales presentan una cierta pérdida de eficacia biológica (w. AA=0, 80) y los homocigotos para la sicklemia sufren una importante disminución de su eficacia biológica (w. SS=0, 17), lo que equivale a unos valores de selección respectivamente de s 1=0, 20 para los homocigotos AA y s 2=0, 83 para los homocigotos SS. Las condiciones de equilibrio indican una frecuencia esperada de q = 0, 19. Esto implica que podría esperarse una incidencia de heterozigotos en la población (2 pq) de cerca del 31 %, ligeramente por
 Polimorfismo balanceado Esquema del funcionamiento de la proteína CFTR La fibrosis quística o mucoviscidosis es la más común entre las enfermedades de herencia recesiva. El gen responsable codifica para la proteína CFTR (abreviatura del inglés Cystic Fibrosis Transmembrane Regulator), cuyas alteraciones dan lugar a la enfermedad e interviene en el transporte de los iones cloruro (Cl-) a través de las membranas celulares. La enfermedad es altamente invalidante y a menudo mortal antes de la edad de 20 años. Se observan, sin embargo, diferentes grados de gravedad. Los niños afectados presentan un índice anormalmente alto de iones Cl- en su sudor, sufren una insuficiencia pancreática que acarrea trastornos digestivos y producen en los pulmones una mucosidad demasiado espesa que da origen a infecciones crónicas. No obstante, algunos niños (muy pocos), pueden presentar funciones pancreáticas normales (suficiencia pancreática), en cuyo caso sufren esencialmente la afección pulmonar. Otros, más raros todavía, no parecen presentar ninguna afección pulmonar, sino la llamada forma asintomática de la enfermedad.
Polimorfismo balanceado Esquema del funcionamiento de la proteína CFTR La fibrosis quística o mucoviscidosis es la más común entre las enfermedades de herencia recesiva. El gen responsable codifica para la proteína CFTR (abreviatura del inglés Cystic Fibrosis Transmembrane Regulator), cuyas alteraciones dan lugar a la enfermedad e interviene en el transporte de los iones cloruro (Cl-) a través de las membranas celulares. La enfermedad es altamente invalidante y a menudo mortal antes de la edad de 20 años. Se observan, sin embargo, diferentes grados de gravedad. Los niños afectados presentan un índice anormalmente alto de iones Cl- en su sudor, sufren una insuficiencia pancreática que acarrea trastornos digestivos y producen en los pulmones una mucosidad demasiado espesa que da origen a infecciones crónicas. No obstante, algunos niños (muy pocos), pueden presentar funciones pancreáticas normales (suficiencia pancreática), en cuyo caso sufren esencialmente la afección pulmonar. Otros, más raros todavía, no parecen presentar ninguna afección pulmonar, sino la llamada forma asintomática de la enfermedad.
 Polimorfismo balanceado GRUPO INCIDENCIA La fibrosis quística La mutación aparece sobre todo en caucasoides (es decir, poblaciones originarias de Europa, Africa del Norte y Próximo Oriente). En estas poblaciones se encuentra en una frecuencia muy elevada, con un valor promedio de 0, 02. De cada 2. 500 nacidos, uno está afectado, lo que significa que un individuo de cada 25 es portador sano de un ejemplar del gen CFTR mutado Caucasoides europeos Alemania Francia Inglaterra Irlanda del Norte Italia República Checa Suecia Caucasoides extraeuropeos Australia Hawaii Israel Sudáfrica USA No caucasoides Hawaii (orientales) Inglaterra (asiáticos) USA (negros) 1/3. 300 1/1. 800 1/2. 700 1/1. 800 1/2. 000 1/3. 000 1/7. 700 1/2. 500 1/3. 800 1/5. 000 1/6. 500 1/2. 800 1/90. 000 1/17. 000
Polimorfismo balanceado GRUPO INCIDENCIA La fibrosis quística La mutación aparece sobre todo en caucasoides (es decir, poblaciones originarias de Europa, Africa del Norte y Próximo Oriente). En estas poblaciones se encuentra en una frecuencia muy elevada, con un valor promedio de 0, 02. De cada 2. 500 nacidos, uno está afectado, lo que significa que un individuo de cada 25 es portador sano de un ejemplar del gen CFTR mutado Caucasoides europeos Alemania Francia Inglaterra Irlanda del Norte Italia República Checa Suecia Caucasoides extraeuropeos Australia Hawaii Israel Sudáfrica USA No caucasoides Hawaii (orientales) Inglaterra (asiáticos) USA (negros) 1/3. 300 1/1. 800 1/2. 700 1/1. 800 1/2. 000 1/3. 000 1/7. 700 1/2. 500 1/3. 800 1/5. 000 1/6. 500 1/2. 800 1/90. 000 1/17. 000
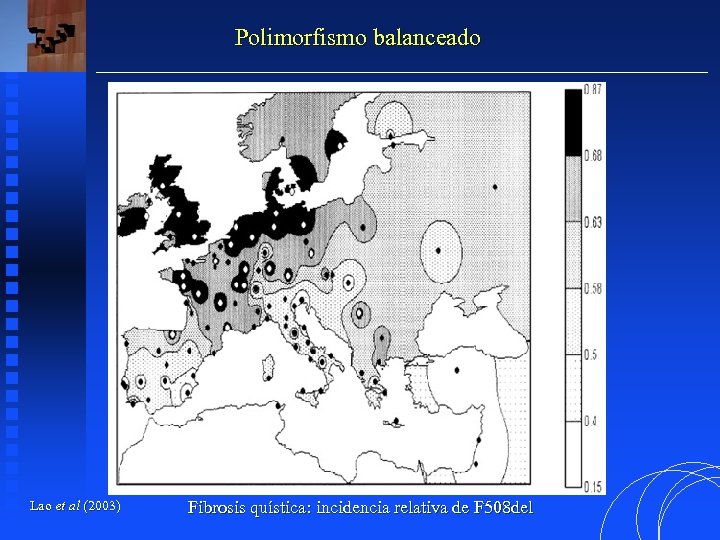 Polimorfismo balanceado Lao et al (2003) Fibrosis quística: incidencia relativa de F 508 del
Polimorfismo balanceado Lao et al (2003) Fibrosis quística: incidencia relativa de F 508 del
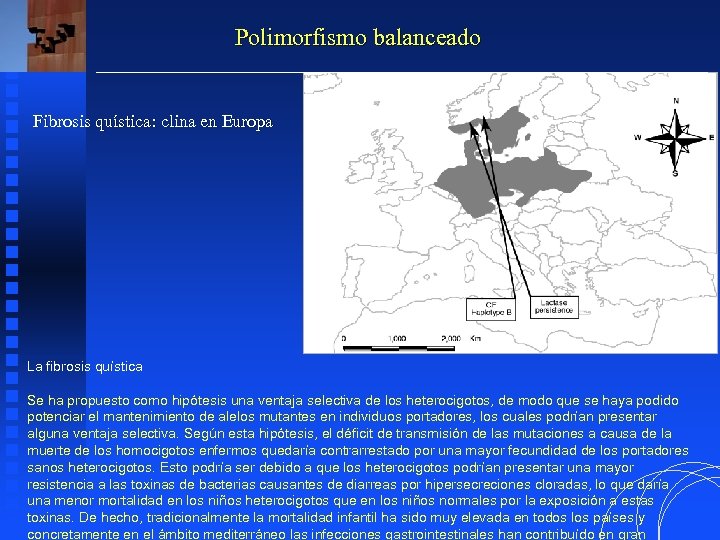 Polimorfismo balanceado Fibrosis quística: clina en Europa La fibrosis quística Se ha propuesto como hipótesis una ventaja selectiva de los heterocigotos, de modo que se haya podido potenciar el mantenimiento de alelos mutantes en individuos portadores, los cuales podrían presentar alguna ventaja selectiva. Según esta hipótesis, el déficit de transmisión de las mutaciones a causa de la muerte de los homocigotos enfermos quedaría contrarrestado por una mayor fecundidad de los portadores sanos heterocigotos. Esto podría ser debido a que los heterocigotos podrían presentar una mayor resistencia a las toxinas de bacterias causantes de diarreas por hipersecreciones cloradas, lo que daría una menor mortalidad en los niños heterocigotos que en los niños normales por la exposición a estas toxinas. De hecho, tradicionalmente la mortalidad infantil ha sido muy elevada en todos los países y concretamente en el ámbito mediterráneo las infecciones gastrointestinales han contribuído en gran
Polimorfismo balanceado Fibrosis quística: clina en Europa La fibrosis quística Se ha propuesto como hipótesis una ventaja selectiva de los heterocigotos, de modo que se haya podido potenciar el mantenimiento de alelos mutantes en individuos portadores, los cuales podrían presentar alguna ventaja selectiva. Según esta hipótesis, el déficit de transmisión de las mutaciones a causa de la muerte de los homocigotos enfermos quedaría contrarrestado por una mayor fecundidad de los portadores sanos heterocigotos. Esto podría ser debido a que los heterocigotos podrían presentar una mayor resistencia a las toxinas de bacterias causantes de diarreas por hipersecreciones cloradas, lo que daría una menor mortalidad en los niños heterocigotos que en los niños normales por la exposición a estas toxinas. De hecho, tradicionalmente la mortalidad infantil ha sido muy elevada en todos los países y concretamente en el ámbito mediterráneo las infecciones gastrointestinales han contribuído en gran
 Selección contra alelos del cromosoma X Si consideramos un locus dialélico, donde A es el alelo dominante, de frecuencia p, a el alelo recesivo, de frecuencia q, s es la desventaja selectiva de los varones hemizigotos a y H la proporción de mujeres heterocigotas, entonces pueden expresarse las frecuencias genotípicas en ambos sexos del siguiente modo GENOTIPO Mujeres AA Aa aa Varones A a EFICACIA BIOLÓGICA FRECUENCIA 1 1 <1 1 -H H 0 1 1 -s p q
Selección contra alelos del cromosoma X Si consideramos un locus dialélico, donde A es el alelo dominante, de frecuencia p, a el alelo recesivo, de frecuencia q, s es la desventaja selectiva de los varones hemizigotos a y H la proporción de mujeres heterocigotas, entonces pueden expresarse las frecuencias genotípicas en ambos sexos del siguiente modo GENOTIPO Mujeres AA Aa aa Varones A a EFICACIA BIOLÓGICA FRECUENCIA 1 1 <1 1 -H H 0 1 1 -s p q
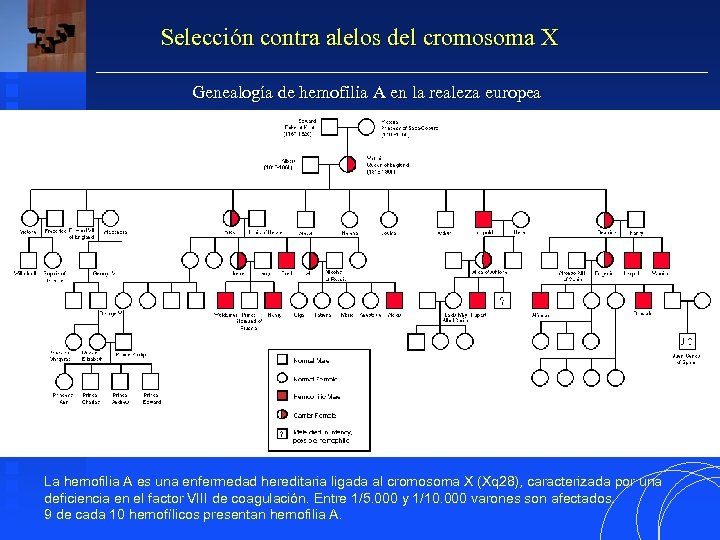 Selección contra alelos del cromosoma X Genealogía de hemofilia A en la realeza europea La hemofilia A es una enfermedad hereditaria ligada al cromosoma X (Xq 28), caracterizada por una deficiencia en el factor VIII de coagulación. Entre 1/5. 000 y 1/10. 000 varones son afectados. 9 de cada 10 hemofílicos presentan hemofilia A.
Selección contra alelos del cromosoma X Genealogía de hemofilia A en la realeza europea La hemofilia A es una enfermedad hereditaria ligada al cromosoma X (Xq 28), caracterizada por una deficiencia en el factor VIII de coagulación. Entre 1/5. 000 y 1/10. 000 varones son afectados. 9 de cada 10 hemofílicos presentan hemofilia A.


