

БЫСТРОПРОГРЕССИРУЮЩИЙ ГЛОМЕРУЛОНЕФРИТ

БЫСТРОПРОГРЕССИРУЮЩИЙ ГЛОМЕРУЛОНЕФРИТ БЫСТРОПРОГРЕССИРУЮЩИЙ НЕФРИТИЧЕСКИЙ СИНДРОМ – клинико-морфологический синдром, вариант течения различных ГН с быстрым развитием почечной недостаточности

БЫСТРОПРОГРЕССИРУЮЩИЙ НЕФРИТИЧЕСКИЙ СИНДРОМ Характеризуется: o Быстронарастающей почечной недостаточностью (увеличение s. Cr в ≥ 2 раз каждые 3 месяца или s. Cr>0, 178 ммоль/л) o В анализах мочи - протеинурия (обычно субнефротического уровня) c «богатым» мочевым осадком (часто как трансформация ОНС в БПНС) o Морфологическая основа – гломерулонефрит с полуниями в более чем 50% клубочков o При отсутствии лечения - ТПН у 90% в течение 1 года
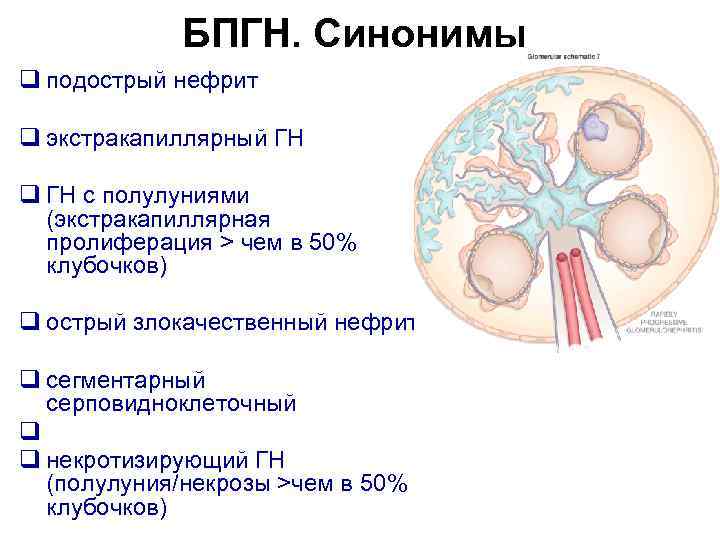
БПГН. Синонимы q подострый нефрит q экстракапиллярный ГН q ГН с полулуниями (экстракапиллярная пролиферация > чем в 50% клубочков) q острый злокачественный нефрит q сегментарный серповидноклеточный q q некротизирующий ГН (полулуния/некрозы >чем в 50% клубочков)
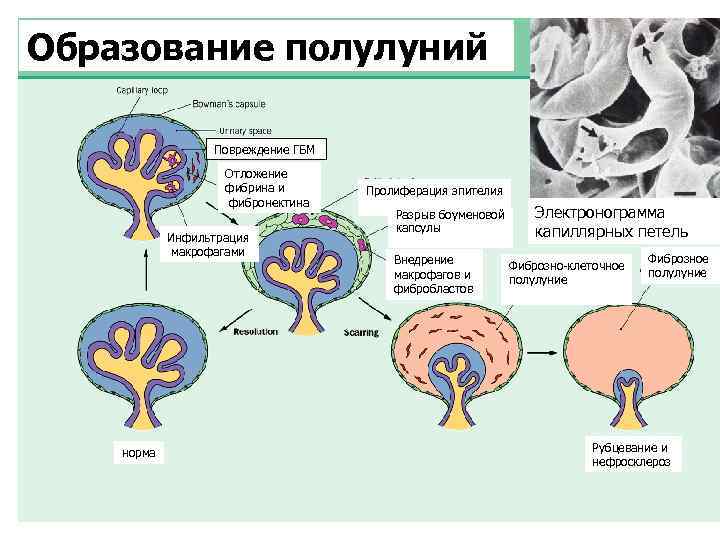
Образование полулуний Повреждение ГБМ Отложение фибрина и фибронектина Инфильтрация макрофагами норма Пролиферация эпителия Разрыв боуменовой капсулы Внедрение макрофагов и фибробластов Электронограмма капиллярных петель Фиброзно-клеточное полулуние Фиброзное полулуние Рубцевание и нефросклероз
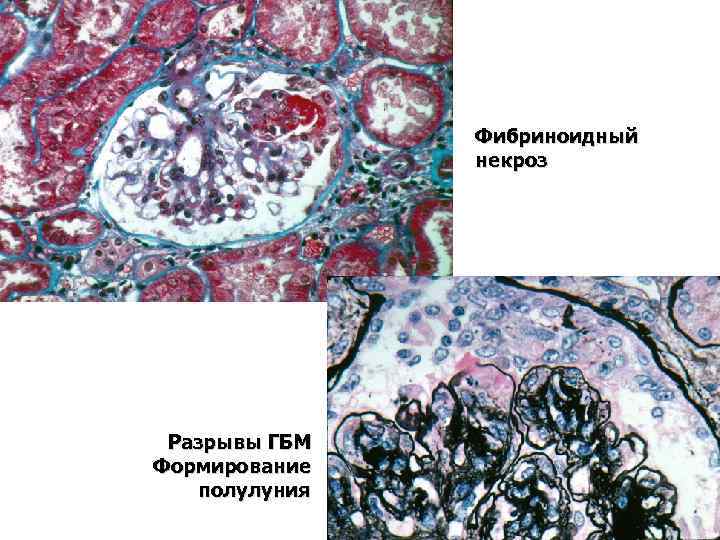
Фибриноидный некроз Разрывы ГБМ Формирование полулуния
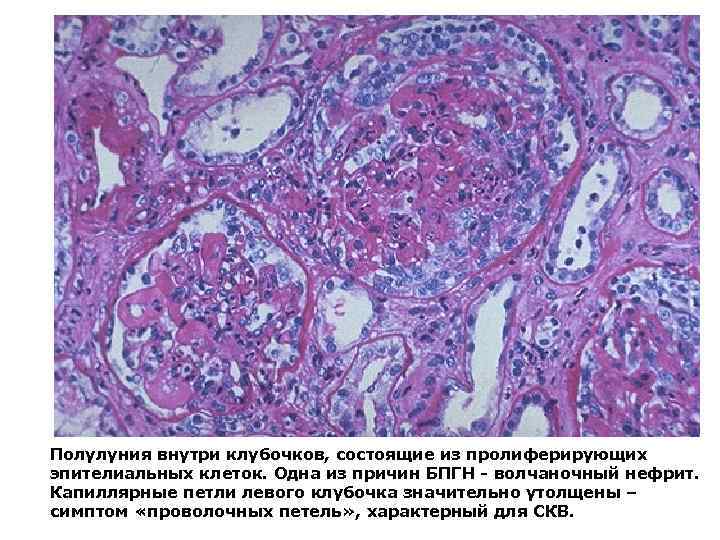
Полулуния внутри клубочков, состоящие из пролиферирующих эпителиальных клеток. Одна из причин БПГН - волчаночный нефрит. Капиллярные петли левого клубочка значительно утолщены – симптом «проволочных петель» , характерный для СКВ.
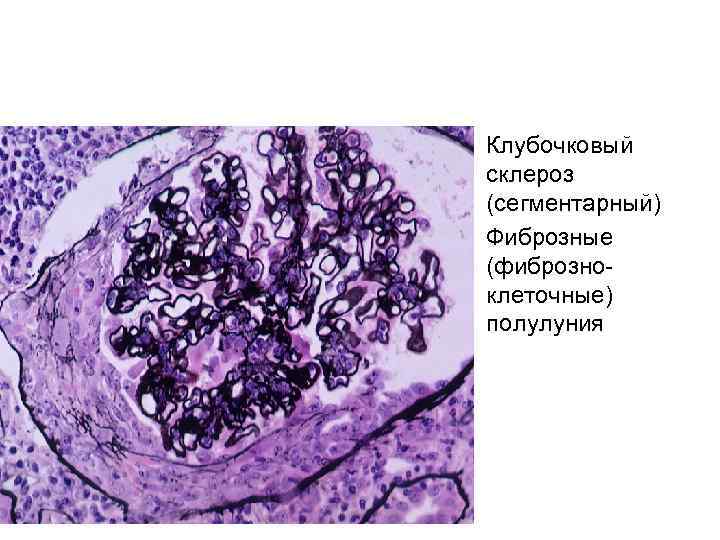
• Клубочковый склероз (сегментарный) • Фиброзные (фиброзноклеточные) полулуния
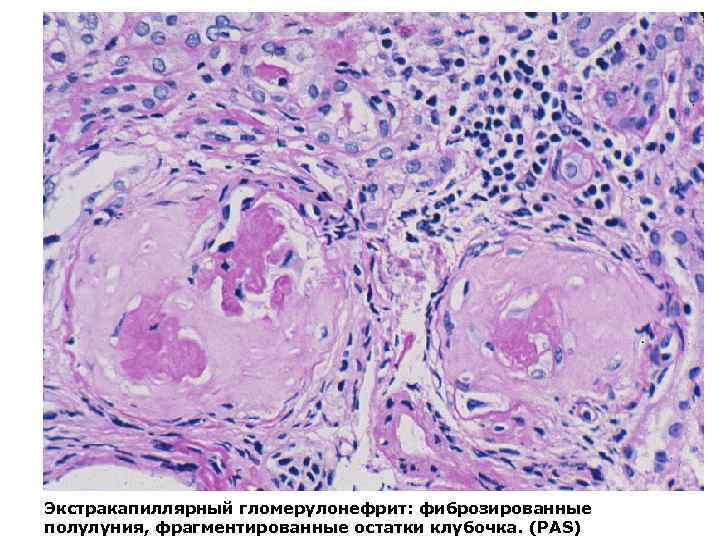
Экстракапиллярный гломерулонефрит: фиброзированные полулуния, фрагментированные остатки клубочка. (PAS)

Классификация (Glassock, 1997) • Тип I ( «анти-ГБМ нефрит» ) появление АТ к ГБМ. Характеризуется «линейным» свечением АТ в почечном биоптате и наличием циркулирующих АТ к ГБМ в сыворотке крови. • Тип II ( «иммунокомплексный» ) – иммунные депозиты в мезангии и капиллярной стенке В почечном биоптате - «гранулярный» тип свечения, у многих больных снижен уровень комплемента (анти-ГБМ-АТ и АНЦА отсутствуют в сыворотке). Наиболее характерен для БПГН, связанных с инфекциями (инфекционный эндокардит), криоглобулинемический ГН, люпус-нефрит класс 4. • Тип III ( «малоиммунный» ) – повреждение вызывается нейтрофилами и моноцитами, активированными АНЦА. Свечение Ig и комплемента в биоптате отсутствует (pauci-immune, «малоиммунный» ГН), в сыворотке выявляются АНЦА, направленные к протеиназе-3 (анти-ПР 3) или миелопероксидазе (анти-МПО). Этот тип почечного поражения является проявлением АНЦА- ассоциированных васкулитов мелких сосудов.
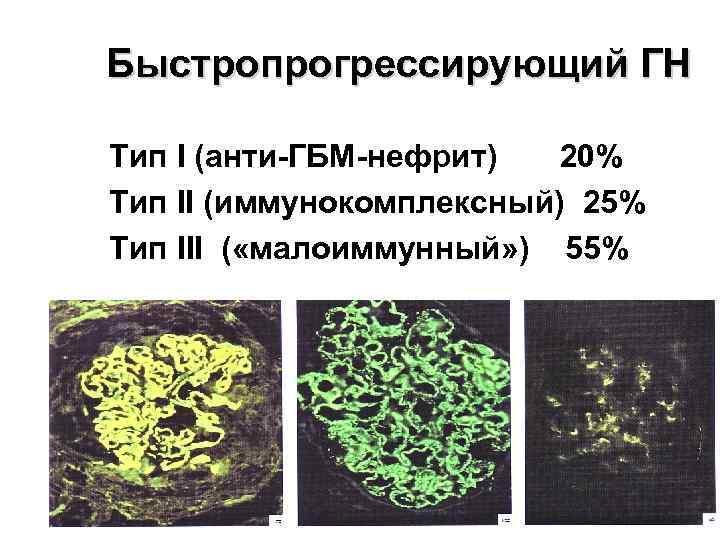
Быстропрогрессирующий ГН Тип I (анти-ГБМ-нефрит) 20% Тип II (иммунокомплексный) 25% Тип III ( «малоиммунный» ) 55%
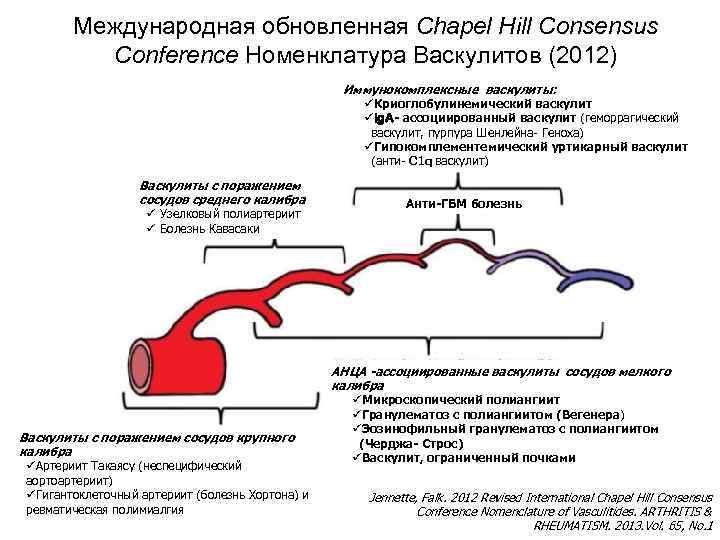
Международная обновленная Chapel Hill Consensus Conference Номенклатура Васкулитов (2012) Иммунокомплексные васкулиты: üКриоглобулинемический васкулит üIg. A- ассоциированный васкулит (геморрагический васкулит, пурпура Шенлейна- Геноха) üГипокомплементемический уртикарный васкулит (анти- C 1 q васкулит) Васкулиты с поражением сосудов среднего калибра ü Узелковый полиартериит ü Болезнь Кавасаки Васкулиты с поражением сосудов крупного калибра üАртериит Такаясу (неспецифический аортоартериит) üГигантоклеточный артериит (болезнь Хортона) и ревматическая полимиалгия Анти-ГБМ болезнь АНЦА -ассоциированные васкулиты сосудов мелкого калибра üМикроскопический полиангиит üГранулематоз с полиангиитом (Вегенера) üЭозинофильный гранулематоз с полиангиитом (Черджа- Строс) üВаскулит, ограниченный почками Jennette, Falk. 2012 Revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. ARTHRITIS & RHEUMATISM. 2013. Vol. 65, No. 1

Анти-ГБМ болезнь – васкулит, поражающий клубочковые или легочные капилляры, или те и другие вместе, • с депозитами ауто-АТ к базальной мембране. • Поражение легких вызывает кровохарканье, почек - ГН с некрозами и полулуниями (CHCC 2012). • Достигнут консенсус относительно названия «Анти-ГБМ болезнь» при пересмотре номенклатуры • Термин «Синдром Гудпасчура” использовался ранее для обозначения анти-ГБМ болезни с с почечно-легочным поражением J. Jennette, R. Falk et al. 2012 Revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. ARTHRITIS & RHEUMATISM Vol. 65, No. 1, 2013, pp 1– 11

Ernest Goodpasture (1886 – 1960) В 1919 – опубликовал аутопсийные данные 18 летнего больного, который умер от геморрагической пневмонии, сочетавшейся с поражением почек – синдром Гудпасчура В середине 1960 -х годов у части больных БПГН, сочетающимся с легочным кровотечением, были обнаружены анти-ГБМ АТ и доказана их патогенность (анти-ГБМ нефрит)

Анти-ГБМ болезнь – аутоиммунная болезнь, связанная с образованием ауто-АТ к неколлагеновому домену (NC 1) α 3 цепи коллагена IV типа в составе ГБМ. • 2 нефритогенных эпитопа известны как EA и EB. • Эпитопы обычно спрятаны в Коллаген IV типа состоит из 6 гексамере NC 1 доменов и, как цепей (a 1 –а 6), которые собираются в тройные спиральные конфигурации считают, обнажаются после – протомеры. Каждая спираль воздействия токсинов (напр. , табака, состоит из 3 доменов: 1) 7 S домен на N-конце, летучих углеводородов) или инфекции, известных как триггеры 2) коллагеновый - в центре, на 3) неколлагеновый домен (NC 1) развития болезни. С-конце. • Генетические факторы участвуют в NC 1 и 7 S домены спиралей соединяются, образуя сеть. развитии болезни: HLA аллели DR 15 и Эпитопы EA и EB, встроенные внутри NCI домена цепи а. З DR 4 предрасполагают к болезни, а являются антигенной мишенью для DR 7 и DR 1 - защищают от нее АТ при анти-ГБМ болезни

Патогенез • Связывание анти-ГБМ АТ с Аг ГБМ вызывает активацию комплемента с развитием бурного воспаления, в процессе которого происходят разрывы ГБМ в петлях клубочка. • Полулуния - следствие разрывов ГБМ и проникновения плазменных белков и воспалительных клеток в пространство капсулы Шумлянского. Боумена. • Клеточный состав полулуний представлен пролиферирующим париетальным эпителием и макрофагами (МФ). • Эволюция полулуний – обратное развитие или фиброз - зависит от степени накопления МФ в пространстве капсулы и ее структурной целостности. • Преобладание в клеточных полулуниях МФ сопровождается разрывом капсулы, последующим поступлением из интерстиция фибробластов и миофибробластов, синтезом ими матриксных белков – коллагенов I и III типов, фибронектина, что ведет к необратимому фиброзу полулуний.

Анти-ГБМ болезнь • Частота 1: 1 млн населения/год • Развивается в любом возрасте, пик – 3 -я и 6 -7 декады • У молодых обычно возникает внезапно с кровохарканья, резкого падения Hb (не зависит от выраженности кровохарканья), лихорадки, одышки и гематурии. • Иногда провоцируется инфекцией или токсическим агентом. • Основные симптомы – кровохарканье или проявления почечной недостаточности • Кровохарканья в основном бывает у курильщиков, сейчас наблюдается в ~ 50%; • начало с кровохарканья ассоциируется с лучшим исходом (более раннее выявление).

Клиника -1 • Кровохарканье – 1 -й симптом болезни почти в 50 -70%, как правило, на несколько месяцев опережающий признаки поражения почек. • Начало легочного поражения может быть острым, включая массивное кровотечение, удушье и смерть, или симптомы - кровохарканье, одышка, кашель, лихорадка, тахикардия и слабость - возникают повторно на протяжении недель и месяцев прежде, чем будет установлен диагноз. • БПГН дебютирует с ОНС (эволюция от N функции до появления ОПП у может составлять <12 ч) с переходом в БПНС, развитием ТПН в пределах года. • Фатальная потеря функции может развиться за 1 -2 нед • Редко - постепенное, бессимптомное, медленно прогрессирующее течение, пока не появятся уремические симптомы.

Клиника-2 • Начало с олигоурии ассоциируется с плохим исходом • Протеинурия обычно <3 г/сут • У некоторые – макрогематурия, сильные боли в пояснице, что м. б. признаком тяжелой болезни • Без лечения анти-ГБМ болезнь почти всегда прогрессирует до ТПН • и в настоящее время смертность в остром периоде болезни варьирует от 10 до 40% • Синтез анти-ГБМ АТ временный, часто длится <2 мес. • Рецидивы анти –ГБМ – редко • трансплантацию выполняют, когда АТ уже не определяются (минимум через 6 мес после исчезновения АТ)

Диагностика анти-ГБМ болезни Диагноз устанавливается при • выявлении АТ (к α 3 NC 1 домену коллагена IV) в циркуляции и/или • данных нефробиопсии • Имеется корреляция между титром анти-ГБМ АТ и тяжестью почечного поражения (? ? ? ); • степень поражения легких не зависит от титра АТ • Другие показатели неспецифичны • У 10 -15% пациентов также находят АНЦА АТ направленные против МПО (эта подгруппа больных с АНЦА -ассоциированным вариантом имеет лучший!! прогноз при лечении) • Rg легких – N или альвеолярное затенение (признаки появляются и исчезают быстрее, чем при инфекции)

Почки у больных быстропрогрессирующим гломерулонефритом чаще бывают увеличены в размерах (иногда до 13 -14 см по УЗИ), бывают и нормальных размеров, но никогда – уменьшенными
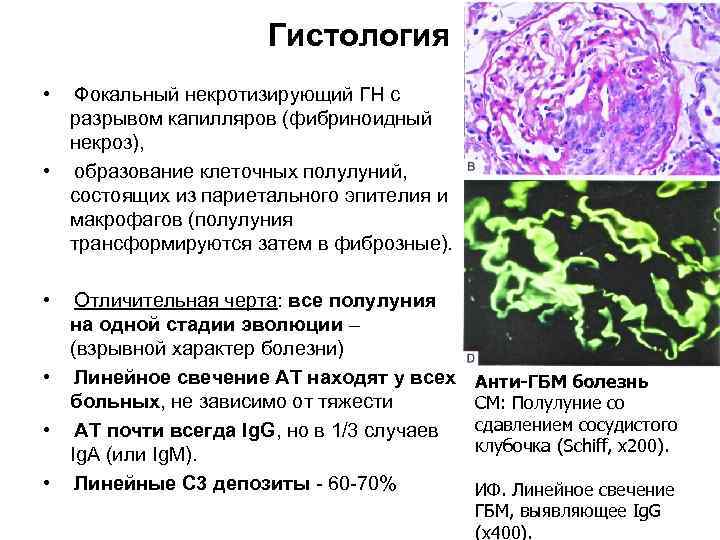
Гистология • Фокальный некротизирующий ГН с разрывом капилляров (фибриноидный некроз), • образование клеточных полулуний, состоящих из париетального эпителия и макрофагов (полулуния трансформируются затем в фиброзные). • Отличительная черта: все полулуния на одной стадии эволюции – (взрывной характер болезни) • Линейное свечение АТ находят у всех больных, не зависимо от тяжести • АТ почти всегда Ig. G, но в 1/3 случаев Ig. A (или Ig. M). • Линейные C 3 депозиты - 60 -70% Анти-ГБМ болезнь СМ: Полулуние со сдавлением сосудистого клубочка (Schiff, x 200). ИФ. Линейное свечение ГБМ, выявляющее Ig. G (x 400).

Дифференциальный диагноз проводят между заболеваниями, способными вызвать ОНС с БПНС, особенно при сочетании с легочным поражением: • АНЦА-ассоциированные васкулиты (гранулематозный полиангиит, или Вегенера, микроскопический полиангиит), • криоглобулинемический ГН, • инфекция -ассоциированные ГН (ОПСГН, при инфекционный эндокардит), • люпус-нефрит, • пурпурой Шенлейн-Геноха, БЛЦ, • острым тубулоинтерстциальным нефритом, канальцевым некрозом. • Выявление анти-ГБМ АТ делает диагноз очень вероятным, но их также находят у небольшой части больных с АНЦА-васкулитами • АНЦА чаще анти-МПО, титр обычно ниже, а анти-ГБМ АТ у них легче подавляются. Почечная функция может восстановиться, даже если ОПП была очень тяжелой при выявлении
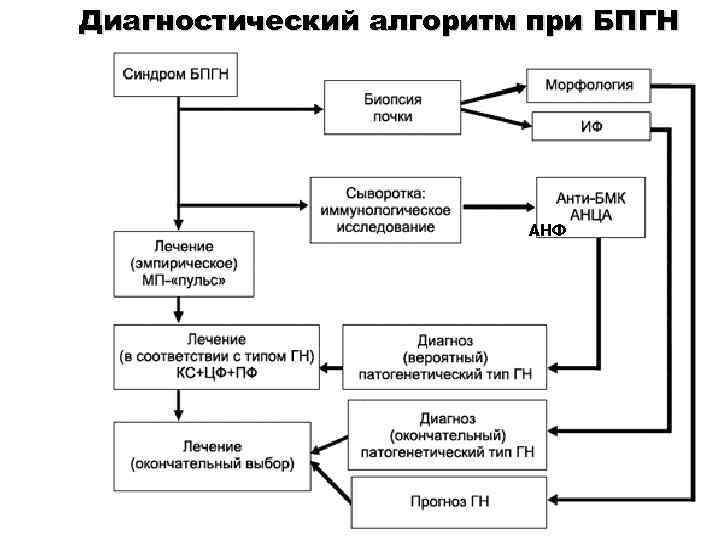
Диагностический алгоритм при БПГН АНФ

Лечение анти-ГБМ ГН Всем пациентам ЦФ+ КС + плазмаферез (е/дневно в течение 14 дней или до тех пор, пока АТ не исчезнут) Исключение: • Диализ-зависимые пациенты на момент диагноза, 100% полулуний и без легочных кровотечений. Лечение следует начинать безотлагательно, как только диагноз подтвержден. • Если имеется высокий индекс подозрения, целесообразно начать лечение высокими дозами КС и плазмаферезом и проводить его пока диагноз не будет подтвержден • Поддерживающая иммуносупрессивная терапия при анти -ГБМ ГН не проводится. (ID) • Трансплантацию почки следует отложить на 6 мес после исчезновения анти-ГБМ АТ в сыворотке

KDIGO, 2012 Поддерживающая иммуносупрессивная терапия при анти-ГБМ ГН более 6 мес не проводится

Прогноз плохой, если • • в нефробиоптате >50% фиброзных полулуний, s. Сr >0, 6 ммоль/л, Олигоурия в дебюте или потребность в ОГД При наличии этих факторов большинство никогда не восстанавливают функцию при терапии КС и плазаферезом. • Пациенты с тяжелой ПН и кровохарканьем нуждаются в продолжении лечения, т. к. угрожающие легочные кровотечения отвечают на лечение плазаферезом. • Обострения синдрома Гудпасчера после успешного лечения первого эпизода бывают крайне редко

Иммуно-морфологическая дифдиагностика МБПГН • При БПД только в 25% случаев при СМ выявляются типичные признаки МБПГН; • в 44% диагностируется МЗПГН, • в 17% ГН с полулуниями, в • 11% - о. экссудативно-пролиферативный ГН, а в • 3% морфологические признаки не поддаются классификации. • Поэтому в основу современной классификации МБПГН положены сведения об иммунопатогенезе, о которых можно судить по данным ИФ. • На основании анализа депозитов Ig и фракций комплемента выделяют МБПГН Ig+ и МБПГН Ig-, далее С 3 + и С 3 (-)

Дифференциальный диагноз Болезни, протекающие с ОПП и острой легочной недостаточностью • • Отек легких, вторичный к ОПП любой другой этиологии Тяжелая СН с легочной гипоперфузией и легочным отеком Тяжелая пневмония (напр. , Legionello) , ассоциированная с ОТН Системные васкулиты- ГПА, МПА, ЧСС Вторичные васкулиты – СКВ, РА, Бехчета, криоглобулинемии Почечный венозный тромбоз с ТЭЛА Отравление гербицидами Тромботическая микроангиопатия (гемолитико-уремический синдром) с острым легочным синдромом. • Выявление анти-ГБМ АТ делает диагноз очень вероятным, но их также находят у небольшой части больных с АНЦА-васкулитами • АНЦА чаще анти-МПО, титр обычно ниже, а анти-ГБМ АТ у них легче подавляются. Почечная функция может восстановиться, даже если ОПП была очень тяжелой при выявлении

Этиология и патогенез С 3 гломерулопатии (прод. ) Причина того факта, что в одном случае С 3 -позитивной гломерулопатии формируется морфологическая картина МБПГН I или III типа, а в другом – выявляется БПД, остается невыясненной. • При моноклональных гаммапатиях, при которых обычно формируется иммуноглобулин-позитивный МБПГН (для которого характерен классический путь активации комплемента), недавно был открыт иной путь патогенеза. • Оказалось, что моноклональный Ig может действовать как АТ к фактору Н и к другим регуляторным протеинам, приводя к дисрегуляции альтернативного пути комплемента и к формированию С 3 -позитивной гломерулопатии. •

Этиология иммуноглобулин- и С 3 негативного МБПГН • заключается в первичном поражении эндотелиоцитов (тромботическая микроангиопатия, синдром злокачественной гипертензии и др. ), за которым следует репаративная фаза в форме пролиферативных изменений в клубочке, идентифицируемых светооптически, как МБПГН. • При ЭМ в этих случаях не выявляются электронноплотные депозиты, а следовательно, установить тип МБПГН не представляется возможным
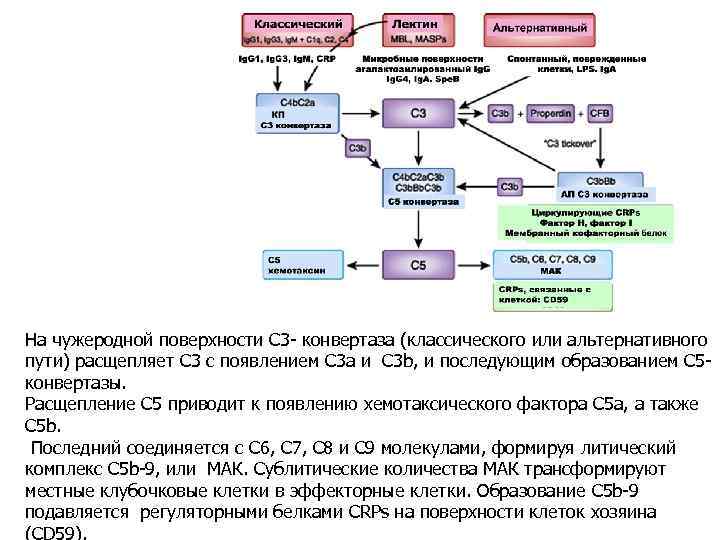
На чужеродной поверхности С 3 - конвертаза (классического или альтернативного пути) расщепляет С 3 с появлением C 3 a и C 3 b, и последующим образованием С 5 конвертазы. Расщепление С 5 приводит к появлению хемотаксического фактора C 5 a, а также C 5 b. Последний соединяется с C 6, C 7, C 8 и C 9 молекулами, формируя литический комплекс C 5 b-9, или МАК. Сублитические количества МАК трансформируют местные клубочковые клетки в эффекторные клетки. Образование C 5 b-9 подавляется регуляторными белками CRPs на поверхности клеток хозяина (CD 59).
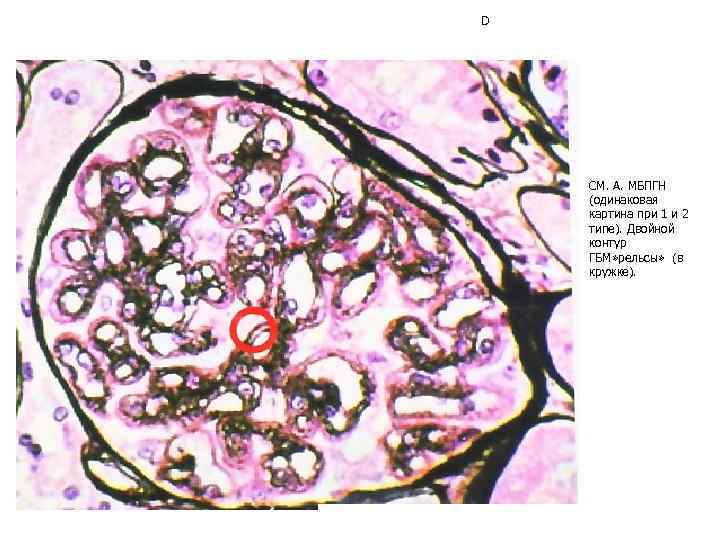
D СМ. А. МБПГН (одинаковая картина при 1 и 2 типе). Двойной контур ГБМ» рельсы» (в кружке).
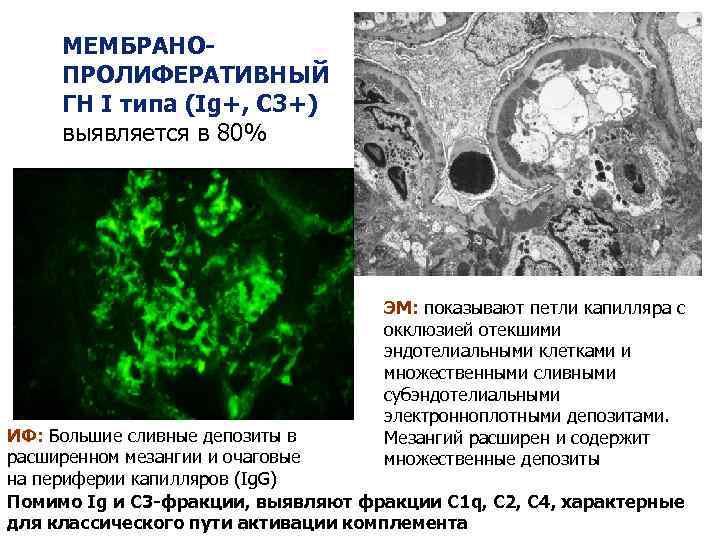
МЕМБРАНОПРОЛИФЕРАТИВНЫЙ ГН I типа (Ig+, C 3+) выявляется в 80% ЭМ: показывают петли капилляра с окклюзией отекшими эндотелиальными клетками и множественными сливными субэндотелиальными электронноплотными депозитами. Мезангий расширен и содержит множественные депозиты ИФ: Большие сливные депозиты в расширенном мезангии и очаговые на периферии капилляров (Ig. G) Помимо Ig и С 3 -фракции, выявляют фракции С 1 q, С 2, С 4, характерные для классического пути активации комплемента Ig. G

Трансплантационная гломерулопатия занимает особое место. • Долгое время ее рассматривали с точки зрения механизмов хронического отторжения трансплантата • Теперь выделяют в самостоятельную нозологическую единицу с иммунным патогенезом. • Первоначально - повреждение эндотелиоцитов ауто-АТ к антигенам HLA- II класса, которые присутствуют на наружной клеточной мембране эндотелиальных клеток. • В острой фазе развивается, т. н. , гломерулит, характеризующийся повреждением капилляров мигрирующими из крови, мононуклеарами и нейтрофилами. • Острую, экссудативную реакцию в клубочке (гломерулит) сменяет репаративная фаза, в которую происходит пролиферация и экспансия Мз матрикса, развивается дупликация ГБМ, и морфологическая картина при СМ становится аналогичной МБПГН Ig+. • При ИФ регистрируется отложение вдоль петель капилляров клубочка С 4 d - продукта активации комплемента по классическому пути
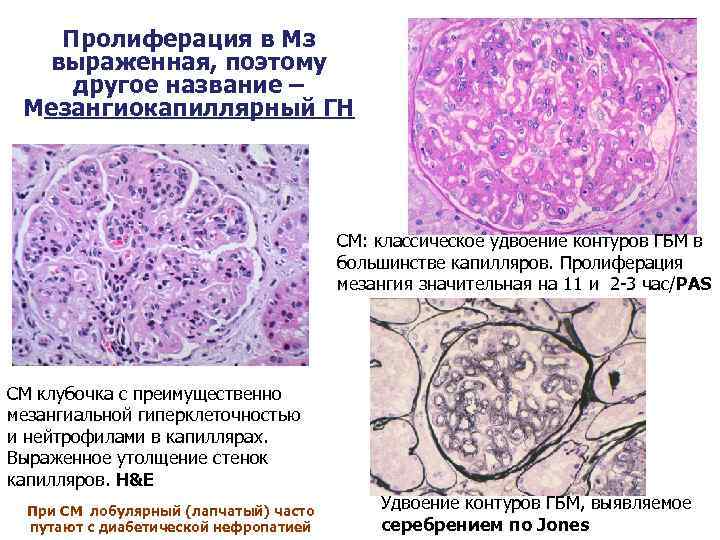
Пролиферация в Мз выраженная, поэтому другое название – Мезангиокапиллярный ГН СМ: классическое удвоение контуров ГБМ в большинстве капилляров. Пролиферация мезангия значительная на 11 и 2 -3 час/PAS СМ клубочка с преимущественно мезангиальной гиперклеточностью и нейтрофилами в капиллярах. Выраженное утолщение стенок капилляров. H&E При СМ лобулярный (лапчатый) часто путают с диабетической нефропатией Удвоение контуров ГБМ, выявляемое серебрением по Jones
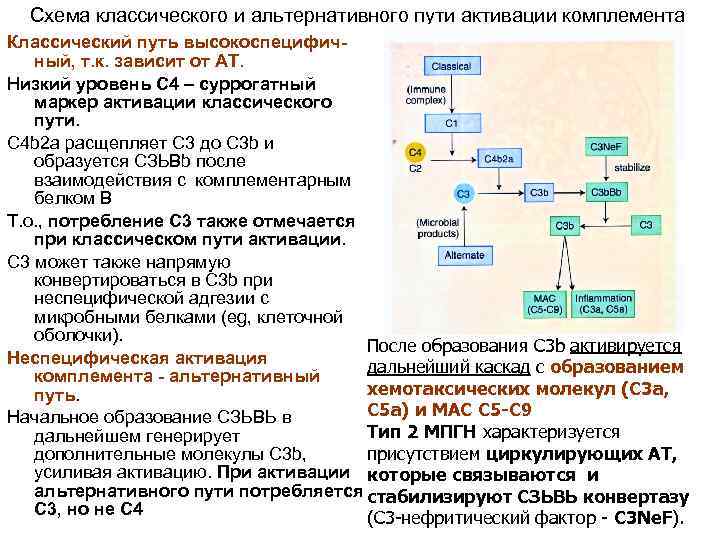
Схема классического и альтернативного пути активации комплемента Классический путь высокоспецифичный, т. к. зависит от АТ. Низкий уровень C 4 – суррогатный маркер активации классического пути. C 4 b 2 a расщепляет C 3 до C 3 b и образуется СЗЬВb после взаимодействия с комплементарным белком В Т. о. , потребление С 3 также отмечается при классическом пути активации. C 3 может также напрямую конвертироваться в C 3 b при неспецифической адгезии с микробными белками (eg, клеточной оболочки). После образования C 3 b активируется Неспецифическая активация дальнейший каскад с образованием комплемента - альтернативный хемотаксических молекул (C 3 a, путь. C 5 a) и MAC C 5 -C 9 Начальное образование СЗЬВЬ в Тип 2 МПГН характеризуется дальнейшем генерирует присутствием циркулирующих АТ, дополнительные молекулы C 3 b, усиливая активацию. При активации которые связываются и альтернативного пути потребляется стабилизируют СЗЬВЬ конвертазу C 3, но не С 4 (С 3 -нефритический фактор - C 3 Ne. F).
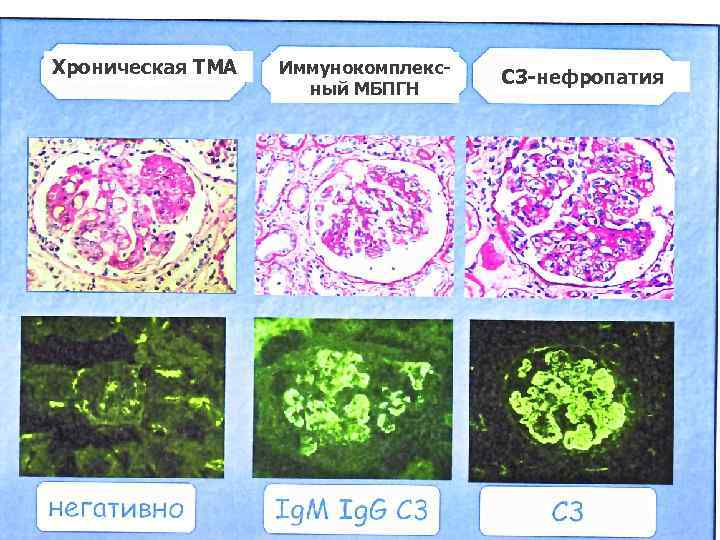
Хроническая ТМА Иммунокомплексный МБПГН С 3 -нефропатия
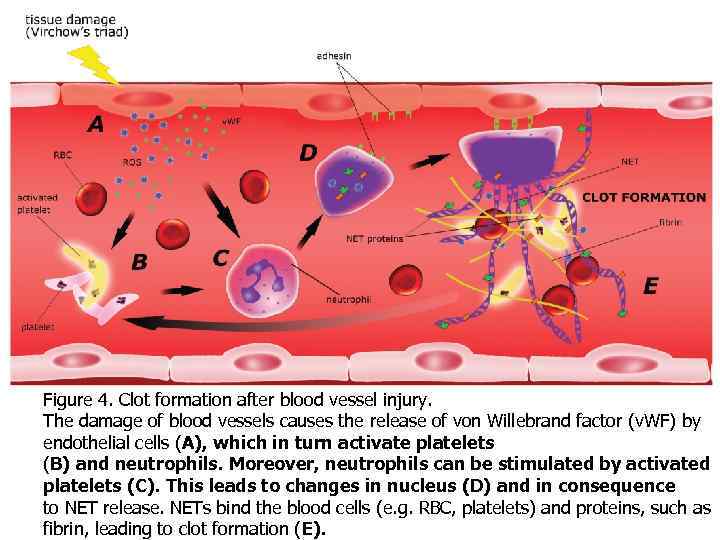
Figure 4. Clot formation after blood vessel injury. The damage of blood vessels causes the release of von Willebrand factor (v. WF) by endothelial cells (A), which in turn activate platelets (B) and neutrophils. Moreover, neutrophils can be stimulated by activated platelets (C). This leads to changes in nucleus (D) and in consequence to NET release. NETs bind the blood cells (e. g. RBC, platelets) and proteins, such as fibrin, leading to clot formation (E).
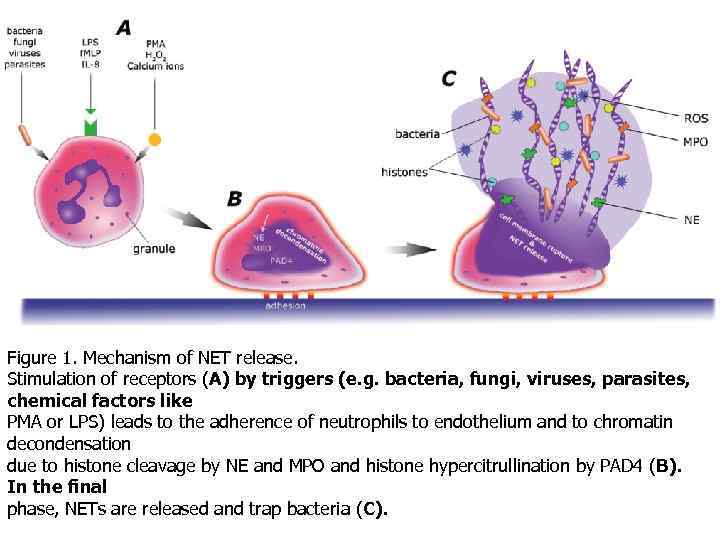
Figure 1. Mechanism of NET release. Stimulation of receptors (A) by triggers (e. g. bacteria, fungi, viruses, parasites, chemical factors like PMA or LPS) leads to the adherence of neutrophils to endothelium and to chromatin decondensation due to histone cleavage by NE and MPO and histone hypercitrullination by PAD 4 (B). In the final phase, NETs are released and trap bacteria (C).
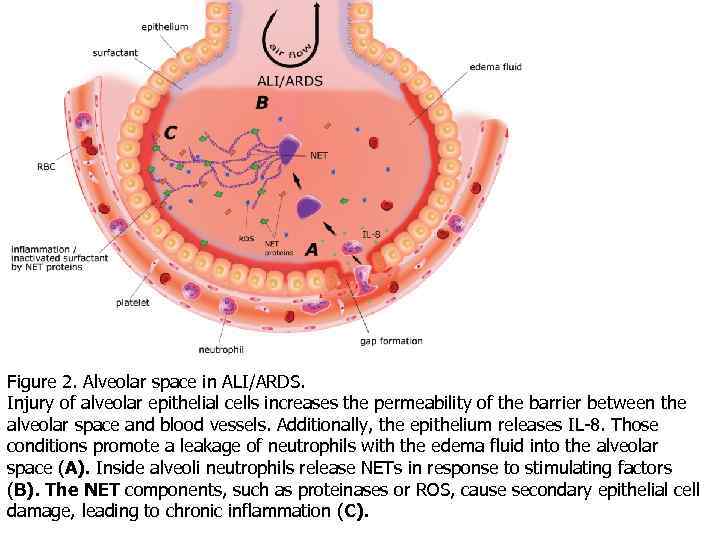
Figure 2. Alveolar space in ALI/ARDS. Injury of alveolar epithelial cells increases the permeability of the barrier between the alveolar space and blood vessels. Additionally, the epithelium releases IL-8. Those conditions promote a leakage of neutrophils with the edema fluid into the alveolar space (A). Inside alveoli neutrophils release NETs in response to stimulating factors (B). The NET components, such as proteinases or ROS, cause secondary epithelial cell damage, leading to chronic inflammation (C).