буферные системы.pptx
- Количество слайдов: 22

БУФЕРНЫЕ РАСТВОРЫ ПЛАН: q Определение, классификация q механизм буферного действия q буферная емкость q зона буферного действия q буферные системы крови

Буферный раствор – это раствор, содержащий протолитическую равновесную систему, способную поддерживать практически постоянное значение р. Н при разбавлении или при добавлении небольших количеств кислоты или щелочи.

КОМПОНЕНТЫ: донор протона и акцептор протона, представляющие собой сопряженную кислотноосновную пару.

Классификация I тип. Кислотная буферная система: слабая кислота и её анион; в растворе слабая кислота и её соль. Примеры: ацетатный буфер: CН 3 СООН / СН 3 СОО–, в растворе CН 3 СООН и CН 3 СООNa гидрокарбонатный буфер: Н 2 СО 3 / НСО 3–, в растворе Н 2 СО 3 и Na. HCO 3 гемоглобиновый буфер: HHb / Нb–, в растворе НHb и KHb НHb. O 2 / Нb. О 2–, в растворе НHb. O 2 и KHb. O 2

II тип. Основная буферная система слабое основание и её катион; в растворе слабое основание и её соль Примеры: аммиачный буфер: NН 3 / NН 4+, в растворе NН 3 и NН 4 Сl

III тип. Солевая буферная система: анионы кислой и средней соли или анионы двух кислых солей; в растворе кислая и средняя соль или две кислые соли с различной степенью замещения протона. Примеры: гидрофосфатный буфер: Н 2 РО 4– / НРО 42–, в растворе Na. Н 2 РО 4 и Na 2 НРО 4 карбонатный буфер: НСО 3– / СО 32–, в растворе Na. НСО 3 и Na 2 CO 3

IV тип. Амфотерная органическая буферная система: ионы и молекулы амфолитов. Примеры: аминокислотный буфер: белковый (протеиновый) буфер: анионный – HProt / (Prot)– катионный – (Н 2 Prot)+ / HРrot

Механизм буферного действия Уравнение буферной системы р. Н = р. Ка – ℓg р. Н зависит от соотношения концентраций компонентов и величины р. Ка Для кислотной буферной системы р. Ка - показатель константы диссоциации слабой кислоты Для основной буферной системы р. Ка - показатель константы диссоциации сопряженной кислоты

При разбавлении: Ка не изменяется концентрации всех компонентов , а соотношение их не меняется ⇒ р. Н не изменится Добавление сильной кислоты или щелочи Н+ связывает акцептор протона ОН– связывает донор протона

гидрокарбонатный буфер Компоненты: Н 2 СО 3 / НСО 3 – донор протона - Н 2 СО 3 – акцептор протона - НСО 3 Н+ – + НСО 3 ⇄ Н 2 СО 3 ⇄ СО 2 + Н 2 О ОН– + Н 2 СО 3 ⇄ НСО 3– + Н 2 О

Буферная емкость раствора – это величина, характеризующая способность буферного раствора противодействовать смещению реакции среды при добавлении сильных кислот или щелочей. Это мера буферного действия.

Буферная емкость измеряется количеством моль эквивалентов кислоты или щелочи, добавление которых к 1 л буферного раствора изменяет р. Н на единицу. Обозначается В и измеряется в моль/л. Вк = ; Вщ =

Буферная емкость максимальна при максимальной абсолютной концентрации компонентов при соотношении компонентов равным единице При разбавлении буферного раствора величина буферной емкости уменьшается

Зона буферного действия Рабочий участок буферной системы, т. е. способность противодействовать изменению р. Н при добавлении кислот и щелочей р. Н = р. К 1

Буферные системы крови в плазме: Ø гидрокарбонатная Ø гидрофосфатная Ø органических фосфатов Ø белковая в клетках крови: Ø гемоглобиновая Ø гидрокарбонатная Ø фосфатная

Гидрокарбонатная (бикарбонатная) буферная система Гидрокарбонаты: Na. HCO 3 – во внеклеточной жидкости КНСО 3 – внутри клеток СО 2 + Н 2 О ⇄ СО 2·Н 2 О ⇄ Н 2 СО 3 содержится также в эритроцитах, межклеточной жидкости и в почечной ткани

Гидрофосфатная буферная система Дигидрофосфаты и гидрофосфаты: Na. H 2 РO 4 и Na 2 HРO 4 – вне клеток КН 2 РО 4 и К 2 HРO 4 – внутри клеток + НРО 4 – 2– ⇄ Н 2 РО 4 – – ОН + Н 2 РО 4 ⇄ НРО 4 2– + Н 2 О Органические фосфаты также обладают буферными свойствами, но мощность их слабее неорганического фосфатного буфера.

Белковая (протеиновая) буферная система Анионный белковый буфер HProt / Prot – Катионный белковый буфер + H 2 Prot / НProt В крови работает анионный буфер

Гемоглобиновая буферная система Гемоглобинат и оксигемоглобинат: КHb и КНb. О 2 главная буферная система эритроцитов Эта система эффективно функционирует только в сочетании с другими буферными системами крови.
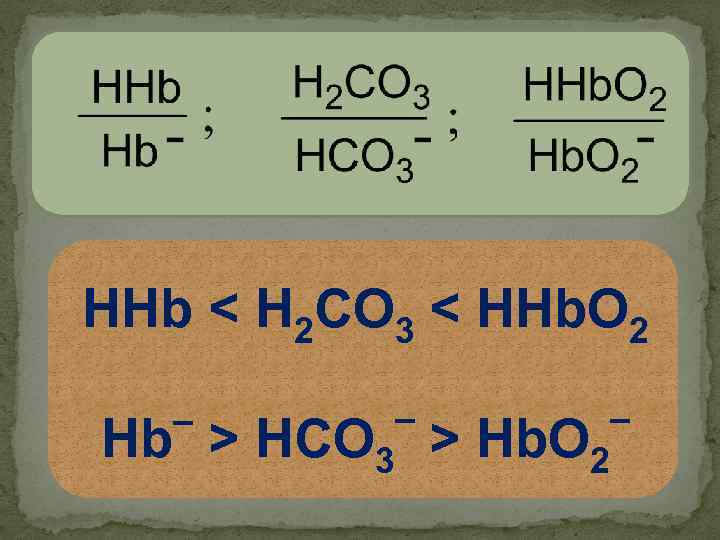
HHb < H 2 CO 3 < HHb. O 2 – – Hb > HCO 3 > Hb. O 2 –
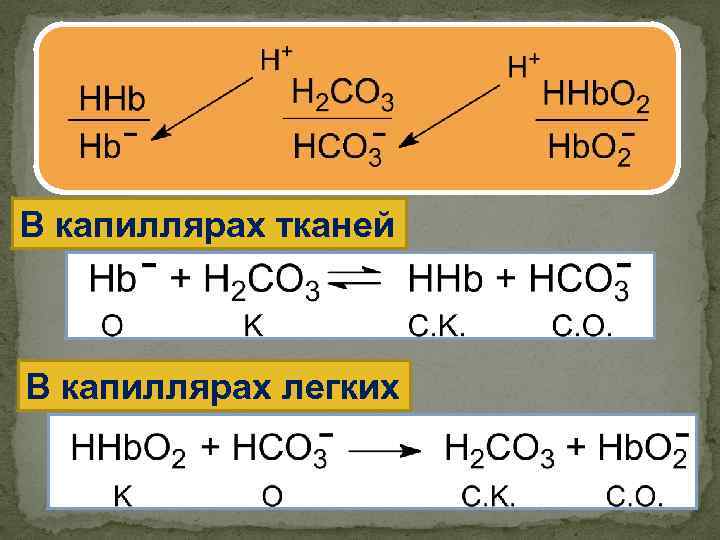
В капиллярах тканей В капиллярах легких

СТАРОСТЫ 3, 4, 5 ГРУПП ПОДОЙДИТЕ К ПРЕПОДАВАТЕЛЮ 2 ГРУППА ОСТАНЬТЕСЬ
буферные системы.pptx