Bronkholyogochnaya_displvzia_u_detey.ppt
- Количество слайдов: 25
БРОНХОЛЕГОЧНАЯ ДИСПЛАЗИЯ У ДЕТЕЙ д. мед. н. Одинец Ю. В. , к. мед. н. Алексеева Н. П. (ХГМУ); Кашпур Н. А. , Промская Н. В. , Раковская Л. А. (ДГКБ № 16)

Бронхолегочная дисплазия (бронхопульмональная дислазия, БЛД) – приобретенное хроническое обструктивное заболевание легких, развивающееся вследствие респираторного дистресс-синдрома новорожденных и/или искусственной вентиляции легких (ИВЛ) с высокими концентрациями кислорода, сопровождающееся гипоксемией, измененной реактивностью бронхов с гиперчувствительностью дыхательных путей и характерными рентгенологическими изменениями.

ЧАСТОТА БЛД n Частота БЛД зависит от массы тела при рождении и гестационного возраста: ее частота составляет 73% в группе детей с массой тела при рождении менее 1000 г, 41% - с массой тела 1000 – 1499 г и 16% среди новорожденных с массой тела выше 1499 г (A. Figueras и соавт. – 1991 г). С учетом гестационного возраста БЛД выявляется у всех (100%) новорожденных со сроком гестации менее 28 недель беременности, у 38% новорожденных с гестационным возрастом 28 – 30 недель и у 4% новорожденных с гестационным возрастом старше 30 недель. n С развитием технологий выхаживания и респираторной терапии недоношенных детей одновременно со снижением смертности среди детей с массой тела менее 1000 г и гестационным возрастом менее 30 недель отмечается рост частоты БЛД. n В г. Харькове ежегодно рождается около 900 недоношенных новорожденных. Таким образом примерно у 150 – 200 этих детей вероятность развития БЛД достаточно высока. На диспансерном учете по БЛД в настоящее время находится всего 50 детей в возрасте от 2 -х месяцев до 3 -х лет. Частота выявления и диагностики БЛД у детей нашего региона чрезвычайно низкая, что объясняется недостаточной осведомленностью об этой патологии врачей педиатров и семейных докторов.

ИСТОРИЧЕСКАЯ СПРАВКА n Первое описание БЛД было опубликовано W. Н. Northway в 1967 г. и представляло собой обзор историй болезней, данных рентгенограмм и патологоанатомических заключений 32 недоношенных детей, перенесших СДР и требовавших ИВЛ и кислородной поддержки в течение 24 часов и более. Наблюдавшиеся дети имели средний гестационный возраст 32 недели и среднюю массу тела при рождении 2200 г. На основании этих данных W. Н. Northway сделал заключение о появлении нового хронического заболевания легких - БЛД, развитие которого он связывал с проведением ИВЛ и длительным (более 150 часов) использованием для дыхания 80100% кислорода. n Критерии БЛД были предложены E. Bankalary в 1979 г. и включают указания в анамнезе больного на проведение ИВЛ в течение первых трех дней жизни, сохранение в возрасте 28 суток жизни симптомов дыхательной недостаточности (тахипноэ, хрипы при аускультации, ретракция грудной клетки при дыхании и т. п. ), наряду с характерными рентгенологическими изменениями и необходимостью в кислородной поддержке для поддержания уровня р. О 2 более 50 мм рт. ст.

Этиология БЛД Первоначально БЛД рассматривалась как результат повреждающего действия кислорода и ИВЛ на легкие новорожденного, что нашло отражение в классической формуле A. Philip (1975): "кислород+давление+время". В настоящее время БЛД рассматривается как полиэтиологическое заболевание. Факторами, способствующими развитию бронхолегочной дисплазии являются следующие: n n n n Незрелость легкого недоношенного ребенка Токсическое действие кислорода Баротравма легких Респираторные расстройства Инфекция Отек легких Наследственная предрасположенность Гиповитаминозы А и Е

Схема образования сурфактанта АК - альвеолярный капилляр; ЭАК - эндотелий альвеолярного капилляра; ЯАЦ 2 - ядро альвеолоцита II типа; АЦ 1 - альвеолоцит I типа; 1 - поступление из альвеолярных капилляров материала, содержащегося в плазме крови; 2 - синтез предшественников сурфактанта в гладком эндоплазматическом ретукулуме (ГЭР), шероховатом эндоплазматическом ретикулуме (ШЭР) и в аппарате Гольджи (АГ); 3 - образование мультивезикулярных (МТ) и пластинчатых телец (ПТ); 4 - открытие вакуолей в просвет альвеолы и экскреция пластинчатых телец (ПТ); 5 - трансформация в миелиновые трубки (МЕТ); 6 - образования поверхностей пленки, покрывающей АЦ 1. n n Этиология БЛД - Незрелость легкого недоношенного ребенка: незрелость анатомических структур легкого, системы сурфактанта и созревающей одновременно с ней, в третьем триместре беременности, антиоксидантной системы легких, включающих супероксиддисмутазу, глютатион пероксидазу и каталазу, играет роль в избаточном растяжении дыхательных путей и предрасполагает к баротравме и повреждению кислородом (Fitzerald D. et al. , 1994). n - Токсическое действие кислорода: гипероксидное повреждение легких приводит к некрозу эпителия дыхательных путей, эндотелия легочных капилляров, трансформации альвеолоцитов II типа в альвеолоциты I типа (Evans M. J. , 1994). Следствием «окислительной атаки» является нарушение мукоцилиарного клиренса, развитие ателектазов и легочной гипертензии.

Этиология БЛД n - Баротравма легких: n - Респираторные расстройства: токсическое действие высоких концентраций О 2 во вдыхаемой смеси приводит к повреждению эпителиального и эндотелиального клеточных барьеров и развитию протеинсодержащего отека легочной ткани, что сопровождается снижением растяжимости альвеол, уже нарушенной вследствие дефицита сурфактанта. Снижение комплайнса легких и нарастающие нарушения вентиляционноперфузионных отношений обуславливают необходимость использования более высоких параметров ИВЛ, что замыкает порочный круг, усиливая повреждение легких. Применение ИВЛ с постоянным положительным давлением способствует возникновению разрывов альвеол с образованием интерстициальной эмфиземы и пневмоторакса. первичные (СДР, болезнь гиалиновых мембран, ателектаз, болезни утечки воздуха) и вторичные (персистирующее фетальное кровообращение и другие формы врожденных болезней сердечно-сосудистой системы, в частности ВПС, особенно с обогащением малого круга кровообращения).

Этиология БЛД n Инфекция: колонизация дыхательных путей новорожденных такими микроорганизмами, как Chlamydia trachomatis (Sollecito D. et al. , 1992), Ureaplasma urealyticum (Jonsson B. et al. , 1994, Pacifico L. et al. , 1997), Mycoplasma hominis (Pacifico L. et al. , 1997), цитомегаловирус (Sawyer M. N. , 1987), ассоциируется с высоким риском развития БЛД по сравнению с неинфицированными. n - Отек легких: причинами отека легких могут быть избыточный объем инфузионной терапии, нарушение выведения жидкости, открытый артериальный проток. n - Легочная гипертензия: Фиброзные изменения части артерий приводят к снижению суммарного поперечного сечения артериального русла легких. Повышенная проницаемость капилляров, низкое онкотическое давление крови, повышенный вследствие ИВЛ синтез вазопрессина и альдостерона и ухудшение лимфатического дренажа на фоне фиброзных изменений лимфатических сосудов способствуют развитию интерстициального отека легких. Это пролонгирует течение тканевой воспалительной реакции и ведет к развитию структурных аномалий сосудов, усугубляющих легочную гипертензию.

Этиология БЛД n Наследственная предрасположенность: генетически обусловленная гиперреактивность дыхательных путей увеличивает риск развития БЛД (Bertrand J. M. , 1985). К факторам риска относят также мужской пол, принадлежность к кавказским национальностям (Гомелла Т. Л. , Каннигам М. Д. , 1995) n Гиповитаминозы А и Е: у недоношенных новорожденных с СДР, развивших БЛД, имеет место снижение уровня ретинола и ретинол-связывающего белка в сыворотке крови, что приводит к нарушению мукоцилиарного клиренса, перемещению воды через трахеобронхиальный эпителий и к повышению резистентности дыхательных путей. Дети, находящиеся на парентеральном питании, имеют дефицит витамина Е, селена, серосодержащих аминокислот, что повышает риск развития у них БЛД.
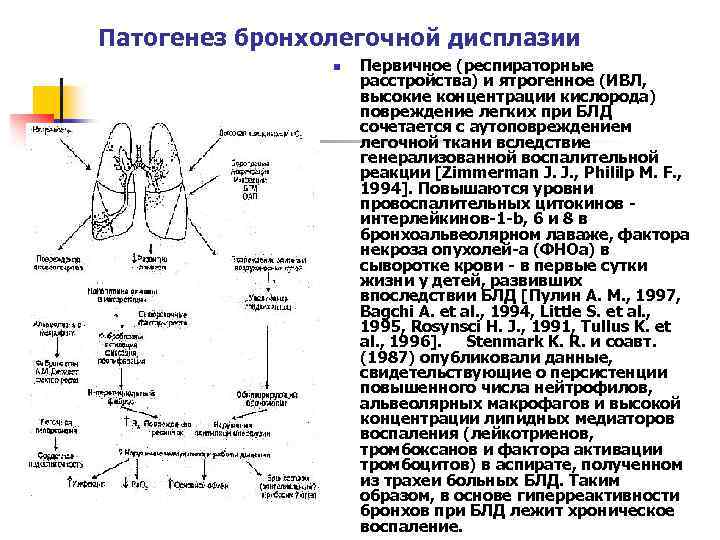
Патогенез бронхолегочной дисплазии n Первичное (респираторные расстройства) и ятрогенное (ИВЛ, высокие концентрации кислорода) повреждение легких при БЛД сочетается с аутоповреждением легочной ткани вследствие генерализованной воспалительной реакции [Zimmerman J. J. , Phililp M. F. , 1994]. Повышаются уровни провоспалительных цитокинов интерлейкинов-1 -b, 6 и 8 в бронхоальвеолярном лаваже, фактора некроза опухолей-a (ФНОa) в сыворотке крови - в первые сутки жизни у детей, развивших впоследствии БЛД [Пулин А. М. , 1997, Bagchi A. et al. , 1994, Little S. et al. , 1995, Rosynsci H. J. , 1991, Tullus K. et al. , 1996]. Stenmark K. R. и соавт. (1987) опубликовали данные, свидетельствующие о персистенции повышенного числа нейтрофилов, альвеолярных макрофагов и высокой концентрации липидных медиаторов воспаления (лейкотриенов, тромбоксанов и фактора активации тромбоцитов) в аспирате, полученном из трахеи больных БЛД. Таким образом, в основе гиперреактивности бронхов при БЛД лежит хроническое воспаление.

Стадии БЛД Морфологическая характеристика Рентгенологическая картина I стадия – 1 -3 день жизни Типичный респираторный дистресссиндром Изменения, как при РДС: нежная нодозно-ретикулярная сеть, положительная воздушная бронхограмма II стадия – 4 -10 день жизни Деструкция клеток альвеолярного эпителия и эндотелия капилляров, отек интерстициального и периваскулярного пространства, некроз бронхиол, сквамозная метаплазия, гипертрофия гладкой мускулатуры, исчезновение клеток мерцательного эпителия Снижение прозрачности легочных полей, участки интерстициальной эмфиземы, нечеткость контуров сердечной тени, но главные бронхи еще воздушны III стадия – 11 -30 -й день жизни Распространенная метаплазия и гиперплазия эпителия бронхов и бронхиол, массивный интерстициальный отек, развитие облитерирующего бронхиолита Мелкокистозные просветления ( «губка» , «пузыри» ), контур сердца визуализируется. Эта стадия отражает начинающийся фиброз легочной стромы. IV стадия – 2 -й месяц жизни Массивный фиброз легких с деструкцией альвеол и стенок воздухоносных путей, гипертрофия мышечного слоя бронхиол, уменьшение количества легочных артериол и капилляров с гипертрофией мышечного слоя артериол и венул Стадия хронической БЛД: кардиомегалия, линейные и лентообразные уплотнения (участки фиброза), чередующиеся с зонами просветления за счет эмфиземы.

Диагностика БЛД • Данные анамнеза: преждевременные роды, масса при рождении менее 1500 г, СДР с первых часов жизни, ИВЛ с жесткими параметрами более 6 суток, кислородозависимость не менее 1 месяца; • Клинические симптомы: кашель и стойкие физикальные изменения, нарастание обструктивных нарушений при наслоении вирусной инфекции, признаки скрытой ДН, выявляемой при нагрузке – сосании, движении, плаче; • Наличие сопутствующих состояний: легочное сердце в раннем возрасте, неврологическая симптоматика, отставание в физическом развитии; • Рентгенологические изменения: признаки фиброза в виде деформации и локального усиления легочного рисунка или легкой завуалированности легочных полей в среднемедиальных отделах, чередующиеся с участками вздутия легочной ткани, преимущественно в нижнелатеральных отделах у детей старше 1 месяца.
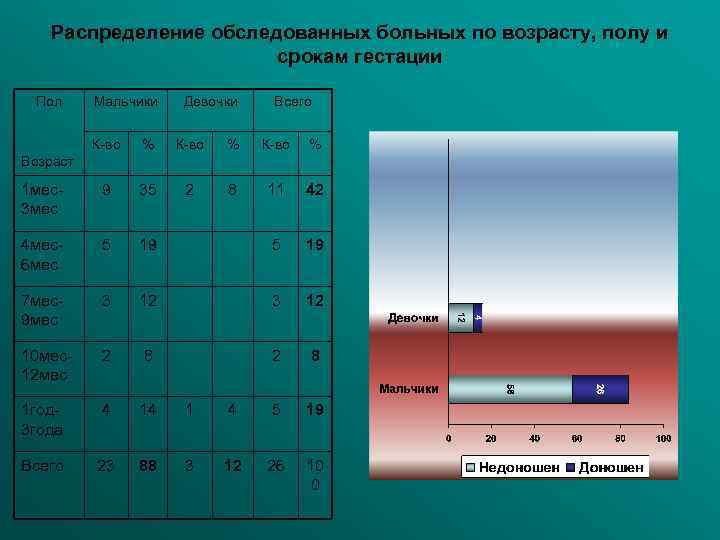
Распределение обследованных больных по возрасту, полу и срокам гестации Пол Мальчики Девочки Всего К-во % 1 мес3 мес 9 35 2 8 11 42 4 мес6 мес 5 19 7 мес9 мес 3 12 10 мес12 мес 2 8 1 год 3 года 4 14 1 4 5 19 Всего 23 88 3 12 26 10 0 Возраст
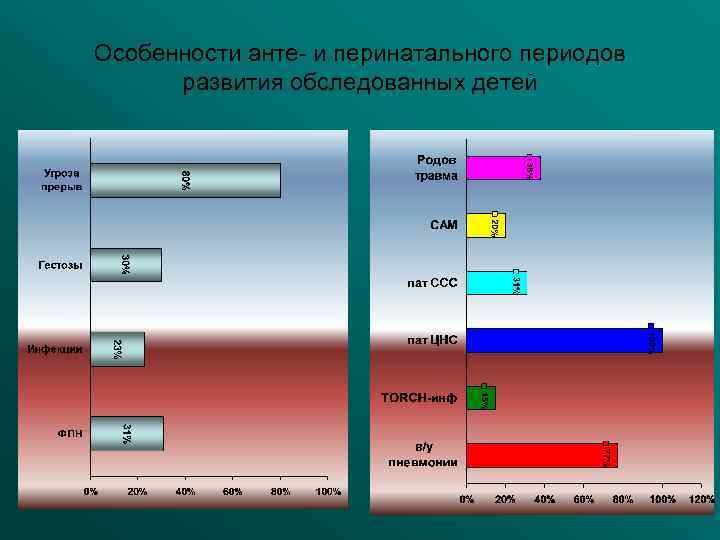
Особенности анте- и перинатального периодов развития обследованных детей
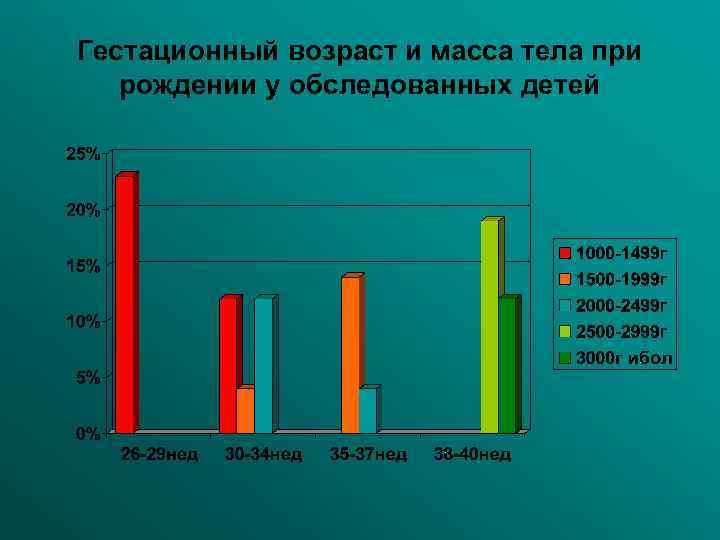
Гестационный возраст и масса тела при рождении у обследованных детей
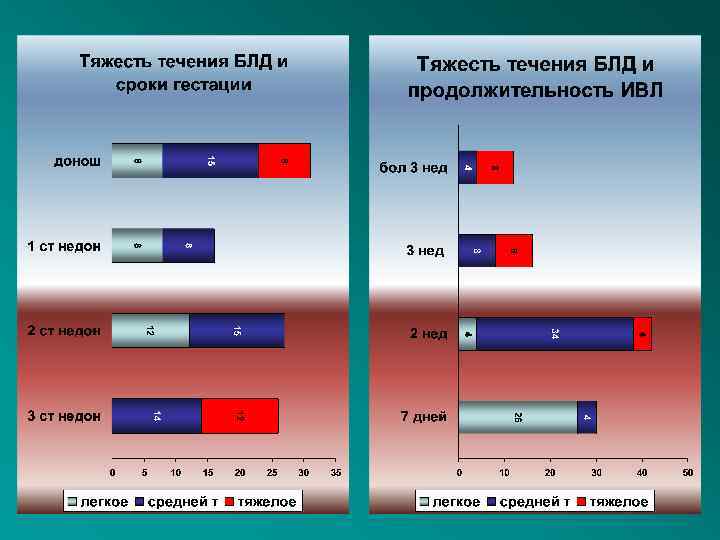

Тяжесть течения БЛД и клинические проявления • • • Легкое течение БЛД: отсутствие тахипноэ в покое, появление симптомов бронхообструкции на фоне ОРЗ, нет отставания в физическом развитии, рентгенологически выявляется умеренная эмфизема. Средней тяжести БЛД: тахипноэ при физической нагрузке (плач, кормление, беспокойство), сухие хрипы на выдохе, влажные мелкопузырчатые ( «целлофановые» ) хрипы в период клинического благополучия. При присоединении ОРЗ – обструктивные нарушения дыхания резко усиливаются. Умеренное отставание в физическом развитии. Рентгенологически – выявляются эмфизема, участки локального пневмосклероза. Тяжелое течение БЛД: тахипноэ в покое и выраженные симптомы бронхообструкции, сочетающиеся с ослаблением дыхания при аускультации легких, отставание в физическом развитии, формирование легочного сердца, стойкие рентгенологические изменения в виде эмфиземы, обеднения легочного рисунка, множественных участков пневмосклероза, ателектазов, дистелектазов, перибронхиальных изменений, кардиомегалии.

Осложнения БЛД • • • Лобарные или сегментарные ателектазы; Пневмоторакс; Хроническое легочное сердце; Хроническая дыхательная недостаточность; Легочные инфекции (бронхиты, бронхиолиты, пневмонии) носят рецидивирующий характер, обычно до 5 -6 -летнего возраста; Трахеобронхомаляция; Рецидивирующий обструктивный бронхит и бронхиальная астма; Эпизоды гипоксии. Больные с БЛД относятся к группе риска по развитию внезапной смерти; Преходящая системная артериальная гипертензия; Задержка роста и отставание в физическом развитии; Задержка нервно-психического развития

Лечение БЛД • Кислородотерапия: ИВЛ и/или обеспечение кислородом в течение недель или месяцев. Поддержание Ра СО 2 на уровне 45 -60 мм рт. ст. , при р. Н более 7. 25, сатурации О 2 – 90 -95%, РО 2 – 55 -70 мм рт. ст. При торпидной гипоксемии, требующей высокого давления на выдохе, применяют курсы высокочастотной осцилляторной ИВЛ, что позволяет уменьшить длительность вентиляции, баротравму и частоту БЛД. После прекращения ИВЛ осуществляют дотацию О 2 в концентрации, позволяющей поддерживать РО 2 на уровне 55 мм рт. ст. Когда эти параметры стабильны у ребенка, находящегося в кислородной палатке с содержанием О 2 менее 30%, можно переходить на подачу О 2 через носовой катетер. • Питание и назначение жидкости: адекватная калорийность питания 120 -140 ккал/кг/сут. Питание может осуществляться парентерально ( с введением аминокислот из расчета белка 2 -3 г/кг/сут и жировых эмульсий из расчета 0. 5 -3 г/кг/сут) или с помощью назогастрального зонда. Раннее введение коллоидных растворов в парентеральное питание (до 5 -6 дня жизни) увеличивает риск развития БЛД. Суточное количество жидкости ограничивают минимальными потребностями – 100 -120 мл/кг/сут из-за опасности развития отека легких, особенно при персистирующем артериальном протоке.

Лечение БЛД • Диуретики: для улучшения легочной эластичности и уменьшения резистентности дыхательных путей за счет выведения излишков натрия и воды. Фуросемид (1 мг/кг в/в или в/м или 2 мг/кг внутрь) от 1 до 3 раз в день применяют короткое время (до 1 недели). Современная тактика применения этого препарата предусматривает введение его через небулайзер 1 мг/кг внутривенного препарата, растворенного в 2 мл 0. 9% р-ра хлорида натрия каждые 6 часов. Для длительной диуретической терапии (до 2 -2. 5 месяцев) наиболее подходит сочетание гипотиазида (хлортиазида) по 2 мг/кг/сут и спиронолактона (верошпирона) 2 мг/кг/сут в 2 приема. • Бронходилятаторы: сальбутамол в ингаляциях доза 2. 5 мг (независимо от возраста и массы). Применяют ингаляции атровента или беродуала. Бронходилятирующее действие эуфиллина выражено меньше, но он обладает другими важными при БЛД эффектами: усиливает диурез, оказывает стимулирующее действие на дыхательный центр. • Муколитики: амброксол (1. 5 -2. 0 мг/кг/сут) энтерально или в ингаляциях через небулайзер

Лечение БЛД • Кортикостероиды: оптимальное время начала кортикостероидной терапии является 2 -3 неделя жизни. • 1) Стандартная схема: 500 мкг/кг дексаметазона внутрь или в/в один раз в день в течение 3 дней, затем по 300 мкг/кг в сутки в следующие 3 дня, далее дозу уменьшают на 10% каждые 3 дня, до достижения дозы 100 мкг/кг в сутки, которую принимают еще 3 сут, после чего в течение недели препарат назначают ч/з день, а затем отменяют. • 2) пульс-терапия: 250 мкг/кг дексаметазона внутрь или в/в дважды в день в течение 3 дней каждые 10 дней до тех пор, пока ребенок не перестанет быть зависимым от О 2. • 3) длительное (6 недель) лечение с использованием высоких доз: начальная доза – 500 мкг/кг внутрь или в/в назначается один раз в день в течение 3 дней, затем доза препарата прогрессивно снижается до 100 мкг/кг через день на последней неделе лечения (Шабалов Н. П. , 2000)

Лечение БЛД • Эффекты стероидов при лечении БЛД: • Побочные эффекты стероидов при лечении БЛД: • • • Поддержание беттаадренергической активности; Стимуляция продукции антиоксидантов Стабилизация клеточных и лизосомальных мембран Торможение агрегации гранулоцитов и улучшение легочной микроциркуляции Угнетение синтеза простогландинов и лейкотриенов Выведение из легких избытка жидкости Супрессия цитокиновой индукции воспалительной реакции в легочной ткани • • • Угроза сепсиса Системная артериальная гипертензия Обратимая гипертрофия желудочков сердца, нередко протекающая с клапанной дисфункцией Интолерантность к глюкозе Гипервозбудимость Перфорация кишечника Супрессия функции надпочечников, персистирующая 2 -4 недели при курсе дексаметазона более 10 дней (Шабалов Н. П. , 2000, Rush M. G. , Hasinski T. A. , 1992)

Лечение БЛД • Кортикостероиды: • Альтернативой системного применения дексаметазона при БЛД являются • Начатая в первые 3 дня жизни профилактическая терапия будесонидом у недоношенных детей менее 32 недель гестации с тяжелым СДР приводит к достоверному снижению частоты БЛД и укорочению длительности ИВЛ. Обычный курс терапии – 3 дня, но у ряда детей его продлевали до 15 дней. (Шабалов Н. П. , 2000). ингаляционные стероиды (будесонид, флутиказон, беклометазон) – суточная доза составляет примерно 400 мкг через аэрочамбер или небулайзер. • Профилактика инфекций: выбор антибиотика с учетом возбудителя – цефалоспорины 3 -го поколения, имипинемы, аминогликозиды при внутрибольничном инфицировании аэробными грамотрицательными бактериями; макролиды – при атипичной инфекции; при подтвержденной респираторно-синтициальной инфекции – рибавирин. Эффективно применение иммуноглобулинов, препаратов, воздействующих на протеазы, уровень которых значительно увеличен при БЛД.

Диспансерное наблюдение • • • Консультация пульмонологом детей с БЛД после выписки из перинатального центра и в дальнейшем наблюдение на протяжении не менее 5 лет; Обучение родителей подсчету частоты дыхания и пульса, диагностике дыхательной недостаточности по наличию свистящего дыхания, комплексу пассивных дыхательных упражнений и массажа. Все родители обязаны получить инструкции по проведению сердечно-легочной реанимации; Гипоаллергенный режим, минимизация контактов с инфекционными больными, адекватная диета с повышенным содержанием белка; Применение ИГКС в дозе от 100 до 400 мкг в сутки от 3 -х месяцев до 1. 5 -2 -х лет в зависимости от тяжести БЛД и выраженности бронхообструктивного компонента; Применение липина в ингаляциях 10 -15 мг/кг на 1 ингаляцию в течение 10 дней ежеквартально в течение 1 -2 лет при среднетяжелом и тяжелом течении БЛД; При развитии интеркуррентной инфекции с нарастанием обструктивных нарушений используются ингаляционные бронхолитики (сальбутамол, беродуал); При необходимости назначения антибиотиков по поводу респираторных инфекций предпочтительно использование макролидов; Повторное рентгенологическое обследование и проведение эхокардиографии в возрасте 6 и 12 месяцев; Применение поливитаминов, профилактика рахита, проведение вакцинации; Осмотр ребенка специалистами – невропатологом, физиотерапевтом, окулистом, иммунологом – помогает оптимизировать лечение с учетом сопутствующей патологии

СПАСИБО ЗА ВНИМАНИЕ!
Bronkholyogochnaya_displvzia_u_detey.ppt