Бронхиальная астма. Этиология и патогенез. Классификация.ppt
- Количество слайдов: 28

Бронхиальная астма. Современные концепции этиологии и патогенеза. Классификация по степени тяжести и по уровню контроля

Бронхиальная астма • Это хроническое воспалительное заболевание дыхательных путей с участием клеток (тучных, эозинофилов, Т-лимфоцитов), медиаторов аллергии и воспаления, сопровождающееся у предрасположенных лиц гиперреактивностью и обратимой обструкцией бронхов, что проявляется приступом удушья, появлением хрипов, кашля или затруднения дыхания, особенно ночью и/или ранним утром

Этиология Предрасполагающие факторы: • Генетитические - гены предрасполагающие к атопии (способность орг-ма к выработке повышенного кол-ва Ig E в ответ на воздей-е аллергенов), гены предрасполагющие к бронхиальной гиперреактивности • Ожирение - БА чаще встречается у людей страдающих ожирением (ИМТ >30) • Пол (среди детей преобладают мальчики, среди взрослых – женщины) Причинные факторы – индукторы - сенсибилизируют дыхательные пути и вызывают начало заболевания: • Аллергены – аллергены помещений (клещи домашней пыли, шерсть домашних животных, аллергены тараканов, грибов), внешние аллергены (пыльца, грибы) • Респираторные инфекции (главным образом, вирусные) • Профессиональные сенсибилизаторы (например, мука у пекарей, древесная пыль у работников лесопилок, латекс у работников медицинских учреждений) • Курение табака • Загрязнение воздуха внутри и снаружи помещений Факторы риска, обостряющие течение заболевания – триггеры (провокаторы): • Физическая нагрузка • Эмоциональный стресс • Изменения погоды (низкая температура, высокая влажность) • Бета-блокаторы • Предменструальный период • Беременность • Индукторы

Патогенез В основе заболевания лежит хроническое воспаление, охватывающее все дыхательные пути, включая верхние отделы и полость носа Особенности воспаления при БА: qактивация тучных клеток qактивация эозинофиллов qактивация Т-киллеров qактивация Т-хелперов 2 типа
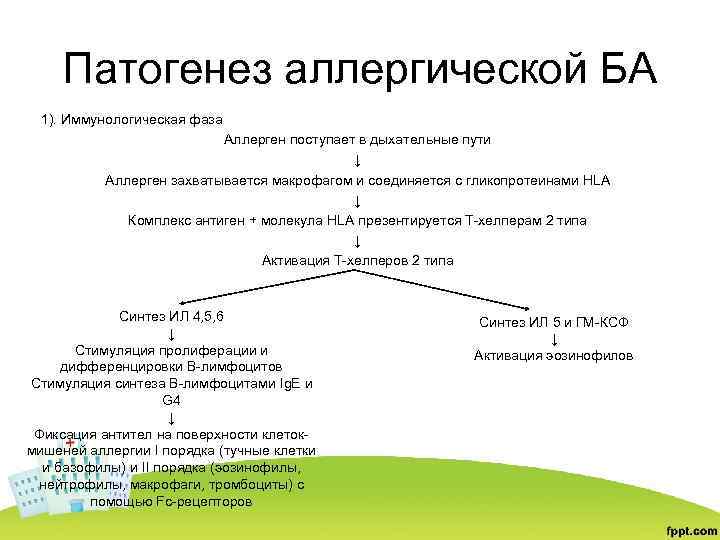
Патогенез аллергической БА 1). Иммунологическая фаза Аллерген поступает в дыхательные пути ↓ Аллерген захватывается макрофагом и соединяется с гликопротеинами HLA ↓ Комплекс антиген + молекула НLA презентируется Т-хелперам 2 типа ↓ Активация Т-хелперов 2 типа Синтез ИЛ 4, 5, 6 ↓ Стимуляция пролиферации и дифференцировки В-лимфоцитов Стимуляция синтеза В-лимфоцитами Ig. E и G 4 ↓ Фиксация антител на поверхности клетокмишеней аллергии I порядка (тучные клетки и базофилы) и II порядка (эозинофилы, нейтрофилы, макрофаги, тромбоциты) с помощью Fc-рецепторов Синтез ИЛ 5 и ГМ-КСФ ↓ Активация эозинофилов

Патогенез аллергической БА 2). Патохимическая стадия Повторное поступление аллергена ↓ Взаимодействие аллергена с антителами на поверхности клеток-мишеней аллергии ↓ Дегрануляция тучных клеток и базофилов, активация эозинофилов ↓ Выделение медиаторов аллергии и воспаления

Патогенез аллергической БА 3). Патофизиологическая стадия – характеризуется развитием бронхоспазма, отека слизистой оболочки и инфильтрации стенки бронха клеточными элементами, воспаления, гиперсекрецией слизи В течении патофизиологической стадии выделяют 2 фазы: v Ранняя фаза или ранняя астматическая реакция – начинается эта фаза через 1 -2 минуты, достигает максимума через 15 -20 минут и продолжается около 2 часов. Основными клетками, участвующими в развитии ранней астматической реакции, являются тучные клетки и базофилы. Ведущий механизм ранней астматической реакции – бронхоспазм. v Поздняя астматическая реакция – развивается приблизительно через 4 -6 часов, максимум ее проявлений наступает через 6 -8 часов, длительность реакции 8 -12 часов. В развитии поздней астматической реакции принимают участие тучные клетки, эозинофилы, нейтрофилы, макрофаги, тромбоциты, Т-лимфоциты. Основные проявления стадии – воспаление, отек слизистой оболочки бронхов, гиперсекреция слизи
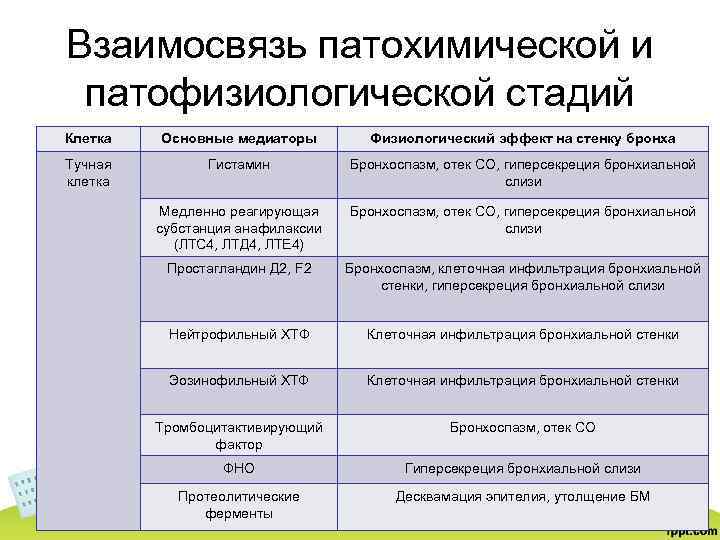
Взаимосвязь патохимической и патофизиологической стадий Клетка Основные медиаторы Физиологический эффект на стенку бронха Тучная клетка Гистамин Бронхоспазм, отек СО, гиперсекреция бронхиальной слизи Медленно реагирующая субстанция анафилаксии (ЛТС 4, ЛТД 4, ЛТЕ 4) Бронхоспазм, отек СО, гиперсекреция бронхиальной слизи Простагландин Д 2, F 2 Бронхоспазм, клеточная инфильтрация бронхиальной стенки, гиперсекреция бронхиальной слизи Нейтрофильный ХТФ Клеточная инфильтрация бронхиальной стенки Эозинофильный ХТФ Клеточная инфильтрация бронхиальной стенки Тромбоцитактивирующий фактор Бронхоспазм, отек СО ФНО Гиперсекреция бронхиальной слизи Протеолитические ферменты Десквамация эпителия, утолщение БМ
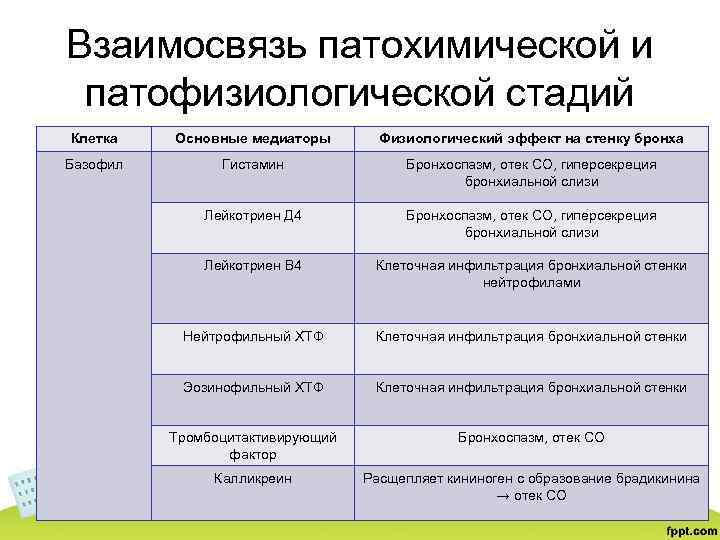
Взаимосвязь патохимической и патофизиологической стадий Клетка Основные медиаторы Физиологический эффект на стенку бронха Базофил Гистамин Бронхоспазм, отек СО, гиперсекреция бронхиальной слизи Лейкотриен Д 4 Бронхоспазм, отек СО, гиперсекреция бронхиальной слизи Лейкотриен В 4 Клеточная инфильтрация бронхиальной стенки нейтрофилами Нейтрофильный ХТФ Клеточная инфильтрация бронхиальной стенки Эозинофильный ХТФ Клеточная инфильтрация бронхиальной стенки Тромбоцитактивирующий фактор Бронхоспазм, отек СО Калликреин Расщепляет кининоген с образование брадикинина → отек СО
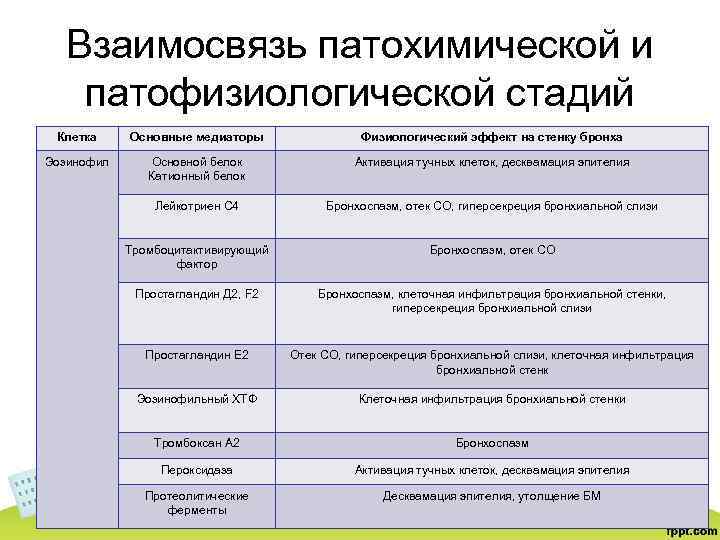
Взаимосвязь патохимической и патофизиологической стадий Клетка Основные медиаторы Физиологический эффект на стенку бронха Эозинофил Основной белок Катионный белок Активация тучных клеток, десквамация эпителия Лейкотриен С 4 Бронхоспазм, отек СО, гиперсекреция бронхиальной слизи Тромбоцитактивирующий фактор Бронхоспазм, отек СО Простагландин Д 2, F 2 Бронхоспазм, клеточная инфильтрация бронхиальной стенки, гиперсекреция бронхиальной слизи Простагландин Е 2 Отек СО, гиперсекреция бронхиальной слизи, клеточная инфильтрация бронхиальной стенк Эозинофильный ХТФ Клеточная инфильтрация бронхиальной стенки Тромбоксан А 2 Бронхоспазм Пероксидаза Активация тучных клеток, десквамация эпителия Протеолитические ферменты Десквамация эпителия, утолщение БМ

Структурные изменения в дыхательных путях при БА – процесс ремоделирования бронхов • В результате отложения волокон коллагена и протеогликанов под базальной мембраной развивается субэпителиальный фиброз • Толщина гладкомышечного слоя увеличивается вследствие гипертрофии и гиперплазии. Этот процесс обусловлен действием таких медиаторов воспаления, как факторы роста. • Под действием факторов роста, например фактора роста эндотелия сосудов, отмечается пролиферация сосудов бронхиальной стенки → утолщение стенки бронха

Бронхиальная обструкция • • 1. 2. 3. 4. Заключительный этап патогенеза БА, приводящий к появлению симптомов заболевания и характерным физиологическим изменениям Обструкция имеет 4 компонента: Острая обструкция – обусловлена спазмом гладкой мускулатуры бронхов в ответ на бронхоконстрикторное действие различных медиаторов и нейротрансимиттеров. Этот процесс является главным механизмом сужения дыхательных путей и практически полностью обратим под действием бронхолитиков Подострая обструкция – вследствие отека слизистой оболочки бронхов. Отек обусловлен повышенной проницаемостью микрососудистого русла, вызванной действием медиаторов воспаления Хроническая обструкция – закупорка бронхов, преимущественно терминальных отделов, вязким секретом. Является результатом повышенной секреции слизи и образования воспалительного экссудата Необратимая (склеротическая) обструкция – вследствие развития склеротических изменений в стенке бронхов при длительном и тяжелом течении заболевания (ремоделирование)

Механизмы бронхоспазма Мускулатура бронхов представлена волокнами гладкой мускулатуры. В миофибриллах присутствуют белки актин и миозин, при взаимодействии их друг с другом образуется комплекс актин+миозин, в результате происходит сокращение бронхиальных миофибрил – бронхоспазм. Образование комплекса актин+миозин возможно только в присутствии ионов кальция. В мышечных клетках присутствует так называемый «кальциевый насос» , благодаря которому возможно перемещение ионов кальция из миофибрилл в саркоплазаматический ретикулум, что ведет к расширению бронхов. Работа «кальциевого насоса» регулируется концентрацией двух внутриклеточных нуклеотидов: • ц. АМФ – стимулирует обратное поступление кальция из миофибрилл в саркоплазматический ретикулум и связь с ним, вследствие этого тормозится активность кальмодулина, не может образоваться комплекс актин+миозин и происходит расслабление бронха • ц. ГМФ – ингибирует работу «кальциевого насоса» и возвращение ионов кальция из миофибрилл в саркоплазматический ретикулум, при этом увеличивается активность кальмодулина, поступление кальция к актину и миозину, формируется комплекс актин+миозин, происходит сокращение бронха

Роль вегетативной нервной системы в регуляции тонуса бронхов • Соотношение ц. АМФ/ц. ГМФ регулируется нейромедиаторами вегетативной нервной системы, активностью соответствующих рецепторов на мембране гладкомышечных клеток бронхов и ферментами аденилатциклазой и гуанилатциклазой, которые стимулируют образование соответственно ц. АМФ и ц. ГМФ

Роль вегетативной нервной системы в регуляции тонуса бронхов • • • ü ü ü Парасимпатическая нервная система – ацетилхолин взаимодействует с мускариновыми рецепторами, при этом активируется гуанилатциклаза и происходит сокращение гладкой мускулатуры (бронхоспазм) Симпатическая нервная система – при активации α-адренорецепторов происходит сокращение гладкой мускулатуры бронхов, уменьшение отека СО бронхов, сокращение кровеносных сосудов. При активации β 2 адренорецепторов происходит расслабление гладкой мускулатуры бронхов (через увеличение активности аденилатциклазы), увеличение мукоцилиарного клиренса, расширение кровеносных сосудов Неадренергическая нехолинергическая нервная система Вазоактивный интестинальный пептид – оказывает бронходилатирующий эффект посредством повышения уровня ц. АМФ; Субстанция Р – умеренная бронхокострикция; Нейрокинин А – выраженная бронхоконстрикция; Нейрокинин В – слабо выраженная бронхокострикция; Кальцитонинподобный пептид – бронхоконстрикция выраженная; Бомбезин – умеренно выраженная бронхоконстрикция

Патогенез инфекционнозависимой БА • ГЗТ - при повторных контактах с инфекционным аллергеном Тлимфоциты гиперсенсибилизируются и выделяют медиаторы замедленного действия: факторы хемотаксиса нейтрофилов, эозинофилов, лимфотаксина, фактора аггрегации тромбоцитов. Данные медиаторы вызывают в тучных клетках, базофилах и макрофагах освобождение простагландинов Д 2 и F 2, лейкотриенов (ЛТС 4, ЛТД 4, ЛТЕ 4), вследствие чего развивается бронхоспазм • Токсины инфекционных агентов повреждают надпочечники (↓ глюкокортикоидная функция) и ↓ активность β 2 адренорецепторов • Высвобождается гистамин и другие медиаторы аллергии и воспаления из тучных клеток и базофилов под влиянием пептидогликанов и эндотоксинов многих бактерий • Гемофильная палочка способна синтезировать гистамин

Патогенез аутоиммунного варианта БА • Сенсибилизация к антигенам бронхопульмональной системы → аутоиммунные реакции

Патогенез глюкокотикоидного варианта БА (дисгормональный вариант) • • v v v v Глюкокортикоидная недостаточность способствует развитию воспаления в бронхах, их гиперреактивности и бронхоспазма ГКС оказывают противоаллергическое и противоастматическое действие: Тормозят дегрануляцию тучных клеток и базофилов → тормозят выделение гистамина, лейкотриенов и других медиаторов аллергии и воспаления Снижают синтез рецепторов к субстанции Р (бронхоконстриктор) Активируют продукцию эндопептидазы разрушающей брадикинин и эндотелин-1 (бронхоконстрикторы) ↓ продукцию ИЛ и ФНО Тормозят образование метаболитов арахидоновой кислоты – бронхоконстрикторных простагландинов Повышают количество и чувствительность β 2 -адренорецепторов → ↑ бронходилатирующий эффект Активируют синтез цитокинов с противовоспалительным эффектом (ИЛ 10)

Патогенез дизовариальной формы БА • • Ø Ø Ø Наблюдается снижение уровня в крови прогестерона во 2 фазе менструального цикла и повышение эстрогенов Ухудшение течение БА возникает перед или во время менструации Прогестерон – оказывает бронходилатирующее действие за счет стимуляции β 2 -адренорецепторов бронхов и синтеза простагландина Е Эстрогены способствуют бронхоконстрикции, т. к. : ингибируют активность АХЭ → ↑ уровень ацетилхолина стимулируют активность бокаловидных клеток, слизистой оболочки бронхов → гиперсекреция слизи усиливают высвобождение гистамина из эозинофилов и базофилов усиливают синтез простагландина F 2 (бронхоконстриктор) снижают активность β 2 -адренорецепторов увеличивают связывание ГКС с белками плазмы

Патогенез выраженного адренергического дисбаланса • Нарушение соотношения между β и αадренорецепторами бронхов с преобладанием активности αадренорецепторов

Патогенез холинергического варианта БА • Повышение тонуса блуждающего нерва • Нарушением обмена ацетилхолина – увеличение его уровня в крови • Снижение уровня АХЭ

Патогенез нервнопсихического варианта БА • Под влиянием стресса повышается чувствительность бронхов к гистамину и ацетилхолину • Стресс вызывает гипервентиляцию, стимуляцию ирритативных рецепторов бронхов, что ведет к рефлекторному бронхоспазму

Патогенез аспириновой БА • Нарушение метаболизма арахидоновой кислоты, при котором в результате активации 5 -липооксигеназного пути образуются лейкотриены, вызывающие бронхоспазм

Патогенез астмы физического усилия Гипервентиляция в ходе физической нагрузки ↓ Респираторная потеря тепла и жидкости ↓ Охлаждение СО и гиперосмолярность бронхиального секрета ↓ Раздражение рецепторов блуждающего нерва и дегрануляция тучных клеток и базофилов

Клинико-патогенетические варианты БА • • • Атопический Инфекционно-зависимый Аутоиммунный Дисгормональный Дизовариальный Выраженный адренергический дисбаланс Холинергический Нервно-психический Аспириновый

Классификация по МКБ-10 • Астма с преобладанием аллергического компонента • Неаллергическая астма • Смешанная астма • Неуточненная астма • Астматический статус

Классификация по степени тяжести • • • Интермиттирующая астма: Симтомы реже 1 раза в неделю Короткие обострения заболевания (от нескольких часов до нескольких дней) Ночные симптомы не чаще 2 раз в месяц Отсутсвие симптомов и нормальная функция легких между обострениями ОФВ 1 более 80% от должного Колебания ПСВ менее 20% Легкая персистирующая астма: Симптомы чаще 1 раза в неделю, но реже 1 раза в день Обострения могут нарушать активность и сон Ночные симптомы астмы возникают чаще 2 раз в месяц ОФВ 1 более 80% от должного Колебания ПСВ 20 -30% • • • Средней тяжести персистирующая астма: Ежедневные симптомы: обострения нарушают активность и сон Ночные симптомы астмы возникают чаще 1 раза в неделю Ежедневный прием бета-2 -агонистов короткого действия ОФВ 1 60 -80% от должного Колебания ПСВ более 30% Тяжелая персистирующая астма: Постоянные симптомы Частые обострения Частые ночные симптомы Физическая активность ограничена проявлениями БА ОФВ 1 меньше 60% от должного Колебания ПСВ более 30%

Классификация по уровню контроля • Оценивается состояние в течение 4 недель 1. Контролируемая БА (д/б все перечисленное): дневные симптомы не более или = 2 раз в неделю, ограничение активности нет, ночных симптомов (пробуждения) нет, потребность в препаратах неотложной помощи нет или не более или = 2 раз в неделю, показатели ПСВ и ОФВ 1 в норме, обострений нет. 2. Частично контролируемая БА (наличие любого проявления в течение 1 недели): дневные симтомы более 2 раз в неделю, ограничение активности любой выраженности, ночные симтомы есть, потребность в преп-тах неотл-й помощи более 2 раз в неделю, пок-ли ОФВ 1 или ПСВ менее или равны 80% от должного, обострения до 1 раза в год. 3. Неконтролируемая – 3 и более признаков частично контролируемой БА в течение недели. • Контроль над БА можно осуществлять с помощью опросников: тест по контролю над астмой, вопросник для оценки эффективности терапии астмы, шкала оценки контроля над астмой
Бронхиальная астма. Этиология и патогенез. Классификация.ppt