Болезнь Паркинсона (Анастасия Ашуйко).pptx
- Количество слайдов: 88

Болезнь Паркинсона

Определение Болезнь Паркинсона – это хроническое дегенеративное заболевание нервной системы, при котором человек теряет способность контролировать свои движения. Болезнь Паркинсона — это заболевание, связанное с постепенной гибелью двигательных нервных клеток (нейронов), вырабатывающих медиатор дофамин. Из за этого нарушается регуляция движений и мышечного тонуса, что проявляется характерным тремором (дрожью), общей скованностью и нарушением позы и движений.

История Болезни Паркинсона Впервые описание этой патологии было сделано английским врачом Джеймсом Паркинсоном, по имени которого и было названо заболевание. В одной из своих публикаций « Эссе о дрожательном параличе» (картинка) он приводит странные изменения, происходившие у его пациентов. Основным из признаков патологии он называл тот факт, что люди постепенно теряли контроль над своим телом. В итоге замедлялись их движения, немели конечности, мышцы же при этом напрягались. Без видимых причин дрожали руки и ноги, а лица каменели. Работа оставалась незамеченной в течение 40 лет после опубликования

«Эссе о дрожательном параличе» Джеймс Паркинсон
Классические исследования неврологов У. Говерса, С. Вильсона, В. Эрба и Ж. Шарко в 1868— 1881 годах позволили выделить болезнь Паркинсона как самостоятельное заболевание. По предложению знаменитого французского невролога Шарко (картинка) заболевание получило имя британского врача Паркинсона, чей труд не был должным образом оценён при жизни.

После определения болезни Паркинсона как самостоятельного заболевания возник вопрос о том, поражение каких структур приводит к его симптомам. Французский невролог Эдуард Бриссо в конце XIX столетия предположил, что за развитие заболевания ответственны субталамическое ядро и ножки мозга. В 1912 году Фредерик Леви обнаружил специфические клеточные включения в клетках ствола мозга, характерные для болезни Паркинсона, впоследствии названные тельцами Леви. Тельце Леви (коричневое пятно) в нейроне чёрного вещества при болезни Паркинсона. Коричневый цвет придаёт окрашивающийся белок α синуклеин.


В 1919 году русский невролог К. Н. Третьяков определил, что основные патологические изменения при заболевании возникают в чёрной субстанции. Предположения К. Н. Третьякова не признавались медицинским сообществом до их подтверждения немецким патологоанатомом Рольфом Хасслером в 1948 году. С того времени прошло более 180 лет. Сегодня уже не является тайной что это за болезнь Паркинсона.

МКБ 10 В соответствии с МКБ 10 данное заболевание кодируют под шифром G 20 «Болезнь Паркинсона» . Оно входит в класс VI «Болезни нервной системы» , раздел «Экстрапирамидные и другие двигательные нарушения» .

Часто болезнь Паркинсона сравнивают с болезнью Альцгеймера, считая их похожими. Основное отличие от болезни Альцгеймера в том, что последнему присущи когнитивные расстройства – в частности, ухудшение памяти и поведенческих функций. В основе болезни Паркинсона при этом лежит расстройство двигательной активности.

Эпидемиология БП По данным ВОЗ в мире насчитывается около 3, 7 млн (0, 06% населения) людей с БП. С возрастом (после 50 лет) наблюдается рост заболеваемости, который достигает максимума в возрасте 70– 79 лет, средний возраст начала заболевания составляет 55 ± 10 лет. Таким образом Болезнью Паркинсона (паркинсонизмом) заболевает примерно каждый сотый человек, перешагнувший шестидесятилетний рубеж, причем у мужчин оно встречается чаще, чем у женщин. Также у 5— 24% пациентов — отягощенный семейный анамнез (в семье были случаи данного заболевания). И БП является наиболее частым нейродегенеративным заболеванием после болезни Альцгеймера.

Что интересно, курильщики практически не подвержены этой болезни, а любители молока, наоборот, сильнее рискуют заболеть ей. Это связано со способностью табачного дыма ингибировать фермент моноаминоксидазу.

Еще интересный факт: От болезни Паркинсона защищает употребление кофеина.

Этиология Причины возникновения болезни Паркинсона еще до конца не изучены. Ученые выдвигают множество теорий: 1. Старение 2. Повреждение клеток черной субстанции свободными радикалами. 3. Повреждение тканей мозга внешними токсинами при различных отравлениях. 4. Наследственность.

5. Наличие измененного гена. 6. Дефицит витамина D 7. Возникновение дефектных митохондрий в результате мутации. 8. Энцефалиты вирусной и бактериальной природы 9. Атеросклероз и другие заболевания сосудов. 10. Черепно мозговые травмы.

Установлено, что после инъекции вещества 1 метил 4 фенил 1, 2, 3, 6 тетрагидропиридин (МФТП) развивается паркинсонизм. МФТП проникает через ГЭБ и под действием МАО B окисляется до 1 метил 4 фенилпиридина (МФП+). МФП+ проникает в митохондрии и ингибирует комплекс I дыхательной цепи. Сходство химического строения МФТП и некоторых пестицидов (например, ротенон, паракват) и гербицидов(например, Агент Оранж) позволило предположить, что МФТП подобные токсины окружающей среды способствуют развитию болезни Паркинсона. К факторам риска относят также проживание в сельской местности и близость промышленных предприятий и карьеров
Патогенез Основным патогенетическим звеном дрожательного паралича и синдрома паркинсонизма является нарушение обмена катехоламинов (дофамина, норадреналина) в экстрапирамидной системе.

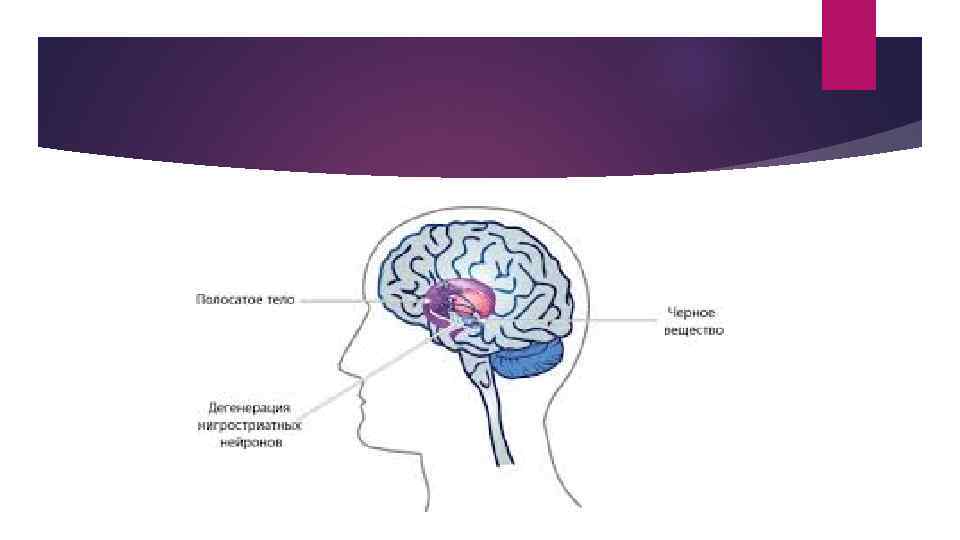
Патогенез Дофамин выполняет самостоятельную медиаторную функцию в реализации двигательных актов. В норме концентрация дофамина в базальных узлах во много раз превышает его содержание в других структурах нервной системы. Ацетилхолин является медиатором возбуждения между полосатым телом, бледным шаром и черным веществом. Дофамин является его антагонистом, действуя тормозяще. При поражении черного вещества и бледного шара снижается уровень дофамина в хвостатом ядре и скорлупе, нарушается соотношение между дофамином и норадреналином, возникает расстройство функций экстрапирамидной системы.

Патогенез При выключении функции черного вещества возникает блокада импульсов, поступающих из экстрапирамидных зон коры большого мозга и полосатого тела к передним рогам спинного мозга. В то же время к клеткам передних рогов поступают патологические импульсы из бледного шара и черного вещества. В результате усиливается циркуляция импульсов в системе альфа– и гамма мотонейронов спинного мозга с преобладанием альфа активности, что приводит к возникновению паллидарно нигральной ригидности мышечных волокон и тремора.

Клиника 1. Слабость, упадок сил и общее недомогание

Клиника 2. Тремор (дрожание). Для паркинсонизма характерен тремор, возникающий в покое. Он обычно начинается в дистальном отделе одной руки, при прогрессировании заболевания распространяясь на противоположную руку и на ноги. Разнонаправленные движения большого и других пальцев внешне напоминают счёт монет или скатывание пилюль (схожесть с ручной техникой создания пилюль в фармацевтике). Иногда также отмечается дрожание головы по типу «да да» или «нет нет» , дрожание век, языка, нижней челюсти. В редких случаях оно охватывает всё тело.

Клиника 3. Гипокинезия — снижение спонтанной двигательной активности. Больной может застывать, часами сохраняя неподвижность. Характерна общая скованность. Активные движения возникают после некоторого промедления, темп их замедлен —брадикинезия]. Умывание, одевание или другие повседневные действия могут занимать несколько часов. Больной ходит мелкими шагами, ступни при этом располагаются параллельно другу — кукольная походка. Лицо маскообразное (амимия), взгляд застывший, мигания редкие. Улыбка, гримаса плача возникают с запозданием и так же медленно исчезают.

Клиника 4. Изменяется почерк – буквы более мелкие и угловатые «дрожащие» картинка(микрография)

Клиника 5. Одним из проявлений олигокинезии (уменьшение количества движений) является отсутствие физиологических синкинезий(содружественных движений). При ходьбе руки не совершают обычных размашистых движений, они остаются прижатыми к туловищу (ахейрокинез). При взгляде вверх не отмечается наморщивания лба. Сжатие пальцев в кулак не сопровождается разгибанием кисти. Больной не может выполнять несколько целенаправленных движений одновременно. Все действия напоминают автоматические.

Клиника 6. Мышечная ригидность — равномерное повышение тонуса мышц по пластическому типу. Конечности при их сгибании и разгибании застывают в приданном им положении. Такая форма повышения мышечного тонуса называется «пластической восковой гибкостью» . Преобладание ригидности в определённых группах мышц приводит к формированию характерной позы просителя(также называют «поза манекена» ): больной сутулится, голова наклонена вперёд, полусогнутые в локтевых суставах руки прижаты к телу, ноги также слегка согнуты в тазобедренных и коленных суставах. При пассивном сгибании разгибании предплечья, головы, круговых движениях в лучезапястном суставе можно ощутить своеобразную прерывистость, ступенчатость напряжения мышц — «симптом зубчатого колеса»


Клиника 7. Феномен Вестфаля, т. е нарушение возвращения конечности в исходную позицию после совершённого движения. 8. Лицо не меняет выражения и имеет вид маски, вплоть до полного исчезновения мимической активности.

Клиника 9. Постуральная неустойчивость развивается на поздних стадиях заболевания. У больного отмечаются затрудения преодоления как инерции покоя, так и инерции движения. Возникают явления пропульсии (лат. propulsio — проталкивание вперёд), латеропульсии и ретропульсии. Иногда у больных определяют «парадоксальные кинезии» , когда вследствие эмоциональных переживаний, после сна либо вследствие других факторов человек начинает свободно передвигаться, пропадают характерные для заболевания симптомы. Через несколько часов симптоматика возвращается

Клиника 10. Нарушение обмена веществ. Следствием может быть либо истощение (кахексия), либо ожирение. Секреторные расстройства проявляются сальностью кожных покровов, особенно лица, повышенным слюноотделением, избыточной потливостью.

Клиника 11. Возникает тяжелая хроническая депрессия и периоды оцепенения. Появляется пугливость и неуверенность в своих силах, боязнь общественных мероприятий, утрачивается мотивация. Сохраняется способность к здравым суждениям, но отмечаются нарушения памяти.

Клиника 12. Нарушения сна. При паркинсонизме затрудняются движения во время сна. Это приводит к нарушению его качества, ночным кошмарам и бессоннице. В результате днем больной ощущает сонливость. 13. Боли различной интенсивности 14. Дисфункция мочевого пузыря.

Клиника

Формы БП Дрожательно-ригидная форма. Акинетико-ригидная форма. Ригидно-дрожательная форма. Дрожательная форма. Акинетическая форма.

Паркинсонизм — неврологический синдром, который характеризуется рядом симптомов: тремором, мышечной ригидностью, постуральной неустойчивостью и брадикинезией. Ядро клинической картины паркинсонизма представляет собой акинетико-ригидный синдром

Классификация паркинсонизма 1. Первичный (идиопатический) паркинсонизм: Болезнь Паркинсона Ювенильный паркинсонизм

2. Вторичный паркинсонизм: Постэнцефалитический, Лекарственный, Сосудистый, Токсический, Травматический, Паркинсонизм, связанный с тиреоидными нарушениями, гипотиреоидизмом, гепатоцеребральной дегенерацией, опухолью мозга, гидроцефалией, сирингомезенцефалией

3. Паркинсонический синдром при мультисистемной дегенерации — «паркинсонизм плюс» : Прогрессирующий супрануклеарный паралич (синдром Стила—Ричардсона), Синдром Шая—Драйжера, Стриато нигральная дегенерация,

Комплекс паркинсонизм—деменция—боковой амиотрофический склероз, Кортико базальная дегенерация Болезнь диффузных телец Леви, Болезнь Галлервордена—Шварца, Оливо понто церебральная

Группы паркинсонизма идиопатический паркинсонизм генетические формы паркинсонизма, семейный синдром паркинсонизма — наследственная форма, обозначается локализацией гена (например, PARK 1) паркинсонизм в рамках других нейродегенеративных заболеваний (атипичные формы паркинсонизма, иногда называемые благодаря дополнительным симптомам «синдром паркинсонизм плюс» ) симптоматические синдромы Паркинсона — например, как следствие некоторых медикаментов, амфетаминов, травм, опухолей, действия токсических веществ, эндокринно метаболических нарушений, воспалительно инфекционных заболеваний

Стадии паркинсонизма по Хён и Яру (Hoehn, Yahr, 1967 Стадия 0 — нет признаков заболевания. Стадия 1 — симптомы проявляются на одной из конечностей. Стадия 1, 5 — симптоматика проявляется на одной из конечностей и туловище. Стадия 2 — двусторонние проявления без постуральной неустойчивости. Стадия 2, 5 — двусторонние проявления с постуральной неустойчивостью. Больной способен преодолевать инерцию движения, вызванную толчком.

Стадии паркинсонизма по Хён и Яру (Hoehn, Yahr, 1967 Стадия 3 — двусторонние проявления. Постуральная неустойчивость. Больной способен к самообслуживанию. Стадия 4 — обездвиженность, потребность в посторонней помощи. При этом больной способен ходить и/или стоять без поддержки. Стадия 5 — больной прикован к креслу или кровати. Тяжёлая инвалидизация.

Диагностика Болезни Паркинсона


Выделяют три группы заболеваний, вызывающих паркинсонизм 1. К первичному паркинсонизму относят Дегенеративные заболевания идиопатического или наследственного характера, при котором паркинсонизм является единственным или доминирующим проявлением (болезнь Паркинсона и аутосомно рецессивный юношеский паркинсонизм). 2. Вторичный (симптоматический) паркинсонизм является осложнением приобретенных заболеваний известной этиологии, интоксикаций или побочным действием лекарственных препаратов (например, лекарственный или сосудистый паркинсонизм).

3. Паркинсонизм при мультисистемных дегенерациях центральной нервной системы сопровождается другими неврологическими синдромами (пирамидным, мозжечковым, вегетативной недостаточностью, деменцией) (паркинсонизм – плюс), которые связаны с поражением иных, помимо экстрапирамидных, систем мозга. К этой же группе относят и наследственные метаболические заболевания ЦНС (например, гепатолентикулярная дегенерация), при которых, в отличие от вышеупомянутых болезней, известен метаболический субстрат.

Диагностика синдрома паркинсонизма . Гипокинезия в сочетании не менее чем с одним из следующих симптомов: Мышечная ригидность. Тремор покоя 4 6 Гц. Постуральная неустойчивость, не связанная с первичными зрительными, вестибулярными, мозжечковыми или проприоцептивными нарушениями.

Критерии, подтверждающие диагноз Болезни Паркинсона ( не менее 3 х) Одностороннее начало. Тремор покоя. Прогрессирующее течение. Сохранение асимметрии симптоматики с преобладанием на первоначально вовлеченной стороне. Высокая эффективность препаратов леводопы (уменьшение симптомов на 70 100%). Выраженные хореиформные дискинезии, индуцированные леводопой. Сохранение реакции на леводопу в течение 5 лет и более. Течение заболевания в течение 10 лет и более.

Диагностика БП Общий анализ крови Общий анализ мочи Биохимическое исследование крови: мочевина, креатинин, общий белок, Ал. АТ, Ас. АТ, билирубин, глюкоза, электролиты (Na, K, Cа общий) ЭКГ Консультация окулиста (глазное дно, острота зрения, поля зрения) Консультация терапевта.

Специальные методы диагностики БП Компьютерная томография. Позитронно эмиссионная томография мозга (ПЭТ) Однофотонная эмиссионная компьютерная томография (ОФЭКТ)

Магнитно-резонансная томография (МРТ) Транскраниальная сонография (TКС, Doppler - сонография) Электроэнцефалограмма (ЭЭГ) Метод вызванных потенциалов Электронейромиография и электромиография (ЭНМГ и ЭМГ). Электромиография Л-ДОФА тестирование.

Лечение Болезни Паркинсона Основное направление в лечении паркинсонизма – восполнение дефицита дофамина, а также – торможение разрушения дофаминергических нейронов и стимуляция производства дофамина.

Придерживаются следующих принципов лечения болезни Паркинсона: Лечение необходимо назначать не позже полугода после обращения пациента. После установки диагноза пациент обязательно непрерывно должен принимать противопаркинсонические препараты до конца жизни Препарат подбирается индивидуально. при отсутствии эффекта монотерапии назначается комбинированное лечение двумя препаратами с аналогичным определением оптимальной дозировки, при появлении устойчивых побочных эффектов от применения отдельных препаратов – необходимо уменьшить дозу или заменить на другой, долгая терапия препаратами леводопы приводит к клиническому патоморфозу, что требует специальной корректировки в лечении.

Лечение БП В лечении болезни Паркинсона можно выделить три основных направления : 1) нейпротекторную терапию, целью которой является замедлить или остановить дегенерацию нейронов головного мозга. 2) симптоматическую терапию, позволяющую уменьшить основные симптомы заболевания за счет коррекции возникающего в мозге нейрохимического и нейрофизиологического дисбаланса. 3) физическую и социально психологическую реабилитацию.

В настоящее время к числу противопаркинсонических средств, применяемых при болезни Паркинсона, относят 6 групп лекарственных средств: препараты, содержащие леводопу, агонисты дофаминовых рецепторов, холинолитики (антихолинергические средства), препараты амантадина, ингибиторы моноаминооксидазы типа В, ингибиторы катехол О метилтрансферазы.

Задачей терапии является восстановление нарушенных двигательных функций при использовании минимальных эффективных доз препаратов.

Препараты левадопы В настоящее время препараты леводопы остаются наиболее эффективными противопаркинсоническими средствами, “золотым стандартом” лечения Препараты леводопы эффективны в отношении всех основных симптомов заболевания – гипокинезии, тремора, ригидности. Терапевтическое действие наступает у 95% больных болезнью Паркинсона.

Побочные эффекты леводопы Периферические Тошнота Рвота Тахикардия Приступы гипергидроза Ортостатическая гипотензия центральные (галлюцинации и другие психические изменения, затрудненное засыпания или сонливость, дискинезии).

Центральные Галлюцинации и другие психические изменения Затрудненное засыпания или сонливость Дискинезии

Агонисты дофаминергических рецепторов Способны непосредственно стимулировать дофаминовые рецепторы на стриарных нейронах в обход дегенерирующих нигростриарных клеток, имитируя действие эндогенного медиатора Агонисты дофаминергических рецепторов подразделяют на два класса : эрголиновые : бромокриптин, перголида мезилат, каберголин неэрголиновые: апоморфин, прамипексол, пирибедил.

В настоящее время в нашей стране для лечения болезни Паркинсона применяют 3 препарата агонистов дофаминергических рецепторов: бромокриптин, прамипексол и пирибедил, все они главным образом стимулируют D 2 рецепторы, прамипексол и пирибедил, кроме того, имеют особое сродство к D 3 рецепторам, однако неясно, насколько это предопределяет особенности клинического действия препарата.

Ингибиторы катехол-Ометилтрансферазы Энтакапон Толкапон Основное показание к назначению ингибитора катехол О метилтрансферазы – наличие феномена «истощения» действия конца дозы.

Ингибиторы катехол-Ометилтрансферазы Побочные эффекты: Усиление дискинезий Тошноты Ортостатической гипотензии Зрительных галлюцинаций Нарушения сна Изменение окраски мочи Диарея

Ингибиторы моноаминоксидазы В В настоящее время в клинической практике применяется лишь один препарат, избирательно ингибирующий моноаминооксидаза типа В – селегилин. Помимо торможения моноаминооксидаза В, селегилин тормозит обратный захват дофамина из синаптической щели. В целом противопаркинсонический эффект селегилина невелик, хотя и способен отсрочить назначение леводопы на 8 10 месяцев.

Препараты амантадина хлорид амантадина сульфат

При применении амантадина возможны существенные центральные побочные эффекты в виде: Спутанности сознания Беспокойства Галлюцинаций Сухости во рту. У части больных развиваются отеки лодыжек и livedo reticularis.

Холинолитические препараты. Холинолитики существенно менее эффективны, чем леводопа, и их применение оправдано главным образом при наличии тремора покоя. Применение холинолитиков ограничивают их побочные эффекта.

Побочные эффекты Мидриаз (и поэтому противопоказаны при закрытоугольной глаукоме) сухость во рту провоцируют задержку мочи (особенно у мужчин с гиперплазией предстательной железы) Но наиболее серьезные побочные действия – усиление когнитивных нарушений и способность вызывать состояние спутанности и зрительные галлюцинации. Эти осложнения чаще возникают у пожилых.

Исключительно важное значение при определении начальной терапии имеют возраст больного и состояние психических функций

Принципы выбора противопаркинсонического препарата. Выбор препарата на начальном этапе лечения проводят с учетом возраста, выраженности двигательного дефекта, трудового статуса, состояния нейропсихологических функ ций, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента. Помимо достижения оптимального симптоматического контроля, выбор препарата определяется необходимостью отсрочить момент развития моторных флуктуаций и дискинезий (табл. ).


У лиц моложе 50 лет при умеренной выраженности двигательных нарушений в отсутствие выраженных когнитивных нарушений назначают один из следующих препаратов: агонист дофаминовых рецепторов, ингибитор моноаминооксидазы (МАО) типа В (селегилин), амантадин, антихолинергические сред ства (тригексифенидил, бипериден). У лиц старше 70 лет лечение следует начинать со средств, содержащих леводопу. Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением

Алгоритм лечения БП

Немедикаментозные методы лечения. нейропсихологический тренинг речевая терапия лечебная гимнастика Регулярные физические упражнения, включающие аэробные упражнения в изометрическом режиме, на растяжение и координацию создание специальной службы

Хирургические методы лечения БП Деструктивные операции: Таламотомия или паллидотомия – эти операции представляют собой точечное изменение тех структур, в которых наблюдаются дегенеративные процессы. Эти методики применяются сегодня редко, они имеют наибольшую эффективность в начальных стадиях болезни. Таламотомия позволяет устранить тремор, который не купируется с помощью лекарственных средств, при этом симптомы брадикинезии сохраняются. Паллидотомия позволяет снизить интенсивность таких симптомов, как ригидность и гипокинезия.

Паллидотомия – это точечное разрушение очень маленькой зоны в глубокой части мозга (бледного шара), которая вызывает симптомы. Может быть назначена, если у больного наблюдается сильное двигательное расстройство. Таламотомия – это точечное разрушение очень маленькой зоны в глубокой части мозга (таламуса), которая вызывает симптомы. Такая операция показана, если основным симптомом болезни является тремор.

Хирургическое лечение БП Стереотоксический метод лечения В Беларуси закуплена одна из лучших стереотаксических систем в мире — Leksell, признанная мировым стандартом стереотаксиса. Станция планирования помогает рассчитывать цель с допуском в 0, 6 мм. Имеет 5 программ, позволяющих проводить общие стереотаксические операции (например, биопсии опухолей), функциональные (при болезни Паркинсона); совмещать изображения КТ и МРТ, радиоизотопных исследований электронно эмиссионной томографии — для получения координат цели мишени; располагает электронным атласом мозга, с помощью которого также определяется точка мишень и контролируется точность попадания.


Лечение в Израиле

Глубокая стимуляция мозга – это метод лечения болезни Паркинсона, некоторых видов тремора и других нарушений движений, при котором происходит подавление активности участков мозга, ответственных за симптомы этих болезней. При глубокой стимуляции головного мозга, специальные электроды вводятся в таламус (для лечения обычного тремора и рассеянного склероза)

Преимущества ГСМ имеет меньше осложнений, чем деструктивные операции электрическая стимуляция является регулируемой Стимулятор можно также отключить в любое время

Насколько эффективна операция? У подавляющего большинства людей (свыше 70%) наблюдается значительное облегчение всех симптомов, связанных с болезнью Паркинсона.

Лечение в Германии Транскраниальная магнитная стимуляция мозга (ТМС) при болезни Паркинсона Лечение стволовыми клетками болезни Паркинсона Физиотерапия при болезни Паркинсона

В новом исследовании американских ученых обнаружился интересный факт: люди, которые регулярно едят ягоды и цитрусовые, защищаются тем самым от тяжелого неврологического заболевания – болезни Паркинсона.

Продолжительность жизни людей с болезнью Паркинсона зависит от своевременной постановки диагноза и эффективности лечения. При обнаружении заболевания на ранних стадиях, эффективного медикаментозного лечения, соблюдения диеты и правильного образа жизни, а также при регулярном проведении различных физиопроцедур (массаж, гимнастика) продолжительность жизни практически не изменяется.

Каков прогноз при болезни Паркинсона? Так как болезнь Паркинсона является неизлечимой, прогноз этого заболевания, как правило, неблагоприятный. Прогрессирование болезни остановить невозможно. Оно зависит от множества факторов, включая генетические, физиологические, экологические и др. Однако, при эффективном лечении, проведении различных физиопроцедур и соблюдении адекватной диеты развитие заболевания можно замедлить, а качество жизни – улучшить.


Спасибо за внимание!
Болезнь Паркинсона (Анастасия Ашуйко).pptx