Лечение болезни Паркинсона.pptx
- Количество слайдов: 32
Болезнь Паркинсона. Лечение. Подготовила врач-интерн Хотько В. А.

Точки приложения патогенетической терапии: Коррекция дисфункции дофаминергической, норадренергической, серотонинергической и холинергической систем; Стимуляция субталамических ядер; Деструктивные операции (паллидотомия, таламотомия).

Влияние на холинергическую систему. Дофамин синтезируется в черной субстанции и аксональным транспортом доставляется в хвостатое ядро. Изучение распределения ацетилхолина в разных структурах головного мозга показало, что наибольшая его концентрация характерна для хвостатого ядра. В норме дофамин оказывает тормозное влияние на хвостатое ядро, тем самым уменьшая его холинергическую активность.

При болезни Паркинсона (БП) имеют место дефицит дофамина в мозге и одновременное избыточное содержание ацетилхолина в некоторых структурах мозга, причем второй феномен является прямым следствием первого.

Действие антихолинергических препаратов основано на коррекции функционального состояния хвостатого ядра. Применяются М-холинолитики: Препараты биперидена (Akineton) Препараты тригексифенидила (Cyclodol) табл. по 1 -2 мг 2 -3 раза в день до достижения эффекта (в среднем до 6 мг/сут).

В настоящее время назначаются относительно молодым пациентам (до 55 лет) с дрожательными формами БП при сохранных когнитивных функциях. Достоинства Недостатки Относительно высокая эффективность при треморе покоя Незначительный контроль гипокинезии и ригидности Уменьшение слюнотечения у некоторых пациентов Ухудшение когнитивных функций Высокая частота побочных эффектов

Побочные эффекты: Нечеткость зрения, задержка мочеиспускания, тошнота, запоры, сухость во рту. Нарушение кратковременной памяти и запоминания, острые психотические нарушения. Противопоказания: Закрытоугольная глаукома; Непроходимость ЖКТ, мегаколон; Тахиаритмии; ДГПЖ и др. .
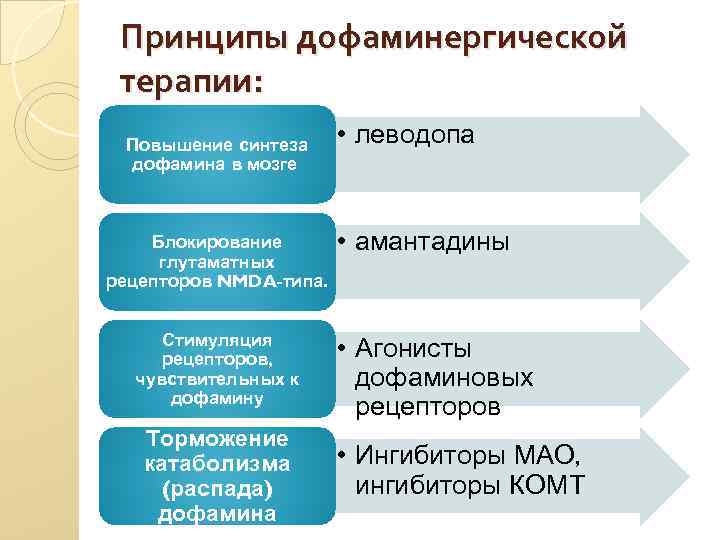
Принципы дофаминергической терапии: Повышение синтеза дофамина в мозге Блокирование глутаматных рецепторов NMDA-типа. Стимуляция рецепторов, чувствительных к дофамину Торможение катаболизма (распада) дофамина • леводопа • амантадины • Агонисты дофаминовых рецепторов • Ингибиторы МАО, ингибиторы КОМТ

Повышение синтеза дофамина в мозге. Леводопа (L-диоксифенилаланин) – нейтральная аминокислота, превращающаяся в дофамин путем декарбоксилирования и возмещающая дефицит дофамина в головном мозге. Превращение в дофамин в периферических тканях – причина побочных эффектов (тошноты, рвоты). Как правило применяется с периферическим ингибитором ДОФАдекарбоксилазы (бенсеразидом, карбидопой).
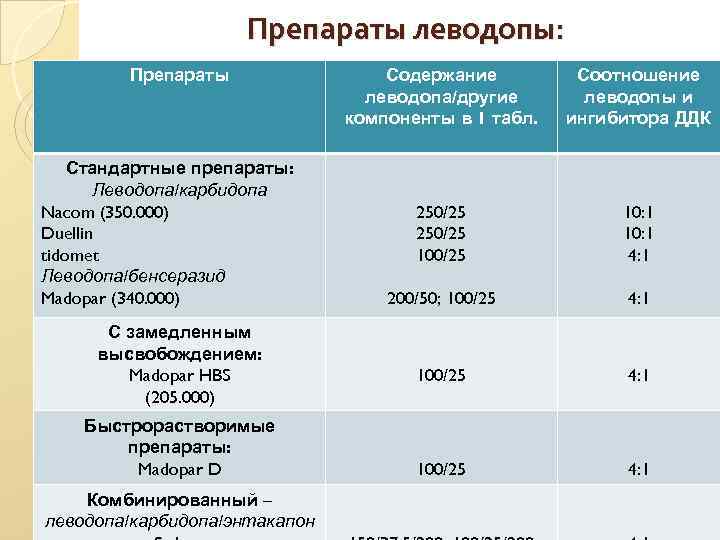
Препараты леводопы: Препараты Стандартные препараты: Леводопа/карбидопа Nacom (350. 000) Duellin tidomet Леводопа/бенсеразид Madopar (340. 000) С замедленным высвобождением: Madopar HBS (205. 000) Быстрорастворимые препараты: Madopar D Комбинированный – леводопа/карбидопа/энтакапон Содержание леводопа/другие компоненты в 1 табл. Соотношение леводопы и ингибитора ДДК 250/25 100/25 10: 1 4: 1 200/50; 100/25 4: 1

Режим дозирования: Начальная терапия На ранней стадии БП рекомендуется начинать лечение с приема 50 мг леводопы 2 -3 раза в сутки. Затем дозу постепенно повышают (не быстрее чем 1 раз в 7 дней) до достижения оптимального эффекта (как правило 300 -800 мг/сут в 3 -5 приемов). Дальнейшее увеличение суточной дозы, в случае необходимости, следует проводить с интервалами в 1 месяц. При переходе на препарат Madopar HBS Дозу необходимо увеличить на 20% (в связи с меньшей биодоступностью). Часто прибегают к комбинации стандартного и пролонгированного препаратов. Последний принимают на ночь.
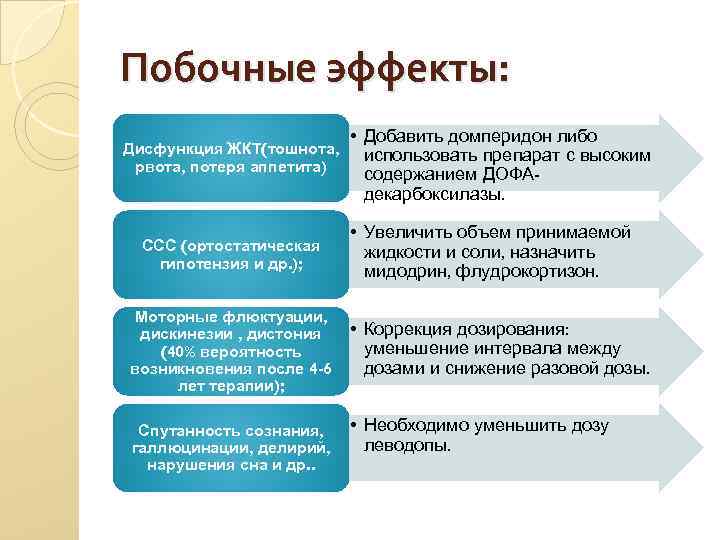
Побочные эффекты: Дисфункция ЖКТ(тошнота, рвота, потеря аппетита) ССС (ортостатическая гипотензия и др. ); Моторные флюктуации, дискинезии , дистония (40% вероятность возникновения после 4 -6 лет терапии); Спутанность сознания, галлюцинации, делирий, нарушения сна и др. . • Добавить домперидон либо использовать препарат с высоким содержанием ДОФАдекарбоксилазы. • Увеличить объем принимаемой жидкости и соли, назначить мидодрин, флудрокортизон. • Коррекция дозирования: уменьшение интервала между дозами и снижение разовой дозы. • Необходимо уменьшить дозу леводопы.

Блокирование глутаматных рецепторов NMDA-типа. Применяются антиглутаматергические средства: Амантадина гидрохлорид (Midantan) Амантадина сульфат (PK-Merz)

Механизм действия: стимулирует выброс дофамина из пресинаптических окончаний, уменьшает обратный захват дофамина в синапсе, тормозит глутаматергические влияния лобной коры на полосатое тело, обладает отчетливым холиноблокирующим эффектом. как антагонист глутаматных рецепторов способен реализовать свое действие на уровне «эксайтотоксического каскада» .

L-глутамат — главный возбуждающий медиатор в мозге человека и животных. Глутамат обнаруживается во всех отделах ЦНС, так как он является не только нейромедиатором, но и предшественником других аминокислот. может вызывать повреждение и смерть дофаминергических нейронов, в связи с чем повреждающее действие глутамата на нейроны обозначено термином «токсичность возбуждающих аминокислот» или «эксайтотоксичность» Эксайтотоксичность глутамата опосредуется NMDA-рецепторами, названными по специфическому антагонисту N-метил-Dаспартату.

Режим дозирования: Начинают со 100 мг утром, постепенно увеличивая дозу каждую неделю до 300 -600 мг/сут. У части пациентов через несколько месяцев возникает толерантность (необходим перерыв в приеме препарата). При злокачественном нейролептическом синдроме, декомпенсации БП, акинетическом кризе - PK-Merz 200 мг в/в капельно 1 -3 раза в день, в течение 7 -14 дней, с последующим переходом на таблетированную форму.

Стимуляция рецепторов, чувствительных к дофамину: В настоящий момент выделяют 5 подтипов D-рецепторов: свойства D 1 рецепторов - D 1, D 5, свойства D 2 рецепторов - D 2, D 3, D 4. Подтипы дофаминовых рецепторов отличаются различной локализацией на пре- и постсинаптических мембранах и разной чувствительностью к эндогенному дофамину и к агонистам дофаминовых рецепторов (АДР).
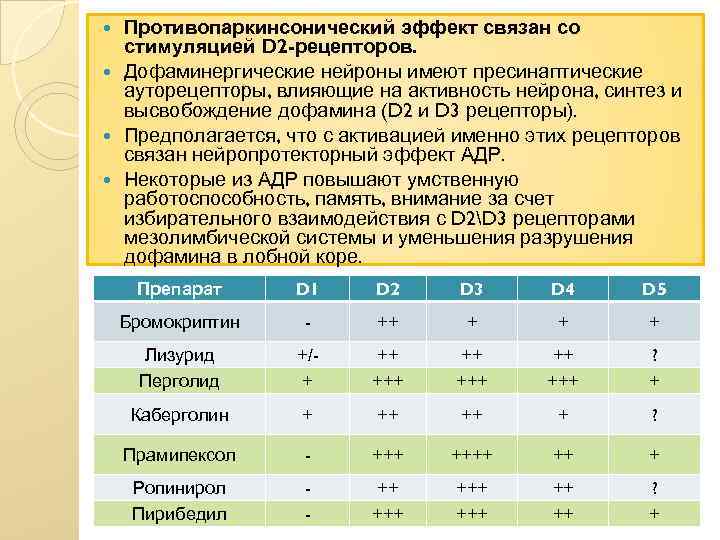
Противопаркинсонический эффект связан со стимуляцией D 2 -рецепторов. Дофаминергические нейроны имеют пресинаптические ауторецепторы, влияющие на активность нейрона, синтез и высвобождение дофамина (D 2 и D 3 рецепторы). Предполагается, что с активацией именно этих рецепторов связан нейропротекторный эффект АДР. Некоторые из АДР повышают умственную работоспособность, память, внимание за счет избирательного взаимодействия с D 2D 3 рецепторами мезолимбической системы и уменьшения разрушения дофамина в лобной коре. Препарат D 1 D 2 D 3 D 4 D 5 Бромокриптин - ++ + Лизурид Перголид +/+ ++ +++ ? + Каберголин + ++ ++ + ? Прамипексол - ++++ ++ + Ропинирол Пирибедил - ++ +++ ++ ++ ? +
Пирибедил (Pronoran 140. 000): 50 мг; увеличивает кровоснабжение тканей мозга, обладает вазодилатирующим действием. Каберголид (Dostinex 160. 000, Kaberlin 70. 000): 0, 5 мг; период полуэлиминации – 65 ч (оптимальное средство для коррекции ночных симптомов). Прамипексол (Mirapex)

Достоинства и недостатки АДР: Достоинства Сопоставимая с леводопой эффективность на ранних стадиях при монотерапии Влияние на тремор Снижение риска развития моторных флуктуаций и лекарственных дискинезий Возможность снижения дозы леводопы за счет аддитивного дофаминергического эффекта Коррекция уже развившихся моторных флуктуаций и лекарственных дискинезий Антидепрессивный эффект у ряда АДР Улучшение когнитивных функций Возможный нейропротекторный эффект Недостатки Относительно высокая частота побочных эффектов (нейропсихические расстройства, нарушения сна)

Торможение катаболизма (распада) дофамина. Предполагается, что 80% дофамина, высвободившегося в синаптическую щель, утилизируется двумя путями – либо подвергается обратному захвату, либо инактивируется при помощи МАО-Б и КОМТ.
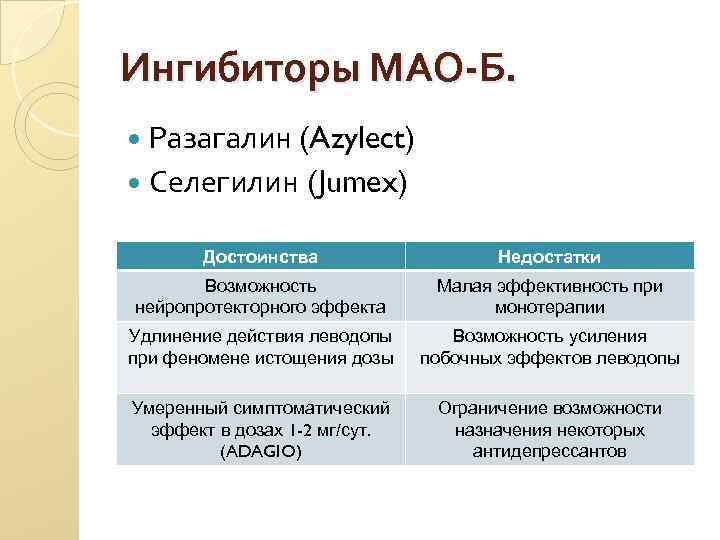
Ингибиторы МАО-Б. Разагалин (Azylect) Селегилин (Jumex) Достоинства Недостатки Возможность нейропротекторного эффекта Малая эффективность при монотерапии Удлинение действия леводопы при феномене истощения дозы Возможность усиления побочных эффектов леводопы Умеренный симптоматический эффект в дозах 1 -2 мг/сут. (ADAGIO) Ограничение возможности назначения некоторых антидепрессантов

Ингибиторы КОМТ. Энтакапон (Comtan, Stalevo) Толкапон (Tasmar) Препятствуют метаболизму леводопы, увеличивая период полувыведения и пролонгируя ее действие. Назначают только в комбинации с леводопой и только для коррекции моторных флюктуаций!

Лечение поздней (осложненной) стадии БП. Двигательные: 1. Моторные флюктуации 2. Дискинезии 1. 2. 3. 4. 5. 6. Недвигательны е: Деменция Психоз Депрессия Ортостатическая гипотензия Нарушение моторики ЖКТ Нарушения сна.

Моторные флюктуации: Феномен «конца дозы» – после приема дозы леводопы клиническое улучшение наблюдается только на короткое время. Скорректировать дозу леводопы до 4 -6 кратного приема. Добавить ингибитор КОМТ или МАО-Б. Добавить дофаминовые агонисты (причем препаратами выбора являются неэрголиновые АДР). Сменить стандартную форму леводопы на форму с контролируемым высвобождением. Добавить амантадин или антихолинергические препараты.

Дискинезии: «эффект пика дозы» – обычно проявляются хореическим гиперкинезом, иногда дистонии или миоклонус. Добавить амантадин (200 -400 мг/сут). Снизить разовую дозу леводопы при увеличении кратности приема. Глубокая стимуляция субталамических ядер (позволяет уменьшить дофаминергическую терапию)

Деменция: Распространенность около 30 -40%. Наибольший фактор риска развития – возраст пациента. Отменить препараты, потенциально вызывающие деменцию (антихолинергические, амантадин, трициклические антидепрессанты и др. ) Добавить ингибиторы ацетилхолинэстеразы (ривастигмин, донепезил, галантамин)
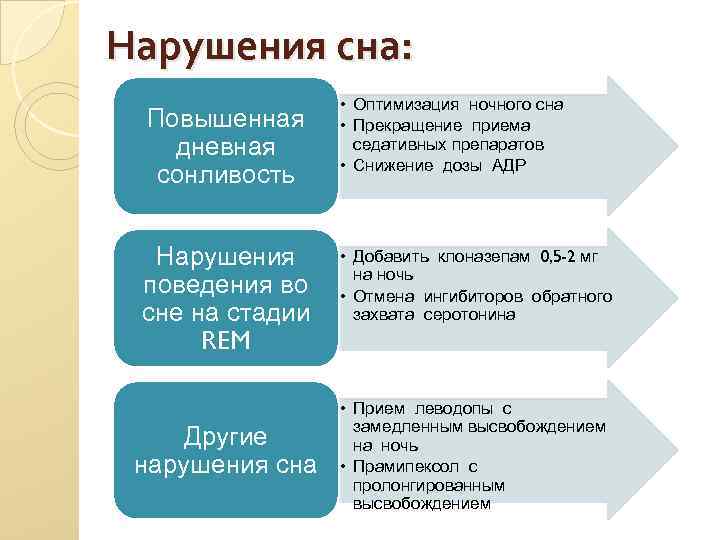
Нарушения сна: Повышенная дневная сонливость Нарушения поведения во сне на стадии REM Другие нарушения сна • Оптимизация ночного сна • Прекращение приема седативных препаратов • Снижение дозы АДР • Добавить клоназепам 0, 5 -2 мг на ночь • Отмена ингибиторов обратного захвата серотонина • Прием леводопы с замедленным высвобождением на ночь • Прамипексол с пролонгированным высвобождением
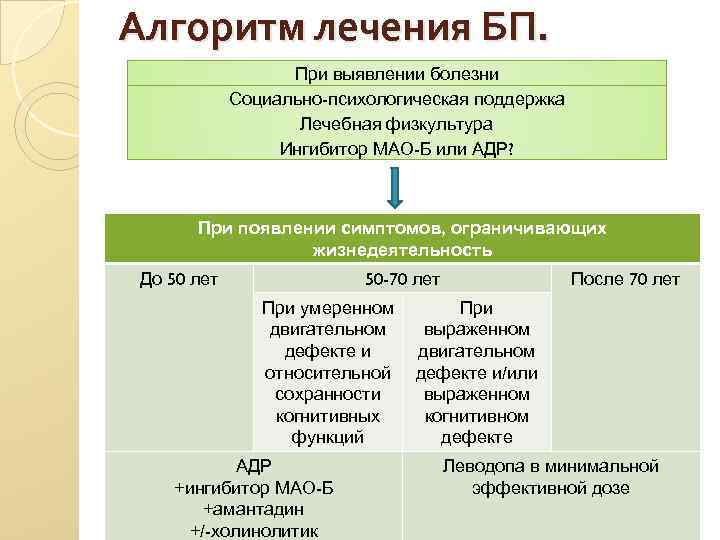
Алгоритм лечения БП. При выявлении болезни Социально-психологическая поддержка Лечебная физкультура Ингибитор МАО-Б или АДР? При появлении симптомов, ограничивающих жизнедеятельность До 50 лет 50 -70 лет При умеренном двигательном дефекте и относительной сохранности когнитивных функций АДР +ингибитор МАО-Б +амантадин +/-холинолитик После 70 лет При выраженном двигательном дефекте и/или выраженном когнитивном дефекте Леводопа в минимальной эффективной дозе
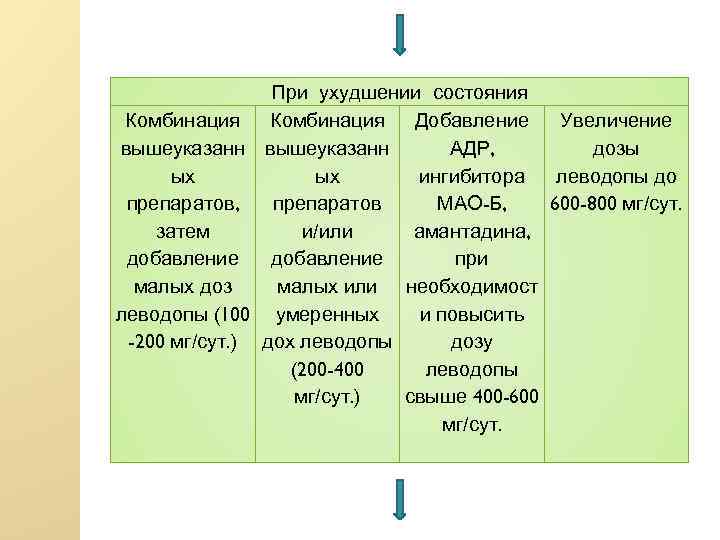
При ухудшении состояния Комбинация Добавление Увеличение вышеуказанн АДР, дозы ых ых ингибитора леводопы до препаратов, препаратов МАО-Б, 600 -800 мг/сут. затем и/или амантадина, добавление при малых доз малых или необходимост леводопы (100 умеренных и повысить -200 мг/сут. ) дох леводопы дозу (200 -400 леводопы мг/сут. ) свыше 400 -600 мг/сут.
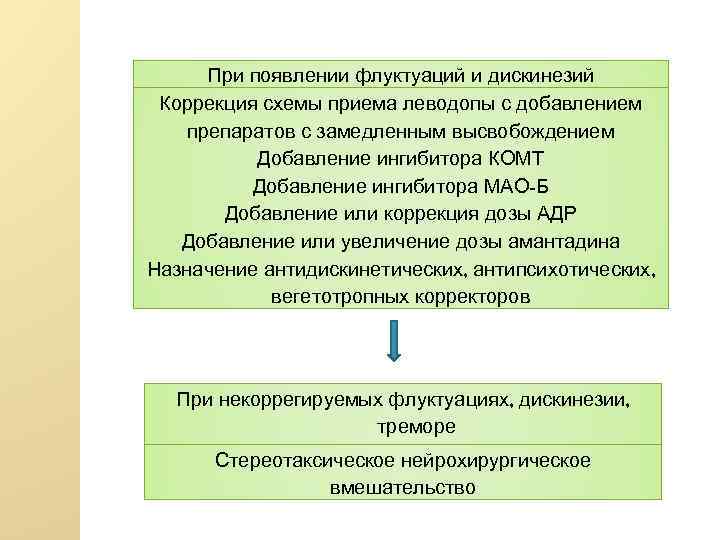
При появлении флуктуаций и дискинезий Коррекция схемы приема леводопы с добавлением препаратов с замедленным высвобождением Добавление ингибитора КОМТ Добавление ингибитора МАО-Б Добавление или коррекция дозы АДР Добавление или увеличение дозы амантадина Назначение антидискинетических, антипсихотических, вегетотропных корректоров При некоррегируемых флуктуациях, дискинезии, треморе Стереотаксическое нейрохирургическое вмешательство

Литература: Карабань И. Н. «Применение блокатора глутаматных рецепторов амантадина в неврологии» . Международный неврологический журнал 2 (48) 2012 г. В. Л. Голубев «Лечение болезни Паркинсона (решённые и нерешённые вопросы)» . Н. В. Федорова Кафедра неврологии РМАПО Центр экстрапирамидных заболеваний МЗ РФ «Агонисты дофаминовых рецепторов – препараты выбора терапии ранних стадий болезни Паркинсона» . «Биохимия паркинсонизма» http: //meduniver. com Левин О. С. «Основные лекарственные средства, применяемые в неврологии» . EFNS «Клинические рекомендации по неврологии» . М. Г. Привес «Анатомия человека» . M. Da Prada «Периферическое ингибирование декарбоксилазы: биохимическое сравнение бенсеразида и карбидопы» . Современные проблемы и ведение болезни Паркинсона (материалы симпозиума, Базель, апрель 1984), изд-во “Рош”, 1985 г.
Лечение болезни Паркинсона.pptx