Лекция Благородные газы.ppt
- Количество слайдов: 19

Благородные (инертные) газы

Элементы нулевой группы периодической системы: 2 He - гелий 10 Ne - неон 18 Ar - аргон 36 Kr - криптон 54 Xe - ксенон 86 Rn - радон
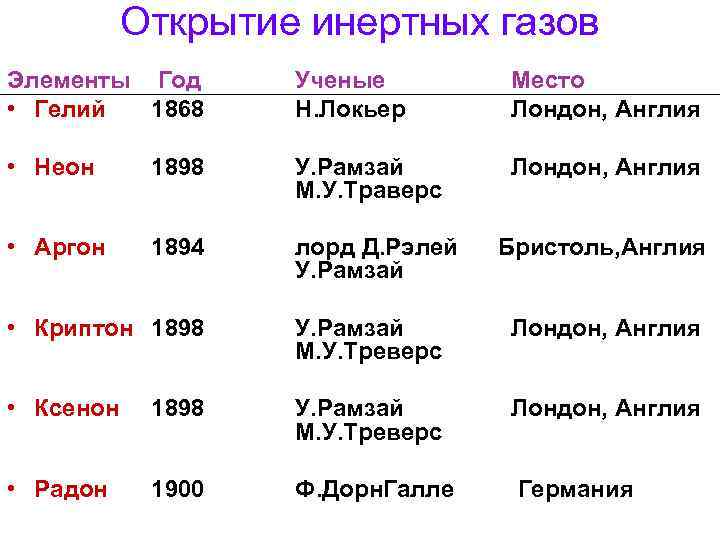
Открытие инертных газов Элементы Год • Гелий 1868 Ученые Н. Локьер Место Лондон, Англия • Неон 1898 У. Рамзай М. У. Траверс Лондон, Англия • Аргон 1894 лорд Д. Рэлей Бристоль, Англия У. Рамзай • Криптон 1898 У. Рамзай М. У. Треверс Лондон, Англия • Ксенон 1898 У. Рамзай М. У. Треверс Лондон, Англия • Радон 1900 Ф. Дорн. Галле Германия

Электронная конфигурация и структура атомов Ø На внешнем электронном уровне все инертные газы содержат октет электронов. Ø Следствие завершенности электронных оболочек – высокий потенциал ионизации.

Явление сверхтекучести гелия Было открыто в 1938 г. российским ученым П. Л. Капицей. Сверхтекучий гелий имеет настолько низкую вязкость, что движется практически без трения, ему не передается вращение земли, и он способен течь вверх. Также сверхтекучий гелий просачивается через тончайшие поры неглазурованного керамического сосуда.
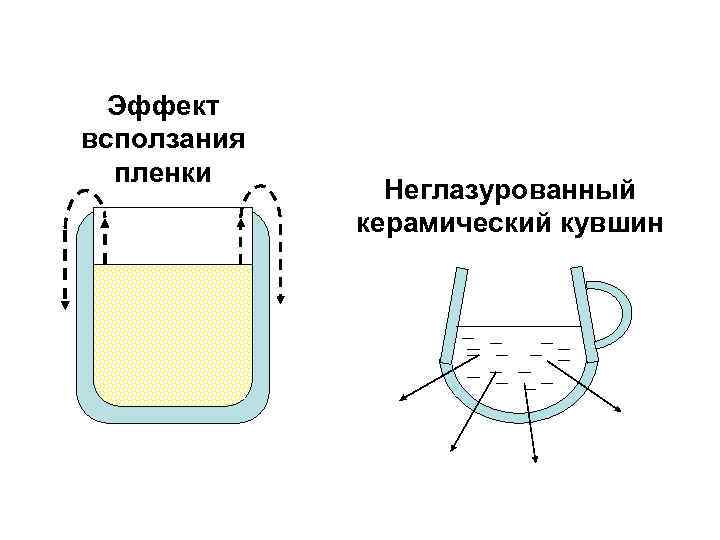
Эффект всползания пленки Неглазурованный керамический кувшин

Ионизация атомов инертных газов возможна, когда на электроды разрядных трубок, содержащие инертные газы, подают высокое напряжение. При этом наблюдается свечение.
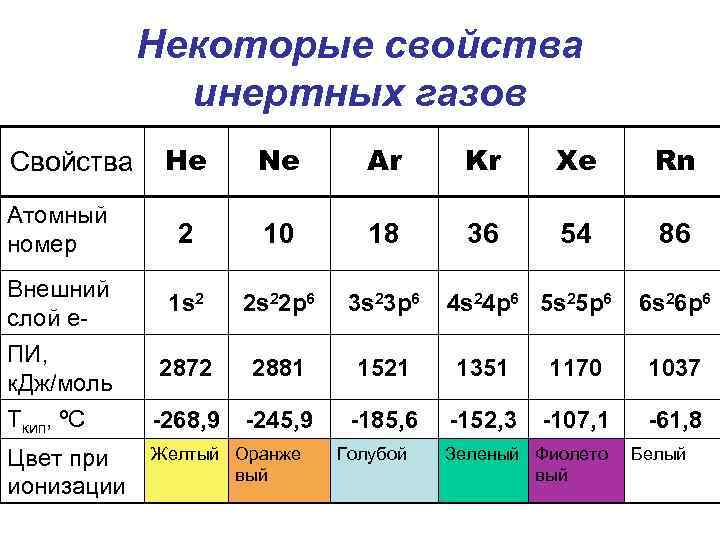
Некоторые свойства инертных газов He Ne Ar Kr Xe Rn Атомный номер 2 10 18 36 54 86 Внешний слой е- 1 s 2 2 s 22 p 6 3 s 23 p 6 2872 2881 1521 1351 1170 1037 -268, 9 -245, 9 -185, 6 -152, 3 -107, 1 -61, 8 Свойства ПИ, к. Дж/моль Ткип, ºС Цвет при ионизации Желтый Оранже вый Голубой 4 s 24 p 6 5 s 25 p 6 Зеленый Фиолето вый 6 s 26 p 6 Белый

Нахождение в природе • Большинство инертных газов – редкие элементы. Они сосредоточены в атмосфере (за исключением Rn) и могут быть получены фракционированной перегонкой жидкого воздуха. • Rn накапливают в результате радиоактивного распада солей Ra. • He выделяют из природного газа (США, Оренбург) или из воды некоторых минеральных источников.

Применение инертных газов Не 1. Наполняют баллоны и лампы дневного света 2. Смесь Не/О 2 используется для глубоководного дыхания вместо N 2/O 2 3. Разжижающие для газообразных анестетиков 4. Смесь Не/О 2 используется для дыхания респираторных больных 5. Используется для передачи тепла в ядерных реакторах 6. В промышленности для сварки легко окисляющихся металлов необходима инертная атмосфера гелия 7. Жидкий Не используется для поддержания низких температур

Ne Ar Kr Xe Rn Неоновые лампы 1. В промышленности для сварки металлов необходима инертная атмосфера аргона 2. Заполняют лампы накаливания Заполняют фонари, находящиеся на взлетной полосе самолетов Смесь Хе и Kr используется для вспышки в фотографировании Лечение пораженных раком тканей

Физиологическое действие инертных газов Вдыхание высших инертных газов в смеси с кислородом (кроме гелия и аргона) приводит человека в состояние, сходное с опьянением алкоголем. Наркотическое действие инертных газов обуславливается растворением в нервных тканях. Чем выше атомный вес инертного газа, тем больше его растворимость и тем сильнее его наркотическое действие.

Химические свойства ü Образуют гидраты (клатраты) постоянного состава Ar· 5, 5 H 2 O; Kr· 5 H 2 O. Клатратные соединения используют для разделения и хранения благородных газов.

Нил Бартлетт в 1962 г. установил: газообразный гексафторид платины Pt. F 6 – сильнейший из всех известных окислителей, настолько сильный, что может отнимать электрон у молекулярного кислорода. В результате было получено твердое вещество красного цвета – диоксигенилгексафторплатинат O 2+[Pt. F 6]–, – которое содержало молекулярный катион кислорода O 2+. Pt. F 6 + O 2 = O 2+[Pt. F 6]- ü Pt. F 6 + Хе = Хе+[Pt. F 6]-

ü После открытия Бартлетта были синтезированы различные соединения Хе и Kr (ст. окисл. : +2, +4, +6, +8) При обычной Т: Хе + F 2 = Хе. F 2 Т=400 °С: Хе + 2 F 2 = Хе. F 4 При нагревании и повышенном давлении фтора: Хе + 3 F 2 = Хе. F 6 И далее: Хе + 4 F 2 = Хе. F 8

• После статьи Бартлетта в журнале «Proceedings of the Chemical Society» за 1962 год, посвященной сделанному им открытию, его эксперимент повторила группа американских исследователей во главе с Черником в Аргоннской национальной лаборатории. • Так был развеян миф об абсолютной инертности благородных газов и заложено начало химии ксенона.

Химические свойства ксенона • Неустойчивая кислота шестивалентного ксенона H 6 Xe. O 6 образуется в результате гидролиза Xe. F 6 при 0° С: Xe. F 6+ 6 H 2 О =6 HF + H 6 Xe. O 6 + Ва (ОН)2 = Ва 3 Хе. О 6 + 6 H 2 О белый аморфный осадок Ксенонат бария 125° С Ва 3 Хе. О 6 = Ва. О + Хе + О 2 • Перксенонат натрия может быть выделен в виде бесцветного кристаллогидрата по реакции: Хе. О 3 + Na. OH = Na 4 Xe. O 6 · 6 Н 2 О

• В распоряжении химиков имеются весьма незначительные количества радона, тем не мене удалось установить, что он также взаимодействует с фтором, образуя нелетучие фториды. • Для криптона выделены и изучены дифторид Kr. F 2 и тетрафторид Kr. F 4 по свойствам, напоминающим соединения ксенона.
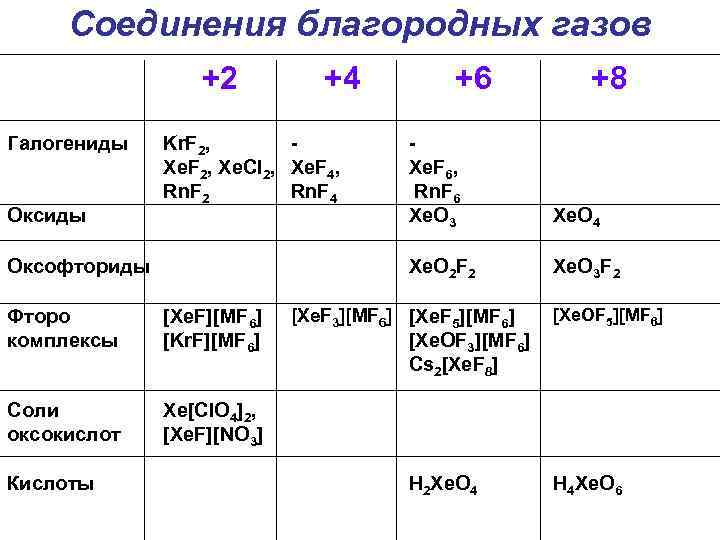
Соединения благородных газов Галогениды +2 +6 +8 Xe. F 4, Rn. F 4 Xe. F 6, Rn. F 6 Xe. O 3 Оксофториды Xe. O 2 F 2 Xe. O 3 F 2 Фторо комплексы [Xe. F][MF 6] [Kr. F][MF 6] [Xe. F 3][MF 6] [Xe. F 5][MF 6] [Xe. OF 5][MF 6] Соли оксокислот Xe[Cl. O 4]2, [Xe. F][NO 3] Кислоты H 2 Xe. O 4 H 4 Xe. O 6 Оксиды Kr. F 2, Xe. F 2, Xe. Cl 2, Rn. F 2 +4 Xe. O 4 [Xe. OF 3][MF 6] Cs 2[Xe. F 8]
Лекция Благородные газы.ppt