Бихимия мышц лекция.ppt
- Количество слайдов: 12

Бихимия мышц лекция

Мышцы - главный биохимический преобразователь потенциальной химической энергии в кинетическую (механическую) n n В организме позвоночных существует три типа мышц: скелетные, сердечные и гладкие. На долю мышечной ткани при рождении приходится 25%, у людей среднего возраста – более 40%, а у пожилых – менее 30% от общей массы тела.

Строение поперечно-полосатой мышцы Саркомер (2, 5 -3 мкм) – функциональная единица, ограниченная двумя Zлиниями, состоит из двух типов параллельных нитей: толстых (миозин, 12 -16 нм) и тонких нитей (актин, 8 нм).
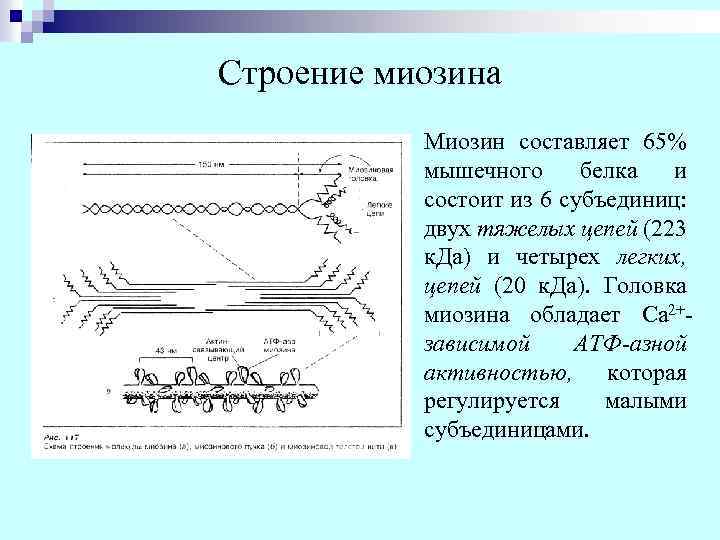
Строение миозина Миозин составляет 65% мышечного белка и состоит из 6 субъединиц: двух тяжелых цепей (223 к. Да) и четырех легких, цепей (20 к. Да). Головка миозина обладает Са 2+зависимой АТФ-азной активностью, которая регулируется малыми субъединицами.

Строение тонких нитей G-актин – это глобулярный белок (42 к. Да). При физиологической величине ионной силы и в присутствии магния G-актин полимеризуется с образованием нерастворимого F-актина – филамента. имеющего двойную спираль. Тропомиозин (64 к. Да) и тропонин (78 к. Да), состоящий из Т, С, I – являются регуляторными белками.

Источники энергии 1. 2. 3. 4. Резерв в виде креатинфосфата. Быстрая регенерация (ресинтез) АТФ за счет переноса фосфатной группы креатинфосфата на АДФ в реакции, катализируемой ферментом креатинкиназой (КК или КФК): Креатинфосфат + АДФ → Креатин + АТФ Гликолиз. Энергетическим резервом является гликоген. При недостаточном поступлении О 2 пируват восстанавливается в молочную кислоту (лактат), которая диффундирует в кровь (цикл Кори). Окислительное фосфорилирование. Субстратами служат глюкоза, жирные кислоты и кетоновые тела. 2 АДФ →АТФ + АМФ, реакция катализируется аденилаткиназой (миокиназой). Образовавшийся АМФ за счет дезаминирования частично превращается в ИМФ, что сдвигает реакцию в нужном направлении.

Сокращение мышц обусловлено продольным скольжением миозиновых и актиновых филаментов относительно друга. n n АТФ-аза головок миозина гидролизует АТФ: АТФ → АДФ + Фн. Гидролиз АТФ вызывает аллостерические изменения в миозиновой головке. Головка миозина образует мостик с молекулой актина. Актин ускоряет выброс продуктов АТФ-азной реакции из активного центра миозина. Что приводит к изменению конформации головки миозина, которая действует подобно «удару весла» (модель весельной лодки). Цикл повторяется до тех пор, пока имеется АТФ

Регуляция мышечного сокращения ионами Са 2+ В покоящихся клетках концентрация Са 2+ менее 10 -7– 10 -5 М. В саркоплазме имеются цистерны и поперечные трубочки Тсистемы СР, в которых Са 2+ связан с кальсеквестрином (55 к. Да). В СР высокий уровень Са 2+ (10 -3) поддерживается Са 2+АТФ-азами. Т-система способствует переносу ПД на СР. Деполяризация мембраны передается на потенциалуправляемый белок SR-foot, который открывает Са 2+-каналы. Результатом является выброс Са 2+ из СР в пространство между филаментами актина и миозина. Увеличение уровня Са 2+ до уровня >10 -5 является пусковым механизмом сокращения миофибрилл

Метаболизм белков и аминокислот n n n В скелетных мышцах активно расщепляются разветвленные аминокислоты валин и изолейцин. Одновременно идет ресинтез и высвобождение в кровь аланина и глутамина. Эти аминокислоты переносят азот, образующийся при расщеплении белков, в печень (цикл аланина) и почки. При голодании мышечные белки служат энергетическим резервом организма. Синтез и расщепление мышечных белков контролируются гормонами.

Биохимия миокарда n n n Сердечные мышцы сокращаются непроизвольно, перекачивая за сутки в среднем 7200 л крови. В сравнении со скелетными мышцами миокард содержит больше миоглобина, фосфоглицеринов, белков стромы, миоальбумина, митохондрий В миокарде преобладает аэробный метаболизм. АТФ синтезируется в результате окисления ВЖК (18 г/сутки), глюкозы (11 г/сутки), лактата (10 г/сутки), ПВК (0, 6 г/сутки) Креатинфосфата в миокарде в 4 -8 раз больше, чем АТФ, и он выполняет 2 функции: участвует в ресинтезе АТФ и переносе энергии из митохондрий в цитозоль, где расположены миофибриллы. Особенностью миокарда является активный пентозофосфатный путь превращения глюкозы.

Биохимические основы диагностики инфаркта миокарда n n n Ферментативная Энзимодиагностика: при инфаркте возрастает активность ЛДГ (изоферментов ЛДГ 1 ЛДГ 2, Ас. АТ, КФК (КФК МВ). Неферментативная Возрастает концентрация кардиоспецифических тропонинов I и Т Возрастает концентрация миоглобина, «средних молекул» (пептидов), нуклеиновых кислот, белков острой фазы.
Инфаркт миокарда (фото предоставлено В. А. Аргуновым)
Бихимия мышц лекция.ppt