Биохимия - углеводы.ppt
- Количество слайдов: 21
Биохимия Углеводы 1. Простые и сложные углеводы. Трансформация углеводов в ЖКТ. Понятия биосинтеза гликогена и гликолиза. Обзор аэробного и анаэробного метаболизма глюкозы.

Функции углеводов n n n Углеводы являются наиболее распространенным классом органических соединений природы и, благодаря их функции, углеводы можно рассматривать как основу существования растительных и животных организмов. Необходимость изучения углеводов заключается в широком спектре их функций. Функции Энергетическая – преимущество углеводов состоит в их способности окисляться как в аэробных, так и в анаэробных условиях (глюкоза) , Защитно-механическая – основное вещество трущихся поверхностей суставов, находятся в сосудах и слизистых оболочках (гиалуроновая кислота и другие гликозаминогликаны), Опорно-структурная – целлюлоза в растениях, гликозаминогликаны в составе протеогликанов, например, хондроитинсульфат в соединительной ткани, Гидроосмотическая и ионрегулирующая – гетерополисахариды обладают высокой гидрофильностью, отрицательным зарядом и, таким образом, удерживают Н 2 О, ионы Са 2+, Mg 2+, Na+ в межклеточном веществе, обеспечивают тургор кожи, упругость тканей, Кофакторная – гепарин является кофактором липопротеинлипазы плазмы крови и ферментов свертывания крови (инактивирует тромбокиназу).

Строение и классификация углеводов n Строение углеводов По своему строению углеводы являются многоатомными спиртами с альдегидной или кетоновой группой (полигидроксиальдегиды и полигидроксикетоны). Наиболее известные углеводы (крахмал, глюкоза, гликоген) обладают эмпирической формулой (CH 2 O)6. Другие представителя класса не соответствуют данному соотношению, и даже могут включать атомы азота, серы, фосфора. n Классификация углеводов Согласно современной классификации углеводы подразделяются на три основные группы: моносахариды, олигосахариды и полисахариды. n n n Моносахариды подразделяются на альдозы и кетозы в зависимости от наличия альдегидной или кетогруппы. Альдозы и кетозы, в свою очередь, разделяются в соответствии с числом атомов углерода в молекуле: триозы, тетрозы, пентозы, гексозы и т. д. В зависимости от конформации НОгруппы первого атома углерода разделяют α- и β-формы. Олигосахариды делятся по числу моносахаридов в молекуле: дисахариды, трисахариды и т. д. Полисахариды подразделяют на гомополисахариды, т. е. состоящие из одинаковых моносахаров, и гетерополисахариды, состоящие из различных моносахаров.
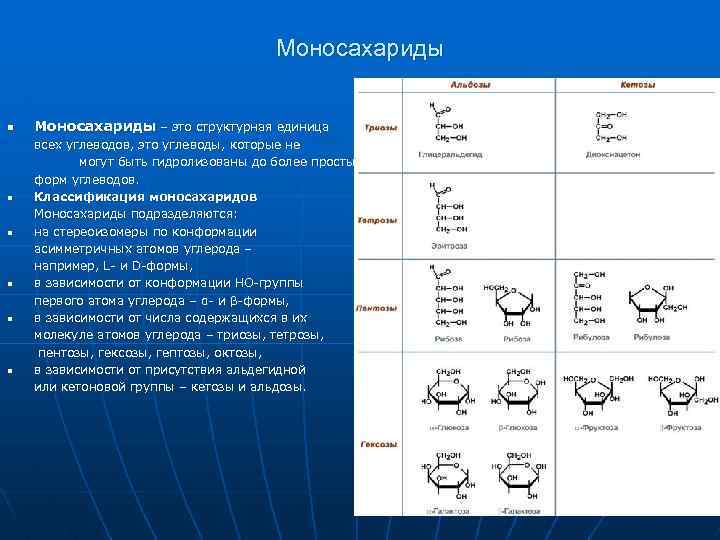
Моносахариды n n n Моносахариды – это структурная единица всех углеводов, это углеводы, которые не могут быть гидролизованы до более простых форм углеводов. Классификация моносахаридов Моносахариды подразделяются: на стереоизомеры по конформации асимметричных атомов углерода – например, L- и D-формы, в зависимости от конформации НО-группы первого атома углерода – α- и β-формы, в зависимости от числа содержащихся в их молекуле атомов углерода – триозы, тетрозы, пентозы, гексозы, гептозы, октозы, в зависимости от присутствия альдегидной или кетоновой группы – кетозы и альдозы.

Дисахариды n Дисахариды – это углеводы, которые при гидролизе дают две одинаковые или различные молекулы моносахарида и связаны друг с другом гликозидной связью. Сахароза – пищевой сахар, в которой остатки глюкозы и фруктозы связаны α 1, 2 -гликозидной связью. В наибольшем количестве содержится в сахарной свекле и тростнике, моркови, ананасах, сорго. Мальтоза – продукт гидролиза крахмала и гликогена, два остатка глюкозы связаны α 1, 4 гликозидной связью, содержится в солоде, проростках злаков. n n n Рис. Строение мальтозы и сахарозы Лактоза – молочный сахар, остаток галактозы связан с глюкозой β 1, 4 -гликозидной связью, содержится в молоке. В некоторых ситуациях (например, беременность) может появляться в моче. Целлобиоза – промежуточный продукт гидролиза целлюлозы в кишечнике, в котором остатки глюкозы связаны β 1, 4 -гликозидной связью. Здоровая микрофлора кишечника способна гидролизовать до 3/4 поступающей сюда целлюлозы до свободной глюкозы, которая либо п потребляется самими микроорганизмами, либо в всасывается в кровь. Рис. Строение лактозы и целлобиозы
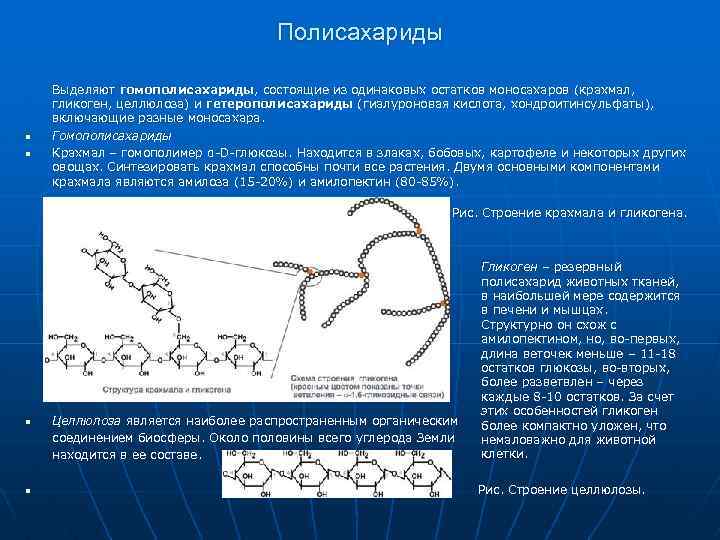
Полисахариды n n Выделяют гомополисахариды, состоящие из одинаковых остатков моносахаров (крахмал, гликоген, целлюлоза) и гетерополисахариды (гиалуроновая кислота, хондроитинсульфаты), включающие разные моносахара. Гомополисахариды Крахмал – гомополимер α-D-глюкозы. Находится в злаках, бобовых, картофеле и некоторых других овощах. Синтезировать крахмал способны почти все растения. Двумя основными компонентами крахмала являются амилоза (15 -20%) и амилопектин (80 -85%). Рис. Строение крахмала и гликогена. n n Гликоген – резервный полисахарид животных тканей, в наибольшей мере содержится в печени и мышцах. Структурно он схож с амилопектином, но, во-первых, длина веточек меньше – 11 -18 остатков глюкозы, во-вторых, более разветвлен – через каждые 8 -10 остатков. За счет этих особенностей гликоген более компактно уложен, что немаловажно для животной клетки. Целлюлоза является наиболее распространенным органическим соединением биосферы. Около половины всего углерода Земли находится в ее составе. Рис. Строение целлюлозы.

Полисахариды 2 n n n Гетерополисахариды. Большинство гетерополисахаридов характеризуется наличием повторяющихся дисахаридных остатков. Эти дисахариды включают в себя уроновую кислоту и аминосахар. Дублируясь, они образуют олиго- и полисахаридные цепи – гликаны. В биохимии используются синонимы – кислые гетерополисахариды (так как имеют много кислотных групп), гликозаминогликаны (производные глюкозы, содержат аминогруппы). Гликозаминогликаны входят в состав протеогликанов (мукополисахаридов) – сложных белков, функцией которых является заполнение межклеточного пространства и удержание здесь воды, что обеспечивает тургор тканей и эластичность хрящей, также они выступают как смазочный и структурный компонент суставов, хрящей, кожи. В частности, гиалуроновая кислота находится в стекловидном теле глаза, в синовиальной жидкости, в межклеточном пространстве. Основными представителями гетерополисахаридов (гликозаминогликанов) являются гиалуроновая кислота, хондроитинсульфаты, кератансульфаты и дерматансульфаты, гепарин. Рис. Строение гиалуроновой и хондроитинсерной кислот. Полисахариды используются в медицине для диагностики (инулин для определения клиренса почек, декстран для хроматографии), для лечения (как кровезаменители - декстран-реополиглюкин, при сердечной недостаточности - сердечные гликозиды, при нарушении перистальтики кишечника – целлюлоза, лактулоза при болезнях суставов – гиалуроновая кислота, хондроитинсульфат, гликозидные антибиотики – стрептомицин, эритромицин. )

Роль ферментов в расщеплении гликогена Синтез гликогена n n n Гликоген способен синтезироваться почти во всех тканях, но наибольшие запасы гликогена находятся в печени и скелетных мышцах. Накопление гликогена в мышцах отмечается в период восстановления после работы, особенно приеме богатой углеводами пищи. В печени гликоген накапливается только после еды, при гипергликемии. Благодаря особенностям фермента глюкокиназы печени (гексокиназа IV), фосфорилирующей глюкозу в глюкозо-6 -фосфат, гепатоцит эффективно захватывает глюкозу после еды и впоследствии метаболизирует ее в любом направлении. При нормальных концентрациях глюкозы в крови ее захват печенью не производится. Непосредственно синтез гликогена осуществляют следующие ферменты: 1. Фосфоглюкомутаза – превращает глюкозо-6 -фосфат в глюкозо-1 -фосфат; 2. Глюкозо-1 -фосфат-уридилтрансфераза – фермент, осуществляющий ключевую реакцию синтеза. Необратимость этой реакции обеспечивается гидролизом образующегося дифосфата; Рис. Реакции синтеза УДФ-глюкозы.
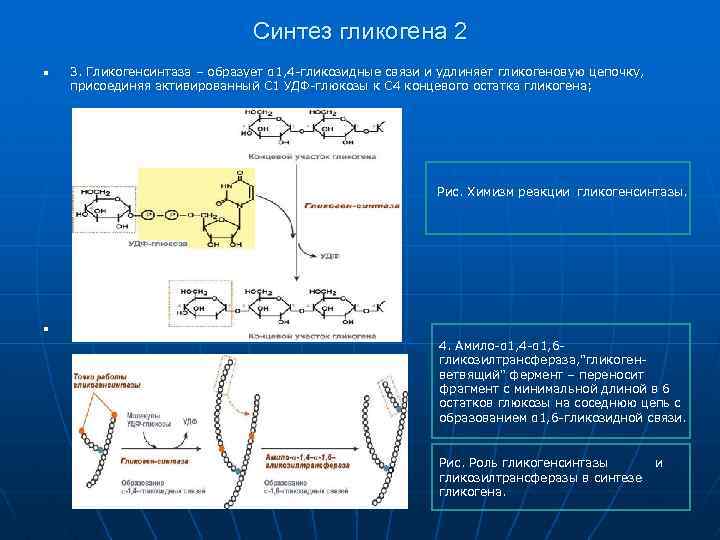
Синтез гликогена 2 n 3. Гликогенсинтаза – образует α 1, 4 -гликозидные связи и удлиняет гликогеновую цепочку, присоединяя активированный С 1 УДФ-глюкозы к С 4 концевого остатка гликогена; Рис. Химизм реакции гликогенсинтазы. n 4. Амило-α 1, 4 -α 1, 6 гликозилтрансфераза, "гликогенветвящий" фермент – переносит фрагмент с минимальной длиной в 6 остатков глюкозы на соседнюю цепь с образованием α 1, 6 -гликозидной связи. Рис. Роль гликогенсинтазы и гликозилтрансферазы в синтезе гликогена.

Синтез и распад гликогена реципрокны. n n n n Метаболизм гликогена в печени, мышцах и других клетках регулируется несколькими гормонами, одни из которых активируют синтез гликогена, а другие – распад гликогена. При этом в одной клетке не могут идти одновременно синтез и распад гликогена – это противоположные процессы с совершенно с разными задачами. Синтез и распад исключают друга или, по-другому, они реципрокны. Активность ключевых ферментов метаболизма гликогенфосфорилазы и гликогенсинтазы изменяется в зависимости наличия в составе фермента фосфорной кислоты – они активны либо в фосфорилированной, либо в дефосфорилированной форме. Присоединение фосфатов к ферменту производят протеинкиназы, источником фосфора является АТФ: фосфорилаза гликогена активируется после присоединения фосфатной группы, синтаза гликогена после присоединения фосфата инактивируется. Скорость фосфорилирования указанных ферментов повышается после воздействия на клетку адреналина, глюкагона и некоторых других гормонов. В результате адреналин и глюкагон вызывают гликогенолиз, активируя фосфорилазу гликогена. Например, во время мышечной работы адреналин вызывает фосфорилирование внутримышечных ферментов обмена гликогена. В результате фосфорилаза гликогена активируется, синтаза инактивируется. В мышце происходит распад гликогена, образуется глюкоза для обеспечения энергией мышечного сокращения. При голодании в ответ на снижение глюкозы крови из поджелудочной железы секретируется глюкагон. Он воздействует на гепатоциты и вызывает фосфорилирование ферментов обмена гликогена, что приводит к гликогенолизу и повышению глюкозы в крови. Рис. Изменение активности ферментов обмена гликогена в зависимости от условий.

Аэробный метаболизм глюкозы n n Энергетика любой клетки нашего организма основана на окислении глюкозы. Окисление глюкозы происходит по двум направлениям: 1. Окисление с образованием пентоз: рибозы, рибулозы, ксилулозы. Этот путь называется пентозофосфатный шунт и не связан с получением энергии 2. Окисление с получением энергии. Второй путь, т. е. тот по которому глюкоза окисляется для получения энергии, называется гликолиз (греч. glykos — сладкий и греч. lysis — растворение). Конечным продуктом гликолиза является пировиноградная кислота (пируват). В зависимости от дальнейшей судьбы пирувата различают аэробное и анаэробное окисление глюкозы. Целью обоих типов окисления является получение АТФ. Рис. Пути метаболизма пирувата в присутствии и в отсутствии кислорода. n n В аэробном процессе пировиноградная кислота превращается в ацетил-SКо. А (реакции ПВКдегидрогеназы) и далее сгорает в реакциях цикла трикарбоновых кислот до СО 2 (реакции ЦТК). Общее уравнение аэробного окисления глюкозы: C 6 H 12 O 6 + 6 O 2 + 38 АДФ + 38 Фнеорг → 6 CO 2 + 44 H 2 О + 38 АТФ

Анаэробный метаболизм глюкозы n n n В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата). Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват. В микробиологии анаэробный гликолиз называют молочнокислым брожением. Суммарное уравнение анаэробного гликолиза имеет вид: C 6 H 12 O 6 + 2 АДФ + 2 Фнеорг → 2 Лактат + 2 H 2 O + 2 АТФ C 6 H 12 O 6 + 2 АДФ + 2 Фнеорг → Бескислородное окисление глюкозы включает два этапа Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии. Клетки скелетной мускулатуры за счет бескислородного расщепления глюкозы способны выполнять мощную, быструю, интенсивную работу, как, например, бег на короткие дистанции, напряжение в силовых видах спорта. Бескислородное окисление глюкозы усиливается при гипоксии клеток при анемиях, нарушении кровообращения в тканях. Гликолиз Анаэробное превращение глюкозы локализуется в цитозоле и включает два этапа из 11 ферментативных реакций.
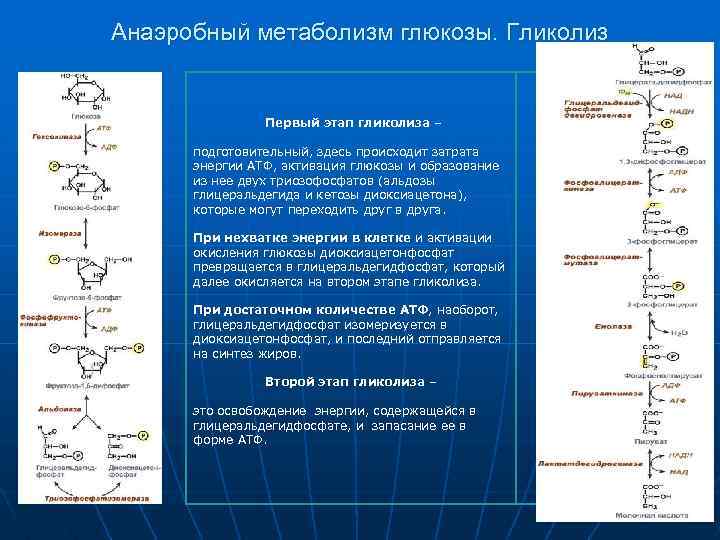
Анаэробный метаболизм глюкозы. Гликолиз Первый этап гликолиза – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее двух триозофосфатов (альдозы глицеральдегида и кетозы диоксиацетона), которые могут переходить друг в друга. При нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза. При достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров. Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.

Переключение между аэробным и анаэробным окислением глюкозы n n n n n Переключение между аэробным и анаэробным окислением происходит автоматически. Прекрасной иллюстрацией способности метаболизма переключаться с одного направления на другой без какого-либо дополнительного вмешательства является эффект Пастера. Эффект Пастера Это снижение потребления глюкозы и прекращение продукции молочной кислоты клеткой в присутствии кислорода. Биохимический механизм эффекта заключается в конкуренции за пируват между пируватдегидрогеназой, превращающей пируват в ацетил-S-Ко. А, и лактатдегидрогеназой, превращающей пируват в лактат. У пируватдегидрогеназы сродство гораздо выше и в обычных аэробных условиях она окисляет большую часть пировиноградной кислоты. Как только поступление кислорода уменьшается (недостаток кровообращения, тромбоз и т. п. ) происходит ингибиция этого фермента, начинает преобладать лактатдегидрогеназа и пировиноградная кислота превращается в молочную. При наличии кислорода ингибирование ПВК-дегидрогеназы прекращается и она, обладая большим сродством к пирувату, выигрывает конкуренцию. Отличной иллюстрацией к сказанному служит чувствительность миокарда и нейронов к недостатку кислорода: В основе высокой чувствительности этих органов к отсутствию кислорода лежит отличие изоферментов лактатдегидрогеназы (ЛДГ) друг от друга. Сердечный изофермент ЛДГ-1, обладая высоким сродством к молочной кислоте, переводит ее в пировиноградную, "стремясь" поднять концентрацию пирувата с целью его включения в цикл трикарбоновых кислот (только в аэробных условиях) и получения энергии для сокращения миокардиоцита. При нехватке кислорода свойства ЛДГ-1 не изменятся, он по-прежнему будет сдвигать реакцию в сторону продукции пировиноградной кислоты ("справа-налево"). Однако "сгореть" в ЦТК пируват не может и выйти из клетки тоже не может, т. к. клеточные мембраны непроницаемы для него. Являясь кислотой, он закисляет цитозоль, изменяя активность ферментов и, возможно, как-то еще проявляет токсичность. Таким образом происходят необратимые повреждения кардиомиоцита и нейрона.

Перенос моносахаров внутрь клетки n n n n Транспорт моносахаров через мембраны. Всасывание в кишечнике. После переваривания крахмала и гликогена, после расщепления дисахаридов в полости кишечника накапливается глюкоза и другие моносахариды, которые должны попасть в кровь. Для этого им необходимо преодолеть, как минимум, апикальную мембрану энтероцита и его базальную мембрану. Всасывание моносахаридов из просвета кишечника происходит по механизму вторичного активного транспорта. Фермент Na+, К+-АТФаза постоянно, в обмен на калий, выкачивает ионы натрия из клетки, именно этот транспорт требует затрат энергии. В просвете кишечника содержание натрия относительно высоко и он связывается со специфическим мембранным белком, имеющим два центра связывания: один для натрия, другой для сахара. Примечательно то, что сахар связывается с белком только после того, как с ним свяжется натрий. Белок-транспортер свободно мигрирует в толще мембраны. При контакте белка с цитоплазмой натрий быстро отделяется от него по градиенту концентрации и сразу отделяется сахар. Результатом является накопление сахара в клетке, а ионы натрия выкачиваются Na+, К+-АТФазой. Выход глюкозы из клетки в межклеточное пространство и далее кровь происходит благодаря простой и облегченной диффузии. После выхода в кровь, оттекающую от кишечника, моносахариды движутся по сосудам воротной системы в печень, частично задерживаются в ней, частично выходят в большой круг кровообращения. Из крови внутрь клеток глюкоза попадает при помощи облегченной диффузии по градиенту концентрации с участием белков-переносчиков (глюкозных транспортеров "Глю. Т"). Различают 5 видов транспортеров глюкозы Глю. Т 1, Глю. Т 2, Глю. Т 3, Глю. Т 4, Глю. Т 5. Глюкозные транспортеры имеются на мембранах всех клеток. В мышцах и жировой ткани находится Глю. Т 4, только эти транспортеры являются чувствительными к влиянию инсулина. При действии инсулина на клетку они поднимаются к поверхности мембраны и переносят глюкозу внутрь. Указанные ткани получили название инсулинзависимых. Некоторые ткани совершенно нечувствительны к действию инсулина, их называют инсулиннезависимыми. К ним относятся нервная ткань, стекловидное тело, хрусталик, сетчатка, клубочковые клетки почек, эндотелиоциты, семенники и эритроциты. Часть клеток занимает промежуточное положение, т. е. на их мембранах находятся Глю. Т 4 и другие типы транспортеров.

Все пищевые моносахариды должны превратиться в глюкозу. n n § § § Поскольку в кишечнике всасываются все поступающие с пищей моносахариды (фруктоза, галактоза, манноза и т. п. ), то перед организмом встает задача превратить полученные гексозы в глюкозу для ее дальнейшего использования в реакциях метаболизма. Этот процесс получил название взаимопревращение сахаров. Цель этого процесса – создание только одного субстрата для реакций метаболизма, а именно α-D-глюкозы, что позволяет сэкономить ресурсы, не образовывать множество ферментов для каждого вида моносахарида. Реакции протекают в эпителии кишечника и, в основном, в гепатоцитах. При нарушении этого процесса, что связано с дефектом необходимых ферментов, развиваются патологические состояния с задержкой умственного и физического развития ребенка, нарушением самочувствия (галактоземия, эссенциальная фруктозурия). Судьба глюкозы. После активации (фосфорилирования) глюкоза в зависимости от условий и вида клетки превращается по различным направлениям: часть глюкозы обязательно используется в энергетическом обмене, она сгорает в реакциях катаболизма для синтеза АТФ, при достаточно большом количестве в клетке глюкоза запасается в виде гликогена, к синтезу гликогена способны большинство тканей, в гепатоцитах (при высокой концентрации) и в адипоцитах глюкоза перенаправляется на синтез триацилглицеролов и в печени на синтез холестерола, при определенных условиях часть глюкозы идет в реакции пентозофосфатного пути, в котором образуются рибозо-5 -фосфат и НАДФН, некоторая доля глюкозы используется для синтеза гликозаминов и далее структурных или иных гетерополисахаридов.

Гликоген - это легкоиспользуемый резерв энергии. n n n Резервы гликогена используются по-разному в зависимости от функциональных особенностей клетки. Гликоген печени расщепляется при снижении концентрации глюкозы в крови, прежде всего между приемами пищи. Через 12 -18 часов голодания запасы гликогена в печени полностью истощаются. В мышцах количество гликогена снижается обычно только во время физической нагрузки – длительной и/или напряженной. Гликоген здесь используется для обеспечения глюкозой работы самих миоцитов. Таким образом, мышцы, как и другие органы, используют гликоген только для собственных нужд. Мобилизация (распад) гликогена или гликогенолиз активируется при недостатке свободной глюкозы в клетке, а значит и в крови (голодание, мышечная работа). При этом уровень глюкозы крови "целенаправленно" поддерживает только печень, в которой имеется глюкозо-6 -фосфатаза, гидролизующая фосфатный эфир глюкозы. Образуемая в гепатоците свободная глюкоза выходит через плазматическую мембрану в кровь. Гликоген способен синтезироваться почти во всех тканях, но наибольшие запасы гликогена находятся в печени и скелетных мышцах. Накопление гликогена в мышцах отмечается в период восстановления после работы, особенно приеме богатой углеводами пищи. В печени гликоген накапливается только после еды, при гипергликемии.

Контроль уровня глюкозы в крови n n n 1. 2. 3. 4. 5. Нервная регуляция концентрации глюкозы в крови выражается в положительном влиянии n. vagus на секрецию инсулина и тормозящем влиянии на этот процесс симпатической иннервации. Кроме этого, выделение адреналина в кровь подвержено симпатическим влияниям. Основными факторами гормональной регуляции являются глюкагон, адреналин, глюкокортикоиды, соматотропный гормон с одной стороны, и инсулин с другой. Все гормоны, кроме инсулина, влияя на печень, увеличивают гликемию. Инсулин является единственным гормоном организма, действие которого нацелено на снижение уровня глюкозы крови. При его влиянии глюкозу усиленно поглощают мышцы и жировая ткань. Уменьшение концентрации глюкозы в крови инсулином достигается следующими путями: переход глюкозы в клетки – активация белков-транспортеров Глю. Т 4 на цитоплазматической мембране, вовлечение глюкозы в гликолиз – повышение синтеза глюкокиназы – фермента, получившего название "ловушка для глюкозы", стимуляция синтеза других ключевых ферментов гликолиза – фосфофруктокиназы, пируваткиназы, увеличение синтеза гликогена – активация гликогенсинтазы и стимуляция ее синтеза, что облегчает превращение излишков глюкозы в гликоген, активация пентозофосфатного пути – индукция синтеза глюкозо-6 -фосфат-дегидрогеназы и 6 фосфоглюконатдегидрогеназы, усиление липогенеза – вовлечение глюкозы в синтез триацилглицеролов или фосфолипидов (схема cинтеза). n Многие ткани совершенно нечувствительны к действию инсулина, их называют инсулиннезависимыми. К ним относятся нервная ткань, стекловидное тело, хрусталик, сетчатка, клубочковые клетки почек, эндотелиоциты, семенники и эритроциты.

Контроль уровня глюкозы в крови n n n n Глюкагон повышает содержание глюкозы крови: увеличивая мобилизацию гликогена через активацию гликогенфосфорилазы, стимулируя глюконеогенез – повышение работы ферментов пируваткарбоксилазы, фосфоенолпируват -карбоксикиназы, фруктозо-1, 6 -дифосфатазы. Адреналин вызывает гипергликемию: активируя мобилизацию гликогена – стимуляция гликогенфосфорилазы, Глюкокортикоиды повышают глюкозу крови за счет подавления перехода глюкозы в клетку, стимулируя глюконеогенез – увеличивают синтез ферментов пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1, 6 -дифосфатазы.

Образование рибозы и НАДФН. Пентозофосфатный путь. n n n Так как в клетках непрерывно просходят реакции синтеза белков, то для этого процесса требуются рибонуклеиновые кислоты. В свою очередь для синтеза самих нуклеиновых кислот, а точнее пуриновых и пиримидиновых нуклеотидов, требуется рибозо-5 -фосфат. Если клетка готовится к делению, то для синтеза ДНК ей нужны дезоксирибонуклеотиды, которые образуются при участии НАДФН. Молекулы НАДФН также используются: для синтеза жирных кислот (печень, жировая ткань), для синтеза холестерола и других стероидов (печень), для синтеза глутаминовой кислоты из α-кетоглутаровой кислоты (реакция восстановительного аминирования), для систем антиоксидантной защиты клетки от свободно-радикального окисления (эритроциты). В клетке существует процесс, обеспечивающий одновременное образование рибозы и НАДФН – это пентозофосфатный путь. Пентозофосфатный путь. Наиболее активно реакции пентозофосфатного пути идут в цитозоле клеток печени, жировой ткани, эритроцитах, коре надпочечников, молочной железе при лактации, в гораздо меньшей степени в скелетных мышцах. Этот путь окисления глюкозы не связан с образованием энергии, а обеспечивает анаболизм клеток. В связи с этим у новорожденных и детей первых лет жизни его активность довольно высока. Пентозофосфатный путь включает два этапа – окислительный и структурных перестроек (неокислительный). Первый этап. На первом, окислительном, этапе глюкозо-6 -фосфат в трех реакциях превращается в рибулозо-5 -фосфат, реакции сопровождаются восстановлением двух молекул НАДФ до НАДФН.

Образование рибозы и НАДФН. Пентозофосфатный путь… n n Второй этап – этап структурных перестроек, благодаря которым пентозы способны возвращаться в фонд гексоз. В этих реакциях рибулозо-5 -фосфат изомеризуется до рибозо-5 -фосфата и ксилулозо-5 -фосфата. Далее под влиянием ферментов транскетолазы и трансальдолазы происходят структурные перестройки с образованием других моносахаридов. При реализации всех реакций второго этапа пентозы превращаются во фруктозо-6 -фосфат и глицеральдегидфосфат. Глицеральдегид-3 -фосфат в зависимости от условий и вида клеток может либо "проваливаться" во 2 й этап гликолиза либо через диоксиацетонфосфат восстанавливаться до глицерол-3 -фосфата и далее направляться в синтез фосфатидной кислоты и далее триацилглицеролов. При необходимости из него могут образоваться и гексозы. Если клетке нужны НАДФН и энергия АТФ (как в эритроците), то фруктозо-6 -фосфат и глицеральдегидфосфат на выходе из 2 -го этапа "провалятся" в гликолитические реакции. n n Если клетка растет и делится, то ей необходимы НАДФН и рибозо-5 -фосфат. В этом случае 2 -й этап идти не будет, весь образуемый на 1 -м этапе рибулозо-5 -фосфат превратится в рибозо-5 -фосфат, который используется для синтеза нуклеотидов. НАДФН будет расходоваться на синтез дезоксирибонуклеотидов. Рис. Особенность пентозного шунта при активном синтезе ДНК.
Биохимия - углеводы.ppt