Химия и патохимия печени.ppt
- Количество слайдов: 59

Биохимия печени

Печень — самый крупный из внутренних органов человека, выполняющий многообразные функции: 1. Принимает и распределяет почти все вещества, проникающие в организм из пищеварительного тракта. Вся кровь, в которую всосались продукты переваривания пищи и другие вещества из кишечника, поступает в печень по воротной вене. 2. Служит местом образования желчи, что обеспечивает участие печени в пищеварении.

Функции печени (продолжение) 3. Осуществляет биосинтез веществ, которые «работают» или используются как субстраты в других органах и тканях — биосинтез «на экспорт» . 4. Обеспечивает обезвреживание токсических продуктов метаболизма, обра зующихся разных в тканях, а также продуктов гниения белков в кишечнике. 5. Печень — место инактивации многих гормонов. 6. Участвует в метаболизме чужеродных соединений и лекарственных веществ. 7. Участвует в выделении некоторых продуктов метаболизма с желчью в кишечник.

Многообразие функций печени связано с особенностями кровообращения (наличие капиллярной сети воротной вены и капиллярной сети печеночной артерии), а также особенностями структуры печеночной дольки.


Роль печени в метаболизме углеводов n Печень поддерживает физиологическую концентрацию глюкозы в крови за счет способности гепатоцитов регулировать поступление в общий кровоток глюкозы, всасывающейся из пищеварительного тракта. Из общего количества поступающей с пищей глюкозы печеночные клетки при нормогликемии извлекают большую ее часть. Элиминированная гепатоцитами глюкоза расходуется: n а) на синтез гликогена (не более 10 15%); n б) в окислительном распаде (более 60%) и n в) на синтез жирных кислот (до 30%). При несбалансированном питании эти соотношения изменяются (например, при преобладании в диете углеводов увеличивается доля, затрачиваемая на синтез гликогена).

Синтез гликогена протекает по следующему пути: Синтез гликогена — процесс, идущий с потреблением энергии: удлинение цепи на один остаток глюкозы потребляет 1 молекулу АТФ и УДФ (первая на образование Глюкозо-6 -фосфата, вторая — на образование УДФ-глюкозы из УТФ и Глюкозо-1 -фосфата). Патологические состояния, сопровождающиеся нарушением генерации макроэргических нуклеотидов (например, поражения паренхиматозной ткани печени), замедляют синтез гликогена.

При физиологической гипогликемии (большой перерыв между приемами пищи или интенсивная мышечная работа) печень вносит вклад в восстановле ние ормогликемии за счет ускорения н процесса распада гликогена: Гликоген + Рн Глюкозо 1 фосфат Глюкозо 6 фосфат. Первую реакцию катализирует фосфорилаза, которую активирует ряд гормонов через аденилатциклазную систему.

Глюкозо-6 -фосфат может расходоваться по одному из трех направлений: 1) по пути гликолиза с образованием пирувата и лактата; 2) по пентозофосфатному пути (энзим —Г-6 фосфатдегидрогеназа); 3) расщепляться под действием фосфатазы на глюкозу и Р н. В печени преобладает последний путь, завершающийся выбросом свободной глюкозы в кровоток, что повышает ее содержание в крови. На втором месте находится пентозофосфатный путь с многочисленными процессами синтеза в печени за счет восстановленной формы НАДФ — источника водорода в биосинтезах. Особенно активно НАДФ • Н 2 потребляется в синтезе липидов. При сахарном
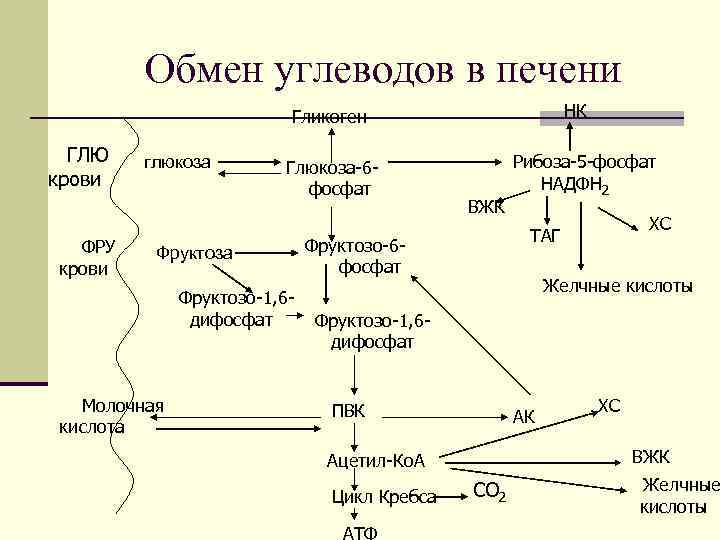
Обмен углеводов в печени НК Гликоген ГЛЮ крови ФРУ крови глюкоза Глюкоза-6 фосфат Фруктоза Фруктозо-1, 6 дифосфат Молочная кислота ВЖК Рибоза-5 -фосфат НАДФН 2 ХС ТАГ Фруктозо-6 фосфат Желчные кислоты Фруктозо-1, 6 дифосфат ПВК АК ВЖК Ацетил-Ко. А Цикл Кребса ХС СО 2 Желчные кислоты
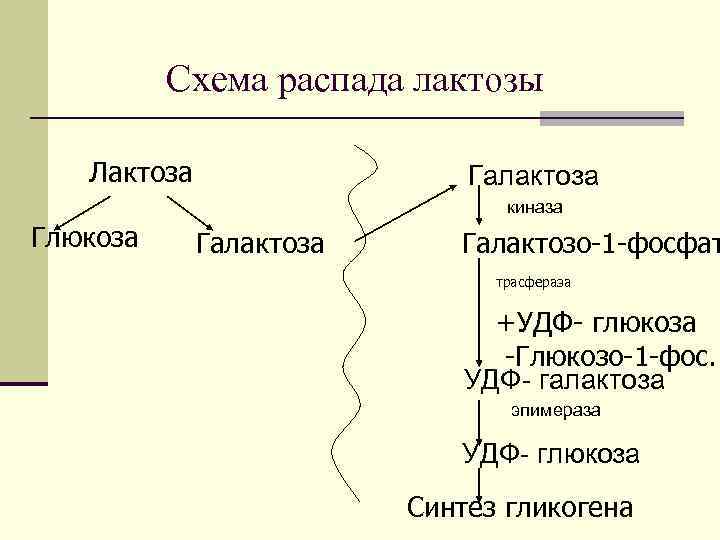
Схема распада лактозы Лактоза Галактоза киназа Глюкоза Галактозо-1 -фосфат трасфераза +УДФ- глюкоза -Глюкозо-1 -фос. УДФ галактоза эпимераза УДФ глюкоза Синтез гликогена

Роль печени в метаболизме липидов Печень как орган, ответственный за продукцию компонентов желчи, прежде всего участвует в переваривании и всасывании липидов. Здесь синтезируются желчные кислоты — эмульгаторы жира и активаторы панкреатической липазы в тонком кишечнике. При их отсутствии переваривание липидов практически не происходит. Затруднено и всасывание жирных кислот.

Роль печени в метаболизме липидов Печени принадлежит главная роль и в регуляции метаболизма липидов. Так, при дефиците основного энергетического материала — глюкозы, в печени ускоряется окисление жирных кислот. При избытке глюкозы для синтеза триацилглицеридов и фосфолипидов используются жирные кислоты. Их источником служат жирные кислоты, поступающие из пищеварительного тракта и из жировой ткани (за счет липолиза).

Роль печени в метаболизме липидов Печени принадлежит важная роль в регуляции обмена холестерола. Исходное вещество в синтезе холестерола ацетил-Ко. А — компонент энергетического фонда клетки. Следовательно, скорость синтеза холестерола зависит от уровня снабжения организма энергией. Разумеется, избыточное питание, сопровождающееся избыточным образованием в гепатоцитах ацетил-Ко. А, стимулирует процессы липогенеза вообще и синтеза холестерола в частности. Тормозят синтез холестерола (по принципу обратной связи) холестерол и желчные кислоты, поступающие в печень с кровью. Эти два продукта тормозят гидро-оксиметил-Ко. Аредуктазу.

Роль печени в метаболизме липидов Гепатоциты участвуют в образовании транспортных форм липидов, а именно α-, β- и пре-βлипопротеинов. Здесь накапливаются липидные компоненты липопротеинов (жирные кислоты, моно-, дии триглицериды, холестерол, фосфолипиды) и синтезируются их белковые компоненты — апопротеины. Из этих соединений происходит сборка липопротеинов.

Роль печени в метаболизме липидов В печени происходит синтез кетоновых тел Жирные кислоты жировой ткани поступают в печень, а печень экспортирует их в виде ацетоацетата. Высокое содержание ацетоацетата угнетает липолиз в жировой ткани (отрицательная обратная связь). Если расщепление жиров преобладает (голодание, нарушение поступления глюкозы в клетку при инсулиновой недостаточности, быстрое потребление глюкозы и запасов гликогена при интенсивной мышечной работе), концентрация оксалоацетата снижается и увеличивается доля ацетил-Ко. А, использующаяся на синтез кетоновых тел — ацетоацетата, βоксимасляной кислоты и ацетона.


Метаболизм этанола n Содержание этанола в алкогольных напитках и в организме человека n Следы этанола (Et. OH, этиловый спирт) можно обнаружить во фруктах. В алкогольных напитках этанол присутствует в существенно более высоких концентрациях. Содержание этанола принято указывать в объемных процентах. Нормы потребления этанола и концентрацию в крови целесообразно давать в граммах (плотность этанола 0, 79 кг/л). Например, в одной бутылке пива (0, 5 л, 4% Et. OH) содержится 20 мл = 16 г этанола, в одной бутылке вина (0, 7 л, 12% Et. OH) — 84 мл = 66 г этанола.

n После поступления в организм этанол быстро всасывается за счет диффузии; максимальная концентрация в крови достигается спустя 60 90 мин. Кроме того, скорость всасывания зависит от самых разных факторов. Так, пустой желудок, высокая температура напитка (например, грога), наличие сахара и углекислоты (например, в шампанском) стимулируют всасывание этанола. Напротив, всасывание этанола замедлено при обильной трапезе. В организме этанол очень быстро распределяется, поступая преимущественно в мышцы и мозг, существенно меньше в жировую и костную ткани, т. е. в ткани и органы, которые составляют примерно 70% общей массы тела. При быстром и полном всасывании этанола, содержащегося в одной бутылке пива (16 г), и массе тела 70 кг (этанол поступает в ткани организма, масса которых составляет 70 г х 0, 7= 49 кг) в крови создается концентрации 16 г/49 кг = 0, 33 промилле (7, 2 м. М). Летальная концентрация составляет примерно 3, 5 промилле (76 м. М).

Метаболизм этанола n Основным местом метаболической трансформации этанола является печень, в этом процессе может также принимать участие эпителий желудка. Этанол дегидрируется алкогольдегидрогеназой в этаналь (ацетальдегид), а затем альдегидрогеназой переводится в ацетат. Уксусная кислота в реакции, катализируемой ацетат-Ко. А-лигазой (тиокиназой) в присутствии АТФ, превращается в ацетил Ко. А (ацетил Со. А). Следует отметить, что весь процесс промежуточного метаболизма хорошо согласован. Наряду с цитоплазматической алкогольдегидрогеназой в метаболизме этанола принимают ограниченное участие каталаза и "индуцибельная" микросомальная алкогольоксидаза.

n Скорость трансформации этанола в печени лимитируется главным образом активностью алкогольдегидрогеназы. Другим лимитирующим фактором является наличие НАД+. Максимальная скорость реакции наблюдается даже при небольших концентрациях этанола. Поэтому уровень этанола в организме понижается с постоянной скоростью (расщепление этанола — реакция нулевого порядка). n «Энергетическая ценность» этанола составляет 29, 4 к. Дж/г (7 ккал/г). Поэтому алкогольные напитки обеспечивают организм значительной частью энергоресурсов (особенно при алкоголизме). n Хотя исследование механизма действия этанола на организм представляется крайне актуальным, этот вопрос все еще остается недостаточно изученным. Вместе с тем действие больших количеств этанола напоминает действие наркотика, что можно объяснить прямым воздействием этанола на мембраны нейронов.

Жировая дистрофия печени n Предельная норма этанола для здорового человека при ежедневном приеме составляет 60 г для мужчин и 50 г для женщин. Эта величина зависит от массы, состояния здоровья, а также от приема лекарственных препаратов. Повышенное потребление этанола в течение года вызывает заболевание печени. Из за высокого уровня НАДН и ацетил Ко. А, вызванных приемом этанола, в печени тормозится цитратный цикл и кетогенез, нарушается биосинтез нейтральных жиров и холестерина, наблюдается повышенное отложение жира (жировая дистрофия). Отложение жира (от 5 до 50% по сухой массе) чаще всего процесс обратимый. При гибели гепатоцитов из за хронического алкоголизма наступает фиброз печени (избыточное развитие соединительной ткани). При циррозе печени заболевание переходит в необратимую форму, для которой характерно прогрессирующее отключение функций печени.


Роль печени в метаболизме белков Аминокислоты, поступающие из пищеварительного тракта, печень использует для синтеза специфических белков печеночных клеток, но большую часть — для биосинтеза белков плазмы крови – фибриноген (2 г/сут) и альбумины крови (12 г/сут). n В гепатоцитах синтезируются наряду с фибриногеном специфические белки свертывания крови: ф. II, Y, YII, X. n Печень занимает центральное место в обмене аминокислот в связи с тем, что здесь интенсивно протекают процессы трансаминирования, дезаминирования и непрямого дезаминирования при участии системы α-кетоглутароваяглутаминовая кислота. n Здесь же в полном объеме обезвреживается высвобождающийся при дезаминировании аммиак (синтез мочевины). Способность печени обезвреживать аммиак имеет примерно десятикратную степень надежности. n
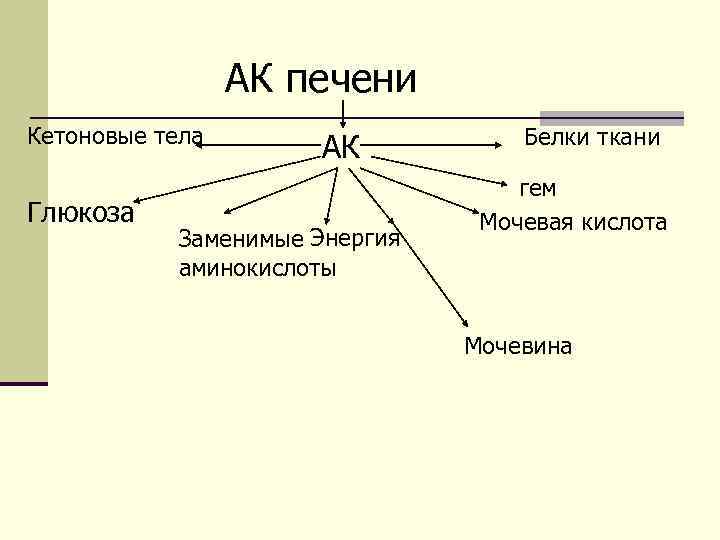
АК печени Кетоновые тела Глюкоза АК Заменимые Энергия аминокислоты Белки ткани гем Мочевая кислота Мочевина

Обезвреживающая функция печени Обезвреживание реализуется путем химической модификации веществ, которая включает две группы превращений: 1)окисление, восстановление или гидролиз с образованием или высвобождением групп ОН, -СООН, -SH, -NH, и др. 2) присоединение к этим группам глюкуроновой или серной кислоты, глицина, глутамина или ацетильного остатка (конъюгация). Обезвреживание может происходить с помощью обоих или одного из этих превращений. Все превращения сводятся к повышению гидрофильности обезвреживающего продукта, что облегчает его выведение из организма.

Обезвреживающая функция печени n В печени происходит обезвреживание нормальных метаболитов — билирубина и аммиака, которые образует коньюгаты с глюкуроновой кислотой (моно- и диглюкуронаты) и в меньшей степени — с серной. Те и другие выводятся с желчью в кишечник. Аммиак потребляется в орнитиновом цикле и входит в состав молекулы мочевины, которая, поступая в кровь, выделяется с мочой. n Инактивация гормонов в печени в зависимости от их природы обеспечивается разными путями. n Пептидные гормоны гидролизуются в печени протеазами. Молекула инсулина инактивируется в два этапа: восстановление дисульфидных связей с высвобождением двух полипептидных цепей и их гидролиз инсулиназой. Процесс протекает быстро, при однократном прохождении крови через печень

Обезвреживающая функция печени n Катехоламины подвергаются в гепатоцитах окислительному дезаминированию при участии моноаминооксидазы, затем метилированию по гидроксильным группам и коньюгации с серной или глюкуроновой кислотой. Продукты катаболизма выводятся с мочой. n Стероидные гормоны в микросомальной фракции гидроксилируются при участии гидроксилаз, коньюгируются с глюкуроновой или серной кислотой и также выводятся с мочой. n Тироксин в гепатоцитах вовлекается в трансаминирование, превращаясь в кетопроизводное, которое коньюгируется с теми же кислотами.

Обезвреживающая функция печени n Чужеродные соединения (ксенобиотики) выводятся частично в неизмененном виде, частично в виде продуктов метаболических превращений. Чем ниже растворимость чужеродного вещества, тем большая часть его метаболизирует. Это связано с тем, что гидрофобные соединения склонны задерживаться в тканях (в комплексах с белками, в клеточных мембранах, жировых депо). В ходе метаболизма, превращаясь в гидрофильные продукты, они ускоренно удаляются.

Обезвреживающая функция печени Обезвреживание продуктов гниения аминокислот, образующихся под действием энзимов микрофлоры в кишечнике, происходит следующим образом. n Так называемые трупные яды (кадаверин и путресцин — продукты декарбоксилирования лизина и орнитина соответственно) — выделяются с мочой в неизменном виде. n Крезол и фенол, образующиеся при распаде тирозина, скатол и индол — при распаде триптофана, всасываются из кишечника в кровоток и в основном задерживаются в печени. Здесь крезол и фенол образуют коньюгаты с глюкуроновой или серной кислотой, а скатол деметилируется, превращаясь в индол. Последний подвергается гидроксилированию, превращаясь в индоксил, который коньюгируется с теми же кислотами. Выделение с мочой калиевой соли индоксилсульфата (животный индикан) пропорционально интенсивности гнилостных процессов в кишечнике и скорости реакций

Обезвреживающая функция печени Метаболизм лекарственных веществ в печени включает окислительные превращения, катализируемые микросомальными оксидазами. Они представляют собой ферментные комплексы с невысокой степенью специфичности, нуждающиеся в молекулярном кислороде и НАДФ • Н 2. Главный из окислительных ферментов — цитохром P 450. Он представляет собой комплекс белка с гемом, обеспечивающим присоединение кислорода.


Обезвреживающая функция печени Последовательные этапы окисления лекарственного вещества при участии цитохрома Р 450 таковы. 1. Цитохром Р 450, содержащий окисленное (трехвалентное) железо, связывает лекарственное вещество, образуя энзимсубстратный комплекс. 2. Железо в геме комплекса восстанавливается до двухвалентного за счет НАДФ • Н 2, а что обеспечивает присоединение молекулы кислорода. 3. Далее один атом кислорода используется для окисления лекарственного вещества, а другой — для образования молекулы воды, железо при этом переходит в трехвалентную форму. 4. Окисленное лекарственное вещество высвобождается, а цитохром Р 450 оказывается в исходном состоянии с трехвалентным железом, что позволяет ему повторить цикл превращений с другой молекулой лекарственного вещества.

Основные патологические состояния и нарушения функции печени

Острый вирусный гепатит Развивается при инфицировании вирусами А (эпидемический вирусный гепатит) и В (сывороточный гепатит). В обоих случаях наблюдаются некрозы печеночных клеток с поражением субклеточных структур, гиперплазия эндоплазматического ретикулума, пролиферация синусоидальных и мезенхимальных клеток, нарушаются печеночное кровообращение и метаболические процессы, свойственные гепатоцитам. Разрушение клеток сопровождается выходом в кровоток печеночных энзимов.

Острый вирусный гепатит В сыворотке крови значительно возрастает активность энзимов гиалоплазмы — глутаматпируваттрансаминазы или аланинаминотрансферазы (АЛТ) (К. Ф. 2. 6. 1. 2. ), глутамат-оксалоацетаттрансаминазы (ACT) (К. Ф. 2. 6. 1. 1. ). Более информативно изменение отношения активности ACT к активности АЛТ — так называемый коэффициент Де Ритиса: в норме он заметно выше единицы, при вирусном гепатите приближается к единице или становится ниже ее. АЛТ и ACT поступают в кровь через поврежденную мембрану гепатоцитов. Время полуциркуляции для ACT — 17, для АЛТ — 10 ч, поэтому при ускоренном выходе энзимов из печеночных клеток отношение возрастает в пользу ACT, длительнее

Острый вирусный гепатит n Повышается также содержание лейцинаминопептидазы (ЛАП) в сыворотке. n При некрозе гепатоцитов в крови повышается активность митохондриальных ферментов, в частности глутаматдегидрогеназы и уже упомянутой ACT. n Определение активности γглутамилтранспептидазы (ГГТ) позволяет не только констатировать наличие холестаза, сопровождающегося выходом энзима в кровоток, но и оценить динамику процесса. Содержание этого энзима в сыворотке нормализуется ранее других, что указывает на начало выздоровления.

Острый вирусный гепатит Изменяются белки крови: содержание сывороточного альбумина падает в связи со снижением белоксинтезирующей функции печени. Содержание иммуноглобулинов (вначале М, а позднее и G) увеличивается в результате активации мезенхимальной ткани. Это проявляется на электрофореграмме приростом фракции γглобулинов. Нередко наблюдается гиперлипидемия, связанная с ростом содержания триацилглицеридов и фосфолипидов (гипертриглицеридемия и фосфолипидемия).

Жировая дегенерация печени Cледствие избыточного накопления триацилглицеридов в гепатоцитах с последующим их разрывом и выходом липидов в межклеточные пространства. Различают три стадии прогрессирования процесса: I — накопление липидов без реакции со стороны мезенхимальной ткани, II — развивается мезенхимальная реакция и III — цирротические изменения на фоне избыточного накопления липидов. Их общая масса может составлять в тяжелых случаях до 40 -50% от массы печени (в норме 2 -4%). Этиологические факторы: алкоголизм, сахарный диабет, первичная гиперлипопротеинеми, хроническая кислородная недостаточность (анемия, легочное сердце), интоксикации. Роль предрасполагающих факторов могут играть избыточный вес, подагра, гликогенозы, порфирии, галактоземия.

Лабораторная диагностика Достаточно рано на возможность жирового перерождения печени указывает изменение бромсульфалеинового теста. n При развитии I стадии повышается активность сорбитол-дегидрогеназы и глутаматдегидрогеназы; n на стадии II растет активность ACT и АЛТ; n на стадии III выявляется нарушение всех функциональных проб. Для алкогольного жирового перерождения характерны повышение активности γ-глутамил -транспептидазы и рост концентрации холестерола.

Циррозы печени Хронический воспалительный процесс ведет к разрастанию соединительной ткани, которая вытесняет функциональную и замещает ее. Повышается активность элементов ретикулоэндотелиальной системы. Нарушается проточность капилляров портальной вены из-за механического сдавления, что ведет к портальной гипертензии, в связи с этим может возникать асцит. Это и наблюдается при декомпенсированном циррозе печени. Нарушение функции гепатоцитов проявляется, в частности, снижением белоксинтезирующей способности, а это вызывает гипоальбуминемию. Замедляется инактивация кортикостероидов, осуществляющаяся преимущественно в печени, что при циррозе проявляется относительным гиперальдостеронизмом. В связи с усилением функционирования портально-кавального шунта в большом круге кровообращения увеличивается

Причины развития цирроза печени: n вирусный гепатит; n злоупотребление алкоголем; n жировая дегенерация; n избыточное накопление в печени железа (гемохроматоз, гемосидероз), меди и гликогена; n внутрипеченочный холестаз. Интенсивность изменений, выявляемых лабораторно, зависит от продолжительности процесса и от степени поражения функциональной ткани печени. Наиболее характерны гипоальбуминемия, гиперглобулинемия (γфракция), патологические бромсульфалеиновый тест и тест с нагрузкой галактозой. Повышение активности трансаминаз и рост содержания аммиака в крови указывает на наступление декомпенсации.

Первичный билиарный цирроз Аутоиммунное заболевание, сопровождающееся появлением антицитоплазматических факторов, которые атакуют клетки печени, затем почек и других органов. Чаще всего заболевание начинается с мучительного кожного зуда, который как единственный признак может существовать в течение многих лет. Далее присоединяется желтуха обструктивного типа с бледным, но не ахолическим стулом и темной мочой. В период появления желтухи температура тела не повышается, самочувствие больных удовлетворительно, болей в животе нет, аппетит сохраняется, так же как и питание. Отмечается неадекватная желтухе пигментация кожи, возможно появление ксантом (плоских или в виде жировых бугорков). Характерны расчесы кожи и барабанные пальцы (в поздних периодах болезни).

Лабораторная диагностика n Наблюдается умеренная гипохромная анемия, высокая гиперлипемия и холестеролемия, а также повышенное содержание фосфолипидов. n Содержание белка в сыворотке крови длительно не изменяется, однако можно выявить рост содержания α 2 - и β-глобулинов. n Отчетливая билирубинемия появляется только на поздних стадиях. Преобладает свободный билирубин за счет усиленного гемолиза и снижения функциональной активности гепатоцитов. В кале повышено содержание жира. Ферментный спектр сыворотки крови отличается высокой активностью ACT и АЛТ, а также глутаматдегидрогеназы. n На поздних стадиях болезни содержание холестерола в крови падает и одновременно значительно возрастает билирубинемия.

Обтурация желчевыводящих путей Внепеченочный холестаз может вызываться камнями, опухолями, хроническими воспалительными процессами (отеки или пролиферация ведут к сдавливанию). Внутрипеченочный холестаз развивается при гепатитах, жировом перерождении печени, циррозах, медикаментозном или первичном билиарном циррозе. В сыворотке крови повышается активность щелочной фосфатазы, γ-глутамилтранспептидазы, растет содержание холестерола, фосфатидов, билирубина, наблюдается билирубинурия. В связи с сопутствующим панкреатитом нередко увеличивается активность αамилазы и липазы в сыворотке крови. Характерный признак — появление атипичного липопротеина X, который выявляется в гепаринкальциевом преципитате сыворотки с помощью

Первичный рак печени Возникновению способствуют злоупотребление алкоголем, наличие цирроза печени, воздействия ряда органических соединений (нитрозамины, ароматические амины) и митотоксинов (афлатоксин). Лабораторными методами исследования обнаруживают изменения, отражающие ту или иную степень нарушения функции гепатоцитов. Специфичные признаки — обнаружение α 1 фетопротеина и положительные пробы на Вантиген гепатита (не всегда).

Метастазы в печени Происходят из опухолей желчевыводящих путей, панкреатической железы, желудка, кишечника, бронхов, грудной железы и матки. Их выявление существенно для решения вопроса о целесообразности хирургического вмешательства. Лабораторно: высокая активность щелочной фосфатазы в сыворотке крови, а также зависящая от размеров и его локализации повышенная активность ACT, АЛТ, глутаматдегидрогеназы и γглутамилтранспептидазы.

Желчные пигменты Высвободившийся из эритроцитов гемоглобин транспортируется при участии гаптоглобина в клетки ретикулоэндотелия селезенки, печени и костного мозга. Здесь гем окисляется при участии микросомальной гемоксигеназы в биливердин. Последний при участии цитоплазматической биливердинредуктазы превращается в билирубин. Свободный (несвязанный) билирубин, будучи жирорастворимым, накапливаясь внутри клетки, может вызывать ее повреждения. Поступая в кровь, свободный билирубин транспортируется в комплексе с альбумином частично в виде альбуминфосфатидного комплекса и в меньшем количестве — в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами в печень. Гепатоциты извлекают билирубин из кровотока, где происходит его конъюгирование при участии УДФ-глюкуронилтрансферазы с образованием моно- и диглюкуронидов. Конъюгаты билирубина носят название связанного или конъюгированного (прямого)

Билирубинглюкурониды выделяются гепатоцитами в желчные ходы и поступают в составе желчи в 12 перстную кишку. В результате последовательно протекающих реакций восстановления, катализируемых бактериальными ферментами, через промежуточный продукт мезобилирубин преобразуются в мезобилиноген. Часть мезобилиногена удаляется с каловыми массами в виде стеркобилиногена, который на воздухе окисляется в стеркобилин. Остальной мезобилиноген всасывается в общий кровоток и выделяется с мочой (уробилиноген), отчасти — в капилляры воротной вены. Извлекается гепатоцитами и секретируется в желчные ходы, где в составе желчи расщепляется на дипиррольные соединения. Они частично всасываются в кровь, частично — выделяются в кишечник и удаляются с каловыми массами


Определение содержания желчных пигментов в крови и моче позволяет установить уровень, на котором произошло нарушение их обмена, проявляющееся возникновением желтушного окрашивания кожных покровов и конъюктив — желтухой. Выделяют три основных уровня, на которых осуществляется метаболизм гема: n надпеченочные; n подпеченочные желтухи.

Надпеченочная желтуха Связана с ускоренным высвобождением гемоглобина из эритроцитов (интенсификация гемолиза), ведущим к избыточному образованию свободного билирубина. Это наблюдается, в частности, при резком снижении осмотического давления (введение гипотонических растворов или дистиллированной воды). Может явиться следствием мембранопатий — врожденного сфероцитоза или врожденного дефицита глюкозо-6 фосфатдегидрогеназы эритроцитов.

Надпеченочная желтуха Количество образующегося свободного билирубина превышает функциональные возможности печени. В крови повышается содержание свободного (непрямого) билирубина, наблюдается билирубинемия, обусловленная ростом его содержания. Свободный билирубин не фильтруется в полость боуменовой капсулы и, следовательно, в моче не появляется. Количество стеркобилина в кале и уробилиногена в моче повышено. При сохраненной функции печени увеличение содержания свободного билирубина сопровождается ростом концентрации связанного продукта, который выделяется с желчью.

Надпеченочная желтуха Итак, для надпеченочных желтух характерны: n гипербилирубинемия за счет свободного пигмента; n прирост содержания уробилиногена в моче и стеркобилина в кале; n отсутствие билирубина в моче; n снижение резистентности эритроцитов (осмотической и кислотной).

Печеночная желтуха Связана с патологическими состояниями, при которых нарушаются: 1. Все три стадии обезвреживания свободного билирубина — элиминация из крови, конъюгирование и выведение. Это характерно для воспалительных процессов в печени, для ее токсических поражений, циррозов. В зависимости от тяжести поражения в крови возрастает уровень свободного билирубина. В повышенном количестве появляется связанный билирубин (нарушено его выведение). Изменяется содержание желчных пигментов в каловых массах. 2. Конъюгирование билирубина в связи с врожденным дефектом УДФ-глюкуронидтрансферазы. 3. Элиминация и транспорт билирубина гепатоцитом. 4. Выведение конъюгированного билирубина.

В клинике существенно различать в первую очередь тип желтухи в зависимости от механизма возникновения: механическую (препятствия на пути движения желчи), паренхиматозную (связанную с нарушением функционирования печеночной паренхимы) гемолитическую (обусловленную ускоренным распадом эритроцитов). Ниже представлены сопоставительные данные, позволяющие проводить дифференциацию этих форм желтухи


Нормальные значения биохимических показателей Используемых в диагностике печеночных заболеваний: n ACT — 0, 1 -0, 45 мкмоль/(ч. мл) (определение по Райтману. Френкелю); n АЛТ — 0, 1 -0, 68 мкмоль/(ч. мл) (те же авторы); n γ- глутамилтранспептидаза — 250 – 1767 нмоль/(с. л) — у мужчин и 167 – 1100 нмоль/(с. л) — у женщин (унифицированный метод); n щелочная фосфатаза — 278 – 830 нмоль/(с. л) (унифицированный метод с р-нитрофенилфосфатом); n глутамат-дегидрогеназа — 3, 48 -21, 0 мкмоль/(ч. л) (унифицированный метод Севела-Товарека); n общий билирубин — 8, 5 -20, 5 мкмоль/л сыворотки (по Ендрашику), из них 75% — на долю свободного; n билирубин в моче в условиях нормы не обнаруживается; n альбумин сыворотки крови — 35 -50 г/л.

Функциональные пробы: 1. Тимоловая — от 0, 0 до 4 ед. , положительна — свыше 4 (по степени помутнения сыворотки в присутствии раствора тимола — унифицированный метод). 2. Сулемовая — 1, 6 -2, 2 мл 0, 1%-ного раствора сулемы на 0, 5 мл сыворотки. Положительна при уменьшении объема раствора сулемы. 3. Вельтмана — 0, 4 -0, 5 мл 0, 5%-ного раствора хлорида кальция. Положительна при образовании осадка с меньшим количеством раствора. 4. Нагрузка галактозой. Пациент получает орально 40 г галактозы в 250 мл воды. Пробы берут через 45 и 90 мин. У здоровых людей через 90 мин концентрация галактозы в крови меньше, чем 1, 39 ммоль/л, через 45 мин — меньше 0, 84. Выделение галактозы с мочой длится при нормальной функции печени около 3 ч. Если за этот период выделяется более 3 -4 г галактозы, можно думать о нарушении функции печени.
Химия и патохимия печени.ppt