Лекция 12 Биохимия печени.pptx
- Количество слайдов: 39

БИОХИМИЯ ПЕЧЕНИ Обеспечивает регуляцию промежуточного обмена всех веществ (белкового, аминокислотного, нуклеотидного, пигментного, водно-солевого, углеводного, липидного и др. обменов). Является депо для различных соединений (углеводов, белков, минеральных веществ, витаминов и др. ). Печень принимает участие в поддержании постоянства внутренней среды организма, в регуляции гомеостаза. В печени происходит обезвреживание различных токсических соединений экзогенного и эндогенного происхождения, инактивация биологически активных соединений. Печень продуцирует желчь и в её составе обеспечивает выведение из организма некоторых метаболитов, минеральных веществ, продуктов детоксикации и др.

Химический состав клеток печени • Содержание воды колеблется в пределах 7075%, белков 12 -24%, липидов 2 -6%, гликоген 510%. • При жировой инфильтрации печени (цирроз печени) уровень липидов возрастает до 20%, • при гликогенозах увеличивается содержание гликогена, • при гемохроматозе - уровень железа и др.

Клетки печени • Звездчатые или купферовские клетки эндотелия печени относятся к ретикуло-эндотеальной системе и расположены вблизи желчных капилляров, а иногда – непосредственно в желчных капиллярах. • Эти клетки содержат большое количество лизосом и своими отростками пересекают просвет синусоидов, проникая через промежутки между соседними клетками эндотелия в пространство Диссе. • Основные клетки печени – гепатоциты, имеют характерную форму, содержат большое количество митохондрий, элементов эндоплазматического ретикулума и комплекса Гольджи, крупное ядро. • К числу клеточных элементов печени, играющих важную метаболическую роль, относятся эпителиальные клетки желчных капилляров и протоков.

Роль печени в обмене углеводов. • 1. Регуляция уровня глюкозы в крови (глюкостатическая функция печени). • Гексозомонофосфатный путь (пентозный или апотомический путь). В результате этого пути образуется большое количество НАДФН 2, необходимое для обеспечения процессов детоксикации, для синтеза холестерина, жирных кислот и др. • В печени интенсивно идет синтез глюкуроновой кислоты и мукоколисахаридов (гепарин).

Особенности липидного обмена в печени. • Продукты переваривания триацилглицеридов в стенке кишечника – жирные кислоты, в основном с короткой углеводородной цепью, из стенки кишечника попадает в кровь и доставляется в печень. • С током крови в печень из кишечника доставляются продукты переваривания липоидов (холин, коламин и др. ), • и ресинтезированные в стенке кишечника фосфолипиды, гликолипиды, холестериды, хотя в печени интенсивно идут процессы синтеза этих соединений.

• Лецитины, кефалины, серинфосфотиды, плазмогены, инозинфосфатиды и сфингомиелины - все эти соединения синтезируются в печени. • В печени человека в расчете на сырой вес содержится около 2, 9% фосфолипидов. • Из печени в комплексе с белками (липопротеидные комплексы) током крови доставляются ко всем тканям, • В тканях они используются, прежде всего, для построения клеточных мембран вновь формирующихся клеток.

Синтез фосфолипидов в печени усиливается при наличии холина, бетаина и метионина. • Поэтому эти соединения называются липотропными факторами. • При недостатке холина снижается синтез лецитина, что может привести к усилению синтеза в печени нейтральных жиров и к жировой инфильтрации этого органа. • Уровень холина, его синтез из коламина зависит от наличия метионина, как донатора метильных групп.
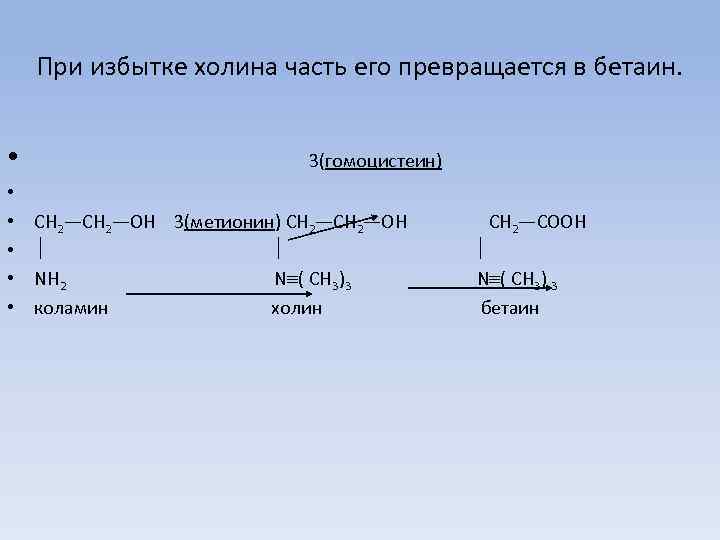
При избытке холина часть его превращается в бетаин. • • • 3(гомоцистеин) СН 2—ОН 3(метионин) СН 2—ОН NH 2 N ( СН 3)3 коламин холин СН 2—СООН N ( СН 3) 3 бетаин
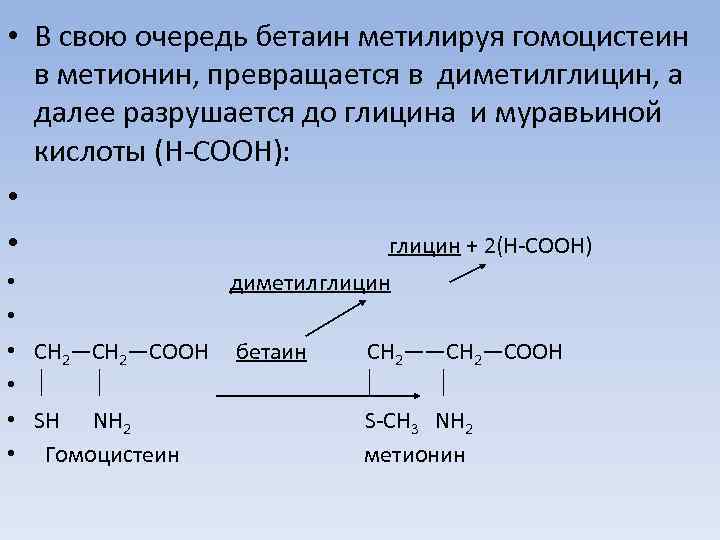
• В свою очередь бетаин метилируя гомоцистеин в метионин, превращается в диметилглицин, а далее разрушается до глицина и муравьиной кислоты (Н-СООН): • • глицин + 2(Н-СООН) • диметилглицин • • СН 2—COOH бетаин СН 2——СН 2—СООН • • SH NH 2 S-СН 3 NH 2 • Гомоцистеин метионин

Печень является основным органом, в котором интенсивно идет синтез холестерина (80%). • В меньшей степени холестерин синтезируется в надпочечниках, яичниках, семенниках, в коже и в стенке кишечника. • Ферменты необходимые для синтеза холестерина имеются во всех клетках, кроме зрелых эритроцитов. • За сутки в печени синтезируется 1, 5 - 4, 0 грамм холестерина (в среднем 2, 0 гр. ).

• С пищей в течение суток человек получает 0, 4 – 0, 5 грамм холестерина. • Общее содержание холестерина в организме человека весом 70 кг составляет 105 -175 г или 0, 2% веса тела. • При этом его содержание наиболее высокое в надпочечниках (4, 5 -10%) и в мозге (2%). • В печени, холестерина всего около 0, 3% , из которых, на долю свободного холестерина (не этерифицированного) приходится 80%, на долю этерифицированного – 20%.

• На интенсивность синтеза холестерина в печени влияет количество экзогенного холестерина поступающего с пищей. • При снижении уровня холестерина в пище скорость синтеза холестерина в печени возрастает и наоборот. • Усиление синтеза холестерина в печени наблюдается при потреблении большого количества жиров, как источника ацетил-Ко. А, который служит источником • для синтеза не только жирных кислот и кетоновых тел, но и холестерина.

• Скорость синтеза холестерина регулируется по механизму отрицательной обратной связи. • Основным пунктом регуляции является фермент, синтезирующий мевалоновую кислоты - ГМГ-Ко. А -редуктаза. • Холестерин ингибирует этот фермент собственного синтеза. • Так при содержании 2 -3 гр. холестерина в суточной пище человека синтез собственного холестерина почти полностью прекращается.

• Если холестерин в пище полностью отсутствует, • то его синтез в тканях происходит с максимальной скоростью. • Чем больше поступление холестерина с пищей, • тем меньше синтезируется холестерин в тканях и • тем большую долю экскретируемого из организма холестерина составляет холестерин пищи.

В печени из холестерина синтезируются желчные кислоты. • Образование желчных кислот включает реакции гидроксилирования и реакции частичного окисления боковой цепи холестерина. • Первым этапом биосинтеза желчных кислот является 7 -гидроксилирование холестерина микросомальной 7 -гидроксилазой при участии кислорода, НАДФН 2, цитохрома Р 450 и витамина С. На этой стадии синтезируется 7 гидроксихолестерол.

При недостатке витамина С образование желчных кислот на стадии 7 гидроксилирования тормозится, что приводит к накоплению холестерина и развитию атеросклероза и др.

Желчные кислоты участвуют в эмульгировании жиров в кишечнике и во всасывании продуктов их переваривания • Вследствие этого, основная часть желчных кислот из полости кишечника всасывается в клетки, с кровью воротной вены попадает в печень и повторно используется при образовании желчи. • Небольшая часть желчных кислот (0, 5 г за сутки) выводится из организма с калом.

В составе смешанных мицелл с желчными кислотами выводится и холестерин. • В пузырной и печеночной желчи холестерин находится в этерифицированной форме, будучи включенной макромицелу липидного комплекса. • В кишечнике при разрушении этого комплекса происходит освобождение холестерина и его частичная реабсорбция.

На реабсорбцию холестерина в стенку кишечника влияют желчные кислоты, активность холэстеразы, наличие пищевых белков, лактозы и другие факторы • Не всосавшийся в стенку кишечника холестерин под воздействием ферментов кишечной микрофлоры гидрируется до копростерина и выводится из организма в составе каловых масс. • Общее количество холестерина выводимого из организма с калом в составе желчи и в виде желчных кислот за сутки составляет у взрослого человека около 1, 3 гр.

В нормальном стационарном состоянии суммарное количество холестерина, поступающего в кишечник с пищей, и холестерина, синтезированного в тканях, должно быть равно суммарному количеству экскретируемого холестерина и холестерина превращенного и экскретируемого в виде желчных кислоты: ХОЛ( пищ ) + ХОЛ(синт) = ХОЛ(экскр) + Желч. кисл. (экскр) Одним из последствий нарушения этого баланса является гиперхолестеринемия, последствиями которой являются желчекаменная болезнь, ишемическая болезнь сердца и атеросклероз.

• При желчекаменной болезни в желчном пузыре или желчных протоках образуются камни в результате осаждения и кристаллизации компонентов желчи холестерина и билирубина. • Обычно в желчных камнях основная масса приходится на холестерин. Образование холестериновых камней, как следствие дестабилизации жидкокристаллической формы холестерина, происходит вследствие увеличения количества холестерина в составе желчи и уменьшения синтеза или экскреции желчных кислот. • Осаждению холестерина способствует застой желчи, воспалительные заболевания желчного пузыря и протоков. • Центрами кристаллизации холестерина могут служить конгломераты белка или слущивающиеся клетки эпителия.

Консервативным способом лечения желчекаменной болезни является использование хенодезоксихолевой кислоты, от которой в наибольшей степени зависит растворимость холестерина. • Кроме того, хенодезоксихолевая кислота ингибирует ГМГ-Ко. А-редуктазу и приостанавливает синтез холестерина на уровне образования мевалоновой кислоты. • Так приеме 1 г хенодезоксихолевой кислоты в день синтез холестерина уменьшается в два раза и его концентрация в желчи уменьшается. • В этих условиях не только прекращается осаждение холестерина, но становится возможным растворение уже имеющихся камней.

Печени принадлежит особая роль в депонировании и метаболизме жирорастворимых витаминов • В тонком кишечнике при участии желчных кислот провитамины группы А (каротины), витамины Д и Е интенсивно всасываются в стенку кишечника и далее доставляются в печень. • В печени каротины вначале накапливаются в купферовских клетках, а затем переносятся в другие структуры.

• Ферментативное разрушение каротинов под воздействием оксигеназ с образованием альдегидной (ретиналь) и спиртовой (ретинол) форм витамина А происходит в гепатоцитах. • При избыточном поступлении с пищей каротинов или витамина А, последний может накапливаться в печени в количествах превышающих средние нормы в десятки, и даже сотни раз. • Витамин А присутствует в тканях, как в виде свободного спирта, так и в виде эфиров пальмитиновой и других жирных кислот. • Витамин А накапливается в особых запасающих жиры клетках печени в виде ретинилпальмитата

• Более существенную роль играет печень в межуточном обмене нафтохинонов - витаминов К: филлохинон (витамин К 1) и менахинон витамин К 2) • Для всасывания витаминов К в тонком кишечнике необходимы желчные кислоты и панкреатическая липаза. • Транспортируются в составе хиломикронов или в комплексе с альбуминами крови, накапливаются в печени, селезенке и сердце. • Витамин К участвует в процессе гемокоагуляции, в частности, способствуя карбоксилированию глутамата с образованием гамма-карбоксиглутамата в молекуле протромбина (фактор II): • НООС-СН-СН 2 -СН-СООН • • NH 2 COOH • гамма-карбоксиглутамат • Аналогичные изменения происходят в молекулах проконвертина (фактор VII), фактора IX (Кристмана) и фактора X (Стюарта). Эти процессы происходят в печени.

• Всосавшиеся в стенку кишечника аминокислоты по системе воротной вены поступают в печень, где включаются в различные анаболитические и катаболитические превращения. • В гепатоцитах и клетках ретикулоэндотелиальной системы аминокислоты используются для синтеза различных белков. • За сутки в печени синтезируется около 12 г альбуминов. • В печени синтезируется большая часть - и глобулинов плазмы крови, фибриноген, протромбин и другие факторы системы гемокоагуляции и противосвертывающей системы крови. • При ишемии печени, при циррозах, токсических гепатитах, нарушениях оттока желчи синтез альбуминов в печени снижается.

• При патологии могут происходить качественные сдвиги синтезируемых в печени белков. • Например, при циррозе печени снижается содержание сульфгидрильных групп в белках плазмы крови, • что приводит к изменениям их электрофоретической подвижности и иммунологических свойств. • Формируются аномальные белки – парапротеины, близкие по своим физикохимическим свойствам к -глобулинам.

• В печени синтезируются белки обеспечивающие транспорт железа (ферритин, трансферрин), меди (церулоплазмин), гормонов (транскортин), транспортирующие витамины и липиды (ЛПОНП, ЛПВП). • Синтезируются семь типов соматомединов А 1, А 2, В 1, В 2, В 3, В 4, С – посредников в реализации эффектов соматотропного гормона гипофиза. • Около 50% вновь синтезируемых в организме человека белков образуется в печени. • При белковом голодании печень быстро мобилизует свои резервные белки для снабжения аминокислотами других тканей. • В гепатоцитах идут процессы синтеза железопорфиринов, структурных компонентов ферментов цитохромной системы, миоглобина и гемоглобина, хотя основную роль в биосинтезе гемоглобина выполняет костный мозг, где созревают эритроциты.

• • Синтез азотистых небелковых соединений (холина, креатина, глутатиона, пуриновых и пиримидиновых оснований, порфиринов) • В печени интенсивно идут процессы взаимопревращения аминокислот, • В печени происходит процесс обезвреживания аммиака • В купферовских клетках печени идет разрушение гема гемоглобина до билирубина, образование коньюгатов желчных пигментов с глюкуроновой кислотой и выведение их в составе желчи.

Механизмы детоксикации в печени. • В печени происходит разрушения лекарственных соединений, и токсинов, чужеродных соединений (ксенобиотики). • Обезвреживание (детоксикация), инактивация в печени осуществляется посредством интеграции следующих двух основных механизмов: • реакциями гидроксилирования (окисления) • реакциями конъюгации

• Реакции гидроксилирования. • Гидроксилирование (окисление) ядов катализируется ферментами «микросомальной» дыхательной цепи, локализованной в эндоплазматическом ретикулуме, с использованием молекулярного кислорода и НАДФН 2. • При этом один атом кислорода идет на формирование в молекуле токсина (R) ОН-группы, а второй восстанавливается, образуя воду, на образование которой используется НАДФН 2. • Основными ферментами этой системы являются: • 1. флавопротеид НАДФН 2 -цитохром Р-450 – редуктаза • (ФАД) • 2. адренодоксин (рубредоксин или ферродоксин) • 3. цитохром Р 450 (Fe+++ Fe++) • Из этих ферментов формируется дыхательная цепь, в которой происходит гидроксилирование ядов: • R • • НАДФН 2 ФАД адренодоксин Р 450 R-OH Н 2 О • • О 2

• Адренодоксин содержит негеминовое железо, посредством которого этот фермент восстанавливает железа цитохрома Р-450. • Известно несколько форм цитохрома Р-450 печени млекопитающих. • Все они прочно связаны с мембранами эндоплазматического ретикулума и их трудно солюбилизировать. • Некоторые их не нуждаются в белках типа рубредоксин и др. , поскольку могут непосредственно восстанавливаться от ФАДН 2. • Различные лекарственные вещества, например фенобарбитал, могут индуцировать синтез цитохром Р 450, увеличивая уровень и активность цитохрома Р-450 почти в 20 раз. • Этот процесс является своеобразным защитным механизмом, ускоряющим процессы детоксикации в основном ароматических соединений в печени.

• Реакции конъюгации. • Обезвреживание в печени может происходить путем присоединения к ядам различных соединений. • В результате образуются нетоксичные (неактивные) конъюгаты. • В качестве веществ присоединяемых к ядам в печени используются: • глюкуроновая кислота (УДФ-глюкуроновой кислоты), • серная кислота, находящаяся в составе фосфоаденозин фосфо-сульфата (ФАФС), • глицин, глутамин, • таурин или цистеин. • ацетильная группа от ацетил-Ко. А, • метильная группа от S-аденозилметионина

Канцерогенез • Подсчитано, что 80% опухолей человека вызывается факторами окружающей среды, в основном химическими веществами. • Воздействие на организм человека этих веществ может быть связано с профессиональной деятельностью (фенол, бензол, асбест, арсенат, бериллий, кадмий, хром), образом жизни (курение), особенностями питания (наличие в пищевых продуктах нитратов, нитрозаминов, ароматических аминов афлотоксина В, продуцируемого плесневым грибком Aspergillus flavus и др. ), • использование некоторых так называемых лекарственных препаратов. • Установлено, что канцерогенные соединения зачастую образуются в печени в тех же реакциях гидроксилирования, метилирования и др.

• Канцерогенные свойства присущи целому ряду химических соединений. • Попадая в организм и подвергаясь метаболическим превращениям, они образуют соединения вызывающие развитие опухолей. • Например, 3 -метилхолантрен, сильный индуктор цитохрома Р 450, в результате гидроксилирования превращается в мощный канцероген. • Аналогично, находящийся в табачном дыме ароматический полициклический углеводород бензантрацен (бензпирен) подвергаясь в печени «обезвреживанию» путем гидроксилирования превращается в канцероген – эпоксид бензантрацена, вызывающий алкилирование ДНК, РНК и белков. •

• У людей занятых в производстве анилиновых красителей в результате контакта с ароматическим амином 2 -нафтиламином в печени в результате гидроксилирования образуется 2 -амино-1 -нафтол канцероген, вызывающий рак мочевого пузыря. • Другой ароматический амин – ацетиламинофлуорен вызывает рак печени. • Нитрозамины, образующиеся из вторичных алифатических аминов и нитритов, попадая в организм с пищей, под воздействием ферментов микросомальной фракции клеток окисляясь, образует высокоактивный ион карбония СН+3. • Этот ион способен метилировать белки и нуклеиновые кислоты и тем самым индуцировать образование опухолей печени, почек, легких, желудка и пищевода.

Желчеобразовательная и экскреторная функции печени. • Желчь как биологическая жидкость, выполняет целый ряд функций: • - вызывает эмульгирование жиров, • - обеспечивают всасывание жирных кислот и холестерина, • - способствуют всасыванию жирорастворимых витаминов, • - участвуют в создании определенного уровня р. Н в тонком кишечнике, необходимого для нормального пищеварения, • - обеспечивают растворимость холестерина и его выведение из организма, • - способствует метаболизму желчных пигментов в пигменты кала и мочи, • выполняет экскреторную функцию – выведение из организма в составе желчи холестерина, желчных пигментов, метаболитов гормонов, токсинов, лекарств и др.
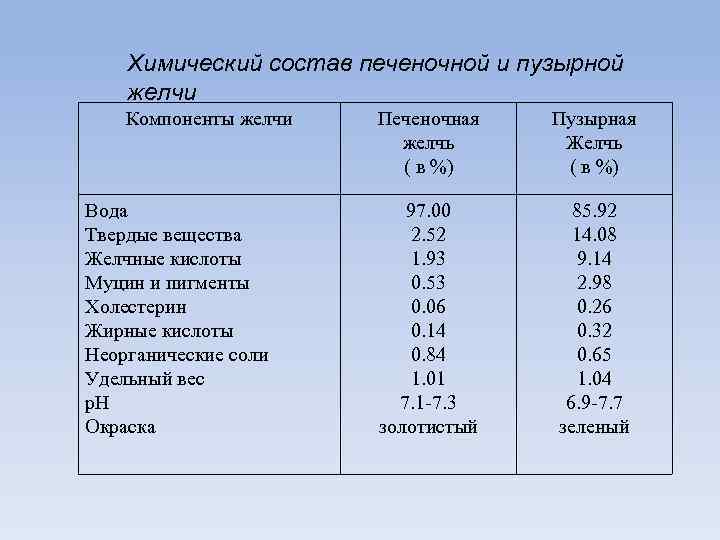
Химический состав печеночной и пузырной желчи Компоненты желчи Вода Твердые вещества Желчные кислоты Муцин и пигменты Холестерин Жирные кислоты Неорганические соли Удельный вес р. Н Окраска Печеночная желчь ( в %) Пузырная Желчь ( в %) 97. 00 2. 52 1. 93 0. 53 0. 06 0. 14 0. 84 1. 01 7. 1 -7. 3 золотистый 85. 92 14. 08 9. 14 2. 98 0. 26 0. 32 0. 65 1. 04 6. 9 -7. 7 зеленый

Thanks for attention
Лекция 12 Биохимия печени.pptx