Биохимия нуклеиновых кислот Фридрих


Биохимия нуклеиновых кислот

Фридрих Мишер в 1869 изолировал из спермы лосося и ядер клеток гноя неизвестное до сих пор вещество. Поскольку он выделил его из ядра (лат. — nucleus), ученый назвал его нуклеином. Позже вещество было названо нуклеиновой кислотой.
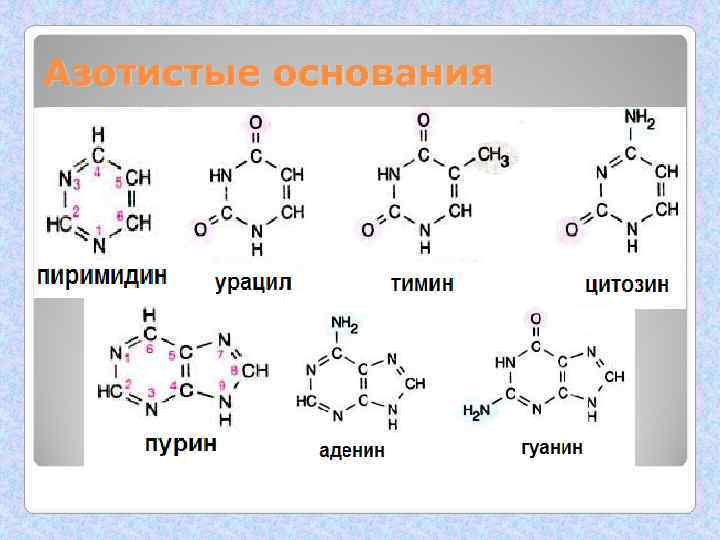
Азотистые основания
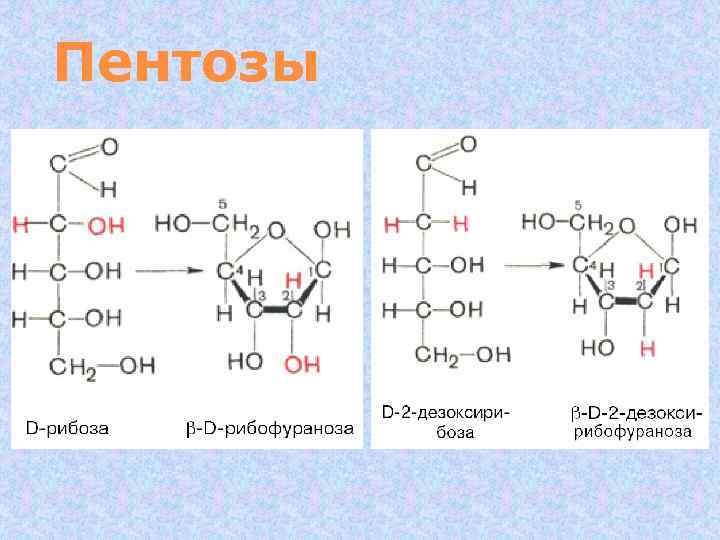
Пентозы
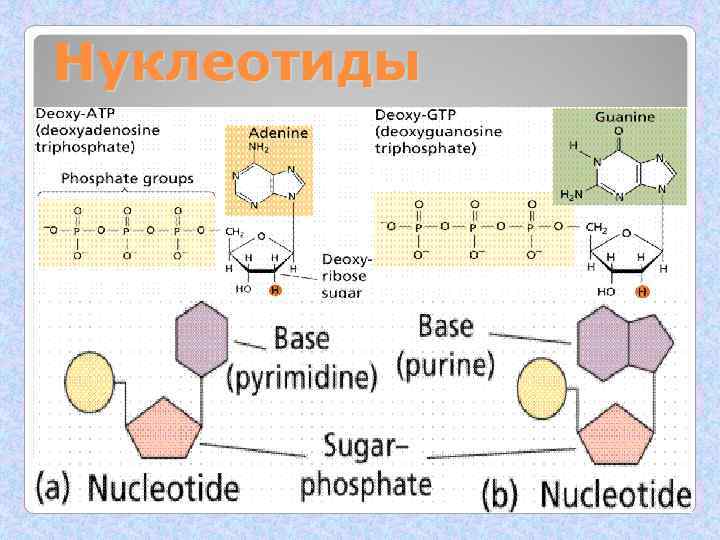
Нуклеотиды
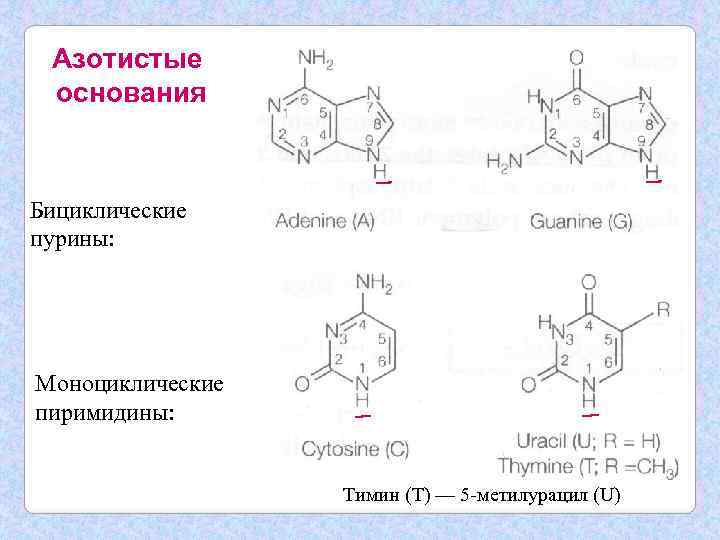
Азотистые основания Бициклические пурины: Моноциклические пиримидины: Тимин (T) — 5 -метилурацил (U)
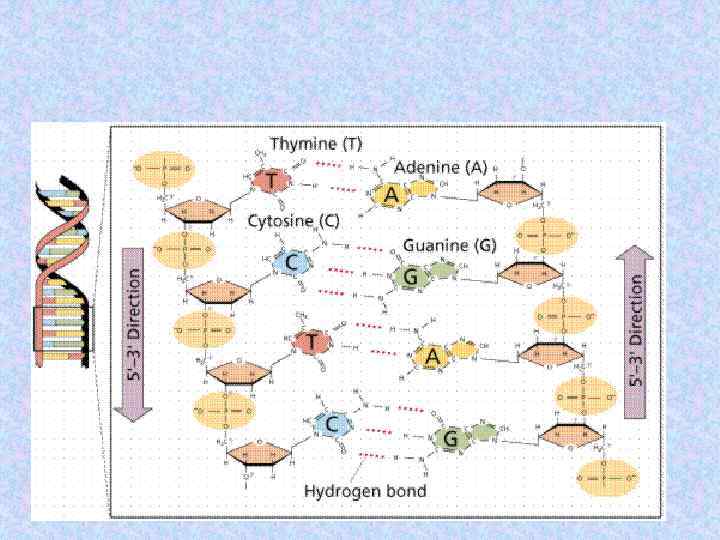
Двойная цепь

Переваривание нуклеотидов и всасывание продуктов их распада осуществляется в желудочно-кишечном тракте. желудочно-кишечном тракте Под влиянием ферментов желудка и кишечника, частично НС l , нуклеопротеиды пищи распадаются на белок и нуклеиновые кислоты Распад нуклеиновых кислот осуществляется в основном гидролитическим путем в тонком кишечнике под действием ДНК-азы и РНК-азы поджелудочного сока. ДНК-азы РНК-азы Продуктами реакции при действии РНК-азы являются: • пиримидиновые мононуклеотиды • смесь ди- и тринуклеотидов • олигонуклеотиды Продуктами реакции при действии ДНК-азы являются: • динуклеотиды • олигонуклеотиды • небольшое количество мононуклеотидов

Полный гидролиз нуклеиновых кислот осуществляется ферментами слизистой оболочки кишечника – фосфодиэстеразами Мононуклеотиды в кишечнике расщепляются под Мононуклеотиды действием неспецифических фосфатаз (кислой и щелочной). Частично распад осуществляется в клетках слизистой оболочки кишечника под действием нуклеотидаз. нуклеотидаз Нуклеозиды могут быть использованы для синтеза нуклеиновых кислот организма. Если же происходит дальнейший распад, то гуанин не используется для синтетических целей. Аденин и урацил могут включаться в состав нуклеиновых кислот.

Таким образом, синтез нуклеиновых кислот определяется скоростью синтеза пуриновых и пиримидиновых нуклеотидов Источником рибозы и дезоксирибозы является глюкоза или ее метаболиты в пентозофосфатном пути. Фосфорная кислота поступает в достаточном количестве с пищей.

Пути распада нуклеиновых кислот Полимерные молекулы нуклеиновых кислот расщепляются в тканях преимущественно гидролитическим путем при участии специфических ферментов – нуклеаз. нуклеаз Ускоряют реакцию разрыва межнуклеотидных фосфодиэфирных связей в молекулах нуклеиновых связей кислот. Ферменты подкласса фосфодиэстераз

1. По месту действия q Эндонуклеазы ü расщепляют внутренние межнуклеотидные связи в молекуле ДНК и РНК ü вызывают деполимеризацию нуклеиновых кислот и образование олигонуклеотидов q Экзонуклеазы ü вызывают последовательное гидролитическое отщепление концевых мононуклеотидов от ДНК, РНК или от олигонуклеотидов ü обеспечивают распад нуклеиновых кислот до свободных нуклеотидов.

2. По специфичности действия q Рибонуклеазы (РНК-азы) ускоряют реакции распада межнуклеотидных связей в молекулах РНК; q Дезоксирибонуклеазы (ДНК-азы) выполняют такую же функцию по отношению ДНК; q Неспецифические нуклеазы действуют и на РНК, и на ДНК.

3. По характеру действия на фосфодиэфирные связи q 3’-нуклеазы – расщепляют связи межнуклеозидного фосфата с 5’-атомом углерода остатка рибозы или дезоксирибозы; q 5’-нуклеазы – расщепляют связи межнуклеозидного фосфата с 3’-атомом углерода остатка рибозы или дезоксирибозы.

Дезоксирибонуклеазы I Ускоряют гидролиз фосфодиэфирных связей в одной гидролиз из цепей ДНК между остатком Н 3 РО 4 и 3’-атомом углерода остатка дезоксирибозы с образованием олигодезоксирибонуклеотидов Пример: панкреатическая ДНК-аза оптимум р. Н – 6, 8 -8, 0 активаторы – Mg 2+, Mn 2+ ингибиторы – олигонуклеотиды и анионы, связывающие Mg 2+ и Mn 2+

Дезоксирибонуклеазы II Вызывают деполимеризацию молекулы ДНК в результате парных разрывов фосфодиэфирных связей обеих цепей с образованием более крупных олигонуклеотидов Пример: ДНК-аза селезенки оптимум р. Н – 4, 5 -5, 5 активаторы – Mg 2+ ингибиторы – SO 42–, РО 43–, As. О 43–, т. РНК

Экзодезоксирибонуклеазы Гидролизуют молекулы ДНК с Гидролизуют образованием дезокисрибонуклеозид- 5’-фосфатов.

Рестриктазы ДНК-азы бактериального происхождения. Расщепляют чужеродные (фаговые) ДНК в строго Расщепляют определенных зонах , имеющих палиндромную структуру, на ограниченное число фрагментов. на ограниченное число фрагментов Рестриктазы применяются в генетической инженерии , так как из ДНК выщепляются фрагменты, которые затем встраиваются в бактериальную ДНК, принося бактерии новые биохимические признаки (например, способность синтезировать интерферон, инсулин и другие белки).

Рибонуклеазы I Ускоряют реакцию гидролиза РНК по РНК пиримидиновым нуклеотидным остаткам.

Гуанилрибонуклеазы Ускоряют гидролиз связей по 5’- углеродному атому рибозы остатка гуаниловой кислоты и межнуклеотидного фосфата в молекуле РНК , образуя гуанозин-3’-фосфат и олигонуклеотиды с концевым гуанозин-3’-фосфатом.

Экзорибонуклеазы Ускоряют реакции отщепления рибонуклеотидов по концевым остаткам рибонуклеотидов РНК. Нуклеиновые кислоты дают при распаде смесь рибо- и дезоксирибонуклеозид-3’ и 5’-фосфатов

Полинуклеотидфосфорилаза Переносит нуклеотидные остатки с 3’-конца РНК на Н 3 РО 4 образованием нуклеозиддифосфатов.
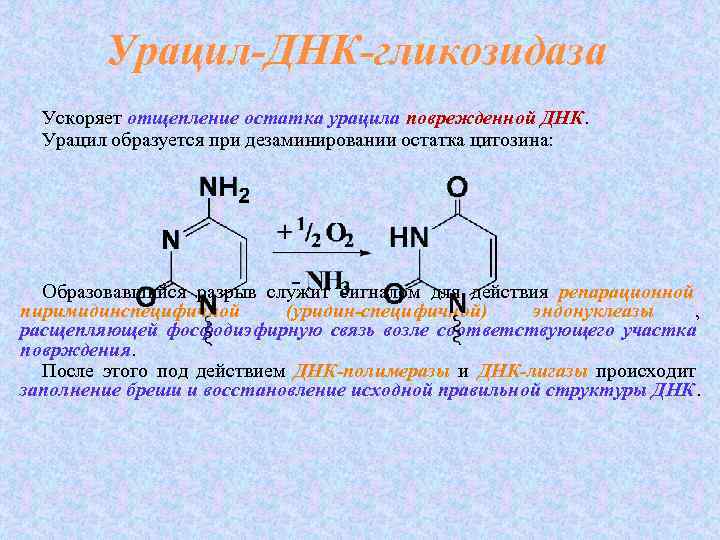
Урацил-ДНК-гликозидаза Ускоряет отщепление остатка урацила поврежденной ДНК. поврежденной ДНК Урацил образуется при дезаминировании остатка цитозина: Образовавшийся разрыв служит сигналом для действия репарационной пиримидинспецифичной (уридин-специфичной) эндонуклеазы , расщепляющей фосфодиэфирную связь возле соответствующего участка поврждения После этого под действием ДНК-полимеразы и ДНК-лигазы происходит заполнение бреши и восстановление исходной правильной структуры ДНК
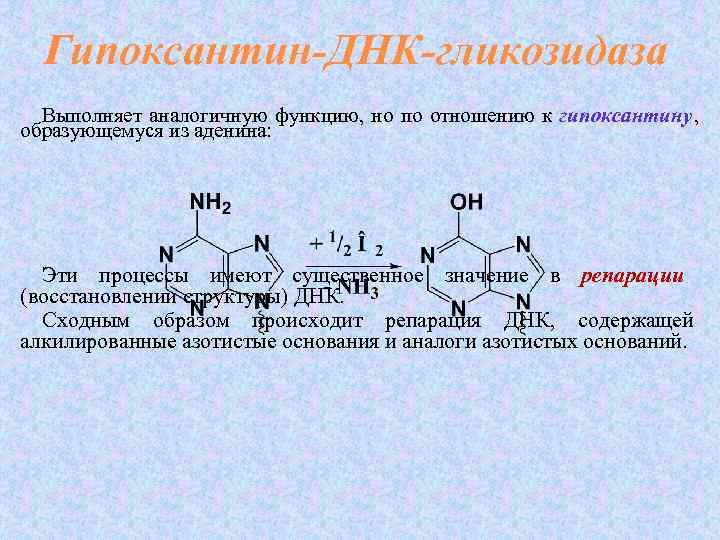
Гипоксантин-ДНК-гликозидаза Выполняет аналогичную функцию, но по отношению к гипоксантину , образующемуся из аденина: Эти процессы имеют существенное значение в репарации (восстановлении структуры) ДНК. Сходным образом происходит репарация ДНК, содержащей алкилированные азотистые основания и аналоги азотистых оснований.

Нуклеозидфосфаты подвергаются гидролизу: 1. нуклеотид (нуклеозидфосфат) + Н 2 О → нуклеозид + Н 3 РО 4 фермент 5’(или 3’)-нуклеотидаза 2. перенос остатка рибозы от нуклеотида на Н 3 РО 4: нуклеозид + Н 3 РО 4 → Р-1 -Ф + АО фермент рибозилтрансфераза или гидролиз: нуклеозид + Н 2 О → АО + рибоза фермент нуклеозидаза

Конечным продуктом пуринового обмена является мочевая кислота. мочевая кислота 18– 20% распадается до СО 2 и N Н 3 и 18– 20% выделяется через кишечник , остальное выводится с мочой ( в сутки до 400– 600 мг). Мочевая кислота является антиоксидантом
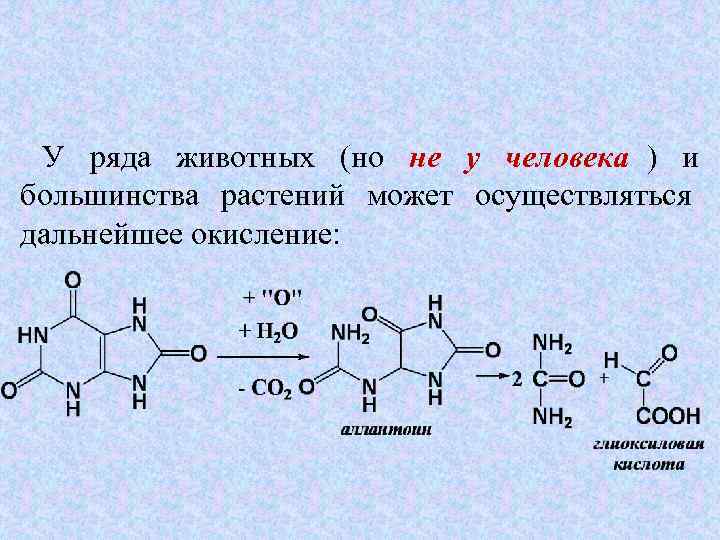
У ряда животных (но не у человека ) и большинства растений может осуществляться дальнейшее окисление:
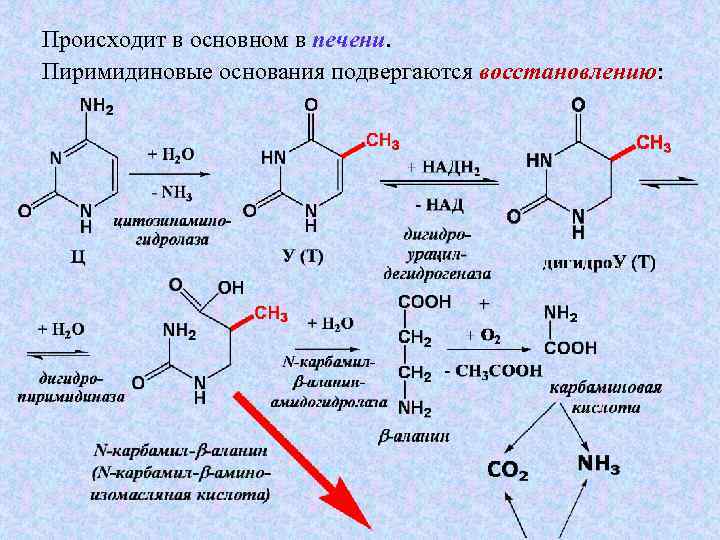
Происходит в основном в печени. печени Пиримидиновые основания подвергаются восстановлению: восстановлению

1. Образование карбамилфосфата из NН 3 и СО 2 при участии АТФ
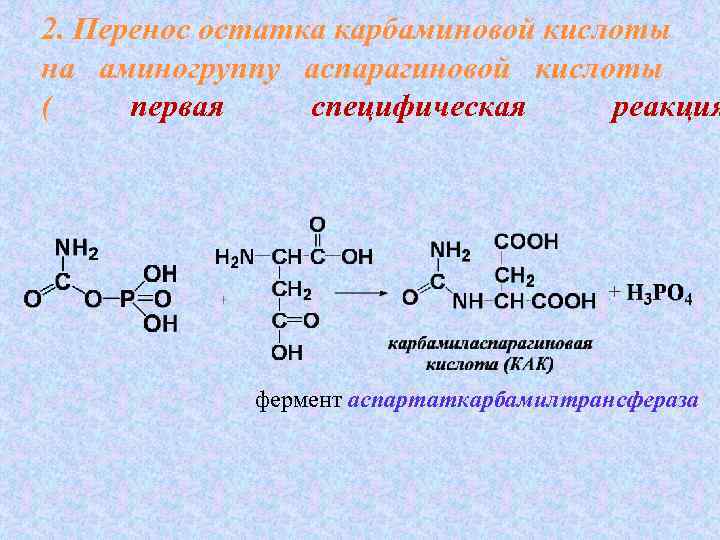
2. Перенос остатка карбаминовой кислоты на аминогруппу аспарагиновой кислоты ( первая специфическая реакция фермент аспартаткарбамилтрансфераза
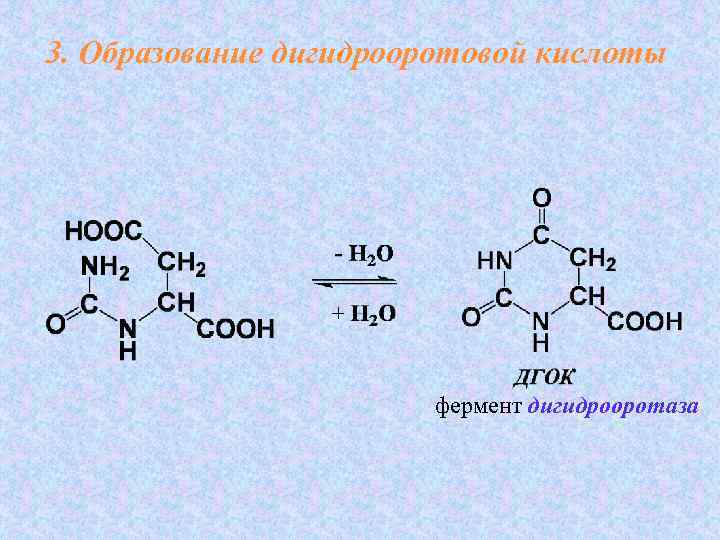
3. Образование дигидрооротовой кислоты фермент дигидрооротаза
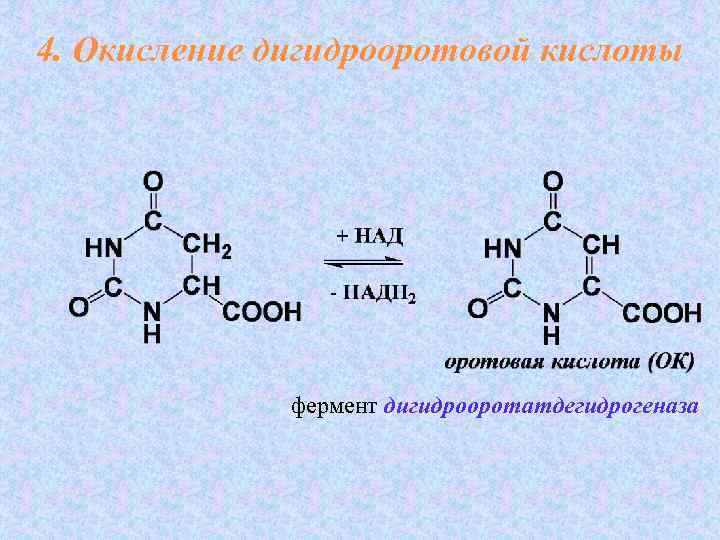
4. Окисление дигидрооротовой кислоты фермент дигидрооротатдегидрогеназа
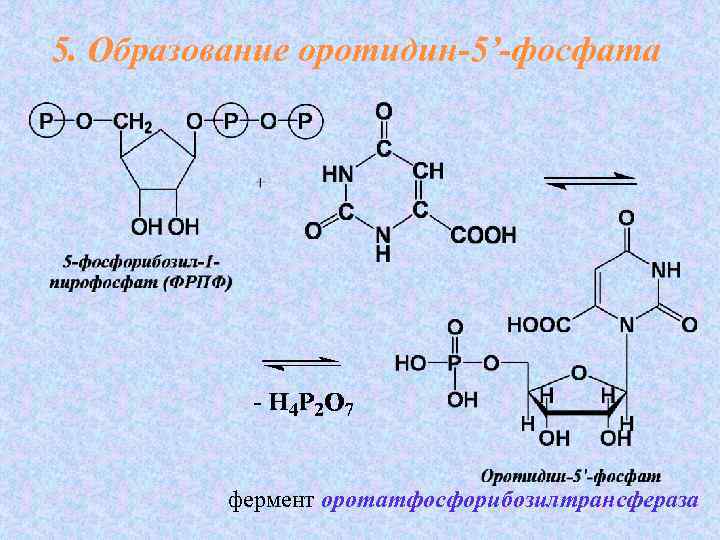
5. Образование оротидин-5’-фосфата фермент оротатфосфорибозилтрансфераза

Все эти реакции происходят в цитозоле клетки, а остальные цитозоле реакции – в митохондриях. митохондриях
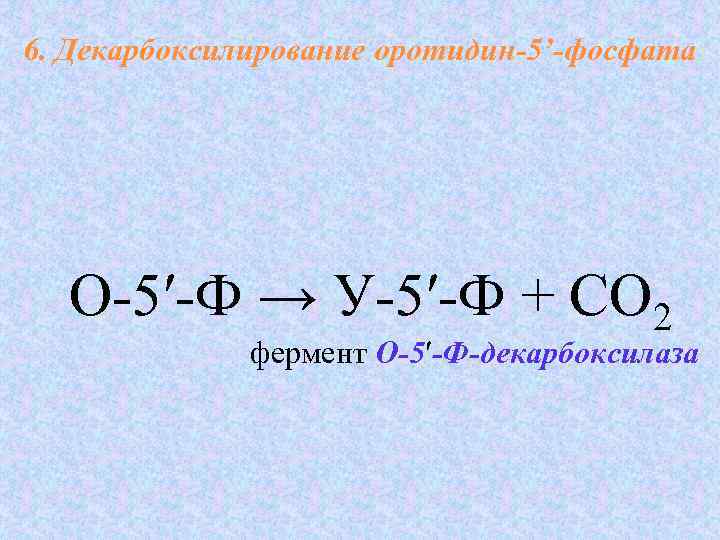
6. Декарбоксилирование оротидин-5’-фосфата О-5′-Ф → У-5′-Ф + СО 2 фермент О-5′-Ф-декарбоксилаза О-5

7. Превращения У-5′-Ф в другие пиримидиновые нуклеотиды Путем реакций восстановления , аминирования и метилирования моно-, ди- и трифосфорных эфиров нуклеозидов. метилирования Трифосфорные эфиры образуются при взаимодействии нуклеозидмонофосфатов с АТФ: УМФ + АТФ → УДФ + АДФ УДФ + АТФ → УТФ + АДФ УТФ аминируется до ЦТФ : УТФ + АТФ + Глн ЦТФ + Глу + АДФ + Н 3 РО 4 фермент ЦТФ-синтаза Восстановление по остатку рибозы приводит к образованию дезоксирибонуклеотидов (фермент рибонуклеотидредуктаза). рибонуклеотидредуктаза Тимидиловые нуклеотиды образуются путем метилирования д. УМФ (фермент тимидилатсинтаза). тимидилатсинтаза

Синтез пиримидиновых нуклеотидов регулируется конечными продуктами

1. Образование 5 -фосфорибозил-1 -пирофосфата Р-5 -Ф + АТФ → 5 -ФР-1 -ПФ + АМФ фермент пирофосфорилаза
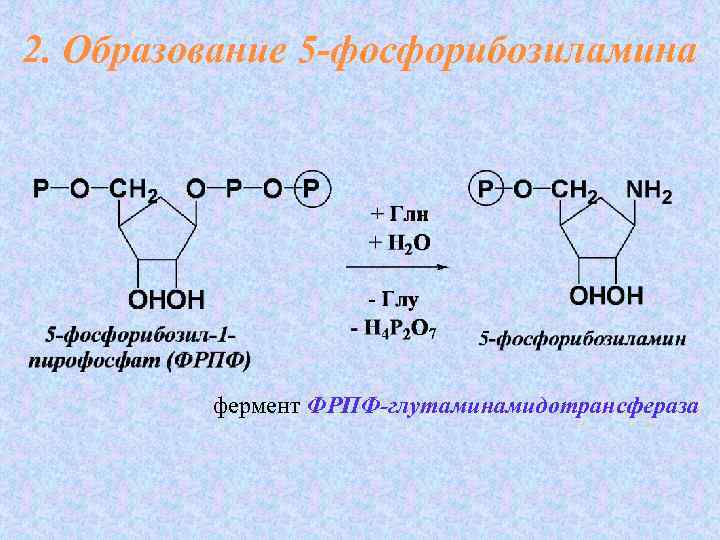
2. Образование 5 -фосфорибозиламина фермент ФРПФ-глутаминамидотрансфераза
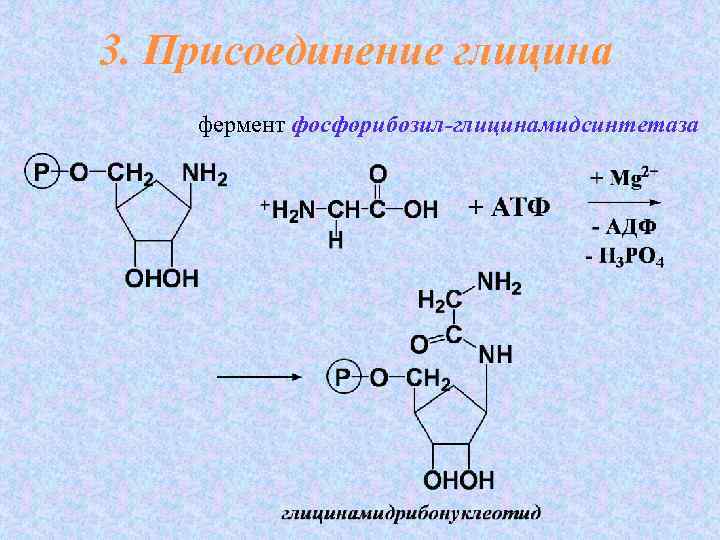
3. Присоединение глицина фермент фосфорибозил-глицинамидсинтетаза
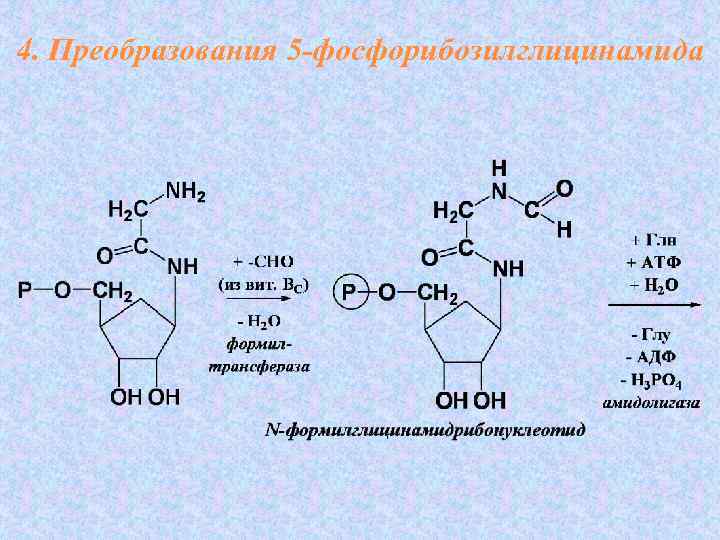
4. Преобразования 5 -фосфорибозилглицинамида

Суммарное уравнение этапа 4: 5 -фосфорибозилглицинамид + 2–СНО(Вит ВС) + Глн + 3 АТФ + СО 2 + Асп → → 2 Н 2 О + Глу + 3 АДФ + 3 Н 3 РО 4 + Фумарата + ИМФ
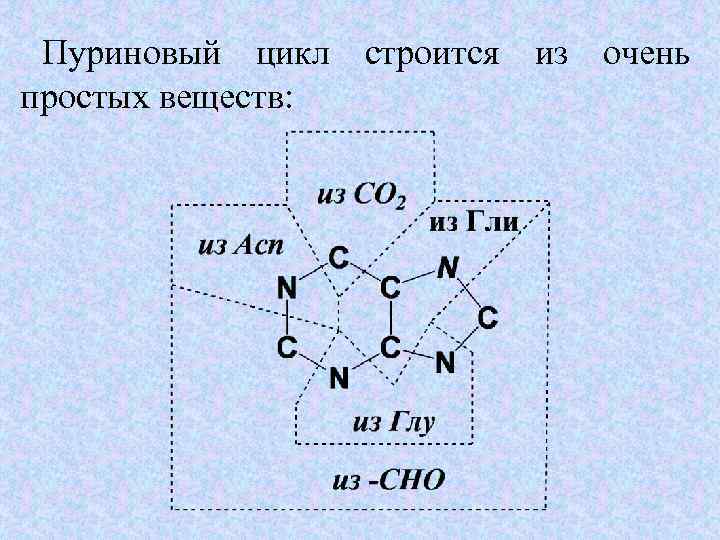
Пуриновый цикл строится из очень простых веществ:
Лекция Обмен нуклеиновых кислот.ppt
- Количество слайдов: 43

