Биохимия миокарда Кафедра биохимии Дмн, проф. Грицук


Биохимия миокарда Кафедра биохимии Дмн, проф. Грицук А. И.
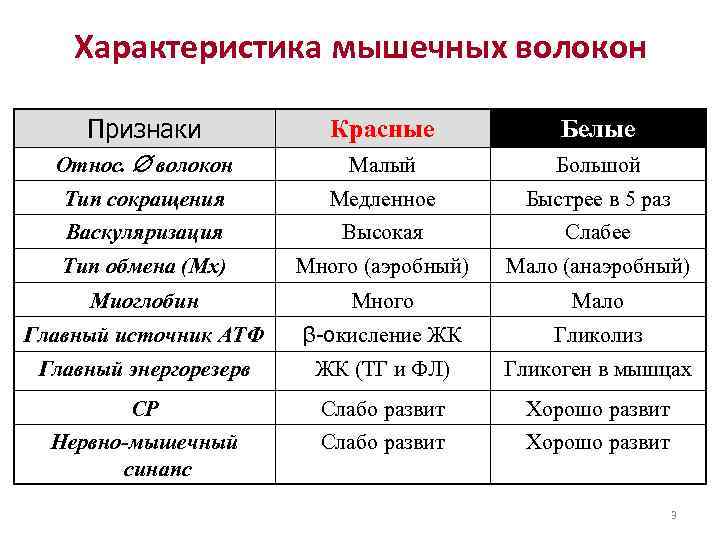
Характеристика мышечных волокон Признаки Красные Белые Относ. волокон Малый Большой Тип сокращения Медленное Быстрее в 5 раз Васкуляризация Высокая Слабее Тип обмена (Мх) Много (аэробный) Мало (анаэробный) Миоглобин Много Мало Главный источник АТФ β-окисление ЖК Гликолиз Главный энергорезерв ЖК (ТГ и ФЛ) Гликоген в мышцах СР Слабо развит Хорошо развит Нервно-мышечный Слабо развит Хорошо развит синапс 3

Сердечная мышца • Сочетают свойства обоих волокон • Значительное количество Мх до 25 -30% объема клетки. • Кардиомиоциты рано перестают делиться. • Очень быстрая замена белков, особенно сократительных – Полная замена за один месяц. 4
![Механизмы стабилизации [АТФ] • В процессе мышечного сокращения АТФ 4– → АДФ Механизмы стабилизации [АТФ] • В процессе мышечного сокращения АТФ 4– → АДФ](https://present5.com/presentation/3/38271257_295460127.pdf-img/38271257_295460127.pdf-4.jpg)
Механизмы стабилизации [АТФ] • В процессе мышечного сокращения АТФ 4– → АДФ 3– + Фн 2 - + Н+ АДФ 3– имеет ~ которую можно использовать в аденилаткиназной реакции 2 АДФ 3– ↔ АТФ 4– + АМФ 2 -, • Для смещения реакции вправо АМФ 2 - гидролизуется АМФ-дезаминазой АМФ 2 - → ИМФ + NH 3 5

Особенности биохимии миокарда • Аэробный фенотип метаболизма - Аэробная ткань (7 -20% всего кислорода) аэробные изоферменты. –ЛДГ 1 и ЛДГ 2 –КФК 2 (MB-изоформа). • Высокая скорость ЦТК, b-окисления ЖК, очень низкая – анаэробного гликолиза (субсарколеммальная локализация). • На сарколемме высокая активность АТФ-аз. • Энергосубстраты – ЖК, кетоновые тела глюкоза, лактат. . –Особенно активно из крови миокард извлекает ненасыщенные ЖК – олеиновую кислоту. • Интенсивный метаболизм АМК Ал. АТ, Ас. АТ. • СР развит хорошо, однако Ca 2+ поступает из внеклеточной среды. 6
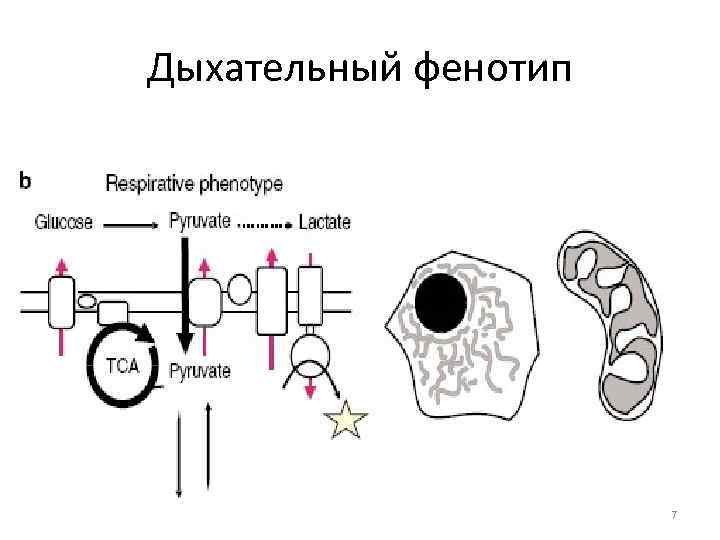
Дыхательный фенотип 7
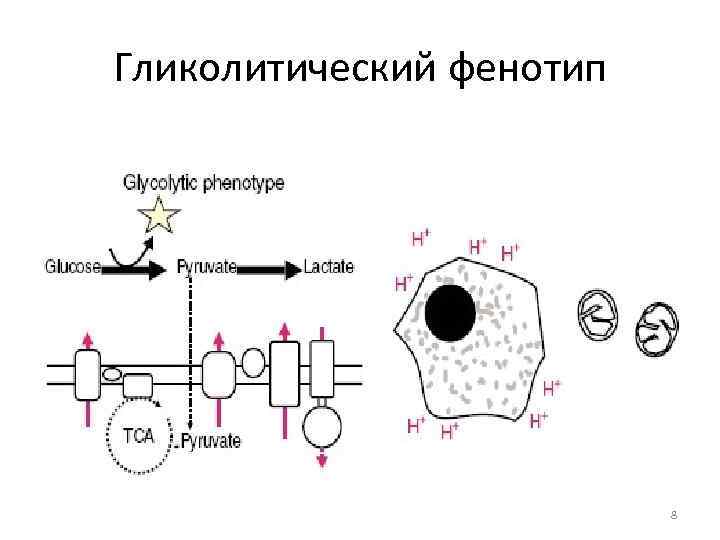
Гликолитический фенотип 8

Двигательная функция • Главная функция мышц. • Мышечное сокращение обеспечивается особыми белками и требует наличия ионов Ca 2+. • Клинические аспекты: – Некоторые мышечные нарушения (миодистрофия Дюшенна, злокачественная гипертермия, кардиомиопатии сердечного клапана) 9

Субстраты метаболизма • Мышечная ткань использует разные субстраты метаболизма: глюкозу, жирные кислоты, кетоновые тела. • Скелетные мышцы различаются по энергозатратам в зависимости от их активности. • В покоящейся мышце главным энергетическим субстратом являются жирные кислоты: – При физической нагрузке главным субстратом становится глюкоза. – Поэтому в мышцах имеется значительный запас гликогена. 10

Субстраты метаболизма: Гликоген мышечной ткани • В скелетных мышцах хранится около ¾ всего гликогена организма. • В печени – большая часть из оставшейся ¼. – Глюкоза не может выйти из мышц, так как в мышцах отсутствует фермент Г 6 Ф-аза. 11

Субстраты метаболизма: лактат, аланин, циклы Кори и Фелига • При физической нагрузке скорость анаэробного гликолиза в мышце выше, чем ЦТК лактат накапливается и выходит из клеток. • Другой продукт метаболизма –Ала образуется при переаминировании ПВК. • Лактат и Ала транспортируются с кровотоком в печень, где снова превращаются в глюкозу (ГНГ). – Глюкозо-лактатный цикл (Кори). – Глюкозо-аланиновый цикл (Фелига). 12

Субстраты метаболизма: Белки – Мышечные белки также могут использоваться для энергообеспечения. – Однако этот процесс энергетически невыгоден и вреден – снижает шансы на выживаемость организма. • Поэтому катаболизм мышечных белков в нормальном состоянии минимален, увеличивается лишь в крайнем случае (напр. при голодании). 13
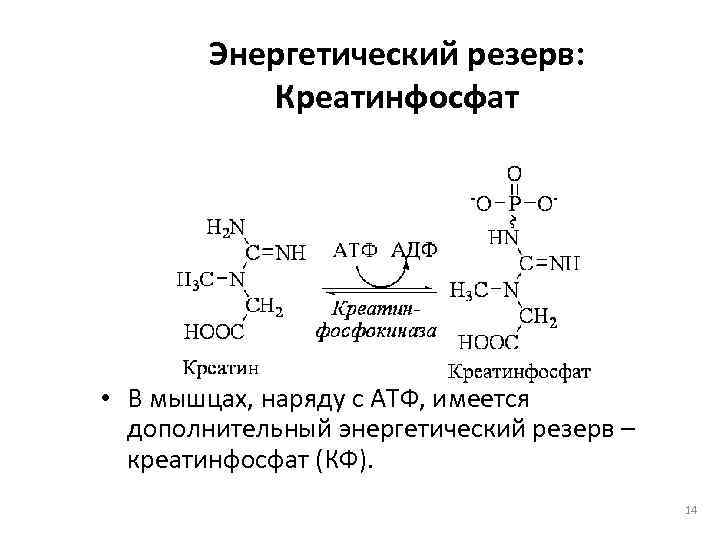
Энергетический резерв: Креатинфосфат • В мышцах, наряду с АТФ, имеется дополнительный энергетический резерв – креатинфосфат (КФ). 14

Энергетический резерв: Креатинфосфат • Содержание КФ может в 5 -7 раз превышать концентрацию АТФ. • Высокая концентрация в клетке АТФ невозможна – тормозятся основные пути энергетического метаболизма. • КФ быстро расходуется в начальном периоде физической нагрузки, поэтому, как и запасы гликогена, должен восполняться в периоде покоя. 15
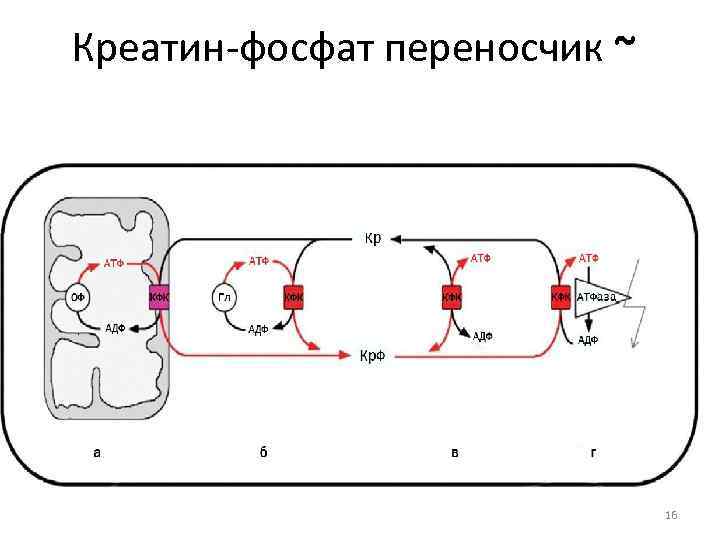
Креатин-фосфат переносчик ~ 16

Энергетический метаболизм мышц • При интенсивной мышечной работе: АТФ 4 - → АДФ 3 - + Фн 2 - + H+ – актомиозин проявляет свойства АТФ-азы; 17
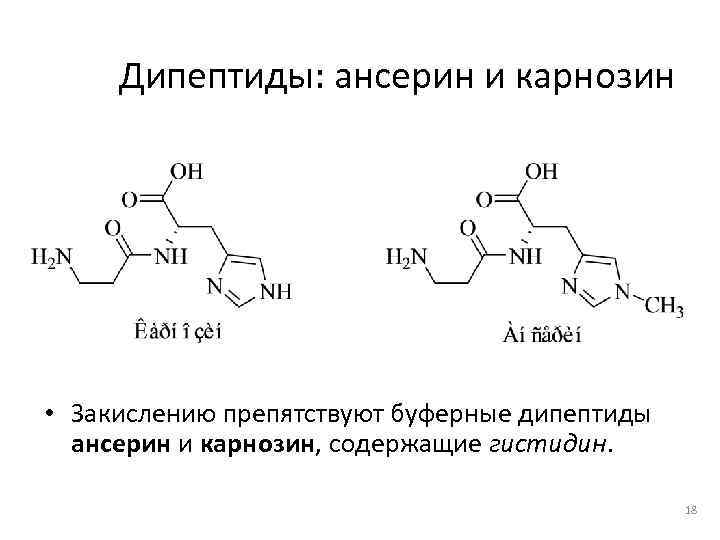
Дипептиды: ансерин и карнозин • Закислению препятствуют буферные дипептиды ансерин и карнозин, содержащие гистидин. 18

Энергетический метаболизм мышц (прод. ) • Скорость гидролиза АТФ превышает скорость его синтеза. • АДФ накапливается, но не используется ни в каких реакциях, кроме аденилаткиназной: – 2 АДФ ↔ АТФ + АМФ (миоаденилаткиназа) • В ходе аденилаткиназной реакции накапливается АМФ. Снижает его концентрацию фермент АМФ- дезаминаза: – АМФ → ИМФ + NH 3 19
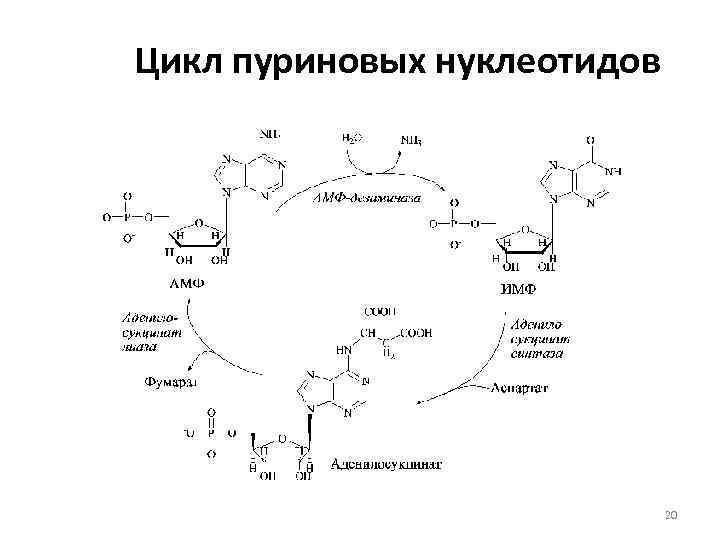
Цикл пуриновых нуклеотидов 20

Пути утилизации АТФ в мышце (АТФ-азная активность ) Механическая работа – АТФ-зависимый процесс • сокращение – миозиновая АТФ-аза ) и • расслабление мышц) – (актомиозиновая АТФ-аза -распад актомиозинового комплекса и ионные АТФ-азы - откачивание Ca 2+ из саркоплазмы) Электрическая работа выполняется АТФ-азами: – Na+/K+-АТФ-аза – способствует поддержанию потенциала покоя; транспорт субстратов. – Ca 2+-АТФ-аза – мышечное сокращение – Mg 2+-АТФ-аза – расслабление и стабилизация [АТФ], и т. д. 21

Электромеханическое сопряжение • Процесс преобразования нервного импульса в мышечное сокращение носит название электромеханическое сопряжение. 22
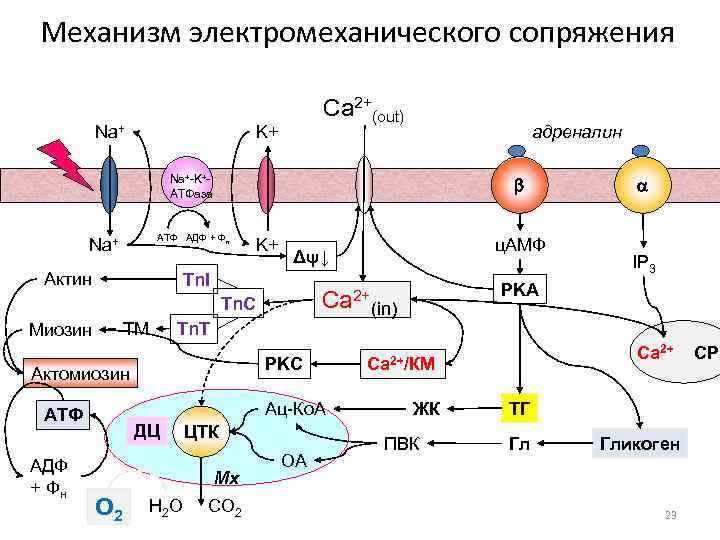
Механизм электромеханического сопряжения Ca 2+(out) Na+ K+ адреналин Na+-K+- АТФаза b a АТФ АДФ + Фн Na+ K+ ц. АМФ Δψ↓ IP 3 Актин Tn. I PKA Tn. C Ca 2+ (in) Миозин TM Tn. T Ca 2+ СР PKC Ca 2+/КМ Актомиозин АТФ Ац-Ко. А ЖК ТГ ДЦ ЦТК ПВК Гликоген АДФ ОА Мх + Фн O 2 H 2 O CO 2 23

Ca 2+ - Фактор электромеханического сопряжения • Ca 2+in – 10 -7 - 10 -8 М. • Ca 2+out – 10 -3 М • Кальций является активатором ряда ферментов: – Дегидрогеназ ЦТК : пируват-ДГ, изоцитрат-ДГ и a-кетоглутарат-ДГ, (малат-ДГ – в нек. тканях); – Триглицеридлипазы. – Кальций-кальмодулинзависимых киназ (характерно для гладкой мускулатуры) • Кальмодулин (КМ) – белок консервативный. Связывает 4 иона кальция. 24

Ригорный комплекс (трупное окоченение) • Ригорный комплекс образуется в результате нарастающего дефицита О 2 АТФ↓ Ca 2+↑ актомиозиновый комплекс не диссоциирует. • Через ≈2 -3 часа ригорный комплекс разрушается (действие лизосомальных протеаз) ткани мышц снова становятся мягкими. 25

Мышечные белки • Мышцы содержат уникальный набор белков, которые можно разделить на следующие группы: • Сократительные: актин и миозин. • Регуляторные: – Основные: Тропомиозин, тропонины (I, C, T) – Минорные: Миомезин; креатинкиназа; M-, C-, F-, H-, I-белки; a-, b-, g-актинины, филамин, паратропомиозин. • Белки цитоскелета: – Тайтин-1, тайтин-2, небулин, винкулин, десмин (скелетин), виментин, синемин, Z-протеин, Z-nin, дистрофин. 26
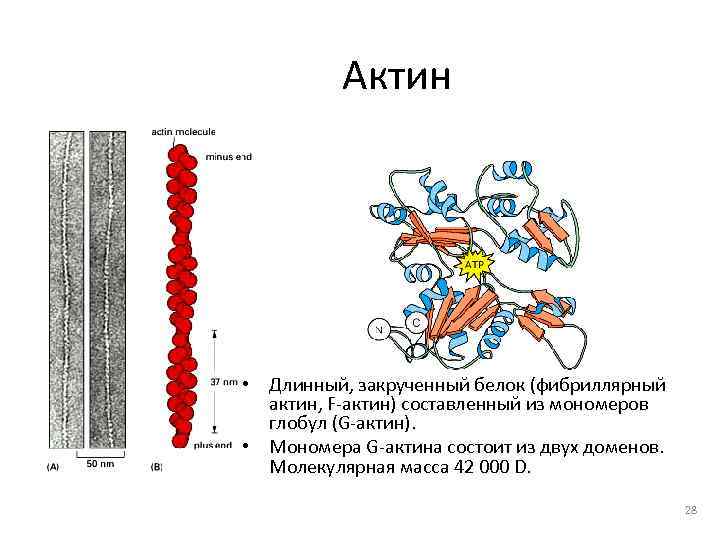
Актин • Длинный, закрученный белок (фибриллярный актин, F-актин) составленный из мономеров глобул (G-актин). • Мономера G-актина состоит из двух доменов. Молекулярная масса 42 000 D. 28

Актин (прод. ) • Связывание АТФ мономером G-актина вызывает полимеризацию (т. е. , формирование F-актина). АДФ, образующийся после гидролиза АТФ, остается связанным с актином. • F-актин образует двойную спираль. • Каждая субъединица актина в тонком филаменте содержит участок, способный связываться с миозином. 29
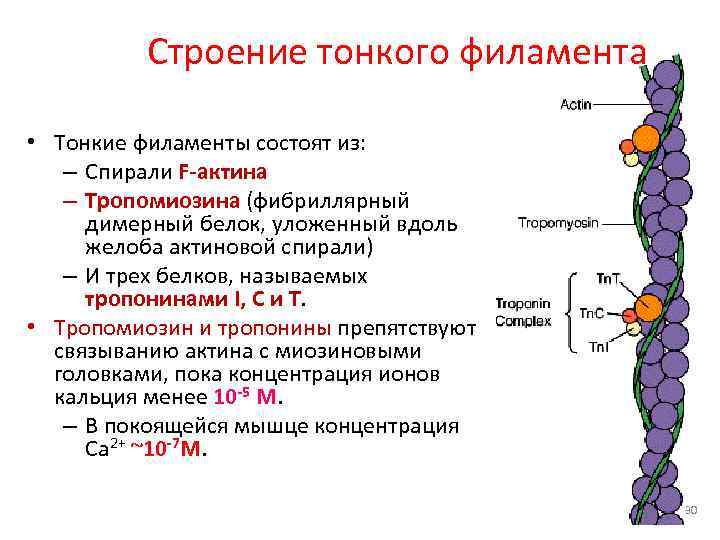
Строение тонкого филамента • Тонкие филаменты состоят из: – Спирали F-актина – Тропомиозина (фибриллярный димерный белок, уложенный вдоль желоба актиновой спирали) – И трех белков, называемых тропонинами I, C и T. • Тропомиозин и тропонины препятствуют связыванию актина с миозиновыми головками, пока концентрация ионов кальция менее 10 -5 М. – В покоящейся мышце концентрация Ca 2+ ~10 -7 M. 30
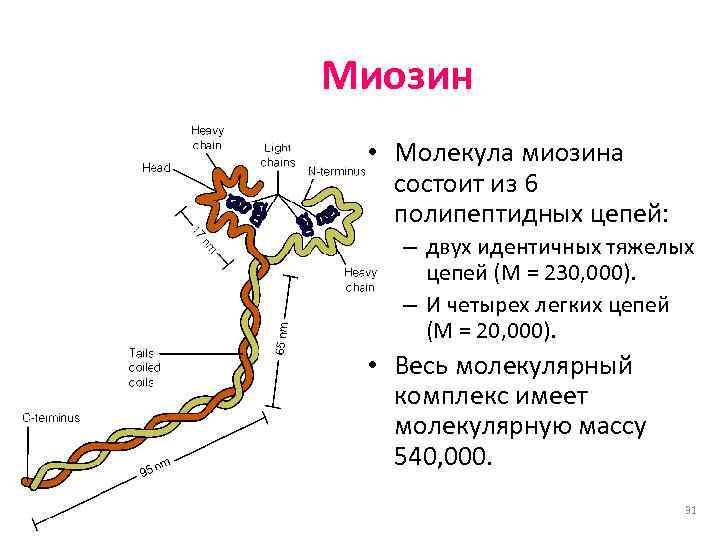
Миозин • Молекула миозина состоит из 6 полипептидных цепей: – двух идентичных тяжелых цепей (M = 230, 000). – И четырех легких цепей (M = 20, 000). • Весь молекулярный комплекс имеет молекулярную массу 540, 000. 31
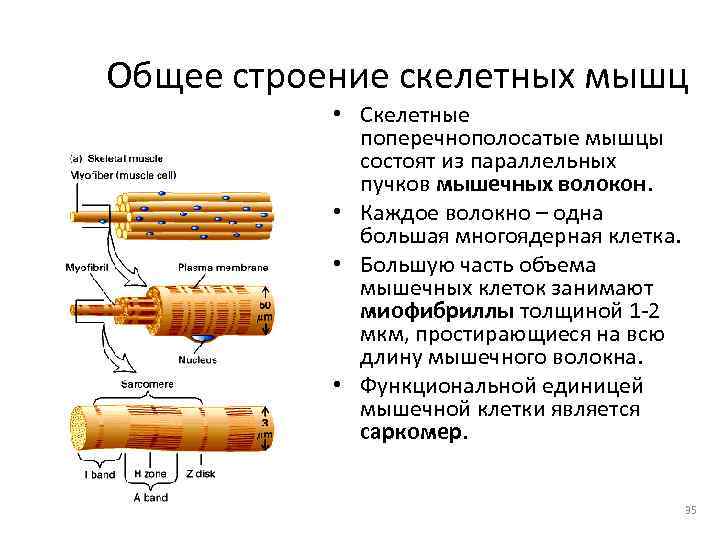
Общее строение скелетных мышц • Скелетные поперечнополосатые мышцы состоят из параллельных пучков мышечных волокон. • Каждое волокно – одна большая многоядерная клетка. • Большую часть объема мышечных клеток занимают миофибриллы толщиной 1 -2 мкм, простирающиеся на всю длину мышечного волокна. • Функциональной единицей мышечной клетки является саркомер. 35

Строение мышечной клетки • Поперечные трубочки (Т- трубочки) – впячивания сарколеммы в мышечное волокно, располагаются в Z- линиях, контактируют с цистернами саркоплазматического ретикулума, образуя триады. 37
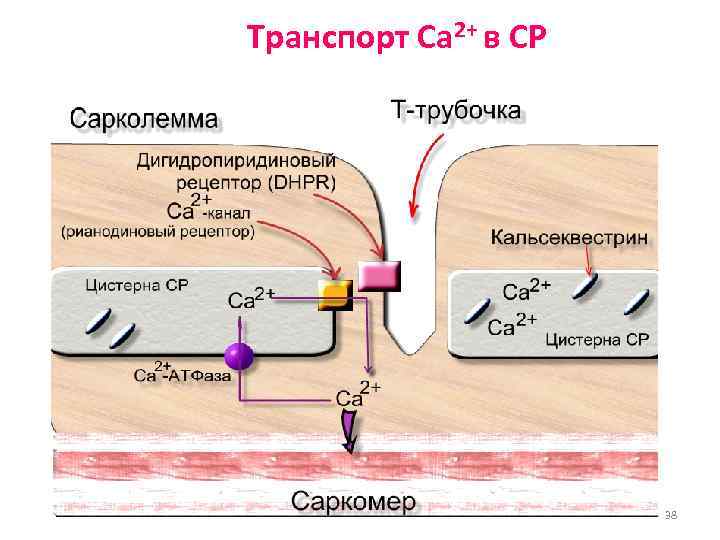
Транспорт Ca 2+ в СР 38

Потенциал-зависимые Ca 2+ каналы (дигидропиридиновые рецепторы, DHPR) • Олигомеры – 2 большие субъединицы (a-1 и a-2) и 3 малые (b, g, и d) • Выполняют ключевую роль в электромеханическом сопряжении. • Чувствительны к блокаторам кальциевых каналов (1, 4 -дигидропиридины - нифедипин). 40
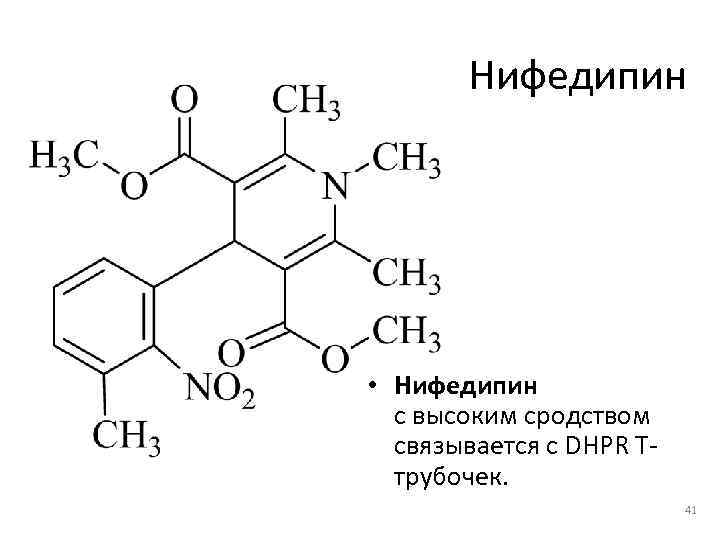
Нифедипин • Нифедипин с высоким сродством связывается с DHPR T- трубочек. 41

Патологии DHPR • Гипокалиемический периодический паралич; • Предрасположенность к тиротоксическому периодическому параличу; • Предрасположенность к злокачественной гипертермии. 42

Ca 2+ каналы – рианодиновые рецепторы • Ca 2+- каналы СР – рианодиновые рецепторы (RYR) – главный источник Са 2+ для мышечного сокращения. • Известны их 3 изоформы : RYR 1, RYR 2 and RYR 3. – RYR 1 – в скелетной мускулатуре, – RYR 2 – в миокарде, – RYR 3 – в головном мозге. 43
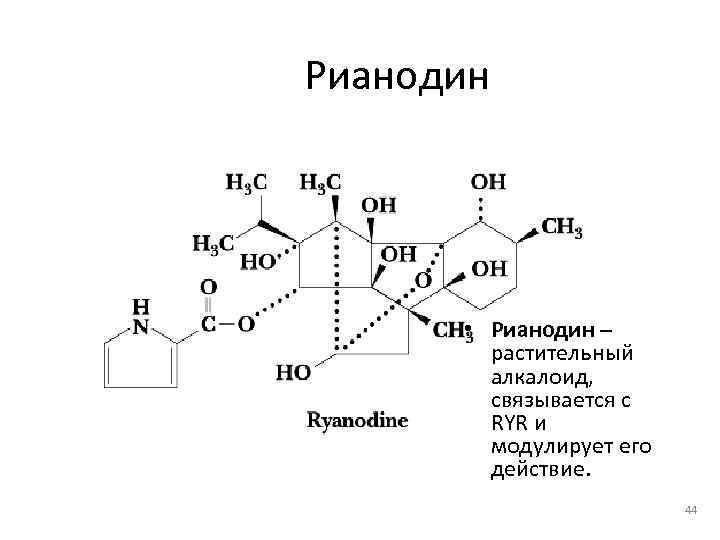
Рианодин • Рианодин – растительный алкалоид, связывается с RYR и модулирует его действие. 44
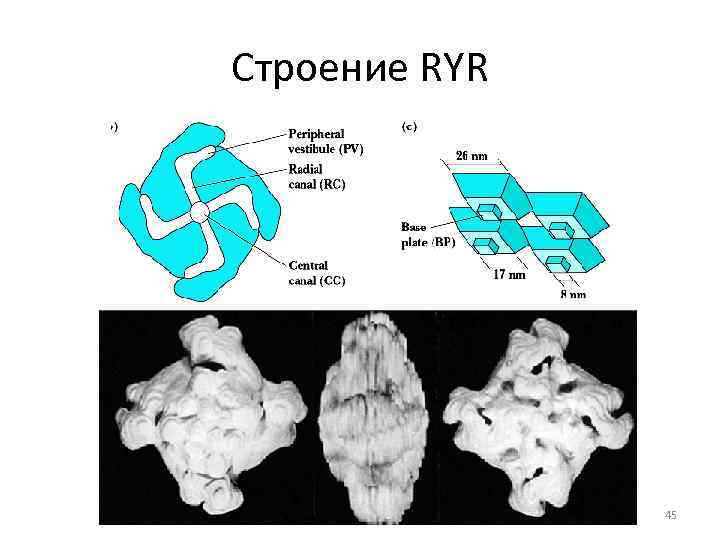
Строение RYR 45

Патология RYR • RYR 1: – Предрасположенность к злокачественной гипертермии; – Миопатии с внешней офтальмоплегией. • RYR 2: – Желудочковая тахикардия, полиморфная стресс- индуцированная тахикардия; – Семейная аритмогенная правожелудочковая дисплазия. – При сердечной недостаточности RYR 2 гиперфосфорилирован под действием протеинкиназы А, что нарушает функцию канала и повышенной чувствительности к активации Са 2+. 46

Болезнь центрального стержня (central core disease) • Непрогрессирующие миопатии - группа заболеваний, со своеобразными изменениями строения миоцита, или специфическими б/х нарушениями. Начало на 1 -3 -м году жизни, имеют сравнительно благоприятное течение. • Болезнь центрального стержня (central core disease) характеризуется резким снижением или полным отсутствием ферментативной активности в центральной части мышечного волокна, что выявляется при окраске препарата мышечной ткани (Cr 3+) по Гомори. • Клиника : снижение мышечного тонуса, дряблость мышц, задержке развития двигательных функций. В позднем возрасте имеется умеренная слабость проксимальных отделов и гипотрофия мышц. На ЭМГ - уменьшение длительности колебаний потенциала и увеличение полифазных потенциалов. Передача по доминантному типу с неполной пенетрант. Са 2+ностью. Часты спорадические случаи. • Диагноз мб поставлен после биопсии мышц, иногда только после электронно-микроскопического исследования 49

Кальсеквестрин (CASQ) • Кальсеквестрин (CASQ) – кислый гликопротеин, находящийся в просвете терминальных цистерн СР • связывает ионы Са 2+ и выполняет запасающую функцию. • 2 изоформы: – CASQ 1 - в скелетных мышцах, – CASQ 2 - в сердечной мышце. 52

Патологии кальсеквестрина • Миссенс-мутация в гене CASQ 2 – причина аутосомального рецессивного заболевания у бедуинов Израиля катехоламин-индуцируемая полиморфная желудочковая тахикардия. 53

Кальмитин • Кальмитин – митохондриальный кальций- связывающий белок, специфичный для быстрых белых мышц. – Отсутствует у пациентов с миодистрофиями Дюшенна и Беккера. 54

Остальные белки мышц • Основные белки мышц: – Миозин и актин – 65% – Тропомиозин и тропонины – 5%. – Остальные белки -25% (выполняют важные функции в поддержании мышечной структуры и регуляции мышечного сокращения). • Регуляторные белки разделяются на: – Связанные с миозином; – Связанные с актином. 55

Белки, связанные с миозином • 3 основных белка, находящихся в области М-дисков. – Белок M (165 k. D), – Миомезин (185 k. D), – Креатин киназа (димер, субъединица 42 -k. D). • Поддерживают структурную целостность миозиновых филаментов. 56

Остальные белки, связанные с миозином • Белок C (135 k. D), – Ингибирует активность мышечной АТФазы при низкой ионной силе, и активирует при физиологических значениях. • Белок F (121 k. D), • Белок H (74 k. D), • Белок I (50 k. D). – Роль белков F, H и I пока неясна. 57

Белки, связанные с актином • Кроме тропомиозина и тропонинов с актином также связаны – a–актинин (гомодимер, субъединица 95 -k. D), • Обнаружен в области Z линий, активирует сокращение актомиозина. Предположительно, участвует в прикреплении актина к Z линиям. – b-актинин (гетеродимер, субъединицы по 37 -k. D и 34 - k. D), – g-актинин (мономер, 35 -k. D), – паратропомиозин (гомодимер, 34 -k. D). 58
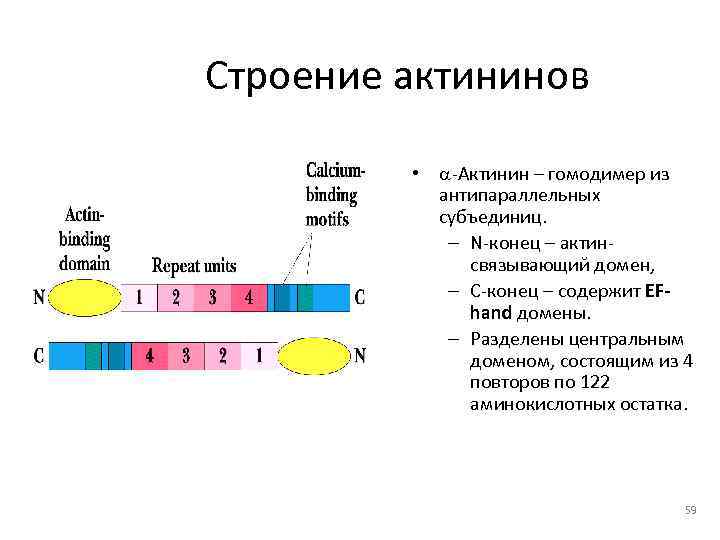
Строение актининов • a-Актинин – гомодимер из антипараллельных субъединиц. – N-конец – актин- связывающий домен, – C-конец – содержит EF- hand домены. – Разделены центральным доменом, состоящим из 4 повторов по 122 аминокислотных остатка. 59

Роль актининов и паратропомиозина • Повторы в a–актинине гомологичны 106 - аминокислотным повторам в спектрине – главном структурном белке цитоскелета эритроцитов. • b-Актинин специфически связывается с концами актиновых нитей. • g-Актинин ингибирует полимеризацию актина. • Паратромомиозин похож на тропомиозин, расположен на стыке зон A и I. 60
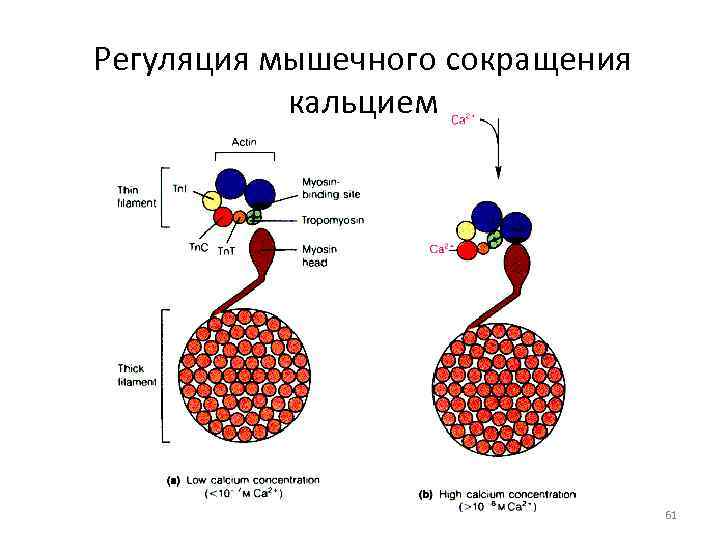
Регуляция мышечного сокращения кальцием 61

Динамика тайтина – Большие филаменты тайтина и небулина остаются связанными с толстыми и тонкими филаментами при мышечном сокращении. 62
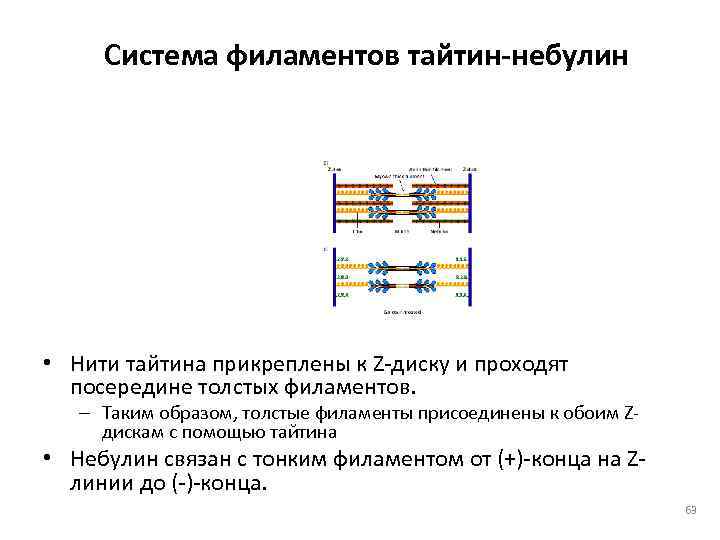
Система филаментов тайтин-небулин • Нити тайтина прикреплены к Z-диску и проходят посередине толстых филаментов. – Таким образом, толстые филаменты присоединены к обоим Z- дискам с помощью тайтина • Небулин связан с тонким филаментом от (+)-конца на Z- линии до (-)-конца. 63
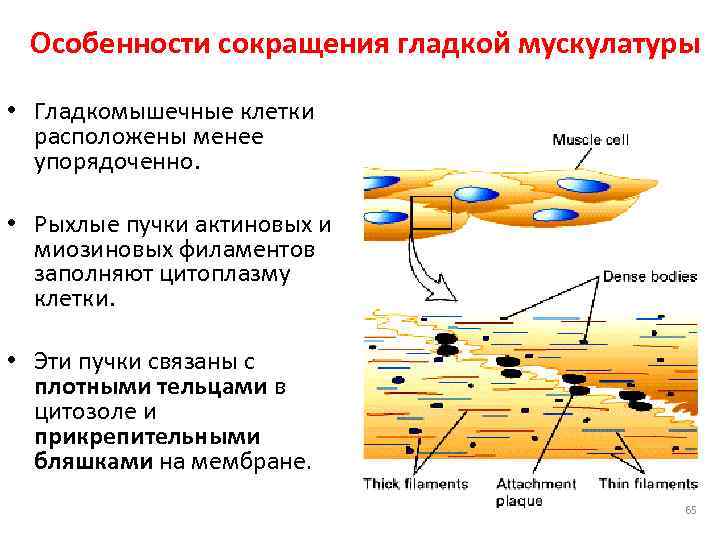
Особенности сокращения гладкой мускулатуры • Гладкомышечные клетки расположены менее упорядоченно. • Рыхлые пучки актиновых и миозиновых филаментов заполняют цитоплазму клетки. • Эти пучки связаны с плотными тельцами в цитозоле и прикрепительными бляшками на мембране. 65

Сокращение гладких мышц • Пусковой механизм в сокращении гладких мышц – повышение [Ca 2+] в клетке. • Ca 2+ связывается с кальмодулином, активирует киназу легких цепей миозина. • Фосфорилирование легких цепей миозина вызывает сокращение. • Процесс сокращения в гладких мышцах происходит значительно медленнее. 66

Биохимические основы развития сердечной недостаточности (СН) • Нарушение энергетического метаболизма. – Дефицит O 2 (ишемия, гипоксия, аноксия) – Несоответствие нагрузки функциональной воможности миокарда – Дефицит субстратов (Гл, ЖК, КТ, лактат, ПВК и др. ) • В саркоплазме накапливается Ca 2+ • Мх аккумулируют значительную часть Ca 2+ • Разобщение дыхания и фосфорилирования. 67
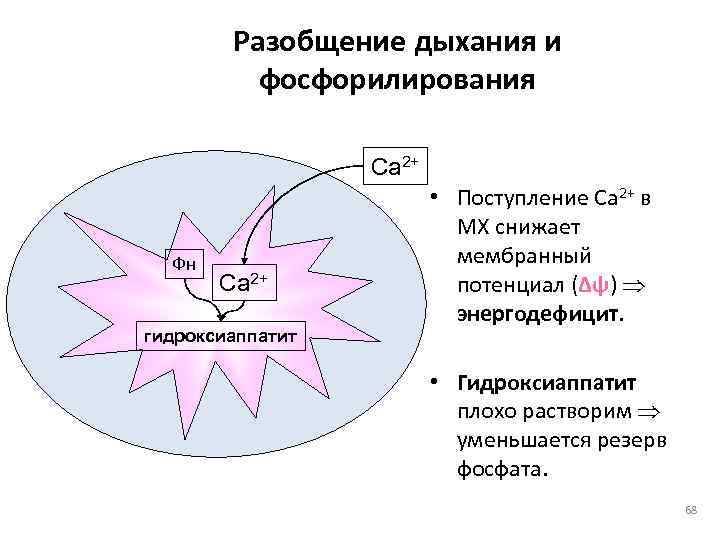
Разобщение дыхания и фосфорилирования Ca 2+ • Поступление Ca 2+ в МХ снижает Фн мембранный Ca 2+ потенциал (Δψ) энергодефицит. гидроксиаппатит • Гидроксиаппатит плохо растворим уменьшается резерв фосфата. 68
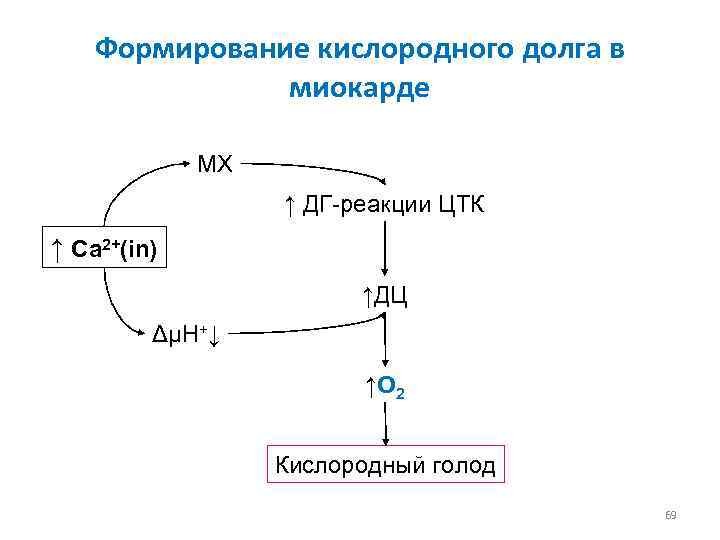
Формирование кислородного долга в миокарде МХ ↑ ДГ-реакции ЦТК ↑ Ca 2+(in) ↑ДЦ ΔμH+↓ ↑О 2 Кислородный голод 69
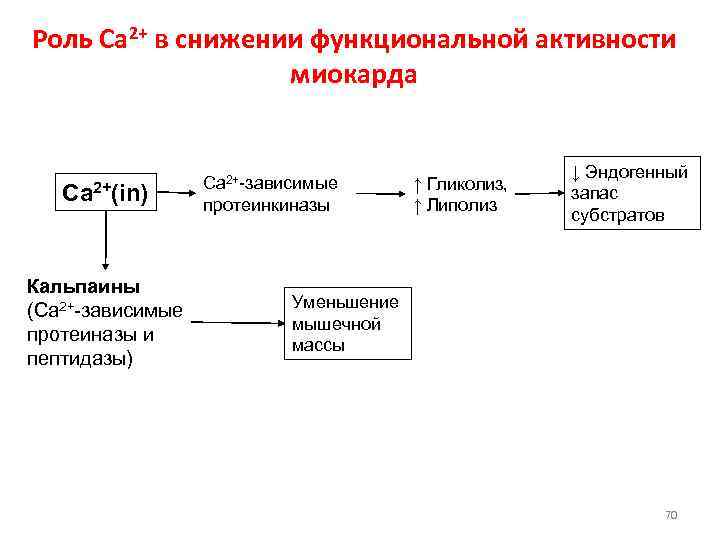
Роль Ca 2+ в снижении функциональной активности миокарда ↓ Эндогенный Ca 2+-зависимые ↑ Гликолиз, Ca 2+(in) протеинкиназы ↑ Липолиз запас субстратов Кальпаины (Ca 2+-зависимые Уменьшение мышечной протеиназы и массы пептидазы) 70

Последовательность развития СН • При сердечной недостаточности (СН): – Слабая мышечная стенка растягивается (дилатация). – Повышается синтез коллагена рубцевание миокарда препятствует дилатации снижается эластичность. – Ca 2+ ↑ анаэробный гликолиз ↑образование волокон белого типа гипертрофия миокарда усиление биосинтеза мышечных белков. – Ca 2+ активирует процессы перекисного окисления (↑ NADH). 71

Биохимические основы коррекции СН (1) 1. Аэрация миокарда 1. Нормализация кровообращения 2. Нормализация ионного и энергетического баланса 2. Препараты K+ (печеный картофель, изюм, урюк и т. п. ) 3. Инъекции препаратов глюкозы, инсулина и K+ 3. Сердечные гликозиды (СГ) (наперстянки, ландыша, строфанта Комбе) – дигитоксин, дигонин, конваллятоксин, строфантин K, коргликон (смесь разных СГ). 4. Высокоспецифичные ингибиторы Na+/K+-АТФазы. 4. Применение ингибиторов кальциевых каналов и антагонистов Ca 2+ - способствует снижению [Са 2+]in. 72

Биохимические основы коррекции СН (2) • Препараты, увеличивающие уровень АТФ в миокарде – Рибоксин (инозин) – Аспаркам, панангин (глу, асп, K+, Mg 2+) • Инозин → ИМФ (+асп) → Аденилосукцинат → АМФ → АДФ → АТФ – L-Карнитин (Элькар®) • Осуществляет транспорт ЖК в МХ. • Антиоксиданты (компл. вит. C, A, E) • Бетаин – аналог SAM – Синтез холина в печени – нормализация липопротеидного обмена. – Синтез креатина – оптимизация энергообеспечения. 73
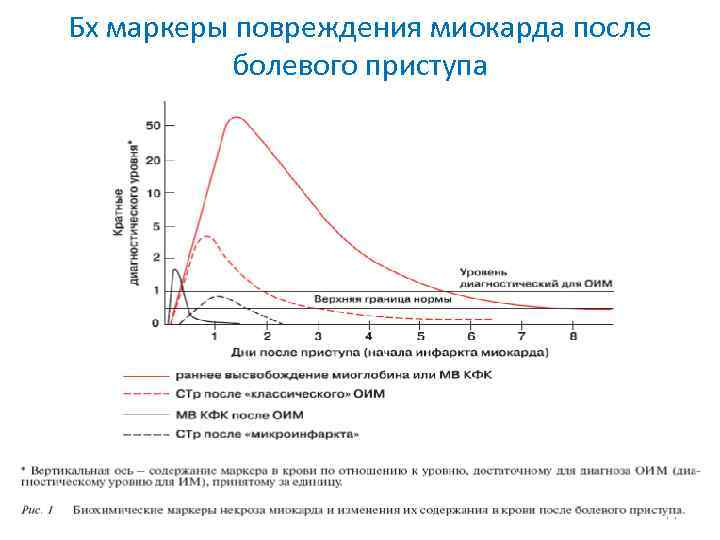
Бх маркеры повреждения миокарда после болевого приступа 74

Воздействие радионуклидов на энергетический метаболизм мышечной ткани (1) • Основной дозообразующий радионуклид нашего региона 137 Cs (IА группа табл. Менделеева) – аналог/антагонист К+ • Инкорпорированный 137 Cs транспортируется по К+ каналам поступает в кардиомиоцит, в Мх стимулирует образование АФК и АФА • Инкорпорация 137 Cs (b-излучатель) ↑ АФК и АФА. • Продолжительно высокий уровень выработки АФК и АФА – угроза окружающим клеткам • Клетки с инкорпорированным радионуклидом воспринимаются как несостоятельные и погибают путем апоптоза. • Апоптоз – элиминация несостоятельных клеток. 75

Воздействие 137 Cs на энергетический метаболизм мышечной ткани (2) • Создаются предпосылки для развития мышечных патологий. • В этих условиях реализуются механизмы неспецифической системы защиты от гипоксических состояний. – При гипоксии ↑ NADH – Клетка продуцирует активные формы кислорода (АФК) и азота (АФА) – сигналы о гипоксии. – Миоциты сосудов при этом расслабляются, сосуды расширяются проблема оксигенации решается 76
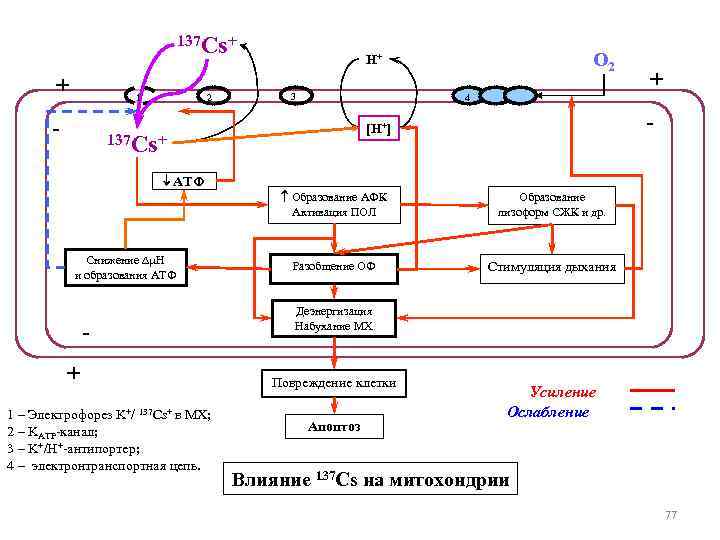
137 Cs+ H+ O 2 + 1 2 3 4 - [H+] - 137 Cs+ АТФ Образование АФК Образование Активация ПОЛ лизоформ СЖК и др. Снижение H Разобщение ОФ Стимуляция дыхания и образования АТФ Деэнергизация - Набухание МХ + Повреждение клетки Усиление 1 – Электрофорез K+/ 137 Cs+ в МХ; Ослабление 2 – KATP-канал; Апоптоз 3 – K+/H+-антипортер; 4 – электронтранспортная цепь. Влияние 137 Cs на митохондрии 77

78
Бх миокарда 12.12.13..ppt
- Количество слайдов: 66

