БИОХИМИЯ МЕЖКЛЕТОЧНОГО МАТРИКСА.ppt
- Количество слайдов: 55

БИОХИМИЯ МЕЖКЛЕТОЧНОГО МАТРИКСА Артюхина А. И. Вол. ГМУ

План n n n Функции межклеточного матрикса Компоненты и организация межклеточного матрикса Коллаген и эластин: АК состав, структурная организация, посттрансляционная модификация Фибриллогенез Адгезивные белки Интегриновый рецептор Протеогликаны Гликозаминогликаны Мукополисахаридозы Биохимия соединительной ткани Биохимические изменения при старении Изменения в процессе заживления ран Роль витамина С, Д, паратгормона Заболевания связанные с нарушением синтеза и созревания коллагена

Межклеточный матрикс супрамолекулярный комплекс, образованный сложной сетью связанных между собой макромолекул в интерстициальном внутритканевом пространстве В ряде тканей (мышцы, печень) заполняет только тонкие промежутки между клетками, n в других (соединительная, хрящевая, костная ткани) на межклеточный матрикс приходится большой объём и именно он выполняет основные функции n
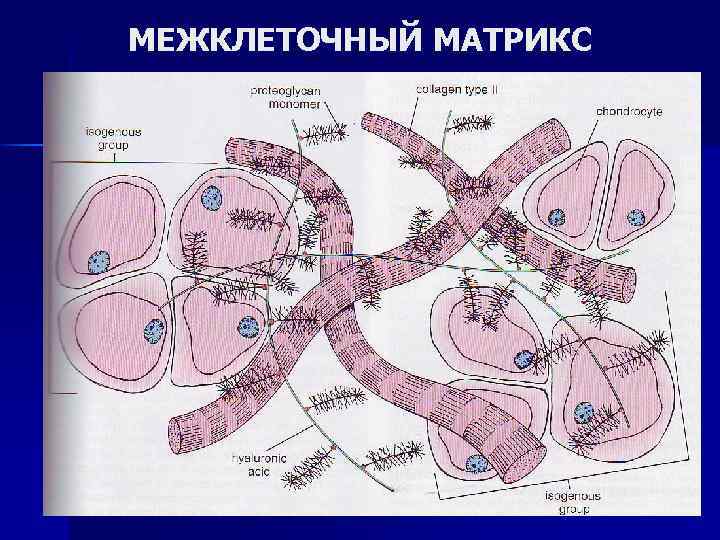
МЕЖКЛЕТОЧНЫЙ МАТРИКС

Функции межклеточного матрикса n n n n окружает клетки и влияет на их развитие, пролиферацию, организацию и метаболизм, служит для клеток механической опорой обеспечивает механические контакты между клетками образует механически прочные высокоспециализированные структуры (суставы, сухожилия, кости, хрящ) составляет основу фильтрующих мембран (почки), изолирует клетки и ткани друг от друга формирует пути миграции клеток, вдоль которых они могут перемещаться, например при эмбриональном развитии.

n n n Матрикс чрезвычайно вариабелен по химическому составу и функциям. Главные компоненты межклеточного матрикса: коллагены, эластин, адгезивные белки (фибронектин и ламинин) и основное вещество (протеогликаны). Белки образуют специализированные структуры внеклеточного матрикса: базальные мембраны, а также разного рода волокна (коллагеновые, эластиновые или фибронектиновые). Волокна погружены в гель, образуемый переплетёнными цепями гликозаминогликанов и обеспечивающий упругость внеклеточного матрикса

КОЛЛАГЕН ЭЛАСТИН Фибриллярные белки, синтез на полисомах фибробластов n Функция: опорная, обеспечивает прочность на разрыв АК состав 30% гли 20% про, оксипро 10% ала, 1%оксилиз 40% остальные АК n высокая растяжимость и быстрое восстановление исходной формы и размера после снятия нагрузки 30% гли 21% ала ( много гидрофобных АК) вал, лей, лиз 13, 10 % 1% оксипро n
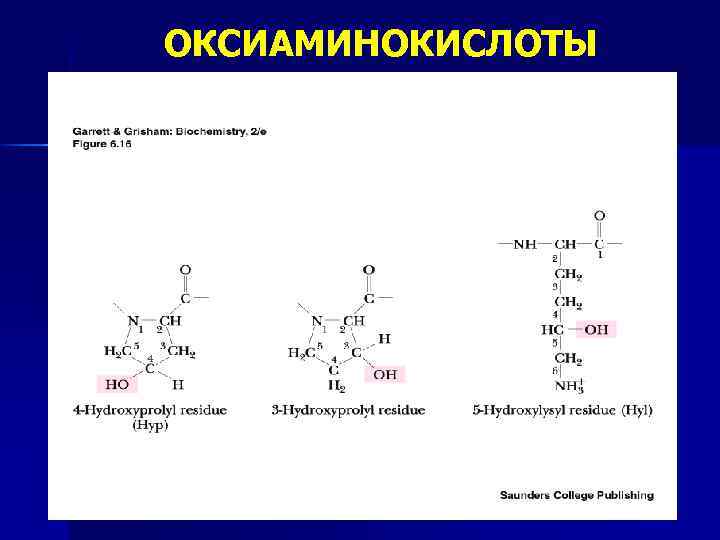
ОКСИАМИНОКИСЛОТЫ

СТРУКТУРНАЯ ОРГАНИЗАЦИЯ коллаген эластин n n n I структура 19 типов коллагенов : три п/п цепи длиной по 1 тысяче АК, одинаковые, или одна отличная, две – одинаковые; -гли-Х-УII структура: ни α -спираль, ни β-слой – так как много про, левая спираль (3 АК на виток), в образовании водородных связей участвует –ОН гр оксипро. III структура: тройная правая суперспираль - тропоколлаген Пептидные цепи не имеют характерной III структуры, Сохраняют гибкую случайную конформацию
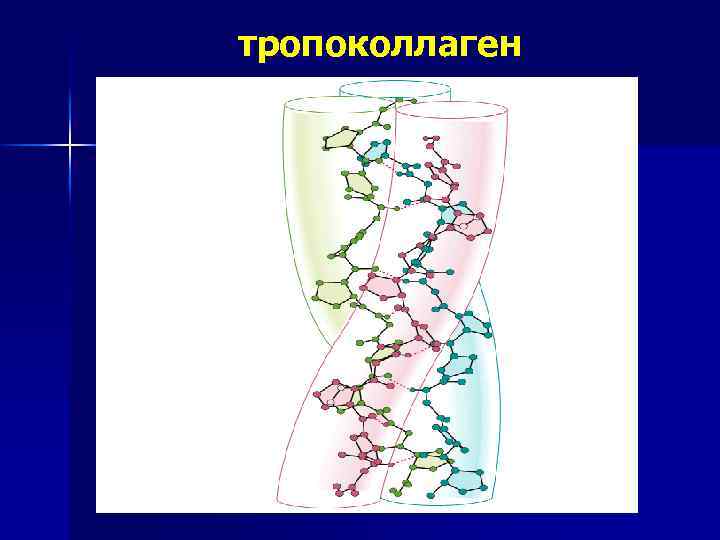
тропоколлаген
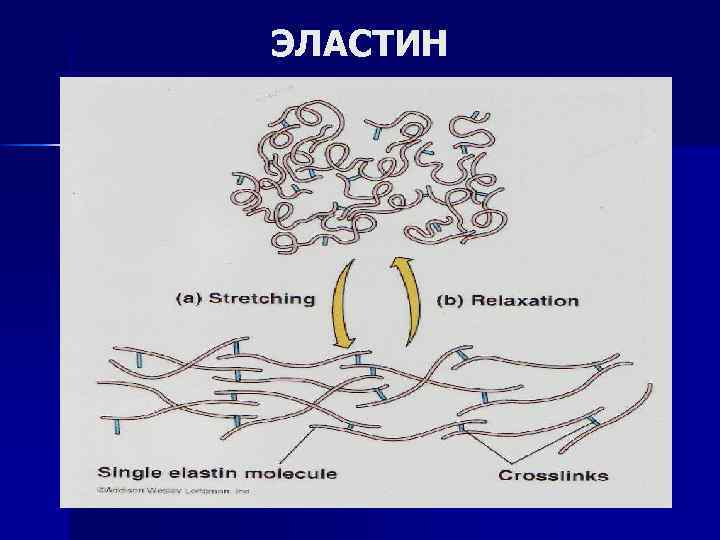
ЭЛАСТИН

Синтез и созревание: сложный многоэтапный процесс, начинается в клетке, заканчивается во внеклеточном пространстве. коллаген эластин Посттрансляционная модификация –в ЭР, протеолиз n гидроксилирование про, лиз n гидроксилирование про (про- и лиз-гидроксилазы, вит. С, αКГК, О 2, Fe 2+ ), n Гликозилирование n гликозилирование: –ОН гр n проэластин растворим, не лиз + глю-гал содержит поперечных (гликозилтрансфераза) связей n проколлаген –выход из фибробластов: протеолиз N и Сконцевых пептидов пептидазами n Биосинтез нарушается при недостатке Cu, ↓ активности тропоколлаген -окисление NН 2 лизиламинооксидазы (или гр лиз до альдегидных --» её генетически аллизин (лизиламиноксидаза обусловленной недостаточности). Сu 2+ зависимая)
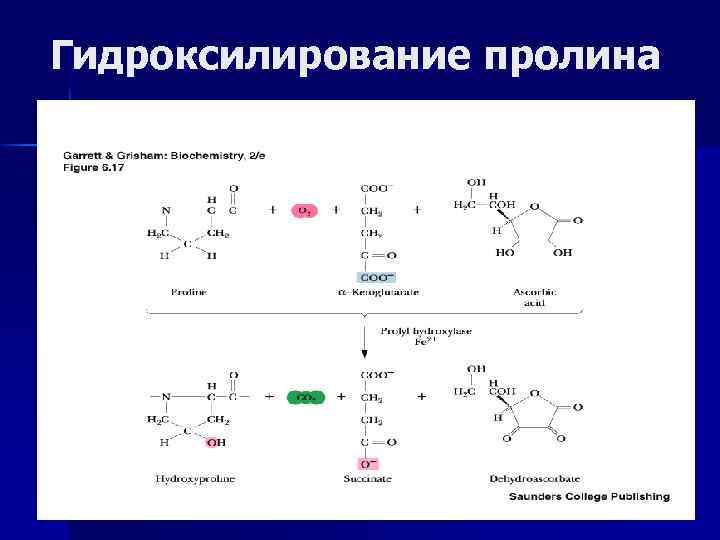
Гидроксилирование пролина
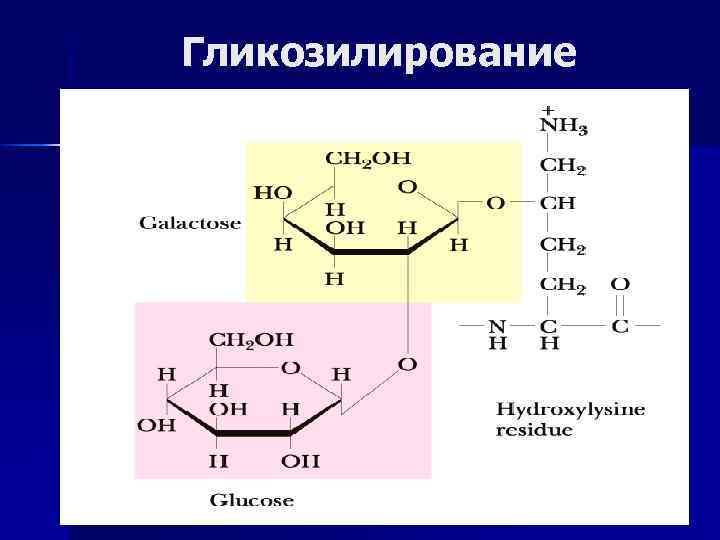
Гликозилирование
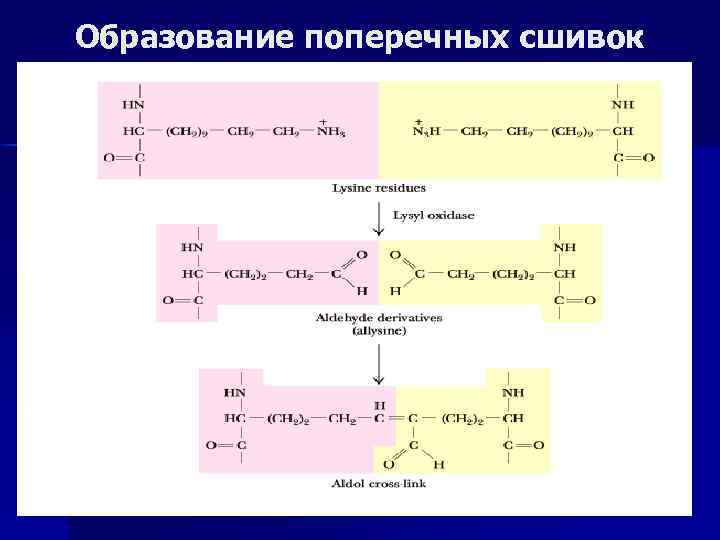
Образование поперечных сшивок

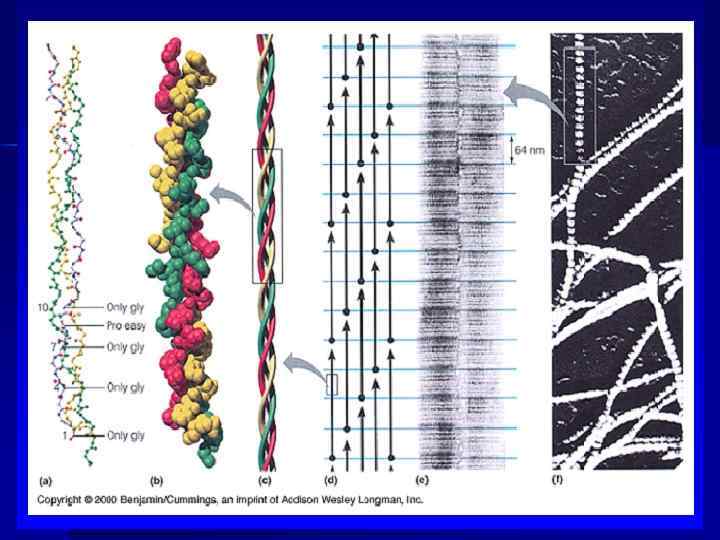
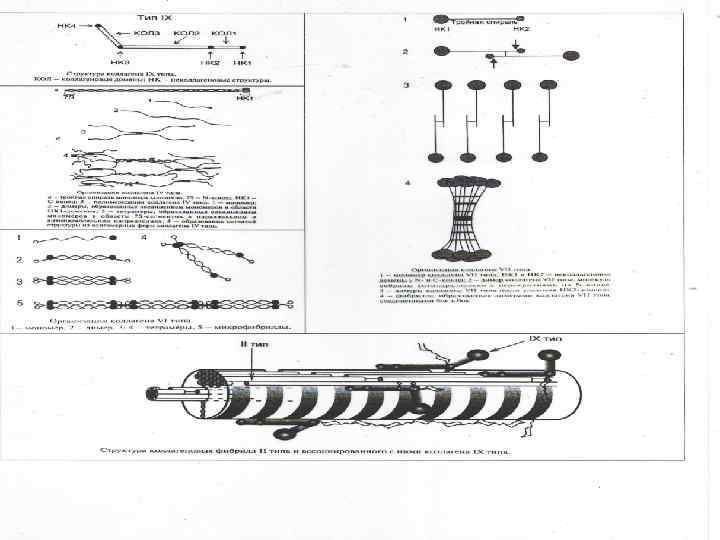
коллаген ФИБРИЛЛОГЕНЕЗ Коллагеновое волокно 1 мм выдерживает нагрузку до 10 кг n Фибриллообразующие (I, III, Y, XI типы) В присутствии вит РР и В 6 – поперечные сшивки, параллельные ряды сдвинуты на 1/4 n Ассоциированные с фибриллами (IX, XII, XIY, XVI типы)-связаны с фибриллами коллагенов других типов. Коллаген IX-три коллагеновых и 4 неколлагеновых домена n IV тип базальных мембран, короткие неспиральные сегменгты, не отщепляются C и N-концы сетчатая структура Микрофибриллярный тип (VI): антипараллельный димер –тетрамер- секреция из клетки конец в конец микрофибриллы (между I, III) n «Заякоренные» фибриллы (VII тип) образуются димерами коллагена, бок в бок присоединение эпидермиса к дерме эластин Молекулы эластина образуют сети n Отдельные молекулы связаны множеством сшивок за счёт: десмозина, изодесмозина, лизиннорлейцина n Десмозин образован 3 молекулами аллизина и 1 молекулой Лиз n
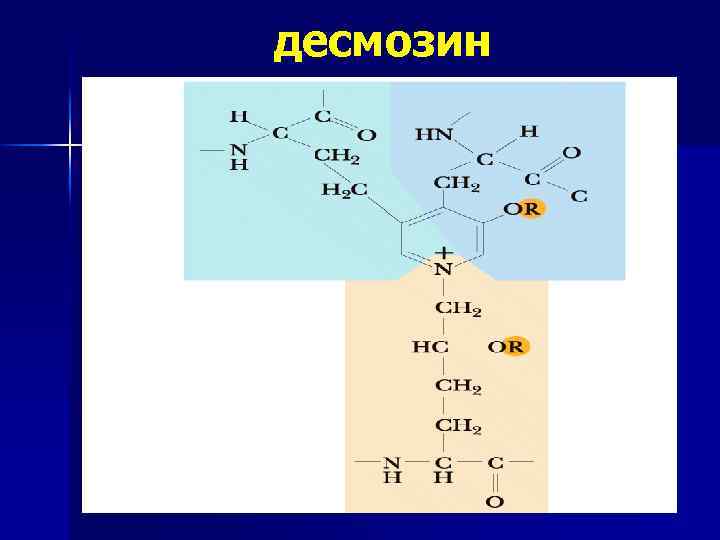
десмозин
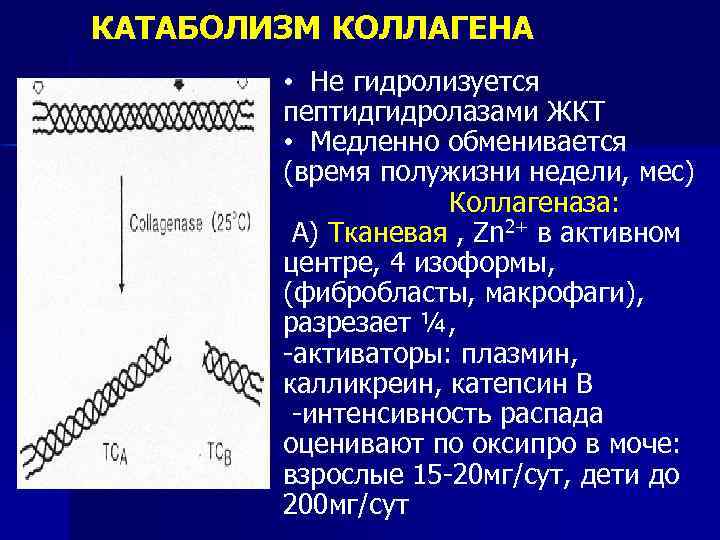
КАТАБОЛИЗМ КОЛЛАГЕНА • Не гидролизуется пептидгидролазами ЖКТ • Медленно обменивается (время полужизни недели, мес) Коллагеназа: А) Тканевая , Zn 2+ в активном центре, 4 изоформы, (фибробласты, макрофаги), разрезает ¼, -активаторы: плазмин, калликреин, катепсин В -интенсивность распада оценивают по оксипро в моче: взрослые 15 -20 мг/сут, дети до 200 мг/сут

НАРУШЕНИЕ КАТАБОЛИЗМА КОЛЛАГЕНА n n Усиление распада при аутоиммунных (ревматоидный артрит, СКВ) Коллагенозы сопровождаются увеличением биосинтеза коллагена фиброз внутренних органов (печени, легких), связок, кожи. Одновременно усилен распад коллагена (в моче увеличен оксипро). Б) Бактериальная коллагеназа из Clostridium histolyticum (газовая гангрена) расщепляет в 200 местах; выделяет, а сам микроорганизм не содержит фермента.

КАТАБОЛИЗМ ЭЛАСТИНА • Эластаза панкреатического сока • Эластаза из нейтрофилов В легких 1 антитрипсин синтезируется альвеолярными макрофагами как защита от эластазы. При дефиците 1 антитрипсина - риск развития эмфиземы, т. к. эластаза разрушает альвеолярную клетку

Регуляция обмена коллагена n n По принципу отрицательной обратной связи коллаген и N пептид тормозят трансляцию. Витамин С стимулирует пролиферацию фибробластов, синтез коллагена, протеогликанов. Глюкокортикоиды (кортизон, кортизол) ингибируют рост, деление фибробластов, транскрипцию проколлагена, активность гидроксилаз про и лиз, фибронектина, протеогликанов Половые гормоны ( в фибробластах есть рецепторы): регулируют обмен коллагена в матке. Синтез коллагена в коже под контролем эстрогенов.

Адгезивные белки - полифункциональные, связывают различные составные компоненты межклеточного матрикса n n n Адгезивные белки обеспечивают фиксацию клеток в межклеточном матриксе за счет взаимодействия с мембранными рецепторами- интегринами. Интегрин состоит из α- (1000 АК, 14 субъединиц, могут связываться более чем с одной цепью) и - (750 АК - 9 разновидностей субъединиц), которые могут связываться нековалентно в различных сочетаниях, формируя более 20 разных типов интегринов. Интегриновый рецептор – трансмембранный белок, имеет вне и внутриклеточные домены. Внутриклеточный домен интегрина через цепь различных соединенных между собой белков (талин, винкулин и др. ) связывается с актиновыми микрофиламентами цитоскелета, осуществляя структурную и функциональную связь между матриксом и цитоскелетом прикрепившейся клетки.
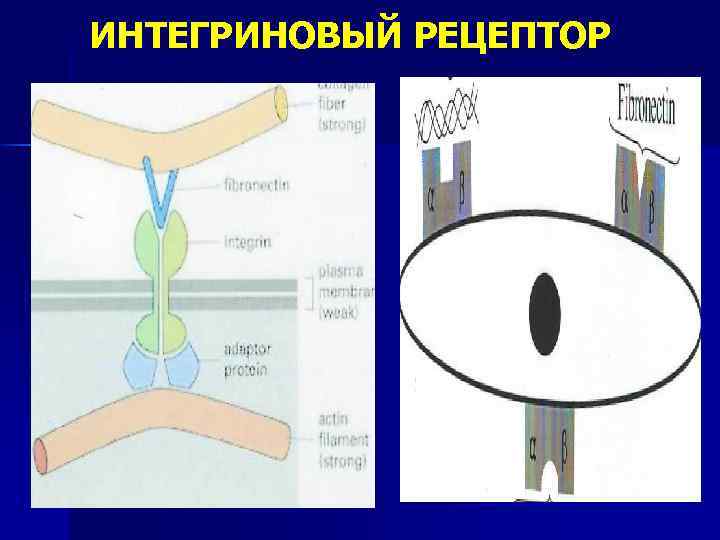
ИНТЕГРИНОВЫЙ РЕЦЕПТОР

МЕЖКЛЕТОЧНЫЙ МАТРИКС
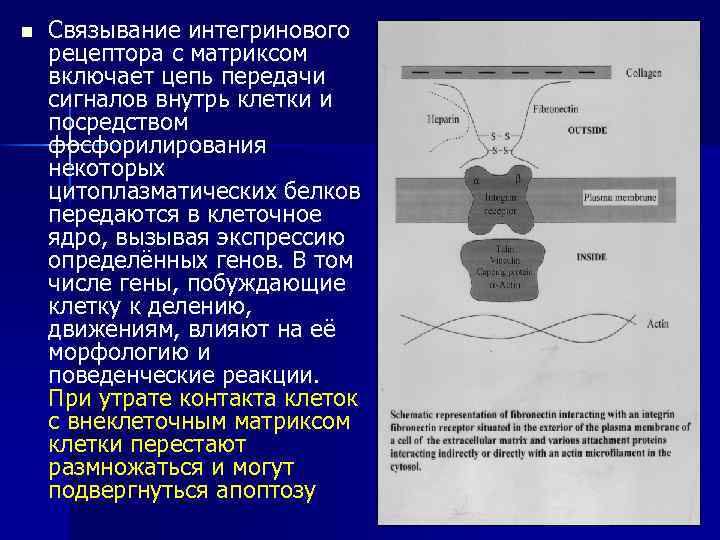
n Связывание интегринового рецептора с матриксом включает цепь передачи сигналов внутрь клетки и посредством фосфорилирования некоторых цитоплазматических белков передаются в клеточное ядро, вызывая экспрессию определённых генов. В том числе гены, побуждающие клетку к делению, движениям, влияют на её морфологию и поведенческие реакции. При утрате контакта клеток с внеклеточным матриксом клетки перестают размножаться и могут подвергнуться апоптозу

n n Тромбастения Гланцманна - больные с дефектом субъединиц 2 3 интегрина, несмотря на нормальное число тромбоцитов, страдают от кровотечений вследствие ретракции сгустка –. Адгезия клеток одного типа к клеткам другого может изменяться в результате увеличения числа молекул адгезии на клеточной поверхности благодаря 2 механизмам: 1) У многих клеток большие запасы этих молекул хранятся во внутриклеточных везикулах, которые способны через несколько минут после активации устремляться к поверхности цитоплазматической мембраны; 2) Синтез таких молекул и перенос их на поверхность (занимает несколько часов)
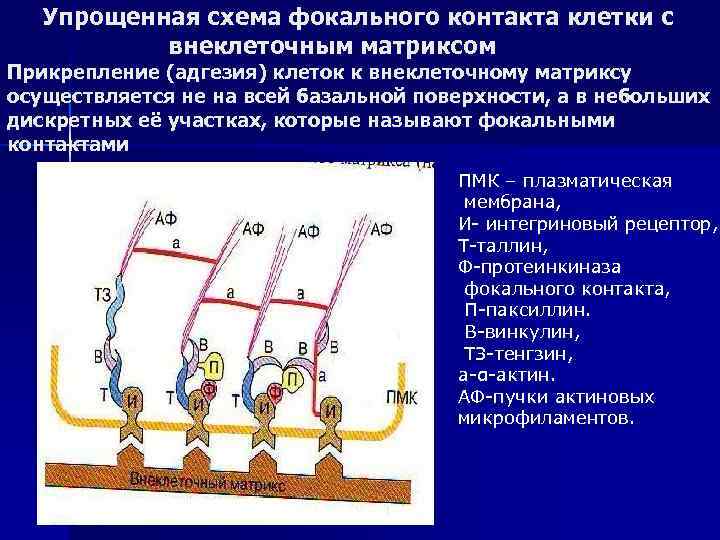
Упрощенная схема фокального контакта клетки с внеклеточным матриксом Прикрепление (адгезия) клеток к внеклеточному матриксу осуществляется не на всей базальной поверхности, а в небольших дискретных её участках, которые называют фокальными контактами ПМК – плазматическая мембрана, И- интегриновый рецептор, Т-таллин, Ф-протеинкиназа фокального контакта, П-паксиллин. В-винкулин, ТЗ-тенгзин, а-α-актин. АФ-пучки актиновых микрофиламентов.
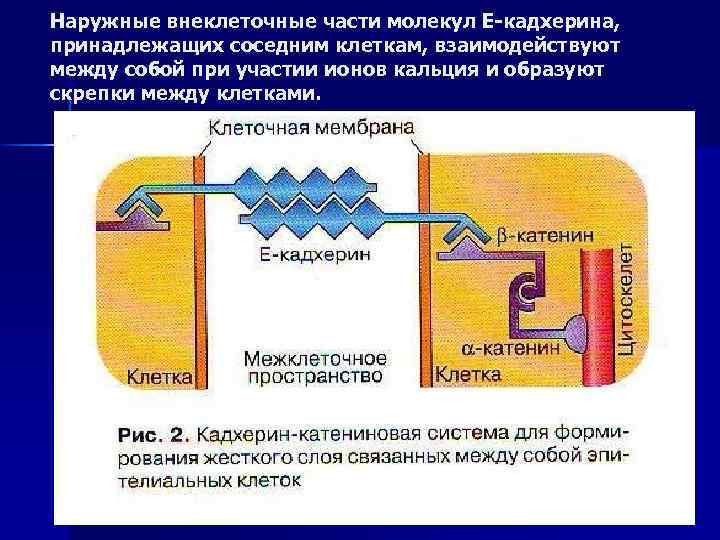
Наружные внеклеточные части молекул Е-кадхерина, принадлежащих соседним клеткам, взаимодействуют между собой при участии ионов кальция и образуют скрепки между клетками.
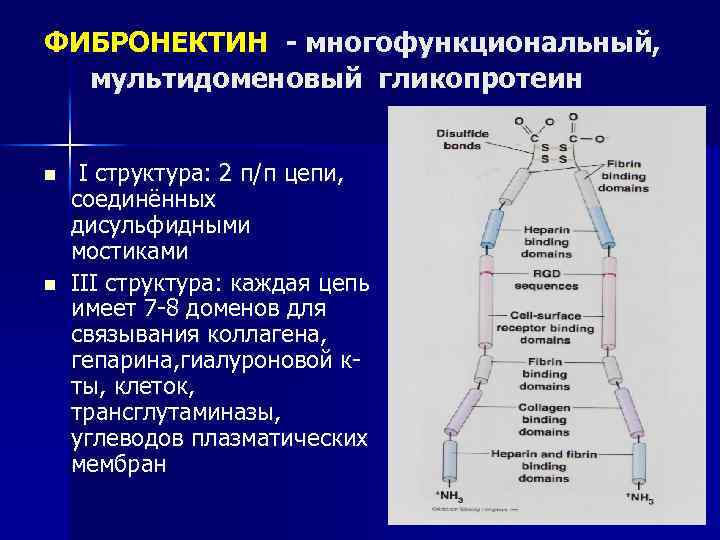
ФИБРОНЕКТИН - многофункциональный, мультидоменовый гликопротеин n n I структура: 2 п/п цепи, соединённых дисульфидными мостиками III структура: каждая цепь имеет 7 -8 доменов для связывания коллагена, гепарина, гиалуроновой кты, клеток, трансглутаминазы, углеводов плазматических мембран
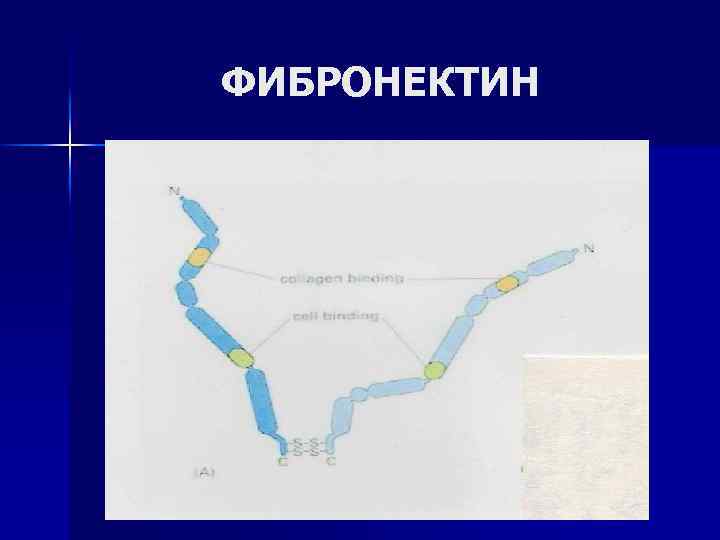
ФИБРОНЕКТИН

ФИБРОНЕКТИН - во всех органах и тканях n модулятор и маркер функционального состояния РЭС, n способен стимулировать фагоцитоз (неспецифический фактор защиты), n способен включаться в состав фибринового сгустка под действием ХIIIа в присутствии Са 2+ играет важную роль в физиологических реакциях тромбоцитов, их адгезии на субъэндотелии. n Патогенетическое значение: - снижение уровня при шоке; - высокоактивный хемоаттрактант для фибробластов важная роль при заживлении ран; - качественные и количественные изменения при малигнизации клеток. При недостаточном синтезе фибронектина, ламинина у онкологических больных происходит метастазирование опухоли.

ЛАМИНИН - многофункциональный, мультидоменовый гликопротеин I структура: 3 п/п цепи: А, В 1 и. В 2, связанных дисульфидными мостиками n Молекула ламинина: крестообразная форма с 3 одноцепочечными ветвями и 1 трёхцепочечной ветвью Каждая цепь имеет несколько глобулярных и стержневых доменов для связывания с коллагеном IV протеогликанами, фибронектином клетками и др. компонентами базальных мембран. n
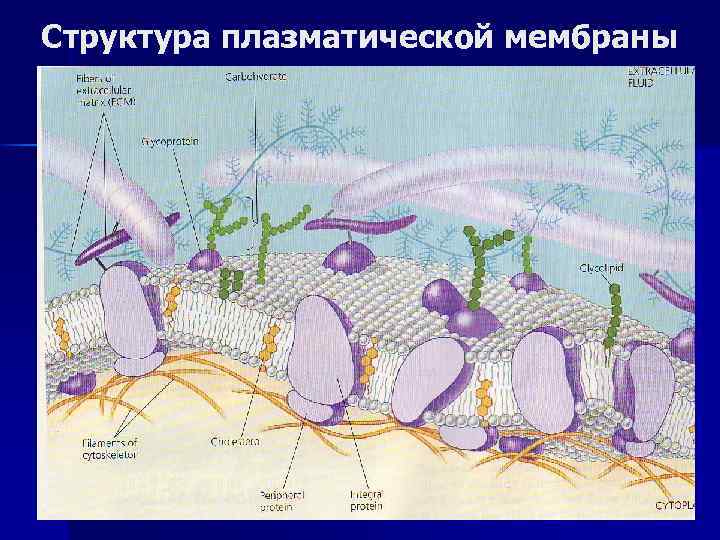
Структура плазматической мембраны

ОРГАНИЗАЦИЯ МЕЖКЛЕТОЧНОГО МАТРИКСА

Протеогликаны выполняют функцию наполнителя (основного вещества). Благодаря полярной природе и сильному отрицательному заряду, они связывают катионы и основную часть воды. Протеогликаны - одни из наиболее крупных молекул; n они включают белковую (5%) и углеводную (95%) части и по форме напоминают ершик для мытья бутылок. Белковые мономеры, несущие множество полисахаридных цепей, ассоциированы с осевой молекулой гиалуроновой кислоты. n
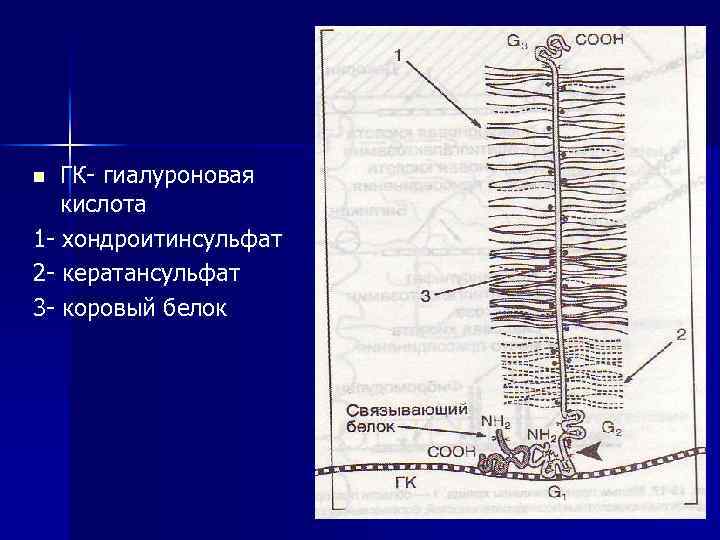
ГК- гиалуроновая кислота 1 - хондроитинсульфат 2 - кератансульфат 3 - коровый белок n
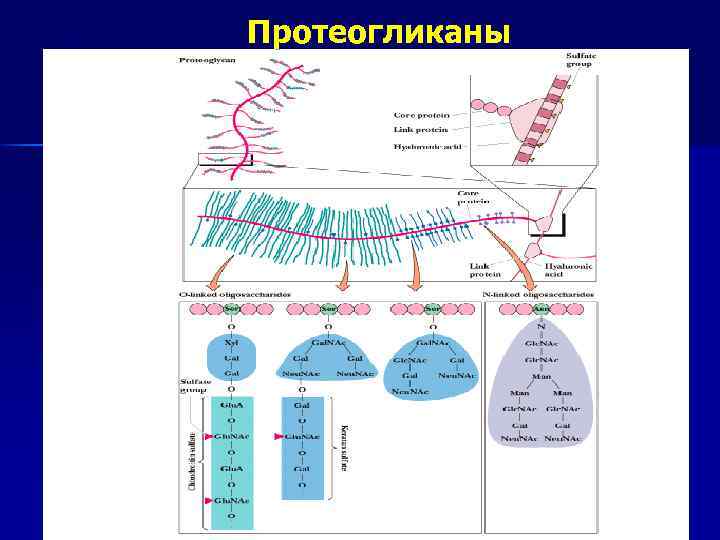
Протеогликаны
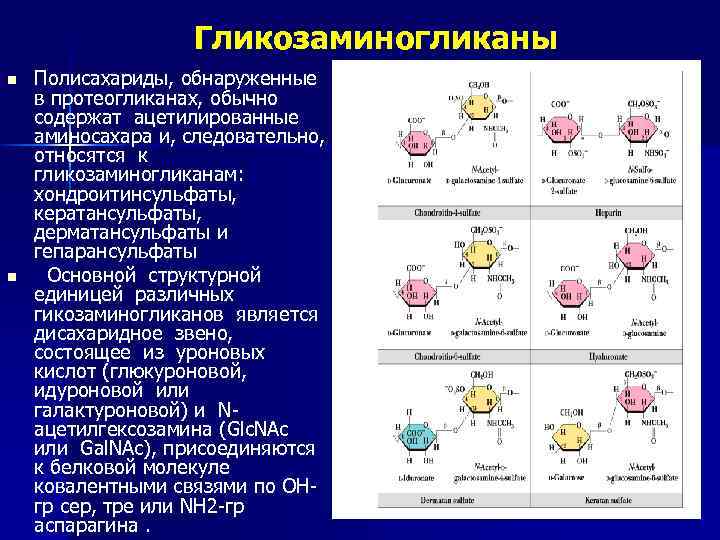
Гликозаминогликаны n n Полисахариды, обнаруженные в протеогликанах, обычно содержат ацетилированные аминосахара и, следовательно, относятся к гликозаминогликанам: хондроитинсульфаты, кератансульфаты, дерматансульфаты и гепарансульфаты Основной структурной единицей различных гикозаминогликанов является дисахаридное звено, состоящее из уроновых кислот (глюкуроновой, идуроновой или галактуроновой) и Nацетилгексозамина (Glc. NAc или Gal. NAc), присоединяются к белковой молекуле ковалентными связями по ОНгр сер, тре или NН 2 -гр аспарагина.

Мукополисахаридозы n n наследственные заболевания, проявляющиеся нарушениями в умственном развитии детей, поражениями сосудов, помутнением роговицы, деформациями скелета, снижением продолжительности жизни. В основе - дефекты гидроксилаз избыточное накопление в лизосомах не полностью разрушенных гликозаминогликанов деформации скелета и увеличение органов, содержащих большие количества внеклеточного матрикса.
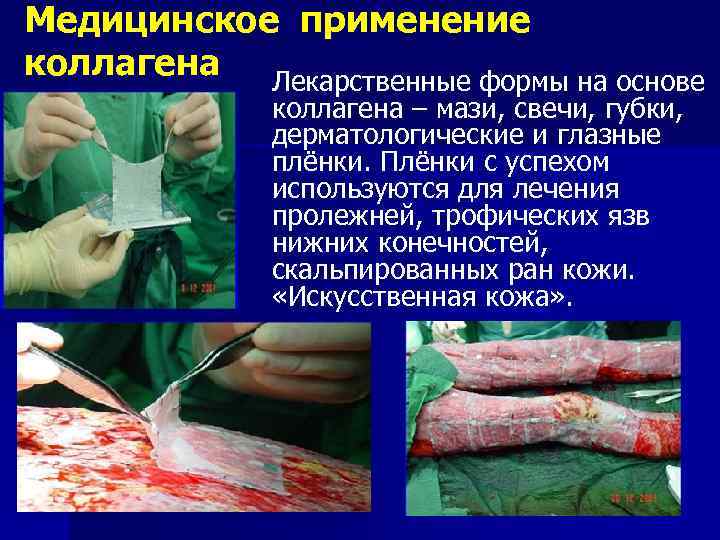
Медицинское применение коллагена Лекарственные формы на основе коллагена – мази, свечи, губки, дерматологические и глазные плёнки. Плёнки с успехом используются для лечения пролежней, трофических язв нижних конечностей, скальпированных ран кожи. «Искусственная кожа» .
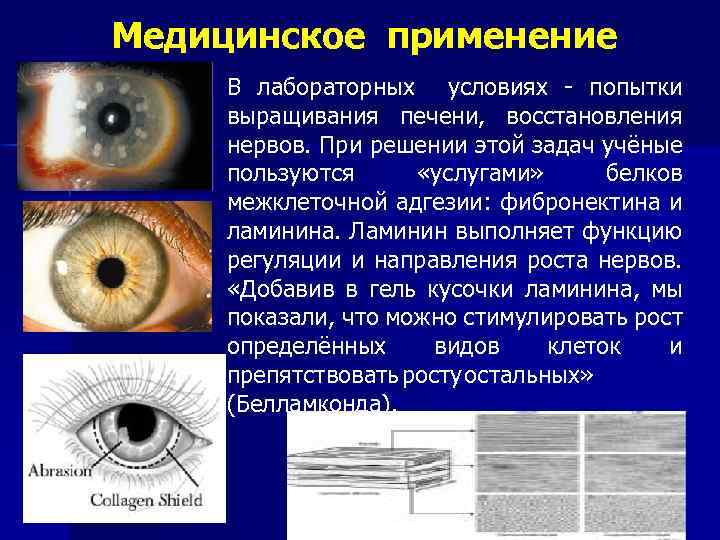
Медицинское применение В лабораторных условиях - попытки выращивания печени, восстановления нервов. При решении этой задач учёные пользуются «услугами» белков межклеточной адгезии: фибронектина и ламинина. Ламинин выполняет функцию регуляции и направления роста нервов. «Добавив в гель кусочки ламинина, мы показали, что можно стимулировать рост определённых видов клеток и препятствовать росту остальных» (Белламконда).

БИОХИМИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ Функции: опорная (основа органов и тканей) ; n - механическая ( прочность тканей); n соединительная ( связывание клеток и межклеточного матрикса в единую ткань) n защитная (препятствует проникновению инфекционных агентов): n пластическая (закрытие крупных дефектов тканей); n специфическая (зубы, сухожилия, кожа, фасции, связки); n поддержание формы органов ( каркас органов). Особенности соединительной ткани: n малое количество клеток (фибробластов, хондробластов, остеобластов, кератобластов); n преобладание межклеточного матрикса; n преобладание фибриллярных белков (коллагена, эластина, фибронектина); n преобладание гликозаминогликанов и протеогликанов.

Биохимические изменения при старении n n n Старение сопровождается уменьшением отношения основное вещество/волокна, уменьшением содержания воды; снижением концентрации гликозаминогликанов; увеличением содержания коллагена; изменением свойств коллагена ( увеличение числа поперечных связей, уменьшение доступности для действия коллагеназы, увеличение регидности сухожилий, связок, снижение эластичности и способности к набуханию). Сходные изменения в эластине.
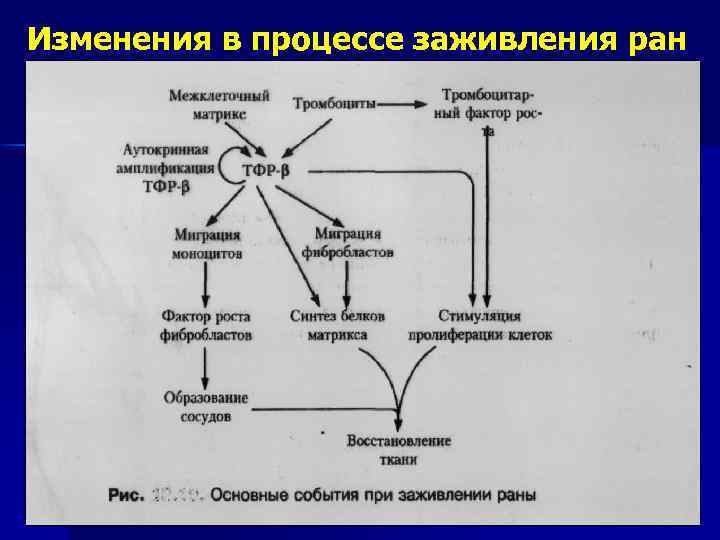
Изменения в процессе заживления ран
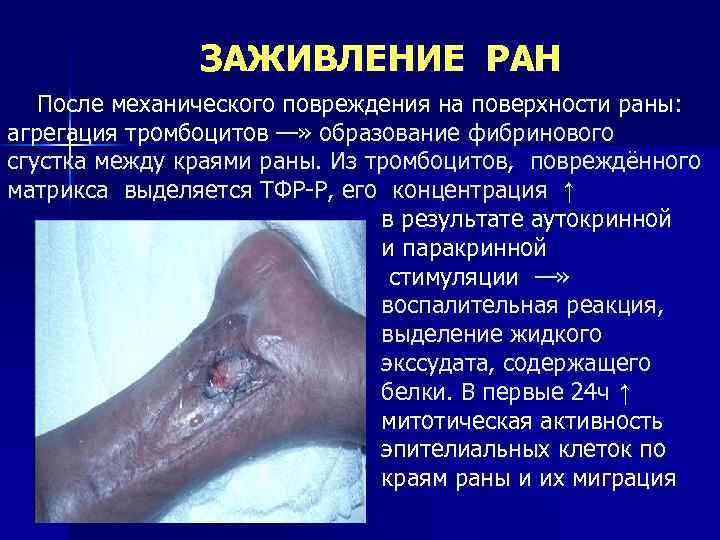
ЗАЖИВЛЕНИЕ РАН После механического повреждения на поверхности раны: агрегация тромбоцитов —» образование фибринового сгустка между краями раны. Из тромбоцитов, повреждённого матрикса выделяется ТФР-Р, его концентрация ↑ в результате аутокринной и паракринной стимуляции —» воспалительная реакция, выделение жидкого экссудата, содержащего белки. В первые 24 ч ↑ митотическая активность эпителиальных клеток по краям раны и их миграция

ЗАЖИВЛЕНИЕ РАН n n ТФР-Р действует как хемоаттрактант: в область повреждения мигрирует ряд клеток, в т. ч. моноциты и фибробласты. ТФР-Р активирует рецепторы тромбоцитарного фактора роста на клетках ткани —» этот цитокин индуцирует клеточную пролиферацию. Пролиферация эпителия продолжается пока не закроется рана. Происходит и пролиферация фибробластов по краям раны (в течение примерно 3 дней). Фактор роста фибробластов (ФРФ- секретируется моноцитами) индуцирует образование новых сосудов, врастающих из краёв раны Образующаяся грануляционная ткань содержит коллагеновые фибриллы (структура лишена регулярности), контактирующие с поверхностью фибробластов.

ЗАЖИВЛЕНИЕ РАН n Трансформирующий фактор роста – ТФР-Р- м. м. 12. 5 к. Да синтезируется в большинстве (если не во всех) клетках организма. n Способен стимулировать накопление матрикса: индуцирует синтез коллагена, фибронектина, ламинина, гликозаминогликанов и одновременно подавляет их деградацию фибробластами и клетками поврежденной ткани n Коллаген вызывает адгезию тромбоцитов и их агрегацию. n Эластин образуется на поздних стадиях заживления.

ЗАЖИВЛЕНИЕ РАН По мере накопления грануляционной ткани и матрикса образуется трёхмерная сеть коллагеновых волокон —» ↑ стягивающее напряжение и образуется рубец —» n Репарация завершается: ↓ ТФР-Р и весь аппарат репарации выключается. n Если выключение запаздывает —» гипертрофированный рубец = келоид n В репарации участвуют также ФНО и ИЛ-1: индуцируют воспаление, клеточную миграцию и пролиферацию

ЗАЖИВЛЕНИЕ, ЕСЛИ УТРАЧЕНА ЧАСТЬ ТКАНИ n n n Образование грануляционной ткани на дне раны и реэпителизация поверхности раны В ране – экссудат (содержит белок), при высыхании образует струп. У краев раны - пролиферация эпителиальных клеток, которые растут под коркой к центру. Многие фибробласты в таких ранах приобретают свойства миофибробластов ( под влиянием ТФР-Р). Эти клетки способны сжимать трёхмерную сеть, построенную из коллагеновых фибрилл, уменьшая объём геля коллагена: фибробласты мигрируют внутрь сети и укладывают фибриллы в пучки. Заживление регулируют в основном те же цитокины, что и в случае резаных ран.

Недостаток вит С : снижение активности пролин и лизингидроксилаз, n уменьшает биосинтез проколлагена и тропоколлагена, n уменьшает прочность структуры коллагена и нарушает прочность стенок кровеносных сосудов, связок, фасций и т. д. Избыток вит Д 3 = избыток кальцитриола : n деструкция органического и минерального компонентов костей n усиление катаболизма коллагена--усиление выделения с мочой оксипролина. Гиперпаратиреоидизм : паратгормон активируя катаболизм коллагена способствует увеличению в моче оксипро и ионов кальция.

ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ СИНТЕЗА И СОЗРЕВАНИЯ КОЛЛАГЕНА I Кости, кожа, сухожилия, склера, строма Несовершенный остеогенез (мутация в генах > 160) n Проявления: ↑ломкость костей, аномалии зубов, гиперподвижность суставов, ∆ форма лица n II Хрящи, м/п диски, стекловидное тело Б-нь. Книста (делеция) С-м Стиклера-Вагнера (терм. кодон, синтез 1/2 мол. ) n Проявления: укорочение и деформация конечностей. тугоподвижность суставов, кифосколиоз, миопия высокой степени —» отслойка сетчатки, остеоартриты n

ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ СИНТЕЗА И СОЗРЕВАНИЯ КОЛЛАГЕНА n III Кожа, сосуды, строма паренхиматозных органов, n IV Базальные мембраны (почки. лёгкие) матка Синдром Альпорта С-м Элерса-Данло-Русакова IV тип (мутации >20, делеции, (мутации) Проявления: поражение вставки, замены) → снижена почек: гематурия, стабильность коллагена протеинурия n Проявления: Синдром Гудпасчера Спонтанные разрывы (АТ к коллагену IV типа) крупных сосудов, разрыв Проявления: беременной матки, гломерулонефрит, пневматорокс, перфорация лёгочный гемосидероз кишечника.

СПАСИБО ЗА ВНИМАНИЕ
БИОХИМИЯ МЕЖКЛЕТОЧНОГО МАТРИКСА.ppt