Лекция_7_строение генов.ppt
- Количество слайдов: 93

БИОХИМИЯ Лекция № 7

Ген • структурная и функциональная единица наследственности, контролирующая развитие определённого признака или свойства. • Совокупность генов родители передают потомкам во время размножения. • В отличие от вертикального переноса, в горизонтальном организм передаёт гены организму, который не является его потомком. • Этот способ передачи широко распространён среди одноклеточных организмов и в меньшей степени среди многоклеточных.

• Таким образом, мы здесь впервые встречаемся с термином ген, который был введен тогда, когда о том, что это такое, были еще весьма смутные представления. Потом понятие гена несколько раз уточнялось до тех пор, пока фактически стало ненужным. Тем не менее, оно осталось, причем в достаточно нестрогом употреблении. • В молекулярной биологии слово ген не используется.

Свойства гена • • • дискретность — несмешиваемость генов; стабильность — способность сохранять структуру; лабильность — способность многократно мутировать; множественный аллелизм — многие гены существуют в популяции во множестве молекулярных форм; аллельность — в генотипе диплоидных организмов только две формы гена;

• специфичность — каждый ген кодирует свой признак; • плейотропия — множественный эффект гена; • экспрессивность — степень выраженности гена в признаке; • пенетрантность — частота проявления гена в фенотипе; • амплификация — увеличение количества копий гена
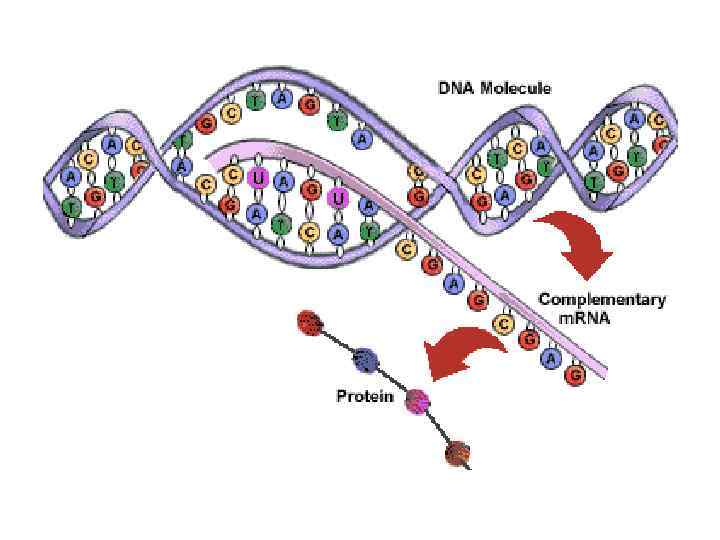

Кодон • (кодирующий тринуклеотид) — единица генетического кода, тройка нуклеотидных остатков (триплет) в ДНК или РНК, обычно кодирующих включение одной аминокислоты. • Последовательность кодонов в гене определяет последовательность аминокислот в полипептидной цепи белка, кодируемого этим геном

• Поскольку существует 4 различных нуклеотида, то общее число кодонов равняется 64, из которых 61 кодируют определённые аминокислоты, а 3 оставшихся кодона сигнализируют об остановке трансляции полипептидной цепи и называются стоп-кодонами. • Так как в процессе биосинтеза белка в полипептидную цепь участвует всего 20 аминокислот, то различные кодоны могут кодировать одинаковые аминокислоты, такие кодоны принято называть изоакцепторными кодонами.

• Латинские и русские коды для нуклеиновых оснований: • • • A — А: Аденин; G — Г: Гуанин; C — Ц: Цитозин; T — Т: Тимин, в ДНК; U — У: Урацил, в РНК

• Стоп-кодоны (UGA, UAG и UAA) выполняют важную функцию завершения (терминацию) сборки полипептидной цепи и также называются терминаторными кодонами. • Кроме того, стоп-кодон, как кодон при котором не происходит включения аминокислоты в белок, ещё называют бессмысленным кодоном или нонсенс-кодоном

• Стартовым кодоном у эукариотических организмов является триплет AUG в м. РНК, кодирующий метионин, с которого начинается образование полипептидной цепи в процессе трансляции. • У некоторых прокариотов стартовыми кодонами так же являются GUG, AUU, CUG, UUG.

Нестандартные значения кодонов • У некоторых организмов генетический код отличается от канонического. • Например многие виды зелёных водорослей Acetabularia транслируют стандартные стоп-кодоны UAG и UAA в аминокислоту глицин, а гриб Candida интерпретирует РНК-кодон CUG не как лейцин, а как серин. • А у митохондрий пекарских дрожжей (Saccharomyces cerevisiae) четыре из шести кодонов, обычно транслирующихся в лейцин, кодируют треонин.

• Существование таких вариаций свидетельствует о возможной эволюции генетического кода. • Представители почти всех трёх доменов живых организмов иногда прочитывают стандартный стоп-кодон UGA как 21 -ю аминокислоту селеноцистеин, не относящуюся к 20 стандартным. • Аналогично у представителей двух доменов (архебактерий и бактерий) стопкодон UAG прочитывается как 22 -я аминокислота пирролизин.

Кепирование • Кепирование - надевание "шапочки". “Сар" представляет собой метилированный ГТФ, присоединенный в необычной позиции 5'-5' и две метилированные рибозы в первых двух нуклеотидах m. РНК. • По мере образования про-m. РНК (еще до 30 -ого нуклеотида), к 5'-концу, несущему пуринтрифосфат, присоединяется гуанин, после чего происходит метилирование. Назначение "Сар" 1. Защита 5'-конца m. РНК от действия экзонуклеаз. 2. За счет узнавания "Сар"-связывающими белками происходит правильная установка m. РНК на рибосоме.

Строение гена • Ген состоит из 2 -х основных элементов: 1) регуляторной части (не транскрибируется) • 2) собственно кодирующей части • Точка начала транскрипции – сайт «О» левее от «О» - минус последовательности правее от «О» - плюс последовательности

• Кодирующая часть гена у прокариот: Только экзоны • Кодирующая часть гена у эукариот: Экзоны и интроны

• Геномы прокариот и эукариот, хотя и имеют определенное сходство, но все же существенно различаются по своей структуре. • Геномы прокариот практически целиком состоят из генов и регуляторных последовательностей. В генах прокариот нет интронов • Часто функционально родственные гены прокариот находятся под единым транскрипционным контролем, то есть транскрибируются вместе, составляя оперон.

• Геномы эукариот существенно больше геномов бактерий, у дрожжей примерно в 2 раза, а у человека – на три порядка, то есть в тысячу раз. • Однако прямой зависимости между количеством ДНК и эволюционной сложностью видов не наблюдается. • геномы некоторых видов амфибий или растений в десять или даже в сто раз превосходят по размеру геном человека. • В некоторых случаях близкие виды организмов могут существенно различаться по количеству ДНК.

• Важным обстоятельством является то, что при переходе от прокариот к эукариотам увеличение генома происходит, главным образом, за счет появления огромного количества некодирующих последовательностей. • Действительно, в геноме человека кодирующие области, то есть экзоны, суммарно занимают не более 3%, а по некоторым оценкам около 1% от общей длины ДНК.

Экзоны и Интроны • Экзон - участок гена, несущий информацию о первичной структуре белка • В гене экзоны разделены некодирующими участками — интронами • Последовательность нуклеотидов, соответствующая интрону, удаляется из транскрибированной с него РНК в процессе сплайсинга до того, как произойдёт считывание белка (трансляция).

Сплайсинг • (от англ. splice — сращивать или склеивать концы) • процесс вырезания определенных нуклеотидных последовательностей из молекул РНК и соединения последовательностей, сохраняющихся в «зрелой» молекуле, в ходе процессинга РНК.

• Наиболее часто сплайсинг встречается при созревании информационной РНК (м. РНК) у эукариот, при этом из м. РНК удаляются участки, не кодирующие белок (интроны) и соединяются друг с другом кодирующие аминокислотную последовательность участки — экзоны. • Таким образом незрелая пре-м. РНК превращается в зрелую м. РНК, с которой транслируются белки клетки.

• Большинство генов прокариот, кодирующих белки, не имеют интронов, поэтому у них сплайсинг пре-м. РНК встречается редко. • У представителей эукариот, бактерий и архей встречается также сплайсинг транспортных РНК и других некодирующих РНК.

• Интроны характерны для всех типов эукариотической РНК, но также найдены в рибосомальной РНК (р. РНК) и транспортной РНК (т. РНК) прокариот. • Число и длина интронов очень различны в разных видах и среди разных генов одного организма.
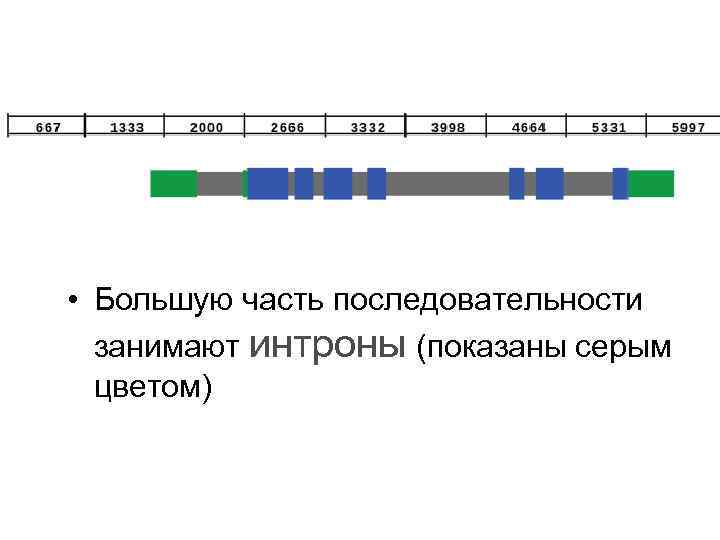
• Большую часть последовательности занимают интроны (показаны серым цветом)
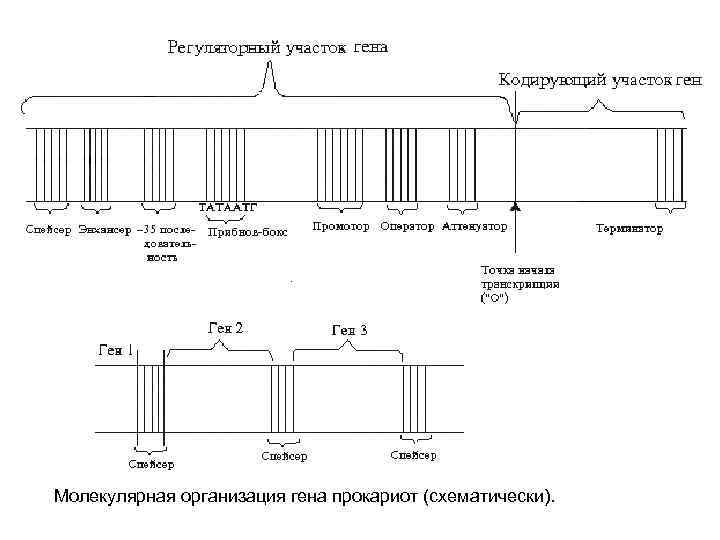
Молекулярная организация гена прокариот (схематически).

Рамка считывания • нуклеотидная последовательность, выраженная в кодирующих триплетах. Один из трех возможных способов считывания нуклеотидной последовательности в виде триплетов. • Различают открытые и закрытые рамки считывания.
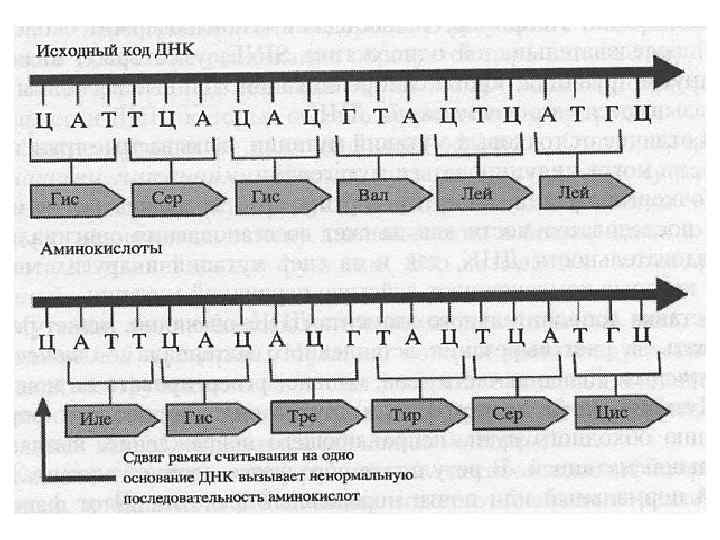

Открытая рамка считывания • Открытая рамка считывания - участок ДНК или РНК между инициирующим кодоном и стоп-кодоном, не содержащая терминирующих кодонов и потенциально способная кодировать белок • Основным параметром наличия ORF служит отсутствие стоп-кодонов, в большинстве случаев — TAA, TGA и TAG на достаточно продолжительном участке последовательности после стартового кодона (в подавляющем случае — ATG).

• Закрытая рамка считывания — рамка считывания, содержащая бессмысленные кодоны, что не позволяет м. РНК, соответствующей этой последовательности, транслироваться в функционально активный белок из-за преждевременной терминации
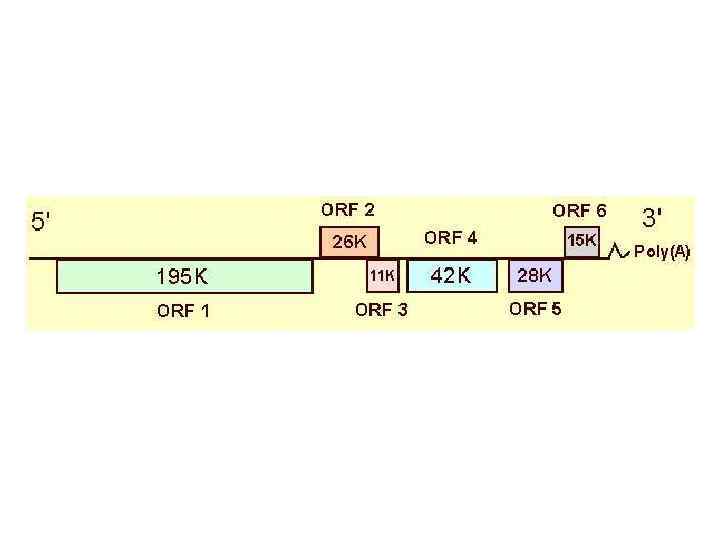

понятие гена не ограничено только кодирующим участком ДНК, а представляет собой более широкую концепцию, включающую в себя и регуляторные последовательности.

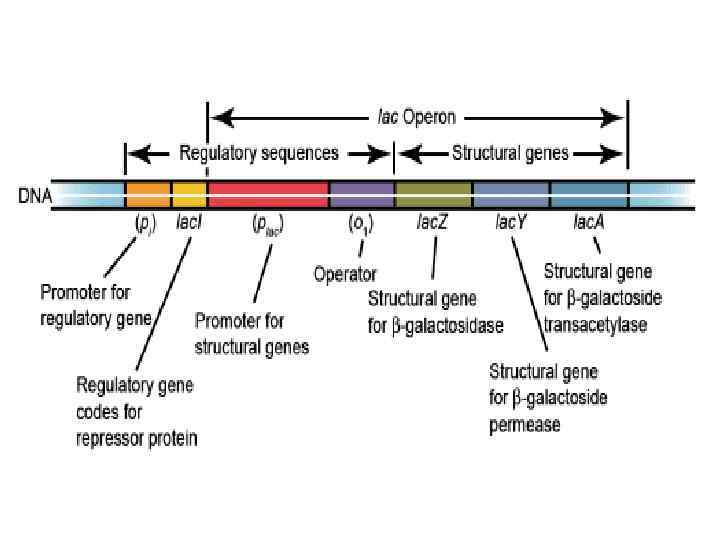
Гены прокариот • У прокариот гены, выполняющие сходные метаболические функции, часто располагаются в функциональные единицы, называемые оперонами и их экспрессия регулируется совместно (полицистронный механзим регуляции активности генов). • Цистрон — участок ДНК, ответственный за синтез определённого белка.

• Оперон — функциональная единица генома у прокариот, в состав которой входят цистроны (гены, единицы транскрипции), кодирующие совместно или последовательно работающие белки и объединенные под одним (или несколькими) промоторами. • Опероны по количеству цистронов делят на моно-, олиго- и полицистронные, содержащие, соответственно, только один, несколько или много цистронов (генов).

• Начинается и заканчивается оперон регуляторными областями — промотором в начале и терминатором в конце, кроме этого, каждый отдельный цистрон может иметь в своей структуре собственный промотор и/или терминатор.

• Оперон состоит из нескольких частей: промотора (П), структурных генов (А, В, С и т. д. ) и терминатора (Т). • Промотор - участок транскрипции, состоящий из нескольких десятков последовательных нуклеотидов ДНК, с которой специфически связан фермент (РНК-полимераза), осуществляющий транскрипцию ДНК; кроме того, промотор определяет, какая из цепей двойной ДНК будет служить матрицей для ДНК.

• Оператор является участком, с которым происходит связывание белка репрессора. • Терминатор - участок, расположенный в конце оперона и дающий сигнал о прекращении транскрипции.

• Одно из самых важных свойств гена - способность к экспрессии. • Многие бактериальные гены устроены таким образом, что они способны функционировать с существенно разной эффективностью. • У E. coli, например, относительное содержание различных белков варьирует в очень широких пределах (от менее чем 0. 1% до 2%) в зависимости от их функций; при этом каждый белок в хромосоме E. coli кодируется единственным геном.

• Такие вариации обусловлены действием системы контроля генной экспрессии, которая осуществляется главным образом на уровне транскрипции ДНК. • Таким образом, чаще всего уровень активности гена связан с количеством синтезируемой на нем м. РНК, то есть с активностью фермента РНК-полимеразы.

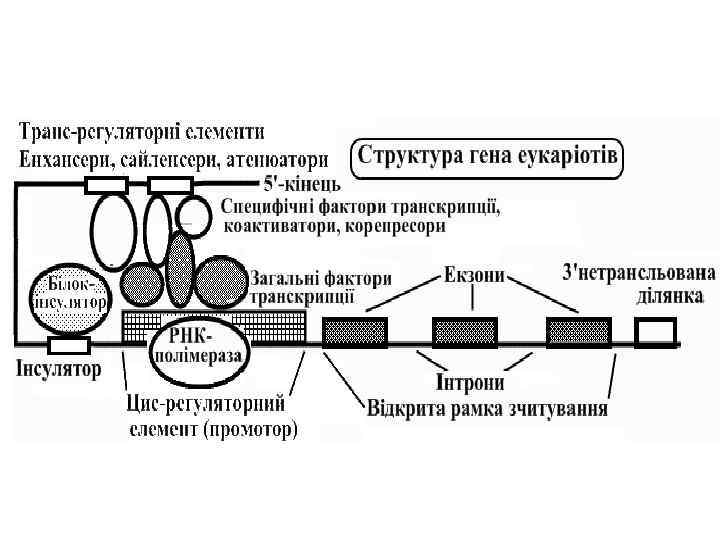
Гены эукариот • Регуляторные последовательности могут находиться как в непосредственной близости от открытой рамки считывания, кодирующей белок, или начала последовательности РНК, как в случае с промоторами (так называемые cisрегуляторные элементы), так и на расстоянии многих миллионов пар оснований (нуклеотидов), как в случае с энхансерами, инсуляторами и супрессорами (иногда классифицируемые как trans-регуляторные элементы).

• Цис-элемент (цис-регуляторный элемент) — участок ДНК или РНК, который регулирует экспрессию генов, локализованных на той же молекуле ДНК (хромосоме). • Цис-элементы обычно являются местами связывания одного или нескольких регуляторных белков (транс-факторами), кодируемых другими генами.

• Транс-регуляторные элементы — гены, которые изменяют экспрессию генов, находящихся на большом расстоянии. • Как правило, транс-регуляторные элементы кодируют факторы транскрипции.

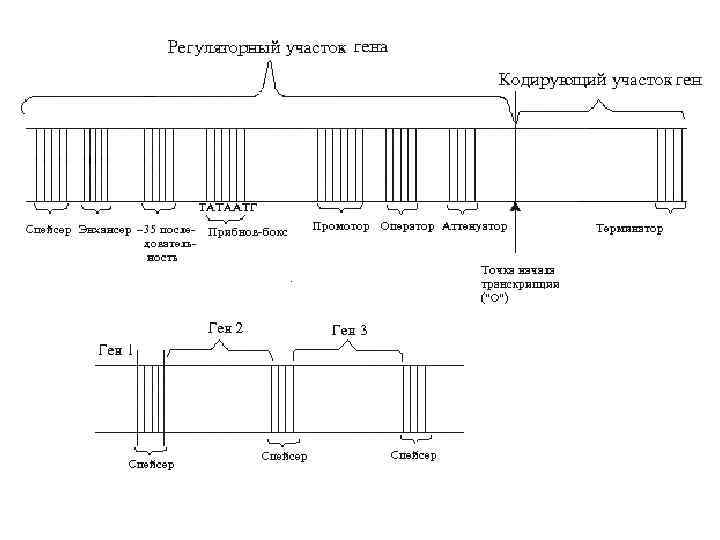
Регуляторная часть гена • Промотор – на 5’ конце (инициация транскрипции) • Спейсеры-некодирующие последовательности • Терминатор – на 3’ конце (терминация транскрипции)

• Оператор - сайт связи с белкомрепрессором • Энхансеры - усиливают скорость транскрипции • Сайленсеры - снижают скорость транскрипции • Аттенуаторы - запускают или останавливают транскрипцию

Промотор • последовательность нуклеотидов ДНК, узнаваемая РНК-полимеразой как стартовая площадка для начала транскрипции. • Промотор асимметричен, что позволяет РНКполимеразе начать транскрипцию в правильном направлении и указывает то, какая из двух цепей ДНК будет служить матрицей для синтеза РНК. • То, под каким промотором находится кодирующий РНК участок ДНК, играет решающее значение в интенсивности экспрессии этого гена в каждом конкретном типе клеток.

Промотор прокариот • Промотор имеет 2 консервативные последовательности: • 1) бокс Прибнова. Нуклеотидная последовательность у прокариот, расположенная за 10 нуклеотидов от точки инициации транскрипции и обычно состоящая из 6 (иногда до 9) оснований, каноническая последовательность - ТАТААТ;

предполагается, что на участке бокса Прибнова происходит расплетение цепей ДНК в момент инициации транскрипции, также необходим для правильного ориентирования РНКполимеразы на промоторе. • аналогом у эукариот является бокс Хогнесса • 2) -35 последовательность. Состоит из 9 нуклеотидов.

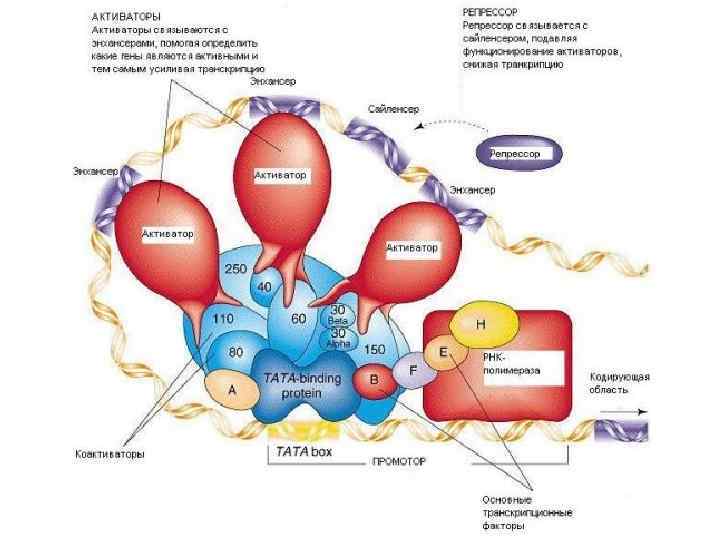
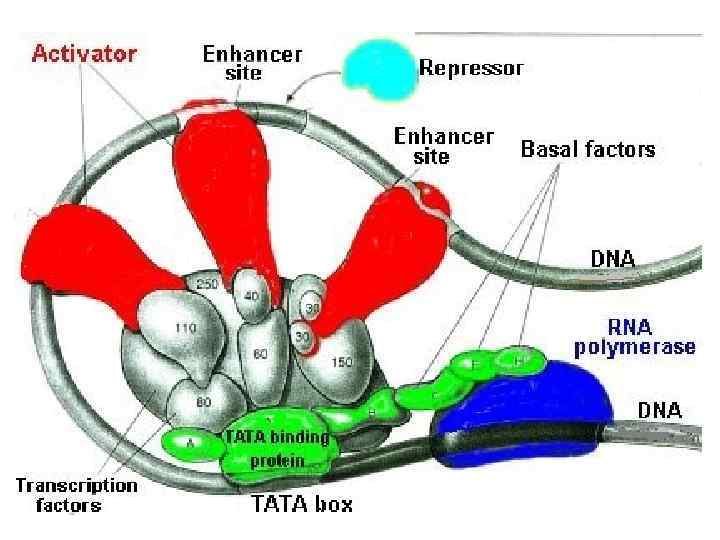
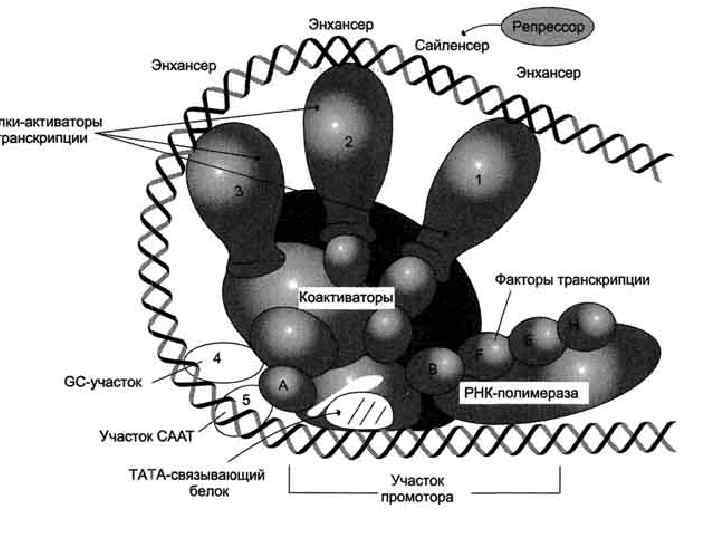
Промотор эукариот • 1. Бокс Голдберга-Хогнесса или ТАТАбокс (наименее активный, соединяется через транскрипционные факторы с РНК • 2. ЦААТ бокс или ЦАТ бокс • 3. ГЦ бокс или последовательность ГГГЦГГ (два последних влияют на эффективность транскрипции)

Оператор Участок ДНК, узнаваемый специфическими белками-репрессорами и негативно регулирующий транскрипцию структурных генов; размер – несколько десятков нуклеотидов. Как правило, оператор непосредственно примыкает к регулируемому структурному гену (согласно модели оперона). Известны точечные мутации оператора, ведущие к постоянной (конститутивной) экспрессии соответствующего гена.

Энхансер небольшой участок ДНК, способный связываться с факторами транскрипции, при этом увеличивая уровень транскрипции гена или группы генов. • Энхансер не обязательно находится в непосредственной близости от генов, на которые он действует, и даже не обязательно располагается с ними на одной хромосоме.

• В эукариотических клетках структура хроматинового комплекса функционально схожа с суперскрученной ДНК прокариот, поэтому, хотя энхансер находится и далеко от генов, на которые он действует, по последовательности нуклеотидов, геометрически он лежит рядом с промотором и генами.

• Непосредственное влияние на промотор энхансеры не оказывают, они действуют опосредованно через белки-активаторы. • Энхансеры также могут находиться внутри интронов.

• В эукариотических клетках структура хроматинового комплекса функционально схожа с суперскрученной ДНК прокариот, поэтому, хотя энхансер находится и далеко от генов, на которые он действует, по последовательности нуклеотидов, геометрически он лежит рядом с промотором и генами. • Непосредственное влияние на промотор энхансеры не оказывают, они действуют опосредованно через белкиактиваторы. • Энхансеры также могут находиться внутри интронов.

• По способу регуляции экспрессии генов различают два типа энхансеров. • Индуцибельные энхансеры реагируют на изменения в окружающей среде (тепловой шок, вирусная инфекция, появление тяжелых металлов, ростовых факторов, стероидов и т. п. ). • Такие энхансеры есть у генов белков теплового шока, металлотионина, (3 интерферона, некоторых онкогенов и др. • неспецифичные и временные энхансеры активны только в определенных клетках или в определенное время развития организма (например, энхансеры генов иммуноглобулинов).

• Механизм работы энхансеров заключается в посадке на них специфичных белков, которые за счет образования петель в ДНК взаимодействуют с транскрипционными факторами, связанными с промотором ближайшего гена, увеличивая тем самым число посадок на него РНК-полимеразы II.

• По-видимому, так же работают и локусы с противоположным эффектом действия — сай-ленсеры (silencer — успокоитель), в присутствии которых транскрипционная активность РНКполимеразы II уменьшается. У дрожжей аналогами энхансеров и сайленсеров являются последовательности URS и UAS.

Сайленсер • участки регуляции процесса транскрипции у эукариот. • Сайленсеры подавляют транскрипционную активность генов путем изменения структуры хроматина. • Связывание белков-репрессоров с сайленсерами приводит к понижению или к полному подавлению синтеза РНК ферментом ДНК-зависимой РНКполимеразой. • Сайленсеры могут находиться на расстоянии до 2500 пар нуклеотидов от промотора

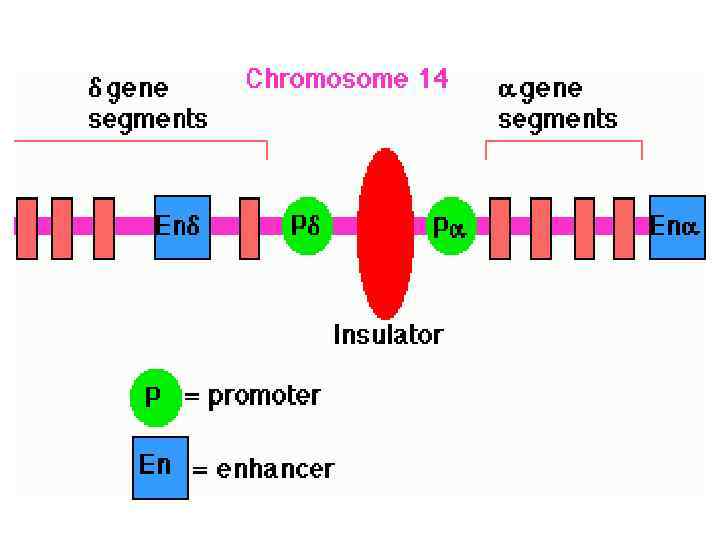
Инсуляторы • последовательности ДНК, особые регуляторные элементы, которые обладают способностью блокировать сигналы, исходящие от окружения. • Во-первых, они блокируют взаимодействие между энхансером и промотором, если находится между ними. При этом инсулятор выполняет только разделительную функцию и не влияет на активность энхансера и промотора.

• Во-вторых, инсулятор выполняет барьерную функцию для распространяющегося конденсированного хроматина. Показано, что существуют инсуляторы, как выполняющие одну из двух функций, так и обе. • Инсуляторы представляют собой сайты связывания особых, инсуляторных, белков. • Энхансеры не обладают специфичностью действия, следовательно, у эукариот должны были выработаться механизмы, обеспечивающие невозможность активации генов в ненужном месте или в ненужное время развития энхансерами соседнего гена.

Аттенуатор • (англ. attenuate — разрежать, разбавлять) — генетический элемент, ослабляющий работу оперона. • Аттенуатор — последовательность нуклеотидов, расположенная между промоторным операторным участком оперона и его первым структурным опероном; она кодирует лидерную РНК, ее длина около 150 пар нуклеотидов.

Спейсер • Между генами находятся спейсеры - неинформативные отрезки ДНК различной длины (иногда более 20 000 пар оснований), которые имеют значение для регулирования транскрипции соседнего гена

• Для эукариот понятия «ген» и «цистрон» в настоящее время являются синонимами. • У эукариот гены, отвечающие за последовательные стадии метаболического пути, могут располагаться как рядом, так и в самых разных участках генома, на разных хромосомах. • Полицистронный механизм регуляции активности генов для эукариот не существует, и экспрессия генов, располагающихся рядом, регулируются независимо.
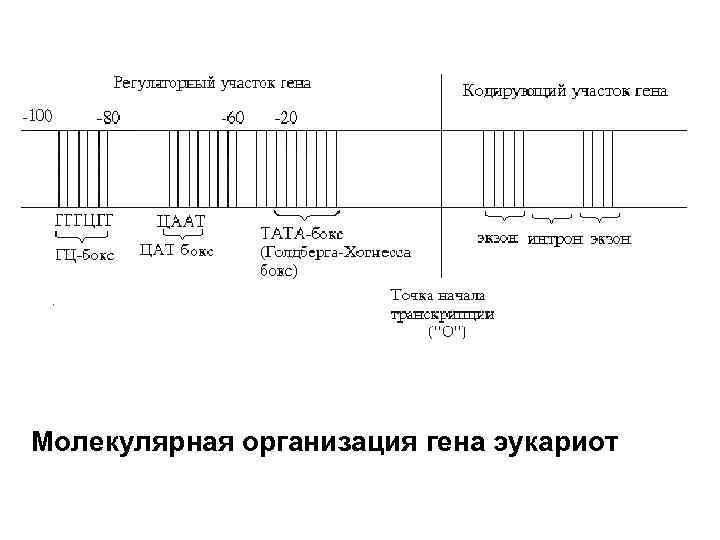
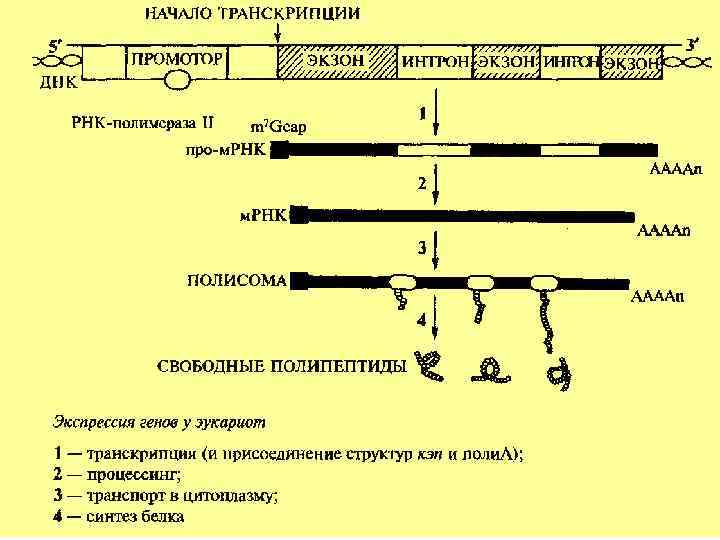
Молекулярная организация гена эукариот
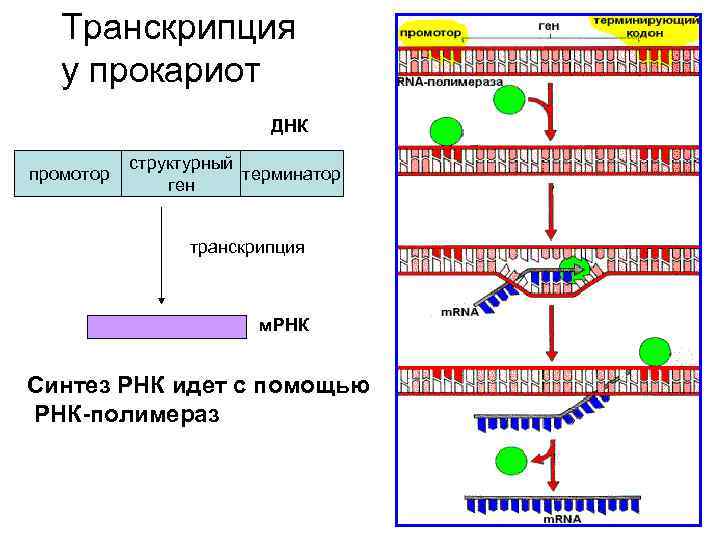
Транскрипция у прокариот ДНК промотор структурный терминатор ген транскрипция м. РНК Синтез РНК идет с помощью РНК-полимераз
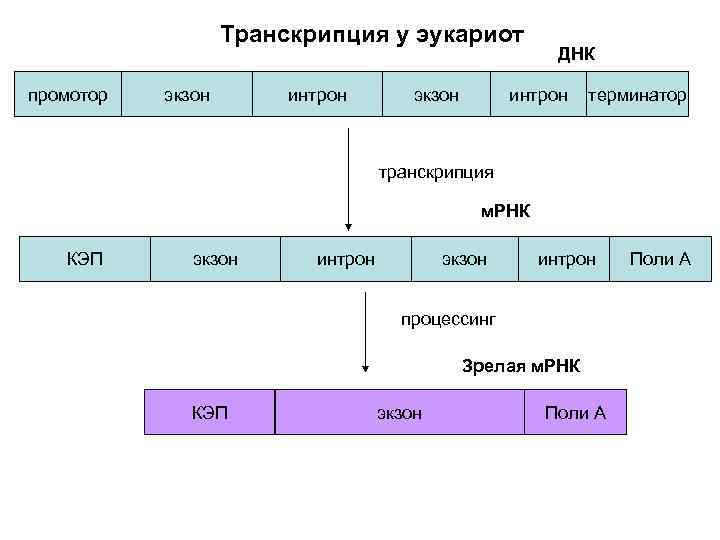
Транскрипция у эукариот промотор экзон интрон экзон ДНК интрон терминатор транскрипция м. РНК КЭП экзон интрон процессинг Зрелая м. РНК КЭП экзон Поли А

• Мутации

• Гены могут подвергаться мутациям — случайным или целенаправленным изменениям последовательности нуклеотидов в цепи ДНК. • Мутации могут приводить к изменению последовательности, а следовательно изменению биологических характеристик белка или РНК, которые, в свою очередь, могут иметь результатом общее или локальное изменённое или анормальное функционирование организма.

• не все изменения последовательности нуклеотидов приводят к изменению структуры белка (благодаря эффекту вырожденности генетического кода) • В частности, геном человека характеризуется однонуклеотидными полиморфизмами и вариациями числа копий ), такими как делеции и дупликации, которые составляют около 1 % всей нуклеотидной последовательности человека. • Однонуклеотидные полиморфизмы, в частности, определяют различные аллели одного гена.

• Мутации (от лат. mutatio. изменение) - наследуемые изменения в генотипе, не связанные с явлениями рекомбинаций. • Изменения последовательности нуклеотидов в ДНК могут быть следствием разных процессов: ошибка при репликации, выпадение участков (делеция), перемещение отдельного участка относительно другого (транслокация) и др.

Мутации изменение последовательности нуклеотидов в ДНК Генные мутации: - замены нуклеотидов - вставки (инсерции) и - выпадения (делеции) нуклеотидов со сдвигом рамки считывания - инверсии Хромосомные мутации: - изменение числа хромосом - делеции - инсерции -транслокации
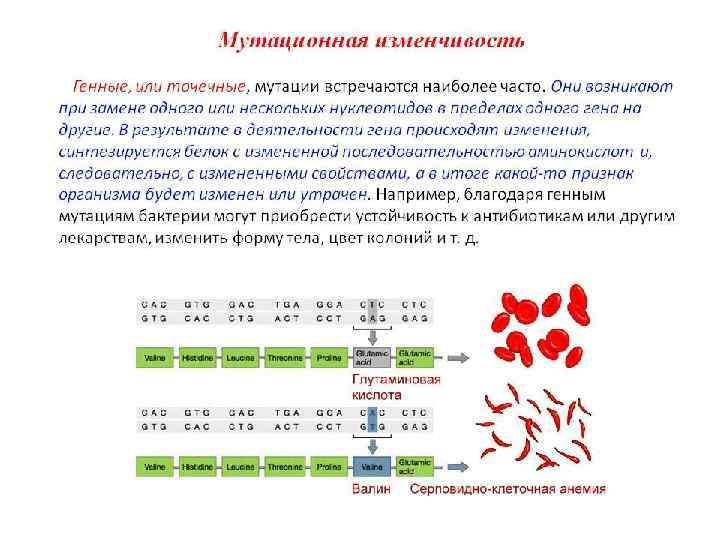
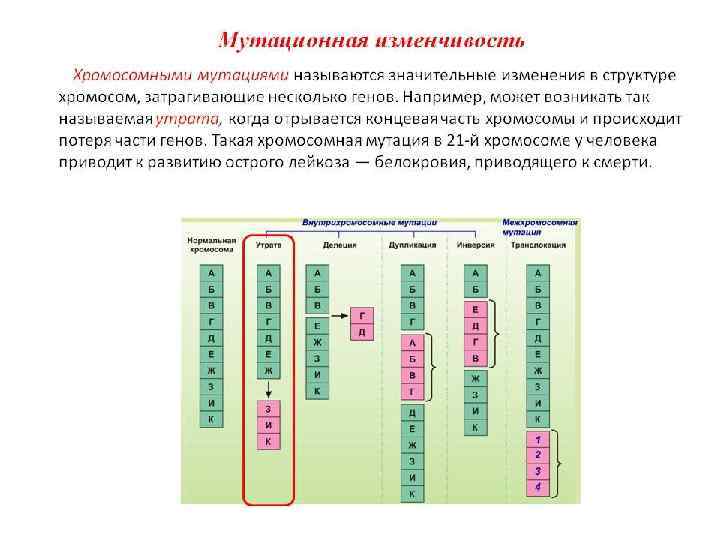

• Большинство происходящих в ДНК изменений приводит к вредным мутациям либо вызывает гибель микроорганизмов. Поэтому все клетки имеют особые механизмы реконструкции, исправления повреждений, называемые репарационными.
Генная инженерия

• В начале 70 -х годов XX века возникла генная инженерия - методы молекулярной биологии и генетики, связанные с целенаправленным конструированием новых, не существующих в природе сочетаний генов

• генная инженерия основана на извлечении из клеток какого-либо организма гена (кодирующего нужный продукт) или группы генов и соединении их со специальными молекулами ДНК, способными проникать в клетки другого организма (главным образом микроорганизмов) и размножаться в них

Генетическая инженерия (генная инженерия) • — совокупность приёмов, методов и технологий получения рекомбинантных РНК и ДНК, выделения генов из организма (клеток), осуществления манипуляций с генами и введения их в другие организмы.

• Генетическая инженерия не является наукой в широком смысле, но является инструментом биотехнологии, используя методы таких биологических наук, как молекулярная и клеточная биология, цитология, генетика, микроби ология, вирусология

• Задачи генной инженерии • Основные направления генетической модификации организмов: • – придание устойчивости к ядохимикатам (например, к определенным гербицидам); • – придание устойчивости к вредителям и болезням (например, Bt-модификация); • – повышение продуктивности (например, быстрый рост трансгенного лосося); • – придание особых качеств (например, изменение химического состава).

• Из истории генетической инженерии. • Генетическая инженерия возникла в 1972 году, в Станфордском университете, в США. • Тогда лаборатория П. Берга получила первую рекомбинатную (гибридную) ДНК или (рек. ДНК). • Она соединяла в себе фрагменты ДНК фага лямбда, кишечной палочки и обезьяньего вируса SV 40.

• Историю развития генетической инженерии можно условно разделить на три этапа: • Первый этап связан с доказательством принципиальной возможности получения рекомбинантных молекул ДНК in vitro. Эти работы касаются получения гибридов между различными плазмидами. Была доказана возможность создания рекомбинантных молекул с использованием исходных молекул ДНК из различных видов и штаммов бактерий, их жизнеспособность, стабильность и функционирование.

• Второй этап связан с началом работ по получению рекомбинантных молекул ДНК между хромосомными генами прокариот и различными плазмидами, доказательством их стабильности и жизнеспособности. • Третий этап - начало работ по включению в векторные молекулы ДНК (ДНК, используемые для переноса генов и способные встраиваться в генетический аппарат клетки-реципиента) генов эукариот, главным образом, животных.

• Методы генной инженерии преобразуют клетки бактерий, дрожжей и млекопитающих в «фабрики» для масштабного производства любого белка. • В настоящее время кишечная палочка (E. coli) стала поставщиком таких важных гормонов как инсулин и соматотропин. • Ранее инсулин получали из клеток поджелудочной железы животных, поэтому стоимость его была очень высока. Для получения 100 г кристаллического инсулина требуется 800 -1000 кг поджелудочной железы, а одна железа коровы весит 200 -250 грамм. Это делало инсулин дорогим и труднодоступным для широкого круга диабетиков.

• Соматотропин - гормон роста человека, секретируемый гипофизом. Недостаток этого гормона приводит к гипофизарной карликовости. Если вводить соматотропин в дозах 10 мг на 1 кг веса три раза в неделю, то за год ребенок, страдающий от его недостатка, может подрасти на 6 см. • Ранее его получали из трупного материала, из одного трупа: 4 - 6 мг соматотропина в пересчете на конечный фармацевтический препарат. Таким образом, доступные количества гормона были ограничены, кроме того, гормон, получаемый этим способом, был неоднороден и мог содержать медленно развивающиеся вирусы.

• Главным объектом генно-инженерного воздействия является носитель генетической информации – ДНК, • Создание новых сочетаний генов оказалось возможным благодаря принципиальному сходству строения молекул ДНК у всех видов организмов, а фактическая универсальность генетического кода делает возможной экспрессию чужеродных генов (проявление их функциональной активности) в любых видах клеток. • Важными предпосылками явились: открытие плазмид, способных к автономной репликации и переходу из одной бактериальной клетки в другую, и явления трансдукции – переноса некоторых генов бактериофагами, что позволило сформулировать представление о векторах – молекулах-переносчиках генов.
Лекция_7_строение генов.ppt