БИОХИМИЯ КРОВИ I.ppt
- Количество слайдов: 74

БИОХИМИЯ КРОВИ I А. И. Артюхина Вол. ГМУ

План 1. Функции крови 2. Эритропоэз и его регуляция 3. Особенности мембраны эритроцита 4. Особенности метаболизма эритроцита 5. Катаболизм глюкозы в эритроците (анаэробный гликолиз, ПФП) 6. Оксигенирование гемоглобина и его регуляция 7. Транспорт диоксида углерода. 8. Дезоксигенирование гемоглобина 9. Анемии и анемическая гипоксия 10. Белки плазмы крови. Белковые фракции 11. Ферменты крови. Энзимодиагностика 12. Механизм изменения активности ферментов в крови при патологических состояниях
Кровь – жидкая подвижная ткань, осуществляет связь организма с внешней средой , интеграцию метаболизма и поддержание гомеостаза.

Функции: дыхательная (перенос кислорода и углекислого газа), n трофическая ( перенос около 50 субстратов из кишечника в органы, перенос глюкозы и кетоновых тел из печени в мышцы), n коммуникативная - регуляторная (транспорт гормонов и других регуляторов метаболизма к клеткам-мишеням), n выделительная (перенос продуктов обезвреживания и катаболизма к органам выделения),

ФУНКЦИИ n защитная (антитела и фагоцитирующие лейкоциты), n гомеостатическая ( поддержание осмотического давления, водно-солевого баланса, температуры, КОС, и др. параметров), n гемостатическая (свёртывание крови для предотвращения кровопотерь).
ПЛАЗМА – кровь без форменных элементов СЫВОРОТКА – дефибринированная плазма n

Биохимия эритроцитов n Процентное содержание форменных элементов в крови (гематокрит) составляет у м 40 -54%, у ж 36 -42%, на долю эритроцитов приходится 36 -48% объёма крови.
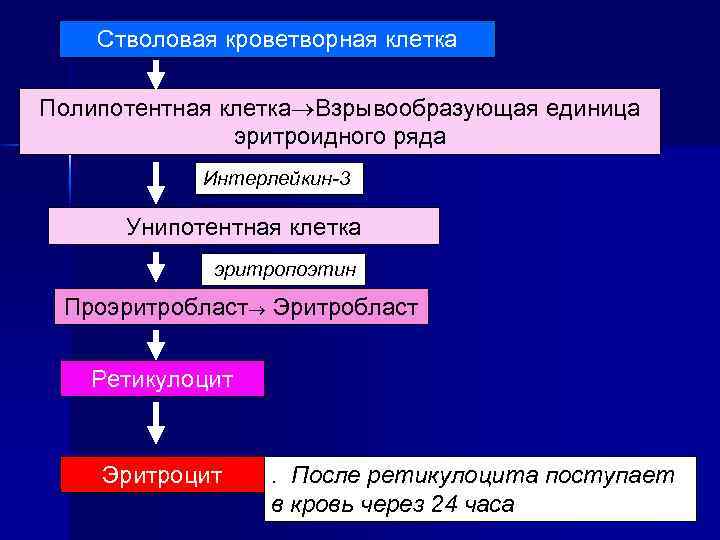
Стволовая кроветворная клетка Полипотентная клетка Взрывообразующая единица эритроидного ряда Интерлейкин-3 Унипотентная клетка эритропоэтин Проэритробласт Эритробласт Ретикулоцит Эритроцит . После ретикулоцита поступает в кровь через 24 часа

Эритропоэз регулируется цитокинами – белково-пептидными факторами, которые осуществляют коротко-дистантную регуляцию межклеточных и межсистемных взаимодействий. Действие на клетку – мишень через высокоаффинные мембранные рецепторы (обладают абсолютной специфичностью, олигомеры, каждый протомер способен связать цитокин, но с более низкой аффинностью) n
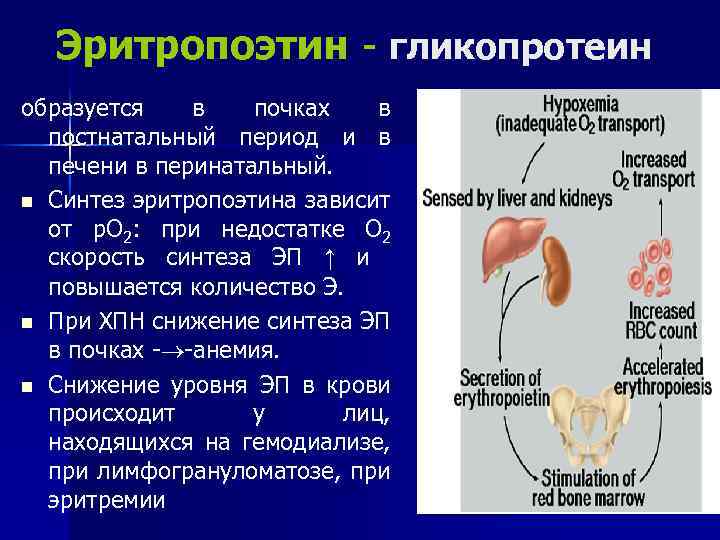
Эритропоэтин - гликопротеин образуется в почках в постнатальный период и в печени в перинатальный. n Синтез эритропоэтина зависит от р. О 2: при недостатке О 2 скорость синтеза ЭП ↑ и повышается количество Э. n При ХПН снижение синтеза ЭП в почках - -анемия. n Снижение уровня ЭП в крови происходит у лиц, находящихся на гемодиализе, при лимфогрануломатозе, при эритремии

ИНТЕРЛЕЙКИН-3 (ИЛ -3) n Гемопоэтический ростовый фактор, М. м. 15, 0 -28, 0 к. Да n Активация гена через 4 часа после стимуляции клетки и поддерживается несколько суток n Синтезирован Т-лимфоцитами и др. клетками (В-лимфоцитами, миелоидными клетками, стромальными клетками костного мозга, кератиноцитами) n Секреция подавляется циклоспорином А и глюкокортикоидами

Колониестимулирующие факторы n n n G-CSF – гранулоцитарный, Gпродуцируется мононуклеарными фагоцитами GM-CSF- гранулоцитарномакрофагальный, продуцируется эндотелиальными клетками M-CSF – моноцитарномакрофагальный продуцируется фибробластами

ИЛ-3 + ЭП n рост и дифференцировка клеток эритроидного ряда; n регуляция ранней стадии дифференцировки Влимфоцитов; n усиление секреции Ig G ИЛ-3 + ИЛ-4 + GM-CSF ростовые факторы для тучных клеток ↑ продукцию гистамина клетками гемопоэтической системы, но не влияют на клетки периферической крови ИЛ-3 + GM-CSF вызывают формирование гранул эозинофилов

Мембрана Э: n 15 белков с М. м. от 15 до 250 к. Д, 60% массы составляют гликофорин, спектрин, белок полосы3 n Гликофорин –интегральный, только в Э, к –Nконцу около 20 олигосахаридных цепей, на поверхности – групповые вещества крови ( антигены) различаются природой концевых участков олигосахаридов, входящих в структуру гликолипидов. По системе АВО детерминантными углеводами являются: n альфа-фукоза для группы крови О, n альфа-N-ацетилгалактозамин для группы А, n галактоза для группы В.

Спектрин- периферический, фибриллярный, доменный, содержит и антипараллельно расположенные цепи. С мембраной взаимодействие n 1) нековалентное, белок полосы 4. 1 образует со спектрином и актином «узловой комплекс» , который связан с цитоплазматическим доменом гликофорина n 2) -цепь спектрина + анкирин + цитоплазматический домен белка полосы 3 n Основной белок цитоскелета Э Белок полосы 3 – интегральный, переносчик ионов Cl-, HCO 3— по механизму пассивного антипорта. n
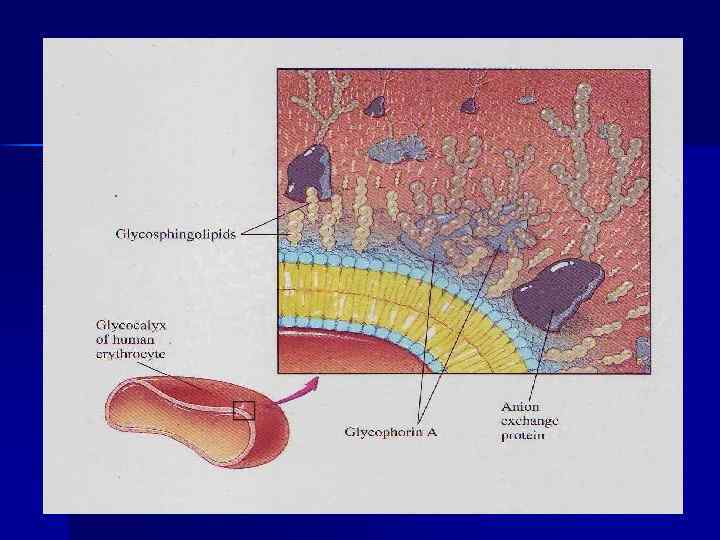
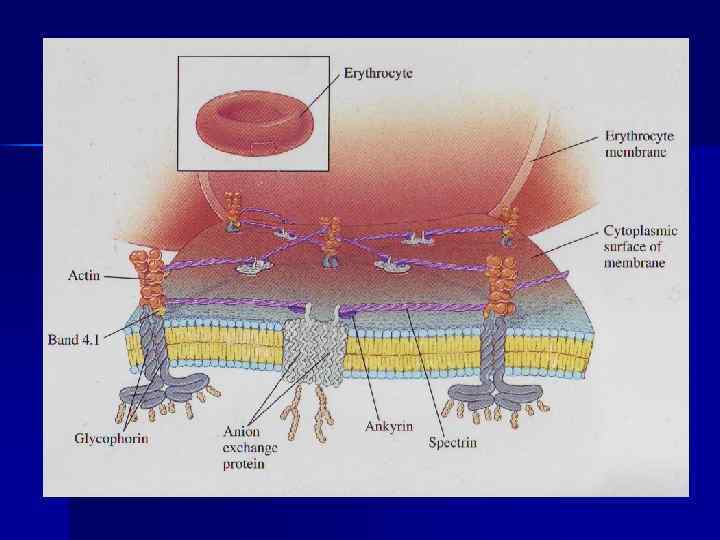

n Большинство белков Э мембраны выполняют функции транспортных систем с АТФ-азной активностью. Главный катион- К+, из анионов преобладает Сl-, НСОз n Э способен набухать или сжиматься при изменении осмотического давления плазмы крови, может гемолизироваться в гипотонической среде, при действии поверхностно-активных веществ, ядов змей, насекомых, содержащих фосфолипазу А 2, при действии сильных окислителей.

В результате дифференцировки Э теряют ядро, рибосомы, митохондрии и эндоплазматический ретикулум, поэтому метаболизм в эритроцитах упрощен и направлен на: n 1) сохранение мембраны эритроцита от перекисного окисления; n 2) предотвращения окисления иона железа Fe 2+ Нb; n 3) получение АТФ путём анаэробного гликолиза n Ферменты, осуществляющие метаболизм синтезируются на стадии созревания Э. n

Особенности метаболизма эритроцита Глюкоза – единственный питательный продукт, утилизируется 20 -30 г/сут. n Анаэробный гликолиз - на который расходуется 90% потребляемой Э глюкозы, поставщик лактата, наличие обходного пути для стадии VII: 1, 3 БФГ бисфосфоглицератмутаза 2, 3 БФГ фосфатаза 3 фосфоглицерат n ПФП - участвует 10% глюкозы. n Мощная АОС. n Протеолитические возможности Э: инактивация ангиотензина II (пролилолигопептидазой) инсулина (инсулиназой) n
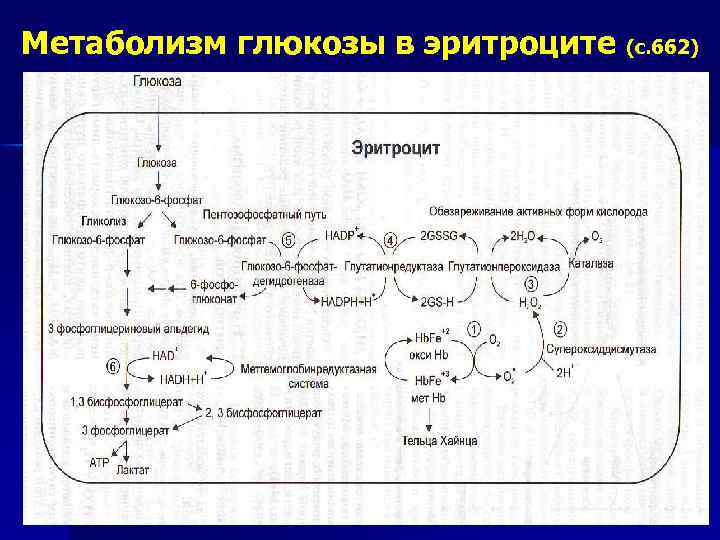
Метаболизм глюкозы в эритроците (с. 662)

Анаэробный гликолиз Единственный источник АТФ, наибольшее количество которой используется транспортными АТФ-азами для поддержания разности концентрации веществ в плазме и эритроцитах; источник НАДН, который может использоваться в качестве кофермента метгемоглобинредуктазы, катализирующей восстановление мет. Нb до Нb: Met. Hb (Fe 3+) + НАДН+Н (из гликолиза) Met. Hbредуктаза Hb(Fe 2+)+НАД++2 Н В норме мет. Hb образуется не более 0, 5% от общего количества Hb n 2, 3 ДФГК –аллостерический регулятор сродства Hb к О 2 ; n лактат выходит из Э и используется другими тканями (печенью, миокардом).

Пентозофосфатный путь окисления глюкозы источник НАДФН+Н (кофермент лутатионредуктазы). n фермент – глюкозо-6 -фосфатдегидрогеназа первый фермент пентозного цикла, важен в метаболизме эритроцитов, так как защищает от повреждения CР, окисляющими агентами. Факторы внешней среды могут модифицировать или даже полностью определять клинические проявления некоторых врожденных нарушений обмена веществ. Если активность фермента=0 – спонтанная анемия за счёт гемолиза, n активность = 10% - анемия возникает при действии факторов, повреждающих эритроцит ( лекарств –примахина, фасоли Vicia faba и т. д. ), n активность 30% и выше – нарушений нет. n

Играют роль взаимодействия с другими ферментами: при нормальной активности глутатионредуктазы существенный дефицит Гл-6 -ф ДГ не вызывает заболевания. n Дефицит данного фермента предохраняет от малярии (быстрый распад зараженных плазмодием эритроцитов). n Число людей с нерезко выраженным дефицитом активности Гл-6 -ф. ДГ составляет около 100 млн. n

n Постоянным источником АФК в Э является неферментативное окисление Hb в Met. Hb, поэтому в Э существует мощная АОС : СОД, каталаза, глутатионпероксидаза и глутатионредуктаза, предотвращающая перекисную деструкцию мембраны Э. При недостаточной активности ферментов обезвреживания АФК между молекулами метгемоглобина образуются дисульфидные связи , что приводит к их агрегации (тельца Хайнца).

Зрелые эритроциты имеют продолжительность жизни 110 -120 дней, n разрушение в клетках РЭС селезёнки, костного мозга, печени. n

Гемоглобин n Первичная структура Hb A 0 2α 2β Вторичная структура – 70% -- α спираль, 30% - аморфные участки n
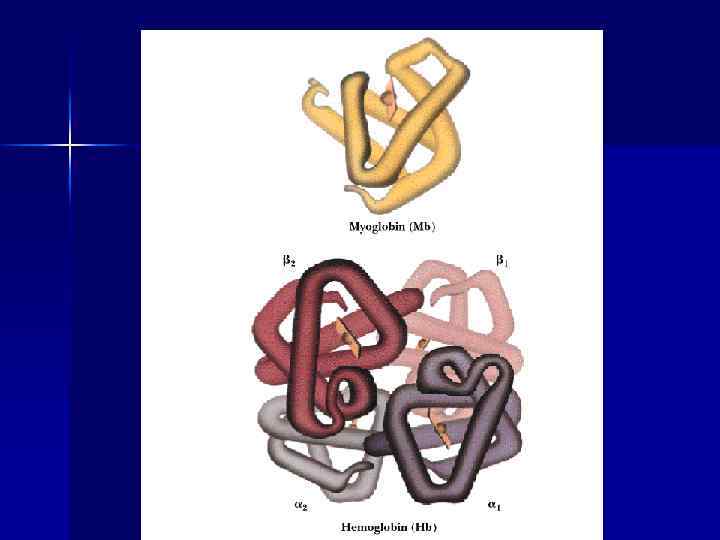
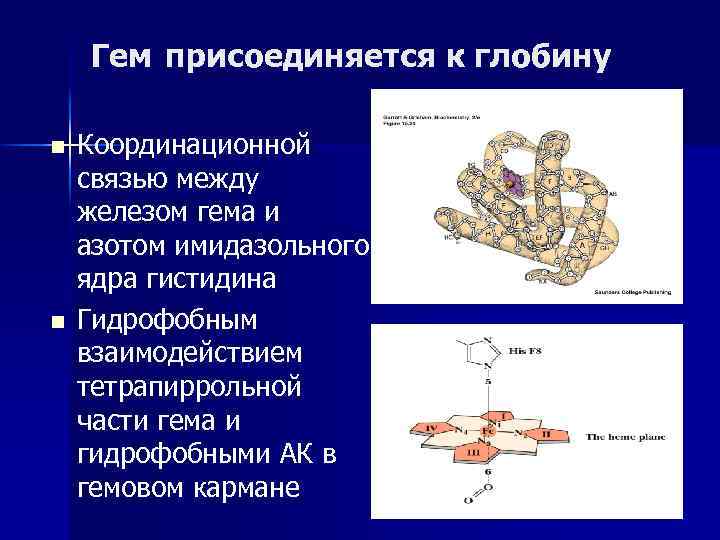
Гем присоединяется к глобину n n Координационной связью между железом гема и азотом имидазольного ядра гистидина Гидрофобным взаимодействием тетрапиррольной части гема и гидрофобными АК в гемовом кармане
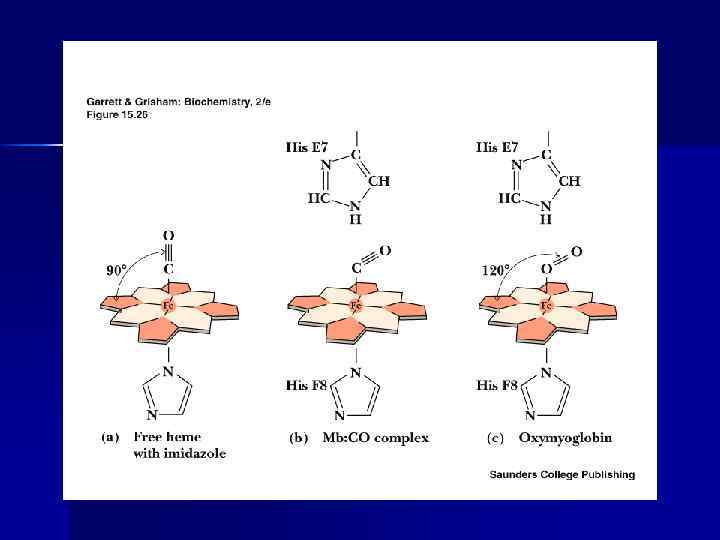
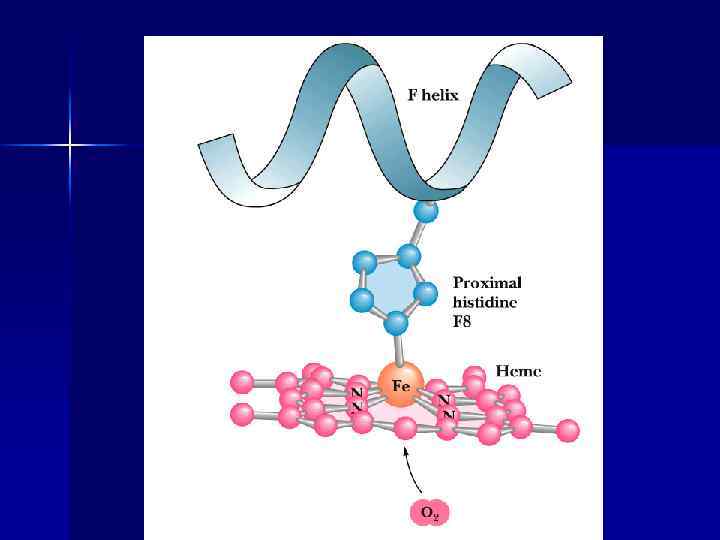

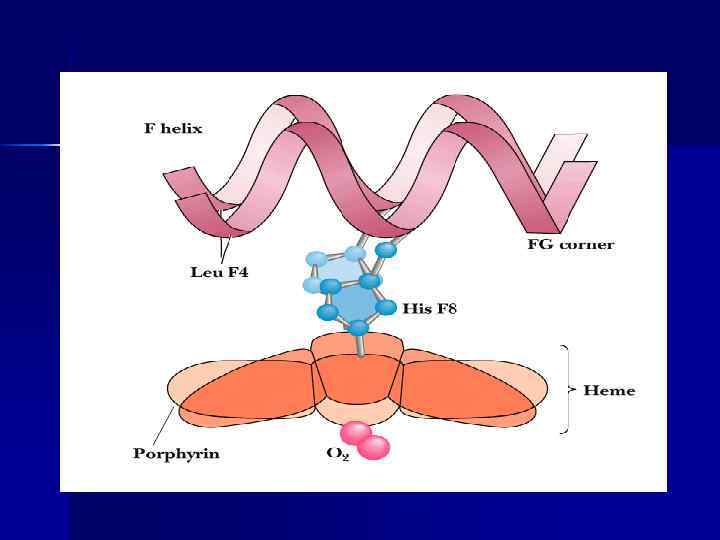

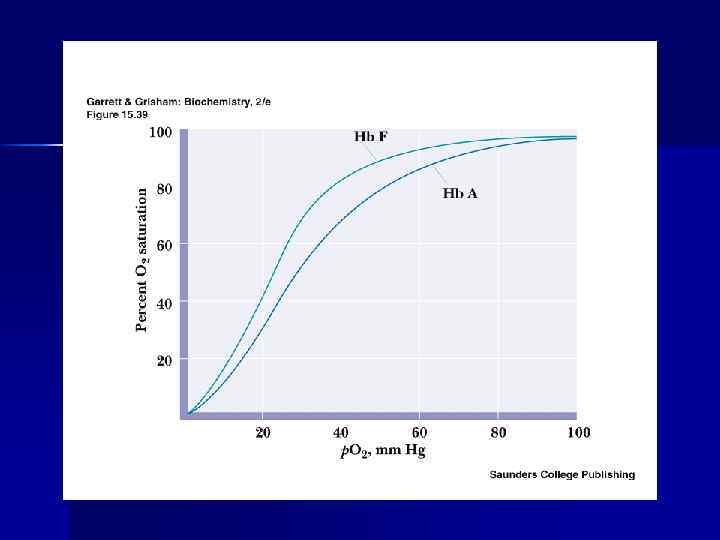
Оксигенирование гемоглобина n n Оксигенирование гемоглобина в лёгких зависит от парциального давления и наличия кооперативного эффекта Кооперативный эффект – увеличение сродства каждого последующего протомера Нb к О 2 вследствие конформационных изменений
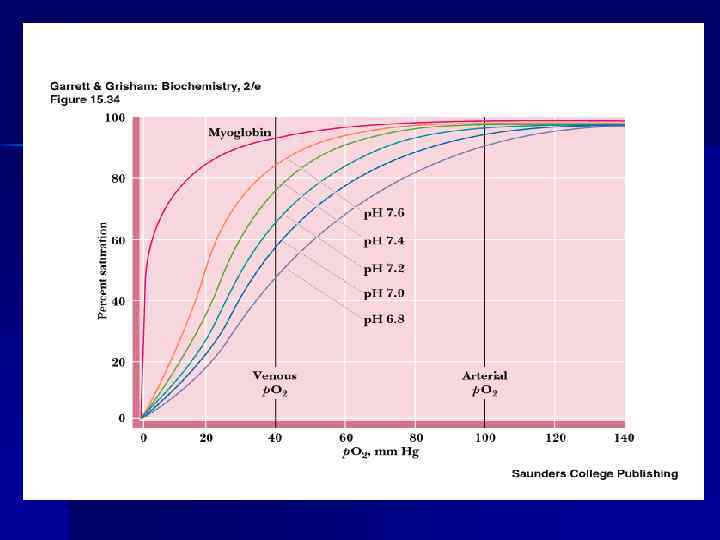
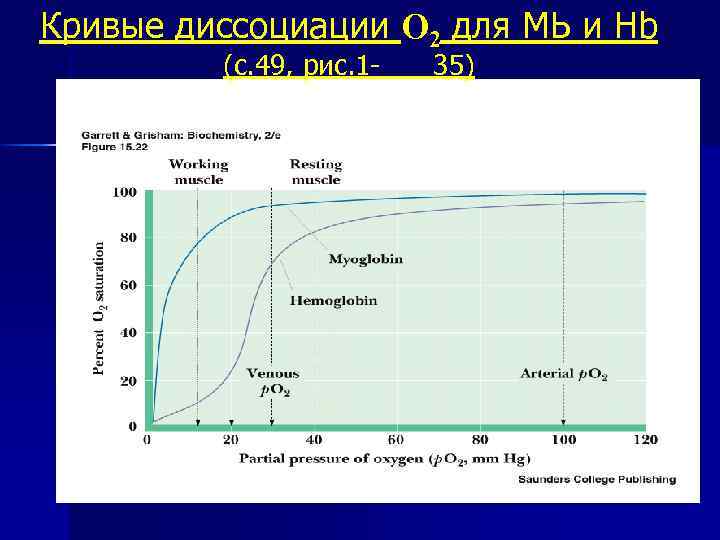
Кривые диссоциации О 2 для MЬ и Hb (с. 49, рис. 1 - 35)

Аллостерическими регуляторами сродства кислорода к гемоглобину выступают диоксид углерода и протон водорода (эффект Бора) и 2, 3 - ДФГ понижают сродство гемоглобина к кислороду. Эффект Бора: n ↑ СО 2 n ↑ Н+ n ↑ t 0 n } понижают сродство Нb к О 2
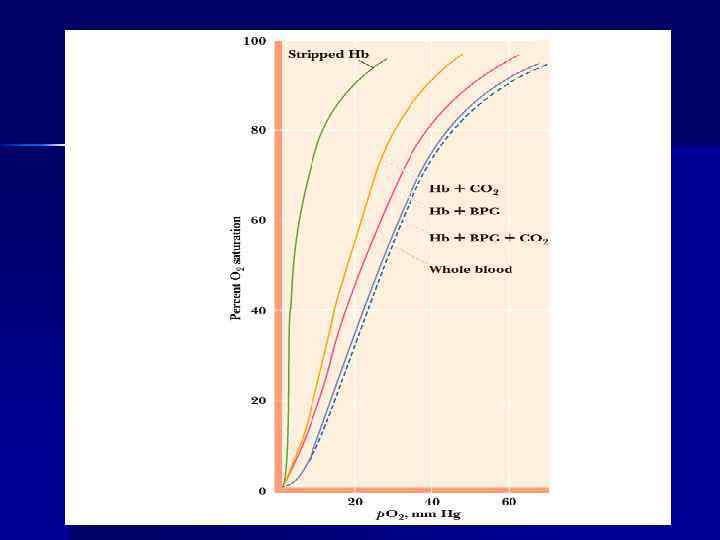
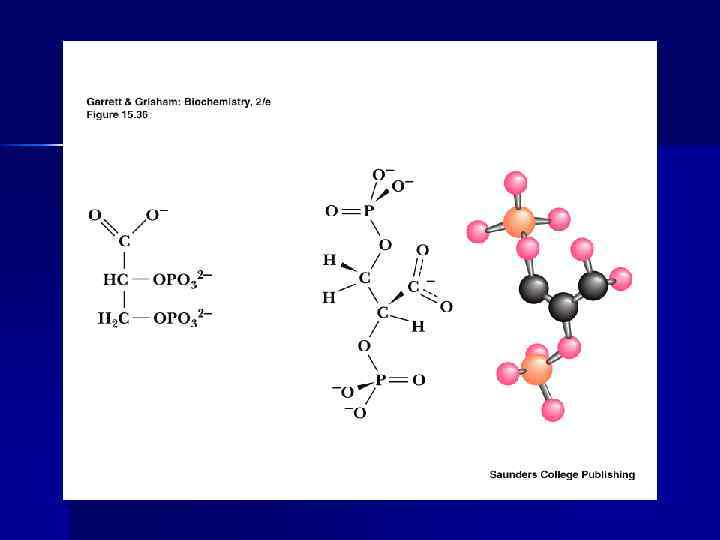

Состав гемоглобинов взрослого человека Фракция n n n n Hb A 0 Hb A 2 Hb F Hb A 1 n Hb A 1 b Hb A 1 с Цепи Содержание % 2α 2 β > 90 2 α 2δ < 1, 5 2 α 2γ < 1, 0 2α(2β фруктозо-1, 6 - дифосфат) <1, 0 2α(2β глюкозо-6 - фосфат) <1, 0 2α(2β фруктоза) <1, 0 В фетальном гемоглобине вместо β-цепей содержатся γ-цепи, имеющие меньше положительных зарядов в месте связывания 2, 3 ДФГ. Поэтому сродство фетального гемоглобина к кислороду выше.

ТРАНСПОРТ ДИОКСИДА УГЛЕРОДА n n n Небольшие количества СО 2 переносятся кровью в растворённом виде Около 75% транспортируется в виде НСОз Около 10 -15 % переносит Hb за счёт образования кислотно-амидных связей с аминогруппами лизина и аргинина

Дезоксигенирование Hb n n Разница р. О 2 в артериальной крови и в работающей мышце (95 мм рт. и 20 мм рт. ст. ) В форме НЬ(О 2)4 - связь О 2 с гемоглобином примерно в 300 раз прочнее, чем в молекуле НЬО 2 Увеличение содержания не полностью насыщенных кислородом молекул Hb Образование СО 2, который превращается в угольную кислоту, диссоциирующую с образованием протона и НСОз: n Протонирование некоторых кислотных групп пептидных цепей гемоглобина и снижение его сродства к О 2 n Присоединения СО 2 к некоторым незаряженным аминогруппам Hb Карбгемоглобин: 2, 3 -БФГ взаимодействует с молекулами гемоглобина, лишенными кислорода, и сдвигает равновесие вправо •
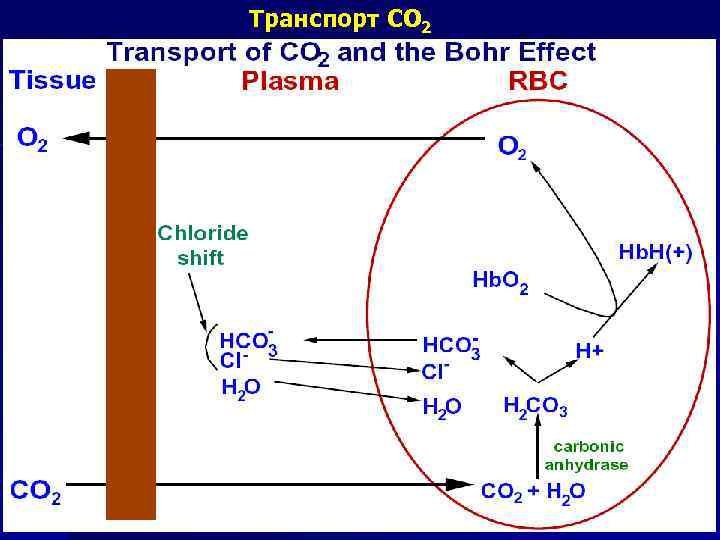
Транспорт СО 2

НАРУШЕНИЕ ДЫХАТЕЛЬНОЙ ФУНКЦИИ Э СО (угарный газ) имеет сродство к Fe 2+ Hb в 300 раз > чем сродство О 2 У здорового человека доля СО менее 1%, при курении ↑ до 10 % Помощь – повысить парциальное давление О 2 n Вещества, способные окислять Fe 2+ гема: оксид азота (NO), нитриты, ароматические и нитросоединения Помощь – введение восстановителей (vit. C). n Наследственные нарушения – гемоглобинопатии, дефицит ферментов гликолиза и ферментных звеньев АО защиты, недостаток цитхрома b 5 ↑ Met Hb n

Гемоглобинопатии группа наследственных заболеваний, обусловленных наличием в эритроцитах аномальных гемоглобинов либо угнетением синтеза полипептидных цепей нормальных гемоглобинов Классификация

Серповидноклеточная анемия n Замена в 6 положении с Nконца β-цепи Глу на Вал меняет физико-химические свойства Hb: дезоксигемоглобины теряют растворимость, выпадают в осадок и изменяют форму клетки, которая напоминает серп.

Hb при серповидноклеточной анемии

Анемия- патологическое состояние, обусловленное уменьшением содержания Hb или количества Э в единице объёма крови или нарушением их функций и в связи с этим ведущее к развитию кислородного голодания тканей. Классификация: I Вследствие кровопотерь (постгеморрагические); II Вследствие нарушенного кровообразования (железодефицитные, В-12 (фолиево)дефицитные состояния, белковое голодание); III Вследствие повышенного кроворазрушения ( гемолитические ) – гемоглобинопатии, анемии, возникающие в результате внутриэритроцитарных энзимопатий при дефектах Гл-6 ф ДГ, пируваткиназы и др. ферментов. Cлайды красного костного мозга: левый – апластическая анемия, правый – почти вернулся к норме.
Анемические гипоксии Анемии любого генеза приводят к гемическому типу гипоксии, биохимические последствия этого: n -снижение синтеза АТФ аэробным путём; n - ингибирование окислительных процессов высокой концентрацией НАДН+Н n - усиление СРО, которое приводит к гибели клеток.

Белки плазмы крови Общий белок – 64 -83 г/л n Диагностическое значение определения (рефрактометрия, биуретовая реакция) общего белка: повышение свыше 90 г/л – гиперпротеинемия – результат гипериммуноглобулинемии либо поликлональной или моноклональной гаммапатии. n Псевдогиперпротеинемия; in vivo – при выраженной гипогидратации; in vitro – при высушивании пробы. .

Гипопротеинемия – снижение ниже 60 г/л связано с 1) потерей белка (при гастроэнтеропатиях, острых ожогах, нефротическом синдроме) или со 2) снижением синтеза белка (при тяжелой белковой недостаточности, хронических заболеваниях печени, синдроме нарушенного всасывания, агаммаглобулинемии). n Уровень общего белка повышен при венозном стазе; снижен при беременности, при разведении крови, в положении лёжа.

Белковые фракции В сыворотке крови можно выявить методом электрофореза на бумаге – 5 фракций, в ПААГе – 12 -19 фракций, методом двухмерного электрофореза – более 300 фракций. n При комплексной оценке изменений белковых фракций принято выделять определённый для ряда патологических состояний тип протеинограммы ( по А. А. Покровскому, 1969) n
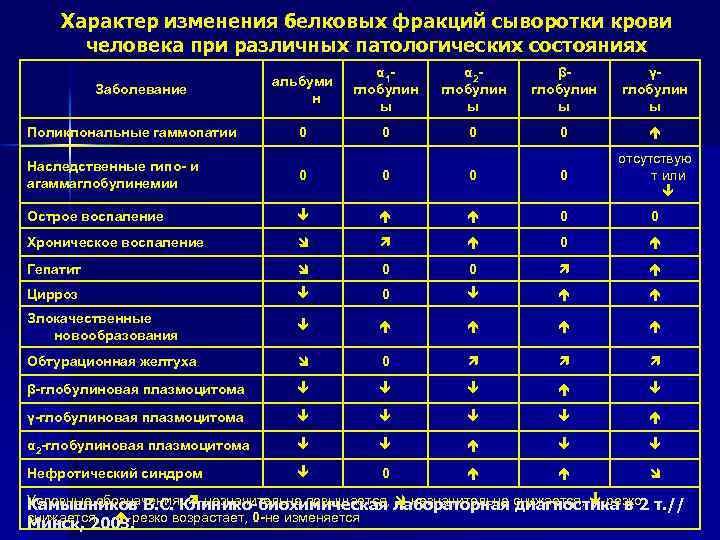
Характер изменения белковых фракций сыворотки крови человека при различных патологических состояниях Заболевание Поликлональные гаммопатии альбуми н α 1 глобулин ы α 2 глобулин ы βглобулин ы γглобулин ы 0 0 Наследственные гипо- и агаммаглобулинемии 0 0 отсутствую т или Острое воспаление 0 0 Хроническое воспаление 0 Гепатит 0 0 Цирроз 0 Злокачественные новообразования Обтурационная желтуха 0 β-глобулиновая плазмоцитома γ-глобулиновая плазмоцитома α 2 -глобулиновая плазмоцитома Нефротический синдром 0 Условные обозначения: -незначительно повышается, лабораторная снижается, -резко т. // Камышников В. С. Клинико-биохимическая -незначительно диагностика в 2 снижается, -резко возрастает, 0 -не изменяется Минск, 2003.
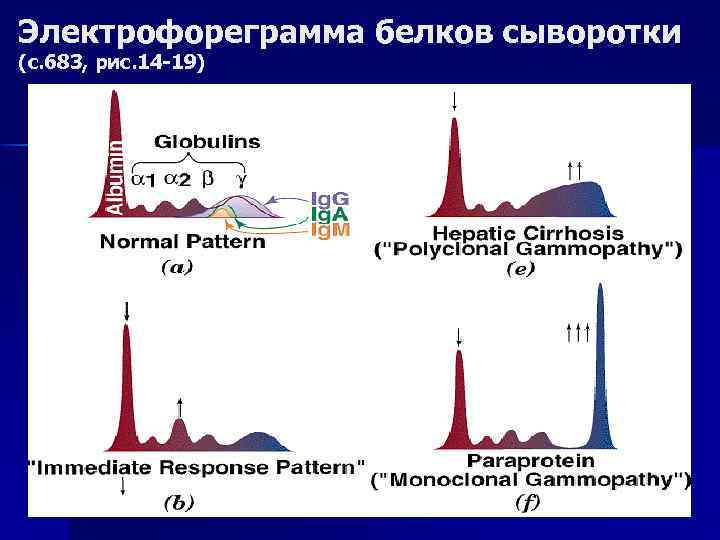
Электрофореграмма белков сыворотки (с. 683, рис. 14 -19) Кривые диссоциации О 2 для MЬ и Hb ) (с. 49, рис. 1 -35)
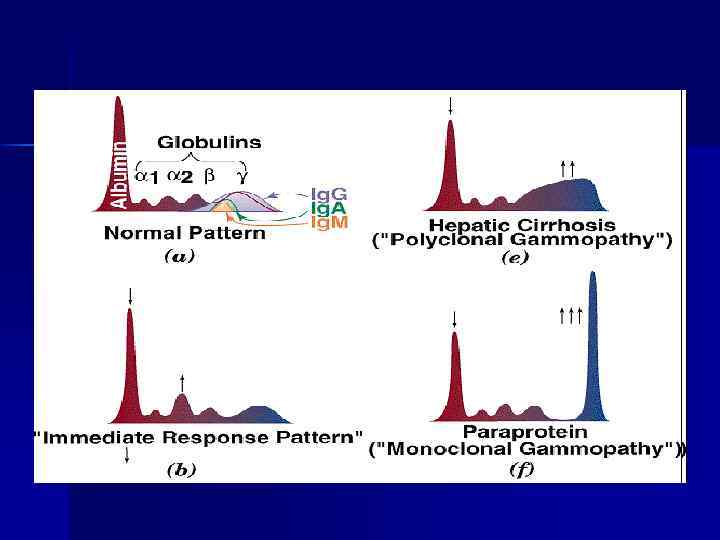
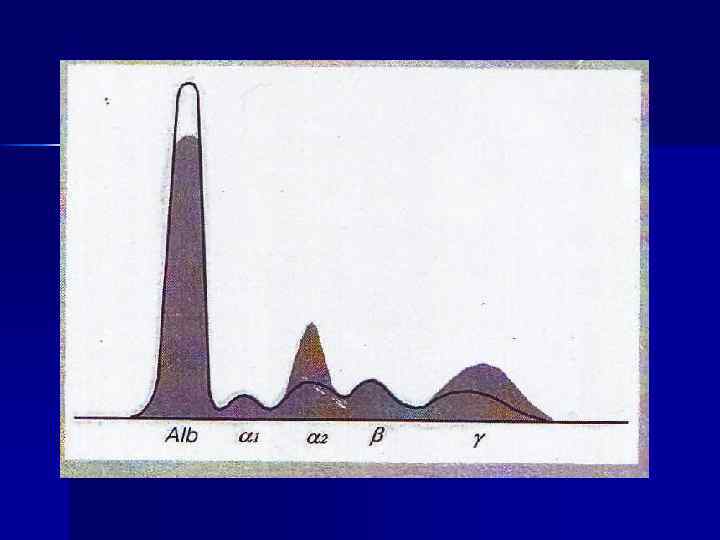
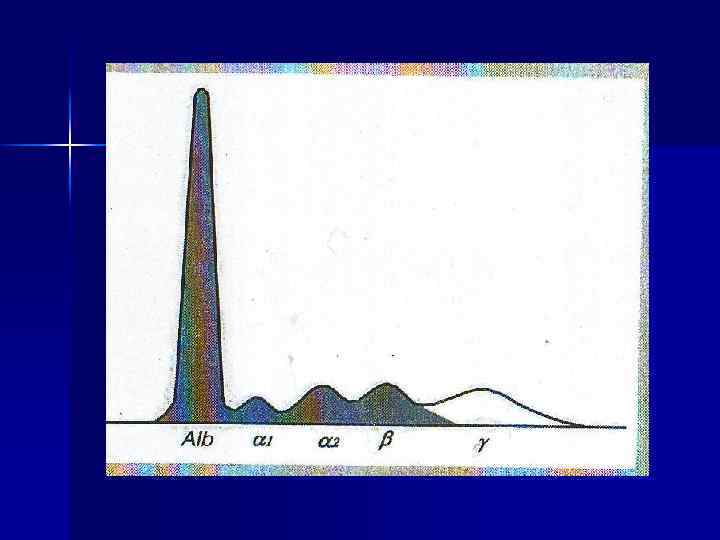


Ферменты крови Энзимодиагностика ферменты секреторные (ферменты свёртывающей системы крови; ХЭ), n экскреторные (ЛАП, ЩФ и др. ) n индикаторные = органоспецифические (ЛДГ, Ас. АТ, Ал. АТ и др. ) Изоферменты-олигомеры, генетически детерминированные различия п/п цепей Изоформы ферментов или изоферментов результат посттрансляционной модификации n
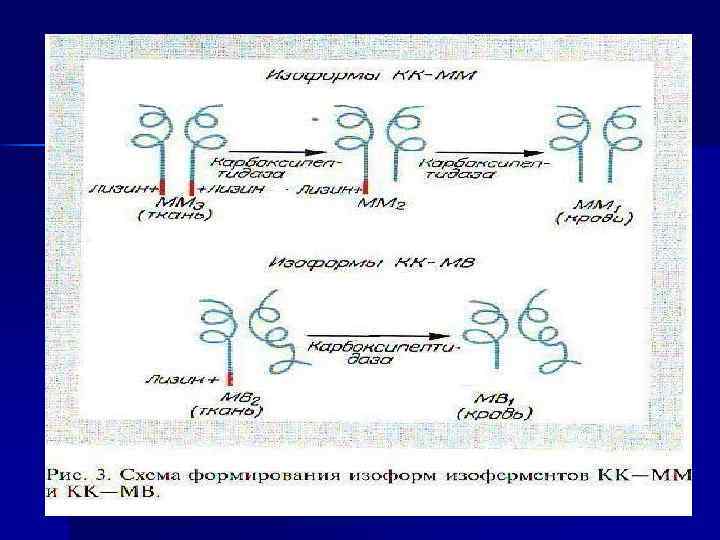
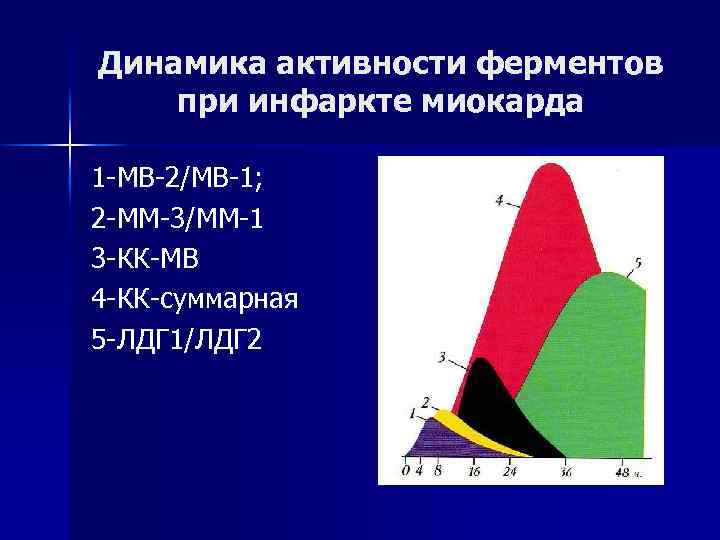
Динамика активности ферментов при инфаркте миокарда 1 -МВ-2/МВ-1; 2 -ММ-3/ММ-1 3 -КК-МВ 4 -КК-суммарная 5 -ЛДГ 1/ЛДГ 2

Механизмы изменения активности ферментов в крови повышение активности Повышение синтеза n Повышение проницаемости мембран n Некроз клеток n Понижение выведения n ЩФ (рахит) n КК (прогрессирующая мышечная дистрофия) n Ас. АТ, Альдолаза, КК n ЩФ, ЛАП (закупорка желчных путей) n

понижение активности n Уменьшение числа n клеток, секретирующих фермент ХЭ (цирроз печени), пепсиноген (гастроэктомия) n Избирательная недостаточность синтеза n Церулоплазмин (болезнь Вильсона), ЩФ (гипофосфатазия) n Усиление выделения фермента n Церулоплазмин (нефроз) n Торможение активности фермента n Трипсин (под влиянием антитрипсина)

Механизмы гиперферментемии при патологических состояниях n n Выход ферментов в кровеносное русло из повреждённых участков органов на фоне усиленного биосинтеза энзимов ( выход ферментов из пораженных тканей и снижение их содержания в клетке стимулирует по принципу обратной связи синтез). Увеличение каталитической активности ферментов как непосредственно в поврежденном органе так и при поступлении их в кровеносное русло.

Содержание фермента в плазме крови зависит от: а) скорости высвобождения из клеток, которая определяется скоростью повреждения клетки, n б) степени повреждения клетки или уровня пролиферации или индукции биосинтеза энзима, n в) скорости клиренса фермента из плазмы крови. n

Факторы, определяющие скорость высвобождения ферментов из повреждённых тканей: Концентрационный градиент – ферменты с более высокими концентрационными градиентами быстрее уходят из клетки, чем энзимы с меньшими градиентами. ЛДГ – содержание в гепатоцитах в 3000 раз выше, чем вне клеток, а в эритроцитах –только в 200 раз. Отношение внутриклеточной активности к внеклеточной для ферментов печени: 50000: 1 –сорбитол. ДГ, 20000: 1 –алкоголь. ДГ, 10000: 1 для Ас. АТ и Ал. АТ. n Размер и мол. масса : более мелкие молекулы диффундируют с большими скоростями, чем крупные; с меньшей относительной мол. Массой высвобождаются на ранней стадии повреждения. n Внутриклеточная локализация ферментов: наиболее легко высвобождаются локализованные в цитозоле клетки Быстрое повреждение относительно небольшого числа клеток (вирусный гепатит) может приводить к очень значительному повышению уровней ферментов в крови, которое понижается по мере выздоровления. Наоборот, при развившемся циррозе степень поражения печени может быть значительно больше, но скорость активного повреждения клеток часто низкая и содержание ферментов в крови бывает лишь незначительно повышено или даже остаётся в пределах нормы. n

Неспецифические причины повышения уровня ферментов в крови Физиологические - возраст, беременность, n Индуцирование ферментов лекарственными средствами, n Обусловленное артефактами (гемолиз и др. ), n Умеренная физическая нагрузка или в/м инъекция большого объёма жидкости могут приводить к повышению содержания в плазме ферментов мышц (КК). Вследствие значительной межиндивидуальной вариации порог решения при определении ферментов примерно на 50% выше верхнего референтного предела. n

n Период полужизни ферментов в сыворотке крови: ХЭ-10 дней, ЩФ-3 -7 дней, ГДГ – 18 час, амилаза – 3 -6 час. Механизм удаления из плазмы ферментов: большинства – неизвестны, n - экскреция с мочой и желчью только с маленькой мол. массо ( амилаза – 45000), у большинства мол. масса выше 65000, n исследования Wilkinson и сотр. (1976) : первая фаза – 2 часачасть ферментов из кровеносного русла после их выведения поглощается клетками РЭС; вторая фаза – 7 часов- внутрисосудистое разрушение ферментов, а также их деградация в тканях; третья фаза спустя 10 часов – активность ферментов в сыворотке остаётся на постоянном уровне, близком к нормальному.

Для достоверности лабораторной диагностики выделяют понятия: норма, диагностически значимый уровень (порог принятия клинического решения) и «серая зона» . Величина активности фермента выше верхней границы нормы, но ниже диагностически значимого уровня – серая зона n Если биохимический маркёр достигает диагностически значимого уровня, то сомнений в лабораторном диагнозе нет. Если биохимический показатель находится в « серой зоне» , то он отражает достоверное повышение активности ферментов, изоферментов, но этого повышения оказывается недостаточно для того, чтобы поставить диагноз только на их основании. Интервал значений « серой зоны» для каждого фермента свой. n


Общие принципы определения активности ферментов по скорости накопления продуктов ферментативной реакции, n по скорости убыли субстрата, n в модельных системах , напр. СОД по степени торможения окисления кверцетина. n


СПАСИБО ЗА ВНИМАНИЕ
БИОХИМИЯ КРОВИ I.ppt