
Биохимия крови - 1

Внутренняя среда организма формируется совокупностью биологических жидкостей (кровь, лимфа, тканевая жидкость), омывающих клетки и структуры тканей. Эти жидкости функционально тесно взаимосвязаны, они постоянно обмениваются между собой клетками и молекулами.
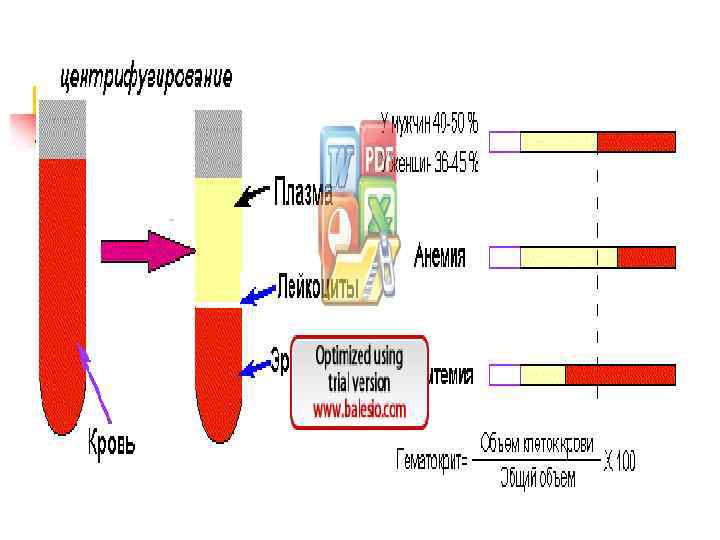

Химический состав плазмы

Функции крови n n 1. 2. Дыхательная -транспорт кислорода от легких к тканям и CO 2 от тканей к легким Выделительная - транспорт конечных продуктов метаболизма к органам выделения (почкам, легким, коже, потовым железам, кишечнику) для удаления. Защитная (иммунитет, гемостаз и др. ) Транспортная Трофическая - транспорт субстратов (поступающих с пищей и метаболитов), обеспечивающих основные жизненные потребности клетки Регуляторная (КОС, водно-электролитный баланс, t°, метаболизма – транспорт БАВ и др. ).

Химический состав крови Большую часть этих функций выполняют компоненты плазмы крови. n Плазма крови состоит на 90 -93% из воды и 10 -7%. сухого остатка – белки, углеводы, липиды, , органич. метаболиты и электролиты n Сухой остаток на 6, 6 -8, 5% состоит из белков плазмы крови и 1, 5 -3, 5% - органических метаболитов (углеводы, липиды, азотосодержащие продукты) и электролитов (Na+, K+, Ca 2+ , Cl-, HCO 3 - и др. ). n Водный и электролитный состав плазмы очень похож на состав др. внеклеточных биологических жидкостей. n Лабораторный мониторинг уровней Na+, K+, Са 2+, Cl-, HCO 3 - и р. Н крови важны для оценки состояния метаболизма.

Характеристика белков плазмы крови 1. 2. 3. 4. 5. 6. 7. 8. содержатся в плазме крови синтезируются в печени или РЭС (реже в специализированных тканях) проявляют основную функцию в пределах сосудистой системы секретируются в кровь, а не попадают в результате повреждения тканей находятся в плазме в концентрации большей, чем в других биологических жидкостях проявляют генетический полиморфизм, имеют вариантные формы, не связанные с тканевым происхождением не являются продуктами катаболизма в плазме, но могут быть продуктами ограниченного протеолиза имеют большее время биологического полураспада в плазме, чем время транспорта по крови.

Состав белков плазмы крови n n В плазме обнаружено более 100 разных белков соответствующих этим критериям, содержание которых колеблется в широких пределах Изучение их функций, содержания, состава при патологии — одна из важных задач клинической биохимии. Уровень ~10 белков составляющих 90 %, и называемых главными достигает высоких значений (альбумин – 40 г/л). Остальные 10 % минорные, следовые белки. приходится свыше 100 различных белков, содержание которых может быть в пределах 50 – 200 мкг/л. Это

Функциональная классификация Б плазмы n Транспортные - специфический (трансферин, транскортин) - неспецифический – альбумин (ЖК, токсины и др. ) n Регуляторные (альбумин) - КОС (буферные свойства) - онкотическое давление (1 гр альбумин связывает 17 мл воды) - метаболизма и функций (связывание БАВ) n Резервные (альбумин) - резерв АК 50% общего кол-ва альбумина - резерв воды, электролитов, БАВ и др. n Защитные - гемостаз - антиинфекционная защита (Ig, комплемент, лизоцим, интерферон) - детоксикация - связывание и транспорт токсинов (альбумин)
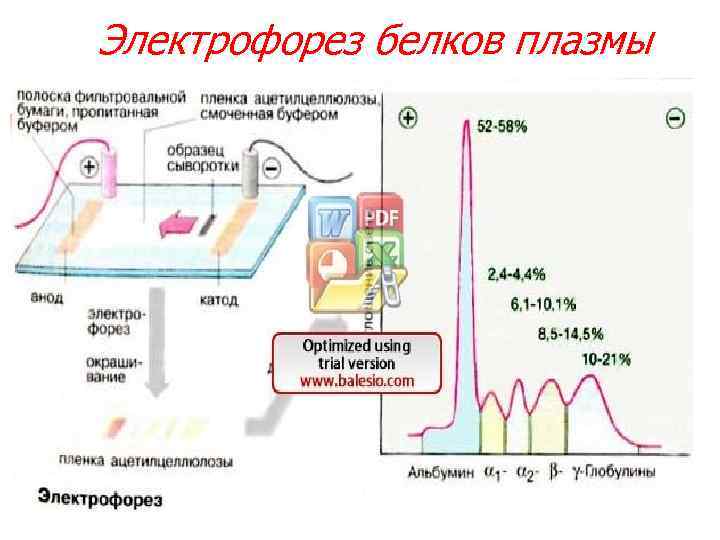
Электрофорез белков плазмы

Остаточный азот Все азотсодержащие вещества плазмы образуют общий пул азота, состоящий из: n n Азота белкового – осаждаемого кислотами Азота небелкового (остаточного) (ОА), представленного конечными продуктами обмена АК, ФЛ, Азот. Осн, Амины и др. азотсодержащих в-в, которые остаются после осаждения белков

Состав ОА n n n Мочевина - 50% (главный компонент) АК - 25% (~ 10% ГЛУ и ГЛН) Ураты - 8% Креатинин - 2. 5% NH 3 и индикан - 0. 5% билирубин, нуклеотиды, биогенные амины, метаболиты АК, АО, холин, олигопептиды и др
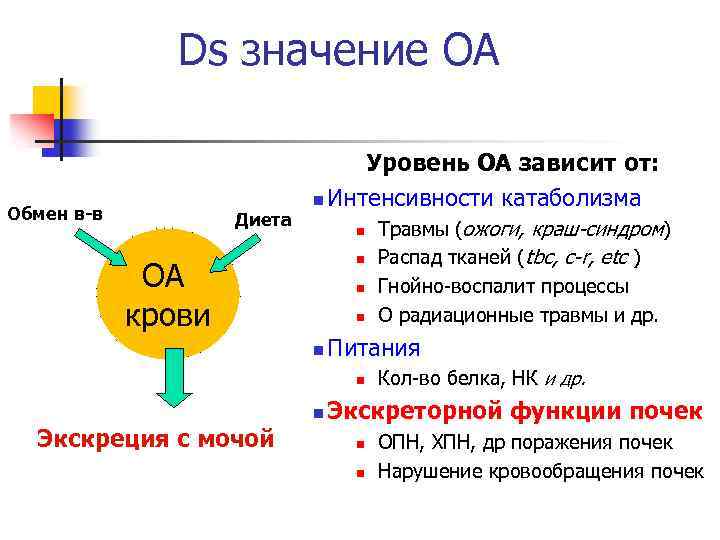
Ds значение ОА Обмен в-в Диета Уровень ОА зависит от: n Интенсивности катаболизма n n ОА крови n n n Питания n n Экскреция с мочой Травмы (ожоги, краш-синдром) Распад тканей (tbc, c-r, etc ) Гнойно-воспалит процессы О радиационные травмы и др. Кол-во белка, НК и др. Экскреторной функции почек n n ОПН, ХПН, др поражения почек Нарушение кровообращения почек

Азотемия - повышение уровня ОА в крови Ретенционная – задержка компонентов ОА в организме из-за нарушения экскреторной функции почек n n n Почечная азот мочевины составляет 90% ОА крови (норма 50%) (ОПН, ХПН – отравления, травмы, гломерулонефриты, пиелонефриты и др поражения почек) Внепочечная азотемия возникает при снижения почечного кровотока из-за недостаточности кровообращения, снижения АД (шок, коллапс, большая кровопотеря) Продукционная – увеличение продукции ОА за счет катаболизма n Комбинированная n

Общие понятия КОС – система гомеостаза р. Н внутри- и внеклеточной среды организма. Единицы измерения : р. Н = -lg [H+], сдвиг р. Н: на 1 ед соответствует 10 кратному изменению [H+] на 2 ед соответствует 100 кратному изменению [H+] nр. Н внутри клеток р. Нi ~ 6. 9 – 7. 0 nр. Н вне клеток р. НО =7. 40± 0. 04 [H+] ~ 40 ± 0. 5 н. М/л + n. Кислоты – доноры H + n. Основания – акцепторы H n. Щелочи - доноры ОН n. Буфер система состоит из слабой кислоты и ее соли, образованной сильным основанием, стабилизирует р. Н,

р. Н – производное метаболизма 1. 2. n n За сутки организм hs образует 50 -100 м. М [Н+] на 15 -20 л ВКЖ. Весь метаболизм представлен преимущественно обменом кислот (Г 6 Ф, ЖК, АК и др. ): Распад 100 г Б дает ~ 30 м. М Н 2 SO 4 и 100 м. М Н 2 РО 4 Распад 100 г Л дает ~ 17 м. М Н 2 РО 4 постоянно образуется ПВК, лактат, ацетат и др. накопление оснований идет значительно меньше: ОН-, NH 3, основные АК, креатинин и др, которые вместе с буферами стабилизируют р. Н

Стабильный р. Н - необходимое условие метаболизма n n Изменение р. Н приводит к изменению: заряда и функции белков (ферментов, каналов, рецепторов и др. ), что обуславливает: р. Н зависимость всех б/х реакций и многих физиологических процессов в организме Наличие мощной гомеостатической системы стабилизации р. Н
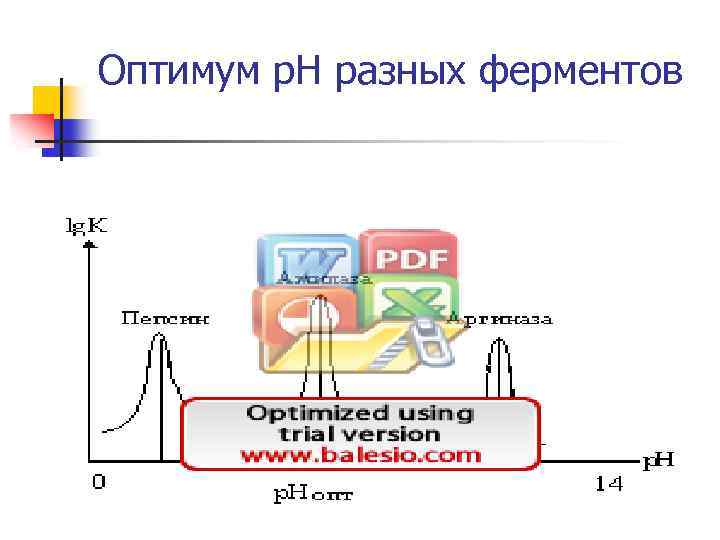
Оптимум р. Н разных ферментов

Принципы организации КОС n Изоосмолярность – осм. давление МКЖ 310 ос. М/л - const любые изменения должны поддерживать эту константу n Электронейтральность – n Постоянство р. Н равное кол-во катионов и анионов (по 155 м. М/л)

Механизмы регуляции КОС 1. Физико-химические – действуют в автоматическом режиме и представлены: + или др. иона из n разбавлением т. е. выходом Н одного компартмента в др. (из клетки в МКЖ или наоборот) n активность буферных систем (см типы, мех-мы действия БС 2. Физиологические – функция экскреторных органов (выделение или задержка Н+ или др. иона ) – легкие, почки, ЖКТ и др.

Классификация нарушений КОС n 1. 2. 3. 4. 1. 2. р. НО =7. 40± 0. 04 р. Н = 7. 35 и ниже – ацидоз р. Н = 7. 45 и выше – алкалоз По этиологии: Респираторный (дыхательный, газовый) Метаболический Выделительный Смешанный По степени компенсации: Компенсированный Декомпенсированный (выраженное истощение буферных систем и сдвиг значений р. Н)
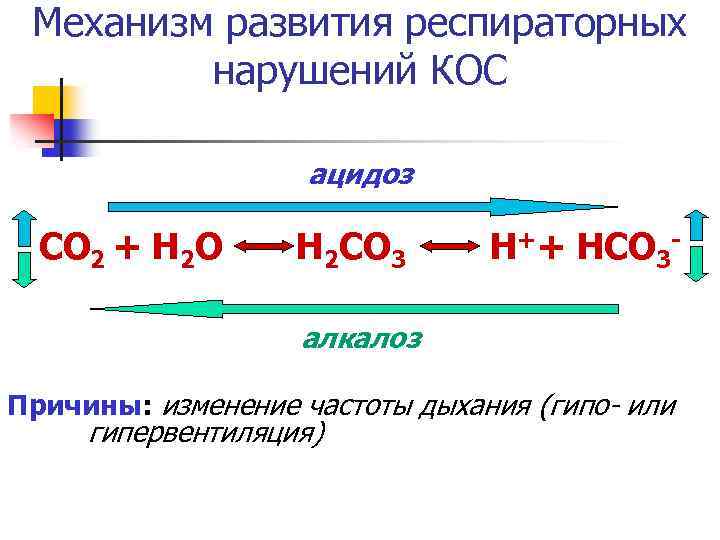
Механизм развития респираторных нарушений КОС ацидоз СО 2 + Н 2 О Н 2 СО 3 Н++ НСО 3 - алкалоз Причины: изменение частоты дыхания (гипо- или гипервентиляция)
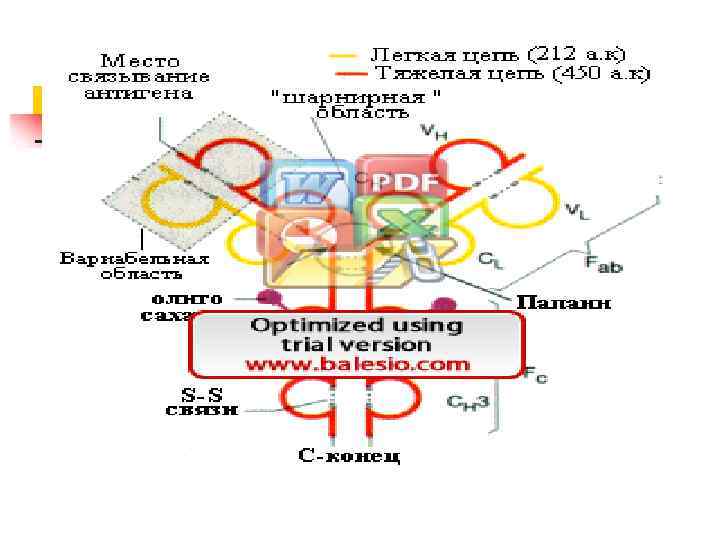
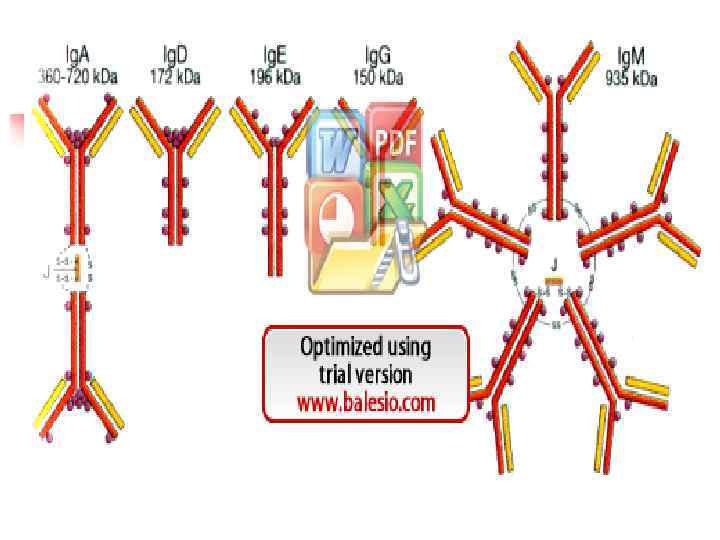


Эритроциты у взрослых образуются (эритропоэз) преимущественно в костном мозге при активном участии специфического регулятора эритропоэтина. Эритропоэтин (Эпо) человека – гликопротеин, состоящий из 166 аминокислот (ММ 34. 000). Его количество в плазме определяется с использованием радиоиммунолических методов (РИА). Эпо синтезируется главным образом почками и скорость его секреции в кровоток увеличивается при гипоксических состояниях. В костном мозге. он взаимодействует с клетками предшественниками при участии специфического рецептора со свойствами тирозинкиназы. Тип вторичного посредника и специфичные гены к настоящему времени точно не установлены. Клетками мишенями Эпо являются КОЕ -ГЭММ и КОЕ-Э способствуя их пролиферации и дифференцировке. Действие Эпо усиливается другими факторами (например, интерлейкином-3 и инсулиноподобным фактором роста). Получение рекомбинантного Эпо позволило использовать его в лечении анемий.

В процессе дифференцировки клетка приобретает способность синтезировать свой главный белок – гемоглобин, постепенно теряет ядро и другие органоиды и превращается в эритроцит, который чаще называют форменным элементом крови, чем клеткой. От более старых эритроцитов, которые уже находились в циркулирующей крови, молодые эритроциты можно отличить по выявляемой при помощи некоторых красителей сеточки, которая состоит из рибосомальной РНК( используемой для синтеза гемоглобина) и других органелл, которые могут функционировать некоторое время (48 часов) после поступления эритроцитов в сосудистую сеть. Такие эритроциты называют ретикулоцитами и их количество в крови составляющее в норме около 1% эритроцитов служит индикатором эритропоэза. Потеря митохондрий приводит к утрате способности использовать процессы, протекающие в них и эритроциты используют пути метаболизма, протекающие в цитозоле (гликолиз, пентозофосфатный путь и др).

n n В норме у взрослых мужчина - 4. 6 -6. 2 миллионов эритроцитов /мкл крови, а у женщин - 4. 2 -5. 4 миллионов /мкл. Общее количество эритроцитов в кровотоке около 2. 5 x 1013. Нормальный уровень Hb для мужчин - 140 -180 г/л ( 14 – 18 г на 100 мл, 8, 7 -11. 2 ммоль/л в пересчете на ММ мономера), и для женщин - 12 -16 г/л. Значение гематокрита (объем упакованных эритроцитов) для мужчин и женщин - 42 -52 % и. 37 -47% соответственно. Продолжительность жизни нормального эритроцита - 120 суток. Около 1 % популяции эритроцитов кровеносного русла (200 миллиардов клеток или 2 миллиона в секунду) заменяются ежедневно. Продолжительность жизни красной клетки крови резко сокращается при гемолитических анемиях. В этих состояниях число ретикулоцитов заметно увеличивается, поскольку костный мозг пытается компенсировать потери, увеличивая количество новых, молодых эритроцитов кровотоке. «Стареющие» эритроциты захватываются клетками ретикулоэндотелиальной системы ( селезенка, костный мозг и печень) и разрушаются. Образующиеся при распаде порфириновых колец желчные пигменты выделяются, а железо и аминокислоты глобина используются повторно. Повышение эритроцитов в крови называют полицетемией, снижение – анемией.
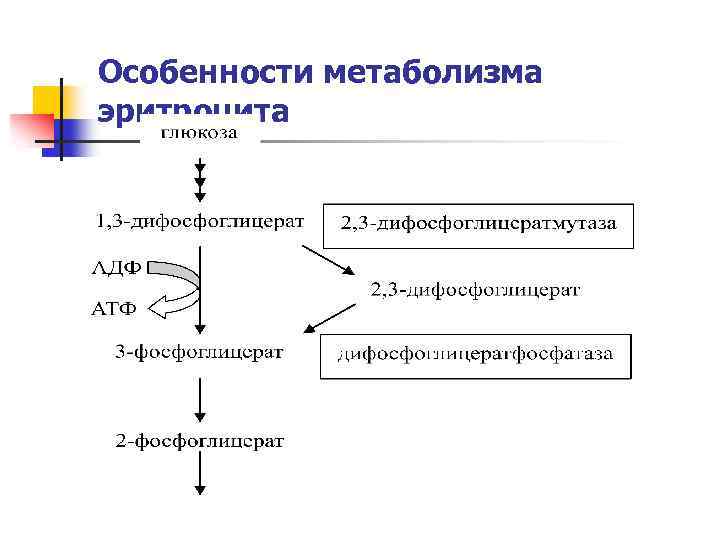
Особенности метаболизма эритроцита

Глюкоза в эритроцитах используется в основном в гликолизе и пентозофосфатном пути. Глюкоза основной источник энергии в эритроцитах. После поступления в клетку и фосфорилирования в глюкозу – 6 -фосфат при помощи гексокиназы около 510% глюкозы идет на образование НАДФН+ Н+ в пентозофосфатном пути и 90 -95% окисляется по гликолитическому пути с образованием АТФ. Особенностью обмена в эритроцитах является боковой путь, ответвляющийся на уровне 1. 3 дифосфоглицерата. Глюкоза в эритроцитах используется в основном в гликолизе и пентозофосфатном пути. Глюкоза основной источник энергии в эритроцитах. После поступления в клетку и фосфорилирования в глюкозу – 6 -фосфат при помощи гексокиназы около 5 -10% глюкозы идет на образование НАДФН+ Н+ в пентозофосфатном пути и 90 -95% окисляется по гликолитическому пути с образованием АТФ. Особенностью обмена в эритроцитах является боковой путь, ответвляющийся на уровне 1. 3 -дифосфоглицерата