Белки, ферменты.pptx
- Количество слайдов: 48

Биохимия белков и ферментов

Структурные единицы белков – аминокислоты Классификация аминокислот 1. 2. 3. 4. 5. 6. Неполярные (гидрофобные) Полярные (гидрофильные) Ароматические (главным образом неполярные) Отрицательно заряженные Положительно заряженные
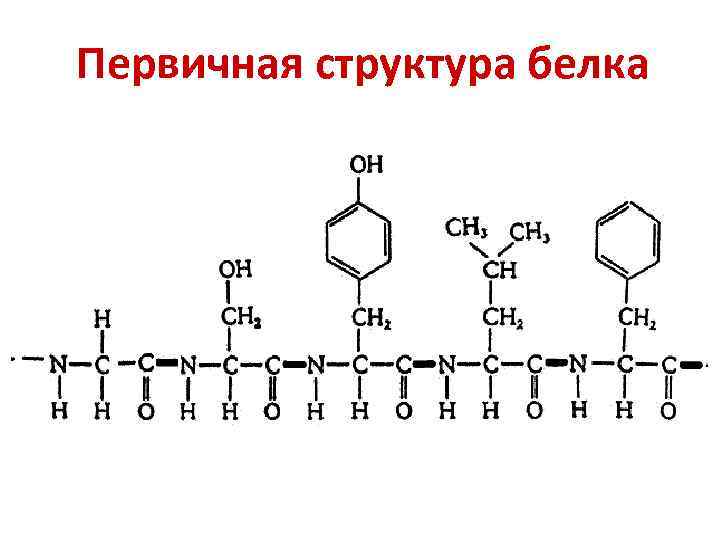
Первичная структура белка
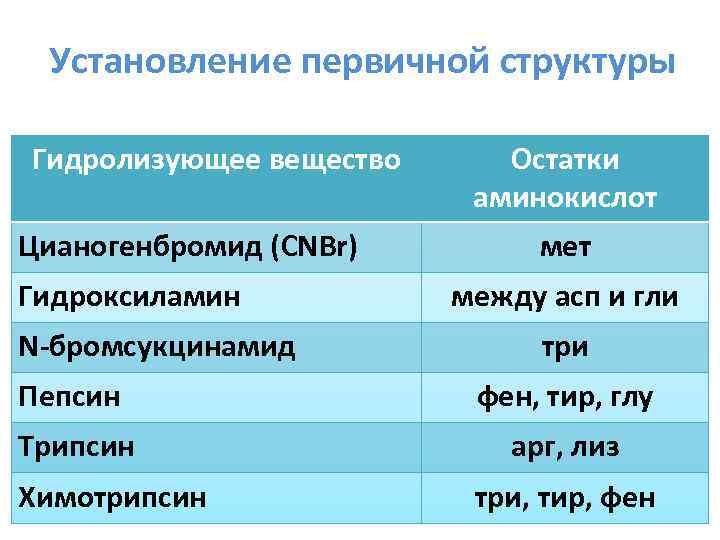
Установление первичной структуры Гидролизующее вещество Цианогенбромид (CNBr) Гидроксиламин N-бромсукцинамид Остатки аминокислот между асп и гли три Пепсин фен, тир, глу Трипсин арг, лиз Химотрипсин три, тир, фен
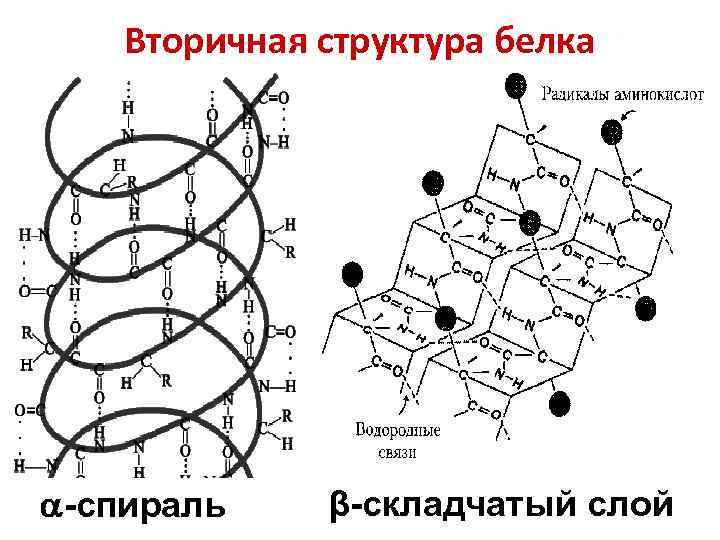
Вторичная структура белка -спираль β-складчатый слой

Третичная структура белка
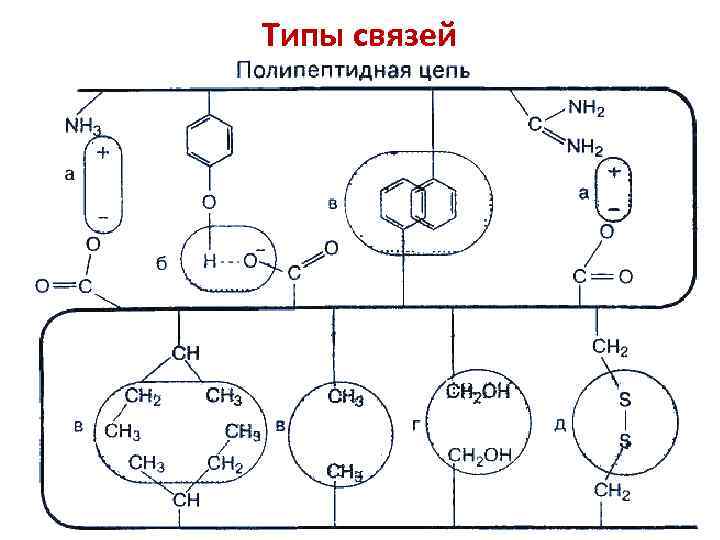
Типы связей
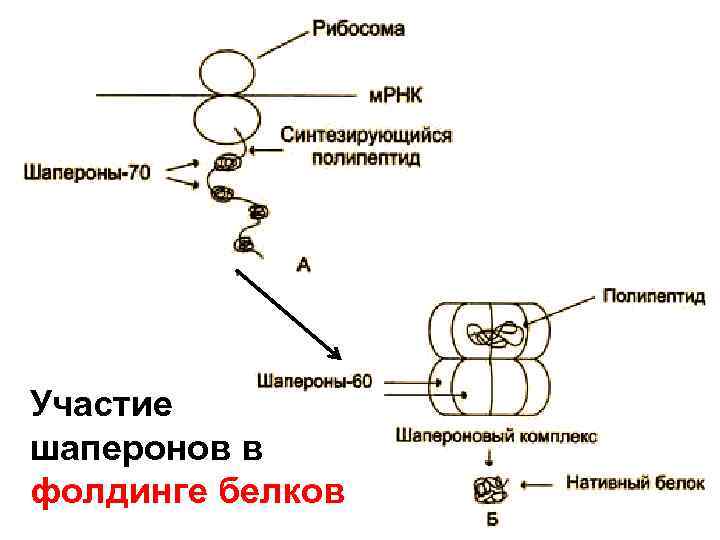
Участие шаперонов в фолдинге белков

Глобулярные домены в gкристаллине (белке хрусталика глаза)

Четвертичная структура гемоглобина
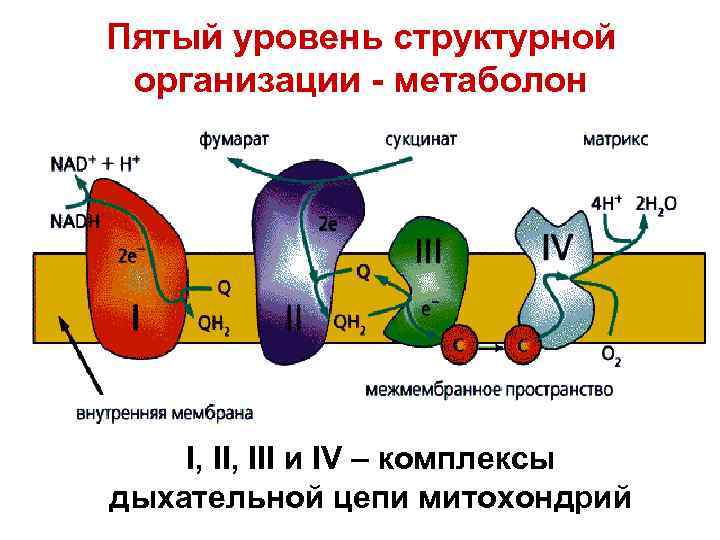
Пятый уровень структурной организации - метаболон I, III и IV – комплексы дыхательной цепи митохондрий
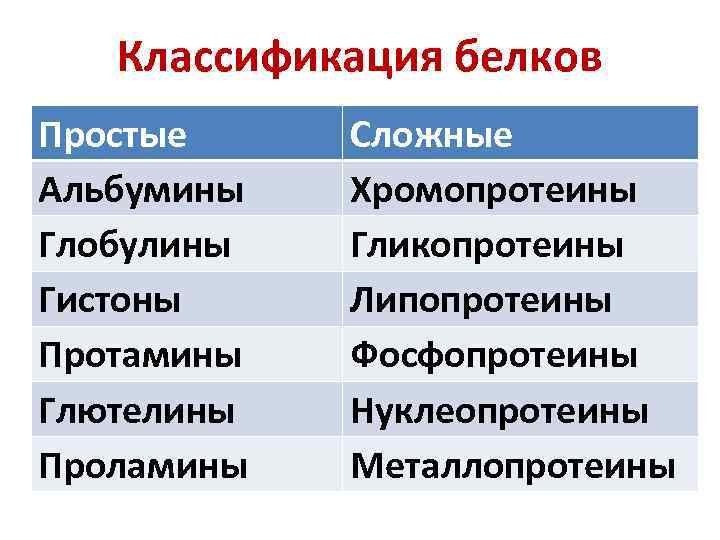
Классификация белков Простые Альбумины Глобулины Гистоны Протамины Глютелины Проламины Сложные Хромопротеины Гликопротеины Липопротеины Фосфопротеины Нуклеопротеины Металлопротеины
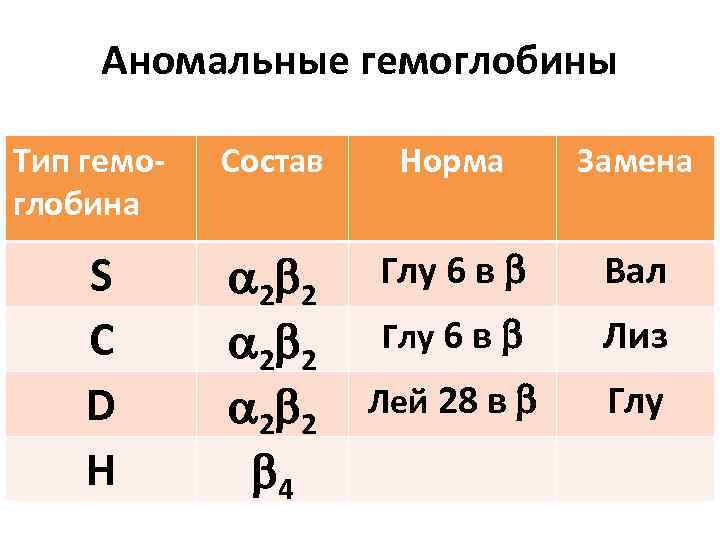
Аномальные гемоглобины Тип гемоглобина S С D Н Состав Норма Замена 2 2 4 Глу 6 в Вал Глу 6 в Лиз Лей 28 в Глу
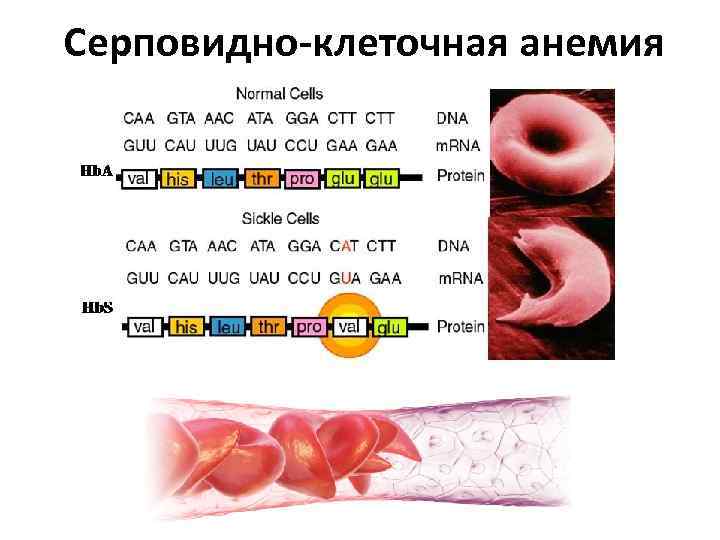
Серповидно-клеточная анемия
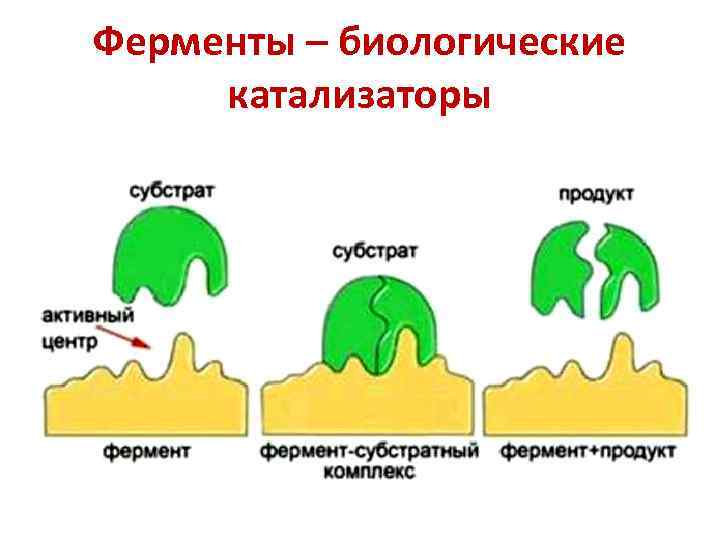
Ферменты – биологические катализаторы

Классификация ферментов 1. Оксидоредуктазы 2. Трансферазы 3. Гидролазы 4. Лиазы 5. Изомеразы 6. Лигазы
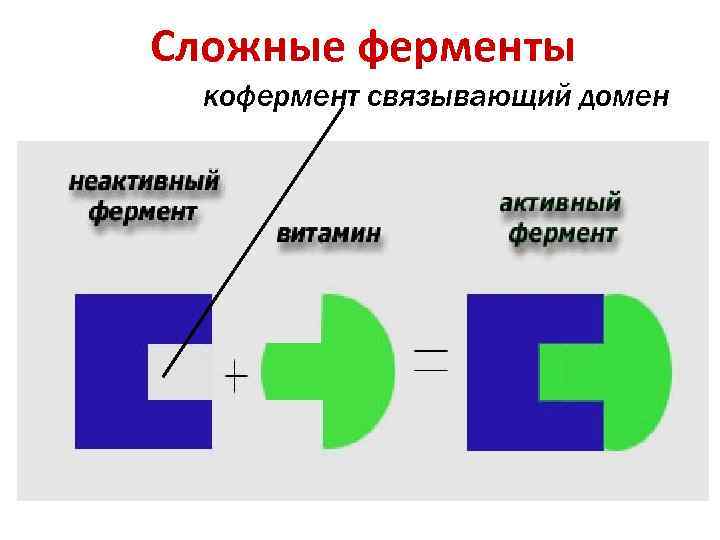
Сложные ферменты кофермент связывающий домен
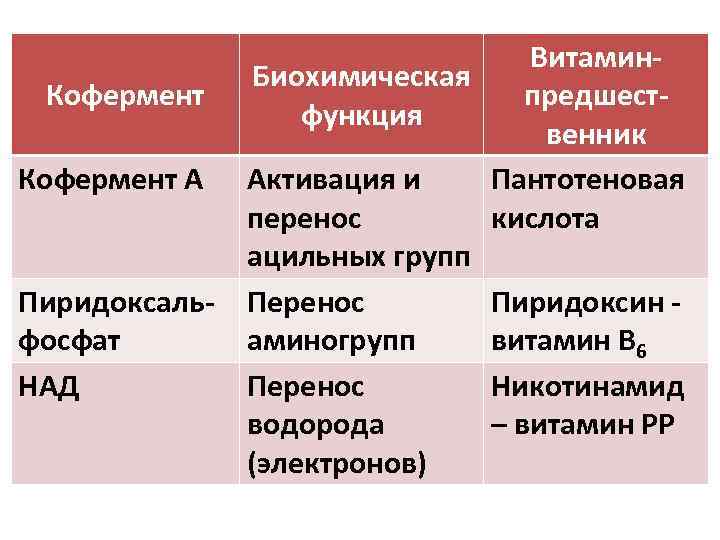
Кофермент А Пиридоксальфосфат НАД Витамин. Биохимическая предшестфункция венник Активация и Пантотеновая перенос кислота ацильных групп Перенос Пиридоксин аминогрупп витамин В 6 Перенос Никотинамид водорода – витамин РР (электронов)
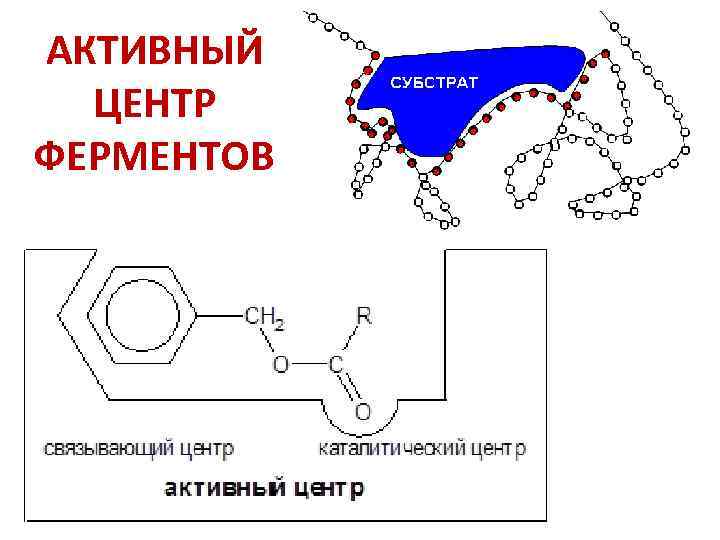
АКТИВНЫЙ ЦЕНТР ФЕРМЕНТОВ
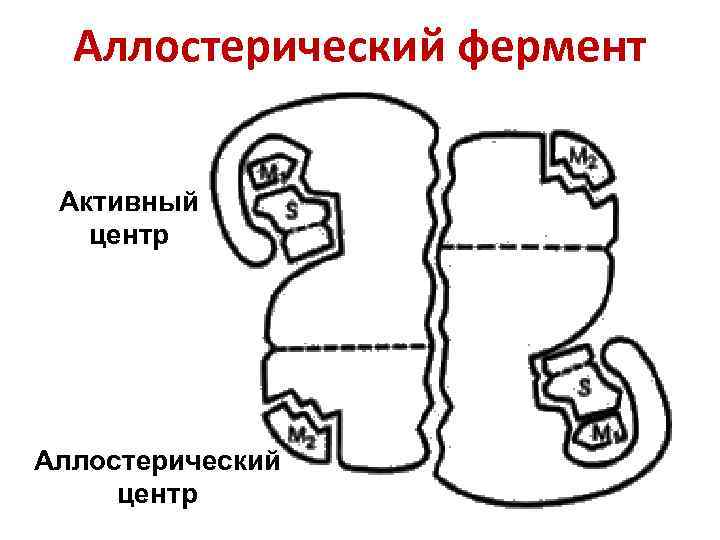
Аллостерический фермент Активный центр Аллостерический центр
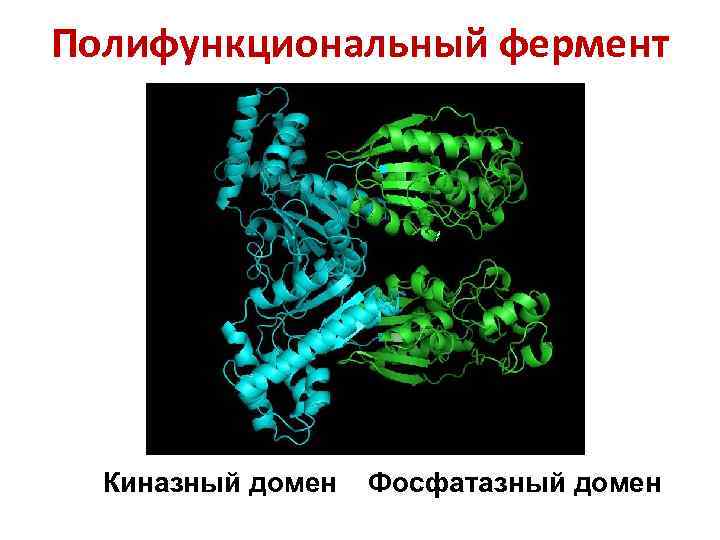
Полифункциональный фермент Киназный домен Фосфатазный домен
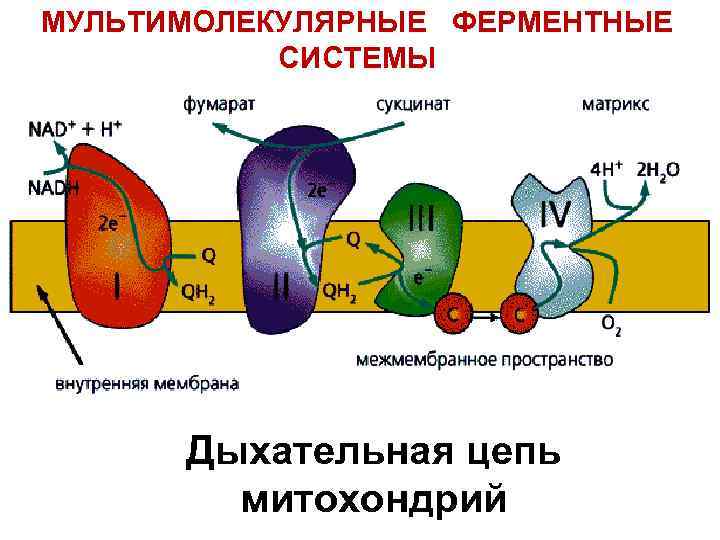
МУЛЬТИМОЛЕКУЛЯРНЫЕ ФЕРМЕНТНЫЕ СИСТЕМЫ Дыхательная цепь митохондрий
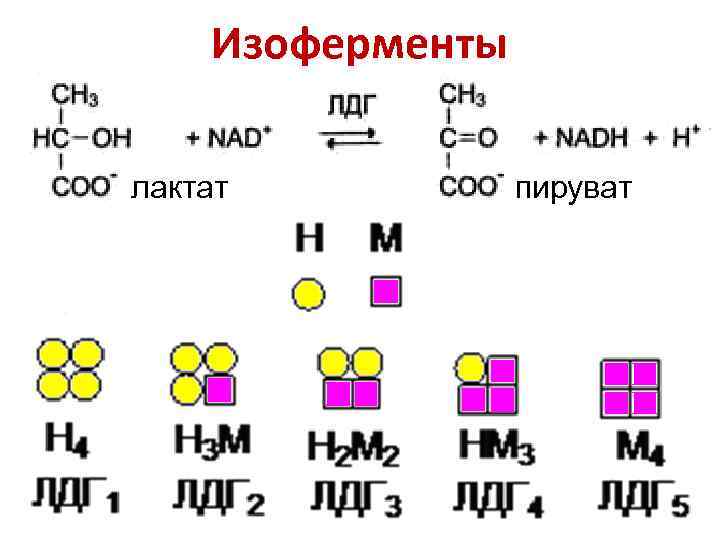
Изоферменты лактат пируват

Теории ферментативного катализа Герман Эмиль Фишер (1852 – 1919)
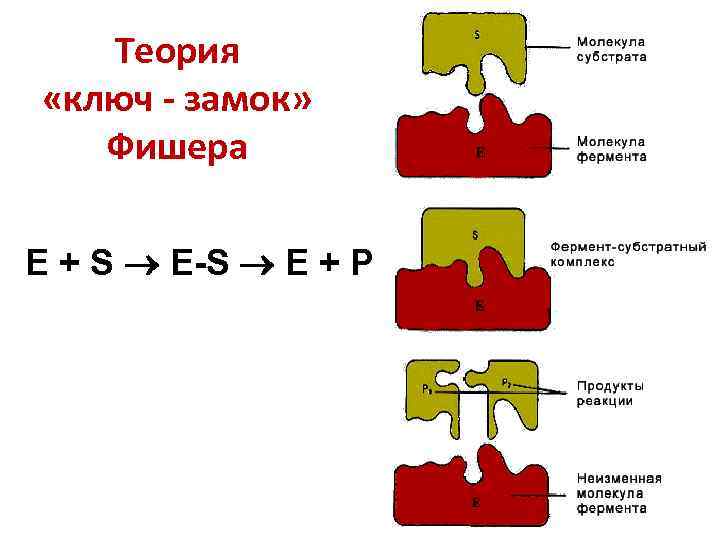
Теория «ключ - замок» Фишера E + S E-S E + P

Дэниел Кошланд (1920 – 2007)
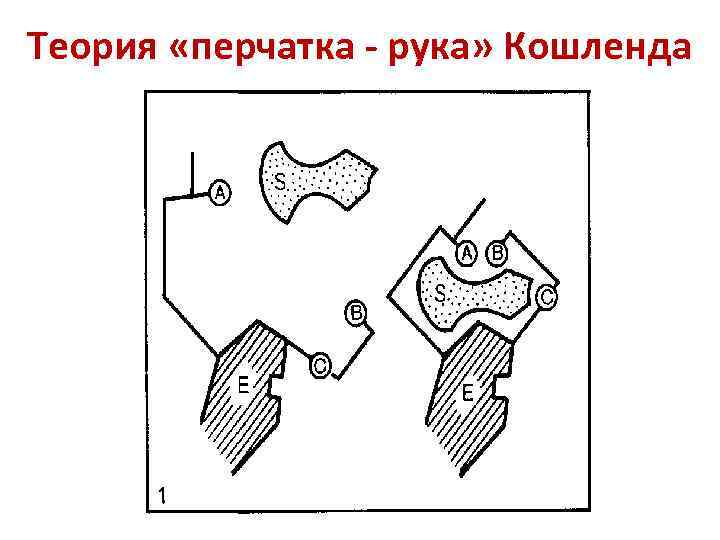
Теория «перчатка - рука» Кошленда
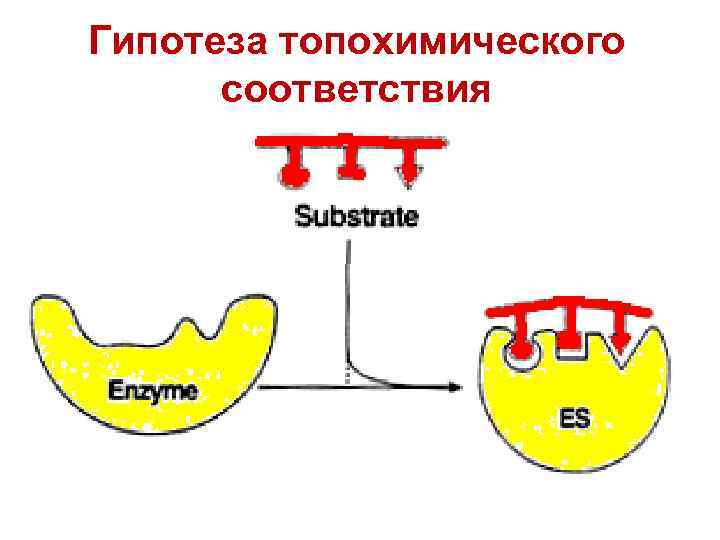
Гипотеза топохимического соответствия

Ферментатив ная кинетика
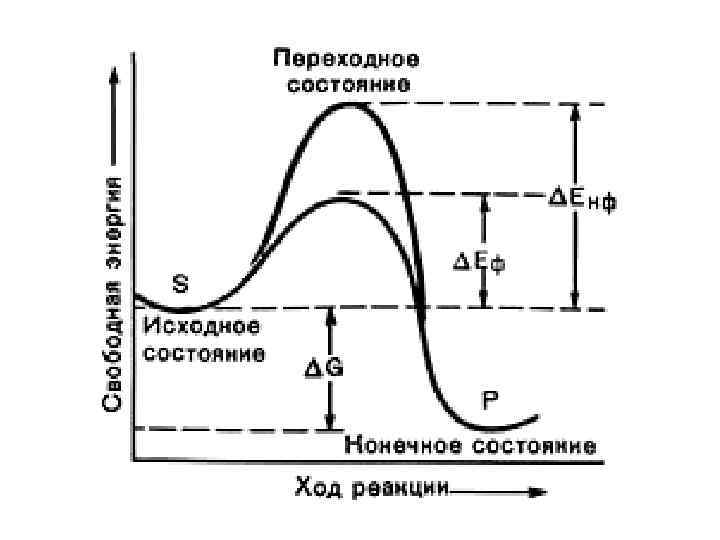

МИХАЭЛИС Леонор МЕНТЕН Мод Леонора

Уравнение Михаэлиса-Ментен Уравнение Бриггса-Холдейна
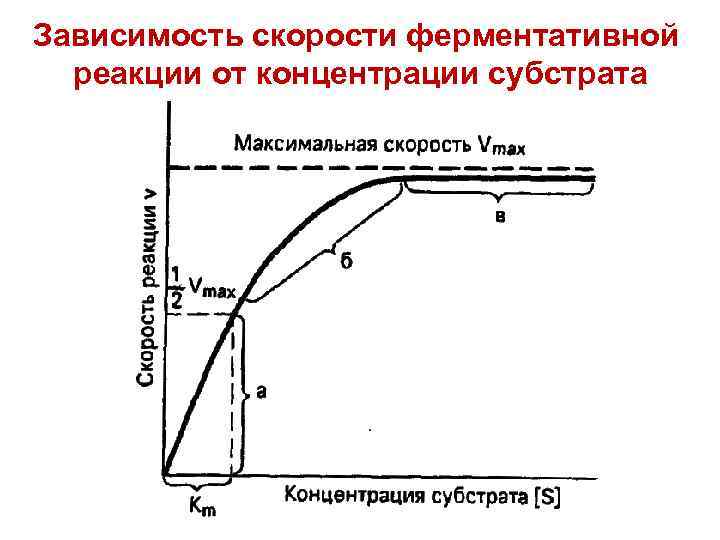
Зависимость скорости ферментативной реакции от концентрации субстрата
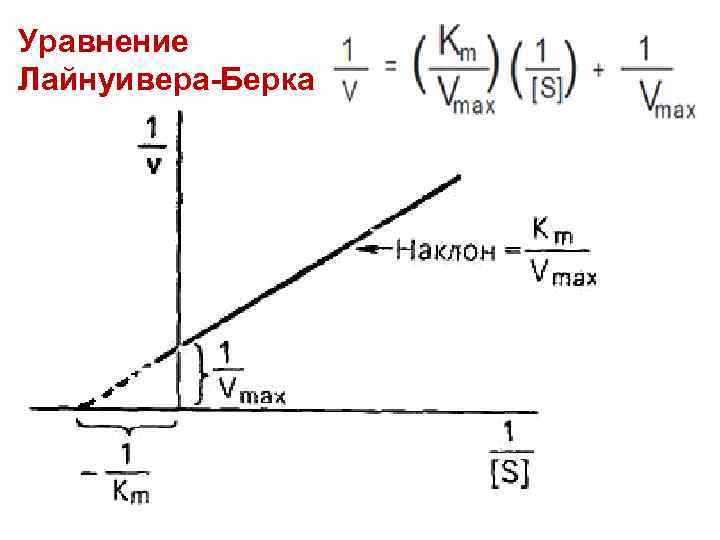
Уравнение Лайнуивера-Берка
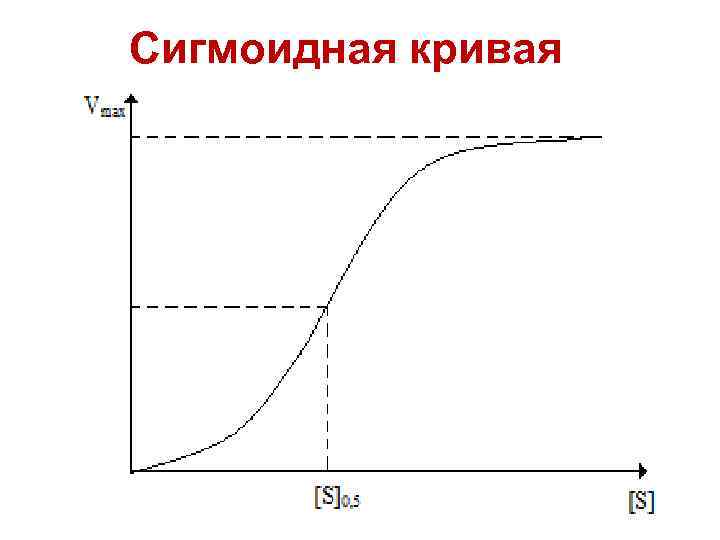
Сигмоидная кривая
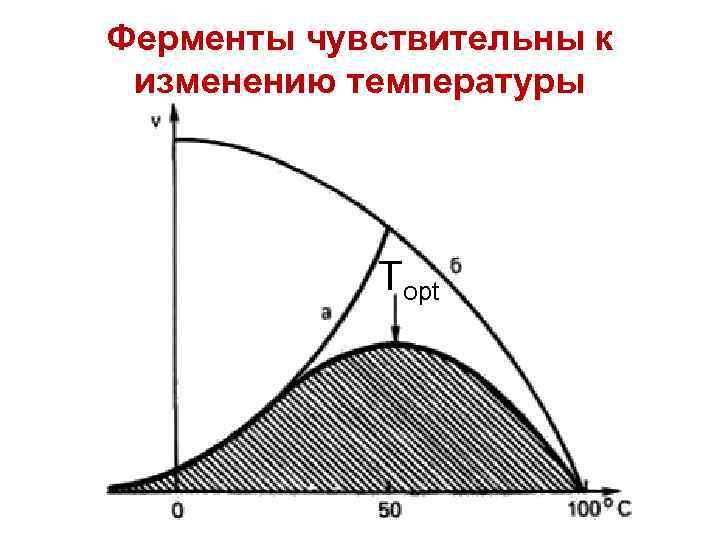
Ферменты чувствительны к изменению температуры Тopt
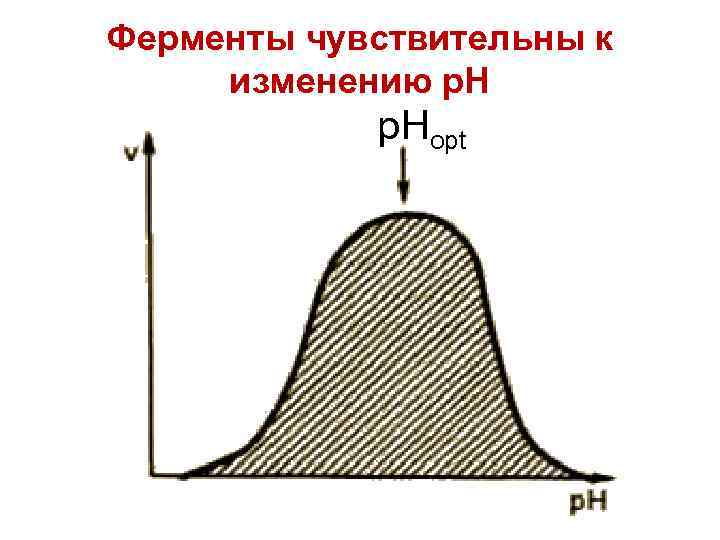
Ферменты чувствительны к изменению р. Н p. Hopt
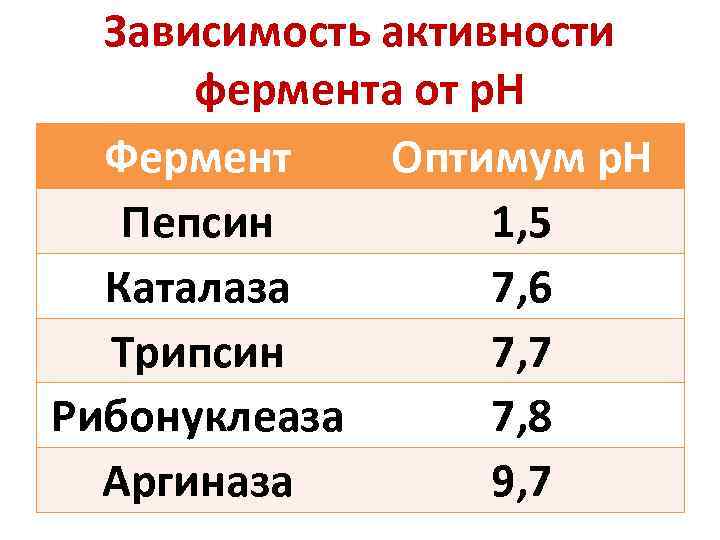
Зависимость активности фермента от р. Н Фермент Оптимум р. Н Пепсин 1, 5 Каталаза 7, 6 Трипсин 7, 7 Рибонуклеаза 7, 8 Аргиназа 9, 7

Ферменты специфичны (действуют только на определенный субстрат)
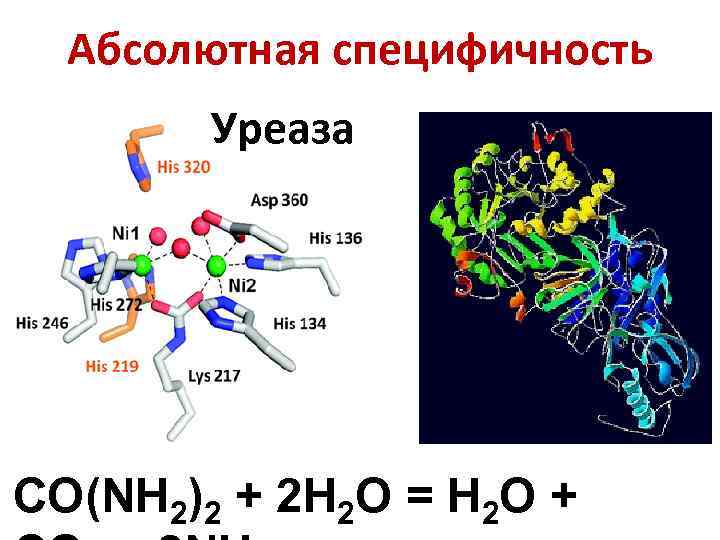
Абсолютная специфичность Уреаза CO(NH 2)2 + 2 H 2 O = H 2 O +
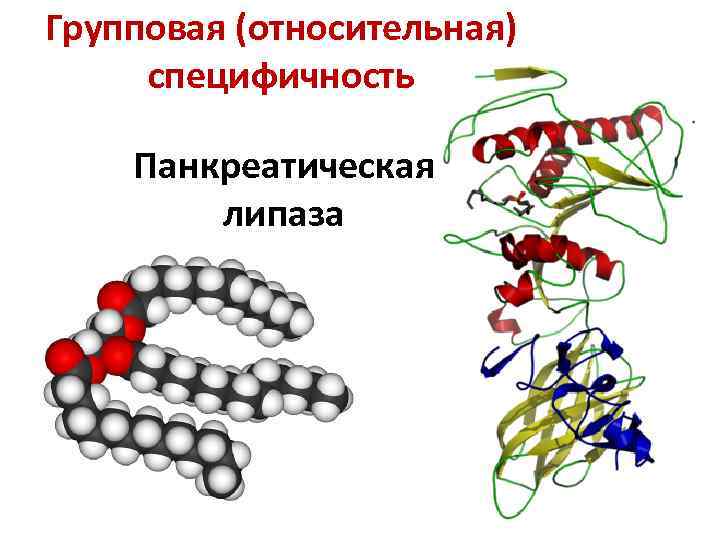
Групповая (относительная) специфичность Панкреатическая липаза
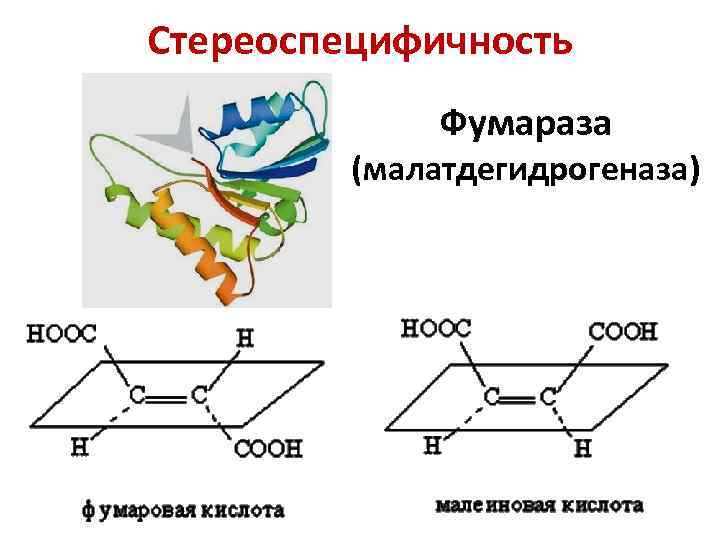
Стереоспецифичность Фумараза (малатдегидрогеназа)
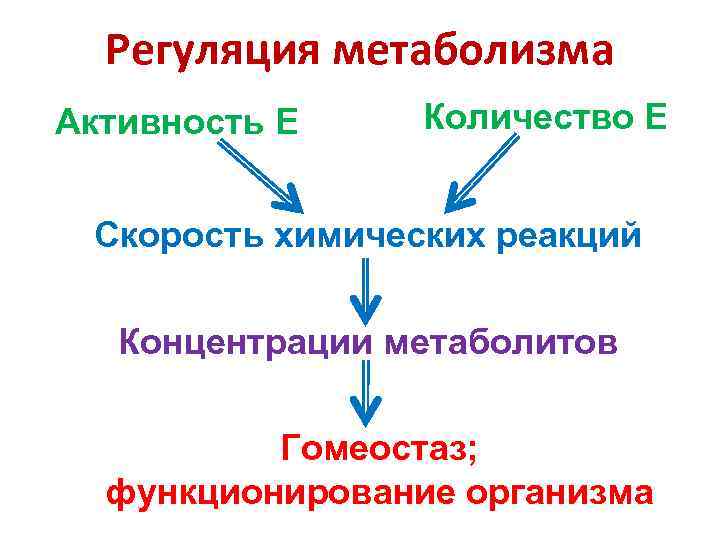
Регуляция метаболизма Активность Е Количество Е Скорость химических реакций Концентрации метаболитов Гомеостаз; функционирование организма
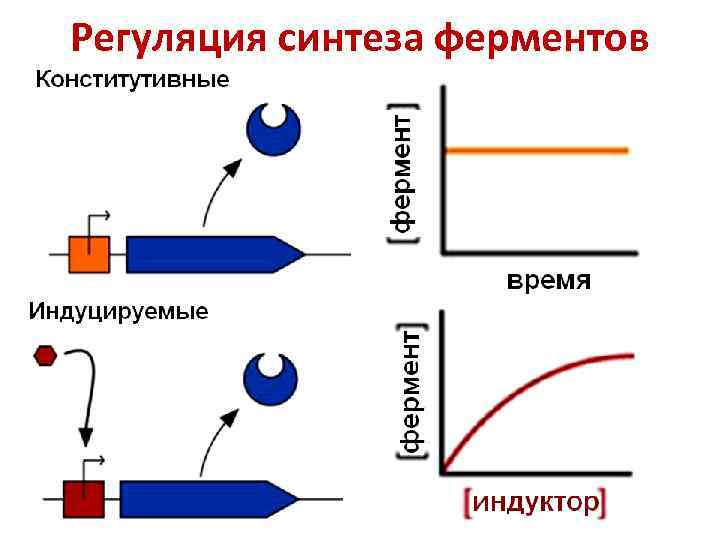
Регуляция синтеза ферментов

Регуляция активности ферментов

Единицы ферментативной активности Е (U) = 1 мкмоль/мин 1 кат = 1 моль/с 1 Е = 16. 67 нкат

Активаторы ферментов Фермент Активатор 2+ Цитохромы Fe 2+ Холинэстераза Mn Амилаза Сl Желчные Липаза кислоты

Типы ингибирования • • неспецифическое необратимое конкурентное неконкурентное бесконкурентное
Белки, ферменты.pptx