Начало белки + аминокислоты.ppt
- Количество слайдов: 44

Биохимия белка

История исследования белка n Беккари Якопо Бартоломео – итальянский учёный, в 1728 г. выделил первое белковое вещество – из пшеничной муки – клейковину. Он показал сходство этого белка с белком животного происхождения – куриным белком. n в 1806 году открыто первое аминокислотное производное - амид аспарагина, а первая аминокислота - цистин в 1810 году). n Бракконо Анри– французский химик, в 1820 году открыл в продуктах гидролиза белков аминокислоту – глицин. n n В 1847 году К. Рейхерт открыл способность белков образовывать кристаллы. В 1836 году Т. Шванн открыл пепсин - фермент, расщепляющий белки. В 1856 году Л. Корвизар открыл еще один подобный фермент - трипсин. В 1888 г. А. Я. Данилевский выдвинул гипотезу строения белка, получившую название “теории элементарных рядов”. Он первым предположил существование в белках CO NH связей, как в биурете.
n В 1890 г. Гофмейстер впервые получил кристаллический белок – яичный альбумин. n В 1902 г. Фишер и Гофмейстер предложили пептидную теорию строения белка. В это же время Фишер с сотр. впервые синтезировал в лаборатории первые пептиды. n В 1925 -1930 гг. Сведберг сконструировал ультрацентрифугу и использовал ее для определения молекулярной массы выделяемых белков. n В 1951 году Полинг и Кори разработали модель вторичной структуры белка, названной -спиралью. n В 1952 году Линдерстрём-Ланг предложил существование трех уровней организации белковой молекулы: первичный, вторичный, третичный. n В 1953 г. Сенгер впервые расшифровал последовательность аминокислот в инсулине. n В 1956 г. Мур и Стейн создали первый автоматический анализатор аминокислот. n В 1963 г. Цае синтезировал природный белок инсулин.
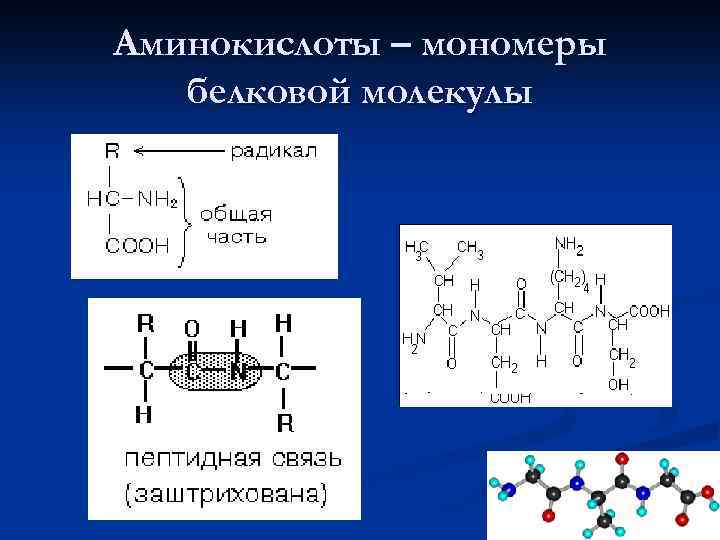
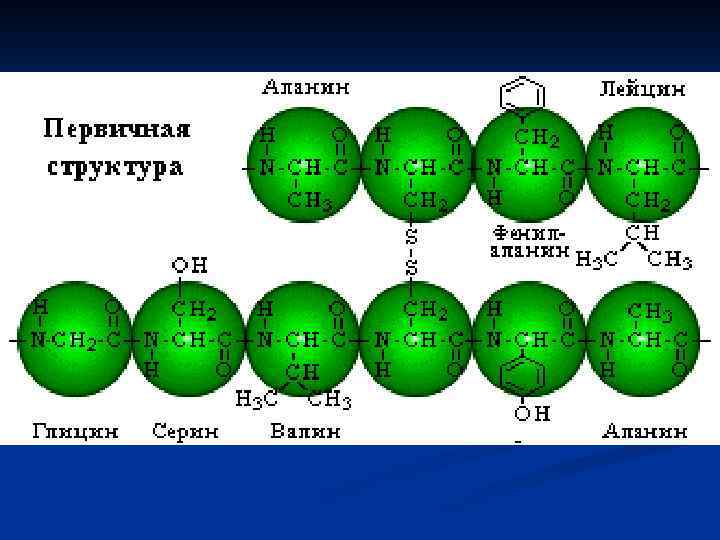
Аминокислоты – мономеры белковой молекулы
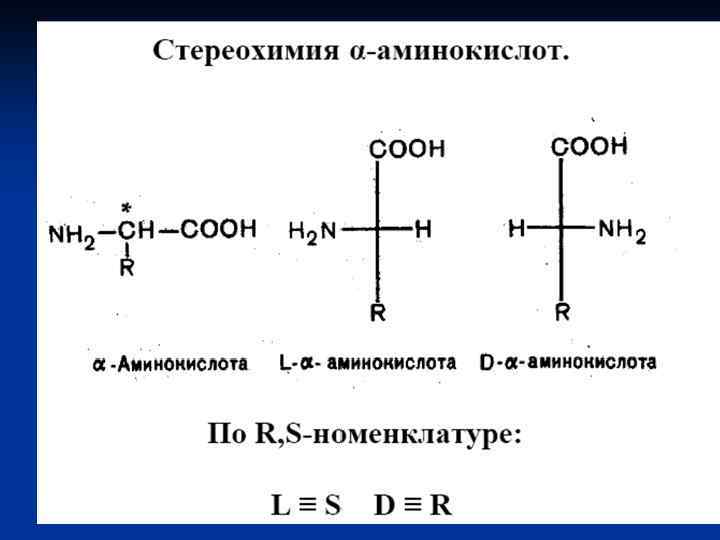
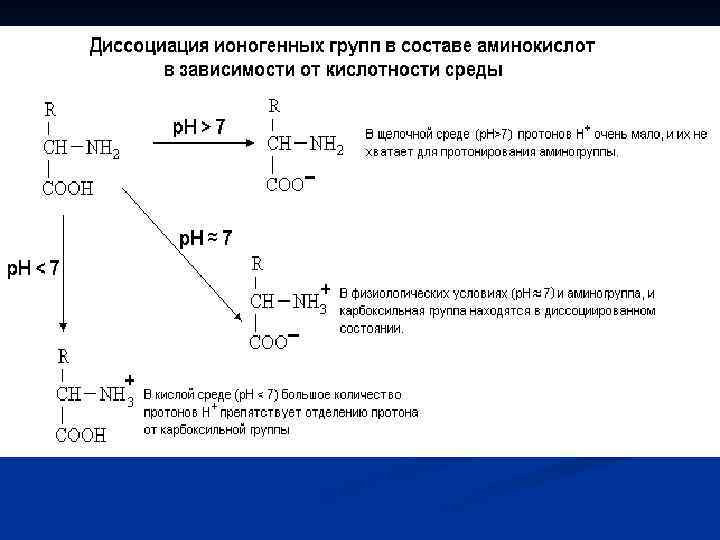

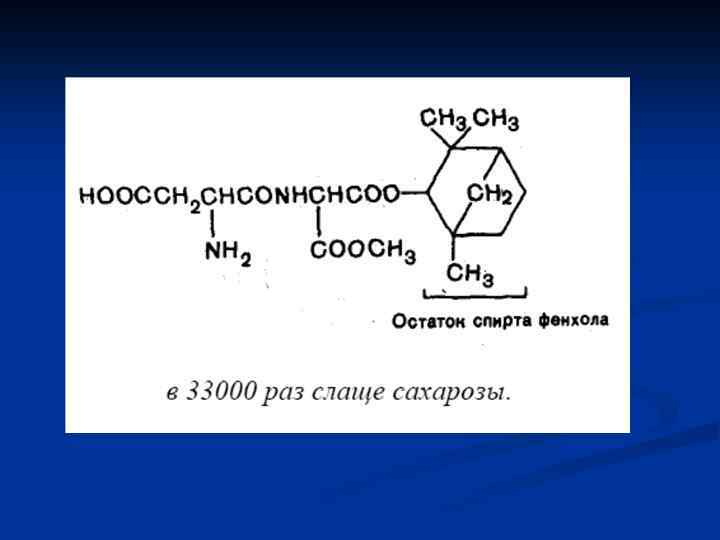

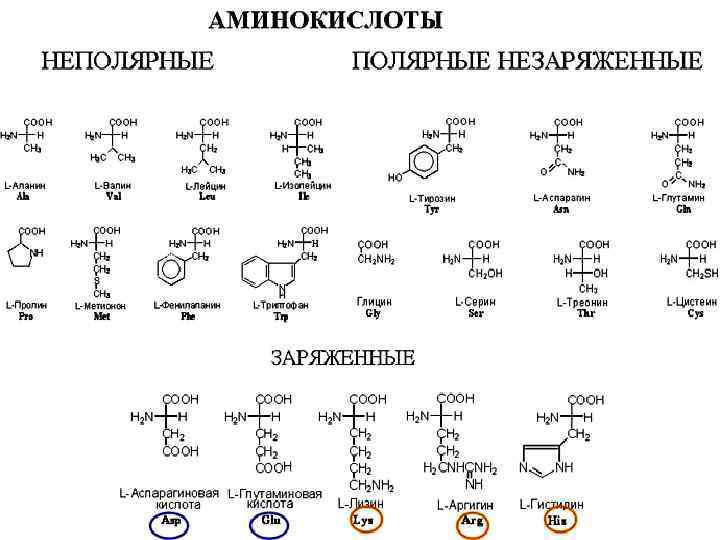
Приняты три классификации аминокислот: 1) структурная, т. е. по строению бокового радикала; 2) электрохимическая – по кислотно-основным свойствам аминокислот; 3) биологическая или физиологическая, т. е. по степени незаменимости для организма. Делят на незаменимые ( для человека восемь: валин, лейцин, изолейцин, треонин, лизин, метионин, фенилаланин, триптофан). Полузаменимые – (для человека три: аргинин, тирозин, гистидин).

Ациклические моноаминомонокарбоновые кислоты Глицин - -аминоуксусная кислота – Гли – (Gly) В 1820 г. Браконно получил глицин из сернокислого гидролизата желатины - “сахар желатины” был назван гликоколлом, а затем глицином. Глицин – замедляет дегенерацию мышечной ткани, так как является источником креатина. Он выполняет функции тормозного нейромедиатора.

Алифатические моноаминомонокарбоновые кислоты Аланин - -аминопропионовая кислота –– Ала (Ala) В 1850 году Штреккер, пытаясь получить молочную кислоту, случайно синтезировал аланин. Через 38 лет Вейл выделил эту аминокислоту из кислотного гидролизата шелка – белка, наиболее богатого аланином.

Алифатические моноаминомонокарбоновые кислоты Валин - -аминоизовалериановая –– Вал (Val) Незаменимая! Валин был открыт в экстрактах поджелудочной железы Горуп-Безанессом в 1856 году. Необходим для метаболизма в мышцах, поддержания обмена веществ. Валин присутствует во многих белках, но обычно – в относительно малых количествах.

Алифатические моноаминомонокарбоновые кислоты (неполярные) Лейцин - -аминоизокапроновая –– Лей (Leu) Незаменимая! Пруст получил лейцин в неочищенной форме из сыра в 1819 году. Браконно выделил кристалическую аминокислоту из кислотных гидролизатов мышц и шерсти и назвал ее лейцином.

Ациклические моноаминомонокарбоновые кислоты Изолейцин - -амино- -метил- -этилпропионовая –– Иле Незаменимая! (Ile) Изолейцин был выделен Эрлихом из мелассы сахарной свеклы в 1904 году, а позднее из неполного гидролизата фибрина, а также из клейковины пшеницы, яичного белка и говяжьего мяса. Необходим для синтеза гемоглобина, регулирует уровень сахара в крови и процессы обеспечения энергией.

Гетероциклическая моноаминомонокарбоновая иминокислота Пролин – пирролидин- - карбоновая –– Про (Pro) Считается, что пролин входит в состав всех белков всех организмов. Особенно богат пролином основной белок соединительной ткани — коллаген. Пролин. Предельно важен для правильного функционирования связок и суставов; также участвует в поддержании работоспособности и укреплении сердечной мышцы.

Алифатические моноаминомонокарбоновые кислоты (полярные) Гидроксикислоты Серин - -амино- -гидроксипропионовая –– Сер (Ser) Серин впервые был выделен Кремером в 1865 году из белка шелка, где имеется относительно большое количество этой аминокислоты. Строение серина было установлено в 1902 году Фишером и Лайксом.

Алифатические моноаминомонокарбоновые кислоты Гидроксикислоты Треонин - -амино- -гидроксимасляная –– Тре (Tre) Незаменимая! Треонин был получен из кислотных гидролизатов фибрина в 1935 году Роузом и др. Работа этих исследователей была направлена на выделение присутствующего в белковом гидролизате фактора, необходимого для роста крыс. Открытие треонина позволило впервые показать, что крысы могут расти на диете, содержащей очищенные аминокислоты.

Алифатические моноаминомонокарбоновые кислоты Тиоаминокислоты Цистеин - -амино- -тиопропионовая –– Цис (Cys) Цистеин входит в состав альфа-кератина, основного белка ногтей, кожи и волос. Он способствует формированию коллагена и улучшает эластичность и текстуру кожи. Цистеин входит в состав и других белков организма, в том числе некоторых пищеварительных ферментов.
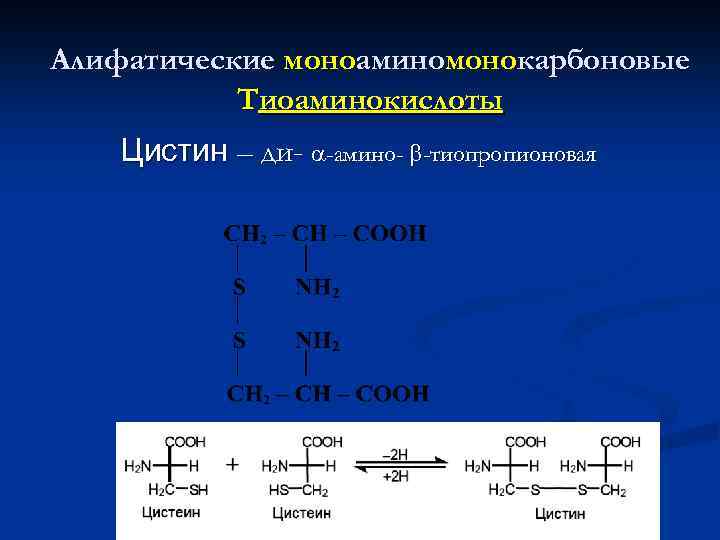
Алифатические моноаминомонокарбоновые Тиоаминокислоты Цистин – ди- -амино- -тиопропионовая

Алифатические моноаминомонокарбоновые Тиоаминокислоты Метионин - -амино- -метилтиомасляная –– Мет (Met) Незаменимая! Выделен в 1922 г. из продуктов кислотного гидролиза казеина. М. — донор метильных групп в организме млекопитающих и человека. В процессах ферментативного переметилирования, приводящих к образованию холина, адреналина и др. биологически важных веществ.

Алифатические моноаминодикарбоновые кислоты Аспарагиновая - -аминоянтарная –– Асп (Asp) Аспарагиновая кислота была сначала описана как продукт гидролиза аспарагина. Позднее Ритгаузен выделил аспарагиновую кислоту из белкового гидролизата.

Алифатические моноаминодикарбоновые кислоты Аспарагин - - амид- -аминоянтарной к-ты –– Асн (Asn) Аспарагин был первой аминокислотой, выделенной из природных продуктов. В 1806 году Вокелен и Робике получили его из сока спаржи. Представляет собой широко распостраненное соединение; он накапливается в значительных количествах у некоторых видов высших растений, а также встречается в свободном состоянии в тканях животных.

Алифатические моноаминодикарбоновые кислоты Глутаминовая - -аминоглутаровая –– Глу (Glu) Глутаминовая кислота была выделена Ритгаузеном в 1866 году из гидролизатов клейковины пшеницы. В 1890 году Вольф осуществил первый химический синтез глутаминовой кислоты. Эта кислота относится к числу наиболее широко распостраненных аминок

Алифатические моноаминодикарбоновые кислоты Глутамин - - амид - -аминоглутаровой к-ты – Глн (Gln)

Алифатические диаминомонокарбоновые кислоты (положительно заряженные радикалы) Лизин - , -диаминокапроновая к-та – Лиз (Lys) Незаменимая!

Алифатические диаминомонокарбоновые кислоты (положительно заряженные радикалы) Аргинин - -амино- -гуанидиновалериановая – Арг (Arg) Полузаменимая!

Алифатическая гетероциклическая аминокислота Гистидин - -амино- -имидазолилпропионовая – Гис (His) Полузаменимая!

Ароматические моноаминомонокарбоновые кислоты Фенилаланин - -амино -фенилпропионовая – Фен (Phe) Незаменимая!
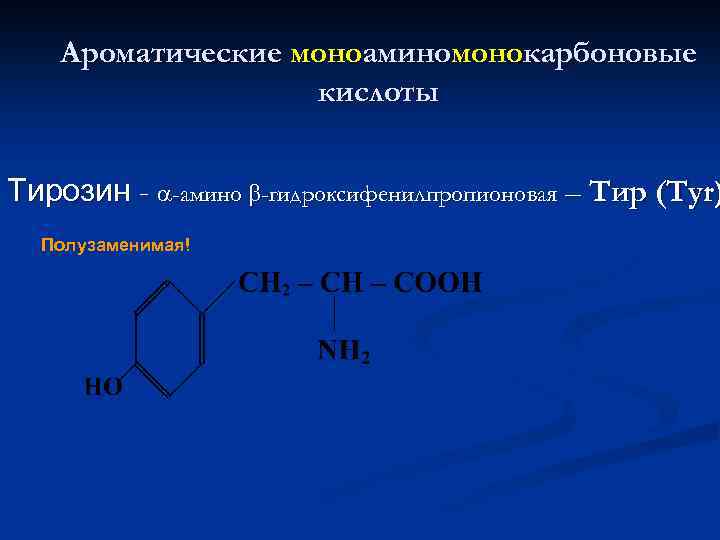
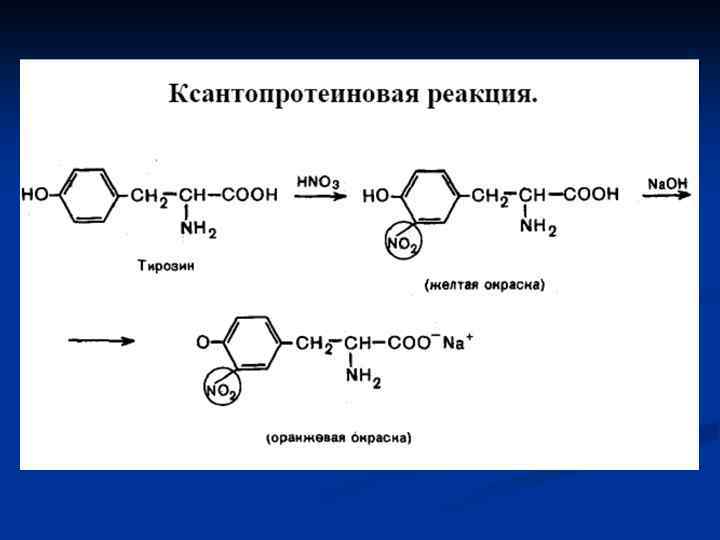
Ароматические моноаминомонокарбоновые кислоты Тирозин - -амино -гидроксифенилпропионовая – Тир (Tyr) Полузаменимая!
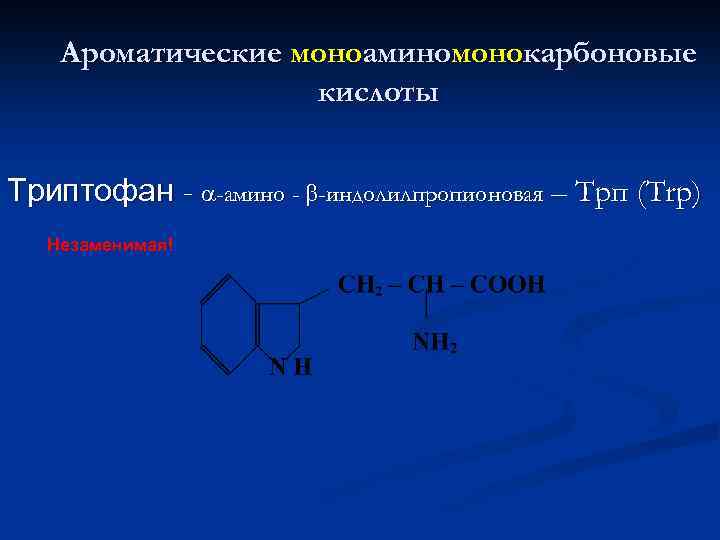
Ароматические моноаминомонокарбоновые кислоты Триптофан - -амино - -индолилпропионовая – Трп (Trp) Незаменимая!
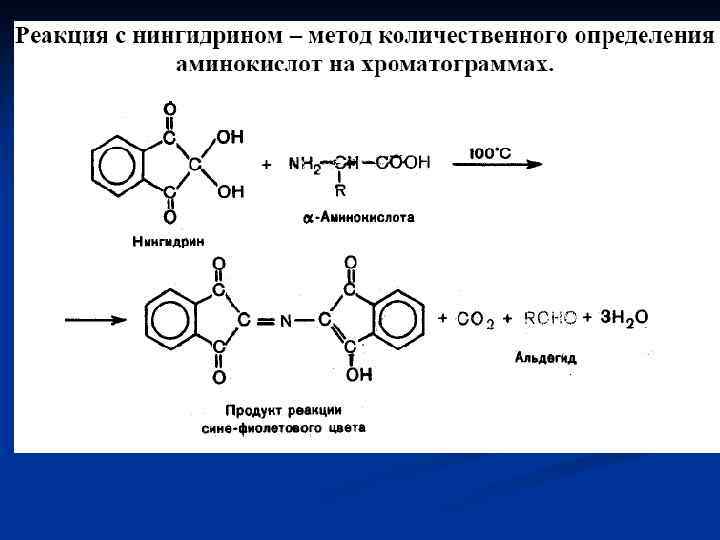
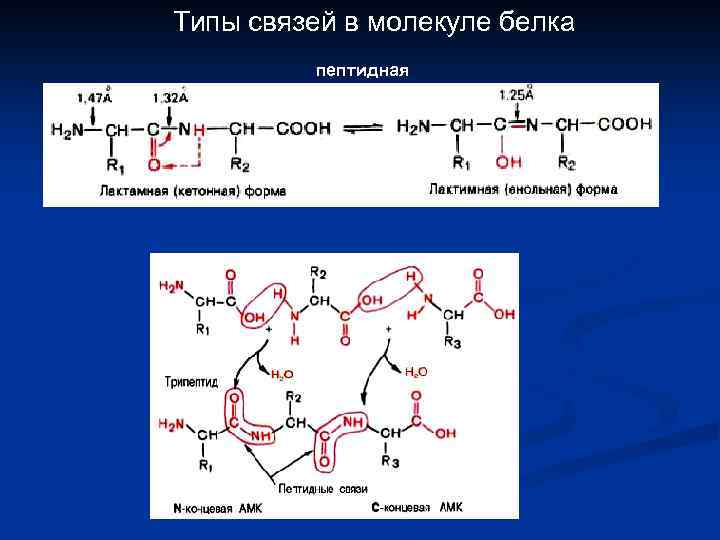
Типы связей в молекуле белка пептидная

Типы связей в молекуле белка дисульфидная водородная гидрофобные взаимодействия
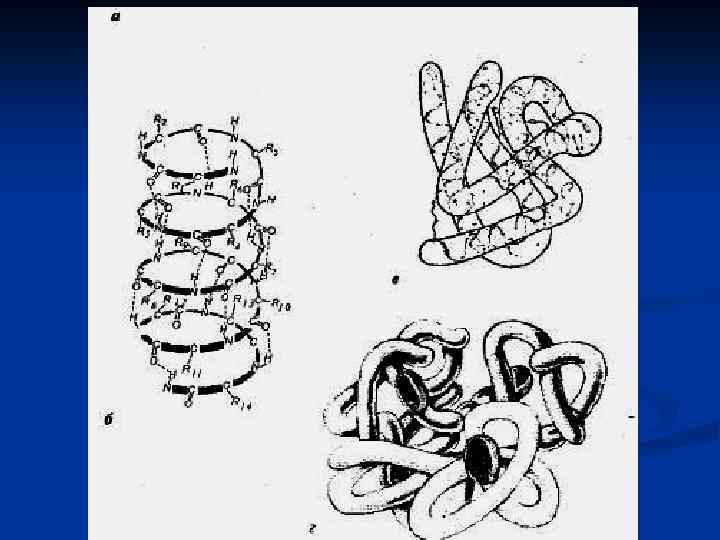
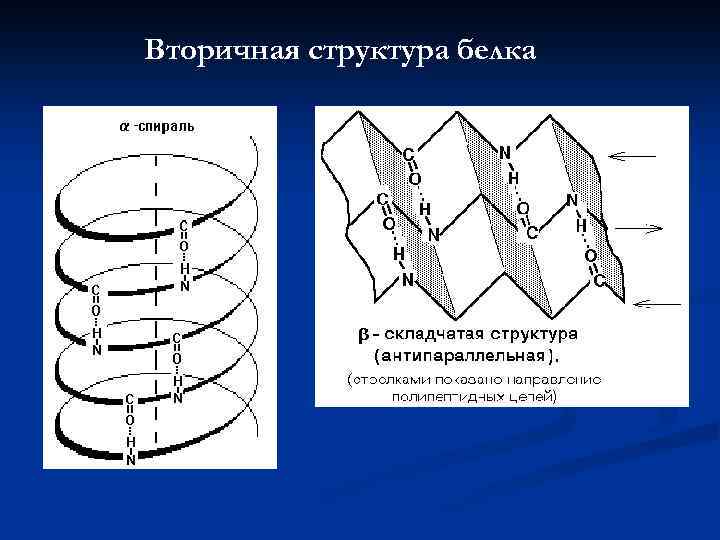
Вторичная структура белка
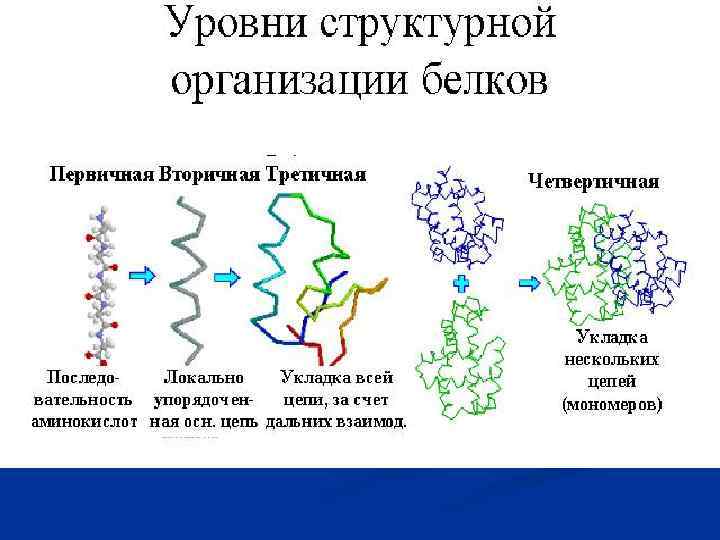
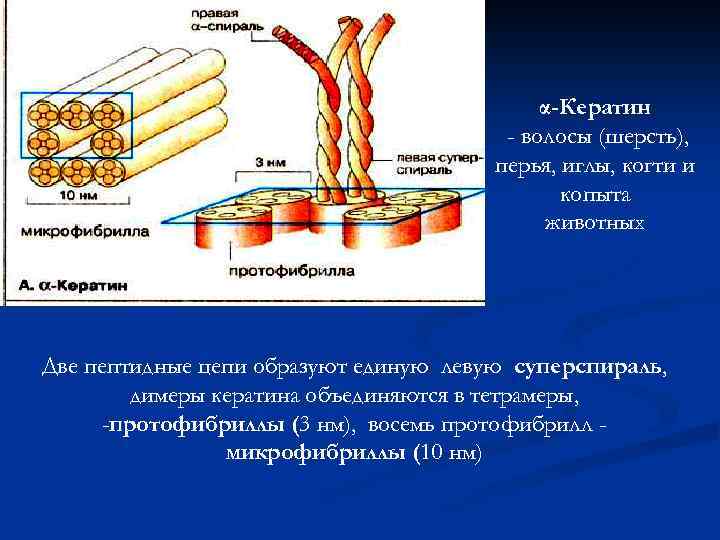
α-Кератин - волосы (шерсть), перья, иглы, когти и копыта животных Две пептидные цепи образуют единую левую суперспираль, димеры кератина объединяются в тетрамеры, -протофибриллы (3 нм), восемь протофибрилл микрофибриллы (10 нм)
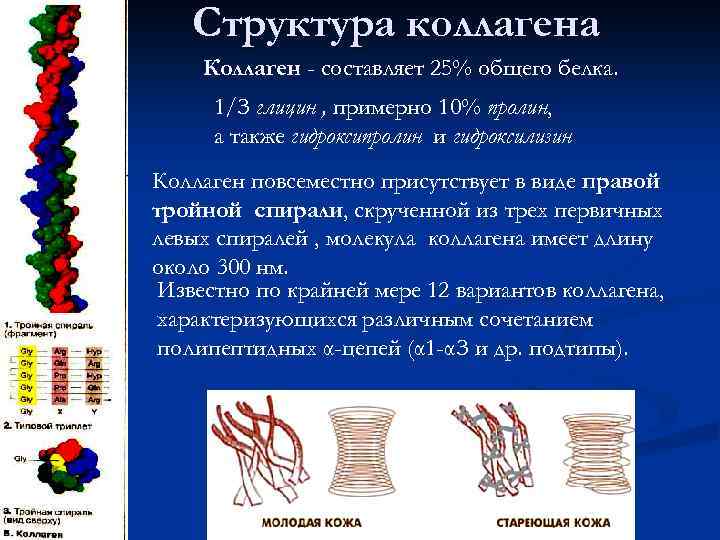
Структура коллагена Коллаген - составляет 25% общего белка. 1/З глицин , примерно 10% пролин, а также гидроксипролин и гидроксилизин Коллаген повсеместно присутствует в виде правой тройной спирали, скрученной из трех первичных левых спиралей , молекула коллагена имеет длину около 300 нм. Известно по крайней мере 12 вариантов коллагена, характеризующихся различным сочетанием полипептидных α-цепей (α 1 -αЗ и др. подтипы).

Ocновной белок шелка, фиброин, обладает структурой антипараллельного складчатого листа Фактически фиброин состоит на 80% из глицина, аланина и серина

Важнейшие функции белков Структурная (коллаген, эластин, кератин) Каталитическая (ферменты) Транспортная (гемоглобин, альбумины, глобулины) Сократительная (актин, миозин) Защитная (иммуноглобулины, фибриноген, плазминоген, лизоцим) Регуляторная (гормоны, рецепторы) Онкотическое давление (белки сыворотки крови); Буферная (гемоглобин, белки сыворотки крови)

Литература к курсу биохимии Основной Эллиот В. , Эллиот Д. Биохимия и молекулярная биология. М. , 2002 Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. М. , 1982 – 2002. Кнорре Д. Г. , Мызина С. Д. Биологическая химия. М. , 2003. Филиппович Ю. Б. Основы биохимии. М. , 1985 – 2000. Коничев А. С. , Севастьянова Г. А. Молекулярная биология. М. , 2003. Ленинджер А. Биохимия. М. , 1976, 1985.
Начало белки + аминокислоты.ppt