Биохимические нарушения белкового обмена.ppt
- Количество слайдов: 83

Биохимические нарушения белкового обмена. Биохимические нарушения соединительной ткани и мышц

Белки — это высокомолекулярные азотсодержащие органические соединения, минимальная структурная единица которых – аминокислота (АК). Аминокислоты соединены между собой пептидной связью. Простые белки состоят только из аминокислот, сложные белки (липопротеиды, гликопротеиды, нуклеопротеиды, хромопротеиды и др. ) помимо аминокислот содержат различные небелковые компоненты: липиды, углеводы, нуклеиновые основания, хромогены и другие вещества.

Функции белков : 1) структурная (структурная основа клеток, органеллы, фибриллярные белки); 2) транспортная (липопротеиды, гемоглобин, альбумин); 3) сократительная (мышечные белки — актин, миозин); 4) каталитическая (ферменты); 5) регуляторная (гормоны); 6) защитная (иммуноглобулины, антитела, интерферон; белки системы свертывания крови и фибринолиза); 7) энергетическая (распад аминокислот обеспечивает до 18% потребляемой энергии). 8) опорная – сухожилия, поверхности суставов соединения костей образованы в значительной степени белковыми веществами (пр. : коллаген, эластин). 9) рецепторная – многие белки участвуют в процессах избирательного узнавания (рецепторы).
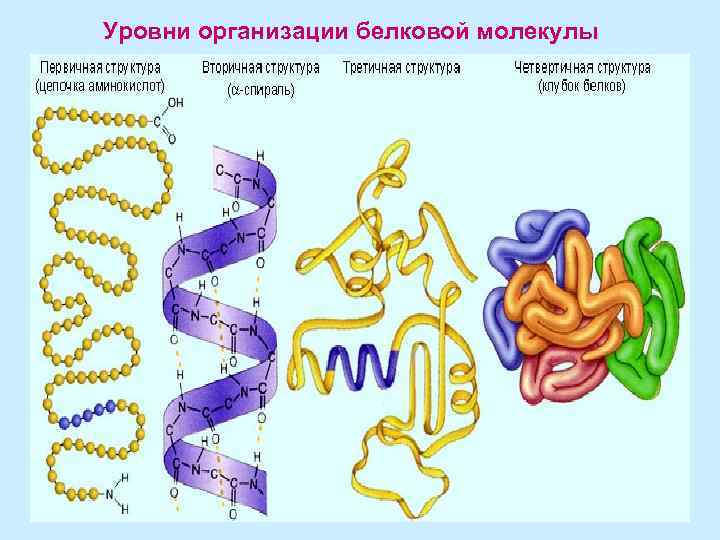
Уровни организации белковой молекулы

Простые белки состоят только из остатков аминокислот, представлены следующими белками: • Альбумины • Глобулины • Гистоны • Протамины Протеиноиды или склеропротеиды – это неполноценные белки, составляющие основу соединительной ткани. Представители: коллагены, эластины, кератины.
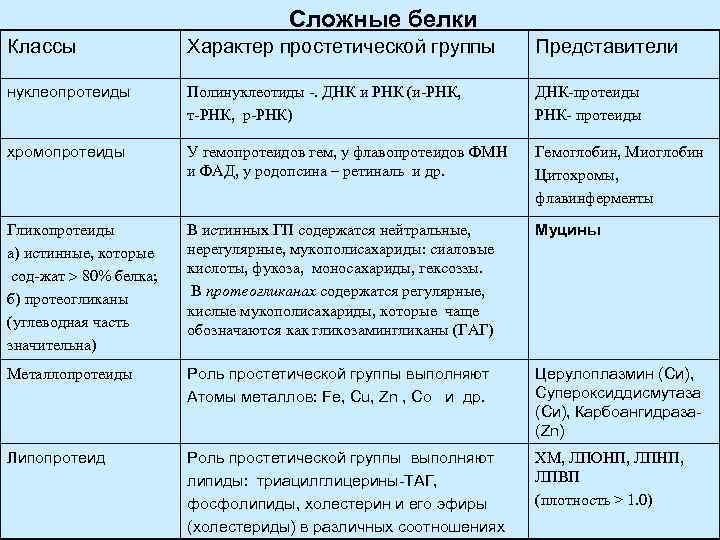
Сложные белки Классы Характер простетической группы Представители нуклеопротеиды Полинуклеотиды -. ДНК и РНК (и-РНК, т-РНК, р-РНК) ДНК-протеиды РНК- протеиды хромопротеиды У гемопротеидов гем, у флавопротеидов ФМН и ФАД, у родопсина – ретиналь и др. Гемоглобин, Миоглобин Цитохромы, флавинферменты Гликопротеиды а) истинные, которые сод-жат 80% белка; б) протеогликаны (углеводная часть значительна) В истинных ГП содержатся нейтральные, нерегулярные, мукополисахариды: сиаловые кислоты, фукоза, моносахариды, гексоззы. В протеогликанах содержатся регулярные, кислые мукополисахариды, которые чаще обозначаются как гликозамингликаны (ГАГ) Муцины Металлопротеиды Роль простетической группы выполняют Атомы металлов: Fe, Cu, Zn , Co и др. Церулоплазмин (Си), Супероксиддисмутаза (Си), Карбоангидраза(Zn) Липопротеид Роль простетической группы выполняют липиды: триацилглицерины-ТАГ, фосфолипиды, холестерин и его эфиры (холестериды) в различных соотношениях ХМ, ЛПОНП, ЛПНП, ЛПВП (плотность > 1. 0)

Обмен белков В обмене белков имеется ряд особенностей: • белки не могут быть заменены углеводами или жирами, так как для биосинтеза белков необходимы незаменимые аминокислоты, которые при обычном питании поступают в организм только с полноценными белками; • в отличие от углеводов и липидов белки в виде запаса в органах и тканях, как правило, не откладываются; исключение составляет печень, в которой синтезируются и откладываются белки плазмы крови.


• Важный критерий пищевой ценности белков – доступность АК. Аминокислоты большинства животных белков полностью высвобождаются в процессе пищеварения. Исключение составляют белки опорных тканей (коллаген и эластин). Белки растительного происхождения перевариваются в организме плотоядных плохо, т. к. содержат много волокон и иногда ингибиторы протеаз (соя, горох). Существенный критерий ценности пищевого белка – аминокислотный состав. Чем больше содержится незаменимых АК, тем полезнее данный белок для организма.

ОСОБЕННОСТИ ОБМЕНА БЕЛКОВ В ДЕТСКОМ ВОЗРАСТЕ Главной функцией белков у детей является пластическая. В первые дни жизни источником белка является материнское молоко, причем часть молочных альбуминов и глобулинов вместе с необходимыми антитоксинами и иммуноглобулинами всасываются из кишечника в кровь, не расщепляясь. Молозиво содержит ингибитор трипсина, предохраняющий иммуноглобулины от быстрого гидролиза. При искусственном вскармливании эти адаптивные особенности могут оборачиваться против новорожденного. Интактные белки коровьего молока и яиц способны всосаться через кишечный барьер и обеспечить энтеральную сенсибилизацию. При раннем переходе на смешанное и искусственное вскармливание перекрестная иммунная реактивность пептидов из состава альбуминов коровьего молока и человеческого инсулина может спровоцировать у носителей антигенов ГКГС D 3D 4 аутоиммунный ответ против собственных В-клеток, что приводит к сахарному диабету 1 типа.

В это время условия для переваривания белков обычной пищи еще мало благоприятны: кислотность желудочного сока мала, активность протеаз панкреатического сока возрастает еще медленнее, чем пепсина. Необходимо, чтобы ребенок получал полноценные белки, т. е, содержащие все незаменимые АК. Критерием благополучия белкового обмена в растущем организме является положительный азотистый баланс. Однако, на третий день после рождения у новорожденных отмечается отрицательный азотистый баланс из-за недостаточного поступления белков с пищей. • Распад, окисление АК и других азотсодержащих продуктов у ребенка идет теми же путями, что и у взрослого человека, с образованием одинаковых конечных продуктов. Своеобразие заключается в иных количественных соотношениях продуктов азотистого обмена: снижено процентное содержание азота мочевины в крови, но больше АК, мочевой кислоты, креатинина, аммонийных солей. • У детей раннего возраста наибольшей активностью отличается ферментная система, обеспечивающая синтез ДНК и РНК, более интенсивно протекает синтез белка во всех органах и тканях.

Концентрация белков плазмы определяется тремя основными факторами: • скоростью синтеза, • скоростью метаболизма и • объемом жидкости, в котором распределены белки. Основная масса белков плазмы синтезируется в печени. Гепатоциты участвуют в синтезе 95% альбуминов, в синтезе фибриногена, альфа и бетаглобулинов, компонентов свертывающей системы.

Нормальная интенсивность биосинтеза белка в тканях и органах определяется действием нескольких факторов: 1. Достаточным поступлением в организм пищевого белка (не менее 100 г/с), содержащего необходимое количество незаменимых АК. 2. Полноценным перевариванием белков в органах ЖКТ - обеспечивается ферментами желудка (пепсином, гастриксином), pancreas (трипсином, химотрипсином, карбоксипептидазой А и В, эластазой) и тонкого кишечника (энтеропептидазой). 3. Всасыванием продуктов гидролиза белков (AK) в тонком кишечнике, что предъявляет серьезные требования к состоянию слизистой оболочки тонкой кишки, ее моторике и наличию соответствующих транспортных белков — переносчиков AK. 4. Адекватным энергетическим обеспечением (АТФ, ГТФ) биосинтеза белков во всех тканях и органах (прежде всего — в печени) и его регуляцией анаболическими гормонами (половые гормоны, инсулин, СТГ гипофиза) и витаминами (С, В 6 и др. ). Нарушение действия любого из перечисленных факторов может привести к угнетению биосинтеза белков в организме и развитию белковой недостаточности. Концентрация белков в плазме здорового человека колеблется от 65 до 85 г/л. Основная часть общего белка плазмы крови (около 90%) приходится на альбумины, глобулины и фибриноген.

Нарушения обмена белков включают: • нарушения количественного поступления белка в организм (белковый перекорм и БЭН); • нарушения качественного состава белков (дефицит и избыток отдельных АК, причем последний может приводить как к их антагонизму, так и прямой токсичности); • нарушения переваривания белков в ЖКТ - кишечная аутоинтоксикация; • нарушения трансмембранного транспорта АК (расстройства кишечного всасывания и АК тубулопатии, синдром аминоацидурии); • нарушения промежуточного обмена АК (расстройства дезаминирования; взаимопревращения т. е. переаминирования; декарбоксилирования); • нарушения композиции белков плазмы (гипо- и диспротеинемии); • нарушения конечных этапов обмена белков (аномалии и недостаточность цикла мочевины)
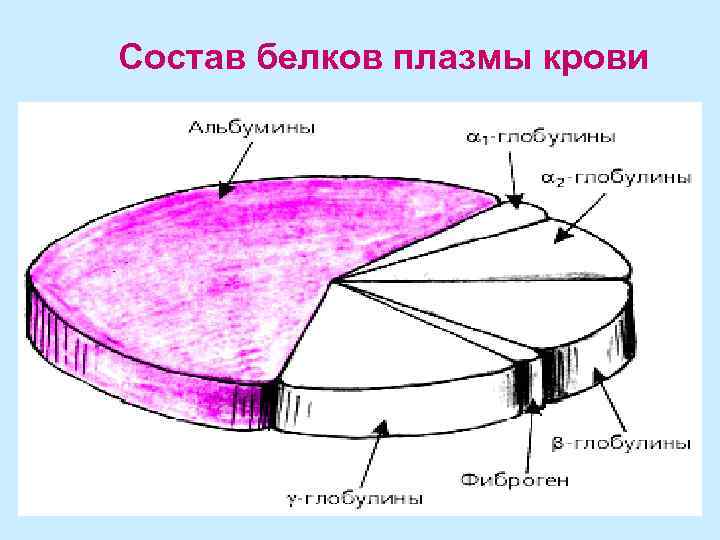
Состав белков плазмы крови

• Альбумины — это наиболее гомогенная фракция простых белков, синтезируются в печени (40% альбуминов - в плазме, а 60% — в межклеточной жидкости). Основные функции альбуминов: • поддержание онкотического давления, • участие в транспорте многих эндогенных и экзогенных веществ (свободных жирных кислот, билирубина, стероидных гормонов, ионов магния, кальция, антибиотиков, сердечных гликозидов, барбитуратов, ацетилсалициловой кислоты и др. ).

Глобулины сыворотки крови представлены 4 фракциями (α 1, α 2, β и γ), каждая из которых не является однородной и содержит несколько белков, отличающихся по своим функциям. • В состав α 1 -глобулинов в норме входят два белка, имеющих наибольшее клинической значение: - α 1 -антитрипсин - ингибитор ряда протеаз (трипсина, химотрипсина, калликреина, плазмина); - α 1 -гликопротеид - участвует в транспорте прогестерона и тестостерона и связывает небольшие количества этих гормонов. • α 2 -глобулины представлены следующими белками: - α 2 -макроглобулин — ингибитор ряда протеолитических ферментов (трипсина, химотрипсина, тромбина, плазмина, калликреина), синтезируется вне печени; - гаптоглобин — белок, связывающий и транспортирующий свободный гемоглобин А в клетки ретикулоэдотелиальной системы; - церулоплазмин — обладает оксидазной активностью и окисляет двухвалентное железо в трехвалентное, что обеспечивает его транспорт трансферрином; - апопротеиды А, В и С, входящие в состав липопротеидов.

Фракция β-глобулинов также содержит несколько белков: • трансферрин — участвует в транспорте трехвалентного железа; • гемопексин — переносчик свободного гема и порфирина, связывает геминсодержащие хромопротеиды (Нв, миоглобин, каталазу) и доставляет их в клетки РЭС и печени; • липопротеиды; • часть иммуноглобулинов; • некоторые белковые компоненты комплемента.

• γ-глобулины — это иммуноглобулины, которым свойственна функция антител, вырабатываемых в организме в ответ на внедрение различных веществ, обладающих антигенной активностью; современные методы позволяют выделить несколько классов иммуноглобулинов (Ig. G, Ig. A, Ig. M, Ig. D и Ig. E). • Фибриноген - важнейший компонент системы свертывания крови (фактор I). Он образует основу кровяного сгустка в виде трехмерной сети, в которой задерживаются клетки крови.

Методы исследования Стандартный набор биохимических показателей, отражающий состояние белкового обмена включает определение содержания • общего белка, • белковых фракций (альбумина, α 1 -, α 2 -, β- и γглобулинов) • фибриногена. При необходимости определяют также СРБ (CRP), содержание серомукоида и других белков сыворотки крови. Общий белок. . • Альбумин. • Белковые фракции – метод электрофореза для определения различных фракций белка (альбуминов, α 1 -, α 2 -, β- и γ-глобулинов); расчет альбуминовоглобулинового коэффициента (А/Г=1, 5)
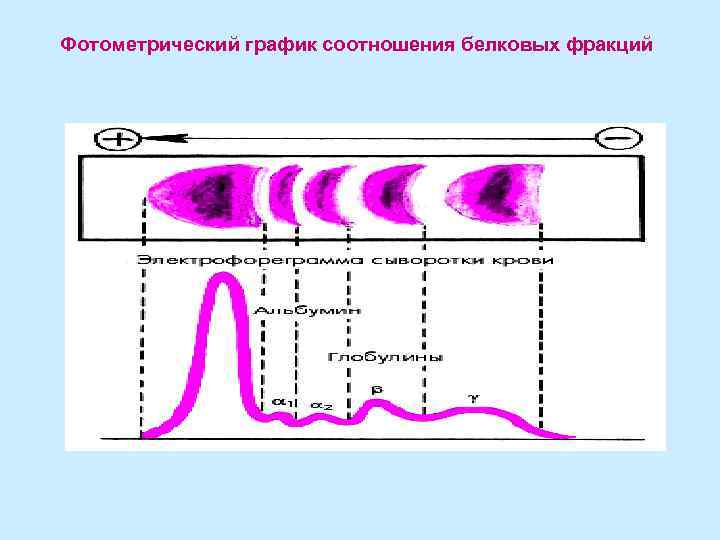
Фотометрический график соотношения белковых фракций
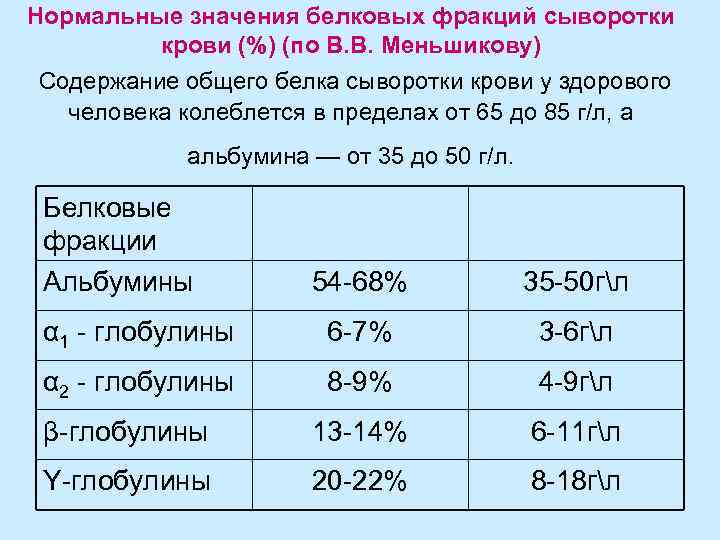
Нормальные значения белковых фракций сыворотки крови (%) (по В. В. Меньшикову) Содержание общего белка сыворотки крови у здорового человека колеблется в пределах от 65 до 85 г/л, а альбумина — от 35 до 50 г/л. Белковые фракции Альбумины 54 -68% 35 -50 гл α 1 - глобулины 6 -7% 3 -6 гл α 2 - глобулины 8 -9% 4 -9 гл β-глобулины 13 -14% 6 -11 гл Y-глобулины 20 -22% 8 -18 гл

Наиболее приемлемые и информативные в настоящее время - электрофоретические методы разделения белков. По скорости движения получают 5 фракций: альбумины, 1 -, 2 -, - и - глобулины. Каждая из них содержит несколько специфичных белков. Процедура электрофореза позволяет установить: • снижение содержания альбумина; • увеличение доли одной или нескольких фракций глобулинов; • появление белков, отсутствующих в крови здорового человека. • Введение в буферный раствор ионов кальция позволяет дополнительно разделить глобулиновую фракцию на две составляющие: 1 - и 2.

Общий белок плазмы – величина достаточно стабильная и у взрослых составляет 65 -85 г/л Изменение нормального содержания белка могут проявляться в 3 направлениях: • гиперпротеинемии • гипопротеинемии • парапротеинемии Изменения концентрации белка могут носить абсолютный или относительный характер и зависят от ОЦК. Так, гидремия приводит к относительной гипопротеинемии, дегидратация – к гиперпротениемии. Поэтому при определении общего количества белка необходимо знать ОЦК или величину гематокрита.
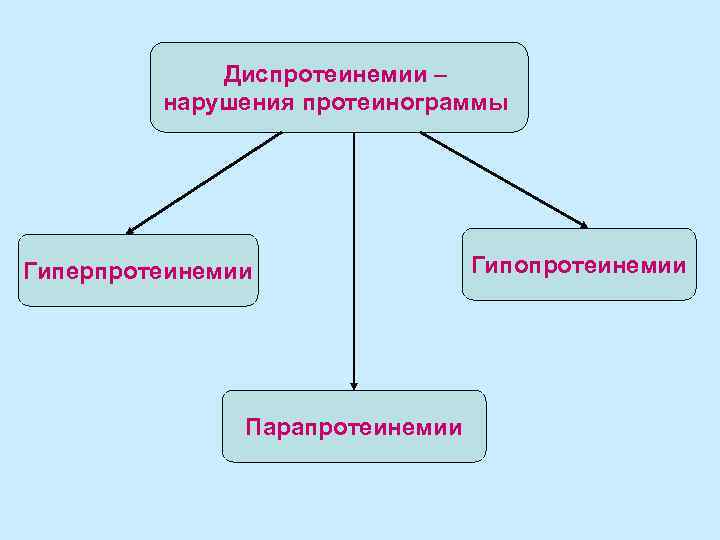
Диспротеинемии – нарушения протеинограммы Гиперпротеинемии Парапротеинемии Гипопротеинемии

Причины гипопротеинемии: • Физиологические: беременность и период лактации • Патологические: 1. Недостаточное поступление белков в организм 2. Недостаточное переваривание и всасывание пищевых белков (язвенная болезнь, гастроэнтериты, дизентерия, диспепсия). Хронические нарушения пищеварительного тракта инфекционного происхождения ведут к гипопротеинемии, выражающейся, прежде всего, гипоальбуминемией, если преобладающим компонентами заболевания являются понос и нарушения питания, связанные с отсутствием аппетита. В случае ведущей роли инфекционного фактора наблюдаются изменения в показателях альфа и гамма-глобулинов. 3. Нарушение синтеза белков печени (дефицит ферментов, участвующих в синтезе белка при ряде наследственных гипопротеинемий, заболевания печени – токсические гепатиты, хронические и острые гепатиты, циррозы печени, жировая дистрофия печени). 4. Резкое снижение реабсорбции белка в почечных канальцах (хронические заболевания почек с нефротическим компонентом, нефрозы). Нефротический синдром – наиболее частое и важное клиническое проявление гипопротениемий. При острых нефрозах гипопротеинемия и гипоальбуминемия незначительны и быстро восстанавливаются. Ведущие факторы, приводящие к снижению белка в этих случаях – рост проницаемости капилляров и переход низкомолекулярных альбуминов в ткань. При хронически протекающих процессах гипоальбуминемия достигает значительных размеров (до 25 -30 г/л) и может отрицательно влиять на течение заболевания.

Абсолютная гипопротеинемия возникает из-за снижения содержания альбумина. Это обусловлено: • недостаточным поступлением белка с пищей; • подавлением синтеза протеинов в печени; • повышенным их распадом в организме; • потерей белка; • его перемещением в другие ткани; • дефектопротеинемиями - наследственно обусловленными нарушениями в синтезе белков; • особенности физиологического состояния организма. Гипопротеинемия почти всегда связана с гипоальбуминемией, тогда как гиперпротеинемия – с гиперглобулинемией.

• Гиперпротеинемия – чаще всего развивается относительная гиперпротеинемия: при нарушениях гемодинамики и сгущении крови, потере жидкости при дегидратации (неукротимая рвота, понос), несахарном диабете, холере, в первые дни ожоговой болезни, в послеоперационном периоде. В ряде случаев развивается и абсолютная гиперпротеинемия, обусловленная увеличением уровня глобулинов. Гиперпротеинемия обнаруживается при паразитарных заболеваниях – малярии, токсоплазмозе (до 100 -120 г/л).

• Парапротеинемия – появление в плазме необычных белков, в норме не присутствующих

Остаточный азот Конечный этап белкового обмена включает в себя биохимические процессы, приводящие к образованию азотсодержащих конечных метаболитов. Термин «остаточный азот» используется для обозначения небелковых азотсодержащих веществ крови. К основным компонентам остаточного азота относятся: • мочевина – 50% • креатин – 5 – 7, 5%, • креатинин – 2, 5 - 3% • АК – 25%, • мочевая кислота – 4% • индикан и другие азот содержащие небелковые соединения Большинство низкомолекулярных азотистых веществ равномерно распределено между плазмой и форменными элементами крови, поэтому ОА с равным успехом можно определять как в сыворотке, так и в цельной крови. • У здорового взрослого человека уровень остаточного азота составляет 14 -25 ммоль/л.

В поддержании постоянного уровня ОА в крови участвуют печень, выполняя мочевинообразовательную функцию и почки, осуществляя выведение азотистых метаболитов; определение ОА и его отдельных компонентов проводится с двоякой целью: • для оценки мочевиносинтетической функции печени и выявления печеночной недостаточности • для диагностики нарушения выделительной функции почек и оценки степени почечной недостаточности
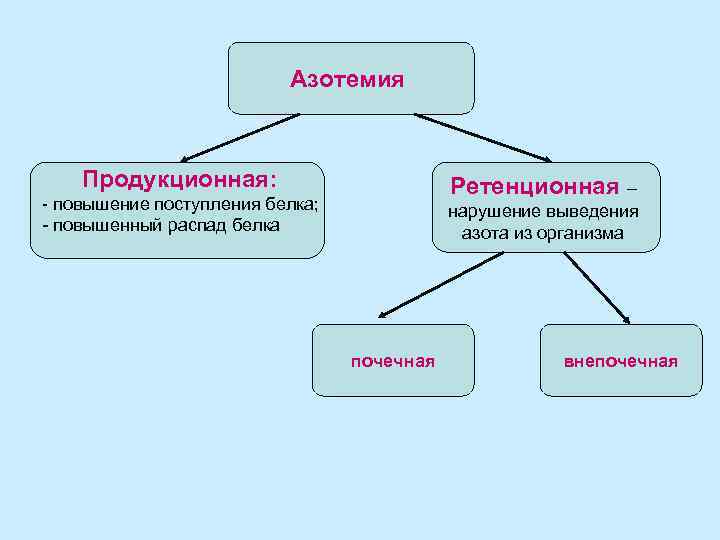
Азотемия Продукционная: Ретенционная – - повышение поступления белка; - повышенный распад белка нарушение выведения азота из организма почечная внепочечная

Мочевина – 2, 5– 8, 3 ммоль/л, беспороговое вещество Почечная ретенционная азотемия Уровень мочевины: ХПН – в начальный период мочевина достигает 13 ммоль/л, в динамике нарастает ОПН – повышение мочевины в крови до 16 ммоль/л – нарушение функции средней тяжести от 16 -33, 2 ммоль/л – тяжелое поражение функции почек выше 49, 8 ммоль/л – очень тяжелое нарушение с неблагоприятным прогнозом

Ретенционная внепочечная: • нарушение гемодинамики при ССН • при обезвоживании (неукротимая рвота, кровотечения, профузный понос, ожоги, травмы) Содержание мочевины при ретенционной внепочечной азотемии не превышает 13 ммоль/л.

Продукционная азотемия • кахексия • лейкоз Уровень мочевины 8 -10 ммоль/л. При нарушении функции печени снижается синтез мочевины, параллельно повышается уровень аммиака: - печеночная кома - острый некроз печени - цирроз - отравления Мочевиносинтетическую функцию печень утрачивает, если поражено 75% паренхимы печени (циррозы печени, хронический активный гепатит и др. ) в результате нарушения синтеза мочевины в печени. В этих случаях не происходит достаточного обезвреживания аммиака в организме, что является одной из причин развития печеночной комы. • Низкая концентрация мочевины может быть обусловлена также диетой с низким содержанием белка или нарушением всасывания аминокислот в тонком кишечнике (целиакия).

Креатинин • Креатинин — это конечный продукт метаболизма креатина. Последний синтезируется в организме (преимущественно в почках и печени) из 3 АК — аргинина, глицина и метионина. При фосфорилировании он превращается в креатинфосфат, являющийся важнейшим источником энергии для мышечного сокращения. В процессе использования энергии органического фосфата образуется креатинин.

Схема биосинтеза креатинина в организме

• Креатинфосфат накапливается ночью, а днем расходуется при физической нагрузке • Креатинин полностью выделяется из организма почками, преимущественно путем клубочковой фильтрации, не реабсорбируясь в почечных канальцах. Это важное свойство креатинина используется для исследования уровня клубочковой фильтрации по клиренсу креатинина в сыворотке крови и моче. Интерпретация результатов • Концентрация креатинина в сыворотке крови здоровых людей относительно постоянна и составляет 1– 2 мг/дл или 60– 125 мкмоль/л. • Увеличение содержания креатинина в сыворотке крови в большинстве случаев свидетельствует о снижении азотовыделительной функции почек и, в первую очередь, о нарушении клубочковой фильтрации, хотя на ранних стадиях острой или хронической почечной недостаточности этот показатель изменяется мало. • Уменьшение концентрации креатинина в некоторых случаях может наблюдаться при уменьшении мышечной массы.

• Креатинурия (креатин в моче) бывает физиологической и патологической • Физиологическая: - у детей-подростков - у стариков – атрофия мышц - у беременных (матка мышечный орган) Почечный порог креатина 120 мкмоль/л

• Патологическая креатинурия - миопатии, мышечные дистрофии, миастении, периферические параличи; - заболевания, связанные с нарушением обмена АТФ (СД, инфекции, переохлаждения, болезни печени – нарушение образования креатинина и креатин в моче); - БА – 10 кратное повышение креатина в моче не связанное с приемом гормонов; - некоторые ЛС – вит С, экстракты печени и поджелудочной железы, АКТГ

Аммиак – 11, 6 мкмоль/л – высокотоксичный продукт, легко проникает через липидные мембраны. Больше всего NH 3 формируют органы с наиболее интенсивным обменом АК и биогенных аминов (мозг, печень, ЖКТ, почки). Повышение NH 3 в крови наблюдается • при заболеваниях печени (цирроз, ХВГ)- 58 мкмоль/л; • печеночная кома – 116 мкмоль/л развивается печеночная энцефалопатия; • шоковая печень – острое отравление, при переливании несовместимой крови – 174 мкмоль/л – глубокая кома.

Мочевая кислота • Мочевая кислота является конечным продуктом метаболизма пуриновых оснований, входящих в состав нуклеотидов (РНК и ДНК) и нуклеопротеидов. Мочевая кислота синтезируется в печени и полностью выводится с мочой, соли плохо растворяются в воде и накапливаются в суставах. Интерпретация результатов • У взрослого здорового человека концентрация мочевой кислоты в сыворотке крови составляет 3– 4 мг/дл, или 180– 530 мкмоль/л. Изменение концентрации мочевой кислоты в сыворотке крови зависит: • от интенсивности ее образования в печени, • от скорости выделения почками. Определенное значение имеет также содержание в крови уратсвязывающего протеина.

Причины повышения содержания мочевой кислоты в крови (гиперурикемии): 1. Подагра - увеличение синтеза мочевой кислоты в связи с повышением активности фосфорибозилпирофосфатсинтетазы, катализирующей первую реакцию синтеза пуриновых оснований. 2. Некоторые болезни крови (лейкозы, полицитемия, В 12 -дефицитные анемии, злокачественные новообразования, массивные ожоги и другие заболевания, сопровождающиеся усиленным распадом белка и образованием нуклеопротеидов). 3. Некоторые заболевания желез внутренней секреции (акромегалия, гипопаратиреоз, сахарный диабет). 4. Нарушение выделения мочевой кислоты почками (почечная недостаточность, свинцовая нефропатия, поликистоз почек, ацидоз, токсикоз беременности). 5. Пища, богатая пуринами (мясо, печень, почки). 6. Ожирение, гиперлипопротеидемии, атеросклероз, артериальные гипертензии. Уменьшение концентрации мочевой кислоты в крови наблюдается при: • 1. Гепатоцеребральной дегенерации печени — болезни Вильсона. Коновалова. • 2. Лимфогранулематозе. • 3. Миеломной болезни и других заболеваниях.

• При многих патологических состояниях в основе нарушений белкового обмена лежит сочетание сразу нескольких механизмов. Например, при злокачественных новообразованиях ЖКТ в основе гипопротеинемии может лежать не только угнетение синтеза белка на уровне клеток, обусловленное раковой интоксикацией, снижением активности анаболических гормонов, недостатком витаминов и нарушением функции печени при ее метастатическом поражении, но и недостаточное поступление вследствие характерной для этих заболеваний анорексии, нарушение переваривания и всасывания пищевых белков в ЖКТ, увеличение катаболизма белков и потеря их через ЖКТ. • Любые причины, приводящие к белковой недостаточности (например белковое голодание), закономерно вызывают усиление катаболизма собственных белков при их распаде, что сказывается на функции всех органов и систем. • Наиболее важными клиническими следствиями гипопротеинемии любого происхождения являются: - похудание, вплоть до кахексии, - анемия, - гипопротеинемические отеки (при снижении альбумина ниже 20 г/л), - нарушение функции различных органов и систем.

• • Запомните 1. Наиболее частыми причинами увеличения содержания α-глобулинов являются острые воспалительные заболевания и заболевания, сопровождающиеся значительным повреждением и распадом тканей. 2. Увеличение β-глобулинов (особенно при сочетании с гипергаммаглобулинемией) чаще свидетельствует об активации иммунной системы организма у больных с разнообразными острыми или хроническими заболеваниями внутренних органов, хотя необходимо также учитывать возможность влияния гиперлипопротеидемии, особенно у больных с атеросклерозом, сахарным диабетом, гипотиреозом и нефротическим синдромом. 3. Увеличение содержания γ-глобулинов может быть также обусловлено значительной активацией иммунной системы или так называемыми парапротеинемиями (миеломной болезнью или макроглобулинемией Вальденстрема). 4. Уменьшение α-глобулинов чаще может быть связано с тяжелыми деструктивными процессами в печени, протекающими с нарушениями синтеза белка. 5. Гипогаммаглобулинемия свидетельствует о наличии ИДС, вызванного истощением иммунной системы организма при длительных хронических заболеваниях, длительном лечении цитостатиками, иммунодепрессантами, глюкокортикоидами и лучевыми воздействиями. 6. Избыточная потеря белка организмом (энтериты, массивные ожоги, нефротический синдром), помимо гипоальбуминемии, может сопровождаться уменьшением содержания γ-глобулинов.

Белки острой фазы воспаления и их значение для организма • На любой повреждающий фактор всегда развивается ряд реакций (воспаление), направленных на локализацию очага повреждения и скорейшее восстановление поврежденных функций. Сумма местных изменений, возникающих в ответ на повреждение, получила наименование острой фазы воспаления. Важнейшую роль в этом процессе играют белки острой фазы (БОФ), синтезируемые в печени и всегда реагирующие на действие повреждающего фактора либо увеличением, либо уменьшением концентрации. Более того, БОФ проявляют свое действие до развития основной защитной реакции местного и общего иммунного ответа.

В понятие БОФ входит около 30 белков плазмы крови Функции БОФ: 1. Ограничение очага повреждения 2. Участие в репаративных процессах 3. Участие в реакции клеточного и гуморального иммунитета 4. Влияние на неспецифическую резистентность организма, в том числе на фагоцитарную активность лейкоцитов. 5. Воздействие на сосудисто-тромбоцитарный гемостаз, процесс свертывания крови и фибринолиз


Реакцию острой фазы вызывают ИЛ-1, ИЛ-6, интерфероны и ФНО Стимулом для системной реакции острой фазы воспаления служат: • травматические и раневые повреждения тканей, • инфекция, • злокачественный клеточный рост Реакцию острой фазы в первую очередь составляют • сонливость и гиподинамия → к защитной мобилизации АК из белков скелетных мышц. • участие иммунитета в реакции острой фазы - нейтрофилия со сдвигом лейкоформулы влево и рост содержания в плазме крови Ig. • сдвиги эндокринной регуляции метаболизма - гипергликемия, рост СЖК и глицерина, высвобождению в кровь несбалансированной смеси аминокислот. • превалирование на системном уровне эффектов контринсулярных гормонов → к толерантности по отношению к глюкозе. • гипоферремия. • на уровне печени реакцию острой фазы - усиленный глюконеогенез и синтез белков острой фазы.

• Белки острой фазы - это иммуномодуляторы, протеины с прямым или опосредованным бактерицидным и (или) бактериостатическим действием, медиаторы воспаления, хемоаттрактанты и неспецифические опсонины, ингибиторы первичной альтерации, синтез которых растет в печени в острый период воспаления после определенного распространения его очага в пределах здоровых тканей. К ним относят белки, мигрирующие при электрофорезе в геле в его области альфа-1 и альфа-2: • альфа-1 -антитрипсин, альфа-1 кислый гликопротеин, амилоид А и Р, антитромбин III, С-реактивный белок, ингибитор С-1 -эстеразы, фракцию комплемента СЗ, церуллоплазмин, трансферрин, гаптоглобулин, орозомукоид, плазминоген. • Рост концентрации БОФ в циркулирующей крови - маркер острого воспаления. Наиболее чувствительна к острому воспалению концентрация в плазме крови СРБ - связывается с полисахаридом С на поверхности Streptococcus pneumoniae. С-реактивный белок активирует • систему комплемента, подавляет функции тромбоцитов и лимфоцитов, • тормозит ретракцию сгустка и стимулирует фагоцитоз нейтрофилами.

Свойства белков острой фазы 1) Антиоксидантные - церулоплазмин, амилоид, гаптоглобин, СРБ, транскобаламин и α 2 -макроглобулин 2) Антимикробные - СРБ, лактоферрин, факторы комплемента 3) Регулирующие гемостаз и антигемостаз - факторы коагуляции и антикоагулянты 4) БОФ ограничивают поступление железа и цинка в ткани, снижают его доступность для микроорганизмов, улавливают и транспортируют в макрофаги эти микроэлементы (гаптоглобин, лактоферрин, и снижение продукции трансферрина). Гипоферремия и гипоцинкемия очень существенны для повышения антибактериальной резистентности (Zn и Fe — ростовые факторы ряда бактерий, в частности, Грам(-), обладающих белками-сидерофиллинами). Ограничение доступности Fe также снижает интенсивность свободно-радикальных цепных процессов, повреждающих ткани.

• Во время ответа острой фазы в ряде мезенхимальных клеток и тканей (остеокластах костей, суставной синовии, хряще, фибробластах и гистиоцитах соединительной ткани, скелетных мышцах) индуцируется синтез коллагеназ и активатора плазминогена. В эндотелии возникает усиление продукции прокоагулянтов и молекул клеточной адгезии, синовиоциты секретируют больше синовиальной жидкости, а мышцы освобождают протеазы. Эпителиальные клетки реагируют укреплением базальных мембран за счёт синтеза коллагена IV типа. Тем не менее, проницаемость капилляров и посткапиллярных венул растёт, так как стимулируется трансцитоз. Увеличивается общая протеолитическая активность плазмы, а при крайне интенсивной реакции утрачивается специфичность протеолиза (протеолитический взрыв), что соответствует активации сторожевой полисистемы плазмы.

• Важные изменения происходят в центральном звене нейроэндокринной регуляции. Усиливается Δ-волновая активность нейронов, способствующая медленному сну. Это вызывает угнетение работоспособности. Активируется микроглия, стимулируется продукция АКТГ и вазопрессина - провоцирует чувство тревоги и способствует стрессу. Меняется состояние центров терморегуляции и аппетита, что сопровождается анорексией и ограничением теплоотдачи, в то время, как теплопродукция может возрастать → лихорадка.

• Происходит усиление катаболизма: распад жира, гликогена, усиление глюконеогенеза, в скелетно-мышечной системе превалирует распад белков до АК → транспортируются в печень и участвуют в глюконеогенезе и синтезе БОФ. • Ослабляется эффективность действия инсулина - гипергликемия и состояние, напоминающее транзиторный псевдодиабет. • Организм переходит на активное использование эндогенных источников энергии: мышечная масса значительно уменьшается → гипераминацидемия, отрицательный азотистый баланс, увеличивается потеря с мочой фосфатов, сульфатов, калия и АК, креатина, креатинина и мочевой кислоты. • Все эти изменения обратимы и не означают дегенерации мышц. Хорошее питание во время острой фазы реакции на повреждение не предотвращает этих изменений, которые носят запрограммированный характер. • Ч. Динарелло считает, что цитокины направляют поток пластических эквивалентов — аминокислот — в костный мозг и лимфоидную ткань, а также в печень. Метаболические нужды ЦНС и сердца при этом предохраняются гормонами стресса. В результате складывается перераспределение метаболических ресурсов в пользу наиболее активных участников острого ответа на травму и антигенную агрессию.

• При ответе острой фазы организм сберегает внеклеточную воду и натрий, экскреция которого в мочу, слюну, пот и другие жидкости сильно уменьшается. Реабсорбция Na растет в почках и в ЖКТ. Увеличивается выведение катионов Н+ в мочу, в обмен на Na. Задерживается бикарбонат, формируется тенденция к внеклеточному дыхательному алкалозу, который может смениться метаболическим лактат-ацидозом, по мере развития относительной гипоксии. • Решающим значением для реализации всей динамики преиммунного ответа обладают ИЛ-6, ИЛ-1, ИЛ-8, ФНО-α, ΦΗΟ-β, ИФН-α, ИФН-γ, а также симпатическая нервная система и гормоны, участвующие в стрессе.
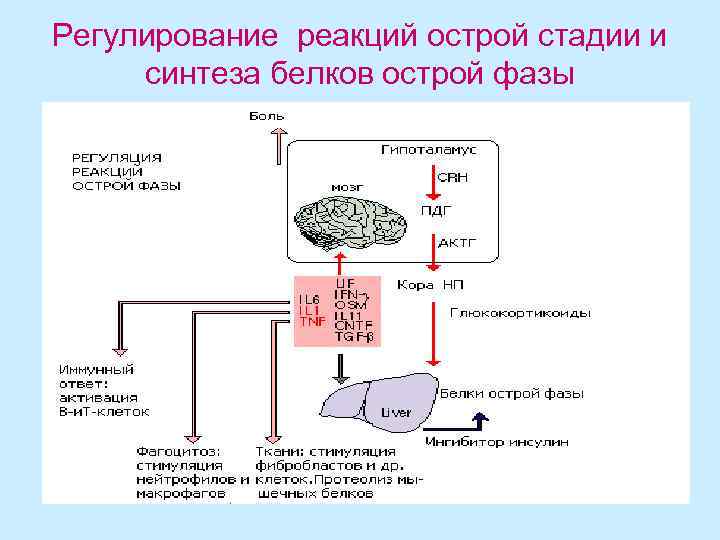
Регулирование реакций острой стадии и синтеза белков острой фазы
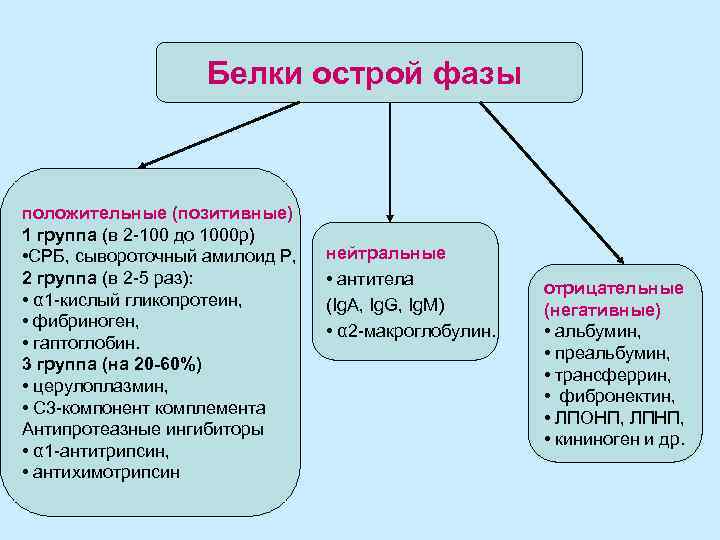
Белки острой фазы положительные (позитивные) 1 группа (в 2 -100 до 1000 р) • СРБ, сывороточный амилоид Р, 2 группа (в 2 -5 раз): • α 1 -кислый гликопротеин, • фибриноген, • гаптоглобин. 3 группа (на 20 -60%) • церулоплазмин, • С 3 -компонент комплемента Антипротеазные ингибиторы • α 1 -антитрипсин, • антихимотрипсин нейтральные • антитела (Ig. A, Ig. G, Ig. M) • α 2 -макроглобулин. отрицательные (негативные) • альбумин, • преальбумин, • трансферрин, • фибронектин, • ЛПОНП, ЛПНП, • кининоген и др.

• Концентрация положительных БОФ увеличивается в первые 24 -48 ч после воздействия повреждающего фактора. При этом создаются условия для ингибиции активности протеаз, нейтрализации токсических молекул, усиления клиренса продуктов разрушающихся мембран и хроматина погибающих клеток. В результате образуются комплексы, которые затем удаляются РЭС или распадаются и утилизируются в печени. • Приблизительно одновременно с позитивными БОФ , или с небольшим запозданием, начинают реагировать и негативные БОФ. Однако их функция сводится к повышению концентрации свободных лигандов (витаминов, гормонов, микроэлементов, БАВ, жирных кислот).

• Основными продуцентами сывороточных БОФ являются гепатоциты. Универсальными продуктами реакций острой фазы воспаления являются ЛПС Гр() бактерий. • При воспалении, инфекционных заболеваниях, ожогах, травме, нормальной и патологической беременности всегда увеличивается содержание провоспалительных цитокинов (IL-1, IL-6, TNFa и др), стимулирующих образование позитивных и снижение продукции негативных БОФ. Чем тяжелее протекает заболевание, тем сильнее изменяется содержание БОФ. Тенденция к нормализации БОФ является важным прогностическим признаком, свидетельствующим о затухании патологического процесса.

• К главным БОФ относят СРБ и сывороточные амилоидные А-белки. Уровень этих БОФ возрастает очень быстро (в первые 6 -8 ч), их концентрация увеличивается в 2 -100, а иногда и в 1000 раз. Нет никакого сомнения, что подобные реакции носят защитный характер.

СРБ - это комплекс соединений, обладающих различными свойствами: • стимулирует продукцию супероксидного аниона в фагоцитах; • увеличивает синтез провоспалительных цитокинов IL-1α и β и TNFa, играющих важную роль не только в развитии воспаления, но и в регуляции синтеза БОФ, а также в иммунном ответе; • оказывает влияние на функцию Т-хелперов, киллеров и NK, что сказывается на интенсивности иммунного ответа и естественной цитотоксичности; • участвует в экспрессии тканевого фактора моноцитами и макрофагами и тем самым усиливает течение ДВС; • способствует агрегации тромбоцитов, секреции серотонина из αгранул; • стимулирует образование тромбаксана А 2 – вызывает необратимую агрегацию тромбоцитов и остановку кровотечения из мелких сосудов с низким кровяным давлением.

• Сывороточные амилоидные А-белки являются апопротеинами ЛПВП и предшественниками основного компонента фибрилл реактивного амилоида. Последний обладает чрезвычайной устойчивостью, он нарушает структуру тканей и мешает выполнению их функций.

Сывороточный амилоид Р или SАР – основная функция - защита матрикса от повреждения протеолитическими ферментами: • в присутствии лиганда способен отменять действие агрегированного СРБ на агрегацию и секрецию тромбоцитов; • усиливает антикоагулянтный эффект низких доз гепарина; • способен вступать во взаимосвязь с белками системы комплемента; • участвует в клиренсе ядерного материала поврежденных клеток.

• Вторую группу составляют белки, концентрация которых может увеличиваться существенно в 2 -5 раз: • α 1 -кислый гликопротеин, сывороточный амилоид Р, α 1 -антитрипсин, фибриноген, гаптоглобин.

α 1 -кислый гликопротеин (1 мг/мл) транспортный белок, способен: • связывать гистамин и некоторые ЛС; • ингибирует образование АТ и подавляет реакции клеточного иммунитета; • проявляя сродство к гепарину препятствует взаимодействию его с АТ 3; • усиливает агрегацию тромбоцитов, способствуя развитию ДВС;

• Фибриноген 2 -4 г/л – увеличение способствует ограничению распространения инфекции; в то же время при свертывании крови от фибриногена отщепляются фибринопептиды А и В, которые обладают выраженным противовоспалительным действием и препятствуют распространению тромбов по сосудам; • фибриноген, переходя в фибрин, способствует репарации поврежденных тканей

• Гаптоглобин – связывает Нв с образованием комплекса, обладающего пероксидазной активностью; • ингибирует катепсины, участвует в утилизации некоторых патогенных бактерий

К 3 группе относятся белки, концентрация которых в течение первых 2 -х суток после воздействия патогенного раздражителя увеличивается незначительно на 20 -60%: • церулоплазмин – переносит медь, мощный антиоксидант, стимулирует гемопоэз, усиливает адгезию лейкоцитов к эндотелию, увеличивает синтез оксида азота • С 3 и С 4 -компоненты комплемента

Нейтральные БОФ • антитела (Ig. A, Ig. G, Ig. M) • α 2 -макроглобулин. Концентрация их изменяется незначительно, так как их усиленный синтез сопровождается не менее сильным расходом.

Отрицательные (негативные) БОФ • альбумин, • преальбумин, • трансферрин, • фибронектин, • ЛПОНП, ЛПНП, • кининоген и др. Их расход при воспалении преобладает над синтезом. Уменьшение концентрации этих белков компенсирует увеличение положительных БОФ и тем самым способствует сохранению постоянства онкотического давления крови.
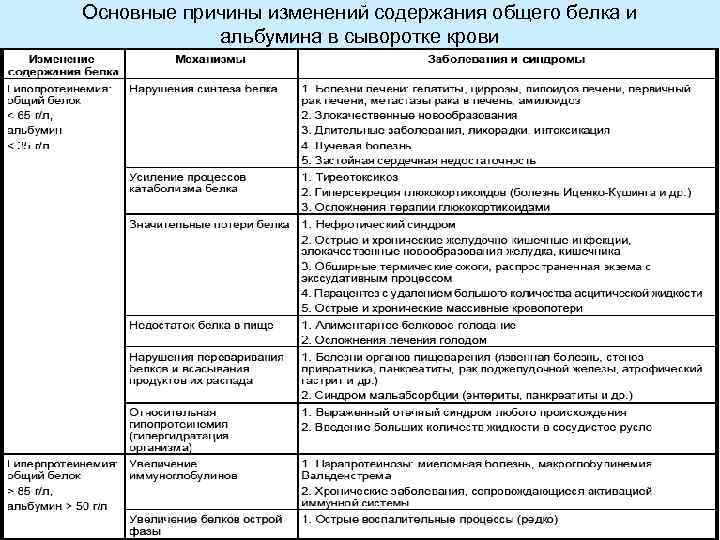
Основные причины изменений содержания общего белка и альбумина в сыворотке крови


• • • увеличение содержания α 1 - и α 2 -фракций глобулинов наблюдается при нескольких патологических состояниях: 1. При острых воспалительных процессах, поскольку в состав α-глобулинов входят так называемые белки острой фазы (α 1 -антитрипсин, α 1 -гликопротеид, α 2 -макроглобулин, гаптоглобулин, церулоплазмин, серомукоид, С-реактивный белок). 2. При значительном повреждении и распаде тканей (дистрофические, некротические процессы), сопровождающемся деструкцией клеток и высвобождением тканевых протеаз, калликреина, тромбина, плазмина и т. д. , что закономерно приводит к увеличению содержания их естественных ингибиторов (α 1 -антитрипсина, α 1 -гликопротеида, α 2 -макроглобулина и др. ). Повреждение тканей приводит также к высвобождению патологического Среактивного белка, являющегося продуктом распада клеток и входящего в состав α 1 -фракции глобулинов. Значительная деструкция тканей наблюдается при злокачественных новообразованиях, метастазировании опухолей, тяжелых травмах, после оперативных вмешательств, при инфарктах различных органов (ишемический инсульт, инфаркт легкого, кишечника и др. ). 3. При заболеваниях, сопровождающихся деполимеризацией гликопротеидов основного вещества соединительной ткани (коллагенозах), преимущественно за счет увеличения содержания гаптоглобулина и других белков. 4. При нефротическом синдроме, в частности за счет увеличения α 2 макроглобулина. 5. Во время беременности — преимущественно за счет стимулирующего действия эстрогенов на синтез церулоплазмина, входящего в состав фракции α 2 -глобулинов.

• • • Уменьшение содержания α-глобулинов в клинической практике встречается достаточно редко. Иногда оно наблюдается: 1. При тяжелых деструктивных процессах в паренхиме печени: при остром инфекционном гепатите, гепатолентикулярной дегенерации печени (болезни Вильсона-Коновалова), синдроме гепатоцеребральной дегенерации (болезни Вестфаль-Штрумпфель. Вильсона), при циррозах и раке печени, хроническом активном гепатите. В этих случаях уменьшение содержания α-глобулинов связывают со снижением синтеза гаптоглобулина, церулоплазмина, α 1 гликопротеида. 2. При гемолизе эритроцитов, гемоглобинуриях, что объясняется усилением процесса связывания гаптоглобулина свободным гемоглобином. 3. При врожденном дефиците α 1 -антитрипсина, входящего в состав α 1 -фракции глобулинов и являющегося ингибитором тканевых протеаз, в том числе эластазы, разрушающей эластические волокна. Дефицит α 1 -антитрипсина может приводить к повреждению легочной ткани и развитию первичной диффузной деструктивной эмфиземы легких. 4. При снижении содержания α 2 -макроглобулина — ингибитора некоторых протеолитических ферментов поджелудочной железы (трипсина, химотрипсина). Считают, что в некоторых случаях (редко) дефицит α 2 -макроглобулина может способствовать поражению поджелудочной железы (панкреатит, сахарный диабет).

• Увеличение фракции β-глобулинов наблюдается: • 1. При первичных и вторичных гиперлипопротеидемиях, особенно II типа (подробнее — см. ниже), поскольку большая часть сложных белков липопротеидов входит в состав βфракции глобулинов. Вторичные гиперлипопротеидемии чаще встречаются при атеросклерозе, сахарном диабете, гипотиреозе, нефротическом синдроме. • 2. При длительных хронических заболеваниях, сопровождающихся увеличением содержания в крови иммуноглобулинов (обычно одновременно с увеличением содержания γ-глобулинов): хронических инфекциях, циррозе печени, болезнях соединительной ткани (ревматизм, РА, СКВ и др. ), злокачественных новообразованиях, аутоиммунных и аллергических заболеваниях. • Уменьшение фракции β-глобулинов встречается редко: • 1. При абеталипопротеидемии. • 2. При атрансферринемии — редком заболевании, обусловленном дефицитом основного транспортного белка — трансферрина, что приводит к развитию железодефицитной анемии и вызывает картину гемосидероза (отложения железа во внутренних органах) с развитием гепатоспленомегалии.

• • • Увеличение фракции γ-глобулинов обнаруживают при следующих патологических состояниях: 1. При заболеваниях, сопровождающихся интенсификацией иммунных процессов, поскольку фракция γ-глобулинов состоит главным образом из иммуноглобулинов: при хронических инфекциях, хронических заболеваниях печени (хронический гепатит и циррозы печени), аутоиммунных заболеваниях (в том числе заболеваниях соединительной ткани — РА, СКВ и др. ), хронических аллергических заболеваниях (бронхиальная астма, рецидивирующая крапивница, лекарственная болезнь, атопический дерматит, экзема и др. ). 2. При парапротеинемиях — заболеваниях, сопровождающихся образованием патологических белков (парапротеинов), относящихся к одному из классов иммуноглобулинов (G, А, реже D и Е): миеломной болезни (плазмоцитоме), макроглобулинемии Вальденстрема, болезни тяжелых цепей и др. Уменьшение фракции γ-глобулинов встречается: 1. При длительных хронических заболеваниях, сопровождающихся истощением иммунной системы и снижением образования иммуноглобулинов (хронических инфекциях, злокачественных новообразованиях, заболеваниях почек, печени, лимфолейкозе, лимфогранулематозе и др. ). 2. При лечении цитостатиками, иммунодепрессантами, глюкокортикоидами, а также в результате рентгеновского облучения, применения радионуклидов или лучевой терапии. 3. При разнообразных иммунодефицитных состояниях, связанных с поражением В- и Тлимфоцитов (агаммаглобулинемия Брутона, атаксия-телеангиоэктазия — синдром Луи-Бар и др. ). 4. При избыточной потере белка (энтериты, нефротический синдром, обширные ожоги). Приведенные данные свидетельствуют о том, что в каждом конкретном случае интерпретация протеинограммы чрезвычайно сложна и должна учитывать не только возможный нозологический диагноз, но и индивидуальные особенности клинической картины заболевания, его длительность, эффективность лечения, факт приема некоторых лекарственных препаратов, применения лучевой терапии, состояние иммунной системы, наличие сопутствующих заболеваний и т. п. Тем не менее в большинстве случаев практический врач должен ориентироваться на следующие принципиальные положения:

• Основные цитокиновые эффекторы ответа острой фазы: 1. Интерлейкин-1, стимуляторами выделения IL-1 являются: • Компоненты клеточных стенок бактерий (ЛПС и мурамилдипептид — бактериальный пептидогликан), действующие на клеточный рецептор CD 14, присущий макрофагам, клеткам Лангерганса и, возможно, гранулоцитам. • Медиаторы воспаления, выделямые активированными клетками. Стимуляция ЛПС ведет к синтезу ИЛ-1 (макрофаги, макрофагоподобные дендритические и глиальные клетки, эндотелий, фибробласты, В-лимфоциты и некоторые эпителиальные клетки – кератиноциты). К экспрессии генов ИЛ-1 способны любые ядерные клетки организма; на всех клетках организма есть его рецепторы. Это делает ИЛ-1 наиболее разнообразным среди всех цитокинов, участвующих в формировании ответа острой фазы. ИЛ-1 — наиболее пирогенный из цитокинов, является пептидом медленного сна. Его снотворный эффект обусловливает снижение работоспособности и гиподинамию при продромальном синдроме; способен оказывать кортиколиберинподобное действие на гипофиз и стимулировать продукцию АКТГ и кортикостероидов. Это ведет к усилению стресса при преиммунном ответе. ИЛ-1β подавляет гипоталамическую секрецию соматолиберина и стимулирует выработку соматостатина, что вызывает ослабление анаболизма при ответе острой фазы. Протеолиз и освобождение аминокислот из скелетных мышц, а также усиление секреции синовиальной жидкости и резорбтивные изменения в костях и хрящах, проявляющиеся костно-мышечно-суставными болями, в значительной степени, зависят от ИЛ-1, индуцирующего синтез коллагеназ и активатора плазмина в этих тканях. ИЛ-1 в высоких дозах снижает продукцию инсулина островками Лангерганса. Это хемоаттрактант лейкоцитов и индуктор дегрануляции нейтрофилов, причём последний эффект он опосредует через ИЛ-8. ИЛ-1 — центральный «провокатор» всей системы цитокинов. Кроме ИЛ-8, он способен активизировать продукцию ИЛ-6 и колониестимулирующих факторов, обеспечивающих лейкоцитоз, а также фактора некроза опухолей, собственного мощного синергиста.

2. Фактор некроза опухолей (ФНО) известен в виде двух фракций — кахексина (ΦΗΟα), вырабатываемого макрофагами, лимфоцитами, адипоцитами и тучными клетками, а также микроглией и лимфотоксина (ΦΗΟβ), продукта Т-лимфоцитов. Первый представляет собой мономер, а второй — тример одной и той же субъединицы с молекулярным весом около 17 к. Д. ФНОα вызывает озноб и лихорадку до 39°С через 1 ч. после внутривенного введения человеку в несколько больших дозах, нежели интерлейкин-1: 50 -100 нг/ кг массы тела. Помимо пирогенного, ФНО проявляет много других важных эффектов. Кахексин тормозит активность центра голода и стимулирует центр насыщения в гипоталамусе, являясь сильным анорексигеном. Гиперпродукция ФНО мононуклеаров и, возможно, глиальными опухолями, служит морфологической основой своеобразного синдрома, который характеризуется полной потерей аппетита и глубоким исхуданием. Ранее это состояние считалось психогенным и носит исторически сложившееся название «нейрогенная анорексия» . Кахексия при инфекциях, особенно, хронических гранулёматозных процессах , а также при опухолях и лейкозах, раневое истощение — связаны с продукцией во всех этих ситуациях ФНОα Именно этот цитокин вызывает анорексию и гиперкатаболизм в ходе ответа острой фазы. Он же является сильным контринсулярным фактором. ФНО это активатор эндотелия и всех видов лейкоцитов (в первую очередь, их цитотоксических функций), стимулятор клеточной адгезии. Он способствует переходу макрофагов в многоядерные гигантские клетки, синтезирующие ещё больше ФНО. Под влиянием ФНО возможно усиление ангиогенеза, он участвует в запуске синтеза белков острой фазы печенью и усиливает экспрессию антигенов ГКГС и Fc-рецепторов на самых разных мишенях. Не детализируя иммунологических функций ФНО, хотелось бы привлечь внимание к его способности при высоких дозах индуцировать апоптоз гепатоцитов, клеток ЖКТ, эндотелиоцитов и даже нейронов ФНО и ИЛ-1 особенно токсичны при совместном действии. Они способны блокировать мембранное пищеварение и перистальтику кишечника, провоцировать рвоту и понос, вызывать деструкцию гепатоцитов, провоцировать гиперкалиемию и ацидоз. Совместное токсическое действие этих цитокинов, при их массированном освобождении и долгом нахождении в кровотоке может быть летально. Они стимулируют эндотелий к продукции коагулянтов, в частности, тромбоксана А 2 и лейкотриена Е 4 и способствуют ДВС-синдрому, увеличивают выработку фактора активации тромбоцитов, окиси азота и миокардиального депрессорного полипептида. Последний вырабатывается в поджелудочной железе и апудоцитарных клетках предсердий, вызывает вазоконстрикцию во внутренних органах и снижение сократимости миокарда.

• • Именно эти медиаторы ответственны за проявления токсико-септического шока, гипотензию, падение сердечного выброса и системные микроциркуляторные расстройства, вызывающие плюриорганную недостаточность при сепсисе и тяжелых инфекциях. Изолированное асептическое введение кахексина в вену крысам в дозах, соответствующих обнаруживаемым при септическом шоке количествам, вызывает у животных гипотензию, ацидоз, гемоконцентрацию, гипергликемию, гипокалиемию и смерть при явлениях дыхательной недостаточности. На вскрытии обнаруживаются проявления тромбогеморрагического синдрома и некротические изменения в почках, ЖКТ и лёгких. ФНО тормозит экспрессию генов эндогенных опиатов — мощных противошоковых агентов. Именно поэтому поликлональная стимуляция лимфоцитов и массированная активация бактериальными липополисахаридами макрофагов ведут к такому гиперергическому ходу ответа острой фазы, который оборачивается шоком. Ниже, в главе «Иммунный ответ» это иллюстрируется при обсуждении эффекта так называемых суперантигенов, сверхактивных стимуляторов продукции ИЛ-1 и ФНО. [362] По некоторым данным, ФНО наиболее активный, ключевой для запуска продукции всех медиаторов шока агент, по крайней мере, антитела к ФНО резко ослабляют проявления септического шока. ФНО очень активно стимулирует продукцию различными клетками эндогенных окислителей, что и приводит к их некробиозу и/или апоптозу. Он вызывает с помощью оксида азота парез микрососудов с падением артериального давления и, активируя эндотелий, способствует ДВС‑синдрому. Выработанный в ответ на ФНО Pg. E 2 служит обратным отрицательным регулятором биосинтеза ФНО. Для предупреждения токсико-септического шока организм располагает и другими ингибиторами действия ФНО и ИЛ-1, которые также входят в цитокиновый каскад

• Интерлейкин-6 (ИЛ-6) синтезируется активированными моноцитами, фибробластами, эндотелиоцитами, Т-лимфоцитами и некоторыми Вклонами. Это важнейший индуктор синтеза «белков острой фазы» , то есть, глобулинов, плазменная концентрация которых возрастает при любом воспалении, инфекции, иммунопатологическом процессе. Мишенью его действия служат гепатоциты, тимоциты и лимфоциты. Для миелоидных полустволовых клеток он служит ростовым фактором, способствуя продукции всех гранулоцитов, моноцитов, тромбоцитов и эритроцитов. Это дифференцировочный пептид для плазматических клеток, синтезирующих антитела, а также для злокачественного клона при миеломной болезни, стимулятор пролиферации кератиноцитов кожи и мезангиальных клеток почек. Есть данные о его роли в терморегуляции и индукции лихорадки, но как регулятор собственно температурного гомеостаза ИЛ-6 наименее пирогенен. если сравнивать его с другими цитокинами. Так. при внутривенном введении человеку он вызывает лихорадку до 39"С в достаточно большой дозе 1 микро-грамм на кг массы тела. По-видимому, этот сигнал, в основном, предназначен для осуществления нетемпературных компонентов ответа острой фазы. Синтез ИЛ-6 стимулируется ИЛ-1 и фактором некроза опухолей. ИЛ-6 гораздо более стабилен, чем его индукторы, поэтому считается, что именно этот цитокин вносит решающий вклад в осуществление ответа острой фазы при его нормергическом течении. Даже значительные позы ИЛ-6 не вызывают некроза или апоптоза клеток и. не являются летальными, в отличие от вышеописанных регуляторов. По-видимому именно данный цитокин направляет нормергический ответ острой фазы.

• ИЛ-8 вырабатываются макрофагами и клетками кожи по сигналу ИЛ -1. Эти регуляторы обусловливают активацию хемотаксиса и краевого стояния различных видов лейкоцитов. ИЛ-8 стимулирует освобождение дефензинов из нейтрофилов, и таким образом усиливает атаку «хозяина» на внедрившиеся микроорганизмы. • Некоторые аспекты ответа острой фазы потенцируются интерферонами (слабый пирогенный эффект, препятствуют репликации и сборке вирусов, оказывают гормоноподобные эффекты). ИФН вырабатываются в фибробластах (ИФН-α). макрофагах (ИФН‑β), и лимфоцитах (ИФН-γ). • Перестройка метаболизма при ответе острой фазы зависит и от активации симпатической нервной системы и стрессорных, нейроэндокринных механизмов. Возрастает продукция и действие КА, ГКС, вазопрессина, альдостерона, глюкагона, парат-гормона. Цитокины стимулируют симпатоадреналовую и кортикостероидную активность. • Основная часть гормонов стресса ингибирует и лихорадку, и ответ острой фазы, в целом. Глюкокортикоиды — мощные ингибиторы экспрессии интерлейкиновых генов и синтеза метаболитов арахидоновой кислоты, сдерживающие интенсивность острофазного ответа. Фактически, стресс и цитокиновый ответ находятся в неоднозначных взаимоотношениях, удерживая острофазную реакцию от чрезмерности.

Помимо глюкокортикоидов и других гормонов существуют и полипептидные тканевые ингибиторы цитокинового каскада, которые понижают интенсивность преиммунного ответа, не давая развиться шокоподобному состоянию. К ним относятся ингибиторы ИЛ-1, выделенные из мочи и плазмы крови: • Гликопротеин с MB 30 -35 к. Д ингибирующий ИЛ-1 -зависимую пролиферацию лимфоцитов и так называемый «уромодулин» (белок Тамма-Хорсфалла), высокоаффинно связывающий ИЛ-1. • Гликопротеин 18 к. Д — конкурентный блокатор клеточных рецепторов для ИЛ-1 (IL-1 Rα). • Ингибирующим действием характеризуются растворимые сывороточные антагонисты самих молекул интерлейкинов -1 и -6, а также рецепторов ФНО. • Ингибиторными функциями обладают цитокины-блокаторы каскада — ИЛ-10, а также трансформирующий фактор роста-β. Интерфероны блокируют некоторые аспекты активации лимфоцитов при ответе острой фазы (пролиферацию иммунокомпетентных клеток (ИФН-α, β), синтез Ig. E (ИФН-γ) и экспрессию антигенов ГКГС II класса (ИФН-α, β).

• Обнаруживаемые в норме и при патологии аутоантитела к интерлейкинам и интерферонам, тоже могут обслуживать ингибиторные механизмы ответа острой фазы. • Итак, цитокиновый ответ, который начинается немедленно, после контакта ретикуло-эндотелиальных элементов и лейкоцитов организма с патогенами и их продуктами, позволяет осуществить координированную перестройку обмена веществ и физиологических функций ряда органов и тканей. Вместе с тем, эта форма системной защиты связана с определёнными издержками для организма: ухудшаются реологические свойства крови в микрососудах, возрастает вероятность тромбоза, уменьшается снабжение тканей железом и цинком. Избыточное функционирование цитохимического каскада ведет к шокоподобным состояниям и ДВС-синдрому. Хроническая гиперпродукция белков острой фазы, особенно, амилоида А и Е, является фактором риска амилоидоза, который может развиваться при затяжных инфекциях и воспалениях. • Наиболее хорошо изученной частью ответа острой фазы является лихорадка, в которую непосредственно переходят продромальные симптомы.
Биохимические нарушения белкового обмена.ppt