РОЛЬ печени в обмене веществ.ppt
- Количество слайдов: 44

БИОХИМИЧЕСКАЯ РОЛЬ И ФУНКЦИИ ПЕЧЕНИ В ОБМЕНЕ ВЕЩЕСТВ.
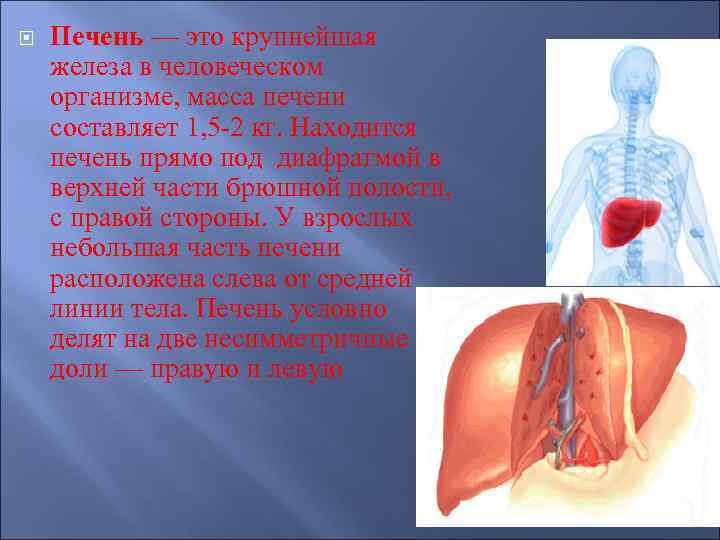
Печень — это крупнейшая железа в человеческом организме, масса печени составляет 1, 5 -2 кг. Находится печень прямо под диафрагмой в верхней части брюшной полости, с правой стороны. У взрослых небольшая часть печени расположена слева от средней линии тела. Печень условно делят на две несимметричные доли — правую и левую

Функции печени. 1. Углеводный обмен 2. Белковый обмен 3. Жировой обмен 4. Желчеобразование 5. Запасание витаминов 6. Гормоны, образование и расщепление 7. Детоксикация

1. Углеводный обмен

Глюкоза и другие моносахариды, поступающие в печень, превращаются ею в гликоген. Гликоген откладывается в печени как «сахарный резерв» . В гликоген помимо моносахаридов превращается и молочная кислота, продукты расщепления белков (аминокислоты), жиров (триглицериды и жирные кислоты). Все эти вещества начинают превращаться в гликоген в том случае, если углеводов пище не хватает. По мере необходимости, при расходовании глюкозы гликоген здесь же в печени превращается в глюкозу и поступает в кровь. Содержание гликогена в печени независимо от приема пищи подвержено определенному ритмическому колебанию в течение суток. Наибольшее количество гликогена содержится в печени ночью, наименьшее – в течении дня. Это связано с активным расходом энергии днем и образованием глюкозы. Синтез гликогена из других углеводов и расщепление до глюкозы имеет место как в печени, так и в мышцах. Однако образование гликогена из белка и жира возможно только в печени[1], в мышцах этот процесс не протекает.

Пировиноградная кислота и молочная, жирные кислоты и кетоновые тела – то, что называют токсинами усталости - утилизируются в основном в печени и преобразуются в глюкозу. В организме высоктренированного спортсмена более 50% всей молочной кислоты преобразуется в печени в глюкозу. Только в печени происходит «цикл трикарбоновых кислот» , которые иначе называют «циклом Кребса» по имени английского биохимика Кребса, который, кстати говоря, жив до сих пор. Ему принадлежат классические труды по биохимии, в т. ч. и современный учебник. Сахарный галлостаз[2] необходим для нормальной деятельности всех систем и органом. В норме количество углеводов в крови составляет 80 -120 мг% (т. е. мг на 100 мл крови), и их колебания не должны превышать 20 -30 мг%. Значительное понижение содержания углеводов в крови (гипогликемия), а также стойкое повышение их содержания (гипергликемия) могут привести к тяжелым для организма последствиям.

Во время всасывания сахара из кишечника, содержание глюкозы в крови воротной вены может достигать 400 мг%. Содержание сахара в крови печеночной вены и в периферической крови повышается при этом лишь незначительно и редко достигает 200 мг%. повышение содержания сахара в крови сразу включает «регуляторы» , встроенные в печень. Глюкоза превращается, с одной стороны, в гликоген, который ускоряется, с другой стороны, она используется для получения энергии, а если и после этого остается избыток глюкозы, то она превращается в жир. В последнее время появились данные о способности образования из глюкозы заменителя аминокислот, однако процесс носит в организме органический характер и развивается только в организме высококвалифицированных спортсменов. При понижении уровня глюкозы (длительное голодание, большой объем физических нагрузок) в печени происходит расщепление глюкогена, а если этого недостаточно, то превращаются в сахар аминокислоты и жиры, которые затем превращаются в гликоген.
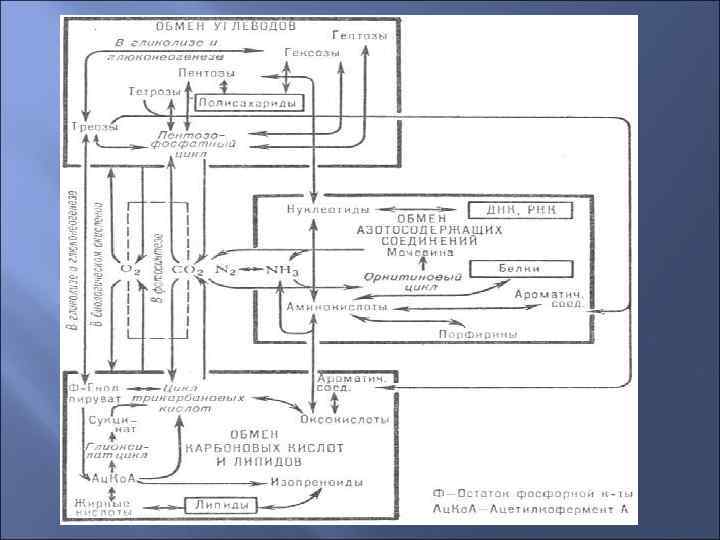

Роль печени в углеводном обмене

Печень — главный орган, в паренхиматозных клетках которого происходят биохимические превращения продуктов пищеварительного гидролиза углеводов и превращение их в глюкозу — форму, доступную для клеток организма. Печень — депо углеводов, так как часть глюкозы хранится здесь в виде гликогена. Печень поддерживает содержание глюкозы в крови на постоянном уровне — в этом состоит глюкостатическая функция печени. При избытке глюкозы в печени происходит синтез гликогена из глюкозы — гликогенез. После приема пищи богатой углеводами содержание гликогена может составлять до 8% веса печени. В среднем, запасы гликогена составляют около 5% веса печени, что у взрослого человека эквивалентно примерно 90 г глюкозы.
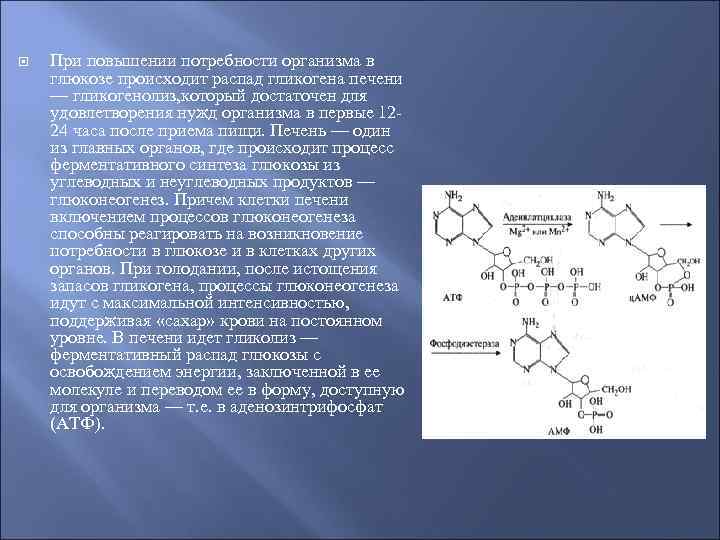
При повышении потребности организма в глюкозе происходит распад гликогена печени — гликогенолиз, который достаточен для удовлетворения нужд организма в первые 1224 часа после приема пищи. Печень — один из главных органов, где происходит процесс ферментативного синтеза глюкозы из углеводных и неуглеводных продуктов — глюконеогенез. Причем клетки печени включением процессов глюконеогенеза способны реагировать на возникновение потребности в глюкозе и в клетках других органов. При голодании, после истощения запасов гликогена, процессы глюконеогенеза идут с максимальной интенсивностью, поддерживая «сахар» крови на постоянном уровне. В печени идет гликолиз — ферментативный распад глюкозы с освобождением энергии, заключенной в ее молекуле и переводом ее в форму, доступную для организма — т. е. в аденозинтрифосфат (АТФ).

2. Белковый обмен Роль печени в белковом обмене заключается в расщеплении и «перестройке» аминокислот, образовании химически нейтральной мочевины из токсичного для организма аммиака, а также в синтезе белковых молекул. Аминокислоты, которые всасываются в кишечнике и образуются при расщеплении тканевого белка, составляют «резервуар аминокислот» организма, который может служить как источником энергии, так и строительным материалом для синтеза белков. Изотонными методами было установлено, что в организме человека в стуки расщепляется и вновь синтезируется 80 -100 г белка. Приблизительно половина этого белка трансформируется в печени. Об интенсивности белковых превращений в печени можно судить по тому, что белки печени обновляются примерно за 7 (!) дней. В других органах этот процесс происходит как минимум за 17 дней. В печени содержится так называемый «резервный белок» , который идет на нужды организма в том случае, если не хватает белка с пищей. При двухдневном голодании печень теряет примерно 20% своего белка, в то время, как общая потеря белка всех других органов составляет только около 4%. Трансформация и синтез недостающих аминокислот могут происходить только в печени; даже если печень удалить на 80%, такой процесс, как дезаминирование, сохраняется. Образование заменимых аминокислот в печени идет через образование глютаминовой и аспарагиновой кислоты, которые служат как бы промежуточными звеном. Избыточное количество той или иной аминокислоты подвергается снижению сначала до пировиноградной кислоты, а потом в цикле Кребса до воды и углекислого газа с образованием энергии, запасаемой в виде АТФ.

В процессе деземинирования аминокислот – отщепления от них аминогрупп, образуется большое количество токсичного аммиака. Печень преобразует аммиак в нетоксичную мочевину (карбамид), который затем почками выводится из организма. Синтез мочевины происходит только в печени и нигде больше. Синтез белков плазмы крови – альбуминов и глобулинов происходит в печени. Если произошла кровопотеря, то при здоровой печени содержание белков плазмы крови очень быстро восстанавливается при больной печени такое восстановление значительно замедляется.

3. Жировой обмен Печень может депонировать жира намного больше, чем гликогена. Так называемый «структурный липоид» – структурные липиды печени фосфолипиды и холестерин составляют 10 -16% сухого вещества печени. Это количество довольно постоянно. Помимо структурного липоида печень имеет включения нейтрального жира, сходного по своему составу с жиром подкожной клетчатки. Содержание нейтрального жира в печени подвержено значительным колебаниям. В целом же, можно сказать, что печень имеет определенный жировой запас, который при дефиците нейтрального жира в организме может расходоваться на энергические нужны. Жирные кислоты при дефиците энергии могут хорошо окисляться в печени с образованием энергии, запасаемой в виде АТФ. В принципе, жирные кислоты могут окисляться и в любых других внутренних органах, однако процентное соотношение будет таким: 60% печень и 40% все остальные органы. Желчь, выделяемая печенью в кишечник, эмульгирует жиры, и только лишь в составе такой эмульсии жиры могут впоследствии всасываться в кишечнике. Половина имеющегося в организме холестерина синтезируется в печени и лишь другая половина имеет пищевое происхождение.

Механизм окисления печенью жирных кислот был выяснен в начале нашего века. Он сводится к так называемому b-окислению. Окисление жирных кислот происходит до 2 -го углеродного атома (b-атома). Получается более короткая жирная кислота и уксусная кислота, которая потом превращается в ацетоуксусную. Ацетоуксусная кислота превращается в ацетон, а новая b-окисленная кислота подвергается окислению с большим трудом. И ацетон и bокисленная кислота объединяют под одним названием «кетоновые тела» .

Для расщепления кетоновых тел нужно достаточно большое количество энергии и при дефиците глюкозы в организме (голодание, диабет, длительные аэробные нагрузки) у человека изо рта может появиться запах ацетона. У биохимиков даже есть такое выражение: «жиры сгорают в огне углеводов» . Для полного сгорания, полной утилизации жиров до воды и углекислого газа с образованием большого количества АТФ необходимо хотя бы небольшое количество глюкозы. Иначе процесс застопорится на стадии образования кетоновых тел, которые сдвигают р. Н крови в кислую сторону, вместе с молочной кислотой принимая участие в формировании усталости. Не зря их поэтому и называют «токсинами усталости» . На жировой обмен в печени влияют такие гормоны, как инсулин, АКТГ, диабетогенный фактор гипофиза, глюкокортикоиды. Действие инсулина способствует накоплению жира в печени. Действие АКТГ, диабетогенного фактора, глюкокортикоидов прямо противоположно. Одна из важнейших функций печени в жировом обмене – это образование жира и сахара. Углеводы – непосредственный источник энергии, а жиры – важнейшие запасы энергии в организме. Поэтому при избытке углеводов и, в меньшей степени белков, преобладает синтез жира, а при недостатке углеводов доминирует глюконеогенез (образование глюкозы) из белка и жира.

4. Желчеобразование Желчь, вырабатываемая печенью, как мы уже говорили, принимает активное участие в переваривании жиров. Однако дело не ограничивается всего лишь их эмульгированием. Желчь активизирует жирорасщепляющий фермент липозу панкреатического и кишечного сока. Желчь также ускоряет всасывание в кишечнике жирных кислот, каротина, витаминов Р, Е, К, холестерина, аминокислот, солей кальция. Желчь стимулирует перистальтику кишечника. За сутки печень вырабатывает не менее 1 л желчи. Желчь представляет собой зеленовато-желтую жидкость слабощелочной реакции. Главные компоненты желчи: соли желчных кислот, желчные пигменты, холестерин, лецитин, жиры, неорганические соли. Печеночная желчь содержит до 98% воды. По своему осмотическому давлению, желчь равна плазме крови. Из печени желчь по внутрипеченочным желчным ходам поступает в печеночный проток, оттуда ее непосредственно выделяется через пузырный проток попадает в желчный пузырь. Здесь происходит концентрация желчи вследствие всасывания воды. Плотность пузырной желчи 1, 026 -1, 095.

Часть веществ, входящих в состав желчи синтезируется непосредственно в печени. Другая часть образуется вне печени и после ряда метаболических изменений выводится с желчью в кишечник. Таким образом, желчь образуется двумя путями. Одни ее компоненты фильтруются из плазмы крови (вода, глюкоза, креатинин, калий, натрий, хлор), другие образуются в печени: желчные кислоты, глюкурониды, парные кислоты и т. д. Важнейшие желчные кислоты холевая и дезоксихолевая в соединении с аминокислотами глицином и таурином образуют парные желчные кислоты – гликохолевую и таурохолевую. Печень человека вырабатывает в сутки 10 -20 г желчных кислот. Попадая с желчью в кишечник, желчные кислоты расщепляются с помощью ферментов кишечных бактерий, хотя большая их часть подвергается обратному всасыванию кишечными стенками и вновь оказывается в печени. С калом выделяется лишь 2 -3 г желчных кислот, которые в результате разлагающего действия кишечных бактерий меняют зеленый цвет на коричневый и изменяют запах.

Таким образом, существует как бы печеночно-кишечный кругооборот желчных кислот. Если необходимо увеличить выведение желчных кислот из организма (например, с целью выведения из организма больших количеств холестерина), то принимаются вещества, необратимо связывающие желчные кислоты, которые не позволяют желчным кислотам всасываться в кишечнике и выводят их из организма вместе с калом. Самыми эффективными в этом плане являются специальные ионообменные смолы (например, холестирамин), которые будучи принятыми внутрь, способны связать в кишечнике очень большое количество желчи и, соответственно, желчных кислот. Ранее с этой целью использовали активированный уголь. Используют, впрочем и теперь. Свойством абсорбировать желчные кислоты и выводить их из организма обладает клетчатка овощей и фруктов, но в еще большей степени пектиновые вещества. Наибольшее количество пектиновых веществ содержится в ягодах и фруктах, из которых можно приготовить желе без применения желатина. В первую очередь, это красная смородина, затем, по желеобразующей способности за ней следуют черная смородина, крыжовник, яблоки. Примечательно, что в печеных яблоках пектинов содержится в несколько раз больше, нежели в свежих. В свежем яблоке содержатся протопектины, которые при печении яблок превращаются в пектины. Печеные яблоки – непременный атрибут всех диет, когда нужно удалить из организма большое количество желчи (атеросклероз, заболевания печени, некоторые отравления и т. д. ).

Желчные кислоты помимо всего прочего могут образовываться из холестерина. При употреблении мясной пищи, количество желчных кислот увеличивается, при голодании – уменьшается. Благодаря желчным кислотам и их солям, желчь выполняет свои функции в процессе пищеварения и всасывания. Желчные пигменты (основной из них билирубин) не принимают участие в пищеварении. Их выделение печенью – чисто экскрегорный выделительный процесс. Билирубин образуется из гемоглобина разрушенных эритроцитов в селезенке и особых клетках печени (купферовские клетки). Не зря селезенку называют кладбищем эритроцитов. В отношении билирубина главной задачей печени является его выделение, а не образование, хотя немалая часть его образуется именно в печени. Интересно то, что распад гемоглобина до билирубина осуществляется при участии витамина С. Между гемоглобином и билирубином имеется множество промежуточных продуктов, способных ко взаимному превращению друг в друга. Часть их выделяется с мочой, а часть с калом. Образование желчи регулируется центральной нервной системой путем разнообразных рефлекторных влияний. Желчеотделение происходит непрерывно, усиливаясь во время еды. Раздражение чревного нерва приводит к уменьшению образования желчи, а раздражение блуждающего нерва и гистамины увеличивают образование желчи. Желчевыделение, т. е. поступление желчи в кишечник происходит периодически в результате сокращения желчного пузыря в зависимости от приема пищи и ее состава.

5. Запасание витаминов

Все жирорастворимые витамины (А, Д, Е, К и др. ) всасываются в стенки кишечника только в присутствии желчных кислот, выделяемых печенью. Некоторые витамины (А, В 1, Р, Е, К, РР и др. ) депонируются печенью. Многие из них участвуют в химических реакция, происходящих в печени (В 1, В 2, В 5, В 12, С, К и др. ). Часть витаминов активизируется в печени, подвергаясь в ней фосфорицированию (В 1, В 2, В 6, холин и др. ). Без фосфорных остатков эти витамины совершенно неактивны и часто нормальный витаминный баланс в организме больше зависит от нормального состояния печени, чем от достаточного поступления того или иного витамина в организм. Как видим, в печени могут депонировать как жирорастворимые, так и водорастворимые витамины, только время депонирования жирорастворимых витаминов, конечно, несоизмеримо больше, нежели водорастворимых.

6. Гормоны, образование и расщепление

Распад стероидных гормонов в печени является ферментативным процессом. Большая часть стероидных гормонов инактивируется, соединяясь в печени с глюкуроновой жирной кислотой. При нарушении функции печени в организме в первую очередь повышается содержание гормонов коры надпочечников, которые не подвергаются полному расщеплению. Отсюда возникает очень много различных заболеваний. Больше всего накапливается в организме альдостерона минералокортикоидного гормона, избыток которого приводит к задержке натрия и воды в организме. В результате возникают отеки, подъем артериального давления и т. д. В печени в значительной степени происходит инактивация гормонов щитовидной железы, антидиуретического гормона, инсулина, половых гормонов. При некоторых заболеваниях печени мужские половые гормоны не разрушаются, а превращаются в женские. Особенно часто такое расстройство возникает после отравления метиловым спиртом. Сам по себе избыток андрогенов, вызванный введением большого количества их извне, может привести к усилению синтеза женских половых гормонов. Существует, очевидно, некий порог содержания андрогенов в организме, превышение которого приводит к превращению андрогенов в женские половые гормоны. Хотя, в последнее время появились публикации о том, что некоторые лекарственные препараты способны предотвратить превращение в печени андрогенов в эстрогены. Такие препараты называют блокаторами.

Помимо вышеперечисленных гормонов печень инактивирует нейромедиаторы (катехоламины, серотонин, гистамин и многие другие вещества). В некоторых случаях даже развитие психических заболеваний вызвано неспособностью печени инактивировать те или иные нейромедиаторы.

7. Детоксикация

Очищение печени: Печень является главной "биохимической фабрикой" организма. Печень сильно влияет на общее самочувствие, функции мозга, качество сна, состояние кожи и другие характеристики организма. Поэтому здоровье печени - ключ к здоровью всего организма. "Очищение печени", разумеется, - термин для упрощения понимания. С научной точки зрения очищение печени предполагает решение следующих задач: 1. Улучшение процессов детоксикации различных вредных веществ (токсинов) в печени. 2. Улучшение процессов образования и оттока желчи, ведь именно с желчью обеспечивается вывод из печени в полость кишечника большинства токсинов. 3. Разгрузка клеток печени от избыточного жира.

Роль печени в белковом обмене
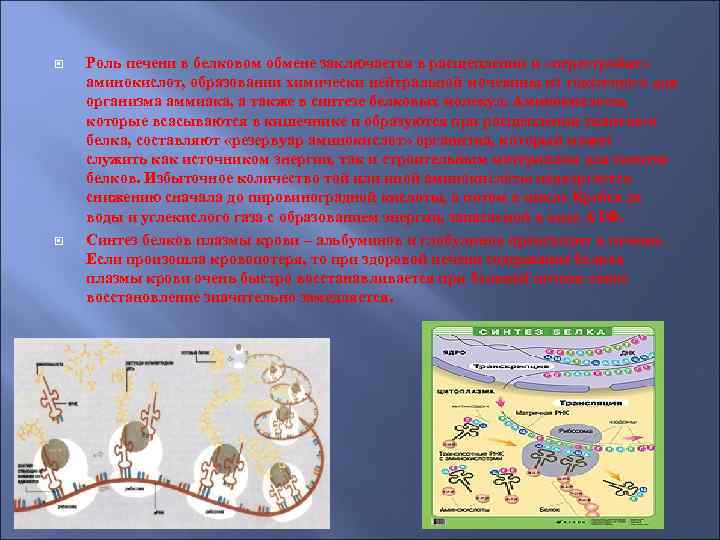
Роль печени в белковом обмене заключается в расщеплении и «перестройке» аминокислот, образовании химически нейтральной мочевины из токсичного для организма аммиака, а также в синтезе белковых молекул. Аминокислоты, которые всасываются в кишечнике и образуются при расщеплении тканевого белка, составляют «резервуар аминокислот» организма, который может служить как источником энергии, так и строительным материалом для синтеза белков. Избыточное количество той или иной аминокислоты подвергается снижению сначала до пировиноградной кислоты, а потом в цикле Кребса до воды и углекислого газа с образованием энергии, запасаемой в виде АТФ. Синтез белков плазмы крови – альбуминов и глобулинов происходит в печени. Если произошла кровопотеря, то при здоровой печени содержание белков плазмы крови очень быстро восстанавливается при больной печени такое восстановление значительно замедляется.

Участие печени в поддержании концентрации глюкозы
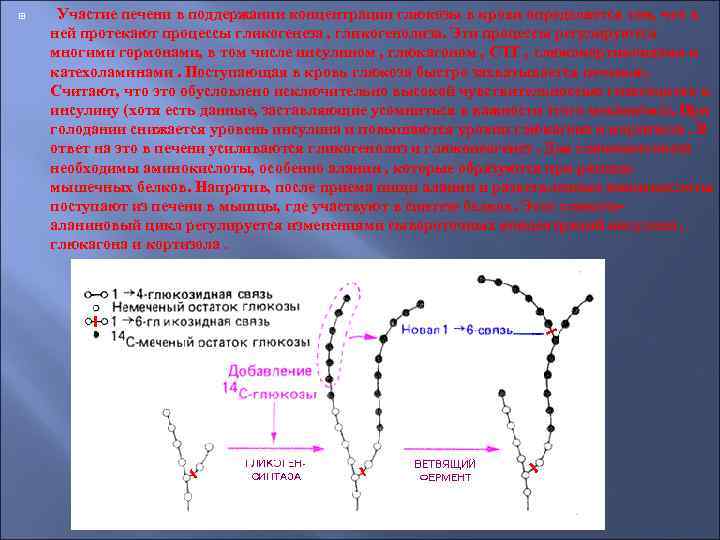
Участие печени в поддержании концентрации глюкозы в крови определяется тем, что в ней протекают процессы гликогенеза , гликогенолиза. Эти процессы регулируются многими гормонами, в том числе инсулином , глюкагоном , СТГ , глюкокортикоидами и катехоламинами. Поступающая в кровь глюкоза быстро захватывается печенью. Считают, что это обусловлено исключительно высокой чувствительностью гепатоцитов к инсулину (хотя есть данные, заставляющие усомниться в важности этого механизма). При голодании снижается уровень инсулина и повышаются уровни глюкагона и кортизола. В ответ на это в печени усиливаются гликогенолиз и глюконеогенез. Для глюконеогенеза необходимы аминокислоты, особенно аланин , которые образуются при распаде мышечных белков. Напротив, после приема пищи аланин и разветвленные аминокислоты поступают из печени в мышцы, где участвуют в синтезе белков. Этот глюкозоаланиновый цикл регулируется изменениями сывороточных концентраций инсулина , глюкагона и кортизола.

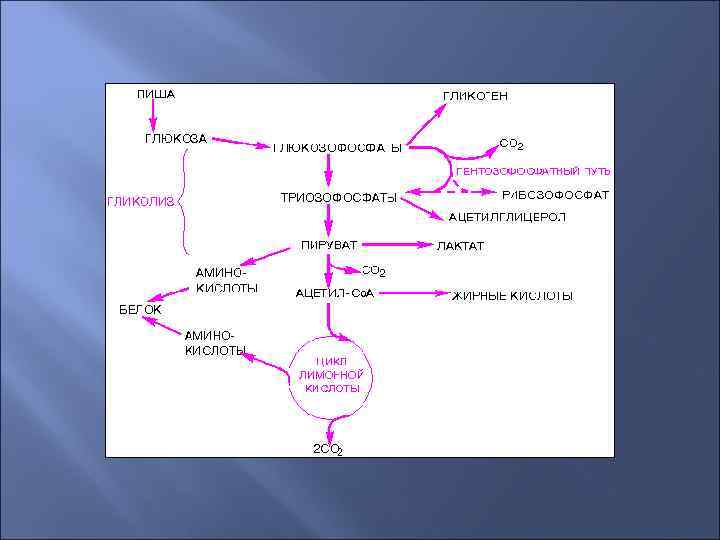
Роль печени в метаболизме углеводов Печень играет ведущую роль в поддержании физиологической концентрации глюкозы в крови. Из общего количества поступающей из кишечника глюкозы печень извлекает ее большую часть и тратит: 10 -15 % от этого количества на синтез гликогена, 60 % на окислительный распад, 30 % на синтез жирных кислот. При физиологической гипогликемии в печени активируется распад гликогена. Первая стадия этого процесса заключается в отщеплении молекулы глюкозы и ее фосфорилировании (фермент фосфорилаза). Далее Глю-5 -Ф может расходоваться по трем направлениям: 1. по пути глтколиза с образованием пировиноградной кислоты и лактата; 2. по пентозофосфатному пути; 3. расщепляться под действием фосфотазы на глюкозу и фосфор. Преобладает последний путь, который приводит к выбросу в общий кровоток свободной глюкозы. В печени активно протекает глюконеогенез, при котором предшественниками глюкозы являются пируват и аланин (поступающий из мышц), глицерол - из жировой ткани и с пищей ряд глюкогенных АК. Избыточное поступление глюкозы с пищей увеличивает в гепатоците интенсивность всех путей ее превращения. Так активируется ее окисление с образованием большого количества пирувата. Для его дальнейшего окисления необходимо также большое количество Ко. А, который также используется и для окисления жирных кислот. В результате окисление жирных кислот и распад липидов в жировых депо замедляется.

Метаболизм липидов
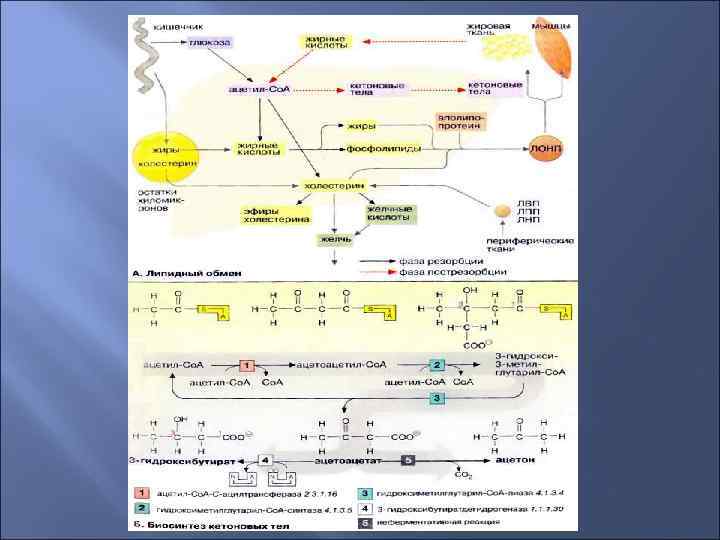

В печени синтезируются желчные кислоты, при дефиците которых переваривания жиров практически не происходит. В регуляции метаболизма липидов печени принадлежит ведущая роль. Так, при дефиците основного энергетического материала - глюкозы, в печени активируется окисление жирных кислот. В условиях избытка глюкозы в гепатоцитах происходит синтез триглицеридов и фосфолипидов из жирных кислот, которые поступают в печень из кишечника. Печени принадлежит ведущая роль в регуляции обмена холестерола. Исходное вещество в его синтезе - ацетил-Ко. А. Т. е. Избыточное питание стимулирует образование холестерола. В печени синтезируются транспортные формы липопротеинов. В печени, кроме того, синтезируются кетоновые тела, в частности ацетоацетат и гидрооксимаслянная кислота, которые разносятся кровью по организму. Сердечная мышца и корковый слой надпочечников предпочитают в качестве источника энергии использовать именно эти соединения, а не глюкозу.

Метаболизм белков

Печень использует АК, поступающие из пищеварительного тракта для синтеза собственных белков, но большая их часть идет на синтез белков плазмы крови. В печени синтезируются фибриноген, альбумины, a- и b-глобулины и липопротеиды. В печени синтезируется также т. н. лабильный резервный белок, который является как бы запасом АК, которые затем могут использоваться различными органами и тканями по мере необходимости. Печень занимает центральное место в обмене АК, т. к. в ней активно протекают процессы их химической модификации. Кроме того, именно в печени происходит синтез мочевины.

Детоксицирующая функция печени

Детоксикация ядовитых метаболитов и чужеродных соединений (ксенобиотиков) протекает в гепатоцитах в две стадии. Реакции первой стадии катализируются монооксигеназной системой, компоненты которой встроены в мембраны эндоплазматического ретикулума. Реакции окисления, восстановления или гидролиза являются первой стадией в системе выведения из организма гидрофобных молекул. Они превращают вещества в полярные водорастворимые метаболиты. Основной фермент гемопротеид цитохромы Р-450. К настоящему времени выявлено множество изоформ этого фермента и отнесено, в зависимости от их свойств и выполняемых функций, к нескольким семействам. У млекопитающих идентифицировано 13 подсемейств цх Р-450, условно считается, что ферменты семейства I-IV участвуют в биотрансформации ксенобиотиков, остальные метаболизируют эндогенные соединения (стероидные гормоны, простатагландины, жирные кислоты и др. ). Важным свойством цх Р-450 является способность к индукции под действием экзогенных субстратов, что легло в основу классификации изоформ в зависимости от индуцируемости тем или веществом определенной химической структуры.

На первой стадии биотрансформации происходит образование или высвобождение гидрокси-, карбоксильных, тиоловых и аминогрупп, которые являются гидрофильными, и молекула может подвергаться дальнейшему превращению и выведению из организма. В качестве кофермента используется НАДФН. Кроме цх Р 450, в первой стадии биотрансформации принимают участие цх b 5 и цитохромредуктаза. Многие лекарственные вещества, попадая в организм, превращаются на первой стадии биотрансформации в активные формы и оказывают необходимый лечебный эффект. Но часто ряд ксенобиотиков не детоксицируется, а наоборот токсифицируется с участием монооксигеназной системы и становится более реакционноспособным. Продукты метаболизма чужеродных веществ, образовавшихся на первой стадии биотрансформации, подвергаются дальнейшей детоксикации с помощью ряда реакций второй стадии. Образующиеся при этом соединения менее полярны и в связи с этим легко удаляются из клеток. Преобладающим является процесс конъюгации, катализируемый глутатион-S-трансферазой, сульфотрансферазой и UDP -глюкуронилтрансферазой. Конъюгацию с глутатионом, приводящую к образованию меркаптуровых кислот, принято рассматривать в качестве основного механизма детоксикации. Глутатион (ведущий компонент редокс-буфера клетки) представляет собой соединение, содержащее реактивную тиоловую группу. Большая его часть находится в восстановленной форме (GSH) и играет центральную роль в инактивации токсических и реактивных продуктов. Восстановление окисленного глутатиона осуществляет фермент - глутатионредуктаза, используя как кофермент НАДФН. Коньюгаты с глутатионом, серной и глюкуроновой кислотами выводятся из организма преимущественно с мочой

Зональность ферментных систем

Зональность метаболических комплексов печени, основного органа поддержания химического гомеостаза, определяет различие в ферментном составе между гепатоцитами перивенозной (центральной) и перипортальной (периферической) зон ацинуса (рис. 4. 16. 1. ). Это связано с их неодинаковой потребностью в кислороде различных ферментных систем. Так, наибольшая концентрация ферментов ЦТК, катаболизма амино- и жирных кислот, цикла мочевины, глюконеогенеза отмечена в перипортальной зоне, получающей более оксигенированную кровь. Поскольку компоненты реакций второй фазы биотрансформации локализованы в клетках этой зоны ацинуса, то они более защищены от действия токсических продуктов. В гепатоцитах перицентральной зоны более активен гликолиз и первая стадия биотрансформации ксенобиотиков.
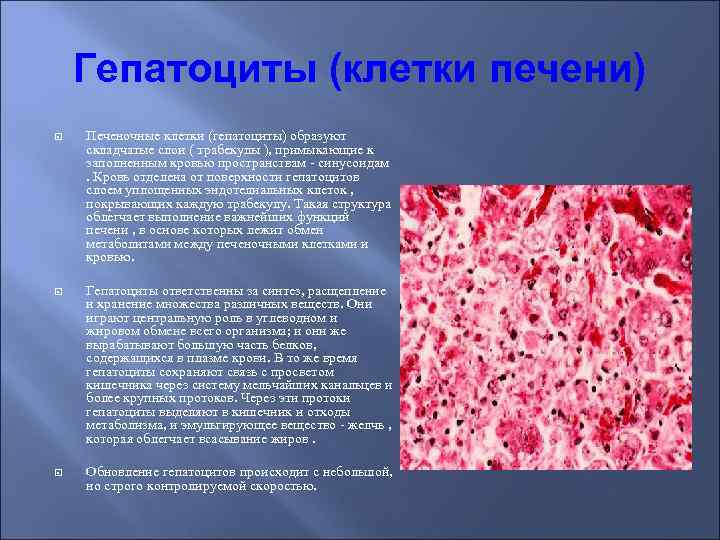
Гепатоциты (клетки печени) Печеночные клетки (гепатоциты) образуют складчатые слои ( трабекулы ), примыкающие к заполненным кровью пространствам - синусоидам. Кровь отделена от поверхности гепатоцитов слоем уплощенных эндотелиальных клеток , покрывающих каждую трабекулу. Такая структура облегчает выполнение важнейших функций печени , в основе которых лежит обмен метаболитами между печеночными клетками и кровью. Гепатоциты ответственны за синтез, расщепление и хранение множества различных веществ. Они играют центральную роль в углеводном и жировом обмене всего организма; и они же вырабатывают большую часть белков, содержащихся в плазме крови. В то же время гепатоциты сохраняют связь с просветом кишечника через систему мельчайших канальцев и более крупных протоков. Через эти протоки гепатоциты выделяют в кишечник и отходы метаболизма, и эмульгирующее вещество - желчь , которая облегчает всасывание жиров. Обновление гепатоцитов происходит с небольшой, но строго контролируемой скоростью.
РОЛЬ печени в обмене веществ.ppt