БИОТРАНСФОРМАЦИЯ ЛЕКАРСЧТВЕННЫХ ВЕЩЕСТВ.ppt
- Количество слайдов: 37

БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ

Лекарства, поступившие в организм, проходят следующие превращения: • всасывание; • связывание с белками и транспорт кровью; • взаимодействие с рецепторами; • распределение в тканях; • метаболизм и выведение из организма

Механизм первого этапа (всасывание) определяется физико-химическими свойствами лекарства. Гидрофобные соединения легко проникают через мембраны простой диффузией, в то время как лекарственные вещества, нерастворимые в липидах, проникают через мембраны путём трансмембранного переноса при участии разных типов транслоказ.

Следующие этапы метаболизма лекарственного вещества в организме тоже определяются его химическим строением гидрофобные молекулы перемещаются по крови в комплексе с альбумином, кислым αгликопротеином или в составе липопротеинов. В зависимости от структуры лекарственное вещество может поступать из крови в клетку или, являясь аналогами эндогенных веществ, связываться рецепторами клеточной мембраны.

Действие на организм большинства лекарств прекращается через определённое время после их приёма. Прекращение действия может происходить потому, что лекарство выводится из организма - либо в неизменённом виде - это характерно для гидрофильных соединений, - либо в виде продуктов его химической модификации (биотрансформации).

В результате биотрансформации лекарственных веществ может произойти: • инактивация лекарственных веществ, т. е. снижение их фармакологической активности; • повышение активности лекарственных веществ; • образование токсических метаболитов.

Инактивация лекарственных веществ, как и всех ксенобиотиков, происходит в 2 фазы. Первая фаза - химическая модификация под действием ферментов монооксигеназной системы ЭР. Например, лекарственное вещество барбитурат в ходе биотрансформации превращается в гидроксибарбитурат, который далее участвует в реакции конъюгации с остатком глюкуроновой кислоты.

Фермент глюкуронилтрансфераза катализирует образование барбитуратглюкуронида, в качестве источника глюкуроновой кислоты используется УДФ-глюкуронил. E 1 - ферменты микросомального окисления; Е 2 - глюкуронилтрансфераза. В первую фазу обезвреживания под действием монооксигеназ образуются реакционно-способные группы -ОН, -СООН, -NH 2, -SH и др. Химические соединения, уже имеющие эти группы, сразу вступают во вторую фазу обезвреживания - реакции конъюгации.
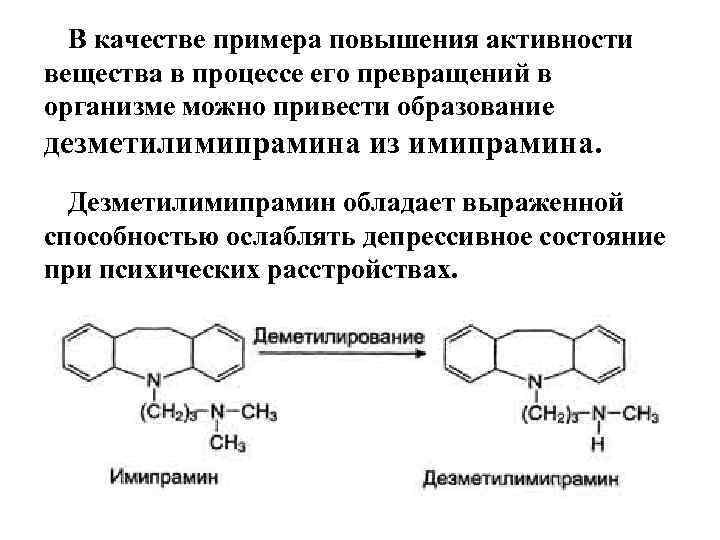
В качестве примера повышения активности вещества в процессе его превращений в организме можно привести образование дезметилимипрамина из имипрамина. Дезметилимипрамин обладает выраженной способностью ослаблять депрессивное состояние при психических расстройствах.
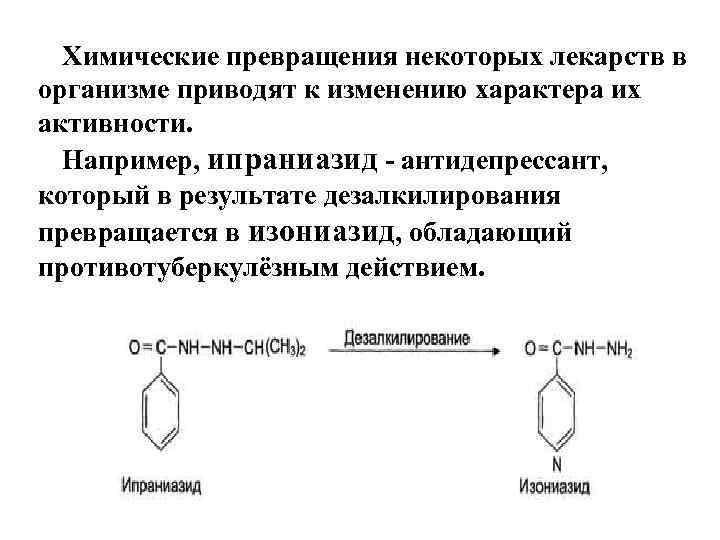
Химические превращения некоторых лекарств в организме приводят к изменению характера их активности. Например, ипраниазид - антидепрессант, который в результате дезалкилирования превращается в изониазид, обладающий противотуберкулёзным действием.
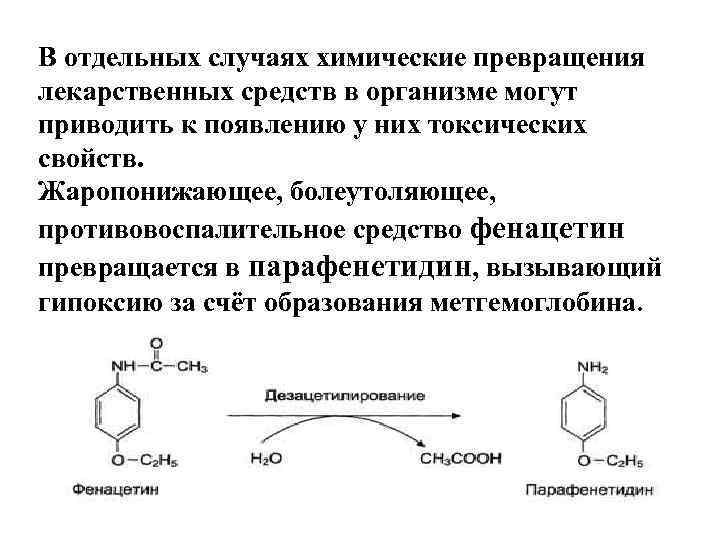
В отдельных случаях химические превращения лекарственных средств в организме могут приводить к появлению у них токсических свойств. Жаропонижающее, болеутоляющее, противовоспалительное средство фенацетин превращается в парафенетидин, вызывающий гипоксию за счёт образования метгемоглобина.

Реакции конъюгации лекарственных веществ

Вторая фаза инактивации - конъюгация (связывание) лекарственных веществ, как подвергшихся каким-либо превращениям на первом этапе, так и нативных препаратов. К продуктам, образованным ферментами микросомального окисления, может присоединяться глицин по карбоксильной группе, глюкороновая кислота или остаток серной кислоты - по ОН-группе, ацетильный остаток - к NH 2 -гpyппe.

В превращениях второй фазы инактивации лекарственных веществ принимают участие эндогенные соединения, образующиеся в организме с затратой энергии SAM (АТФ), УДФ-глюкуронат (УТФ), Ацетил-Ко. А (АТФ).
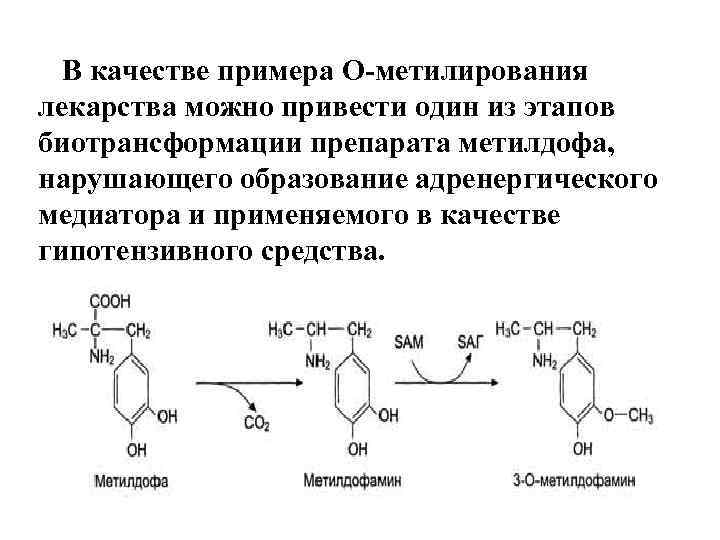
В качестве примера О-метилирования лекарства можно привести один из этапов биотрансформации препарата метилдофа, нарушающего образование адренергического медиатора и применяемого в качестве гипотензивного средства.

Факторы, влияющие на активность ферментов биотрансформации лекарств

Лекарственные средства в результате химической модификации, как правило, теряют свою биологическую активность. Таким образом, эти реакции лимитируют во времени действие лекарств. При патологии печени, сопровождающейся снижением активности микросомальных ферментов, продолжительность действия ряда лекарственных веществ увеличивается.

Некоторые препараты снижают активность монооксигеназной системы. Например, левомицетин ингибирует ферменты микросомального окисления. Антихолинэстеразные средства, ингибиторы моноаминооксидазы, нарушают функционирование фазы конъюгации, поэтому они пролонгируют эффекты препаратов, которые инактивируются этими ферментами. Кроме того, скорость каждой из реакций биотрансформации лекарственного вещества зависит от генетических, физиологических факторов и экологического состояния окружающей среды.

Возрастные особенности Чувствительность к лекарственным средствам меняется в зависимости от возраста. Например, у новорождённых активность метаболизма лекарств в первый месяц жизни существенно отличается от взрослых. Это связано с недостаточностью многих ферментов, участвующих в биотрасформации лекарственных веществ, функции почек, повышенной проницаемостью гематоэнцефалического барьера, недоразвитием ЦНС. Так, новорождённые более чувствительны к некоторым веществам, влияющим на ЦНС (в частности, к морфину). Очень токсичен для них левомицетин; это объясняется тем, что в печени у новорождённых малоактивны ферменты, необходимые для его биотрансформации.

В пожилом возрасте метаболизм лекарственных веществ протекает менее эффективно: снижается функциональная активность печени, нарушается скорость экскреции препаратов почками. В целом чувствительность к большинству лекарственных средств в пожилом возрасте повышена, в связи с чем их доза должна быть снижена.

Генетические факторы Индивидуальные различия в метаболизме ряда препаратов и в реакциях на препараты объясняют генетическим полиморфизмом, т. е. существованием в популяции изоформ некоторых ферментов биотрансформации. В ряде случаев повышенная чувствительность к лекарственным средствам может быть обусловлена наследственной недостаточностью некоторых ферментов, участвующих в химической модификации. Например, при генетической недостаточности холинэстеразы плазмы крови длительность действия миорелаксанта дитилина резко возрастает и может достигать 6 -8 ч и более (в обычных условиях дитилин действует в течение 5 -7 мин).

МЕТАБОЛИЗМ ЭТАНОЛА В ПЕЧЕНИ

Катаболизм этилового спирта осуществляется главным образом в печени. Здесь окисляется от 75% до 98% введённого в организм этанола. Окисление алкоголя - сложный биохимический процесс, в который вовлекаются основные метаболические процессы клетки. Превращение этанола в печени осуществляется тремя путями с образованием токсического метаболита – ацетальдегида. 1 окисление этанола NAD+ зависимой алкогольдегидрогеназой (АДГ); 2 - МЭОС - микросомальная этанолокисляющая система; 3 – окисление этанола каталазой; .

Основную роль в метаболизме этанола играет цинксодержащий NAD+- зависимый фермент алкогольдегидрогеназа, локализующаяся в основном в цитозоле и митохондриях печени (95%). В ходе реакции происходит дегидрирование этанола, образуются ацетальдегид и восстановленный кофермент NADH. Алкогольдегидрогеназа катализирует обратимую реакцию, направление которой зависит от концентрации ацетальдегида и соотношения NADH/NAD+ в клетке. С 2 Н 5 ОН + HAD+ ↔ СН 3 СНО + NADH + H+.

Цитохром Р 450 -зависимая микросомальная этанолокисляющая сисгема (МЭОС) локализована в мембране гладкого ЭР гепатоцитов. МЭОС играет незначительную роль в метаболизме небольших количеств алкоголя, но индуцируется этанолом, другими спиртами, лекарствами типа барбитуратов и приобретает существенное значение при злоупотреблении этими веществами.

Этот путь окисления этанола происходит при участии одной из изоформ Р 450 - изофермента Р 450 II E 1. При хроническом алкоголизме окисление этанола ускоряется на 50 - 70% за счёт гипертрофии ЭР и индукции цитохрома Р 450 II E 1. С 2 Н 5 ОН + NADPH + Н+ + О 2 → СН 3 СНО + NADP+ + 2 Н 2 О. Кроме основной реакции, цитохром Р 450 катализирует образование активных форм кислорода (О 2 -, Н 2 О 2), которые стимулируют ПОЛ в печени и других органах.

Второстепенную роль в окислении этанола играет каталаза, находящаяся в пероксисомах цитоплазмы и митохондрий клеток печени. Этот фермент расщепляет примерно 2% этанола, но при этом утилизирует пероксид водорода. СН 3 СН 2 ОН + Н 2 О 2 → СН 3 СНО + 2 Н 2 О Ацетальдегид, образовавшийся из этанола, окисляется до уксусной кислоты двумя ферментами: FAD зависимой альдегидоксидазой и NAD+ -зависимой ацетальдегидрогеназой (Ал. ДГ). СН 3 СНО + О 2 + H 2 O → СН 3 СООН + Н 2 О 2

Повышение концентрации ацетальдегида в клетке вызывает индукцию фермента алъдегидоксидазы. В ходе реакции образуются уксусная кислота, пероксид водорода и другие активные формы кислорода, что приводит к активации ПОЛ. Другой фермент ацетальдегидрогеназа (Ал. ДГ) окисляет субстрат при участии кофермента NAD+. СН 3 СНО + Н 2 О + NAD+ → СН 3 СООН + NADH + H+.

Полученная в ходе реакции уксусная кислота активируется под действием фермента ацетил-Ко. Асинтетазы. Реакция протекает с использованием кофермента А и молекулы АТФ. Образовавшийся ацетил-Ко. А, в зависимости от соотношения АТФ/АДФ и концентрации оксалоацетата в митохондриях гепатоцитов, может "сгорать" в ЦТК, идти на синтез жирных кислот или кетоновых тел.

Ферменты, участвующие в окислении этанола, алкогольдегидрогеназа и Ал. ДГ по разному распределены: в цитозоле - 80%/20% и митохондриях - 20%/80%. При поступлении больших доз алкоголя (более 2 г/кг) изза разных скоростей окисления этанола и ацетальдегида в цитозоле резко повышается концентрация последнего. Ацетальдегид - очень реакционно-способное соединение; он неферментативно может ацетилировать SH-, NH 2 группа белков и других соединений в клетке и нарушать их функции. В модифицированных белках могут возникать "сшивки", нехарактерные для нативной структуры (например, в белках межклеточного матрикса эластине и коллагене, некоторых белках хроматина и липопротеинов, формирующихся в печени).

Ацетилирование ядерных, цитоплазматических ферментов и структурных белков приводит к снижению синтеза экспортируемых печенью в кровь белков, например альбумина, который, удерживая Na+, поддерживает коллоидно-осмотическое давление, а также участвует в транспорте многих гидрофобных веществ в крови. Нарушение функций альбумина в сочетании с повреждающим действием ацетальдегида на мембраны сопровождается поступлением в клетки по градиенту концентрации ионов натрия и воды, происходит осмотическое набухание этих клеток и нарушение их функций.

ЭФФЕКТЫ ЭТАНОЛА В ПЕЧЕНИ

Характер влияния этанола на метаболизм ксенобиотиков и лекарств зависит от стадии алкогольной болезни: начальная стадия алкоголизма, хронический алкоголизм или острая форма алкогольной интоксикации. Микросомальная этанолокисляющая сисгема (МЭОС) наряду с метаболизмом этанола участвует в детоксикации ксенобиотиков и лекарств.

На начальной стадии алкогольной болезни биотрансформация лекарственных веществ протекает более активно вследствие индукции ферментов системы. Этим объясняют феномен лекарственной "устойчивости". Однако при острой интоксикации этиловым спиртом тормозится биотрансформация лекарственных веществ. Этанол конкурирует с ксенобиотиками за связывание с цитохромом Р 450 П E 1, вызывая гиперчувствительность (лекарственную "неустойчивость") к некоторым принятым одновременно с ним лекарственным препаратам.

Кроме того, у людей, страдающих хроническим алкоголизмом, наблюдают избирательную индукцию изоформы Р 450 II E 1 и конкурентное ингибирование синтеза других изоформ, принимающих участие в метаболизме ксенобиотиков и лекарств. При злоупотреблении алкоголем индуцируется также синтез глюкуронилтрансфераз, но снижается образование УДФ-глюкуроната.

Алкогольдегидрогеназа обладает широкой субстратной специфичностью и может окислять разные спирты, в том числе и метаболиты сердечных гликозидов - дигитоксина, дигоксина и гитоксина. Конкуренция этанола с сердечными гликозидами за активный центр алкогольдегидрогеназы приводит к снижению скорости биотрансформации этой группы лекарств и повышает опасность их побочного эффекта у лиц, принимающих большие дозы алкоголя.

Повышение концентрации ацетальдегида вызывает целый ряд нарушений в структуре белков (ацетилирование), мембран (ПОЛ), модификацию глутатиона, необходимого для одного из самых важных ферментов обезвреживания ксенобиотиков глутатионтрансферазы и фермента антиоксидазной защиты глутатионпероксидазы. Таким образом, представленные данные свидетельствуют, что алкогольное поражение печени сопровождается нарушением ее важнейшей детоксикационной функции.
БИОТРАНСФОРМАЦИЯ ЛЕКАРСЧТВЕННЫХ ВЕЩЕСТВ.ppt