Лекция 2 в НОЦ ИБХ 24 ноября ИБХ.ppt
- Количество слайдов: 115
Биотехнология и персонифицированная медицина Александр Габибов
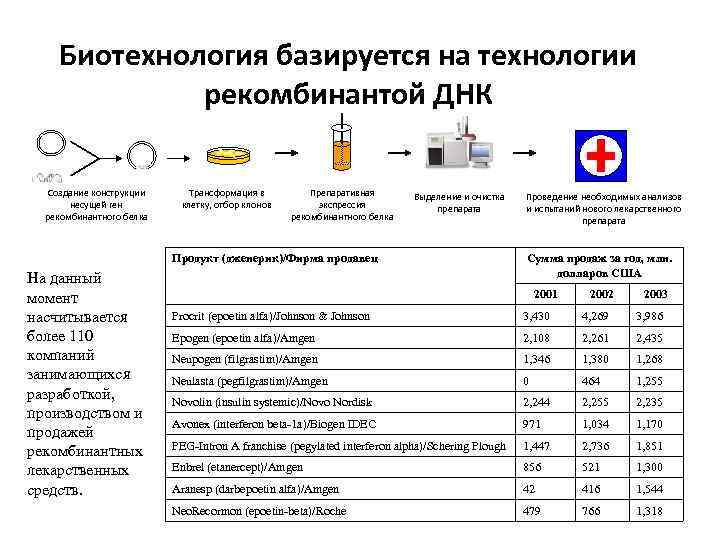
Биотехнология базируется на технологии рекомбинантой ДНК Создание конструкции несущей ген рекомбинантного белка Трансформация в клетку, отбор клонов Препаративная экспрессия рекомбинантного белка Выделение и очистка препарата Продукт (дженерик)/Фирма продавец На данный момент насчитывается более 110 компаний занимающихся разработкой, производством и продажей рекомбинантных лекарственных средств. Проведение необходимых анализов и испытаний нового лекарственного препарата Сумма продаж за год, млн. долларов США 2001 2002 2003 Procrit (epoetin alfa)/Johnson & Johnson 3, 430 4, 269 3, 986 Epogen (epoetin alfa)/Amgen 2, 108 2, 261 2, 435 Neupogen (filgrastim)/Amgen 1, 346 1, 380 1, 268 Neulasta (pegfilgrastim)/Amgen 0 464 1, 255 Novolin (insulin systemic)/Novo Nordisk 2, 244 2, 255 2, 235 Avonex (interferon beta-1 a)/Biogen IDEC 971 1, 034 1, 170 PEG-Intron A franchise (pegylated interferon alpha)/Schering Plough 1, 447 2, 736 1, 851 Enbrel (etanercept)/Amgen 856 521 1, 300 Aranesp (darbepoetin alfa)/Amgen 42 416 1, 544 Neo. Recormon (epoetin-beta)/Roche 479 766 1, 318

Мировой рынок препаратов на основе рекомбинантных белков более 125 миллиардов долларов n Мировой рынок антител более 50 миллиардов долларов n
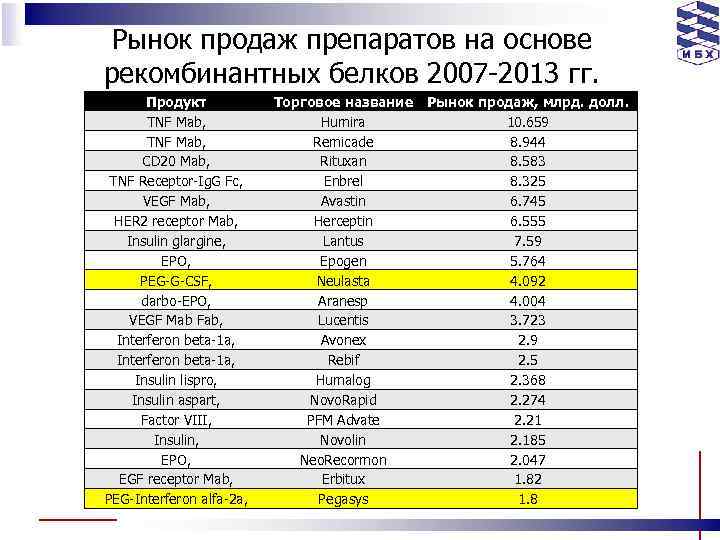
Рынок продаж препаратов на основе рекомбинантных белков 2007 -2013 гг. Продукт TNF Mab, CD 20 Mab, TNF Receptor-Ig. G Fc, VEGF Mab, HER 2 receptor Mab, Insulin glargine, EPO, PEG-G-CSF, darbo-EPO, VEGF Mab Fab, Interferon beta-1 a, Insulin lispro, Insulin aspart, Factor VIII, Insulin, EPO, EGF receptor Mab, PEG-Interferon alfa-2 a, Торговое название Рынок продаж, млрд. долл. Humira 10. 659 Remicade 8. 944 Rituxan 8. 583 Enbrel 8. 325 Avastin 6. 745 Herceptin 6. 555 Lantus 7. 59 Epogen 5. 764 Neulasta 4. 092 Aranesp 4. 004 Lucentis 3. 723 Avonex 2. 9 Rebif 2. 5 Humalog 2. 368 Novo. Rapid 2. 274 PFM Advate 2. 21 Novolin 2. 185 Neo. Recormon 2. 047 Erbitux 1. 82 Pegasys 1. 8
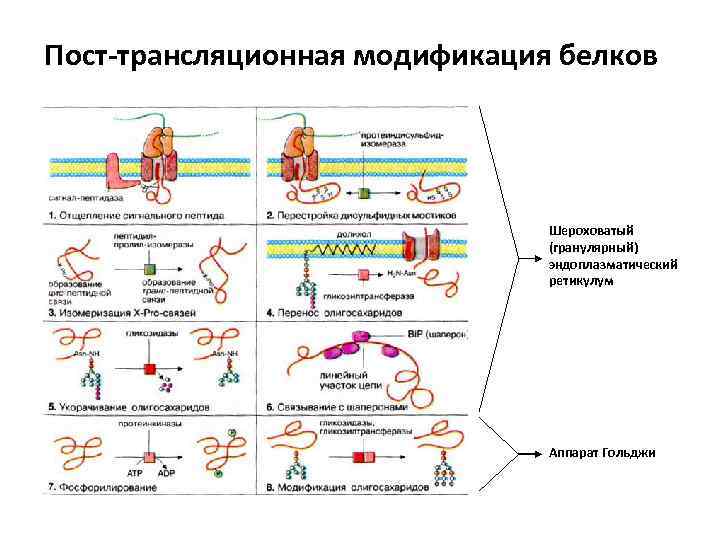
Пост-трансляционная модификация белков Шероховатый (гранулярный) эндоплазматический ретикулум Аппарат Гольджи

Пути выведения белковых лекарственных препаратов из организма пациента ØЗахват клетками и деградация в лизосомах ØВыведение через мочевыделительную систему ØПротеолитическая деградация в кровотоке
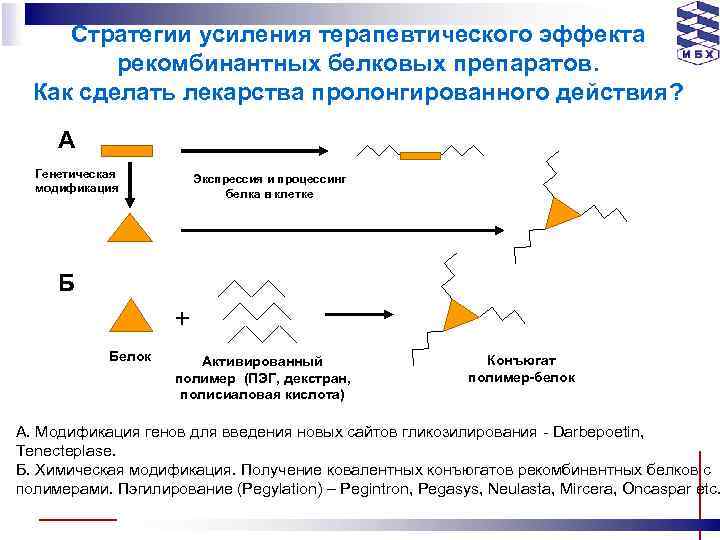
Стратегии усиления терапевтического эффекта рекомбинантных белковых препаратов. Как сделать лекарства пролонгированного действия? A Генетическая модификация Экспрессия и процессинг белка в клетке Б + Белок Активированный полимер (ПЭГ, декстран, полисиаловая кислота) Конъюгат полимер-белок А. Модификация генов для введения новых сайтов гликозилирования - Darbepoetin, Tenecteplase. Б. Химическая модификация. Получение ковалентных конъюгатов рекомбинвнтных белков с полимерами. Пэгилирование (Pegylation) – Pegintron, Pegasys, Neulasta, Mircera, Oncaspar etc.

Основные полимеры используемые для получения препаратов пролонгированного действия

БИОКАТАЛИТИЧЕСКИЕ МЕХАНИЗМЫ ДЕГРАДАЦИИ ФОСФОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
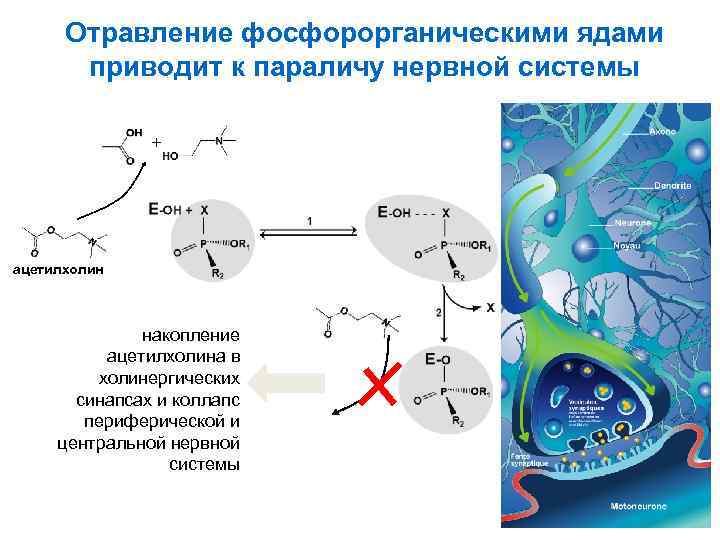
Отравление фосфорорганическими ядами приводит к параличу нервной системы + ацетилхолин накопление ацетилхолина в холинергических синапсах и коллапс периферической и центральной нервной системы

Проблема терапии отравлений ФОТ Из всех изученных аналогов фосфорорганические токсины (ФОТ) обладают наибольшим поражающим действием на холинэстеразы; Экстремально низкое ЛД 50; В год от ФОТ погибает порядка 200 000 человек; современное лечение отравлений ФОТ не совершенно и в 15% случаев не помогает; Террористическая угроза: 20 марта 1995 года в Токио террористы выпустили зарин в поездах на центральных линиях метрополитена. В тот день погибли 27 человек и 5500 человек получили отравления различной степени тяжести.
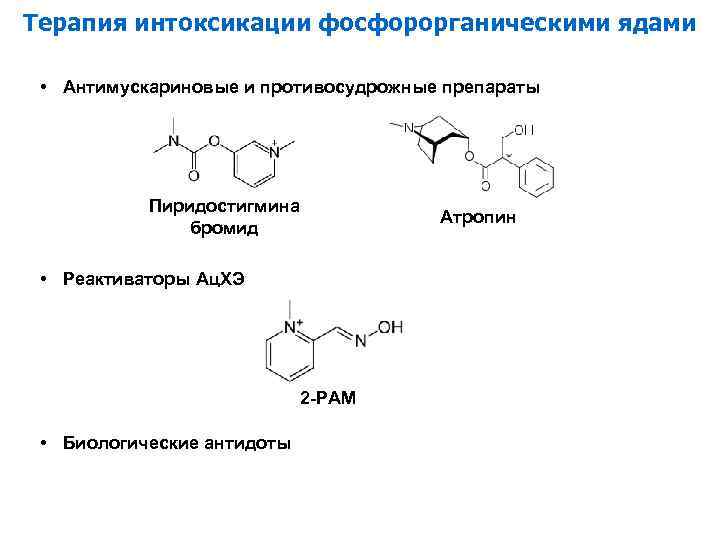
Терапия интоксикации фосфорорганическими ядами • Антимускариновые и противосудрожные препараты Пиридостигмина бромид • Реактиваторы Ац. ХЭ 2 -PAM • Биологические антидоты Атропин
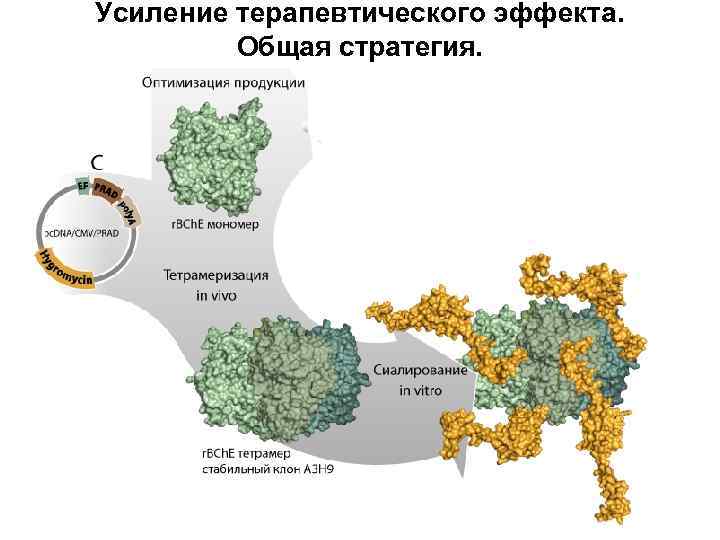
Усиление терапевтического эффекта. Общая стратегия.

Создание биологического антидота пролонгированного действия на основе бутирилхолинэстеразы Ilyushin et al. , PNAS 2013

Анализ фармакодинамических и защитных свойств полисиалированой бутирилхолинэстеразы
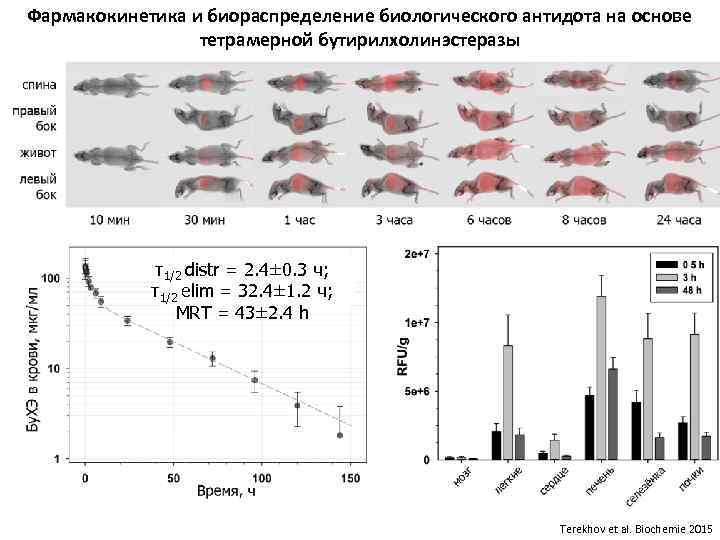
Фармакокинетика и биораспределение биологического антидота на основе тетрамерной бутирилхолинэстеразы τ1/2 distr = 2. 4± 0. 3 ч; τ1/2 elim = 32. 4± 1. 2 ч; MRT = 43± 2. 4 h Terekhov et al. Biochemie 2015
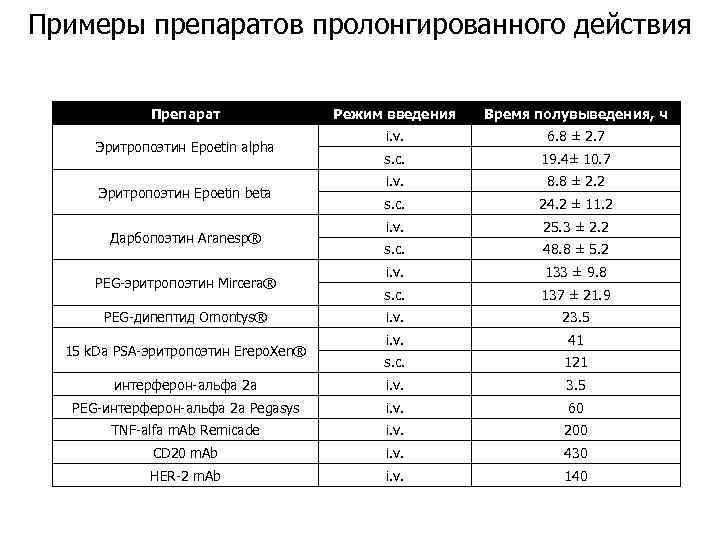
Примеры препаратов пролонгированного действия Препарат Режим введения Время полувыведения, ч i. v. 6. 8 ± 2. 7 s. c. 19. 4± 10. 7 i. v. 8. 8 ± 2. 2 s. c. 24. 2 ± 11. 2 i. v. 25. 3 ± 2. 2 s. c. 48. 8 ± 5. 2 i. v. 133 ± 9. 8 s. c. 137 ± 21. 9 i. v. 23. 5 i. v. 41 s. c. 121 интерферон-альфа 2 а i. v. 3. 5 PEG-интерферон-альфа 2 а Pegasys i. v. 60 TNF-alfa m. Ab Remicade i. v. 200 CD 20 m. Ab i. v. 430 HER-2 m. Ab i. v. 140 Эритропоэтин Epoetin alpha Эритропоэтин Epoetin beta Дарбопоэтин Aranesp® PEG-эритропоэтин Mircera® PEG-дипептид Omontys® 15 k. Da PSA-эритропоэтин Erepo. Xen®

MESSAGE Комбинаторные химия и биология - знаковые технологии в биомедицине ХХI века

Evolution of the Biocatalyst Enzymes Million years of evolution Artificial Enzymes made by Combinatorial Approaches Several months or weeks evolution Selection in the test tube from naïve repertoire 108 in mouse to 109 in semisynthetic libraries Enzyme superfamily of different types could be substituted for immunoglobulin superfamily

Evolution of Substrates de novo selection Is the “natural” substrate most efficient?

What is Ideal Peptide Substrate for a Protease? Optimization: ü Substrate Binding ü Scissile bond cleavage ü Product release David Corey and coauthors selected optimal peptide substrate for Tissue-type Plasminogen Activator using phage display technology. Selected peptide was hydrolyzed 5000 -fold more efficient than a peptide of similar length derived from the native cleavage site in plasminogen. G. S. Coombs et all. JBC 1996 vol 271 pp 4461 -4467

Anthrax Toxin’s Components Protective antigen (PA) binds to PA a cell surface receptor and forms an oligomeric pore that translocates both EF and LF into the cytosol of target cells + Lethal Factor (LF) is a zinc LF -dependent metalloproteinase that cleaves most MAP kinases (MKK) + OR Edema factor (EF)EF calmodulin dependent ADC
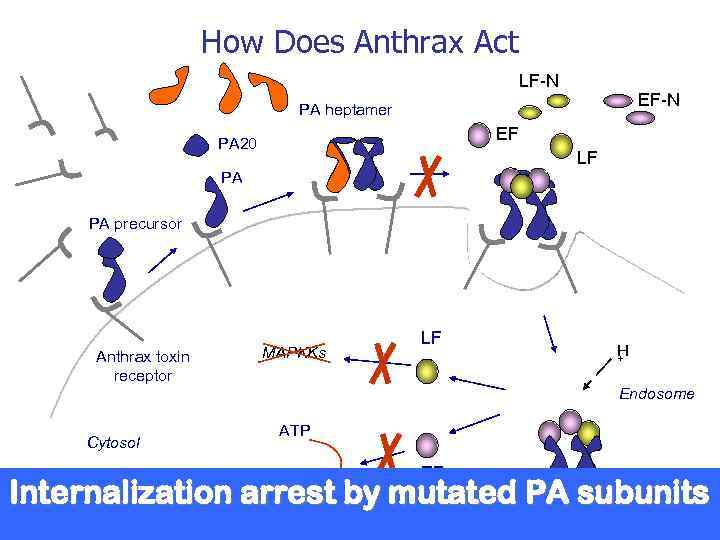
How Does Anthrax Act LF-N EF-N PA heptamer EF PA 20 LF PA PA precursor Anthrax toxin receptor Cytosol MAPKKs LF H + Endosome ATP EF Internalization ofc. AMP complex with truncated the Internalization arrestofby solubleactivity Neutralization of PA enzyme receptors Neutralization by mutated PA subunits effector subunits

Identification of novel LF peptide substrates are essential for • Protease mechanistic studies • LF detection strategy • Development of inhibitor screening technology.

• The problem is: peptides, derived from MAPKK kinase docking sites, are hardly cleaved by LF in vitro. • There are some good LF substrates among rational designed synthetic peptides , for example, RRKKVYPYPME [Turk, et al. (2004). Nat Struct Mol Biol 11(1): 60 -66] , but it is not very specific. • The aim of our investigation was to find specific peptide substrate with appropriate kinetic parameters. • Method : substrate phage display library screening for LF protease sensitivity.
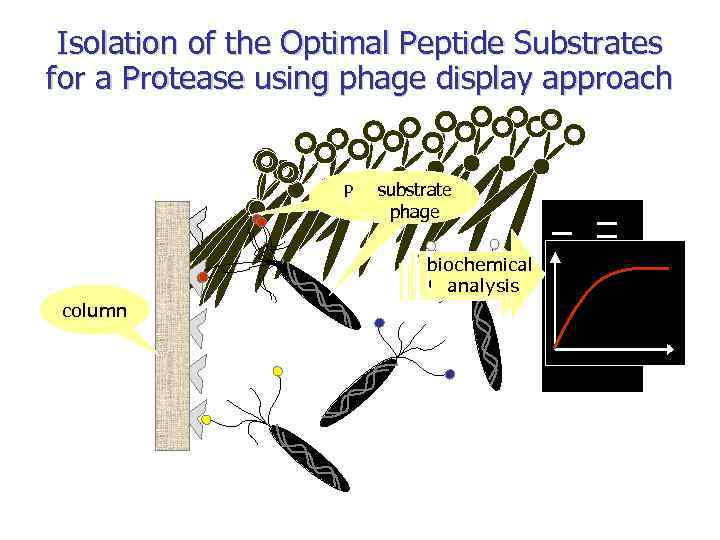
Isolation of the Optimal Peptide Substrates for a Protease using phage display approach substrate Protease LF phage biochemical sequencing analysis column
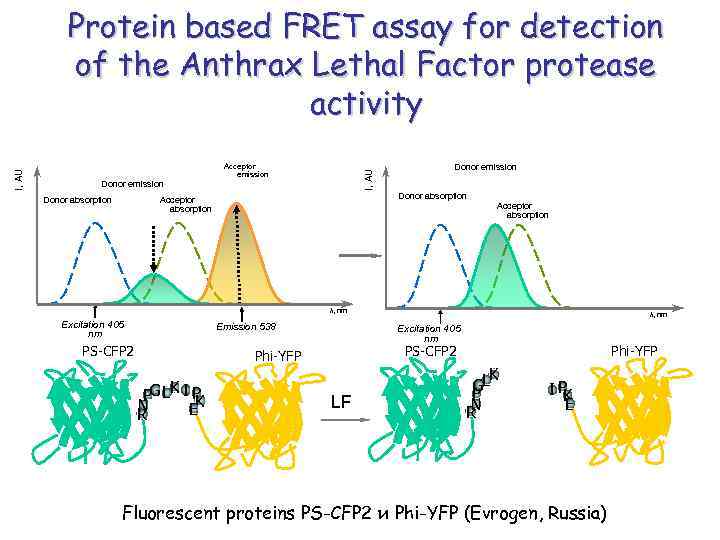
Donor emission Donor absorption Acceptor emission I, AU Protein based FRET assay for detection of the Anthrax Lethal Factor protease activity Donor emission Donor absorption Acceptor absorption λ, nm Excitation 405 nm Emission 538 PS-CFP 2 Phi-YFP K PG L I P N EK R λ, nm Excitation 405 nm LF K GL P N R IP K E Fluorescent proteins PS-CFP 2 и Phi-YFP (Evrogen, Russia)
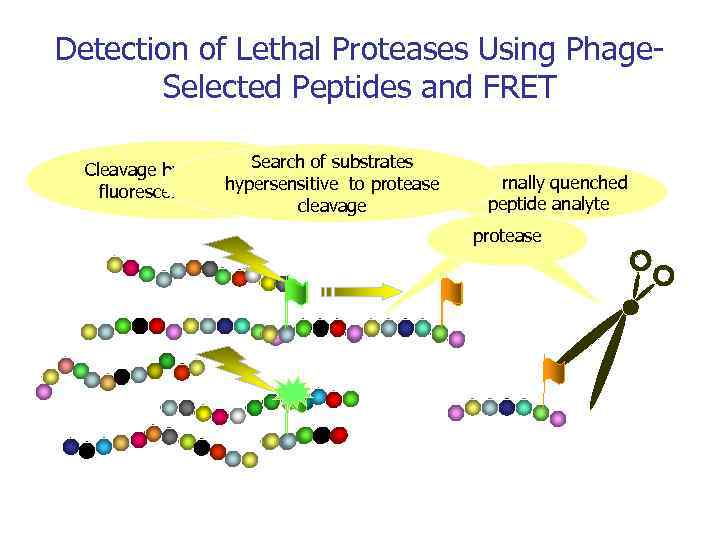
Detection of Lethal Proteases Using Phage. Selected Peptides and FRET Search Cleavage by protease and of substrates hypersensitive to protease fluorescence induction cleavage Internally quenched peptide analyte protease
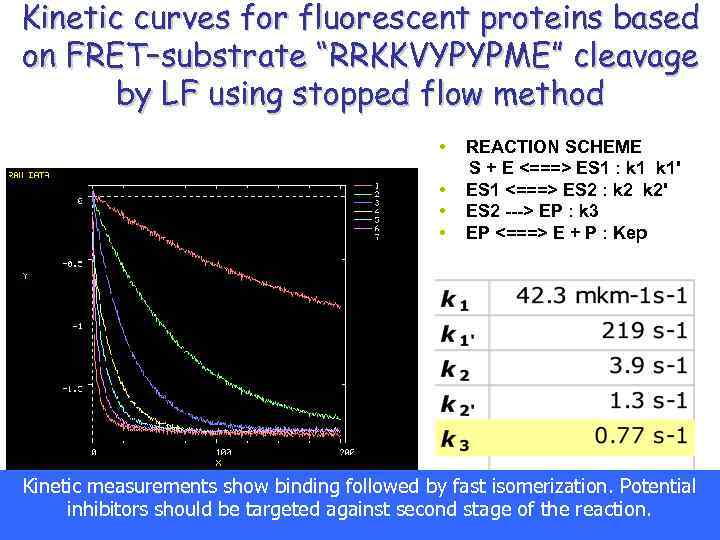
Kinetic curves for fluorescent proteins based on FRET–substrate “RRKKVYPYPME” cleavage by LF using stopped flow method • REACTION SCHEME S + E <===> ES 1 : k 1' • ES 1 <===> ES 2 : k 2' • ES 2 ---> EP : k 3 • EP <===> E + P : Kep Kinetic measurements show binding followed by fast isomerization. Potential inhibitors should be targeted against second stage of the reaction.
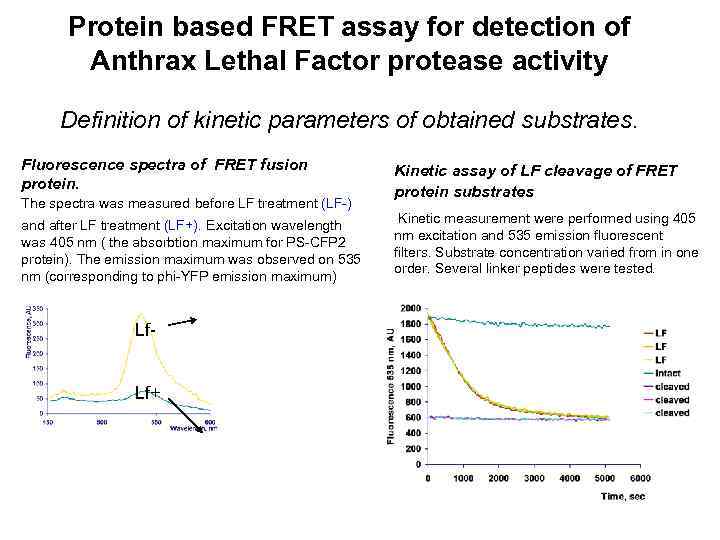
Protein based FRET assay for detection of Anthrax Lethal Factor protease activity Definition of kinetic parameters of obtained substrates. Fluorescence spectra of FRET fusion protein. The spectra was measured before LF treatment (LF-) and after LF treatment (LF+). Excitation wavelength was 405 nm ( the absorbtion maximum for PS-CFP 2 protein). The emission maximum was observed on 535 nm (corresponding to phi-YFP emission maximum) Lf. Lf+ Kinetic assay of LF cleavage of FRET protein substrates Kinetic measurement were performed using 405 nm excitation and 535 emission fluorescent filters. Substrate concentration varied from in one order. Several linker peptides were tested.
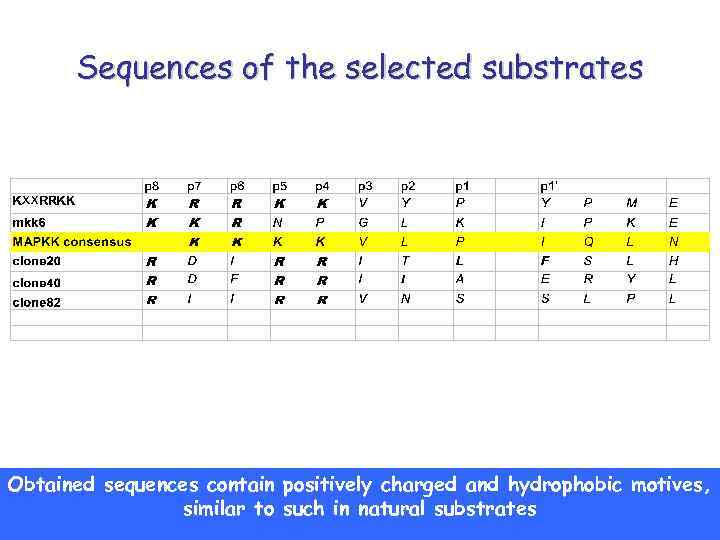
Sequences of the selected substrates Obtained sequences contain positively charged and hydrophobic motives, similar to such in natural substrates
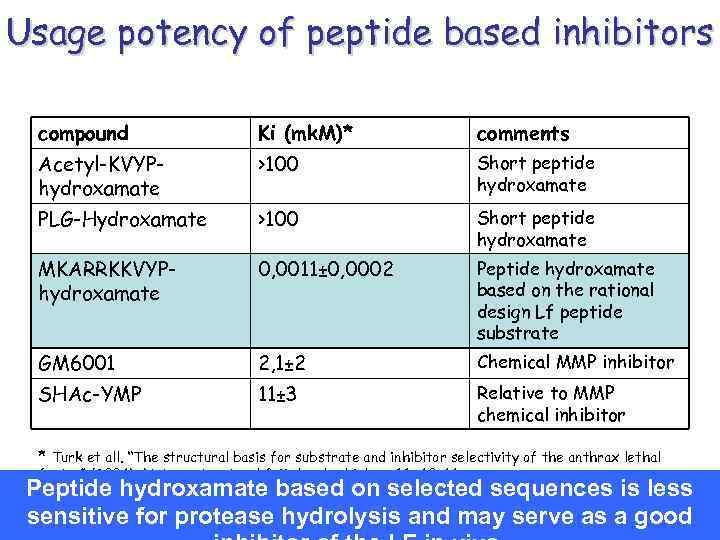
Usage potency of peptide based inhibitors compound Ki (mk. M)* comments Acetyl-KVYPhydroxamate >100 Short peptide hydroxamate PLG-Hydroxamate >100 Short peptide hydroxamate MKARRKKVYPhydroxamate 0, 0011± 0, 0002 Peptide hydroxamate based on the rational design Lf peptide substrate GM 6001 2, 1± 2 Chemical MMP inhibitor SHAc-YMP 11± 3 Relative to MMP chemical inhibitor * Turk et all. “The structural basis for substrate and inhibitor selectivity of the anthrax lethal factor” (2004) Nature structural & Molecular biology 11, 60 -66. Peptide hydroxamate based on selected sequences is less Ki were determined by measuring inhibition of peptide RRKK cleavage (1 mkm) over range of inhibitor sensitive for protease hydrolysis and may serve as a good concentration.
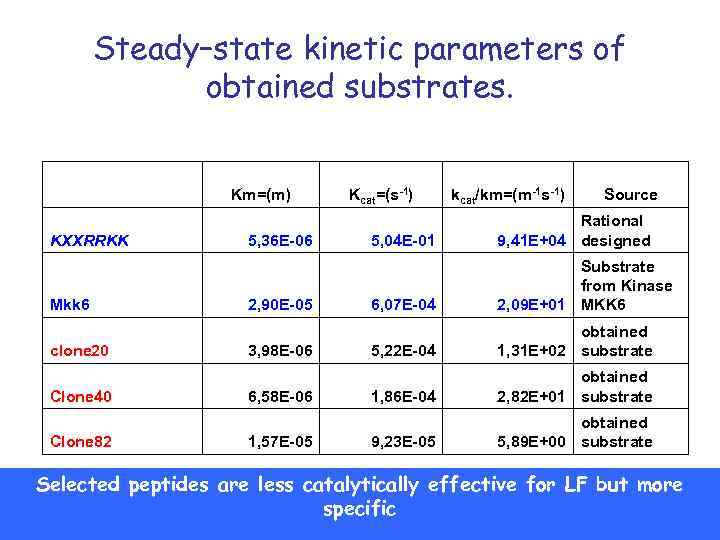
Steady–state kinetic parameters of obtained substrates. KXXRRKK Mkk 6 clone 20 Clone 40 Clone 82 Km=(m) 5, 36 E-06 2, 90 E-05 3, 98 E-06 6, 58 E-06 1, 57 E-05 Kcat=(s-1) kcat/km=(m-1 s-1) Source 5, 04 E-01 Rational 9, 41 E+04 designed 6, 07 E-04 Substrate from Kinase 2, 09 E+01 MKK 6 5, 22 E-04 obtained 1, 31 E+02 substrate 1, 86 E-04 obtained 2, 82 E+01 substrate 9, 23 E-05 obtained 5, 89 E+00 substrate Selected peptides are less catalytically effective for LF but more specific

Reaction mechanism k 1 k 2 k 3 Kep S + E <===> ES 1 <===> ES 2 ---> EP <===> E + P k 1’ k 2’ The observed sequence of events suggests that after primary binding of substrate, LF (and/or substrate) most probably undergoes conformational rearrangements.
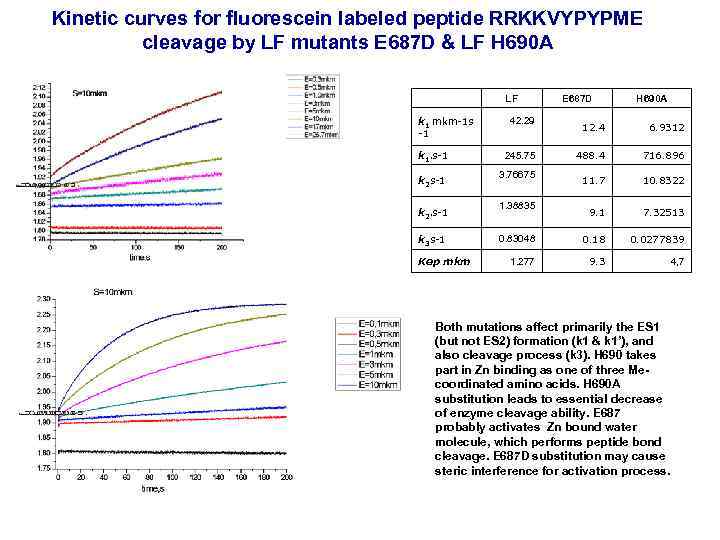
Kinetic curves for fluorescein labeled peptide RRKKVYPYPME cleavage by LF mutants E 687 D & LF H 690 A LF k 1 mkm-1 s -1 k 1's-1 k 2's-1 k 3 s-1 Kep mkm 42. 29 E 687 D H 690 A 12. 4 6. 9312 488. 4 716. 896 11. 7 10. 8322 9. 1 7. 32513 0. 83048 0. 18 0. 0277839 1. 277 9. 3 4, 7 245. 75 3. 76675 1. 38835 Both mutations affect primarily the ES 1 (but not ES 2) formation (k 1 & k 1’), and also cleavage process (k 3). H 690 takes part in Zn binding as one of three Mecoordinated amino acids. H 690 A substitution leads to essential decrease of enzyme cleavage ability. E 687 probably activates Zn bound water molecule, which performs peptide bond cleavage. E 687 D substitution may cause steric interference for activation process.
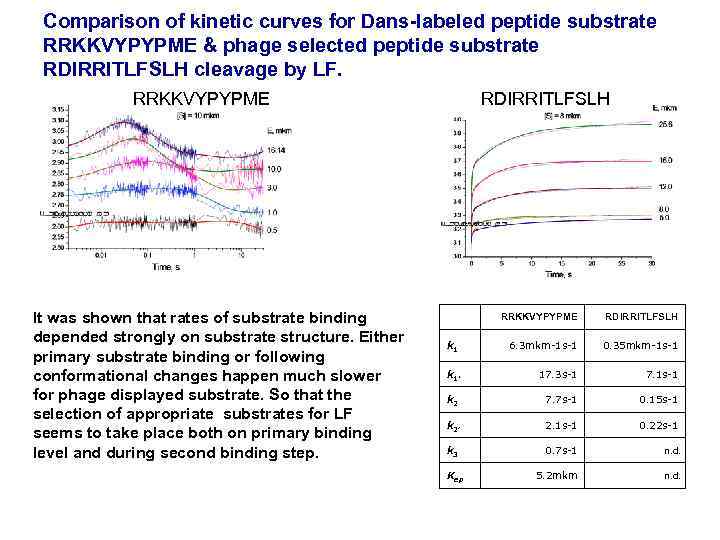
Comparison of kinetic curves for Dans-labeled peptide substrate RRKKVYPYPME & phage selected peptide substrate RDIRRITLFSLH cleavage by LF. RRKKVYPYPME It was shown that rates of substrate binding depended strongly on substrate structure. Either primary substrate binding or following conformational changes happen much slower for phage displayed substrate. So that the selection of appropriate substrates for LF seems to take place both on primary binding level and during second binding step. RDIRRITLFSLH RRKKVYPYPME RDIRRITLFSLH k 1 6. 3 mkm-1 s-1 0. 35 mkm-1 s-1 k 1' 17. 3 s-1 7. 1 s-1 k 2 7. 7 s-1 0. 15 s-1 k 2’ 2. 1 s-1 0. 22 s-1 k 3 0. 7 s-1 n. d. 5. 2 mkm n. d. Kep
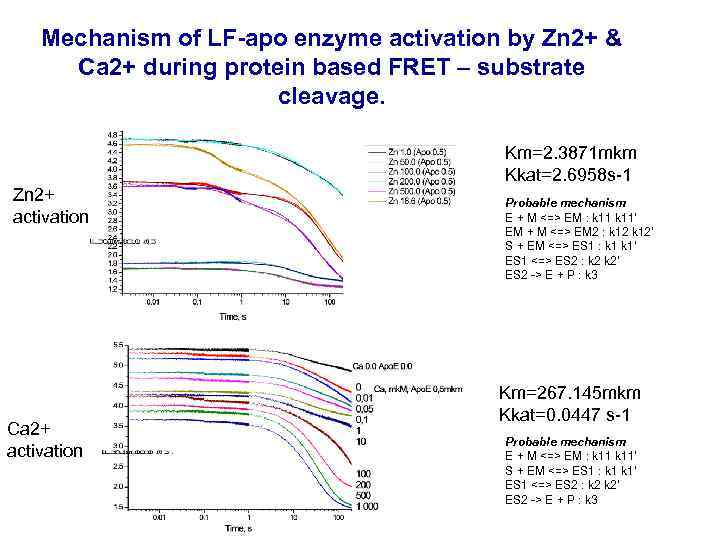
Mechanism of LF-apo enzyme activation by Zn 2+ & Ca 2+ during protein based FRET – substrate cleavage. Km=2. 3871 mkm Kkat=2. 6958 s-1 Zn 2+ activation Ca 2+ activation Probable mechanism E + M <=> EM : k 11' EM + M <=> EM 2 : k 12' S + EM <=> ES 1 : k 1' ES 1 <=> ES 2 : k 2' ES 2 -> E + P : k 3 Km=267. 145 mkm Kkat=0. 0447 s-1 Probable mechanism E + M <=> EM : k 11' S + EM <=> ES 1 : k 1' ES 1 <=> ES 2 : k 2' ES 2 -> E + P : k 3

• The activation by Zn 2+ was shown to be three-phase process. • High concentrations of zinc ions (>500 m. M) inhibits cleavage reaction. • Ca 2+ enzyme activation is one-step process. • Zn 2+ was bound by enzyme active centre approximately 100 times more effective than Ca 2+ and the substrate cleavage was 50 times faster, than for Ca 2+ activated enzyme.

Chemical selection of phage display library
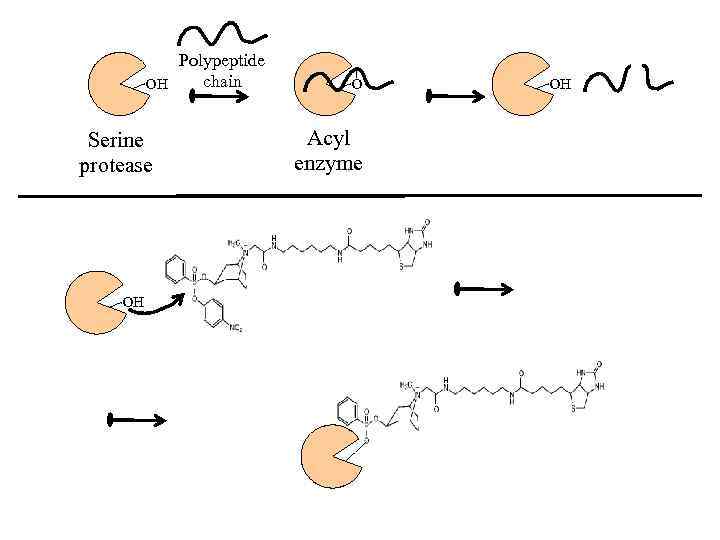
Polypeptide chain OH Serine protease OH O Acyl enzyme OH
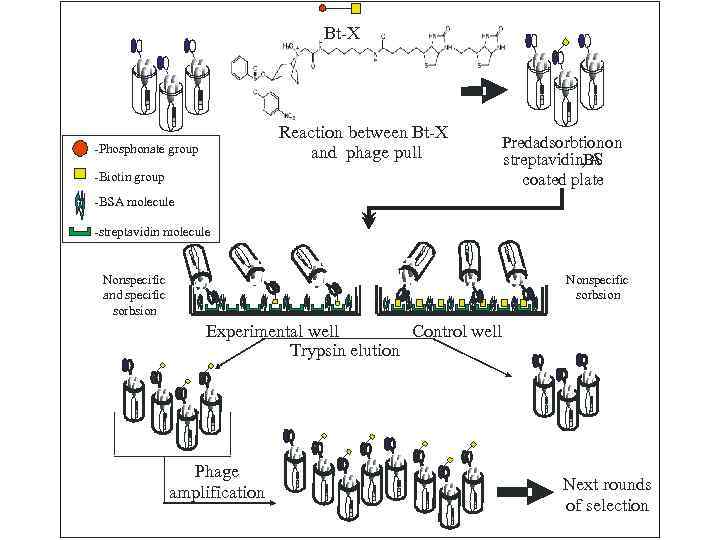
Bt-X Reaction between Bt-X and phage pull -Phosphonate group -Biotin group Predadsorbtion on streptavidin. BS , A coated plate -BSA molecule -streptavidin molecule Nonspecific and specific sorbsion Nonspecific sorbsion Experimental well Control well Trypsin elution Phage amplification Next rounds of selection
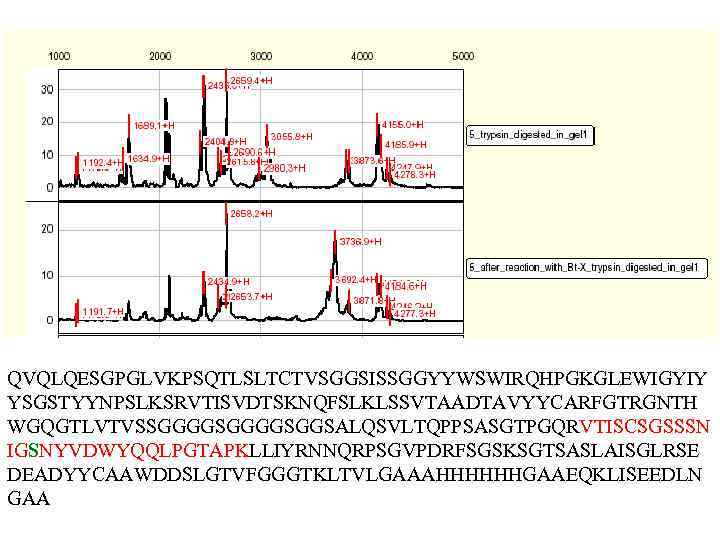
QVQLQESGPGLVKPSQTLSLTCTVSGGSISSGGYYWSWIRQHPGKGLEWIGYIY YSGSTYYNPSLKSRVTISVDTSKNQFSLKLSSVTAADTAVYYCARFGTRGNTH WGQGTLVTVSSGGGGSGGSALQSVLTQPPSASGTPGQRVTISCSGSSSN IGSNYVDWYQQLPGTAPKLLIYRNNQRPSGVPDRFSGSKSGTSASLAISGLRSE DEADYYCAAWDDSLGTVFGGGTKLTVLGAAAHHHHHHGAAEQKLISEEDLN GAA
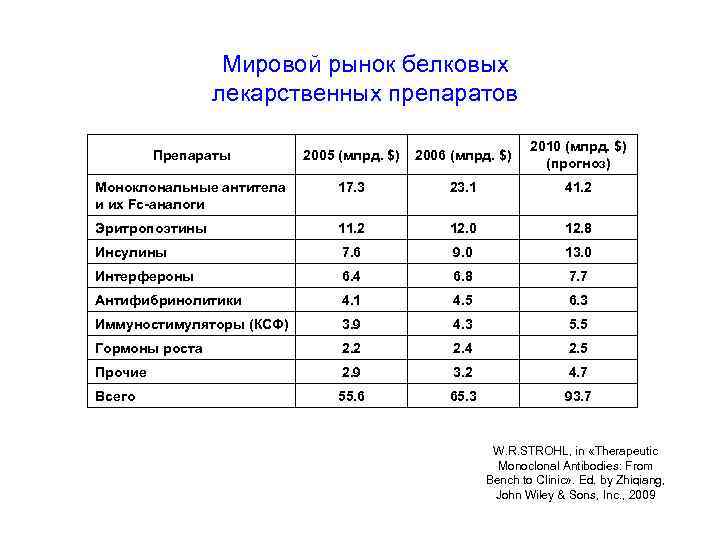
Мировой рынок белковых лекарственных препаратов Препараты 2005 (млрд. $) 2006 (млрд. $) 2010 (млрд. $) (прогноз) Моноклональные антитела и их Fc-аналоги 17. 3 23. 1 41. 2 Эритропоэтины 11. 2 12. 0 12. 8 Инсулины 7. 6 9. 0 13. 0 Интерфероны 6. 4 6. 8 7. 7 Антифибринолитики 4. 1 4. 5 6. 3 Иммуностимуляторы (КСФ) 3. 9 4. 3 5. 5 Гормоны роста 2. 2 2. 4 2. 5 Прочие 2. 9 3. 2 4. 7 Всего 55. 6 65. 3 93. 7 W. R. STROHL, in «Therapeutic Monoclonal Antibodies: From Bench to Clinic» . Ed. by Zhiqiang, John Wiley & Sons, Inc. , 2009
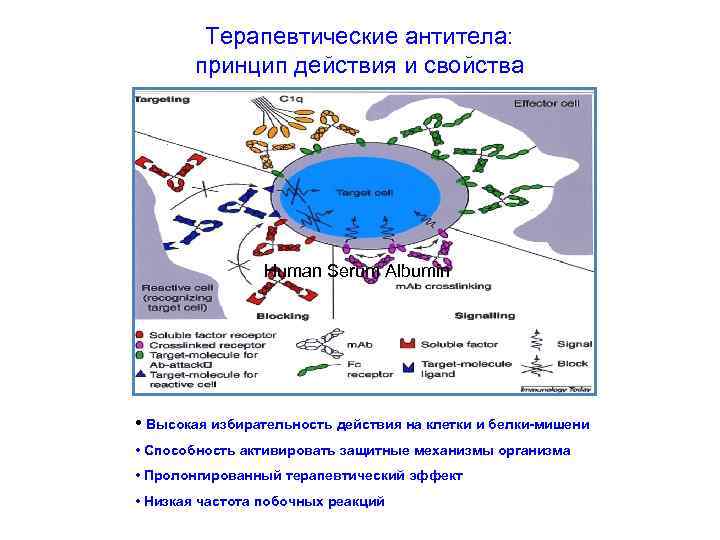
Терапевтические антитела: принцип действия и свойства Human Serum Albumin • Высокая избирательность действия на клетки и белки-мишени • Способность активировать защитные механизмы организма • Пролонгированный терапевтический эффект • Низкая частота побочных реакций
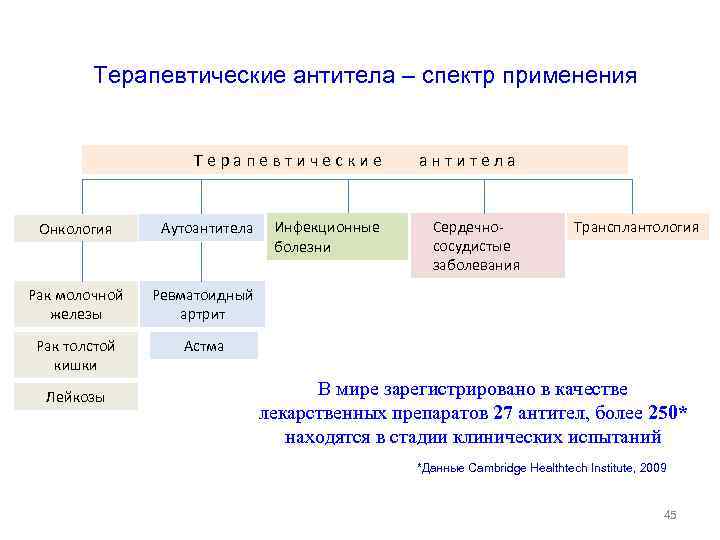
Терапевтические антитела – спектр применения Терапевтические антитела Инфекционные болезни Сердечнососудистые заболевания Онкология Аутоантитела Рак молочной железы Ревматоидный артрит Рак толстой кишки Трансплантология Астма Лейкозы В мире зарегистрировано в качестве лекарственных препаратов 27 антител, более 250* находятся в стадии клинических испытаний *Данные Cambridge Healthtech Institute, 2009 45
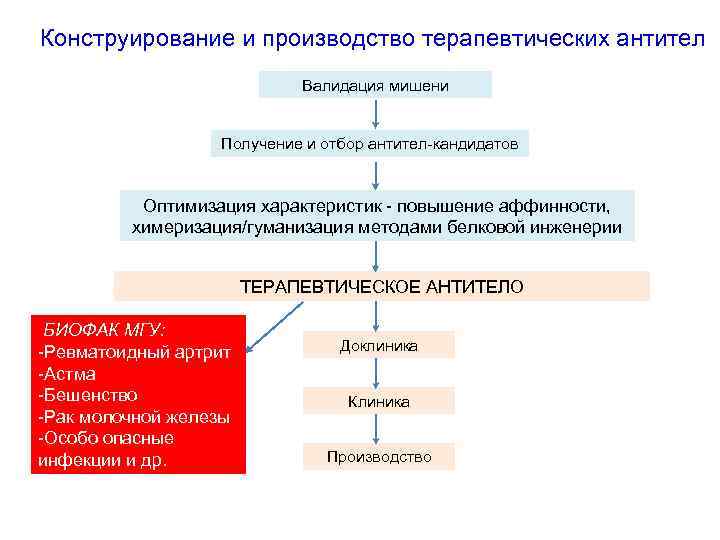
Конструирование и производство терапевтических антител Валидация мишени Получение и отбор антител-кандидатов Оптимизация характеристик - повышение аффинности, химеризация/гуманизация методами белковой инженерии ТЕРАПЕВТИЧЕСКОЕ АНТИТЕЛО БИОФАК МГУ: -Ревматоидный артрит -Астма -Бешенство -Рак молочной железы -Особо опасные инфекции и др. Доклиника Клиника Производство
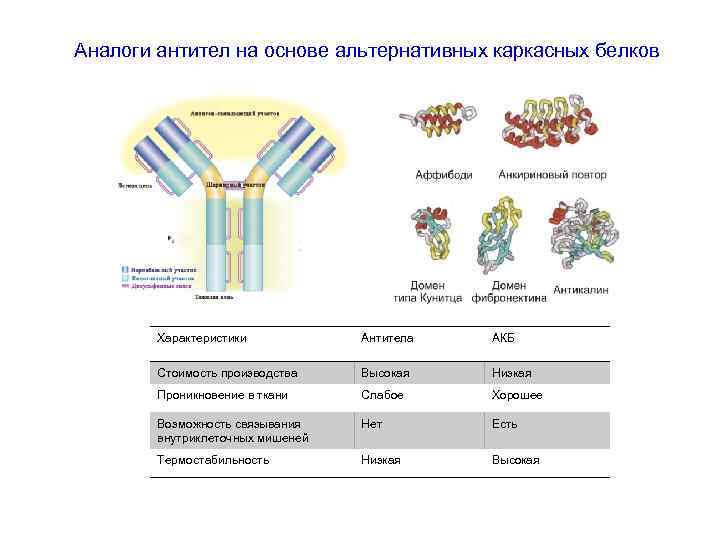
Аналоги антител на основе альтернативных каркасных белков Характеристики Антитела АКБ Стоимость производства Высокая Низкая Проникновение в ткани Слабое Хорошее Возможность связывания внутриклеточных мишеней Нет Есть Термостабильность Низкая Высокая
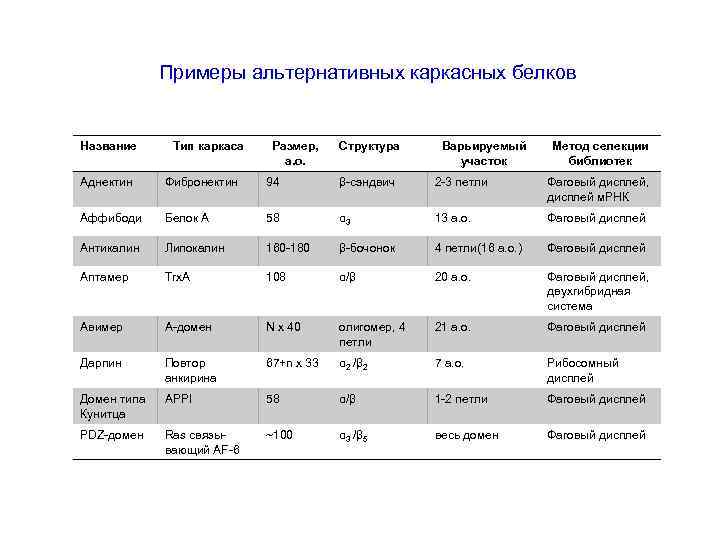
Примеры альтернативных каркасных белков Название Тип каркаса Размер, а. о. Структура Варьируемый участок Метод селекции библиотек Аднектин Фибронектин 94 β-сэндвич 2 -3 петли Фаговый дисплей, дисплей м. РНК Аффибоди Белок А 58 α 3 13 а. о. Фаговый дисплей Антикалин Липокалин 160 -180 β-бочонок 4 петли(16 а. о. ) Фаговый дисплей Аптамер Trx. A 108 α/β 20 а. о. Фаговый дисплей, двухгибридная система Авимер А-домен N х 40 олигомер, 4 петли 21 а. о. Фаговый дисплей Дарпин Повтор анкирина 67+n х 33 α 2 /β 2 7 а. о. Рибосомный дисплей Домен типа Кунитца APPI 58 α/β 1 -2 петли Фаговый дисплей PDZ-домен Ras связывающий AF-6 ~100 α 3 /β 5 весь домен Фаговый дисплей
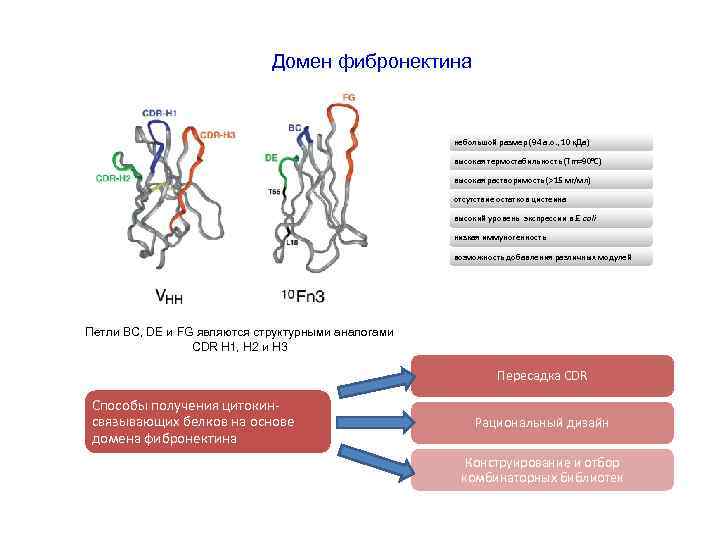
Домен фибронектина небольшой размер (94 а. о. , 10 к. Да) высокая термостабильность (Tm=90°C) высокая растворимость (>15 мг/мл) отсутствие остатков цистеина высокий уровень экспрессии в E. coli низкая иммуногенность возможность добавления различных модулей Петли BC, DE и FG являются структурными аналогами CDR H 1, H 2 и H 3 Пересадка CDR Способы получения цитокинсвязывающих белков на основе домена фибронектина Рациональный дизайн Конструирование и отбор комбинаторных библиотек
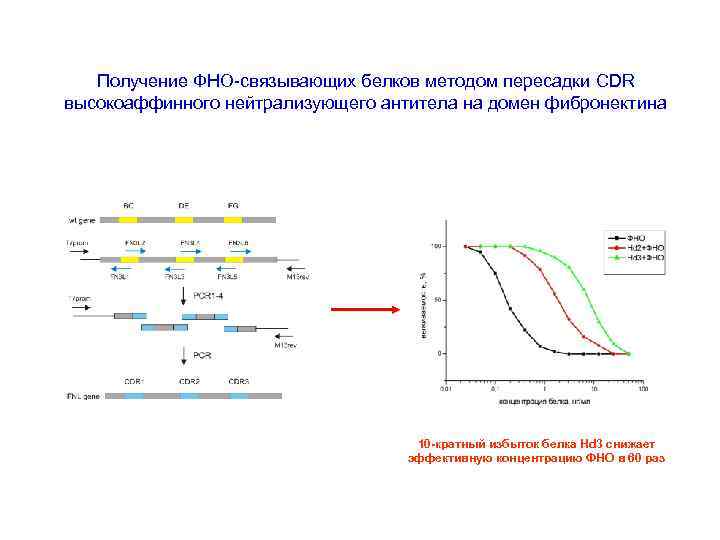
Получение ФНО-связывающих белков методом пересадки CDR высокоаффинного нейтрализующего антитела на домен фибронектина 10 -кратный избыток белка Hd 3 снижает эффективную концентрацию ФНО в 60 раз
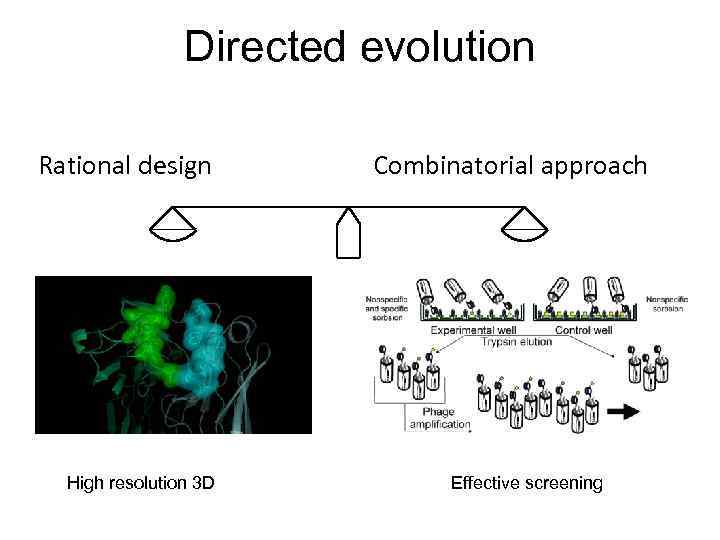
Directed evolution Rational design High resolution 3 D Combinatorial approach Effective screening

Рибосома – мишень множества антибиотиков за определение структуры рибосомы и ее комплексов с антибиотиками была присуждена Нобелевская премия Ада Йонат, Венки Рамакришнан и Том Стайтц
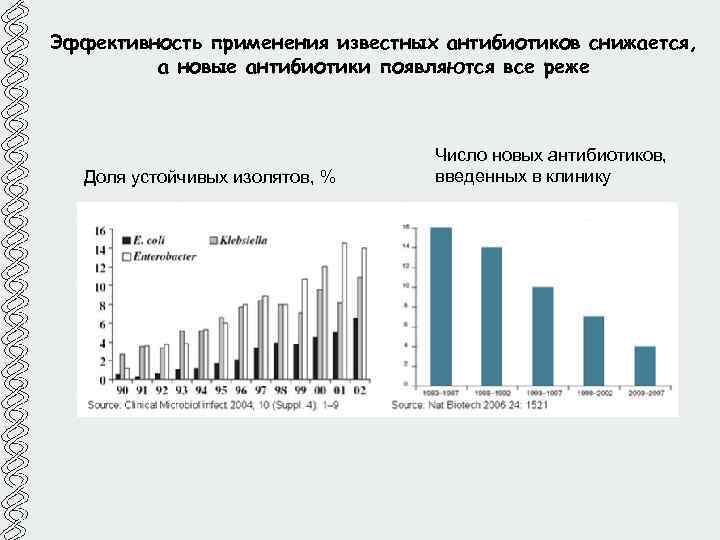
Эффективность применения известных антибиотиков снижается, а новые антибиотики появляются все реже Доля устойчивых изолятов, % Число новых антибиотиков, введенных в клинику

Персонализированная медицина XX век Терапия «блокбастерами» «Одно лекарство для всех» XXI век Индивидуальный подбор терапии в зависимости от иммунологических особенностей пациента и индивидуального течения РС
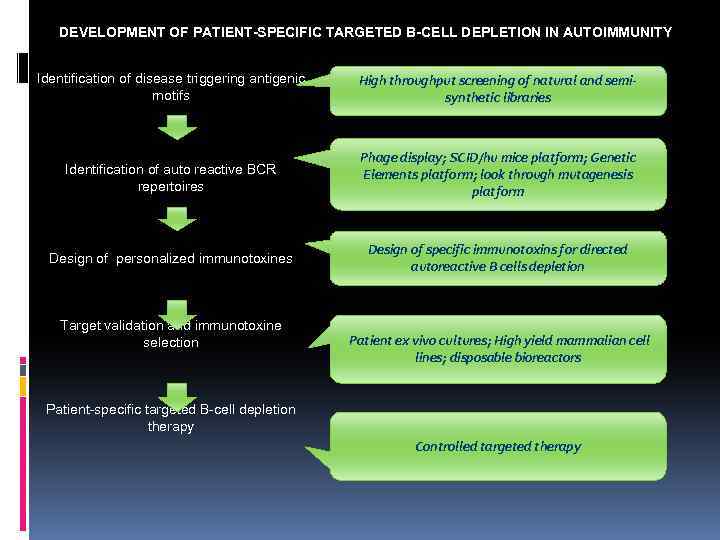
DEVELOPMENT OF PATIENT-SPECIFIC TARGETED B-CELL DEPLETION IN AUTOIMMUNITY Identification of disease triggering antigenic motifs High throughput screening of natural and semisynthetic libraries Identification of auto reactive BCR repertoires Phage display; SCID/hu mice platform; Genetic Elements platform; look through mutagenesis platform Design of personalized immunotoxines Design of specific immunotoxins for directed autoreactive B cells depletion Target validation and immunotoxine selection Patient ex vivo cultures; High yield mammalian cell lines; disposable bioreactors Patient-specific targeted B-cell depletion therapy Controlled targeted therapy

Резюме инвестиционного меморандума ØКраткое описание Инновационного проекта, рынка и рисков Продукт проекта: Технология адъювантного лечения пациента, включающая а себя следующие последовательные стадии q. Идентификация и валидация пациент-специфической молекулярной терапевтической мишени q. Генерация таргетного иммунотоксина или моноклонального антитела q. Оценка безопасности / эффективности с использованием пациент-специфических ex-vivo моделей q. Разработка индивидуализированного лечебного протокола q. Терапия пациента и мониторинг ответа Рынок средств и технологий ПМ: $ 450 млрд. к 2015 году ( PWC, The new science of personalized medicine: Translating the promise into practice. 2010) Риски проекта: q. Типичные для сектора- эффективность q. Проект-специфические- необходимость новых регуляторных парадигм 2/17/2018 Инвестиционный Меморандум КОНФИДЕНЦИАЛЬНО 56

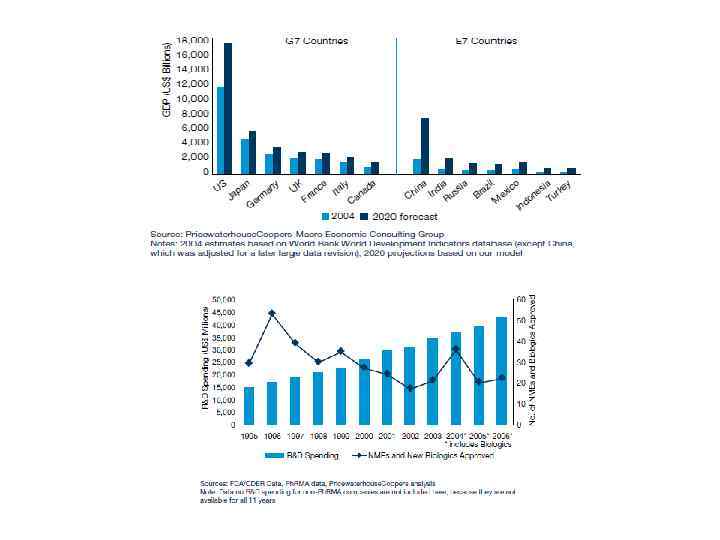
Pharma 2020: The vision. Which path will you take? A growth market US MARKET The global population is projected to rise from 6. 5 billion in 2005 to 7. 6 billion in 2020. It is also aging rapidly; by 2020, about 719. 4 m people – 9. 4% of the world’s inhabitants – will be 65 or more, compared with 477. 4 m (7. 3%) two years ago. Older people typically consume more medicines than younger people; four in five of those aged over 75 take at least one prescription product, while 36% take four or more. The number of deaths from heart attacks has declined by over 50% in most industrialised countries since the 1960 s, for example, while five year survival rates for US patients with cancer (expressed as an average for all sites) have risen from 53% in the mid-1980 s to 66% today. 16% of 300 m US people have no medical cover. In 2005, the US spent almost $2 trillion on healthcare, about $50 -60 billion of which went on providing medical treatment for the indigent. It is extremely difficult to calculate the additional cost of covering the uninsured population as a whole, but one study suggests that it could be between $125 billion and $150 billion a year, depending on the particular model that is used. Pricewaterhouse. Coopers


Background The National Center for Advancing Translational Sciences (NCATS) was established in December 2011 to advance the development, testing and implementation of diagnostics and therapeutics across a wide range of human diseases and conditions. NCATS strives to support research to reduce, remove or bypass costly and time-consuming bottlenecks in therapeutic development pipeline. By improving the process by which these tools and medicines are developed, NCATS aims to make translational science more efficient, less expensive and less risky. In this way, NCATS complements — and does not compete with — the work of the private sector and the other NIH Institutes and Centers. NCATS unifies complementary programs in these cross-cutting areas: ► Clinical and Translational Science Activities o Clinical and Translational Science Awards (CTSA), a consortium of medical research institutions working to improve the way clinical and translational research is conducted nationwide ► Rare Diseases Research and Therapeutics o Office of Rare Diseases Research, which coordinates and supports research on rare diseases Bridging Interventional Development Gaps, which provides access to critical pre-clinical resources needed for the development of new therapeutic agents Therapeutics for Rare and Neglected Diseases, a program to encourage and speed the development of new drugs for rare and neglected diseases ► Re-engineering Translational Sciences o NIH Chemical Genomics Center, which provides researchers with access to the large-scale screening and chemistry capacity necessary to identify compounds that can be used as chemical probes to validate new therapeutic targets Discovering New Therapeutic Uses for Existing Molecules, part of the Rescuing and Repurposing Drugs initiative , matches researchers with a selection of molecular compounds from industry to test ideas for new therapeutic uses Tissue Chips for Drug Screening, which aims to develop 3 -D human tissue chips that accurately model the structure and function of human organs to better predict drug safety Toxicology in the 21 st Century (Tox 21), which is screening a collection of 10, 000 compounds to identify potentially toxic disruptions in biological pathways and develop ways to predict toxicity more accurately In addition, NCATS’ Cures Acceleration Network enables overarching and flexible support for a variety of initiatives and is designed to address scientific and technical challenges that impede transitional research.

NIH Office of the Director (OD) For Immediate Release Friday, September 16, 2011 Contact: NIH Communications 301 -496 -5787 Home > News & Events Subscribe to receive future NIH news releases. NIH, DARPA and FDA collaborate to develop cutting-edge technologies to predict drug safety President Obama announced today that the National Institutes of Health will collaborate with the Defense Advanced Research Projects Agency (DARPA), and the U. S. Food and Drug Administration to develop a chip to screen for safe and effective drugs far more swiftly and efficiently than current methods, and before they are tested in humans. The chip will be loaded with specific cell types that reflect human biology. It will be designed to allow multiple different readouts that can indicate whether a particular compound is likely to be safe or toxic for humans. DARPA and NIH will run separate and independent programs, but they will work closely to ensure maximum benefit and efficiencies. For example, DARPA and NIH will facilitate collaborations between researchers and FDA to advance the goals of both programs. This fall, the two agencies, in coordination with FDA, will solicit proposals from industry, government labs, academic institutions, and other research organizations on how best to develop the chip, bringing together the latest advances in engineering, biology, and toxicology to bear on this complex problem. "Drug toxicity is one of the most common reasons why promising compounds fail, " Francis S. Collins, M. D. , Ph. D. , NIH director said. "We need to know which ones are safe and effective much earlier on in the process. This is an unprecedented opportunity to speed development of effective therapies, while saving time and money. " Over the next five years, the NIH plans to commit up to $70 million and DARPA will commit a comparable amount to this effort. This groundbreaking effort is an example of the types of innovative projects that would be led by the proposed National Center for Advancing Translational Sciences (NCATS). NCATS would help identify barriers to progress and provide science-based solutions to reduce costs and the time required to develop new drugs and diagnostics. FDA will help determine how this new technology can be utilized to assess drug safety, prior to approval for first-in-human studies. "We know the development pipeline has bottlenecks in it, and everyone would benefit from fixing them, "Collins said. "What we need are entirely novel approaches to translational science, to take full advantage of the deluge of new biomedical discoveries that have been made in recent years. " As proposed, NCATS will study the steps in the process of diagnostics and therapeutics development, identify the bottlenecks, and experiment with innovative methods to streamline the process. By focusing on developing innovative new tools and methods for therapeutics development, as opposed to developing therapeutics themselves, NCATS will enable others to bring safer and more effective medical products to market in less time. In this way, NCATS will complement, and not compete with, the work of the private sector and other NIH translational science efforts. About the National Institutes of Health (NIH): NIH, the nation's medical research agency, includes 27 Institutes and Centers and is a component of the U. S. Department of Health and Human Services. NIH is the primary federal agency conducting and supporting basic, clinical, and translational medical research, and is investigating the causes, treatments, and cures for both common and rare diseases. For more information about NIH and its programs, visit http: //www. nih. gov. NIH. . . Turning Discovery Into Health ®
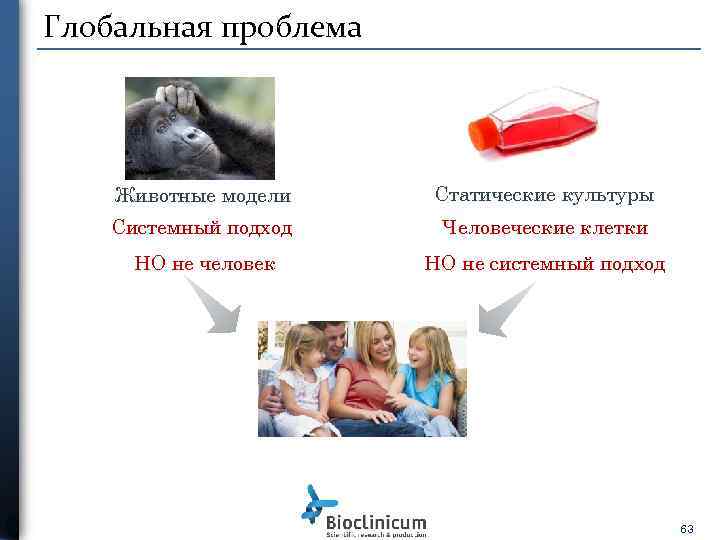
Глобальная проблема Животные модели Статические культуры Системный подход Человеческие клетки НО не человек НО не системный подход 63
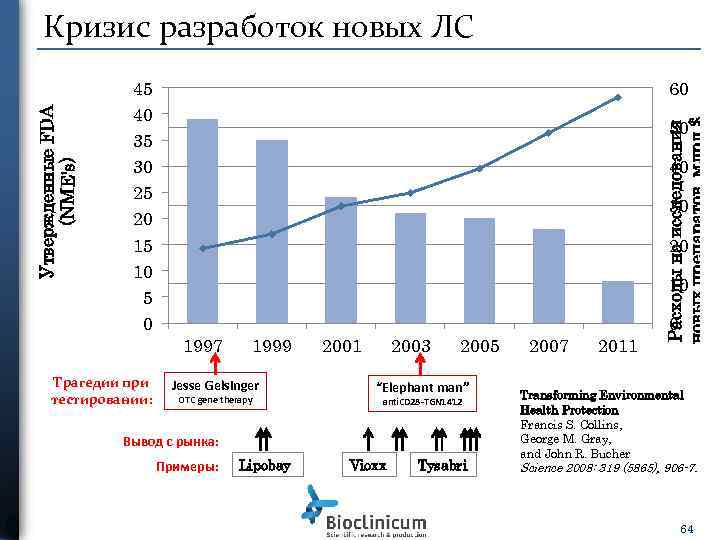
45 40 35 30 25 20 15 10 5 0 60 50 40 30 20 10 0 1997 Трагедии при тестировании: Расходы на исследования новых препаратов, млрд $ Утвержденные FDA (NME's) Кризис разработок новых ЛС 1999 Jesse Gelsinger OTC gene therapy 2001 2003 2005 “Elephant man” anti. CD 28 -TGN 1412 Вывод с рынка: Примеры: Lipobay Vioxx Tysabri 2007 2011 Transforming Environmental Health Protection Francis S. Collins, George M. Gray, and John R. Bucher Science 2008: 319 (5865), 906 -7. 64

Кризис разработок новых ЛС Проблема: Более 50% разрабатываемых фармацевтических препаратов прошедших доклинические исследования, оказываются токсичными для человека. Отсутствуют in-vitro человеческие клеточные модели, которые позволят тестировать новые препараты. Решение: Разработка методик испытаний препаратов с использованием клеточных модели тканей человека, объединенных в единую систему. 65
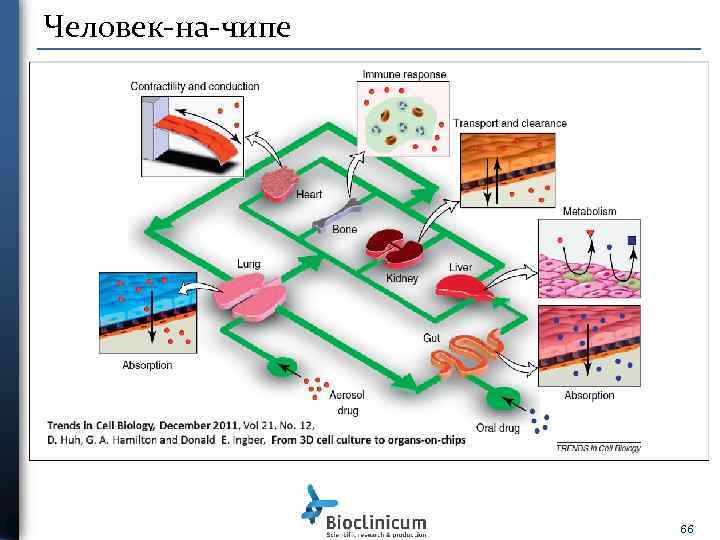
Человек-на-чипе 66

Микробиореактор Homunculus Состоит из сменного клеточного блока и блока управления Ø Динамическая система – Насос на чипе Ø ADMET принцип – много моделей органов Ø Масштаб - 100, 000 раз меньше человека Ø Быстрое прототипирование новых дизайнов чипа 67
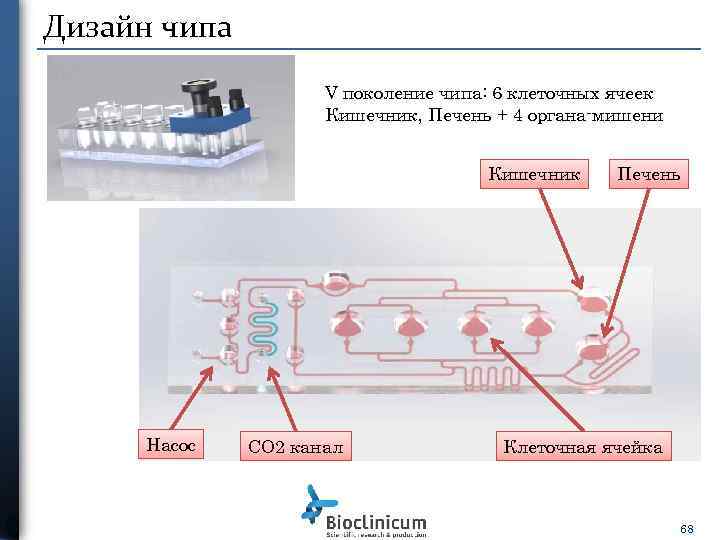
Дизайн чипа V поколение чипа: 6 клеточных ячеек Кишечник, Печень + 4 органа-мишени Кишечник Насос СО 2 канал Печень Клеточная ячейка 68

Возможные сферы использования Микробиореактор Homunculus – биотехнологическая платформа, реализующая на клеточном уровне упрощенную модель взаимодействий тканей человеческого организма 1. Доклиническое изучение безопасности и эффективности новых препаратов и комбинаций препаратов на моделях тканей человека (токсичность, эффективность) 2. Подбор схем терапии на образцах биопсии пациента (персонализированная медицина) 69
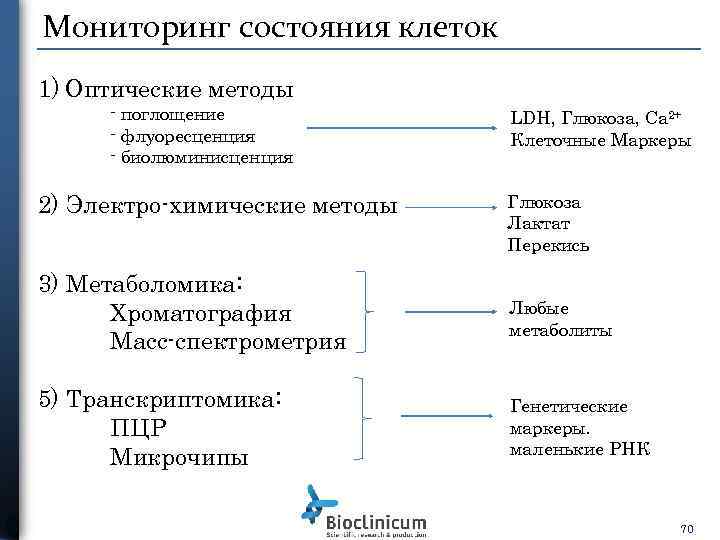
Мониторинг состояния клеток 1) Оптические методы - поглощение - флуоресценция - биолюминисценция 2) Электро-химические методы LDH, Глюкоза, Са 2+ Клеточные Маркеры Глюкоза Лактат Перекись 3) Метаболомика: Хроматография Масс-спектрометрия Любые метаболиты 5) Транскриптомика: ПЦР Микрочипы Генетические маркеры. маленькие РНК 70
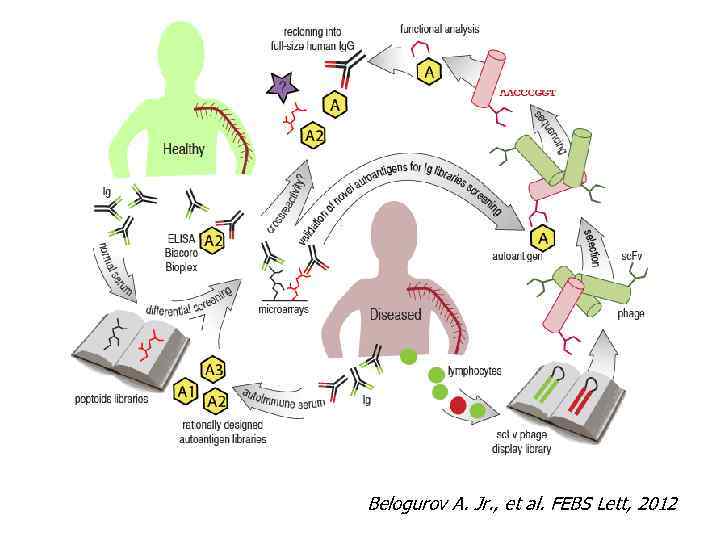
Belogurov A. Jr. , et al. FEBS Lett, 2012

Традиционные подходы к лечению рассеянного склероза Новые подходы к лечению рассеянного склероза, разрабатываемые в лаборатории биокатализа ИБХ РАН Copaxone (глатирамера ацетат)/IFNb Индукция толерантности иммунной – общая иммунносупрессия системы к ОБМ. Пептид основного белка миелина ОБМ 46 -62 Моноклональные антитела Rituximab/Natalizumab – неспецифическое воздействие на Т-/В-клетки Направленная элиминация клонов аутореактивных В-клеток иммунотоксинами Ингибиторы активности протеасомы: Иммунопротеасома в ЦНС как Bortezomib – апоптоз активно мишень для направленного действия пролиферирующих клеток низкомолекулярных ингибиторов
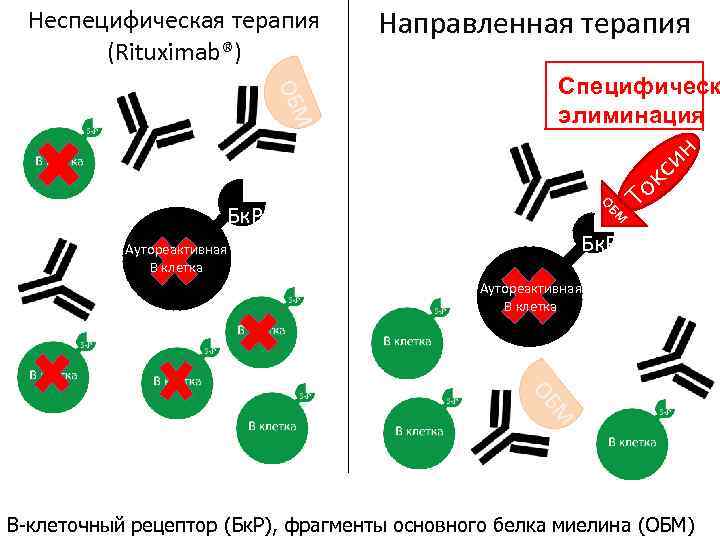
Неспецифическая терапия (Rituximab®) Направленная терапия Аутореактивная В клетка БМ О Бк. Р То кс и н ОБМ Специфическ элиминация CD 4 CD 25 High Бк. Р Аутореактивная В клетка М ОБ B-клеточный рецептор (Бк. Р), фрагменты основного белка миелина (ОБМ)
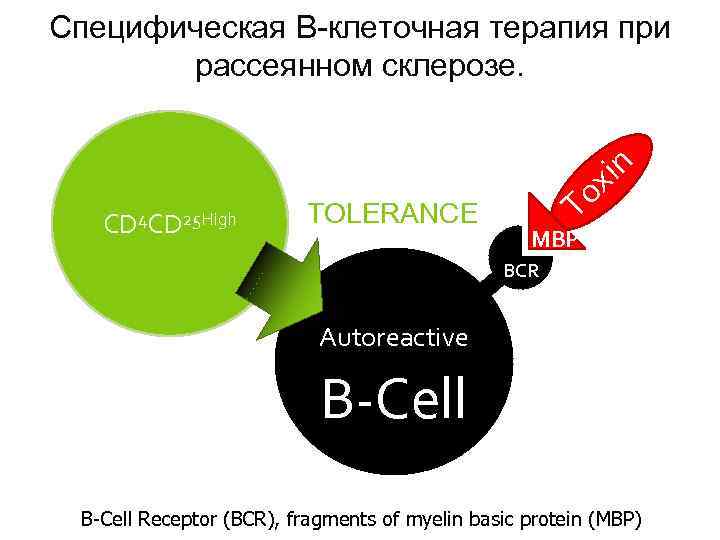
Специфическая B-клеточная терапия при рассеянном склерозе. CD 4 CD 25 High TOLERANCE in x To MBP BCR Autoreactive B-Cell Receptor (BCR), fragments of myelin basic protein (MBP)
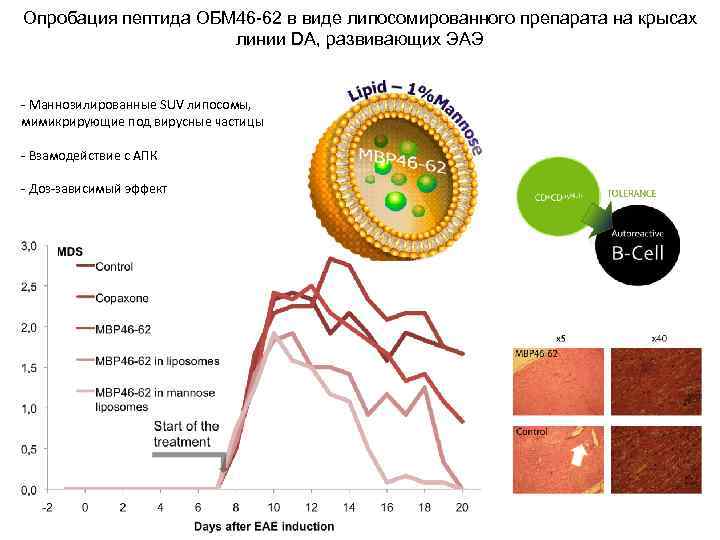
Опробация пептида ОБМ 46 -62 в виде липосомированного препарата на крысах линии DA, развивающих ЭАЭ - Маннозилированные SUV липосомы, мимикрирующие под вирусные частицы - Взамодействие с АПК - Доз-зависимый эффект
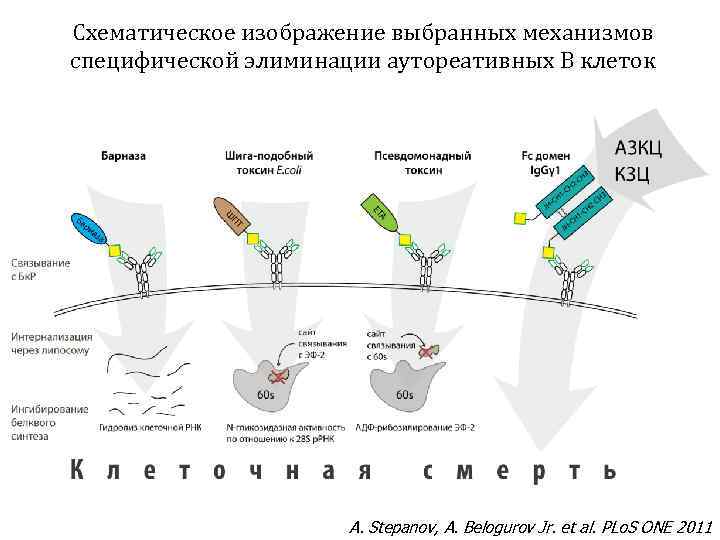
Схематическое изображение выбранных механизмов специфической элиминации аутореативных В клеток A. Stepanov, A. Belogurov Jr. et al. PLo. S ONE 2011
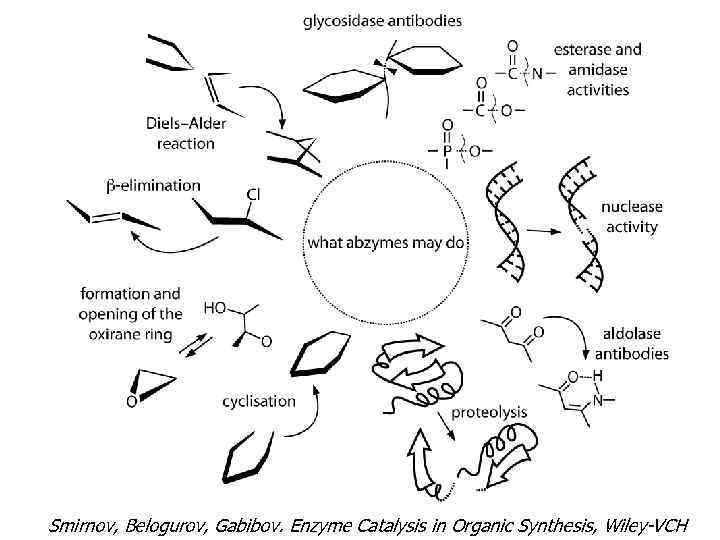
Smirnov, Belogurov, Gabibov. Enzyme Catalysis in Organic Synthesis, Wiley-VCH
A. 17 antibody has unusual deep cavity with nucleophilic tyrosine at its base I. Smirnov, I. Kurkova et al, PNAS 2011
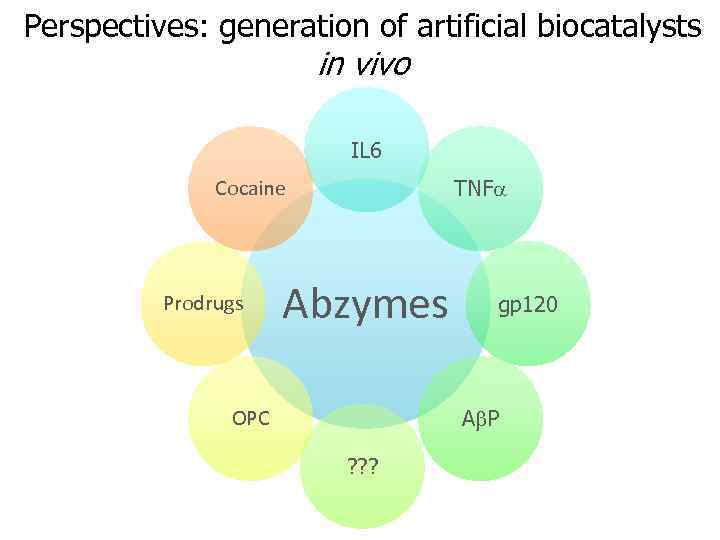
Perspectives: generation of artificial biocatalysts in vivo IL 6 TNFa Cocaine Prodrugs Abzymes gp 120 Ab. P OPC ? ? ?
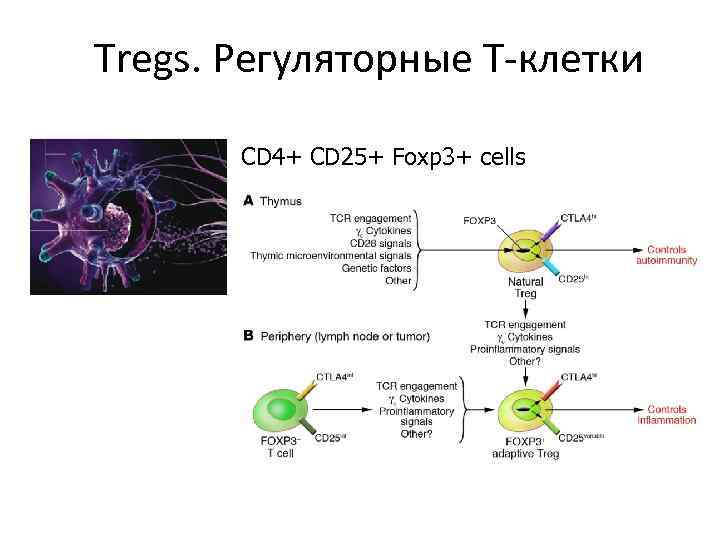
Tregs. Регуляторные Т-клетки CD 4+ CD 25+ Foxp 3+ cells
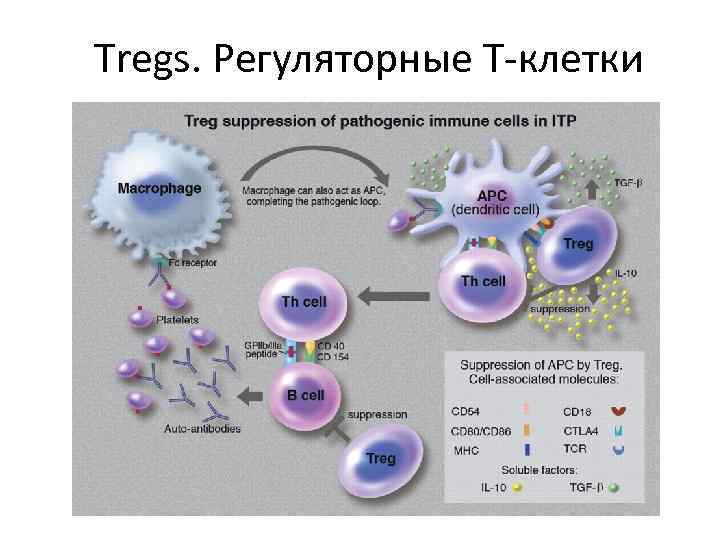
Tregs. Регуляторные Т-клетки
MULTIPLE SCLEROSIS Is it Immunoproteasome in CNS during MS? Is there any pathogenic role of the Immunoproteasome?

Традиционные подходы к лечению рассеянного склероза Новые подходы к лечению рассеянного склероза, разрабатываемые в лаборатории биокатализа ИБХ РАН Copaxone (глатирамера ацетат)/IFNb Индукция толерантности иммунной – общая иммунносупрессия системы к ОБМ. Пептид основного белка миелина ОБМ 46 -62 Моноклональные антитела Rituximab/Natalizumab – неспецифическое воздействие на Т-/В-клетки Направленная элиминация клонов аутореактивных В-клеток иммунотоксинами Ингибиторы активности протеасомы: Иммунопротеасома в ЦНС как Bortezomib – апоптоз активно мишень для направленного действия пролиферирующих клеток низкомолекулярных ингибиторов
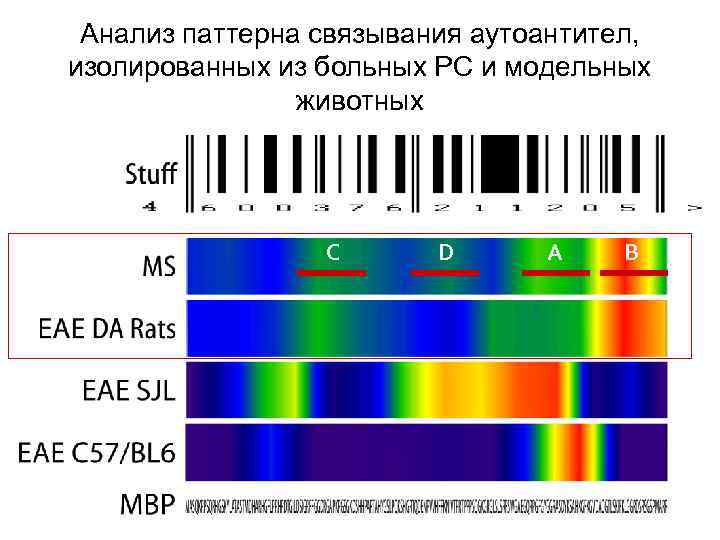
Анализ паттерна связывания аутоантител, изолированных из больных РС и модельных животных C D A B
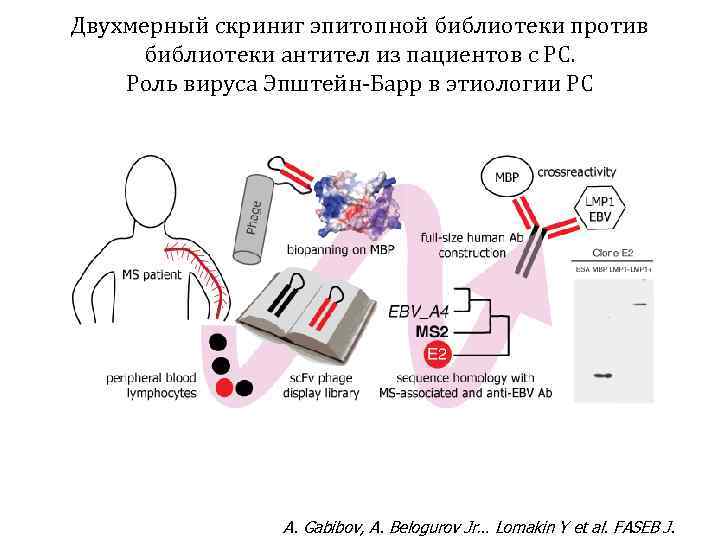
Двухмерный скриниг эпитопной библиотеки против библиотеки антител из пациентов с РС. Роль вируса Эпштейн-Барр в этиологии РС A. Gabibov, A. Belogurov Jr… Lomakin Y et al. FASEB J.
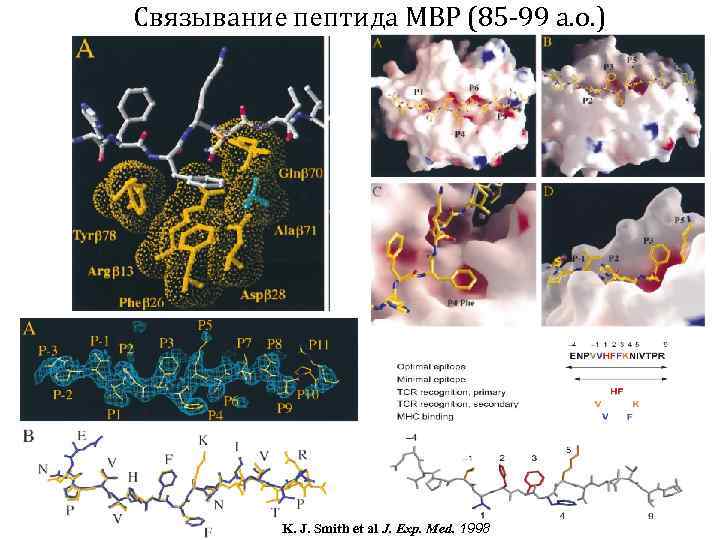
Связывание пептида MBP (85 -99 а. о. ) K. J. Smith et al J. Exp. Med. 1998
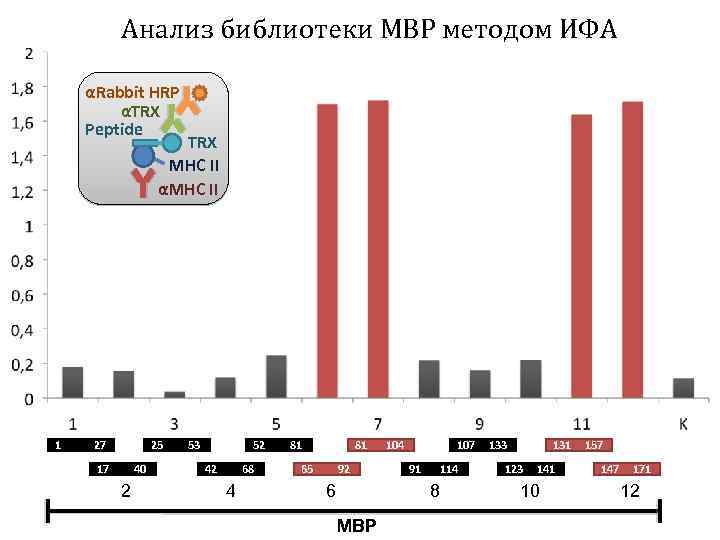
Анализ библиотеки MBP методом ИФА αRabbit HRP αTRX Peptide TRX MHC II αMHC II 1 27 25 17 40 2 53 52 42 68 4 81 81 65 92 6 104 107 91 114 8 MBP 133 131 123 141 10 157 147 171 12
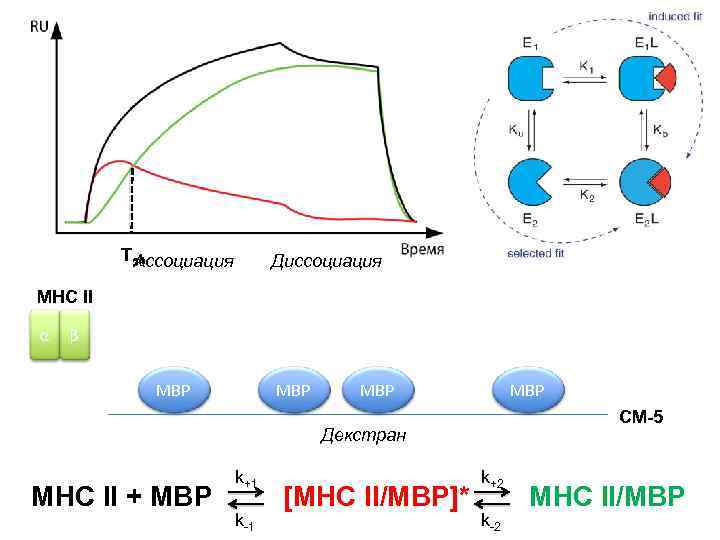
T 50 Ассоциация Диссоциация MHC II α β MBP MBP CM-5 Декстран MHC II + MBP k+1 k-1 [MHC II/MBP]* k+2 k-2 MHC II/MBP
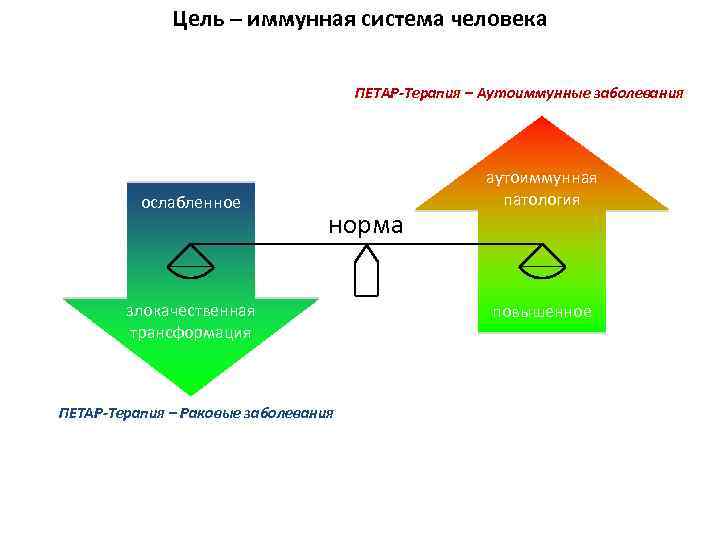
Цель – иммунная система человека ПЕТАР-Терапия – Аутоиммунные заболевания ослабленное норма злокачественная трансформация ПЕТАР-Терапия – Раковые заболевания аутоиммунная патология повышенное
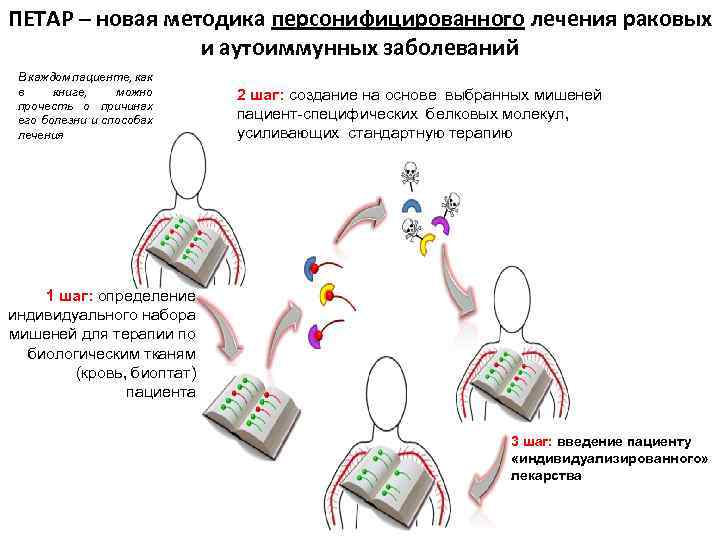
ПЕТАР – новая методика персонифицированного лечения раковых и аутоиммунных заболеваний В каждом пациенте, как в книге, можно прочесть о причинах его болезни и способах лечения 2 шаг: создание на основе выбранных мишеней пациент-специфических белковых молекул, усиливающих стандартную терапию 1 шаг: определение индивидуального набора мишеней для терапии по биологическим тканям (кровь, биоптат) пациента 3 шаг: введение пациенту «индивидуализированного» лекарства
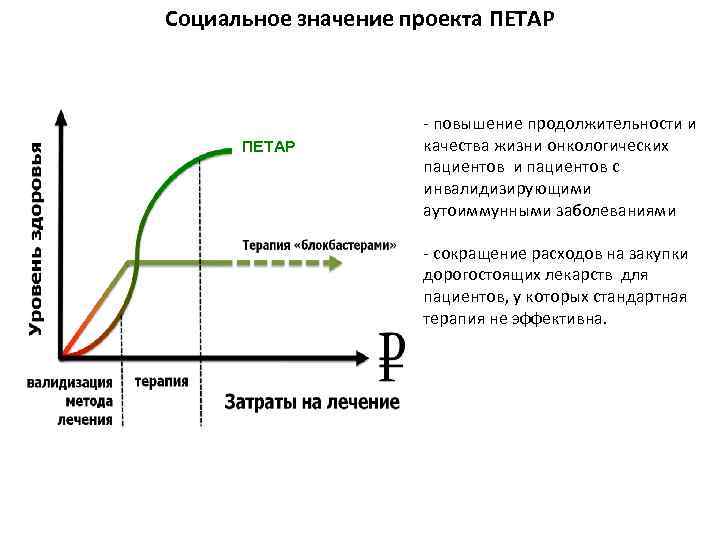
Социальное значение проекта ПЕТАР - повышение продолжительности и качества жизни онкологических пациентов и пациентов с инвалидизирующими аутоиммунными заболеваниями - сокращение расходов на закупки дорогостоящих лекарств для пациентов, у которых стандартная терапия не эффективна.
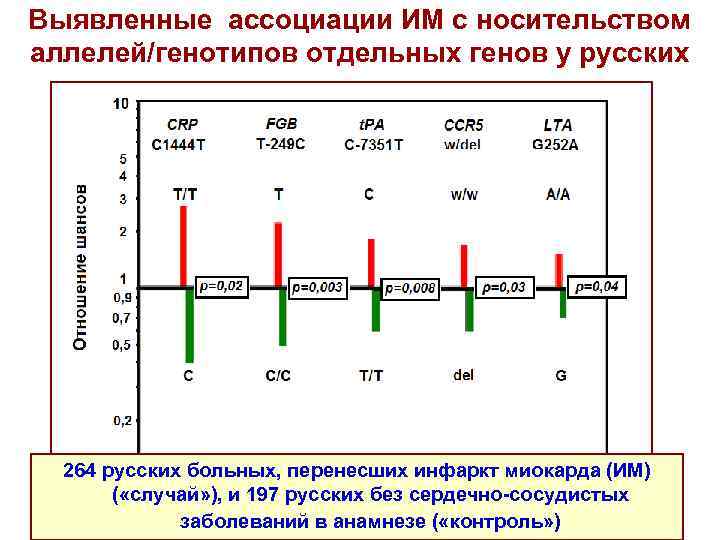
Выявленные ассоциации ИМ с носительством аллелей/генотипов отдельных генов у русских 264 русских больных, перенесших инфаркт миокарда (ИМ) ( «случай» ), и 197 русских без сердечно-сосудистых заболеваний в анамнезе ( «контроль» )
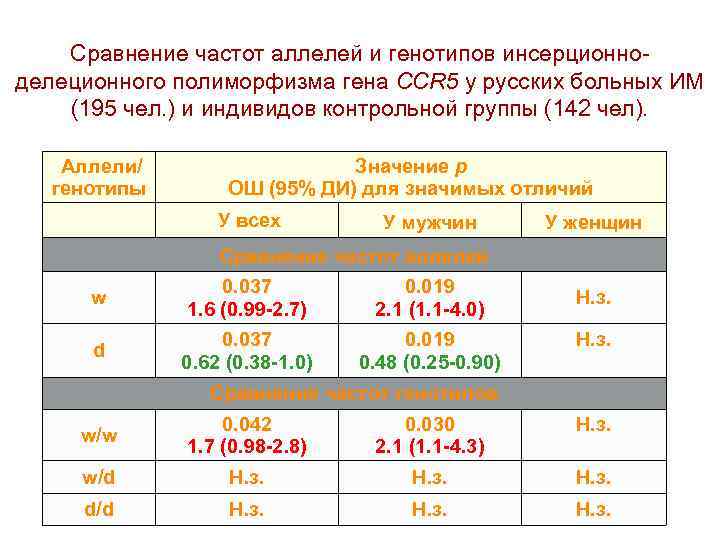
Cравнение частот аллелей и генотипов инсерционноделеционного полиморфизма гена ССR 5 у русских больных ИМ (195 чел. ) и индивидов контрольной группы (142 чел). Аллели/ генотипы Значение р ОШ (95% ДИ) для значимых отличий У всех У мужчин У женщин Cравнение частот аллелей w 0. 037 1. 6 (0. 99 -2. 7) 0. 019 2. 1 (1. 1 -4. 0) d 0. 037 0. 62 (0. 38 -1. 0) 0. 019 0. 48 (0. 25 -0. 90) Н. з. Cравнение частот генотипов w/w 0. 042 1. 7 (0. 98 -2. 8) 0. 030 2. 1 (1. 1 -4. 3) Н. з. w/d Н. з. d/d Н. з.
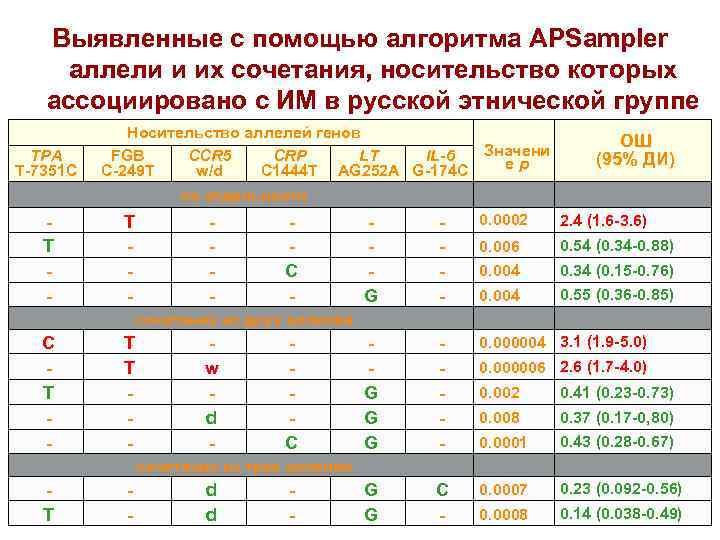
Выявленные с помощью алгоритма APSampler аллели и их сочетания, носительство которых ассоциировано с ИМ в русской этнической группе TPA T-7351 C Носительство аллелей генов Значени FGB CCR 5 CRP LT IL-6 е р C-249 T w/d C 1444 T AG 252 A G-174 C ОШ (95% ДИ) по отдельности T - - C - G - 0. 0002 2. 4 (1. 6 -3. 6) 0. 006 0. 54 (0. 34 -0. 88) 0. 004 0. 34 (0. 15 -0. 76) 0. 004 0. 55 (0. 36 -0. 85) G G G - 0. 000004 3. 1 (1. 9 -5. 0) G G C - сочетания из двух аллелей C T - T T - w d - C 0. 000006 2. 6 (1. 7 -4. 0) 0. 002 0. 41 (0. 23 -0. 73) 0. 008 0. 37 (0. 17 -0, 80) 0. 0001 0. 43 (0. 28 -0. 67) 0. 0007 0. 23 (0. 092 -0. 56) 0. 0008 0. 14 (0. 038 -0. 49) сочетания из трех аллелей T - d d -

Сравнение данных по генетической предрасположенности к инфаркту миокарда и ишемическому инсульту (инфаркту мозга) у русских • Уровень значимости выявленных ассоциаций ИМ с генными ансамблями, в отличие от ИИ, очень высок. • Вероятно, генетическая компонента как фактор риска более существенна для развития ИМ, чем ИИ. • При обоих заболеваниях прослеживается аддитивный вклад аллелей/генотипов в выявляемые генные ансамбли; при ИМ, возможно, в случае сочетания TPA (-7351)C c FGB (-249)T (p = 0. 000004) проявляются эпистатические взаимодействия.

Характер течения ишемического инсульта у якутов: генетический полиморфизм и степень остаточной неврологической симптоматики
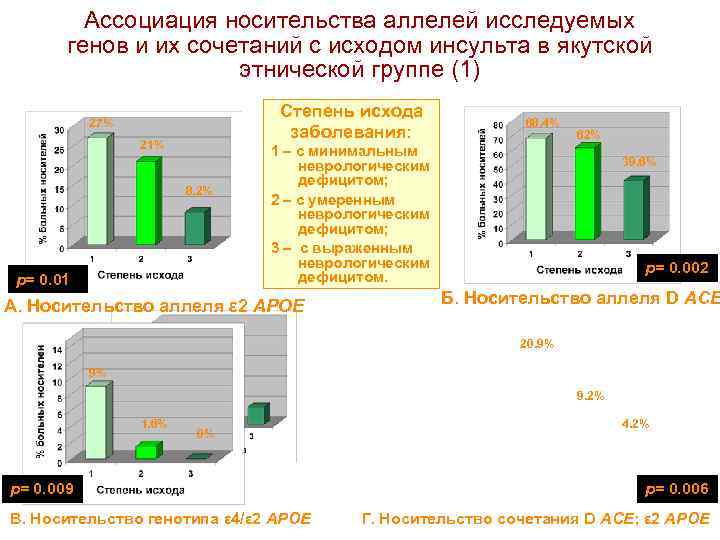
Ассоциация носительства аллелей исследуемых генов и их сочетаний с исходом инсульта в якутской этнической группе (1) Степень исхода заболевания: 27% 21% 8. 2% р= 0. 01 68. 4% 62% 1 – с минимальным неврологическим дефицитом; 2 – с умеренным неврологическим дефицитом; 3 – с выраженным неврологическим дефицитом. А. Носительство аллеля ε 2 APOE 39. 6% р= 0. 002 Б. Носительство аллеля D ACE 20. 9% 9% 9. 2% 1. 6% 0% р= 0. 009 В. Носительство генотипа ε 4/ε 2 APOE 4. 2% р= 0. 006 Г. Носительство сочетания D ACE; ε 2 APOE
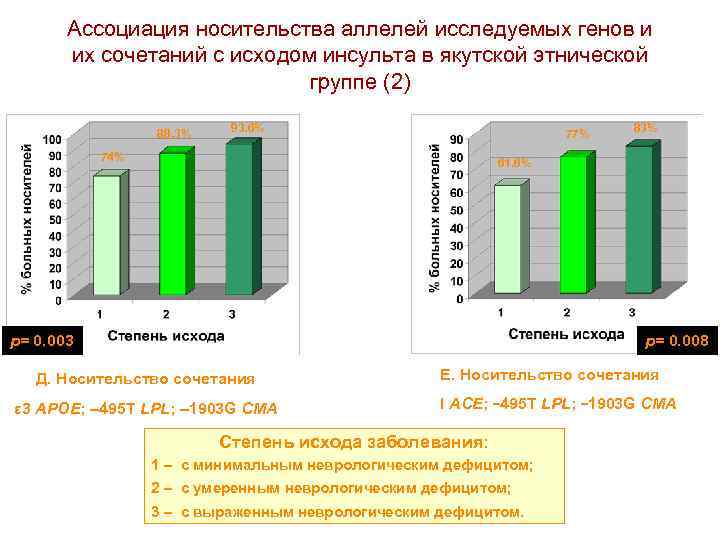
Ассоциация носительства аллелей исследуемых генов и их сочетаний с исходом инсульта в якутской этнической группе (2) 88. 3% 93. 6% 77% 74% 83% 61. 6% р= 0. 003 р= 0. 008 Д. Носительство сочетания ε 3 АРОЕ; – 495 Т LPL; – 1903 G СМА Е. Носительство сочетания I ACE; – 495 Т LPL; – 1903 G СМА Степень исхода заболевания: 1 – с минимальным неврологическим дефицитом; 2 – с умеренным неврологическим дефицитом; 3 – с выраженным неврологическим дефицитом.

Прогнозирование исходов ИИ • • • На исход ИИ влияет носительство аллелей генов APOE (ε 2 – благоприятный, ε 3 – неблагоприятный) и ACE (D – благоприятный, I – неблагоприятный) , а также их сочетаний друг с другом и с аллелями генов LPL и СМА. Влияние на исход ИИ таких модифицируемых факторов риска как гиперхолестеринемия и избыточная масса тела проявляется в основном для исхода с выраженным неврологическим дефицитом. Проведенное нами исследование дает основание предполагать, что у якутов генетическая компонента в большей степени определяет характер исхода ИИ, чем его развитие и клиническое течение. Полученные данные открывают возможность для предсказания исхода ИИ на основании генотипирования больных, перенесших ИИ, по генам APOE, АСЕ, LPL и CMA или даже только по генам APOE и АСЕ. С практической точки зрения прогноз характера течения и исхода заболевания на основании анализа генетического полиморфизма представляется легче реализуемым и, возможно, более значимым, чем прогноз риска заболевания, поскольку может обеспечить дифференцированный лечебный подход.

Работа выполнена: § В РКНПК и на кафедре молекулярной биологии и медицинской биотехнологии РГМУ, Москва Р. М. Барсова, Н. А. Матвеева, М. Г. Парфенов, М. Я. Руда, М. А. Судомоина, Т. С. Сухинина, Б. В. Титов, О. О. Фаворова, Р. М. Шахнович § На кафедре неврологии и нейрохирургии РГМУ, Москва А. Б. Гехт, Е. И. Гусев, О. В. Кобылина, М. Ю. Мартынов § На кафедре неврологии Якутского государственного университета им. М. К. Аммосова, Якутск Т. Я. Николаева, С. А. Чугунова § В ГНЦ “Гос. НИИгенетика” и в The Johns Hopkins University, Baltimore, USA А. В. Фаворов, M. F. Ochs, G. Parmigiani

Спасибо за внимание!

Персонализированная медицина, ориентированная на конкретного пациента в соответствии с его генотипом - современная стратегия развития здравоохранения В основе достижений персонализированной медицины лежит расшифровка генома человека и фундаментальные исследования, направленные на выявление роли вариантов генов в развитии заболеваний и эффективности их лечения. Пример такого подхода – исследования, проводимые в Российском кардиологическом научно-производственном комплексе по договору с ИБХ им. М. М. Шемякина и Ю. А. Овчинникова РАН в рамках ФЦП «Национальная технологическая база» на 2007 -2011 гг. (Гос. контракт № ГП/07/ 440/НТБ/К , Шифр «ГЕН» ).
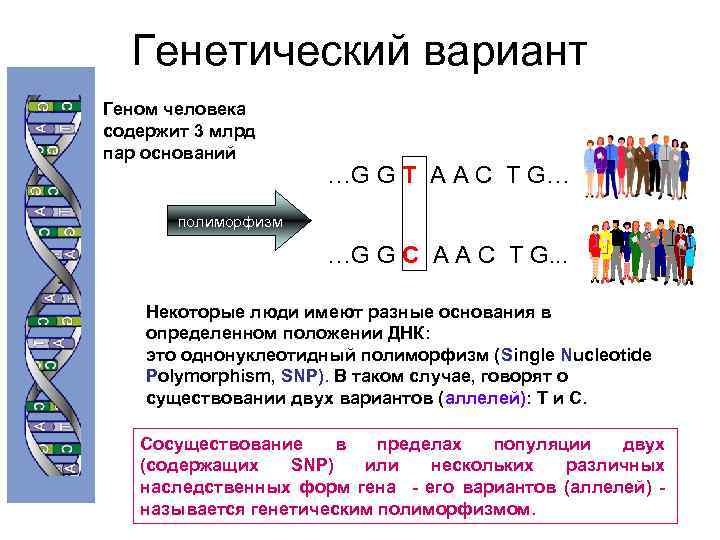
Генетический вариант Геном человека содержит 3 млрд пар оснований …G G T A A C T G… полиморфизм …G G C A A C T G. . . Некоторые люди имеют разные основания в определенном положении ДНК: это однонуклеотидный полиморфизм (Single Nucleotide Polymorphism, SNP). В таком случае, говорят о существовании двух вариантов (аллелей): T и С. Сосуществование в пределах популяции двух (содержащих SNP) или нескольких различных наследственных форм гена - его вариантов (аллелей) - называется генетическим полиморфизмом.
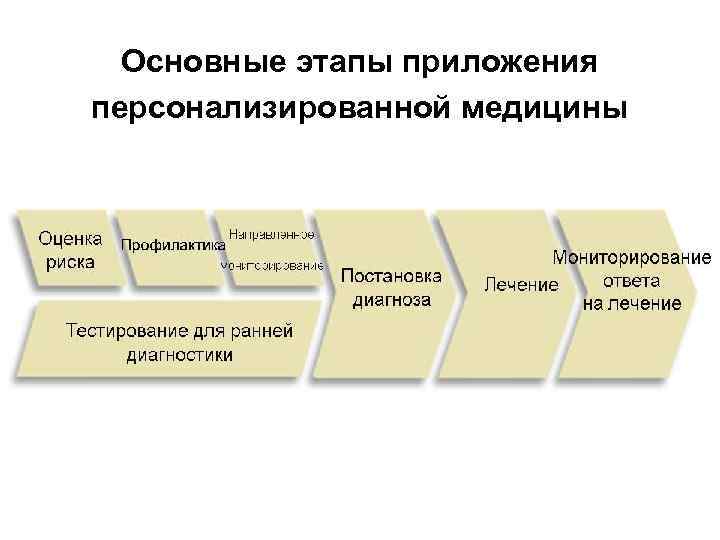
Основные этапы приложения персонализированной медицины

Направление исследований: создание рациональных методов прогнозирования социально-значимых заболеваний и эффективности их лечения с учетом индивидуальных генетических вариантов человека ü Исследуемые сердечно-сосудистые и неврологические заболевания (ишемический и геморрагический инсульт, рассеянный склероз, инфаркт миокарда, гипертония) являются комплексными (мультифакторными, многофакторными) – их развитие зависит и от генетических факторов, и от факторов внешней среды ü Эти заболевания являются полигенными - их развитие зависит от нескольких генов ü В работе анализируется не только роль вариантов отдельных генов, но и роль их сочетаний (генных ансамблей), отражающая совместный вклад ряда независимых или взаимодействующих генов. ü Для анализа генных ансамблей разработан новый биоинформатический подход, и на его основе создано программное обеспечение APSampler. ü Разрабатываются протоколы индивидуального предсказания предрасположенности к исследуемым заболеваниям и эффективности их лечения для населения России.

Инсульт в России > 450 000 новых случаев ежегодно 200 000 смертей >1 000 выживших после инсульта >800 000 - с инвалидизацией Инвалидизация после инсульта составляет 3, 2 на 10 000 населения Лишь 20% выживших возвращаются к прежней работе 67, 8% всех инсультов в России составляет ишемический инсульт – острое нарушение мозговой деятельности вследствие недостаточности кровообращения.
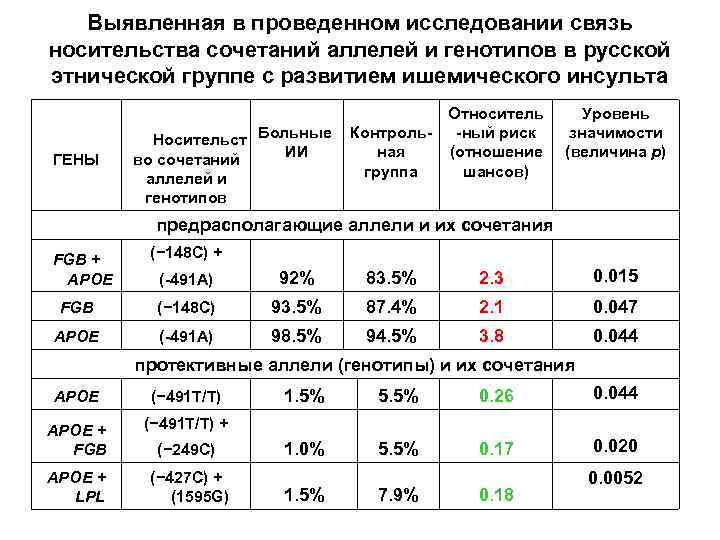
Выявленная в проведенном исследовании связь носительства сочетаний аллелей и генотипов в русской этнической группе с развитием ишемического инсульта ГЕНЫ Носительст Больные ИИ во сочетаний аллелей и генотипов Контрольная группа Относитель -ный риск (отношение шансов) Уровень значимости (величина р) предрасполагающие аллели и их сочетания FGB + APOE (− 148 C) + (-491 A) 92% 83. 5% 2. 3 0. 015 FGB (− 148 C) 93. 5% 87. 4% 2. 1 0. 047 APOE (-491 A) 98. 5% 94. 5% 3. 8 0. 044 протективные аллели (генотипы) и их сочетания APOE (− 491 Т/T) APOE + FGB (− 427 C) + (1595 G) 5. 5% 0. 26 0. 044 1. 0% 5. 5% 0. 17 0. 020 (− 491 Т/T) + APOE + LPL 1. 5% (− 249 C) 1. 5% 7. 9% 0. 18 0. 0052
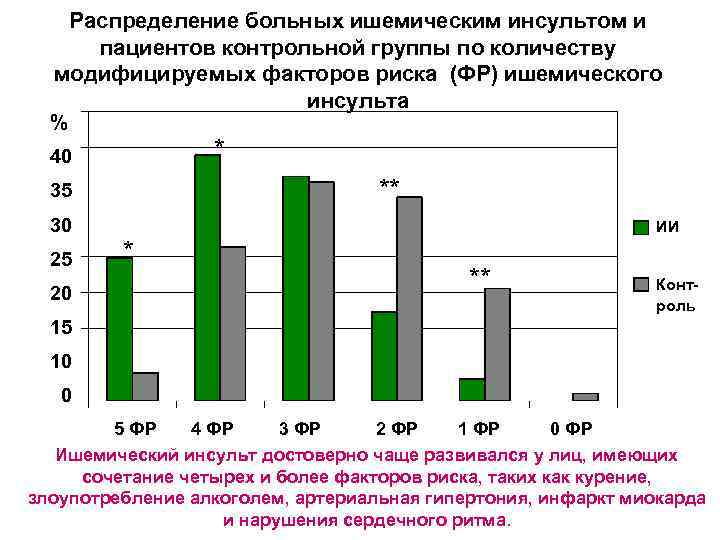
Распределение больных ишемическим инсультом и пациентов контрольной группы по количеству модифицируемых факторов риска (ФР) ишемического инсульта % * 40 ** 35 30 25 20 * ИИ ** Контроль 15 10 0 5 ФР 4 ФР 3 ФР 2 ФР 1 ФР 0 ФР Ишемический инсульт достоверно чаще развивался у лиц, имеющих сочетание четырех и более факторов риска, таких как курение, злоупотребление алкоголем, артериальная гипертония, инфаркт миокарда и нарушения сердечного ритма.
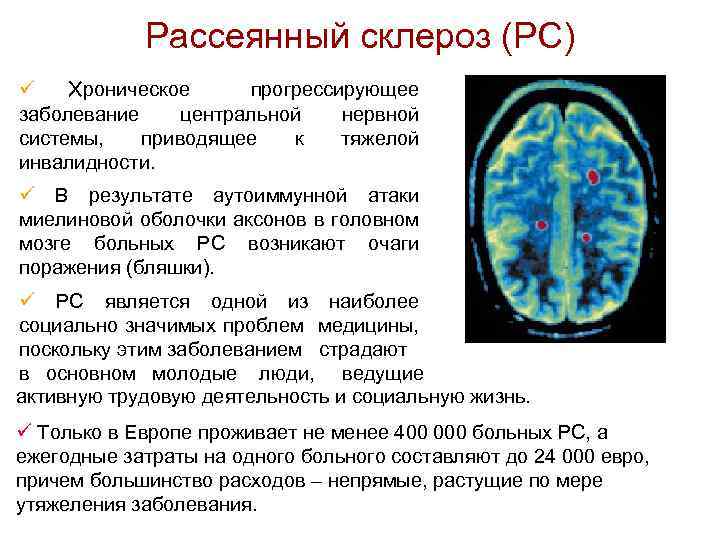
Рассеянный склероз (РС) ü Хроническое прогрессирующее заболевание центральной нервной системы, приводящее к тяжелой инвалидности. ü В результате аутоиммунной атаки миелиновой оболочки аксонов в головном мозге больных РС возникают очаги поражения (бляшки). ü РС является одной из наиболее социально значимых проблем медицины, поскольку этим заболеванием страдают в основном молодые люди, ведущие активную трудовую деятельность и социальную жизнь. ü Только в Европе проживает не менее 400 000 больных РС, а ежегодные затраты на одного больного составляют до 24 000 евро, причем большинство расходов – непрямые, растущие по мере утяжеления заболевания.
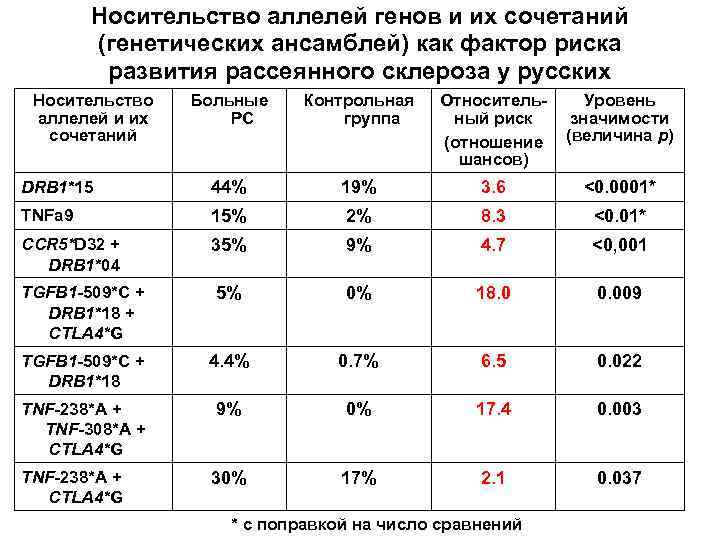
Носительство аллелей генов и их сочетаний (генетических ансамблей) как фактор риска развития рассеянного склероза у русских Носительство аллелей и их сочетаний Больные РС Контрольная группа Относительный риск (отношение шансов) Уровень значимости (величина р) DRB 1*15 44% 19% 3. 6 <0. 0001* TNFa 9 15% 2% 8. 3 <0. 01* CCR 5*D 32 + DRB 1*04 35% 9% 4. 7 <0, 001 TGFB 1 -509*C + DRB 1*18 + CTLA 4*G 5% 0% 18. 0 0. 009 TGFB 1 -509*C + DRB 1*18 4. 4% 0. 7% 6. 5 0. 022 TNF-238*A + TNF-308*A + CTLA 4*G 9% 0% 17. 4 0. 003 TNF-238*A + CTLA 4*G 30% 17% 2. 1 0. 037 * с поправкой на число сравнений
Фармакогенетика и концепция персонализированной медицины Фармакогенетика - наука, изучающая наследственные различия в нуклеотидной последовательности ДНК, которые обуславливают различия в метаболизме лекарств и различия в ответе организма на их действие.

http: //www. dsm. ru/marketnews/675_01. 08. 2008 ТОП-10 брендов в госпитальных закупках по стоимостному объему за 1 -ое полугодие 2008 г. * Рейтинг Бренд Объем, млн. руб. Доля 1 ГИКАМТИН 617 2, 10% 2 НАТРИЯ ХЛОРИД 554 1, 90% 3 ПЕГИНТРОН 490 1, 70% 4 БЕТАФЕРОН 471 1, 60% 5 ПЕГАСИС 457 1, 60% 6 КОПАКСОН-ТЕВА 431 1, 50% 7 МЕРОНЕМ 402 1, 40% 8 ГЛИВЕК 368 1, 30% 9 РЕБИФ 314 1, 10% 10 ГОРДОКС 302 1, 10% * объемы приведены в закупочных ценах ЛПУ Только на госпитальные закупки препаратов, изменяющих течение рассеянного склероза: интерферона-бета (Бетаферон и Ребиф) и копаксона в 1 -ом полугодии 2008 года потрачено 1216 млн руб
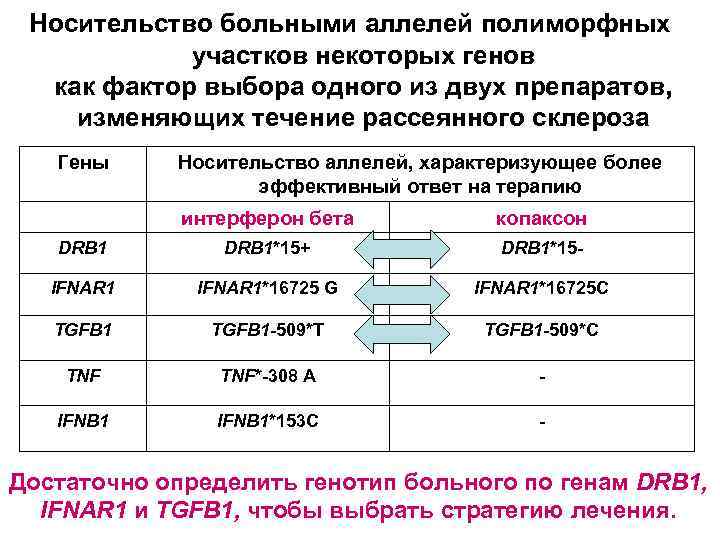
Носительство больными аллелей полиморфных участков некоторых генов как фактор выбора одного из двух препаратов, изменяющих течение рассеянного склероза Гены Носительство аллелей, характеризующее более эффективный ответ на терапию интерферон бета копаксон DRB 1*15+ DRB 1*15 - IFNAR 1*16725 G IFNAR 1*16725 С TGFB 1 -509*Т TGFB 1 -509*С TNF*-308 А - IFNB 1*153 С - Достаточно определить генотип больного по генам DRB 1, IFNAR 1 и TGFB 1, чтобы выбрать стратегию лечения.

Первые итоги проведенных фармакогенетических исследований рассеянного склероза у русских ü Полученные данные указывают на возможность выбрать как более эффективный для больного РС русской этнической принадлежности один из двух препаратов – интерферон бета или копаксон – исходя из носительства аллелей нескольких генов, причем в случае трех генов (DRB 1; IFNAR 1; TGFB 1) выбор однозначен. ü Эти результаты не имеют аналогов в литературе и, в соответствии с принятыми мировым сообществом нормами, нуждаются в проверке на независимой выборке (валидации). ü В случае подтверждения этих результатов, выигрыш для больных очевиден, а здравоохранение может сэкономить порядка $20 000 в год на одного больного, напрасно потраченных на его неэффективное лечение.
Лекция 2 в НОЦ ИБХ 24 ноября ИБХ.ppt