БИОТЕРАПИЯ ОПУХОЛЕЙ.ppt
- Количество слайдов: 68

БИОТЕРАПИЯ ОПУХОЛЕЙ иммунная система и рак

Существует ли в организме противоопухолевый иммунный надзор?

Существует ли в организме противоопухолевый иммунный надзор? меланома кожи (69 случаев), рак почки – 68 случаев, неходжкинские лимфомы – 68 случаев, ретинобластома – 33 случая, рак молочной железы – 22 случая

Существует ли в организме противоопухолевый иммунный надзор? - среди больных различными иммунодефицитами риск развития рака, в частности неходжкинских лимфом, повышен более, чем в 100 раз - у детей с первичными иммунодефицитами редко развиваются опухоли, характерные для детского возраста - саркомы, но чаще возникают НХЛ, лейкозы, различные аденокарциномы и болезнь Ходжкина.

Существует ли в организме противоопухолевый иммунный надзор? - успешное иммунологическое восстановление у больных с врожденным иммунодефицитом путем трансплантации им костного мозга может предотвратить развитие у них НХЛ - у детей с иммунодефицитом лимфома Ходжкина возникает в более молодом возрасте, ремиссии наступают реже, заболевание хараткеризуется более неблагоприятным прогнозом.

Существует ли в организме противоопухолевый иммунный надзор? - в структуре смертности при СПИДе в 1989 году пневмонии явились причиной смерти лишь в 3 % случаев, в то время, как смерть от СК зарегистрирована в 32% случаев, смерть от НХЛ – в 16%. Также в популяции больных СПИДом повышена заболеваемость раком шейки матки у женщин – 28%.

Существует ли в организме противоопухолевый иммунный надзор? - риск развития злокачественных опухолей также выше у пациентов после транплантации органов, получающих иммуносупрессивную терапию. До января 1994 года в Регистр пострансплантационных опухолей (Цинциннатти, США) поступили данные по 7935 видам злокачественных опухолей у 7449 рецепиентов орагнов. У 419 из них было по 2 опухоли разных видов, у 32 – по 3, и у одного – 4. - в этой группе пациентов течение опухолевой болезни отличается крайней агрессивностью

Существует ли в организме противоопухолевый иммунный надзор? Пациент, 21 год, поступил в отделение биотерапии РОНЦ 15 июня 2006 года с клиническим диагнозом: Меланома кожи спины T 4 b. N 0 M 0, состояние после хирургического лечения в сентябре 2005 года. Прогрессирование: метастазы в паховые, подвздошные, забрюшинные лимфоузлы справа, состояние после 2 -х курсов химиотерапии. Прогрессирование: рост метастазов в пахово-подвздошной, забрюшинной областях. Сопутствующие заболевания: Б-нь Вильсона. Коновалова, состояние после трансплантации печени в январе 2005 года, в процессе иммуносупрессивной терапии.

Существует ли в организме противоопухолевый иммунный надзор? В январе 2005 года в исходе болезни Вильсона-Коновалова трансплантация печени от живого родственного донора в РНЦХ РАМН. После операции по июнь 2006 – иммуносупрессивная терапия. В сентябре 2005 года в РНЦХ РАМН произведено иссечение пигментного образования кожи поясничной области, гитологически верифицирована меланома IIB стадии. В 2006 году – прогрессирование заболевания. 13 июня 2006 года, перед поступлением: - по органам грудной клетки – без патологии, - метастатически измененные лимфоузлы в правой паховой области, забрюшинном пространстве – до 3 см.

Существует ли в организме противоопухолевый иммунный надзор? 15. 06 – 21. 06 клинически состояние больного без отрицательной динамики, идет подготовка к проведению курса полихимиотерапии. 21. 06 пациент предъявляет жалобы на кашель, повышение температуры тела. Аускультативно – в нижних отделах легких ослабление дыхания, рентгенологически – появились множественные метастазы в нижних отделах легких. 23. 06 – отрицательная динамика в состоянии больного, рентгенологически – увеличения количества метастазов в легких.

Существует ли в организме противоопухолевый иммунный надзор? 26. 06 – присоединение грибковой пневмонии, начата антибактериальная, противогрибковая терапия. 29. 06 – присоединение почечной недостаточности, интенсивная терапия. 30. 06 – 06. 07. 06 развитие дыхательной недостаточности. 06. 07. 06 – смерть больного на фоне полиорганной недостаточности.

Как иммунная система распознает раковые клетки?
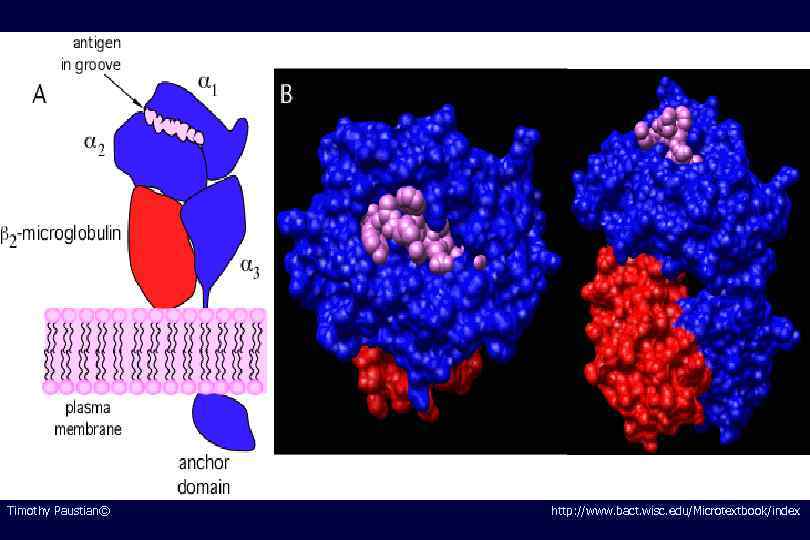
Timothy Paustian© http: //www. bact. wisc. edu/Microtextbook/index
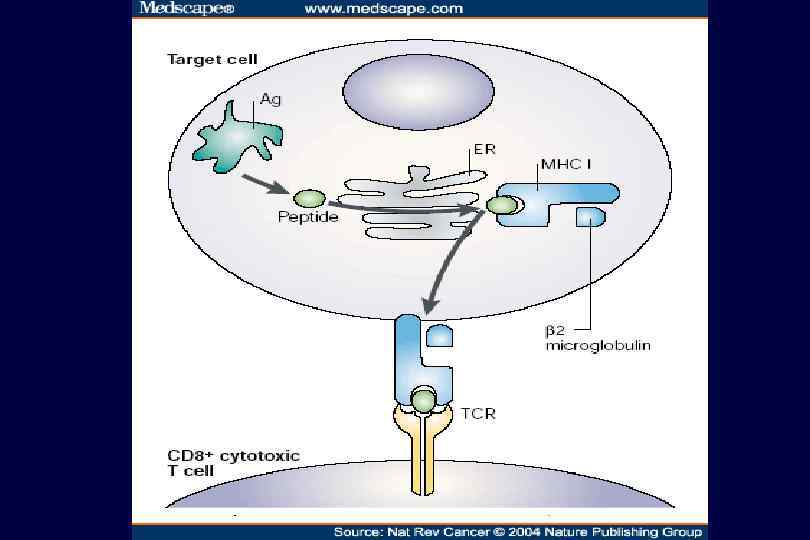

Распознавание опухолевых клеток иммунной системой Поверхностные молекулярные комплексы «антигены» отличают опухолевую клетку от нормальной и могут/должны распознаваться ДК, иммуноцитами. Т -клетками и/или антителами n опухолевые клетки имеют «неантигенные» отличия, которые могут распознаваться другими эффекторами «естественной» иммунной системы (NK-клетки). n

Опухолеассоциированные антигены Раково-тестикулярные антигены встречаются практически на всех опухолевых клетках, различных по своему гистогенезу. На нормальных клетках их не бывает, за исключением герминогенных клеток яичек. Раково-тестикулярные антигены можно считать классом общеспецифичных опухолеассоциированных антигенов, что делает их универсальными для производства вакцин.

Опухолеассоциированные антигены Меланоцитарные дифференцировочные антигены являются антигенами меланомы и представляют собой класс антигенов, которые встречаются в процессе дифференцировки пигментной клетки меланоцита, а также при перерождении меланоцита в опухолевую клетку.

Опухолеассоциированные антигены Мутационные антигены – мутантные белки на поверхности клетки, например при РМЖ часто экспрессируются p 53 и ras. Гиперэкспрессионные антигены – нормальные антигены, экспрессируемые в ненормальных количествах на поверхности клетки. Например рецепторы к факторам роста. Примером такого рецептора служит Her-2/neu на поверхности клеток РМЖ. Вирусные антигены – белки, экспрессирующиеся вследствие внедрения в геном клетки вируса, таких как вирусов Эпштейна-Барр, гепатитов В и С.

Эффекторы противоопухолевого ответа

Цитотоксические Т-лимфоциты (CTL)

Цитотоксические Т лимфоциты Классическая цитотоксическая клетка иммунной системы, имеющая «память» n антиген-специфический рецептор обуславливает эту «память» n Т-клеточные рецепторы распознают чужеродные антигены в комплексе с MHC-I класса n
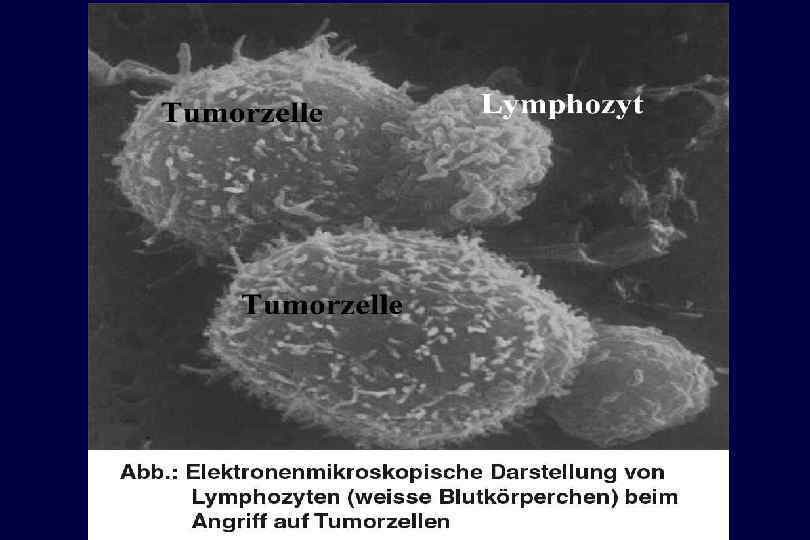
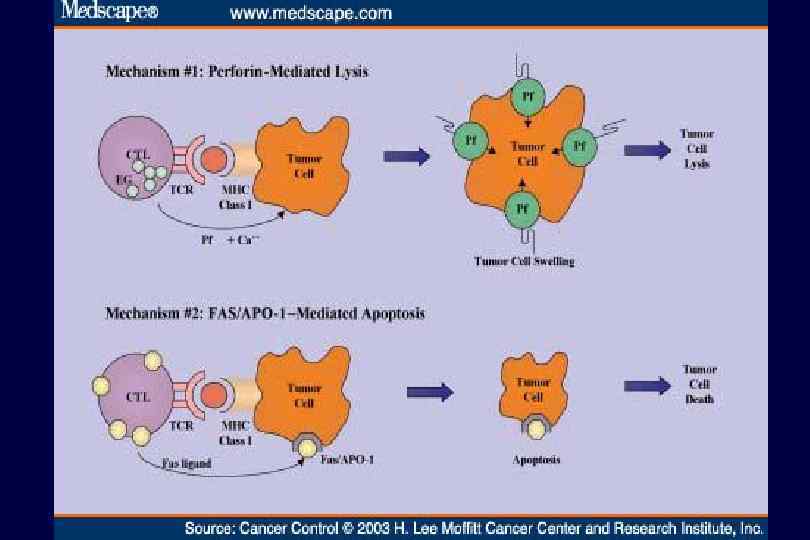
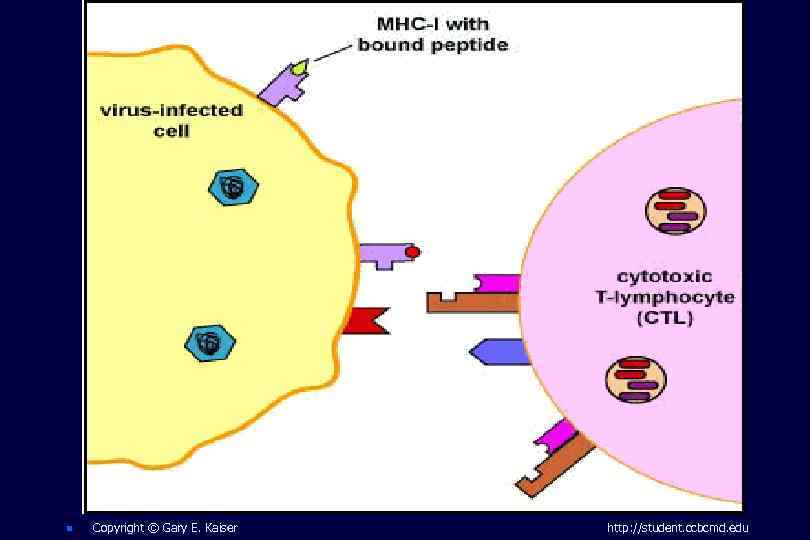
n Copyright © Gary E. Kaiser http: //student. ccbcmd. edu

Антигенпрезентирующие клетки

Мононуклеарные фагоциты n n n Играют важную роль в иммунном ответе Клетки этой системы представлены циркулирующими моноцитами, макрофагами и дендритными клетками в л/узлах, селезенке, легких, коже циркулирующие моноциты первыми реагируют на воспаление и, возможно, на опухоль антиген-презентирующая функция процесс активации стимулируется IFN-гамма, IL 1, эндотоксинами и любыми мишенями, образующими комплекс антиген-антитело
© Steve Haley - William Bowers - Richard Hunt http: //pathmicro. med. sc. edu/
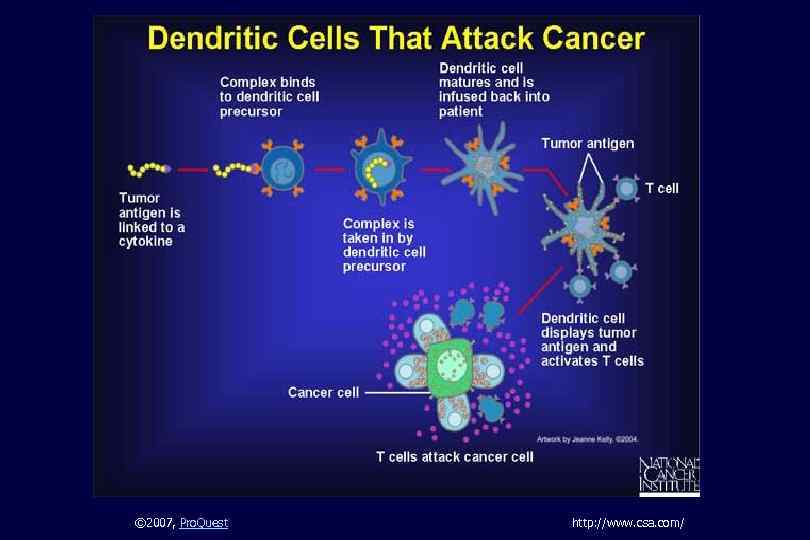
© 2007, Pro. Quest http: //www. csa. com/
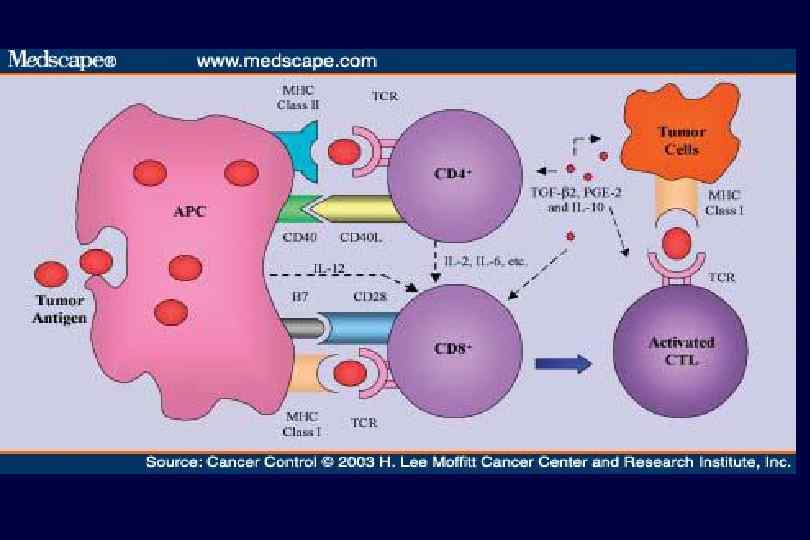

Естественные киллеры (NK)

Естественные киллеры (NK-клетки) n n n Составляют до 5% от лейкоцитов периферической крови являются крупными гранулярными лимфоцитами способны уничтожать некоторые виды опухолевых клеток in vitro процесс уничтожения не связан с MHC и не имеет памяти IL-2, IFN усиливают NK-активность Prostaglandin E 2 ослабляет NK-активность
A color enhanced scanning electron microscope image of a Natural Killer Cell (NK-cell). (SEM 11, 000 x) Credit: Eye of Science / Photo Researchers , Inc. http: //db 2. photoresearchers. com/
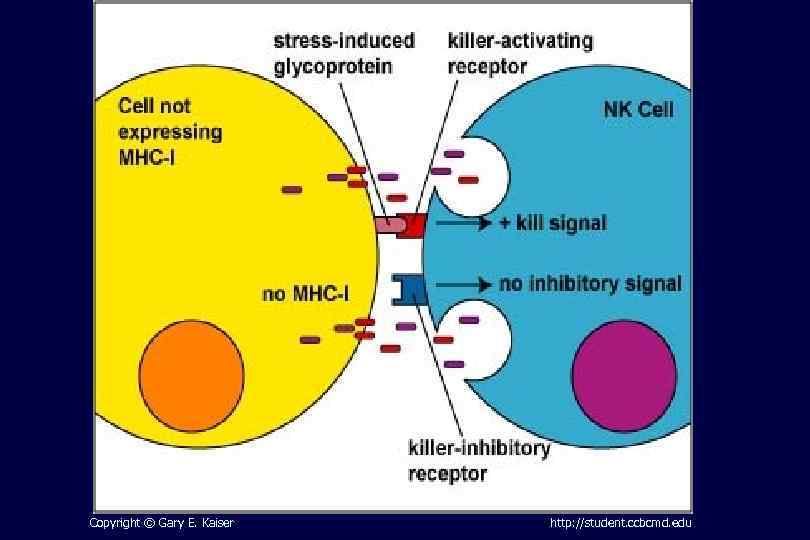
Copyright © Gary E. Kaiser http: //student. ccbcmd. edu

Биотерапия опухолей Биологическая терапия – метод лечения злокачественных опухолей, основанный на использовании модификаторов биологического ответа, непосредственно или косвенно влияющих на уменьшение объема опухолевой массы. Под термином "иммунотерапия" подразумевается раздел биотерапии, ограниченный применением методов, воздействующих на эффекторы иммунной системы.

Общие свойства методов БТ: - подавляют ростовые факторы, обуславливающие опухолевую прогрессию, - повышают распознаваемость опухолевых клеток клетками иммунной системы, - повышают цитотоксичность клеток иммунной системы, таких как Т-клетки, NK-клетки, макрофаги, - блокируют процессы трансформации клеток в злокачественные,

Общие свойства методов БТ: - регулируют апоптоз, - блокируют неоангиогенез - блокируют некоторые регуляторные системы иммунной системы, ответственные за иммуносупрессию, - снижают риск метастазирования, - повышают восстановление числа иммунокомпетентных клеток после воздействия химио- или лучевой терапии.

На современном этапе направлениями биотерапии являются: - вакцинотерапия - терапия МКА - адоптивная терапия - использвание рекомбинантных цитокинов - антисенс-терапия - антиангиогенная терапия - вирусная терапия (гетерогенизация опухолей и канцеротропные вирусы)

Направления и методы современной иммунотерапии рака

Применение цитокинов

Цитокины - пептиды иммунной системы Медиаторы естественного иммунитета (IL -1, TNF, IL-6) n регуляторы дифференцировки и активации лимфоцитов (IL-2, IL-4, IL-12) n активаторы эффекторов иммунитета (IL -5, IF-γ) n стимуляторы гемопоэза (G-CSF, GM-CSF, IL-3, IL-7) n

Интерфероны - секреторные гликопротеины n ИФ-1: ИФ-α (лейкоцитарный) , ИФ-β (фибробластный) - подавляют репликацию вирусов, клеточную пролиферацию, стимулируют NK, модулируют экспрессию MHC-1 класса n ИФ-2: ИФ-γ (лимфоцитарный/иммунный) повышает экспрессию MHC-I и MHC-II классов, активирует мононуклеары, нейтрофилы и NK-клетки, влияет на дифференцировку Т и В лимфоцитов, активирует эндотелиальные клетки -

Клиническое использование рекомбинантного интерферона-α n В онкогематологии: волосатоклеточный лейкоз, хронический миелолейкоз, лимфомы низкой степени злокачественности, острый лимфобластный лейкоз у детей n В лечении солидных опухолей: профилактика метастазов меланомы кожи и рака почки у больных с плохим прогнозом; лечение метастазов злокачественного карциноида в печень; в сочетании со стандартными режимами х/терапии для лечения метастазов многих солидных опухолей

Интерлейкин-2 (Proleukin) Фактор роста Т-клеток, физиологический митоген для предшественников ЦТТ n стимулирует NK с образованием LAK n фактор роста В лимфоцитов, стимулятор синтеза антител n стимулирует синтез других, продуцируемых Т-клетками цитокинов n

IL-2: клиническое применение Является компонентом биотерапии метастатической меланомы и рака почки n позволяет добиться стойкого излечения у 5% больных n используется для получения LAK и последующей сочетанной иммунотерапии LAK + IL-2 n

антисенсы

Антисенс-терапия Выключение функции гена путем ингибирования кодируемого белка n синтезируется последовательность нуклеотидов, комплементарно связываемая с участком информационной РНК. n синтезированы антисенс-олигонуклеотиды блокирующие белки онкогенов c-myc, Bcl -2 (G 3139), erb. B 2, c-raf (ISIS 5132) n

Семейство генов BCL-2 Белки индукторы/ингибиторы апоптоза n индукторы - Bax, Bcl-XS, Bad; ингибиторы Bcl-2, Bcl-XL, Mcl-1 n соотношение про/анти определяет возможность апоптоза n экспрессия Bсl-2 предопределяет возможность лекарственной устойчивости на проводимое лечение n Генасенс - препарат антисенс к Bcl-2 n

Противоопухолевые вакцины

разнообразие принципов создания противоопухолевых вакцин и их разновидности n n n Пептидные (на основе общеспецифичных АГ опухоли) модифицированные (трансфецированные генами IL-2, GM-CSF) поливалентные ( пептидные АГ + другие) с адъювантным компонентом (АГ + адъювант) векторные дендритные

Вакцины, на основе модицицированных опухолевых клеток n В данной системе пациент вакцинируется аллогенными или аутологичными опухолевыми клетками, в которые внедрен новый ген. n генномодифицированные опухолевые клетки, синтезирующие цитокины n генномодифицированные опухолевые клетки, представляющие на своей поверхности новые, распознаваемые иммунной системой антигены.

Дендритные вакцины n n n забор опухолевой ткани у больного и приготовление лизата праймирование (загрузка лизатом) дендритных клеток, взятых у того же больного, инкубация дендритных клеток с лизатом, вакцинация больного (в/к) После вакцинации праймированные дендритные клетки попадают в регионарные лимфоузлы, где и происходит презентация антигенов Т-лимфоцитам, которые после этого способны узнавать опухолевые клетки и развивать иммунный ответ.
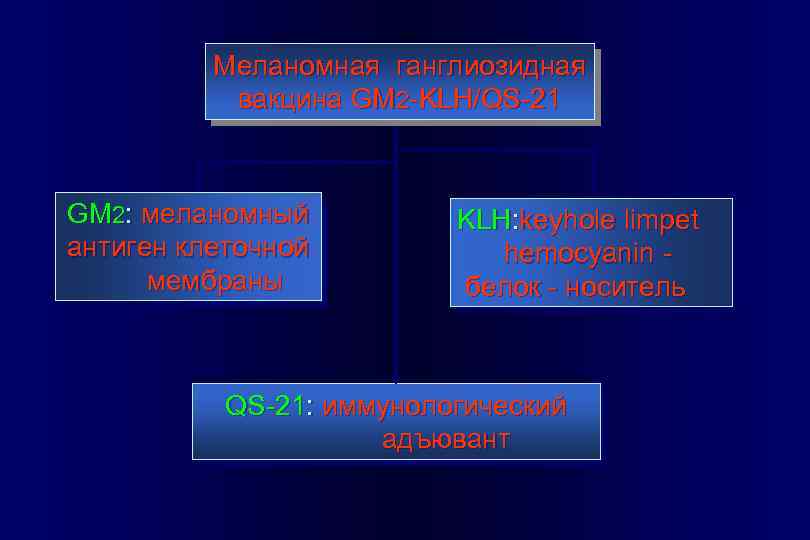
Меланомная ганглиозидная вакцина GM 2 -KLH/QS-21 GM 2: меланомный антиген клеточной мембраны KLH: keyhole limpet hemocyanin белок - носитель QS-21: иммунологический адъювант

Ганглиозид GM 2 определяется в клеточной культуре МК с высокой концентрацией в 95% случаев n Естественные анти-GM 2 антитела в организме больных вырабатываются в недостаточном количестве n Антитела на GM 2 у больных с МК благоприятный фактор прогноза n

Выбор KLH в качестве носителя Введение GM 2 в чистом виде не приводит к измеряемому иммунному ответу n Соединение GM 2 антигена с белкомгемоцианином KLH позволяет получить постоянную гуморальную реакцию с образованием антиганглиозидных антител классов Ig. M и Ig. G n

Выбор QS-21 в качестве адъюванта Очищенный сапонин QS-21 (Quillaja saponaria) усиливает иммуногенность антигенов n Использование QS-21 c конъюгатом GM 2 -KLH позволило получить наиболее постоянный, продолжительный иммунный ответ с образованием антител классов Ig. M и Ig. G n
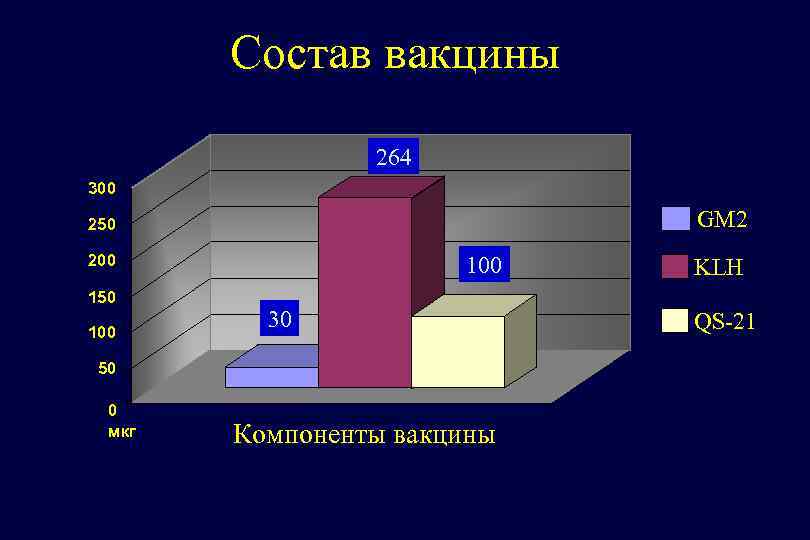
Состав вакцины 264 300 GM 2 250 200 150 100 30 50 0 мкг Компоненты вакцины KLH QS-21

Режим введения вакцины Вводится подкожно n дни первого месяца лечения: 1, 8, 15, 22 n последующие недели: 12, 24, 36, 48, 60, 72, 84, 96 n общая продолжительность лечения - 2 года n

Клеточная терапия рака

Принципы клеточной терапии Генерация LAK-клеток n Получение TIL n Выделение дендритных клеток n Использование стволовых клеток n Трансплантация костного мозга (минитрансплантация) n

Вирусная терапия

n Метод основан на использовании цитотоксичных штаммов вирусов, модифицированных по генам, ответственным за репликацию вируса на нормальных тканях. Основная перспектива этого метода терапии – тропность вирусов к определенным органам и тканям.

n Дикие штаммы аденовирусов, внедряясь в клетку, синтезируют белок, кодируемый геном Е 1 В, блокирующий активность р53. Следствием этого является невозможность ухода в апоптоз инфицированной клетки и свободная репликация вируса в ней, с последующим ее лизисом и инфицированием новых клеток. n В вирусных препаратах, созданных на основе диких штаммов, удален ген Е 1 В. Таким образом, вирус не может селиться на нормальных клетках. Препараты: ONIX-015, Канцеролизин.

моноклональные антитела

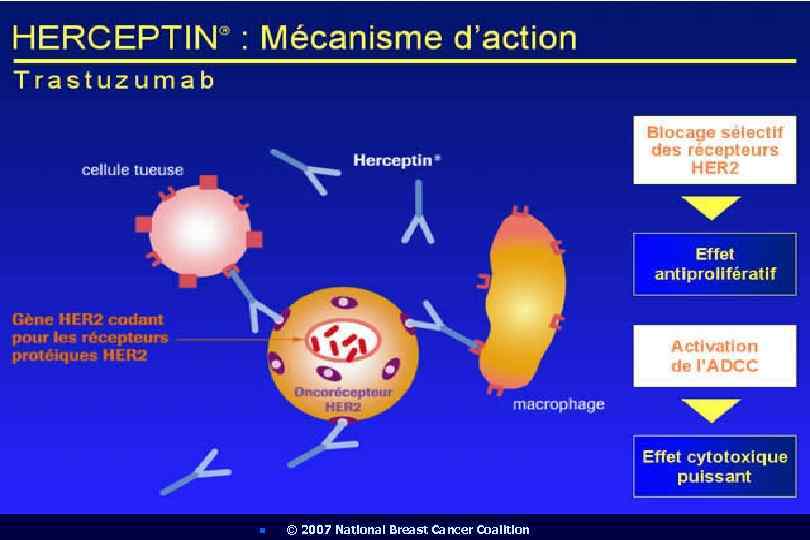
Иммунотерапия антителами n n Anti-HER 2/neu (Herceptin) при раке молочной железы, клетки которого экспрессируют рецептор HER-2 Anti-CD 20 (Rituxan - Mabthera) при рецидивной, устойчивой к х/терапии В-клеточной лимфоме низкой степени злокачественности Anti-CO 17 -1 A Mo. Ab при раке толстой кишки Anti-CTLA-4 при меланоме.

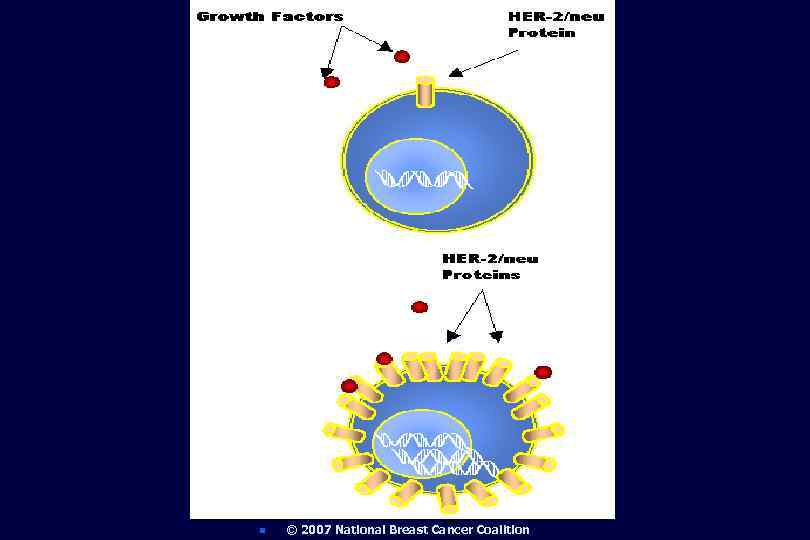
Роль HER 2 при раке молочной железы n n HER 2 - прото-онкоген, вовлеченный в регуляцию клеточного роста амплификация или гиперэкспрессия гена HER 2 активируют рецепторы HER 2 на клетках и стимулируют их рост амплификация гена HER 2 или его гиперэкспрессия выявляются у 25 -30% больных раком молочной железы HER 2 -положительные опухоли имеют неблагоприятное течение и короткий безрецидивный период

HER 2 гиперэкспрессия при РМЖ n n n HER 2 гиперэкспрессирован или амплифицирован в 25 -30% РМЖ, а также при других опухолях человека Больные РМЖ с гиперэкспрессией или амплификацией HER 2 имеют плохой прогноз и низкую выживаемость Иммуногистохимические методы позволяют измерить гиперэкспрессию HER 2 протеина в ткани РМЖ
n © 2007 National Breast Cancer Coalition
n © 2007 National Breast Cancer Coalition
БИОТЕРАПИЯ ОПУХОЛЕЙ.ppt