Metabolism.ppt
- Количество слайдов: 74

БИОСИНТЕЗ И МЕТАБОЛИЗМ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
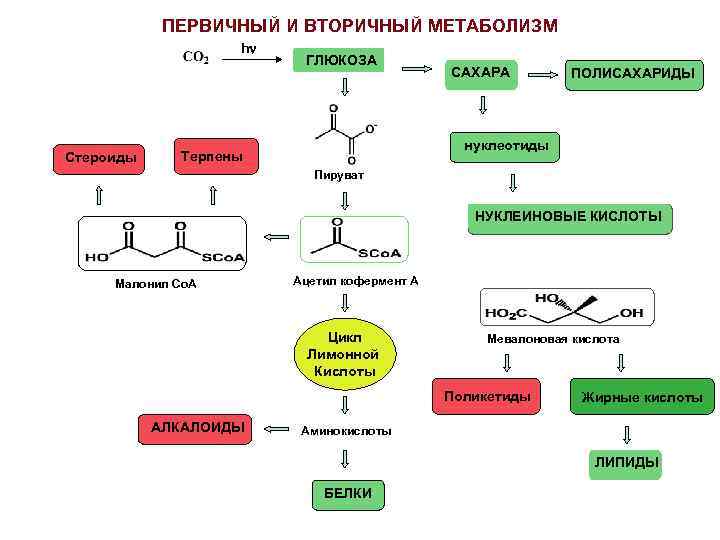
ПЕРВИЧНЫЙ И ВТОРИЧНЫЙ МЕТАБОЛИЗМ h Стероиды ГЛЮКОЗА САХАРА ПОЛИСАХАРИДЫ нуклеотиды Терпены Пируват НУКЛЕИНОВЫЕ КИСЛОТЫ Малонил Со. А Ацетил кофермент А Цикл Лимонной Кислоты Мевалоновая кислота Поликетиды АЛКАЛОИДЫ Жирные кислоты Аминокислоты ЛИПИДЫ БЕЛКИ
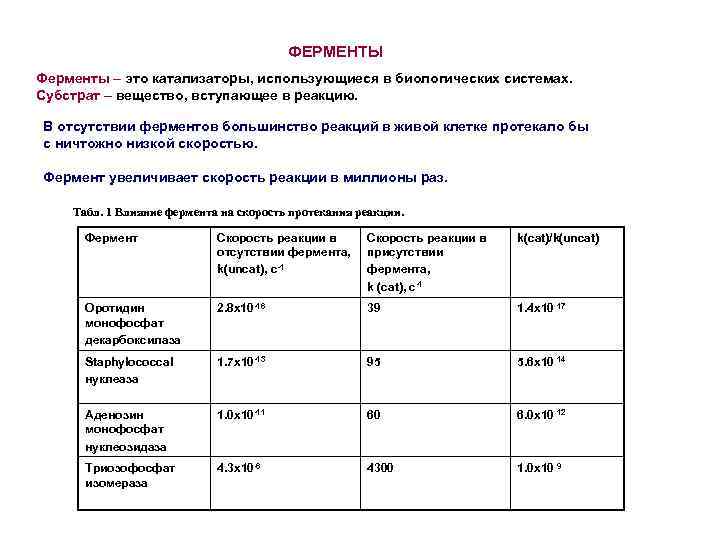
ФЕРМЕНТЫ Ферменты – это катализаторы, использующиеся в биологических системах. Субстрат – вещество, вступающее в реакцию. В отсутствии ферментов большинство реакций в живой клетке протекало бы с ничтожно низкой скоростью. Фермент увеличивает скорость реакции в миллионы раз. Табл. 1 Влияние фермента на скорость протекания реакции. Фермент Скорость реакции в отсутствии фермента, k(uncat), с-1 Скорость реакции в присутствии фермента, k (cat), с-1 k(cat)/k(uncat) Оротидин монофосфат декарбоксилаза 2. 8 х10 -16 39 1. 4 х10 17 Staphylococcal нуклеаза 1. 7 х10 -13 95 5. 6 х10 14 Аденозин монофосфат нуклеозидаза 1. 0 х10 -11 60 6. 0 х10 12 Триозофосфат изомераза 4. 3 х10 -6 4300 1. 0 х10 9
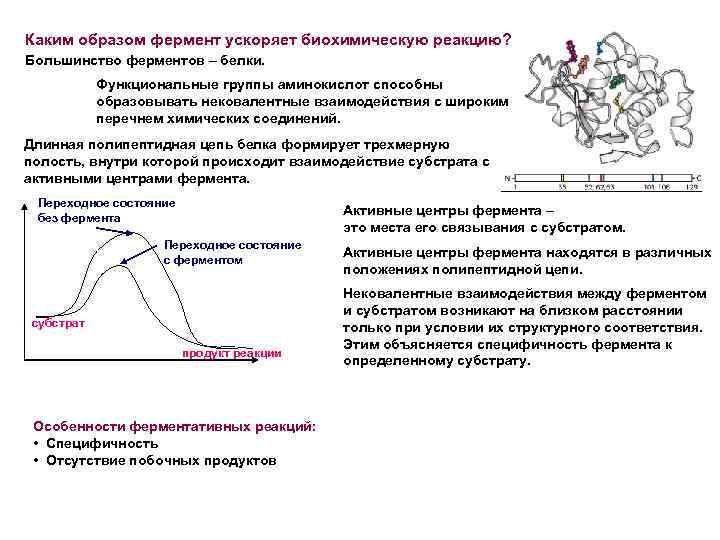
Каким образом фермент ускоряет биохимическую реакцию? Большинство ферментов – белки. Функциональные группы аминокислот способны образовывать нековалентные взаимодействия с широким перечнем химических соединений. Длинная полипептидная цепь белка формирует трехмерную полость, внутри которой происходит взаимодействие субстрата с активными центрами фермента. Переходное состояние без фермента Активные центры фермента – это места его связывания с субстратом. Переходное состояние с ферментом субстрат продукт реакции Особенности ферментативных реакций: • Специфичность • Отсутствие побочных продуктов Активные центры фермента находятся в различных положениях полипептидной цепи. Нековалентные взаимодействия между ферментом и субстратом возникают на близком расстоянии только при условии их структурного соответствия. Этим объясняется специфичность фермента к определенному субстрату.

Номенклатура и классификация ферментов Исторически фермент получал название в зависимости от типа катализируемой им реакции, наименования субстрата или объекта, из которого он был выделен. В 1964 году Международный союз по биохимии создал комиссию с целью создания единой систематической номенклатуры ферментов. Основные классы ферментов: № Класс Тип катализируемой реакции 1. Оксидоредуктазы Окислительновосстановительная 2. Трансферазы Транспорт групп 3. Гидролазы Реакции гидролиза 4. Лиазы Присоединение или отщепление групп с образованием двойной связи 5. Изомеразы Изомеризация
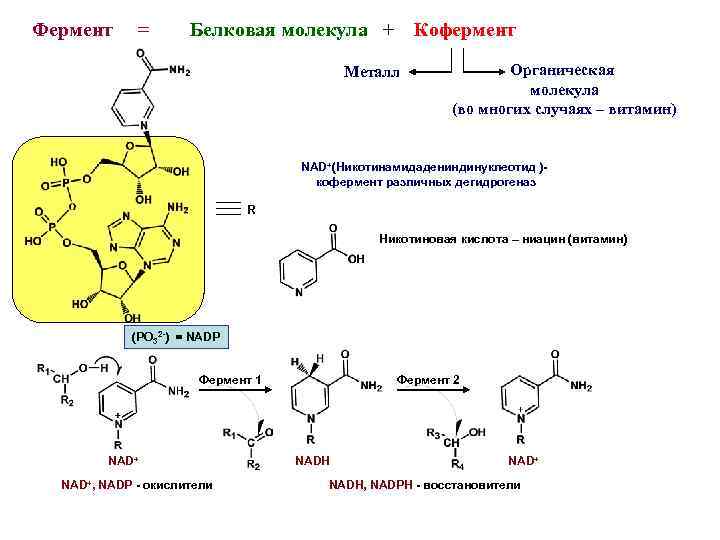
Фермент = Белковая молекула + Кофермент Металл Органическая молекула (во многих случаях – витамин) NAD+(Никотинамидадениндинуклеотид )- кофермент различных дегидрогеназ R Никотиновая кислота – ниацин (витамин) (PO 32 -) = NADP Фермент 1 NAD+, NADP - окислители Фермент 2 NADH NAD+ NADH, NADPH - восстановители
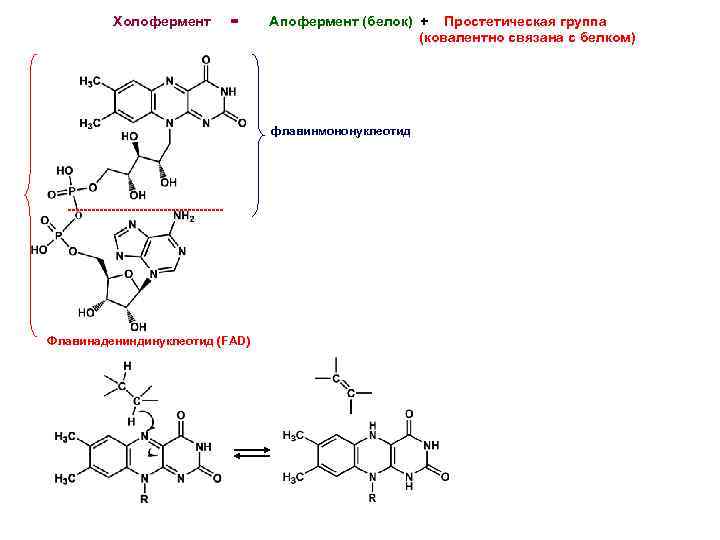
Холофермент = Апофермент (белок) + Простетическая группа (ковалентно связана с белком) флавинмононуклеотид -------------------- Флавинадениндинуклеотид (FAD)
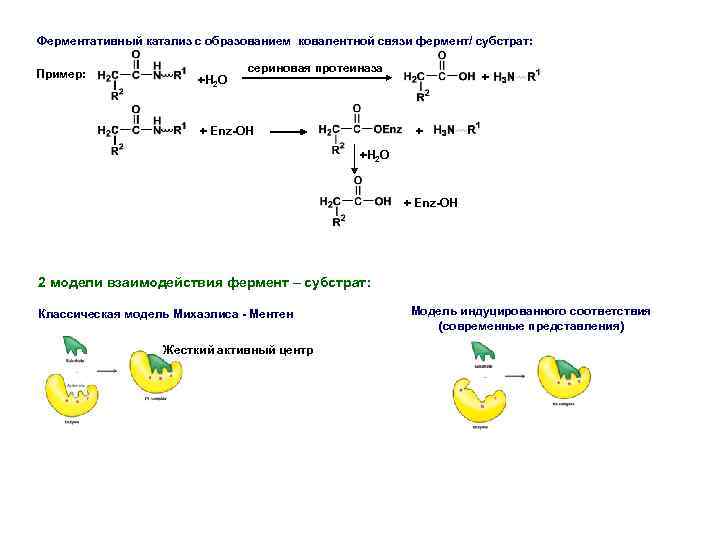
Ферментативный катализ с образованием ковалентной связи фермент/ субстрат: Пример: +H 2 O сериновая протеиназа + Enz-OH + + +H 2 O + Enz-OH 2 модели взаимодействия фермент – субстрат: Классическая модель Михаэлиса - Ментен Жесткий активный центр Модель индуцированного соответствия (современные представления)
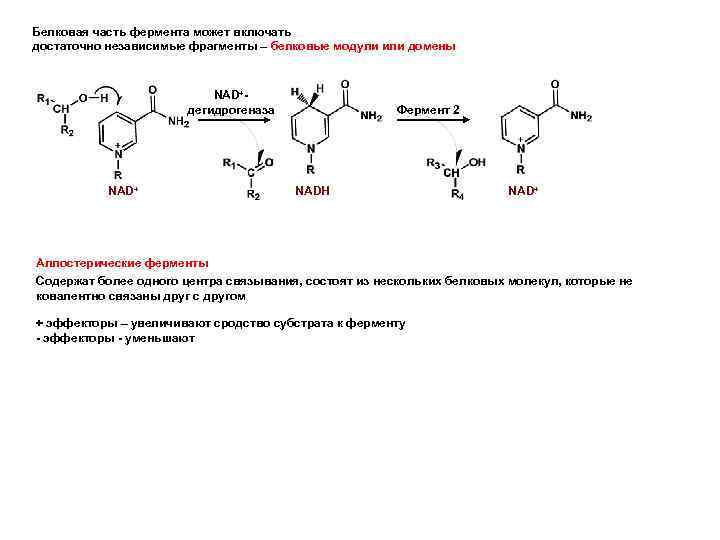
Белковая часть фермента может включать достаточно независимые фрагменты – белковые модули или домены NAD+дегидрогеназа NAD+ Фермент 2 NADH NAD+ Аллостерические ферменты Содержат более одного центра связывания, состоят из нескольких белковых молекул, которые не ковалентно связаны друг с другом + эффекторы – увеличивают сродство субстрата к ферменту - эффекторы - уменьшают
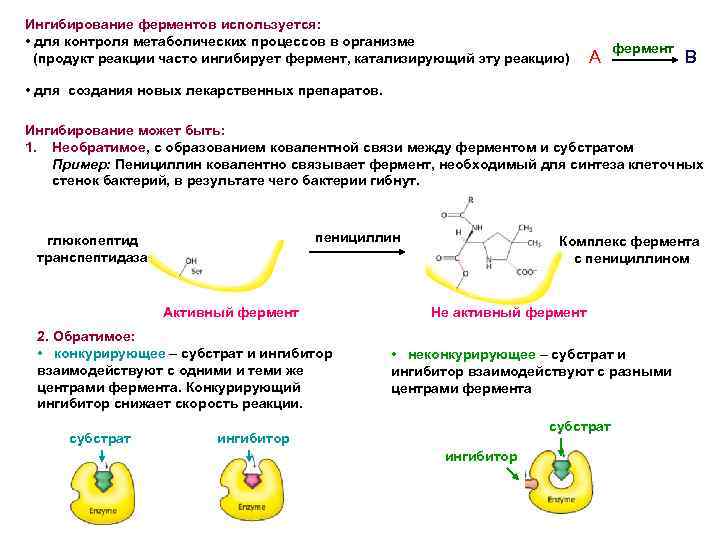
Ингибирование ферментов используется: • для контроля метаболических процессов в организме (продукт реакции часто ингибирует фермент, катализирующий эту реакцию) А фермент В • для создания новых лекарственных препаратов. Ингибирование может быть: 1. Необратимое, с образованием ковалентной связи между ферментом и субстратом Пример: Пенициллин ковалентно связывает фермент, необходимый для синтеза клеточных стенок бактерий, в результате чего бактерии гибнут. пенициллин глюкопептид транспептидаза Активный фермент 2. Обратимое: • конкурирующее – субстрат и ингибитор взаимодействуют с одними и теми же центрами фермента. Конкурирующий ингибитор снижает скорость реакции. субстрат Комплекс фермента с пенициллином Не активный фермент • неконкурирующее – субстрат и ингибитор взаимодействуют с разными центрами фермента субстрат ингибитор

2 основных способа регулирования метаболических процессов: -Изменение количества фермента -Изменение активности фермента 1. аллостерическая регуляция 2. ковалентная модификация белка (обычно фосфорилирование / дефосфорилирование) Фосфорилированию подвергаются –ОН группы аминокислот – серина и треонина АТФ протеинкиназа H 2 O фосфатаза
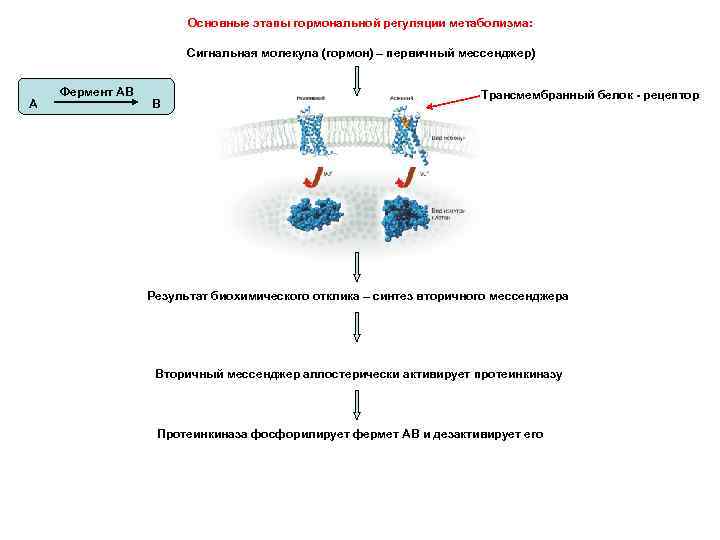
Основные этапы гормональной регуляции метаболизма: Сигнальная молекула (гормон) – первичный мессенджер) А Фермент АВ В Трансмембранный белок - рецептор Результат биохимического отклика – синтез вторичного мессенджера Вторичный мессенджер аллостерически активирует протеинкиназу Протеинкиназа фосфорилирует фермет АВ и дезактивирует его
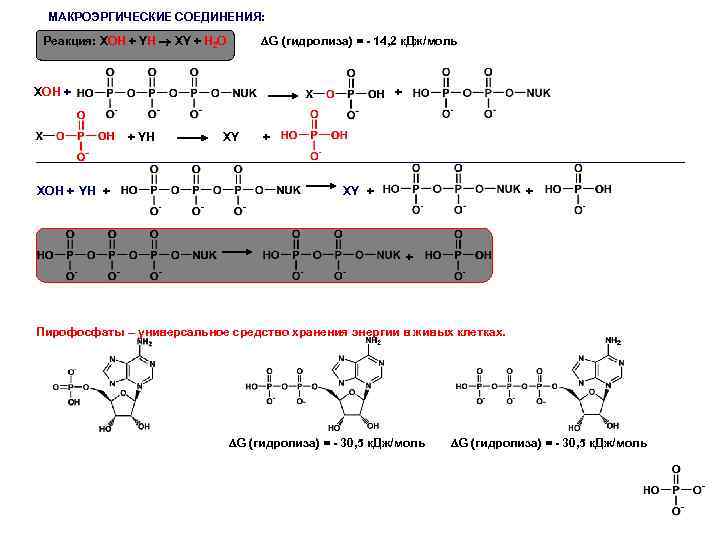
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ: G (гидролиза) = - 14, 2 к. Дж/моль Реакция: ХОН + YH XY + H 2 O ХОН + + + YH ХОН + YH + XY + + + Пирофосфаты – универсальное средство хранения энергии в живых клетках. G (гидролиза) = - 30, 5 к. Дж/моль
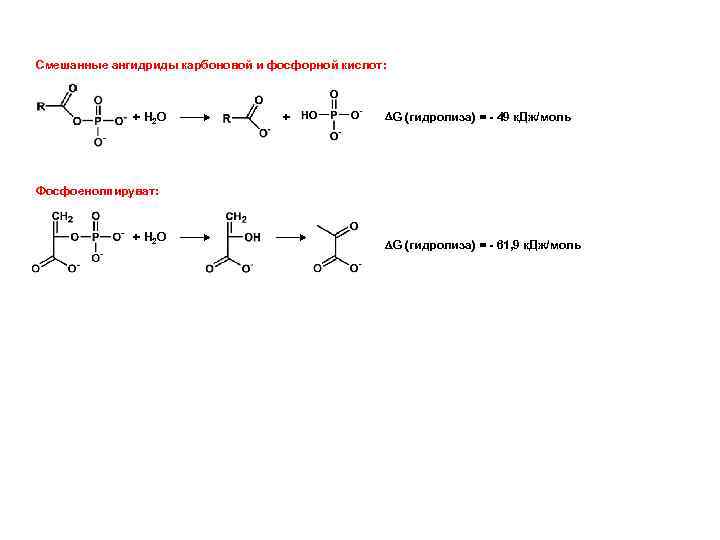
Смешанные ангидриды карбоновой и фосфорной кислот: + H 2 O + G (гидролиза) = - 49 к. Дж/моль Фосфоенолпируват: + H 2 O G (гидролиза) = - 61, 9 к. Дж/моль
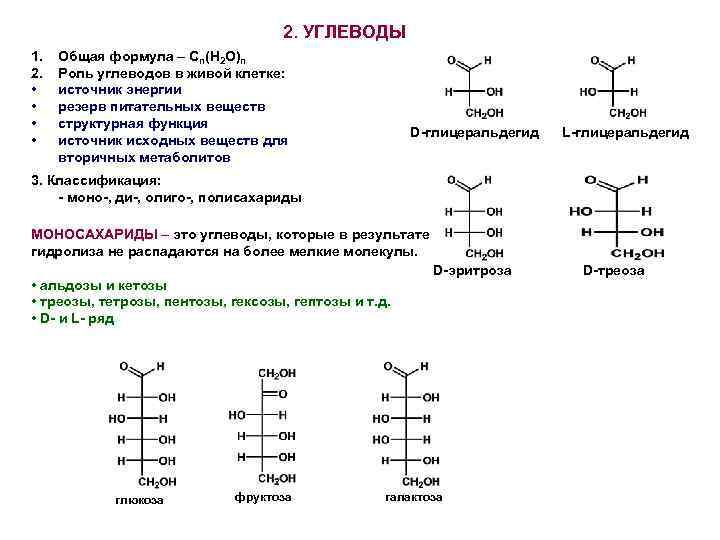
2. УГЛЕВОДЫ 1. 2. • • Общая формула – Сn(H 2 O)n Роль углеводов в живой клетке: источник энергии резерв питательных веществ структурная функция источник исходных веществ для вторичных метаболитов D-глицеральдегид L-глицеральдегид 3. Классификация: - моно-, ди-, олиго-, полисахариды МОНОСАХАРИДЫ – это углеводы, которые в результате гидролиза не распадаются на более мелкие молекулы. D-эритроза • альдозы и кетозы • треозы, тетрозы, пентозы, гексозы, гептозы и т. д. • D- и L- ряд глюкоза фруктоза галактоза D-треоза
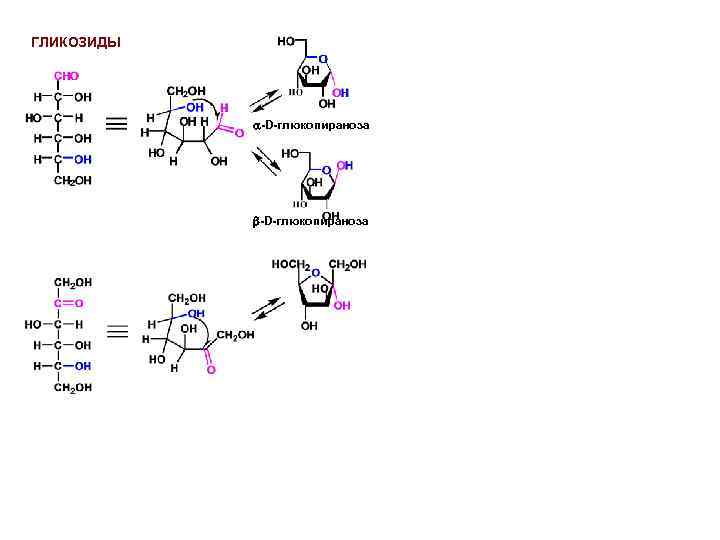
ГЛИКОЗИДЫ -D-глюкопираноза

ДИСАХАРИДЫ ПОЛИСАХАРИДЫ КРАХМАЛ – гомополимер, синтезируемый в растениях. Содержит молекулы глюкозы, соединенные 1 -4 гликозидной связью: Мальтоза -D-глюкопиранозил-(1 4)- -D-глюкопираноза АМИЛАЗА – линейный гомополимер, содержащий около 100 молекул глюкозы. ГЛИКОГЕН - гомополимер глюкозы, синтезируемый у животных. Содержащий около 1 000 молекул глюкозы, соединенных 1 -4 и 1 -6 гликозидными связями. белок гликогенин АМИЛОПЕКТИН – разветвленный гомополимер, содержащий около 100 000 молекул глюкозы, соединенных 1 -4 и 1 -6 гликозидными связями. невосстанавливающий конец
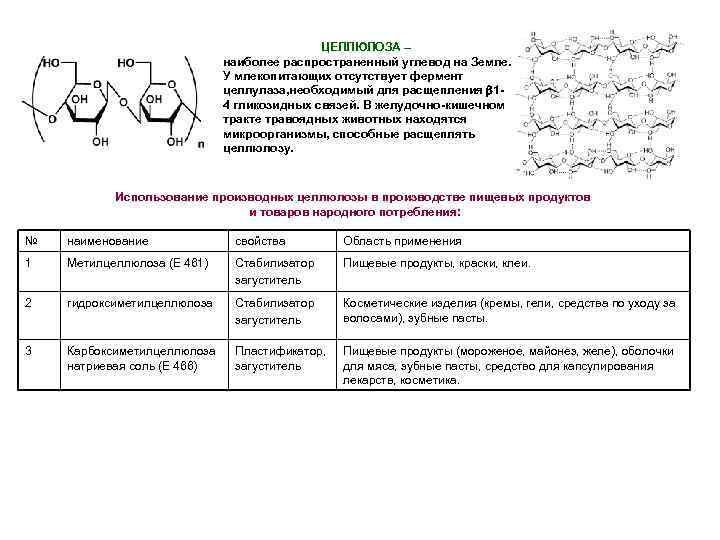
ЦЕЛЛЮЛОЗА – наиболее распространенный углевод на Земле. У млекопитающих отсутствует фермент целлулаза, необходимый для расщепления 14 гликозидных связей. В желудочно-кишечном тракте травоядных животных находятся микроорганизмы, способные расщеплять целлюлозу. Использование производных целлюлозы в производстве пищевых продуктов и товаров народного потребления: № наименование свойства Область применения 1 Метилцеллюлоза (Е 461) Стабилизатор загуститель Пищевые продукты, краски, клеи. 2 гидроксиметилцеллюлоза Стабилизатор загуститель Косметические изделия (кремы, гели, средства по уходу за волосами), зубные пасты. 3 Карбоксиметилцеллюлоза натриевая соль (Е 466) Пластификатор, загуститель Пищевые продукты (мороженое, майонез, желе), оболочки для мяса, зубные пасты, средство для капсулирования лекарств, косметика.
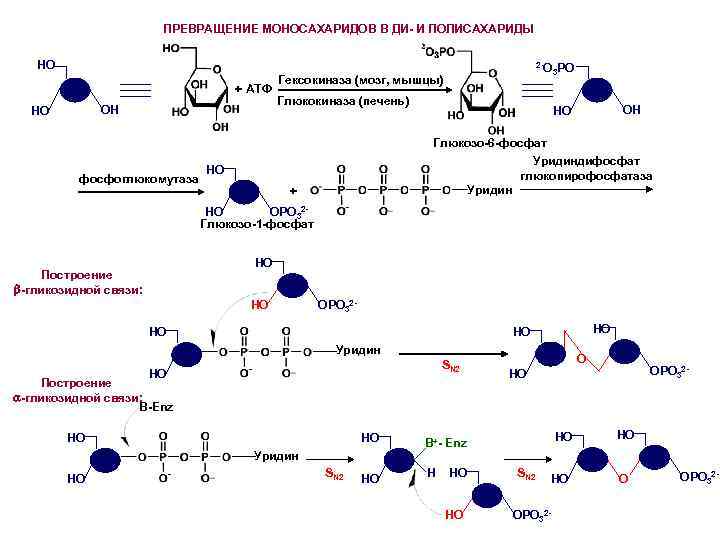
ПРЕВРАЩЕНИЕ МОНОСАХАРИДОВ В ДИ- И ПОЛИСАХАРИДЫ НО + АТФ ОН НО фосфоглюкомутаза 2 -O Гексокиназа (мозг, мышцы) Глюкокиназа (печень) 3 PO ОН НО Глюкозо-6 -фосфат Уридиндифосфат глюкопирофосфатаза Уридин HO + НО ОPO 32 Глюкозо-1 -фосфат HO Построение -гликозидной связи: НО ОPO 32 HO HO HO Уридин SN 2 НО Построение -гликозидной связи: В-Enz HO HO SN 2 НО H HO НО ОPO 32 - НО HO B+- Enz Уридин НО О SN 2 НО ОPO 32 - HO О ОPO 32 -
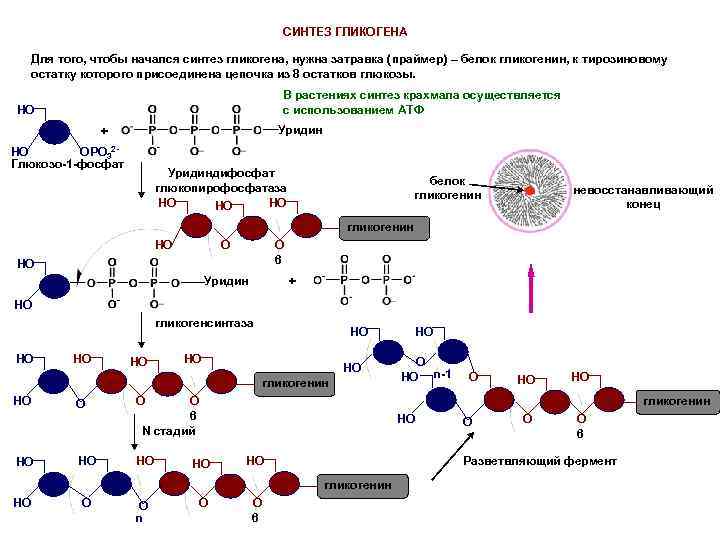
СИНТЕЗ ГЛИКОГЕНА Для того, чтобы начался синтез гликогена, нужна затравка (праймер) – белок гликогенин, к тирозиновому остатку которого присоединена цепочка из 8 остатков глюкозы. В растениях синтез крахмала осуществляется с использованием АТФ HO Уридин + ОPO 32 НО Глюкозо-1 -фосфат Уридиндифосфат глюкопирофосфатаза HO HO HO белок гликогенин невосстанавливающий конец гликогенин НО О O 6 HO + Уридин НО гликогенсинтаза HO HO HO НО гликогенин НО HO О О HO n-1 O HO HO гликогенин О O 6 N стадий HO HO НО HO О n О O 6 О О O 6 Разветвляющий фермент гликогенин НО HO
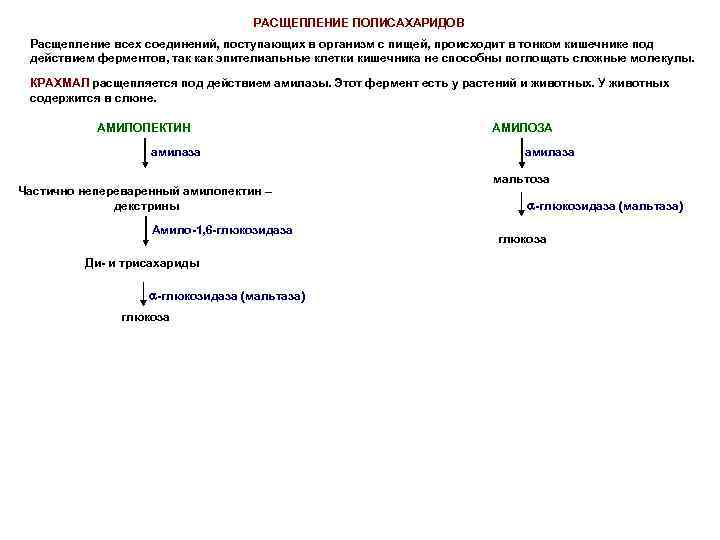
РАСЩЕПЛЕНИЕ ПОЛИСАХАРИДОВ Расщепление всех соединений, поступающих в организм с пищей, происходит в тонком кишечнике под действием ферментов, так как эпителиальные клетки кишечника не способны поглощать сложные молекулы. КРАХМАЛ расщепляется под действием амилазы. Этот фермент есть у растений и животных. У животных содержится в слюне. АМИЛОПЕКТИН амилаза Частично непереваренный амилопектин – декстрины Амило-1, 6 -глюкозидаза Ди- и трисахариды -глюкозидаза (мальтаза) глюкоза АМИЛОЗА амилаза мальтоза -глюкозидаза (мальтаза) глюкоза
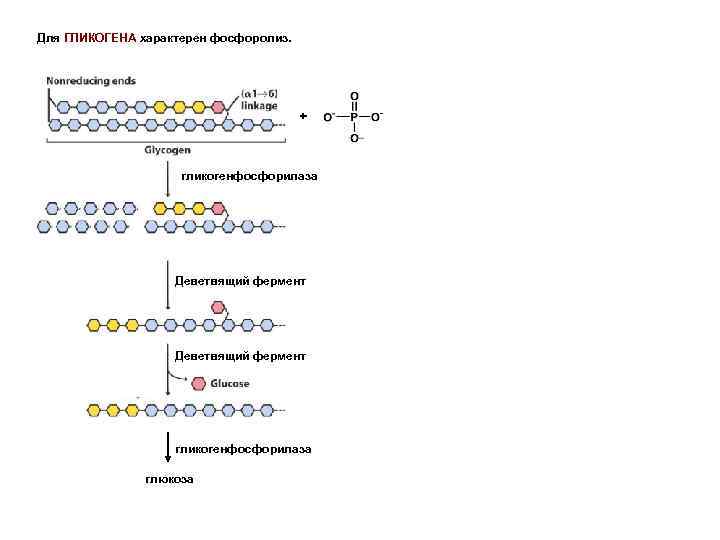
Для ГЛИКОГЕНА характерен фосфоролиз. + гликогенфосфорилаза Деветвящий фермент гликогенфосфорилаза глюкоза
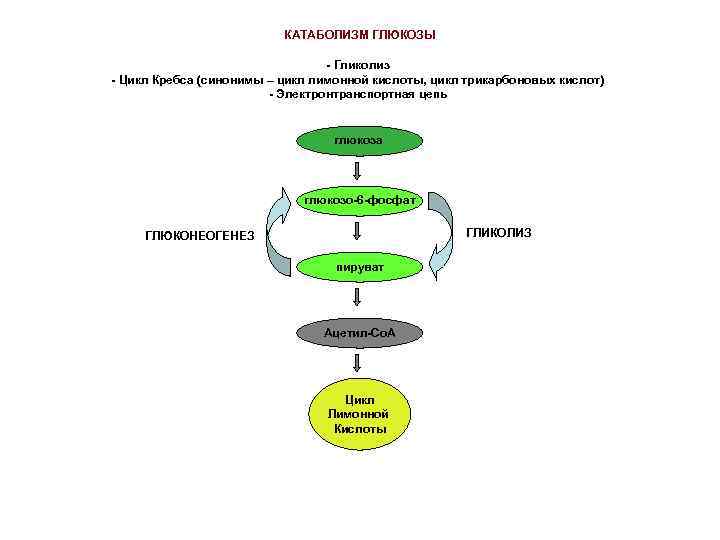
КАТАБОЛИЗМ ГЛЮКОЗЫ - Гликолиз - Цикл Кребса (синонимы – цикл лимонной кислоты, цикл трикарбоновых кислот) - Электронтранспортная цепь глюкоза глюкозо-6 -фосфат ГЛИКОЛИЗ ГЛЮКОНЕОГЕНЕЗ пируват Ацетил-Со. А Цикл Лимонной Кислоты
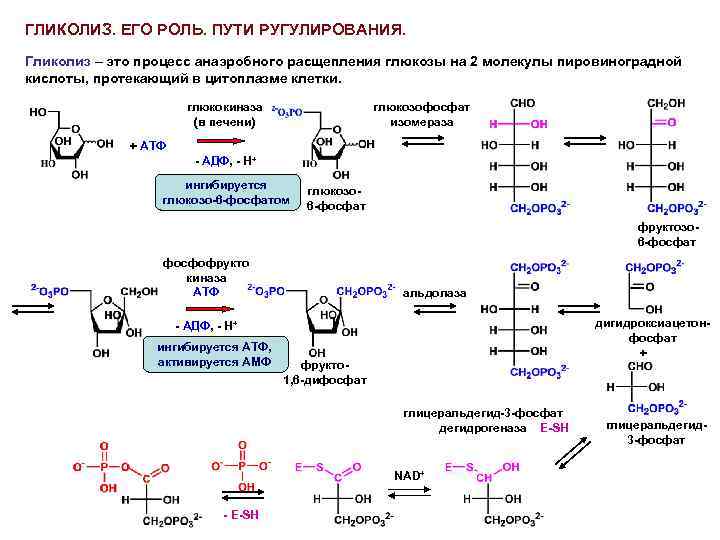
ГЛИКОЛИЗ. ЕГО РОЛЬ. ПУТИ РУГУЛИРОВАНИЯ. Гликолиз – это процесс анаэробного расщепления глюкозы на 2 молекулы пировиноградной кислоты, протекающий в цитоплазме клетки. глюкокиназа (в печени) глюкозофосфат изомераза + АТФ - АДФ, - Н+ ингибируется глюкозо-6 -фосфатом глюкозо 6 -фосфат фруктозо 6 -фосфат фосфофрукто киназа АТФ альдолаза дигидроксиацетонфосфат + - АДФ, - Н+ ингибируется АТФ, активируется АМФ фрукто 1, 6 -дифосфат глицеральдегид-3 -фосфат дегидрогеназа E-SH NAD+ - E-SH глицеральдегид 3 -фосфат
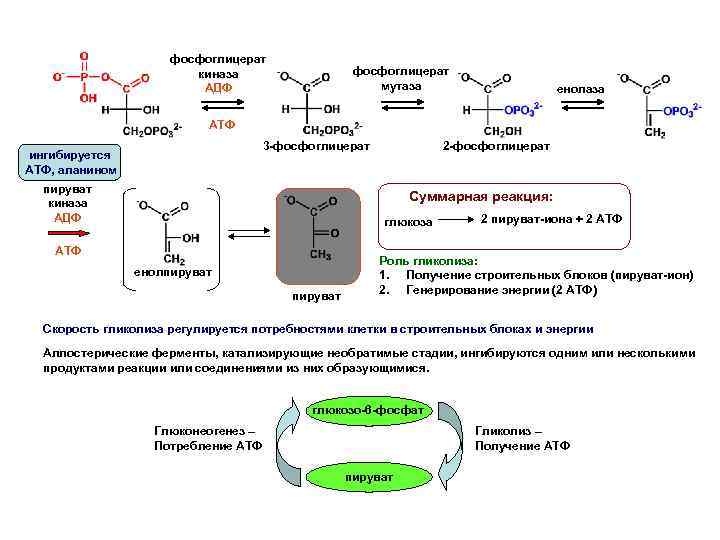
фосфоглицерат киназа АДФ фосфоглицерат мутаза енолаза АТФ 3 -фосфоглицерат ингибируется АТФ, аланином пируват киназа АДФ 2 -фосфоглицерат Суммарная реакция: глюкоза АТФ енолпируват 2 пируват-иона + 2 АТФ Роль гликолиза: 1. Получение строительных блоков (пируват-ион) 2. Генерирование энергии (2 АТФ) Скорость гликолиза регулируется потребностями клетки в строительных блоках и энергии Аллостерические ферменты, катализирующие необратимые стадии, ингибируются одним или несколькими продуктами реакции или соединениями из них образующимися. глюкозо-6 -фосфат Глюконеогенез – Потребление АТФ Гликолиз – Получение АТФ пируват
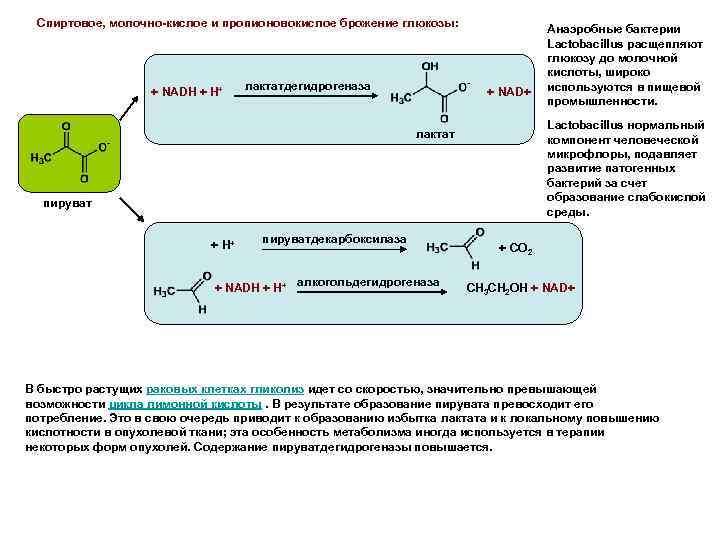
Спиртовое, молочно-кислое и пропионовокислое брожение глюкозы: + NADH + H+ лактатдегидрогеназа + NAD+ Lactobacillus нормальный компонент человеческой микрофлоры, подавляет развитие патогенных бактерий за счет образование слабокислой среды. лактат пируват + H+ пируватдекарбоксилаза + NADH + H+ алкогольдегидрогеназа Анаэробные бактерии Lactobacillus расщепляют глюкозу до молочной кислоты, широко используются в пищевой промышленности. + CO 2 CH 3 CH 2 OH + NAD+ В быстро растущих раковых клетках гликолиз идет со скоростью, значительно превышающей возможности цикла лимонной кислоты. В результате образование пирувата превосходит его потребление. Это в свою очередь приводит к образованию избытка лактата и к локальному повышению кислотности в опухолевой ткани; эта особенность метаболизма иногда используется в терапии некоторых форм опухолей. Содержание пируватдегидрогеназы повышается.
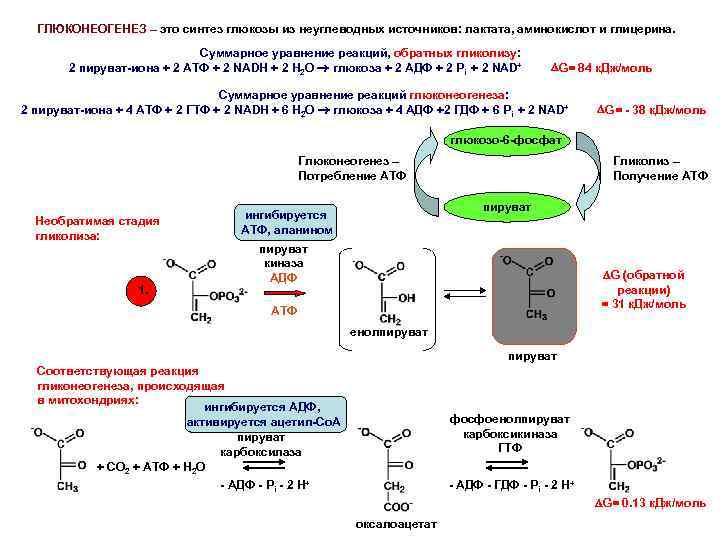
ГЛЮКОНЕОГЕНЕЗ – это синтез глюкозы из неуглеводных источников: лактата, аминокислот и глицерина. Суммарное уравнение реакций, обратных гликолизу: 2 пируват-иона + 2 АТФ + 2 NADH + 2 H 2 O глюкоза + 2 АДФ + 2 Рi + 2 NAD+ G= 84 к. Дж/моль Суммарное уравнение реакций глюконеогенеза: 2 пируват-иона + 4 АТФ + 2 ГТФ + 2 NADH + 6 H 2 O глюкоза + 4 АДФ +2 ГДФ + 6 Рi + 2 NAD+ G= - 38 к. Дж/моль глюкозо-6 -фосфат Глюконеогенез – Потребление АТФ Необратимая стадия гликолиза: 1. Гликолиз – Получение АТФ пируват ингибируется АТФ, аланином пируват киназа АДФ G (обратной реакции) = 31 к. Дж/моль АТФ енолпируват Соответствующая реакция гликонеогенеза, происходящая в митохондриях: ингибируется АДФ, активируется ацетил-Со. А пируват карбоксилаза + CO 2 + AТФ + H 2 O - АДФ - Рi - 2 H+ фосфоенолпируват карбоксикиназа ГТФ - АДФ - ГДФ - Рi - 2 H+ G= 0. 13 к. Дж/моль оксалоацетат
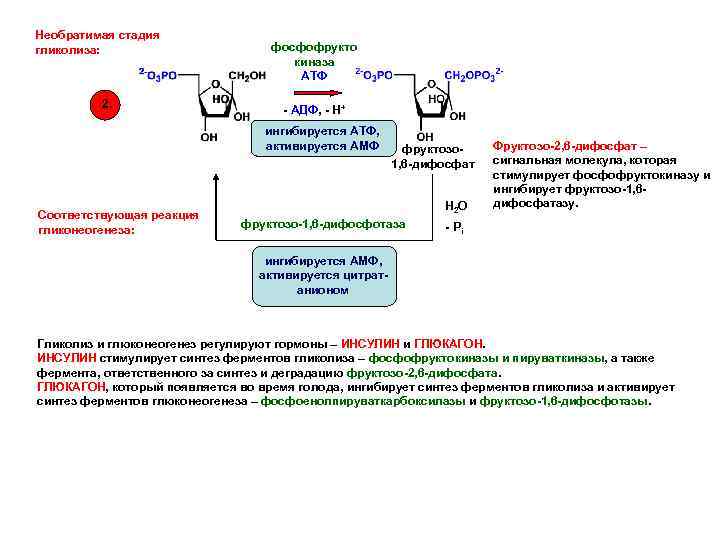
Необратимая стадия гликолиза: 2. фосфофрукто киназа АТФ - АДФ, - Н+ ингибируется АТФ, активируется АМФ Соответствующая реакция гликонеогенеза: фруктозо 1, 6 -дифосфат H 2 O фруктозо-1, 6 -дифосфотаза Фруктозо-2, 6 -дифосфат – сигнальная молекула, которая стимулирует фосфофруктокиназу и ингибирует фруктозо-1, 6 дифосфатазу. - Pi ингибируется АМФ, активируется цитратанионом Гликолиз и глюконеогенез регулируют гормоны – ИНСУЛИН и ГЛЮКАГОН. ИНСУЛИН стимулирует синтез ферментов гликолиза – фосфофруктокиназы и пируваткиназы, а также фермента, ответственного за синтез и деградацию фруктозо-2, 6 -дифосфата. ГЛЮКАГОН, который появляется во время голода, ингибирует синтез ферментов гликолиза и активирует синтез ферментов глюконеогенеза – фосфоенолпируваткарбоксилазы и фруктозо-1, 6 -дифосфотазы.
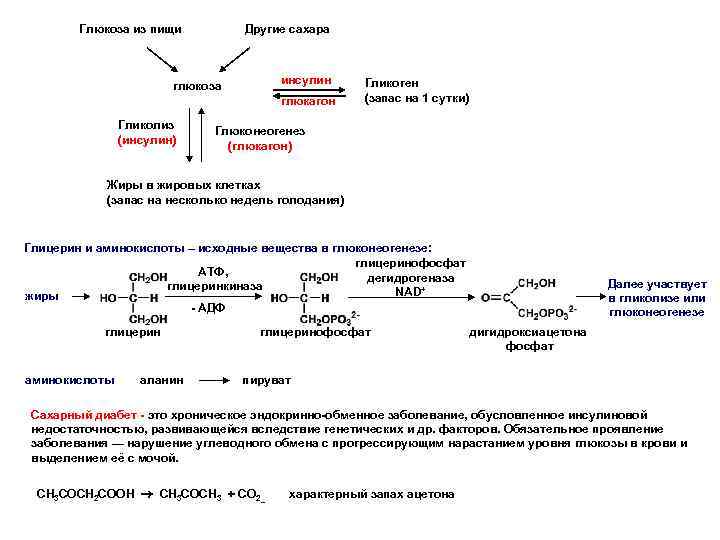
Глюкоза из пищи Другие сахара инсулин глюкоза глюкагон Гликолиз (инсулин) Гликоген (запас на 1 сутки) Глюконеогенез (глюкагон) Жиры в жировых клетках (запас на несколько недель голодания) Глицерин и аминокислоты – исходные вещества в глюконеогенезе: глицеринофосфат АТФ, дегидрогеназа глицеринкиназа NAD+ жиры - АДФ глицерин аминокислоты аланин глицеринофосфат Далее участвует в гликолизе или глюконеогенезе дигидроксиацетона фосфат пируват Сахарный диабет - это хроническое эндокринно-обменное заболевание, обусловленное инсулиновой недостаточностью, развивающейся вследствие генетических и др. факторов. Обязательное проявление заболевания — нарушение углеводного обмена с прогрессирующим нарастанием уровня глюкозы в крови и выделением её с мочой. CH 3 COCH 2 COOH CH 3 COCH 3 + CO 2_ характерный запах ацетона
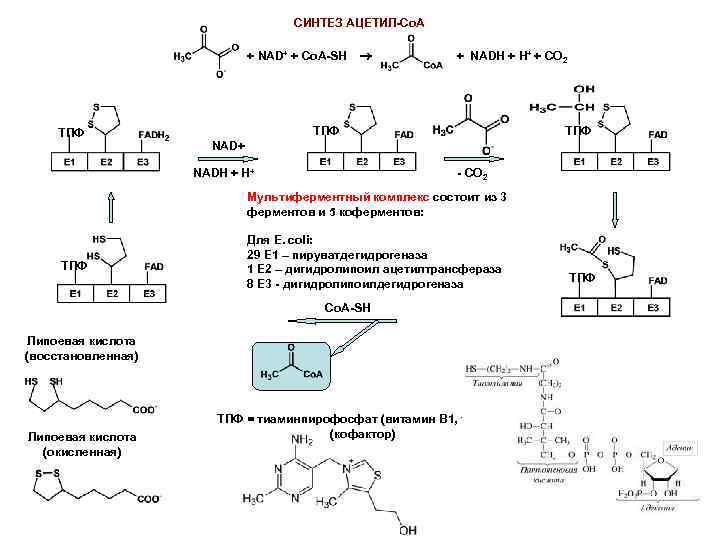
СИНТЕЗ АЦЕТИЛ-Сo. A + NAD+ + Co. A-SH + NADH + H+ + CO 2 ТПФ ТПФ NAD+ NADH + H+ - СO 2 Мультиферментный комплекс состоит из 3 ферментов и 5 коферментов: ТПФ Для E. coli: 29 Е 1 – пируватдегидрогеназа 1 Е 2 – дигидролипоил ацетилтрансфераза 8 Е 3 - дигидролипоилдегидрогеназа Co. A-SH Липоевая кислота (восстановленная) Липоевая кислота (окисленная) ТПФ = тиаминпирофосфат (витамин В 1, тиамин) (кофактор) ТПФ

Пантенол, бипантен – препараты на основе пантотеновой кислоты, при возникновении проблем с кожей. Бе ри-бе ри — болезнь, которая вызвана недостатком витамина В 1 в организме человека (авитаминоз В 1 ). Витамин В 1 способствует нормальному протеканию процессов углеводного и жирового обмена. Его дефицит приводит к накоплению в крови человека пировиноградной кислоты и её повышенной концентрации в нервной системе. Последствием такого биохимического нарушения обмена веществ является энцефалопатия Вернике (острое поражение среднего мозга) или полиневрит (поражения нервной системы), такое состояние возникает у людей, питающихся преимущественно рисом, лишенным оболочки, и некоторыми видами других зерновых культур. В современном обществе заболевание встречается редко, в связи с тем что с пищей поступает достаточное количество витаминов
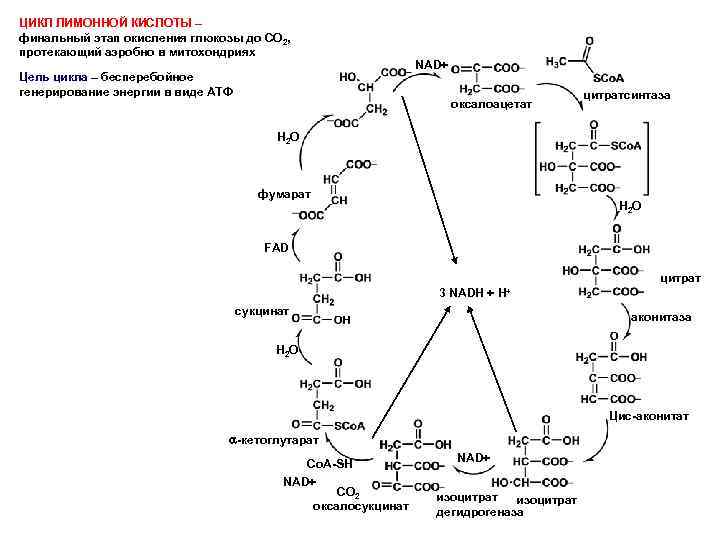
ЦИКЛ ЛИМОННОЙ КИСЛОТЫ – финальный этап окисления глюкозы до CO 2, протекающий аэробно в митохондриях Цель цикла – бесперебойное генерирование энергии в виде АТФ NAD+ оксалоацетат цитратсинтаза H 2 O фумарат H 2 O FAD цитрат 3 NADH + H+ сукцинат аконитаза H 2 O Цис-аконитат -кетоглутарат Co. A-SH NAD+ CO 2 оксалосукцинат NAD+ изоцитрат дегидрогеназа
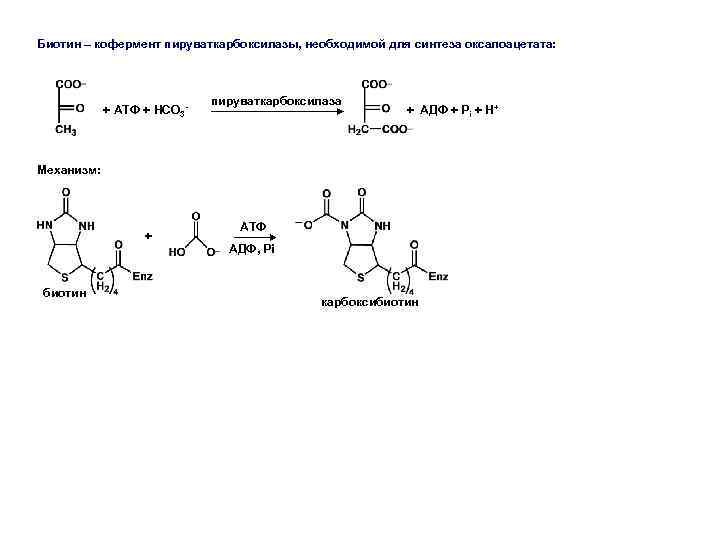
Биотин – кофермент пируваткарбоксилазы, необходимой для синтеза оксалоацетата: пируваткарбоксилаза + АТФ + HCO 3 - + АДФ + Pi + H+ Механизм: + биотин АТФ АДФ, Pi карбоксибиотин
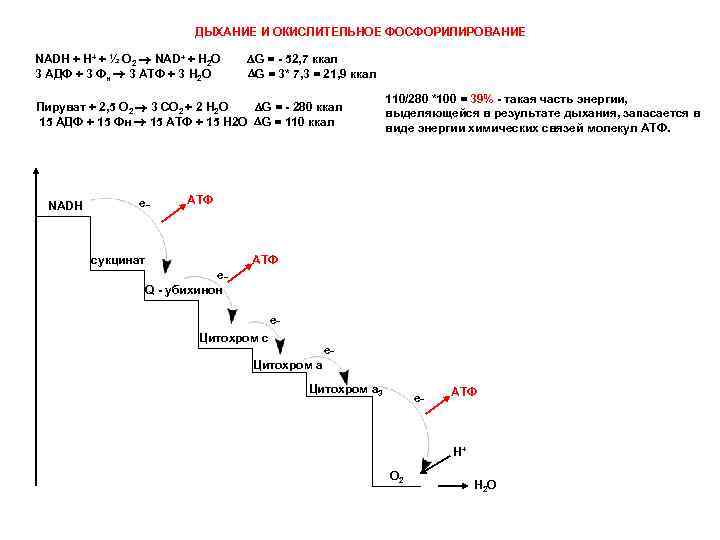
ДЫХАНИЕ И ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ NADH + H+ + ½ О 2 NAD+ + H 2 O G = - 52, 7 ккал 3 АДФ + 3 Фн 3 АТФ + 3 H 2 O G = 3* 7, 3 = 21, 9 ккал Пируват + 2, 5 O 2 3 CO 2 + 2 H 2 O G = - 280 ккал 15 АДФ + 15 Фн 15 АТФ + 15 H 2 O G = 110 ккал NADH e_ 110/280 *100 = 39% - такая часть энергии, выделяющейся в результате дыхания, запасается в виде энергии химических связей молекул АТФ сукцинат e_ Q - убихинон e_ Цитохром с e_ Цитохром а 3 e_ АТФ H+ O 2 H 2 O
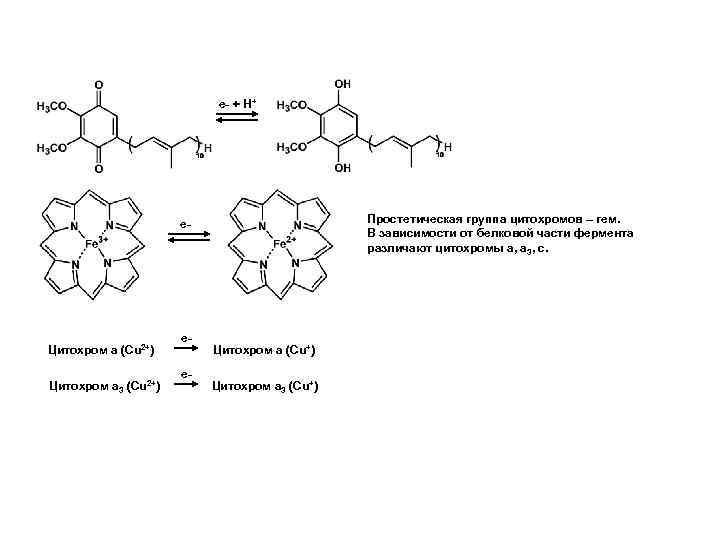
e_ + H+ Простетическая группа цитохромов – гем. В зависимости от белковой части фермента различают цитохромы а, а 3, с. e_ Цитохром а (Cu 2+) Цитохром а 3 (Cu 2+) e_ e_ Цитохром а (Cu+) Цитохром а 3 (Cu+)
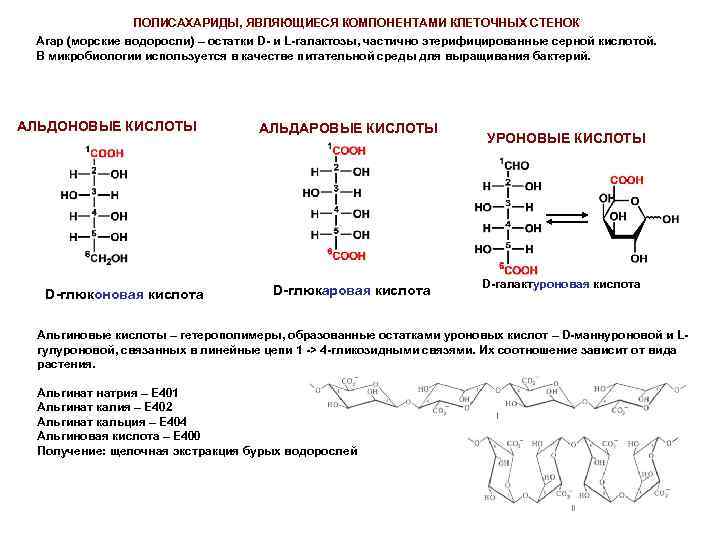
ПОЛИСАХАРИДЫ, ЯВЛЯЮЩИЕСЯ КОМПОНЕНТАМИ КЛЕТОЧНЫХ СТЕНОК Агар (морские водоросли) – остатки D- и L-галактозы, частично этерифицированные серной кислотой. В микробиологии используется в качестве питательной среды для выращивания бактерий. АЛЬДОНОВЫЕ КИСЛОТЫ D-глюконовая кислота АЛЬДАРОВЫЕ КИСЛОТЫ D-глюкаровая кислота УРОНОВЫЕ КИСЛОТЫ D-галактуроновая кислота Альгиновые кислоты – гетерополимеры, образованные остатками уроновых кислот – D-маннуроновой и L- гулуроновой, связанных в линейные цепи 1 -> 4 -гликозидными связями. Их соотношение зависит от вида растения. Альгинат натрия – Е 401 Альгинат калия – Е 402 Альгинат кальция – Е 404 Альгиновая кислота – Е 400 Получение: щелочная экстракция бурых водорослей

УРОНОВЫЕ КИСЛОТЫ Источник: клеточные стенки водорослей, фруктов (цитрусовые), овощей. Применение: пищевая добавка Е 440, гелеобразователь (желе, мармелад и др. ), загуститель (мороженое и др. ), капсулирование лекарственных средств. D-галактуроновая кислота Пектовая кислота - полимер D-галактуроновой кислоты Пектины – продукты метилирования пектовой кислоты Камеди относятся к полисахаридам, в состав которых входят арабиноза, рамноза, галактоза, а также одна или несколько уроновых кислот. Камеди из растений выделяются в виде вязких растворов; застывая, они превращаются в стекловидную массу. Образуются при механическом повреждении или инфекционном поражении тканей растений. Камедь бобов рожкового дерева (средиземноморская акация) (Е 410) состоит из остатков D-маннозы, связанных 1 -4 гликозидной связью, из которых каждый четвертый остаток связан 1 -6 гликозидной связью с D-галактозой, замедляет образование кристалликов льда, используется при изготовлении мороженого, в организме человека не расщепляется ферментами. Гуаровая камедь – производится из семян Cyamopsis tetraganoloba, известного как гуар, или гороховое дерево. Ксантановая камедь (Е 415) – производится бактериями, основная цепь сходна с целлюлозой, ответвления содержат глюкуроновую кислоту, глюкозу, маннозу. Защищает клетку бактерии от пересыхания, используется в увлажняющих кремах, пищевая добавка.

Важным действующим началом экстракта корня алтея являются слизи, состоящие из полисахаридов, содержащих арабинозу, глюкозу и галактозу. Данные моно- и дисахариды связаны между собой остатками галактуроновой кислоты. Одним из самых популярных и известных препаратов на основе корня алтея является «Мукалтин» Лечебные свойства алтея обусловлены высоким содержанием полисахаридов, способных в водных настоях набухать, увеличиваться в объеме и покрывать тонким слоем слизистые оболочки и кожу. Этот слой предохраняет слизистые оболочки от воздействия вредных факторов (холодный или сухой воздух; раздражающее влияние компонентов пищи, высыхание). Кроме того, слизисто-полисахаридный комплекс впитывает, адсорбирует микробные, вирусные и токсические продукты, выделяемые пораженными клетками эпителия, инактивирует, не допускает контакта токсинов со слизистой оболочкой.

Клеточная стенка бактерий: Клеточная стенка бактерий – жесткая структура, защищающая ее от воздействия окружающей среды. Представляет собой достаточно большую молекулу, состоящую из параллельных полисахаридных цепей, связанных между собой поперечными короткими полипептидными цепями. Муропептид = 1 -4 (N-ацетил-D-глюкозамин + N-ацетилмурамовая кислота)n Единая замкнутая структура называется муреиновый мешок. N-ацетилмурамовая кислота У граммположительных бактерий – тейхоевая кислота: R = глюкоза, N-ацетил-D-глюкозамин, D-аланин
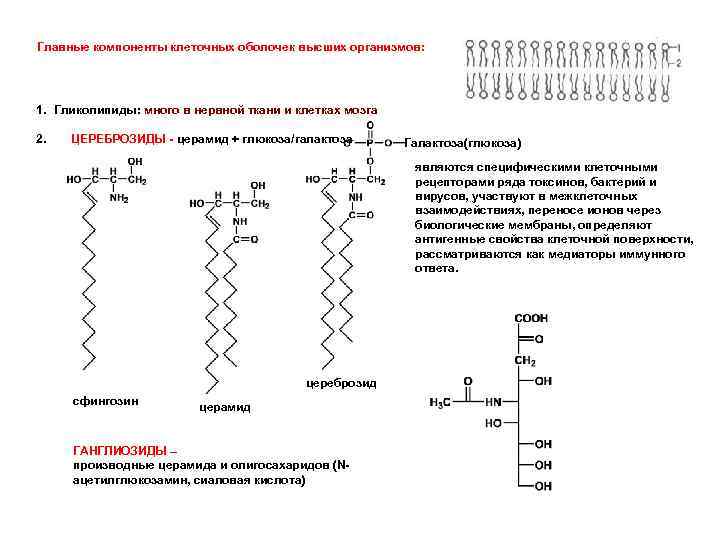
Главные компоненты клеточных оболочек высших организмов: 1. Гликолипиды: много в нервной ткани и клетках мозга 2. ЦЕРЕБРОЗИДЫ - церамид + глюкоза/галактоза Галактоза(глюкоза) являются специфическими клеточными рецепторами ряда токсинов, бактерий и вирусов, участвуют в межклеточных взаимодействиях, переносе ионов через биологические мембраны, определяют антигенные свойства клеточной поверхности, рассматриваются как медиаторы иммунного ответа. цереброзид сфингозин церамид ГАНГЛИОЗИДЫ – производные церамида и олигосахаридов (Nацетилглюкозамин, сиаловая кислота)
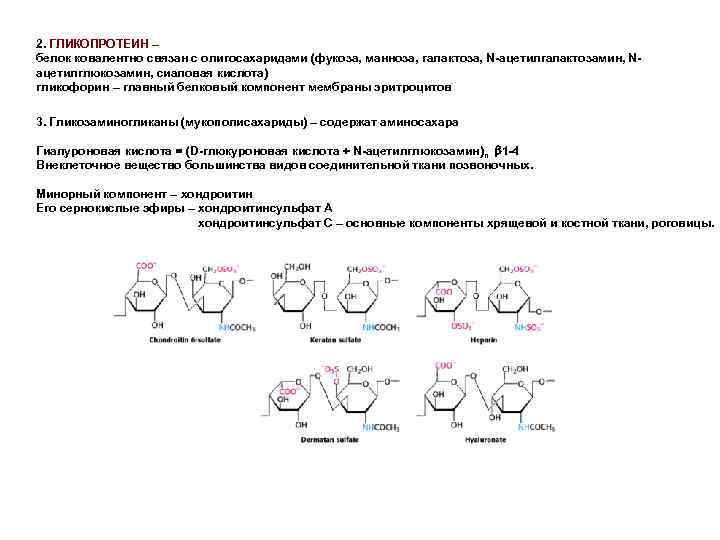
2. ГЛИКОПРОТЕИН – белок ковалентно связан с олигосахаридами (фукоза, манноза, галактоза, N-ацетилгалактозамин, Nацетилглюкозамин, сиаловая кислота) гликофорин – главный белковый компонент мембраны эритроцитов 3. Гликозаминогликаны (мукополисахариды) – содержат аминосахара Гиалуроновая кислота = (D-глюкуроновая кислота + N-ацетилглюкозамин)n 1 -4 Внеклеточное вещество большинства видов соединительной ткани позвоночных. Минорный компонент – хондроитин Его сернокислые эфиры – хондроитинсульфат А хондроитинсульфат С – основные компоненты хрящевой и костной ткани, роговицы.
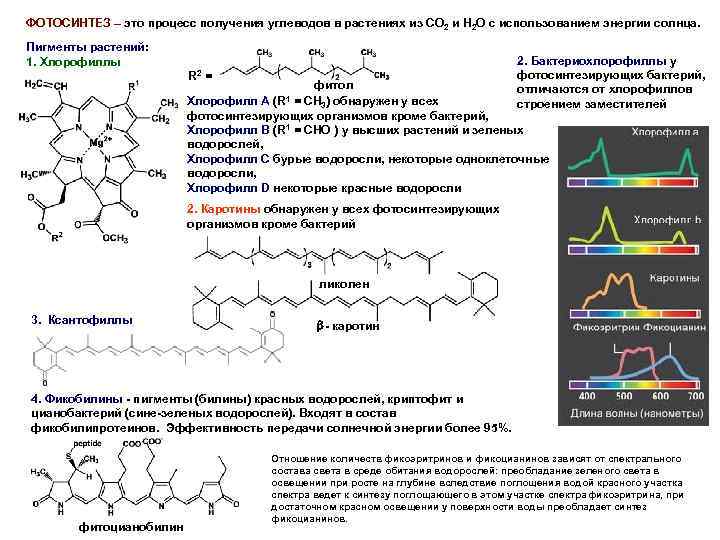
ФОТОСИНТЕЗ – это процесс получения углеводов в растениях из СО 2 и H 2 O с использованием энергии солнца. Пигменты растений: 1. Хлорофиллы R 2 = 2. Бактериохлорофиллы у фотосинтезирующих бактерий, отличаются от хлорофиллов строением заместителей фитол 3) обнаружен у всех фотосинтезирующих организмов кроме бактерий, Хлорофилл В (R 1 = CHО ) у высших растений и зеленых водорослей, Хлорофилл С бурые водоросли, некоторые одноклеточные водоросли, Хлорофилл D некоторые красные водоросли Хлорофилл А (R 1 = CH 2. Каротины обнаружен у всех фотосинтезирующих организмов кроме бактерий ликолен 3. Ксантофиллы - каротин 4. Фикобилины - пигменты (билины) красных водорослей, криптофит и цианобактерий (сине-зеленых водорослей). Входят в состав фикобилипротеинов. Эффективность передачи солнечной энергии более 95%. фитоцианобилин Отношение количеств фикоэритринов и фикоцианинов зависят от спектрального состава света в среде обитания водорослей: преобладание зеленого света в освещении при росте на глубине вследствие поглощения водой красного участка спектра ведет к синтезу поглощающего в этом участке спектра фикоэритрина, при достаточном красном освещении у поверхности воды преобладает синтез фикоцианинов.
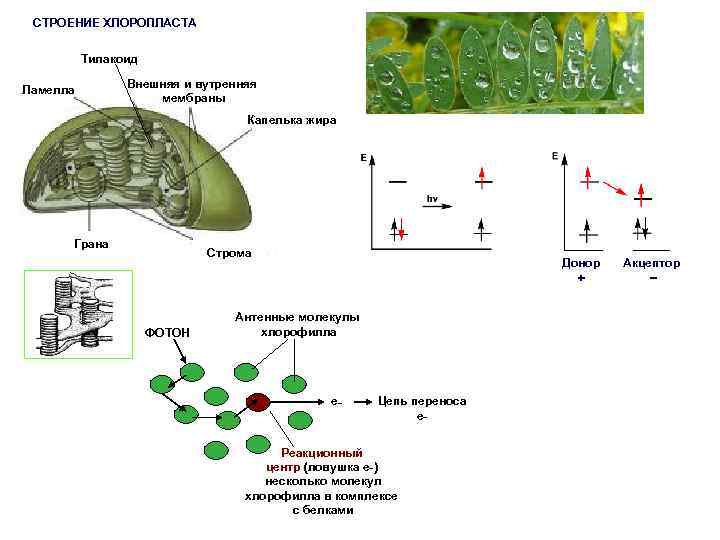
СТРОЕНИЕ ХЛОРОПЛАСТА Тилакоид Ламелла Внешняя и вутренняя мембраны Капелька жира Грана Строма ФОТОН Донор + Антенные молекулы хлорофилла e_ Цепь переноса e_ Реакционный центр (ловушка e_) несколько молекул хлорофилла в комплексе с белками Акцептор
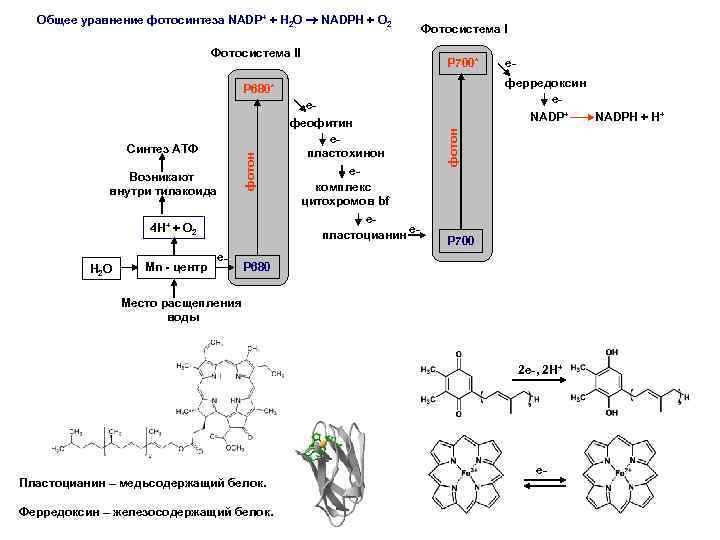
Общее уравнение фотосинтеза NADP+ + H 2 O NADPH + O 2 Фотосистема II Фотосистема I P 700* ферредоксин e_ P 680* Возникают внутри тилакоида 4 H+ + O 2 H 2 O Mn - центр e_ e_ комплекс цитохромов bf e_ e_ пластоцианин NADP+ фотон Синтез АТФ e_ феофитин e_ пластохинон e_ P 700 P 680 Место расщепления воды 2 e_, 2 H+ Пластоцианин – медьсодержащий белок. Ферредоксин – железосодержащий белок. e_ NADPH + H+

Синтез АТФ Хемиосматический механизм Митчелла Протондвижущая сила ГЕРБИЦИДЫ Разновидность – ингибиторы фотосинтеза. Эти гербициды проникают в хлоропласты растений; некрые из них препятствуют захвату электронов ферредоксином и нарушают процесс восстановления кофермента никотинамидадениндинуклеотидфосфата (НАДФ) в т. наз. фотосистеме I, другие (из групп арилмочевин, сим-триазинов, 1, 2, 4 -триазинонов, урацилов, гидроксибензонитрилов, пиридазинонов) препятствуют переносу электроновк пластохинону в так называемой фотосистеме II.
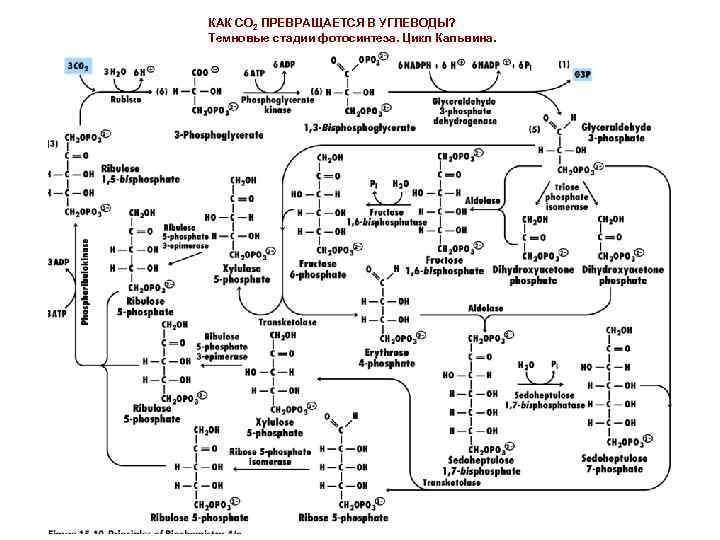
КАК СО 2 ПРЕВРАЩАЕТСЯ В УГЛЕВОДЫ? Темновые стадии фотосинтеза. Цикл Кальвина.
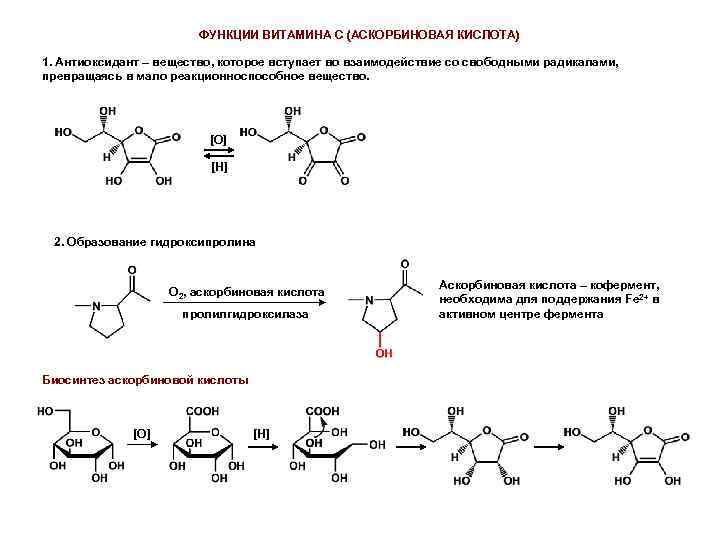
ФУНКЦИИ ВИТАМИНА С (АСКОРБИНОВАЯ КИСЛОТА) 1. Антиоксидант – вещество, которое вступает во взаимодействие со свободными радикалами, превращаясь в мало реакционноспособное вещество. [O] [H] 2. Образование гидроксипролина О 2, аскорбиновая кислота пролилгидроксилаза Биосинтез аскорбиновой кислоты [O] [H] Аскорбиновая кислота – кофермент, необходима для поддержания Fe 2+ в активном центре фермента
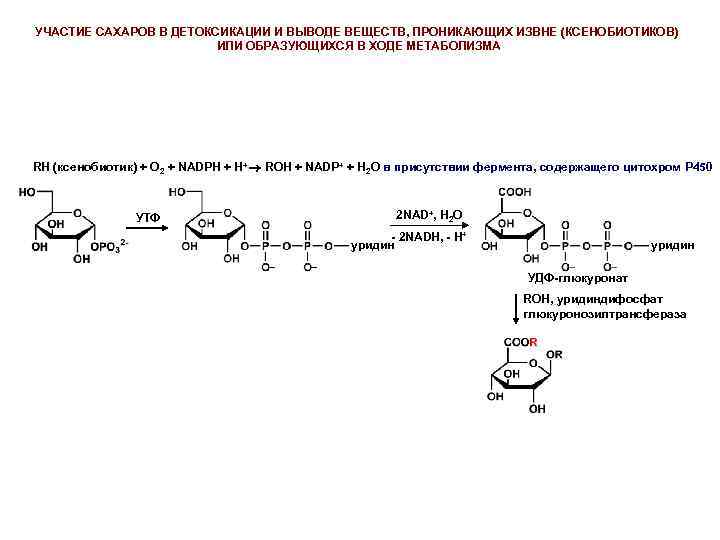
УЧАСТИЕ САХАРОВ В ДЕТОКСИКАЦИИ И ВЫВОДЕ ВЕЩЕСТВ, ПРОНИКАЮЩИХ ИЗВНЕ (КСЕНОБИОТИКОВ) ИЛИ ОБРАЗУЮЩИХСЯ В ХОДЕ МЕТАБОЛИЗМА RН (ксенобиотик) + О 2 + NADPH + H+ ROH + NADP+ + H 2 O в присутствии фермента, содержащего цитохром Р 450 УТФ 2 NAD+, H 2 O - 2 NADH, - H+ уридин УДФ-глюкуронат RОН, уридиндифосфат глюкуронозилтрансфераза

Нуклеотиды, нуклеиновые кислоты, их биологическая роль. Пуриновые основания аденин гуанин Пиримидиновые основания урацил тимин цитозин Основание + рибоза + фосфатная группа = нуклеотид нуклеозид аденозин монофосфат (АМФ) В общем случае, чем сложнее организм, тем больший размер имеет молекула ДНК. В качестве исключения, в крупных клетках бобов молекула ДНК крупнее, чем в организме человека. ДНК земноводных крупнее, чем ДНК других видов животных.
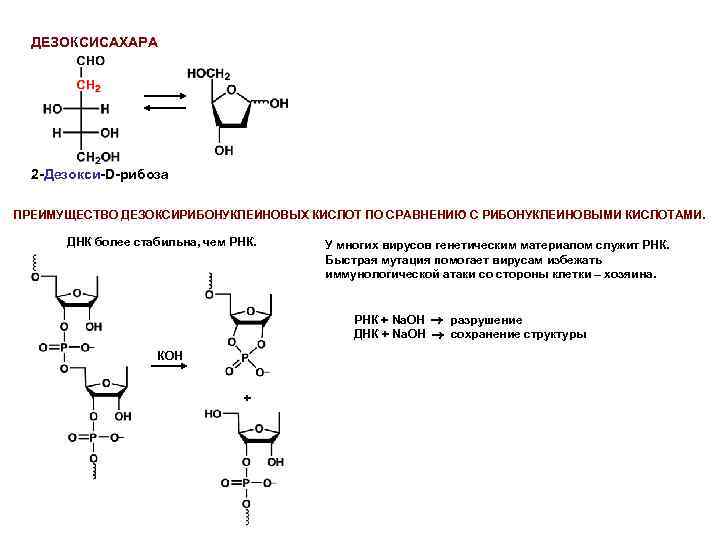
ДЕЗОКСИСАХАРА 2 -Дезокси-D-рибоза ПРЕИМУЩЕСТВО ДЕЗОКСИРИБОНУКЛЕИНОВЫХ КИСЛОТ ПО СРАВНЕНИЮ С РИБОНУКЛЕИНОВЫМИ КИСЛОТАМИ. ДНК более стабильна, чем РНК. У многих вирусов генетическим материалом служит РНК. Быстрая мутация помогает вирусам избежать иммунологической атаки со стороны клетки – хозяина. РНК + Na. OH разрушение ДНК + Na. OH сохранение структуры КОН +

ИСПЛЬЗОВАНИЕ АНАЛОГОВ НУКЛЕОТИДОВ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ Вирус представляет собой нуклеиновую кислоту, окруженную несколькими оболочками. У ретровирусов (к ним относится вирус СПИДа) генетическая информация представлена одной молекулой РНК. Ретровирус содержит фермент – обратную транскриптазу. При попадании вируса в чужой организм этот фермент копирует РНК вируса в ДНК. Затем тот же фермент создает вторую цепь ДНК. Другой вирусный фермент – интеграза – подсоединяет полученную 2 -х цепочечную ДНК вируса к ДНК клетки-хозяина. После этого генетическая информация вируса будет поступать из клетки в клетку при делении клетки-хозяина. Некоторые аналоги нуклеотидов являются ингибиторами обратной транскриптазы, обрывают элонгацию цепи ДНК из-за отсутствия 3, - ОН. Используются в качестве лекарственных средств. Азотимидин (ВИЧ) Ламивудин (лечение хронического гепатита С) Дезоксигуанозин (лечение герпеса) Ацикловир (зовиракс) (лечение герпеса) ГЕНОТЕРАПИЯ – доставка к клеткам больного, у которого присутствует дефектный ген, «хороший» ген, способный исправить дефект.
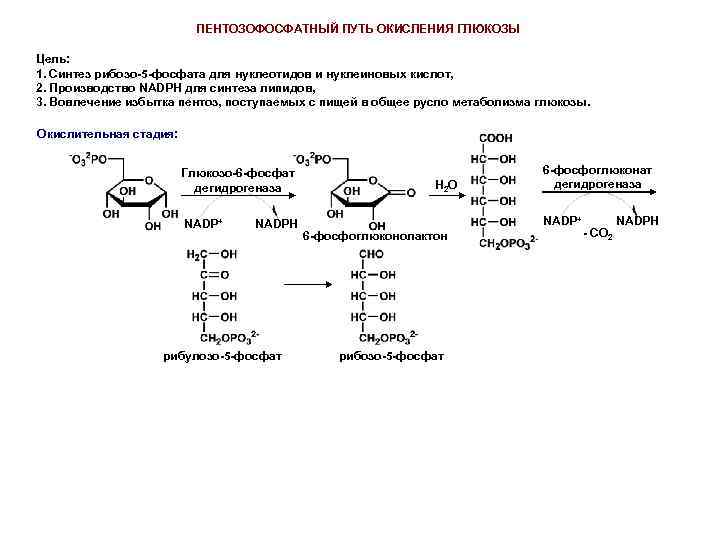
ПЕНТОЗОФОСФАТНЫЙ ПУТЬ ОКИСЛЕНИЯ ГЛЮКОЗЫ Цель: 1. Синтез рибозо-5 -фосфата для нуклеотидов и нуклеиновых кислот, 2. Производство NADPH для синтеза липидов, 3. Вовлечение избытка пентоз, поступаемых с пищей в общее русло метаболизма глюкозы. Окислительная стадия: Глюкозо-6 -фосфат дегидрогеназа NADP+ NADPH рибулозо-5 -фосфат H 2 O 6 -фосфоглюконат дегидрогеназа NADP+ 6 -фосфоглюконолактон рибозо-5 -фосфат - CO 2 NADPH
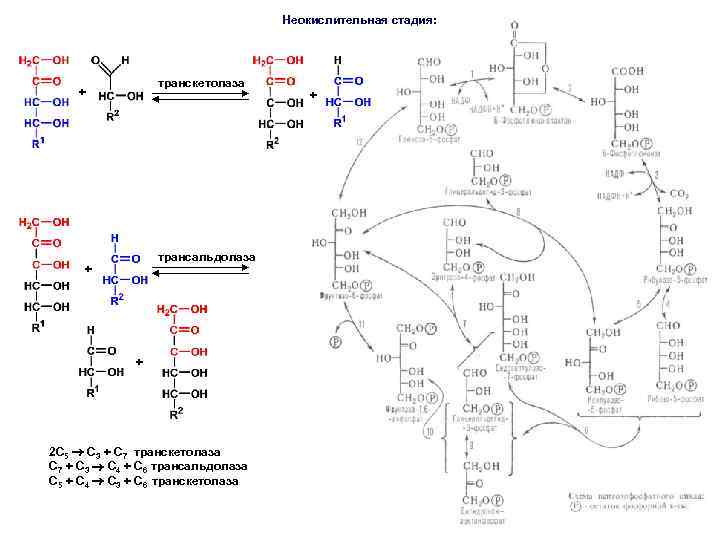
Неокислительная стадия: транскетолаза + трансальдолаза + + 2 С 5 С 3 + С 7 транскетолаза С 7 + С 3 С 4 + С 6 трансальдолаза С 5 + С 4 С 3 + С 6 транскетолаза +
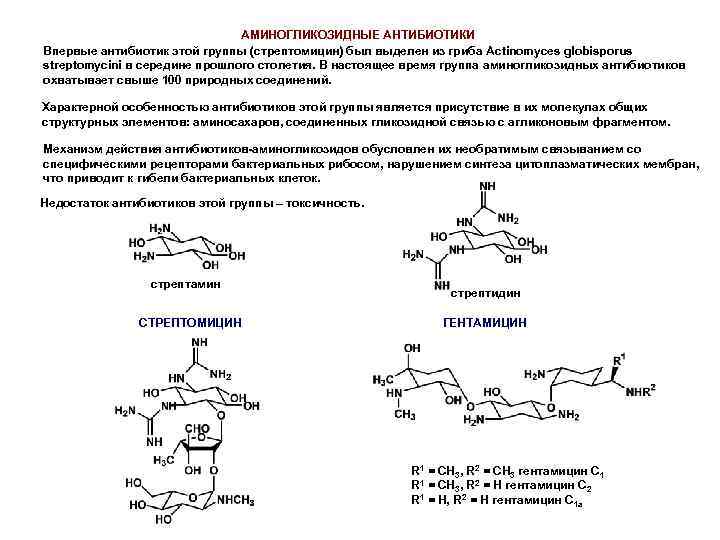
АМИНОГЛИКОЗИДНЫЕ АНТИБИОТИКИ Впервые антибиотик этой группы (стрептомицин) был выделен из гриба Actinomyces globisporus streptomycini в середине прошлого столетия. В настоящее время группа аминогликозидных антибиотиков охватывает свыше 100 природных соединений. Характерной особенностью антибиотиков этой группы является присутствие в их молекулах общих структурных элементов: аминосахаров, соединенных гликозидной связью с агликоновым фрагментом. Механизм действия антибиотиков-аминогликозидов обусловлен их необратимым связыванием со специфическими рецепторами бактериальных рибосом, нарушением синтеза цитоплазматических мембран, что приводит к гибели бактериальных клеток. Недостаток антибиотиков этой группы – токсичность. стрептамин СТРЕПТОМИЦИН стрептидин ГЕНТАМИЦИН R 1 = CH 3, R 2 = CH 3 гентамицин С 1 R 1 = CH 3, R 2 = H гентамицин С 2 R 1 = H, R 2 = H гентамицин С 1 а
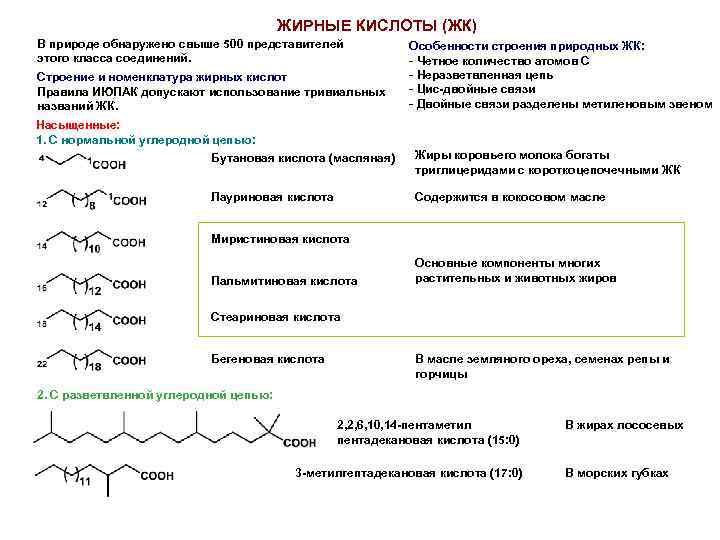
ЖИРНЫЕ КИСЛОТЫ (ЖК) В природе обнаружено свыше 500 представителей этого класса соединений. Строение и номенклатура жирных кислот Правила ИЮПАК допускают использование тривиальных названий ЖК. Насыщенные: 1. С нормальной углеродной цепью: Бутановая кислота (масляная) Лауриновая кислота Особенности строения природных ЖК: - Четное количество атомов С - Неразветвленная цепь - Цис-двойные связи - Двойные связи разделены метиленовым звеном Жиры коровьего молока богаты триглицеридами с короткоцепочечными ЖК Содержится в кокосовом масле Миристиновая кислота Пальмитиновая кислота Основные компоненты многих растительных и животных жиров Стеариновая кислота Бегеновая кислота В масле земляного ореха, семенах репы и горчицы 2. С разветвленной углеродной цепью: 2, 2, 6, 10, 14 -пентаметил пентадекановая кислота (15: 0) 3 -метилгептадекановая кислота (17: 0) В жирах лососевых В морских губках
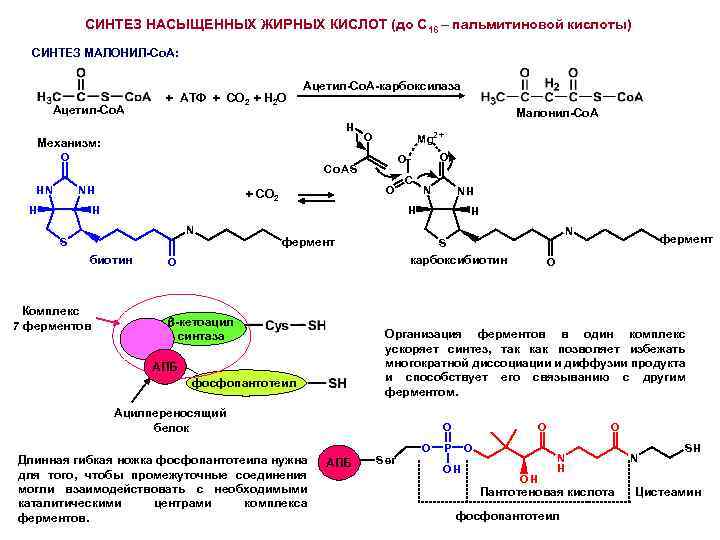
СИНТЕЗ НАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ (до С 16 – пальмитиновой кислоты) СИНТЕЗ МАЛОНИЛ-Co. A: Ацетил-Со. А-карбоксилаза Малонил-Со. А H Механизм: O O_ C o AS NH H O + CO 2 H N NH H N S биотин Комплекс 7 ферментов C O H фермент N S карбоксибиотин O -кетоацил синтаза АПБ фосфопантотеил Ацилпереносящий белок O O O АПБ Ser ------ Длинная гибкая ножка фосфопантотеила нужна для того, чтобы промежуточные соединения могли взаимодействовать с необходимыми каталитическими центрами комплекса ферментов. фермент Организация ферментов в один комплекс ускоряет синтез, так как позволяет избежать многократной диссоциации и диффузии продукта и способствует его связыванию с другим ферментом. O P O ------ HN M g 2+ O OH OH O N H N ------ Ацетил-Со. А + АТФ + CO 2 + H 2 O SH Пантотеновая кислота Цистеамин --------------------------фосфопантотеил
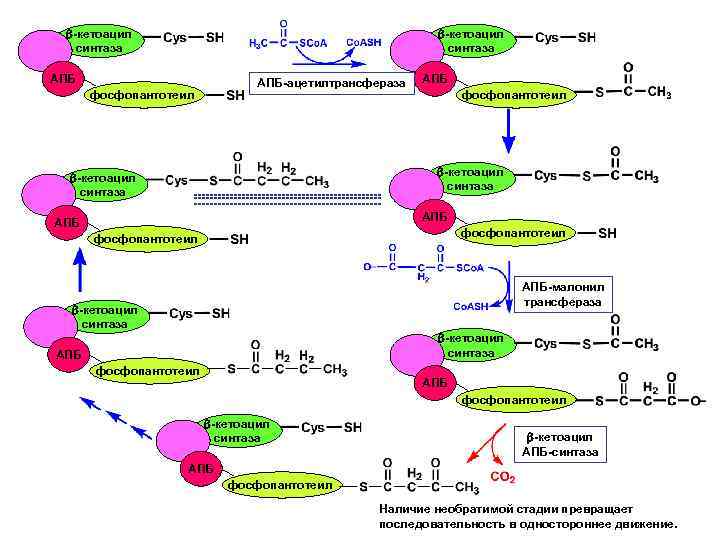
-кетоацил синтаза АПБ АПБ-ацетилтрансфераза фосфопантотеил -кетоацил синтаза ---------------------------------------------------------------------- АПБ фосфопантотеил -кетоацил синтаза АПБ фосфопантотеил АПБ-малонил трансфераза -кетоацил синтаза АПБ фосфопантотеил -кетоацил синтаза -кетоацил АПБ-синтаза АПБ фосфопантотеил Наличие необратимой стадии превращает последовательность в одностороннее движение.
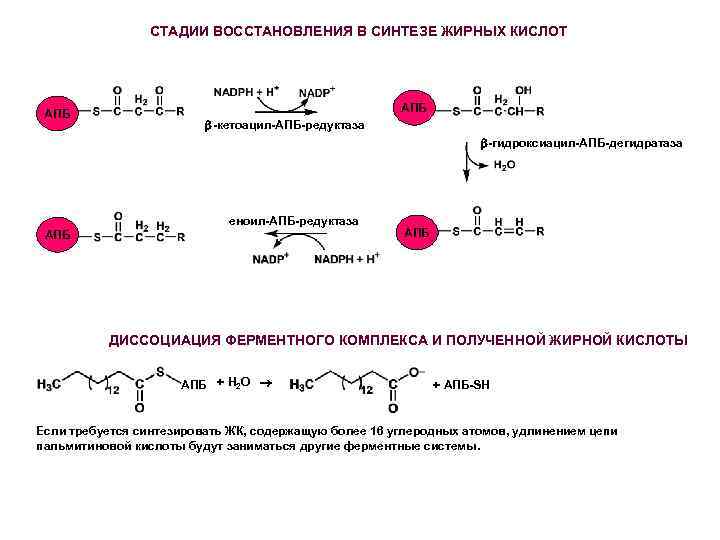
СТАДИИ ВОССТАНОВЛЕНИЯ В СИНТЕЗЕ ЖИРНЫХ КИСЛОТ АПБ -кетоацил-АПБ-редуктаза -гидроксиацил-АПБ-дегидратаза еноил-АПБ-редуктаза АПБ ДИССОЦИАЦИЯ ФЕРМЕНТНОГО КОМПЛЕКСА И ПОЛУЧЕННОЙ ЖИРНОЙ КИСЛОТЫ АПБ + H 2 O + АПБ-SH Если требуется синтезировать ЖК, содержащую более 16 углеродных атомов, удлинением цепи пальмитиновой кислоты будут заниматься другие ферментные системы.

3. С карбоциклическим фрагментом: n = 9, 11 В сливочном масле и липидах некоторых микроорганизмов n = 9, 11 В липидах красных водорослей
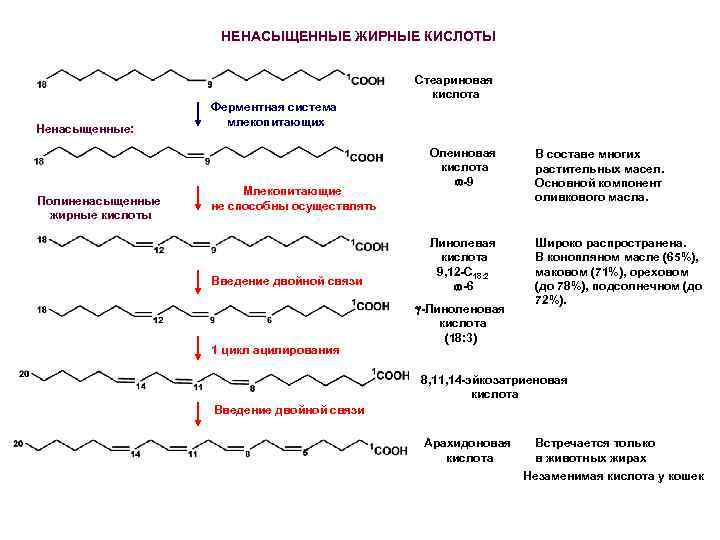
НЕНАСЫЩЕННЫЕ ЖИРНЫЕ КИСЛОТЫ Ненасыщенные: Полиненасыщенные жирные кислоты Ферментная система млекопитающих Млекопитающие не способны осуществлять Введение двойной связи 1 цикл ацилирования Стеариновая кислота Олеиновая кислота -9 В составе многих растительных масел. Основной компонент оливкового масла. Линолевая кислота 9, 12 -С 18: 2 -6 Широко распространена. В конопляном масле (65%), маковом (71%), ореховом (до 78%), подсолнечном (до 72%). -Линоленовая кислота (18: 3) 8, 11, 14 -эйкозатриеновая кислота Введение двойной связи Арахидоновая кислота Встречается только в животных жирах Незаменимая кислота у кошек
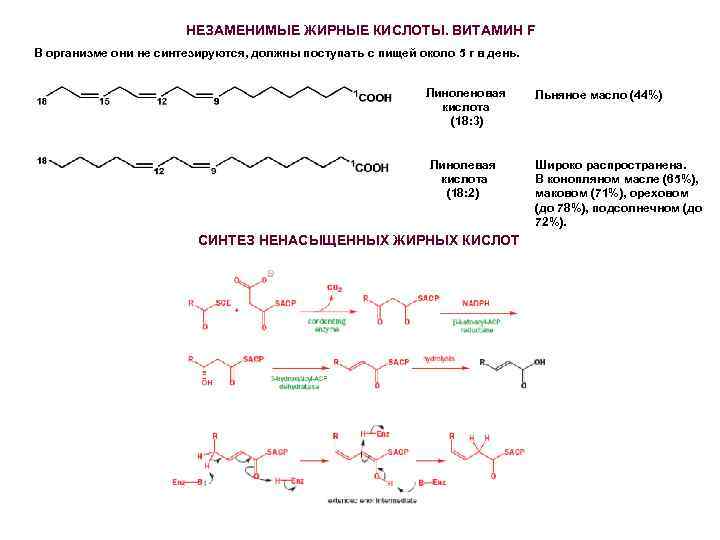
НЕЗАМЕНИМЫЕ ЖИРНЫЕ КИСЛОТЫ. ВИТАМИН F В организме они не синтезируются, должны поступать с пищей около 5 г в день. Линоленовая кислота (18: 3) Линолевая кислота (18: 2) СИНТЕЗ НЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ Льняное масло (44%) Широко распространена. В конопляном масле (65%), маковом (71%), ореховом (до 78%), подсолнечном (до 72%).

Ненасыщенные кислоты дают высыхающие масла. Под действием кислорода воздуха происходит инициирование радикалов и сшивка цепей между собой. На поверхности масла образуется плотная пленка. Принцип индуцированной воздухои полтмеризации положен в основу масляных красок, которые представляют собой суспензию пигмента в высыхающем масле, обычно льняном с добавлением катализатора, ускоряющего окисление и полимеризацию краски. Стабильность алкидных красителей, в состав которых входят жирные кислоты зависит от степени сшивки этих кисло поперечными связями.
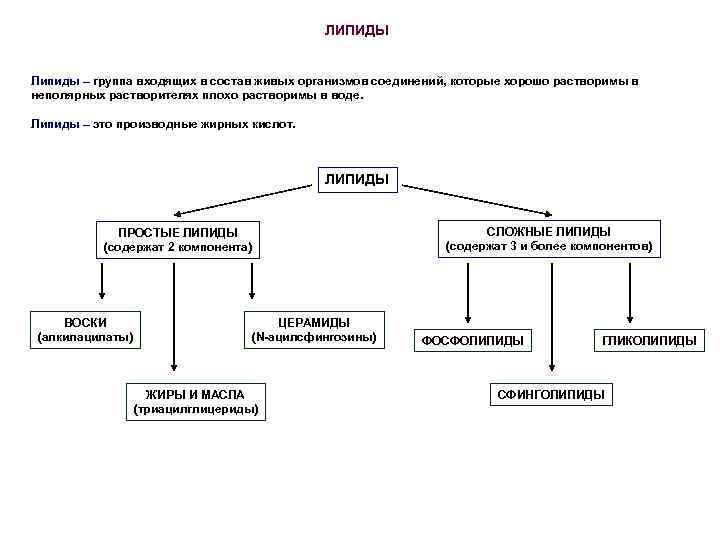
ЛИПИДЫ Липиды – группа входящих в состав живых организмов соединений, которые хорошо растворимы в неполярных растворителях плохо растворимы в воде. Липиды – это производные жирных кислот. ЛИПИДЫ ПРОСТЫЕ ЛИПИДЫ (содержат 2 компонента) ВОСКИ (алкилацилаты) ЦЕРАМИДЫ (N-ацилсфингозины) ЖИРЫ И МАСЛА (триацилглицериды) СЛОЖНЫЕ ЛИПИДЫ (содержат 3 и более компонентов) ФОСФОЛИПИДЫ ГЛИКОЛИПИДЫ СФИНГОЛИПИДЫ

ВОСКИ – сложные эфиры высших жирных кислот и высших одноатомных спиртов. Образуют защитную смазку на коже человека и животных, предохраняют растения от высыхания. Ланолин – шерстяной воск, воск выделяется кожными железами овец в волосяную луковицу и обильно покрывает шерсть. Получают из промывных вод шерстомоек или экстрагированием шерсти органическими растворителями. Представляет собой смесь сложных эфиров высокомолекулярных спиртов (холестерина, эргостерина) с высшими жирными кислотами (миристиновой, пальмитиновой, церотиновой и др. ) и свободных высокомолекулярных спиртов. Используется при изготовлении кремов, пластырей, основы для мазей. Мелиссиловый эфир пальмитиновой кислоты - компонент пчелиного воска Воск бактерий покрывает поверхность кислотоупорных бактерий, например туберкулезных, обеспечивая их устойчивость к внешним воздействиям. Содержит сложные эфиры миколевой кислоты С 88 Н 172 О 4 и эйкозанола СН 3(СН 2)17 СНОНСН 3, а также октадеканола СН 3(СН 2)15 СНОНСН 3. Применение: • В натуральной косметике (основной компонент помад, твердых духов), • Компонент политур и мастик для полировки и защиты мебели, деревянных изделий, паркетных полов, • Для защиты продуктов питания (фруктов, сыров) при транспортировке.

ЖИРЫ И МАСЛА –сложные эфиры глицерина и высших жирных кислот. Выполняют роль запасных веществ ( «жировое депо» ). В жирах отсутствуют свободные гидроксильные группы, поэтому они не растворимы в воде, что имеет важное физиологическое значение, жиры не вымываются из организма, а наоборот накапливаются, являясь важным источником питательных веществ для организма. В глицеридах цепи кислот переплетены между собой и с цепями других молекул в достаточно плотную упаковку. Глицериды насыщенных кислот являются твердыми веществами. Наличие двойных связей в структуре молекулы препятствует ее плотной упаковке, поэтому глицериды ненасыщенных кислот являются маслами. триглицерид Большинство масел и жиров представляют собой сложные смеси триглицеридов, Тпл которых лежит в широком диапазоне температур. Триглицерид стеариновой кислоты – основной компонент животного жира. Жир – это теплоизолирующая оболочка. Жир – это источник питательных веществ, энергии и воды для животных (горбы верблюда, находящийся в спячке медведь). Если коровы питались травой, то их жир имеет желтоватый оттенок, так как вместе с травой в организм поступает каротин, который хорошо растворяется в жирах. Если животные выращиваются преимущественно на искусственных кормах, то их жир будет белым. Семена в большей степени, чем стебли богаты маслами. Масла получают из семян кукурузы, подсолнечника, хлопка, бобов, льна, сои, рапса. В настоящее время маргарин получают из ряда веществ, в том числе растительных масел. Эти масла после частичного гидрирования используются в производстве маргарина. Маргарин по-гречески означает «жемчуг» , был изобретен в 1869 году в качестве заменителя масла. В соответствии с оригинальным рецептом того времени состоял из молока, измельченного коровьего вымени и говяжьего жира. Ненасыщенными ЖК богаты жиры рыб (печень трески), так как они не должны твердеть при низких температурах воды.
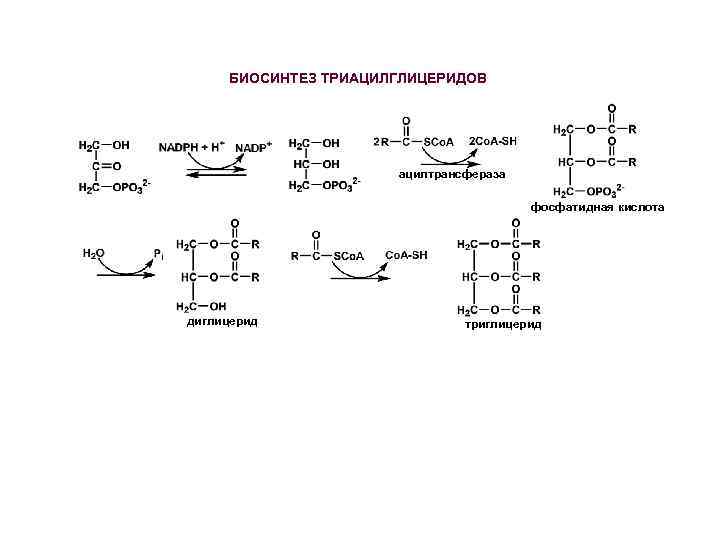
БИОСИНТЕЗ ТРИАЦИЛГЛИЦЕРИДОВ ацилтрансфераза фосфатидная кислота диглицерид триглицерид

ПЕРЕВАРИВАНИЕ И ВСАСЫВАНИЕ ПИЩИ липаза триглицерид + Достаточно полярное соединение, чтобы всасываться эпителиальными клетками Хиломикроны состоят из глицеридов и холестерина, разносятся кровью по всем органам. Атеросклероз На внутренних гладких стенках артерий образуются жироподобные отложения. Они состоят из липидов, холестерина и сложных углеводов. Эти отложения (бляшки) отвердевают по мере накопления ионов кальция, забираемых из протекающей крови. Затвердевшие бляшки частично закупоривают сосуды. Ограничиваю доступ обогащенной кислородом крови к миокарду и могут привести к ишемической болезни сердца (кислородной недостаточности).
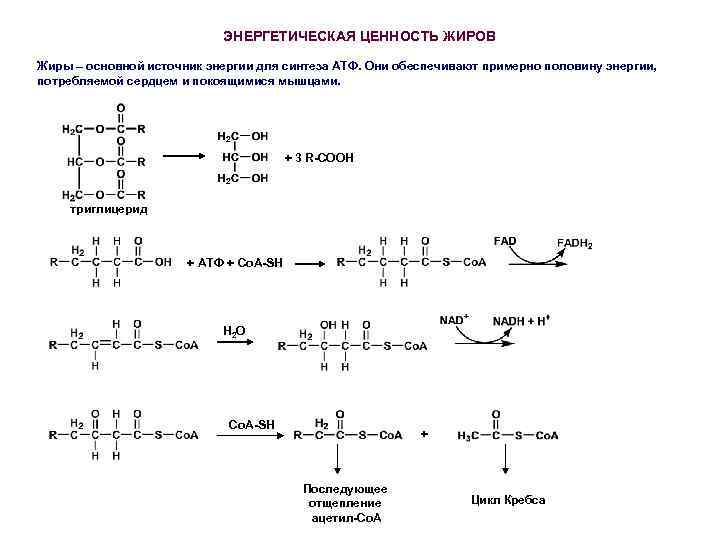
ЭНЕРГЕТИЧЕСКАЯ ЦЕННОСТЬ ЖИРОВ Жиры – основной источник энергии для синтеза АТФ. Они обеспечивают примерно половину энергии, потребляемой сердцем и покоящимися мышцами. + 3 R-COOH триглицерид + АТФ + Со. А-SH H 2 O Со. А-SH + Последующее отщепление ацетил-Со. А Цикл Кребса
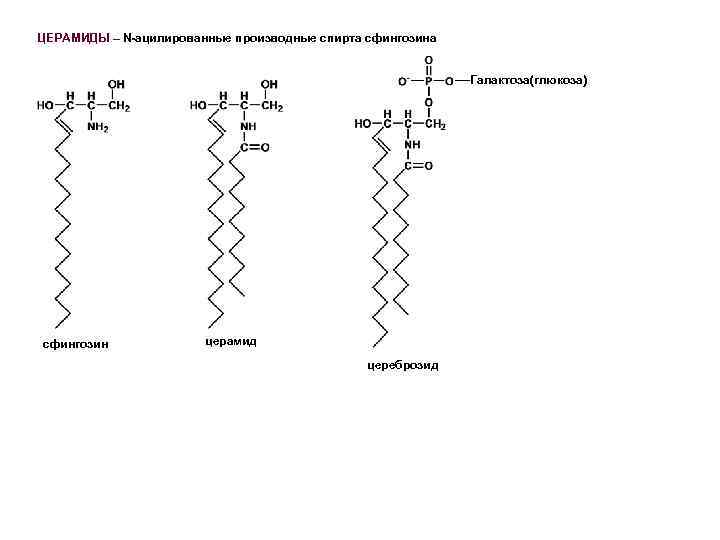
ЦЕРАМИДЫ – N-ацилированные производные спирта сфингозина Галактоза(глюкоза) сфингозин церамид цереброзид
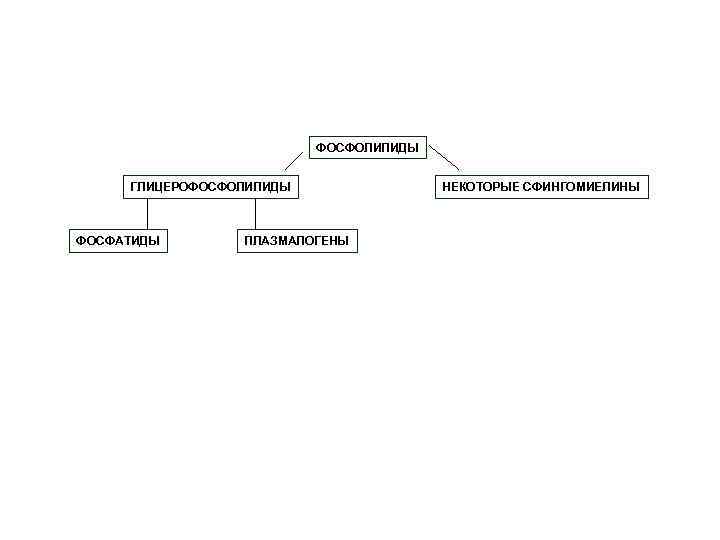
ФОСФОЛИПИДЫ ГЛИЦЕРОФОСФОЛИПИДЫ ФОСФАТИДЫ ПЛАЗМАЛОГЕНЫ НЕКОТОРЫЕ СФИНГОМИЕЛИНЫ
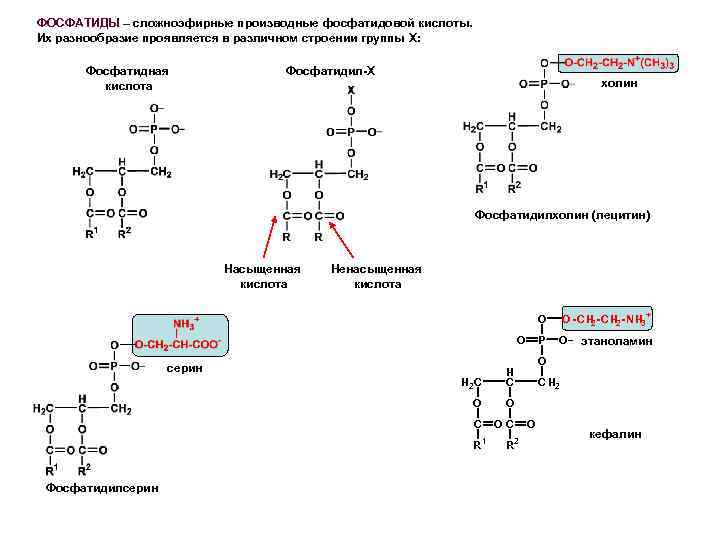
ФОСФАТИДЫ – сложноэфирные производные фосфатидовой кислоты. Их разнообразие проявляется в различном строении группы X: Фосфатидная кислота Фосфатидил-Х холин Фосфатидилхолин (лецитин) Насыщенная кислота Ненасыщенная кислота O P O серин H 2 C O C OC R 1 Фосфатидилсерин O_ этаноламин O H C O O -C H 2 -N H 3+ 2 R 2 C H 2 O кефалин
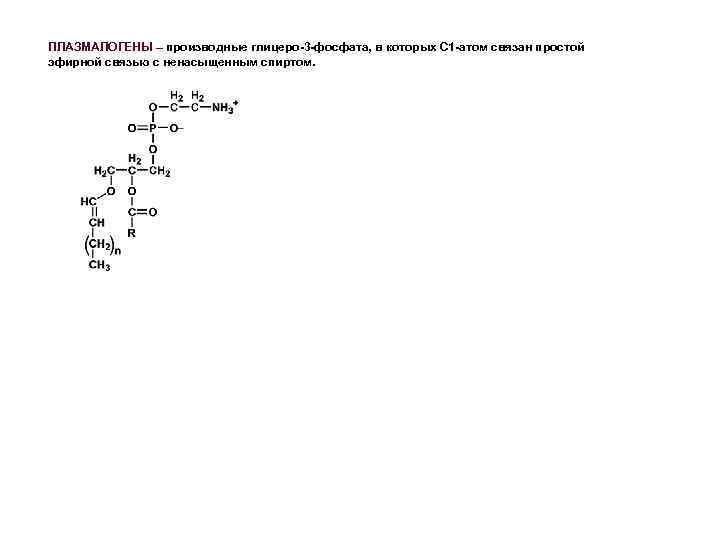
ПЛАЗМАЛОГЕНЫ – производные глицеро-3 -фосфата, в которых С 1 -атом связан простой эфирной связью с ненасыщенным спиртом.
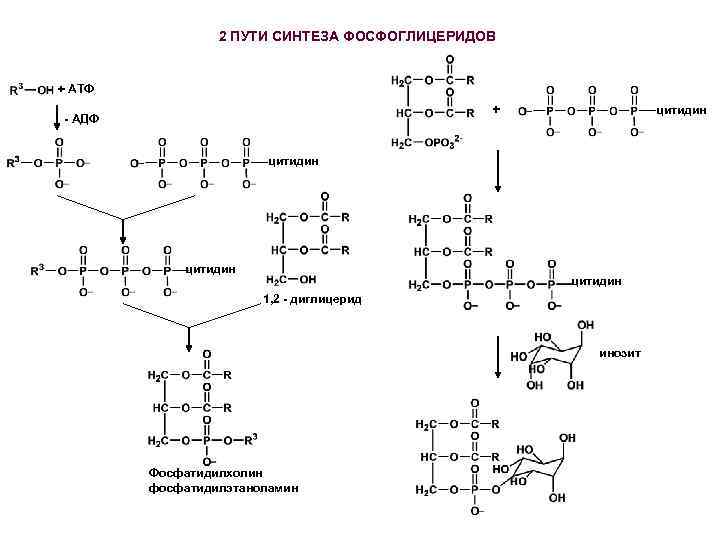
2 ПУТИ СИНТЕЗА ФОСФОГЛИЦЕРИДОВ + АТФ + - АДФ цитидин 1, 2 - диглицерид инозит Фосфатидилхолин фосфатидилэтаноламин
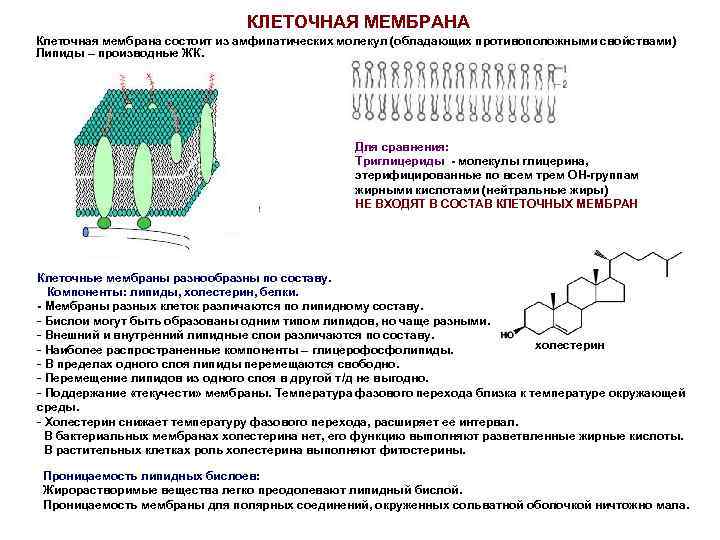
КЛЕТОЧНАЯ МЕМБРАНА Клеточная мембрана состоит из амфипатических молекул (обладающих противоположными свойствами) Липиды – производные ЖК. Для сравнения: Триглицериды - молекулы глицерина, этерифицированные по всем трем OH-группам жирными кислотами (нейтральные жиры) НЕ ВХОДЯТ В СОСТАВ КЛЕТОЧНЫХ МЕМБРАН Клеточные мембраны разнообразны по составу. Компоненты: липиды, холестерин, белки. - Мембраны разных клеток различаются по липидному составу. - Бислои могут быть образованы одним типом липидов, но чаще разными. - Внешний и внутренний липидные слои различаются по составу. холестерин - Наиболее распространенные компоненты – глицерофосфолипиды. - В пределах одного слоя липиды перемещаются свободно. - Перемещение липидов из одного слоя в другой т/д не выгодно. - Поддержание «текучести» мембраны. Температура фазового перехода близка к температуре окружающей среды. - Холестерин снижает температуру фазового перехода, расширяет ее интервал. В бактериальных мембранах холестерина нет, его функцию выполняют разветвленные жирные кислоты. В растительных клетках роль холестерина выполняют фитостерины. Проницаемость липидных бислоев: Жирорастворимые вещества легко преодолевают липидный бислой. Проницаемость мембраны для полярных соединений, окруженных сольватной оболочкой ничтожно мала.
Metabolism.ppt