14. БИОСИНТЕЗ БЕЛКА.ppt
- Количество слайдов: 48

БИОСИНТЕЗ БЕЛКА

ЭТАПЫ БИОСИНТЕЗА 1. Активация аминокислот 2. Инициация полипептидной цепи 3. Элонгация 4. Терминация 5. Сворачивание и процессинг

Этот этап протекает не в рибосоме, а в цитоплазме. Каждая из 20 -и аминокислот ковалентно присоединяется к определённой т-РНК, используя Этот процесс протекает в для этого энергию АТФ. 2 стадии: Активизация происходит под действием определённых ферментов – амино-ацил-т-РНК-синтетаз.
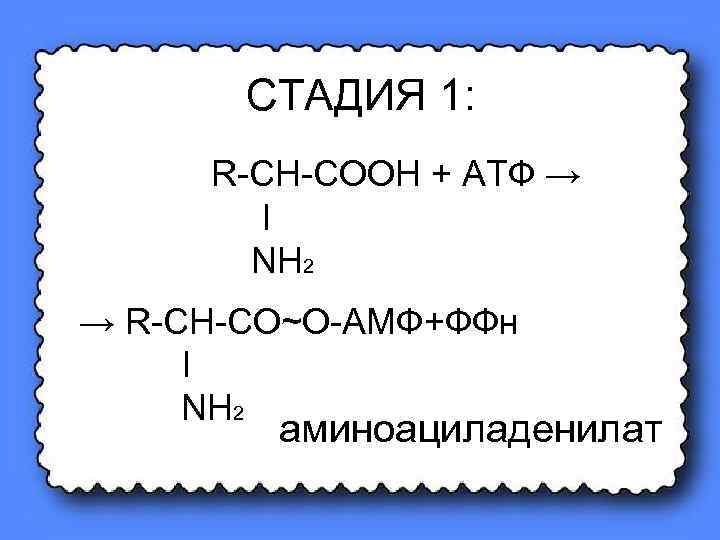
СТАДИЯ 1: R-CH-COOH + АТФ → Ι NH 2 → R-CH-CO~O-AMФ+ФФн Ι NH 2 аминоациладенилат
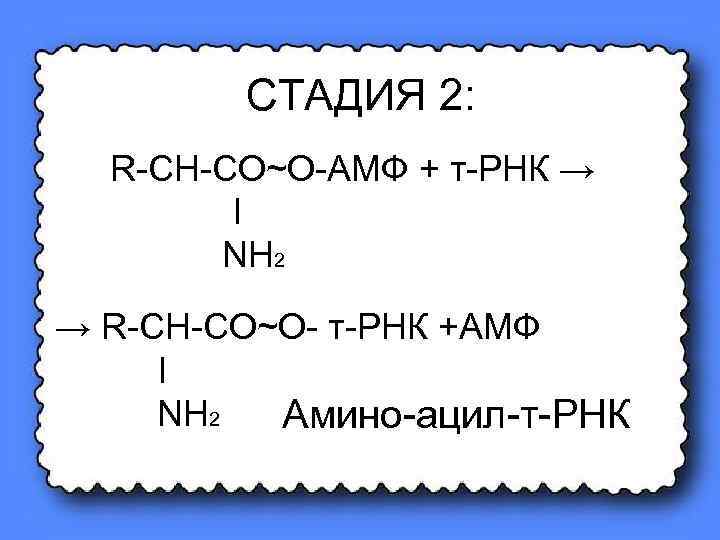
СТАДИЯ 2: R-CH-CO~O-AMФ + т-РНК → Ι NH 2 → R-CH-CO~O- т-РНК +АМФ Ι NH 2 Амино-ацил-т-РНК
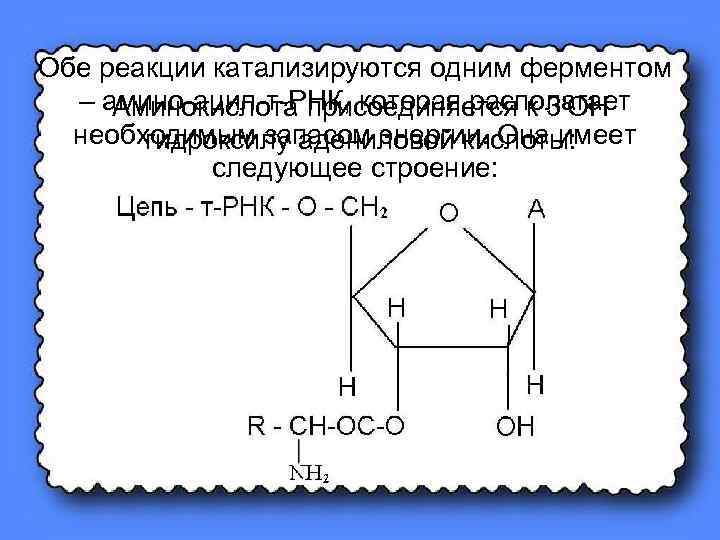
Обе реакции катализируются одним ферментом – амино-ацил-т-РНК, которая располагает Аминокислота присоединяется к 3'ОН необходимым запасом энергии. Она имеет гидроксилу адениловой кислоты: следующее строение:

ЭТАПЫ БИОСИНТЕЗА 1. Активация аминокислот 2. Инициация полипептидной цепи 3. Элонгация 4. Терминация 5. Сворачивание и процессинг

Этот этап биосинтеза белка происходит в рибосоме. Этап является точкой отсчёта синтеза белка. Он требует соблюдения ряда условий, в частности, наличие в системе помимо 70 S или 80 S рибосом, инициаторной амино-ацил-т-РНК, инициирующих кодонов в составе м-РНК и белковых факторов инициации.

CH 2―S―CH 3 N 10–формилтетра. CH 2―S―CH 3 | -гидрофолиевая кислота | CH 2 (N 10 – СНО – ТГФ )→ ТГФ CH 2 | + т-РНК ――――→ ДГФ | CH―NH 2 CH ― NH ― С=О | | COOH CO~О-т-РНК Н Метионин. N-формилметионин-т-РНК -аденилат N-формилметионин-т-РНК является первой амино-ацил-т-РНК, которая определяет включение N-концевого остатка аминокислоты и тем самым начало трансляции.

ИНИЦИАЦИЯ БИОСИНТЕЗА БЕЛКА происходит при наличии трёх белковых факторов инициации: IF 1 IF 2 IF 3 IF 1 стимулирует процесс связывания IF 2 играет центральную рольрибосомы, и фактора IF 2 с 30 S частицей в связывании формилметиониновой т-РНК к ней м-РНК. способствует присоединению с субчасицей 30 S и в гидролизе ГТФ необходим для осуществления инициации биосинтеза белка.

IF 3 вызывает конформационные изменения в 30 S субчастице рибосомы, способствующие связыванию его с формил-метионил-т-РНК. Присоединение последней обеспечивает поступление в рибосомальный аппарат первой N-концевой аминокислоты, а именно – формил -метионина, которым открывается полипептидная цепь любого белка, синтезируемого у бактерий. Именно IF 3 присоединяется первым к 30 S субчастице рибосомы, открывая этап инициации белкового синтеза. IF 3 способствует созданию на субчастице 30 S м-РНК-связывающего центра.
ФАКТОР IF 3

Присоединение IF 1, IF 2 формилметионил-т-РНК и ГТФ к 30 S субчастице осуществляется в виде комплекса. Как только оно произойдёт, к ней присоединяется м-РНК. Причём в результате взаимодействия антикодона формилметиониловой т-РНК с кодоном м-РНК предопределяется такое расположение м-РНК на рибосоме, которое обеспечивает дальнейшее считывание содержащейся в последовательности её нуклеотидных остатков информации о первичной структуре синтезируемого белка.
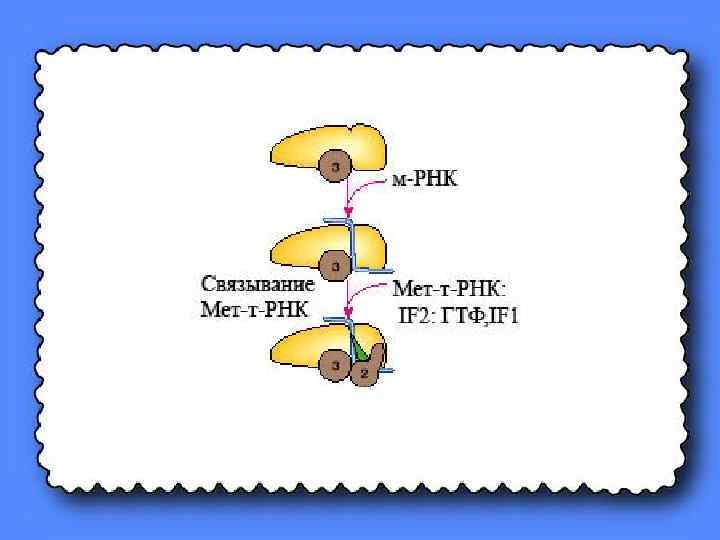

Т. е. именно формилметиониловая-т-РНК помогает м-РНК найти на 30 S субчастице ту позицию, которая необходима для трансляции информации о последовательности аминокислотных остатков в белке.

Присоединение м-РНК к комплексу, состоящему из 30 S субчастицы, факторов инициации и ГТФ сопровождается высвобождением фактора IF 3.
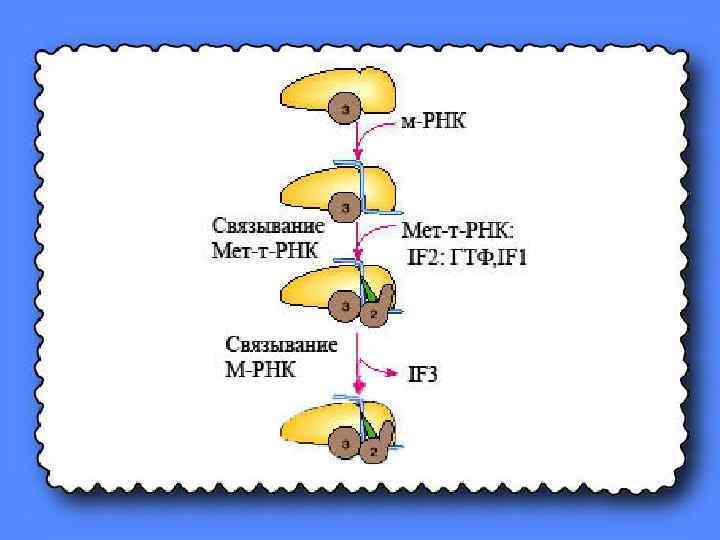

Далее комплекс притягивает 50 S субчастицу и соединяется с ней, образуя 80 S рибосому, причём IF 1 в этот момент покидает рибосому, т. к. он тоже выполнил свою роль – стабилизацию в рибосоме м-РНК.
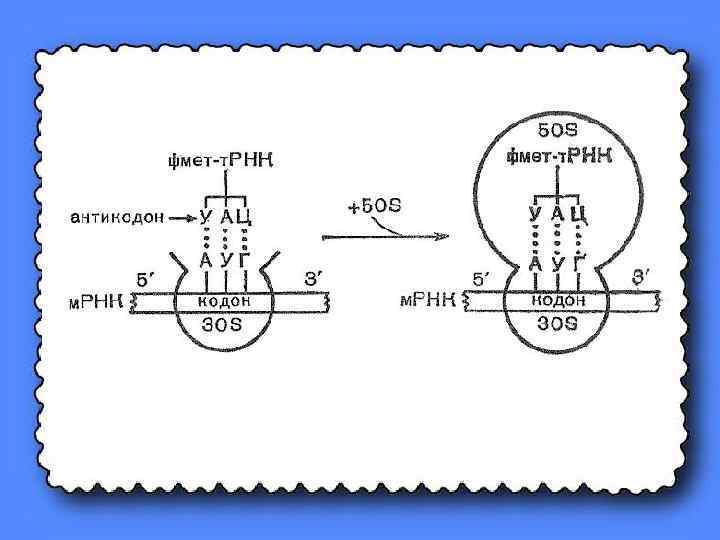
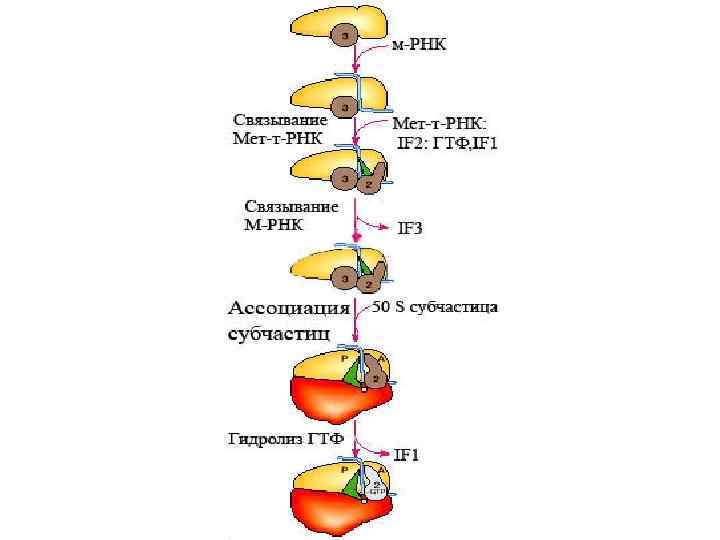

Сохранившийся ещё в возникшей 70 S рибосоме IF 2, связанный с ГТФ, обеспечивает ускорение распада ГТФ на ГДФ и Н 3 РО 4 и высвобождается из рибосомы вместе с продуктами гидролиза ГТФ. Высвободившаяся энергия необходима для сборки белковой молекулы. Такая рибосома называется - -ТРАНСЛИРУЮЩЕЙ.
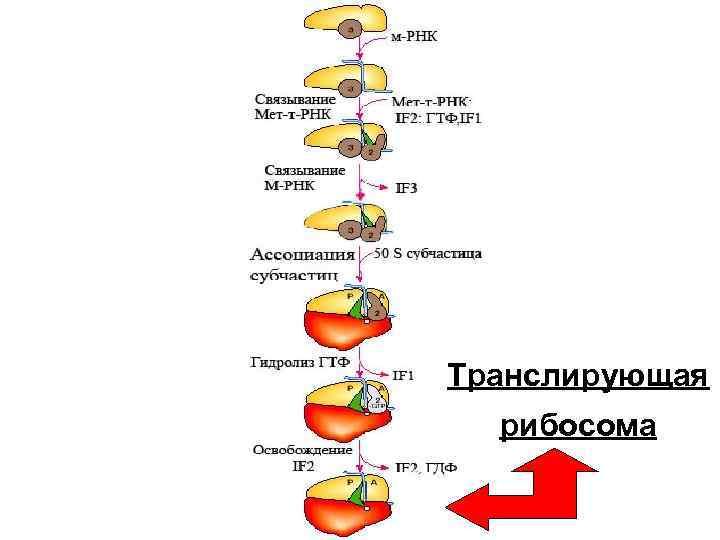
Транслирующая рибосома

Формилметионил-т-РНК из аминоацильного центра перемещается в пептидильный центр рибосомы. У образовавшейся активной рибосомы 70 S, оказывается свободный аминоацильный центр, который может реагировать с определённой амино-ацил-т-РНК в строгом соответствии с очередным кодоном м -РНК.


С этого момента начинается третий этап биосинтеза белка.

ЭТАПЫ БИОСИНТЕЗА 1. Активация аминокислот 2. Инициация полипептидной цепи 3. Элонгация 4. Терминация 5. Сворачивание и процессинг

Этот процесс связан с большой субчастицей (50 S) рибосомы, содержащей два центра для связывания т-РНК: один из них называется аминоацильный, другой – пептидильный. ЭЛОНГАЦИЯ начинается со связывания амино- ацил-т-РНК (аминокислотный остаток которого является вторым с N-конца после формилметионила) с белковыми факторами и присоединению всего комплекса к аминоацильному центру в соответствии с кодовым триплетом м-РНК.


Далее в пептидильном центре осуществляется ферментативная реакция ТРАНСПЕПТИДИРОВАНИЯ – формилметионин переносится на свободную NH 2 -группу амино-ацил-т-РНК, и замыкается первая пептидная связь в будущей полипептидной цепи.
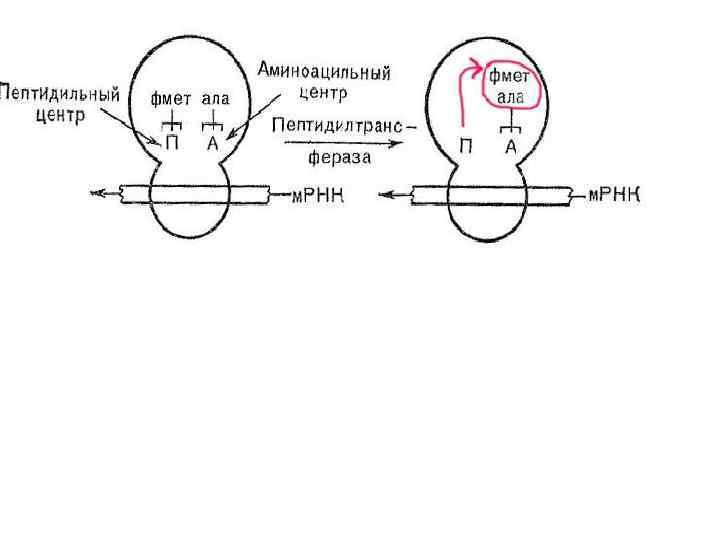

Фермент, катализирующий эту реакцию, получил название пептидил-трансфераза. Для дальнейшего процесса элонгации требуется, чтобы аминоацильный центр был свободным для следующей амино-ацил-т-РНК. Для этого в следующей стадии, благодаря процессу «транслокации» , пептидил-т-РНК переносится из аминоацильного на пептидильный центр.
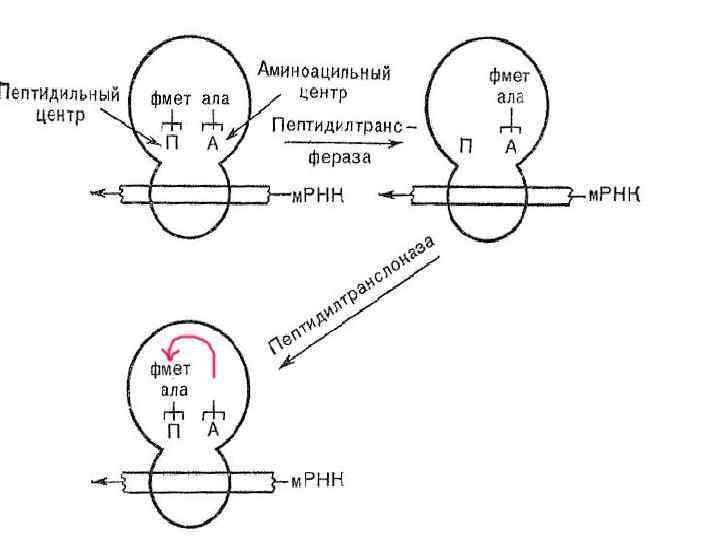

Достигается транслокация благодаря миграции рибосомы относительно м-РНК при участии фермента «ТРАНСЛОКАЗЫ» , фактора EFG у прокариот, и TF 2 у эукариот, а также энергии распада Г Т Ф. В результате транслокации дипептидин-т-РНК занимает место в пептидильном центре рибосомы, а аминоацильный центр, будучи «важнейшим» , может присоединять новую амино-ацил-т-РНК в соответствии с кодоном м-РНК. Параллельно с транслокацией перемещается и м-РНК точно на один триплет.


Таким образом на стадии элонгации происходит последовательное наращивание полипептидной цепи по одной аминокислоте в строгом соответствии с порядком триплетов (кодонов) в молекуле м-РНК.
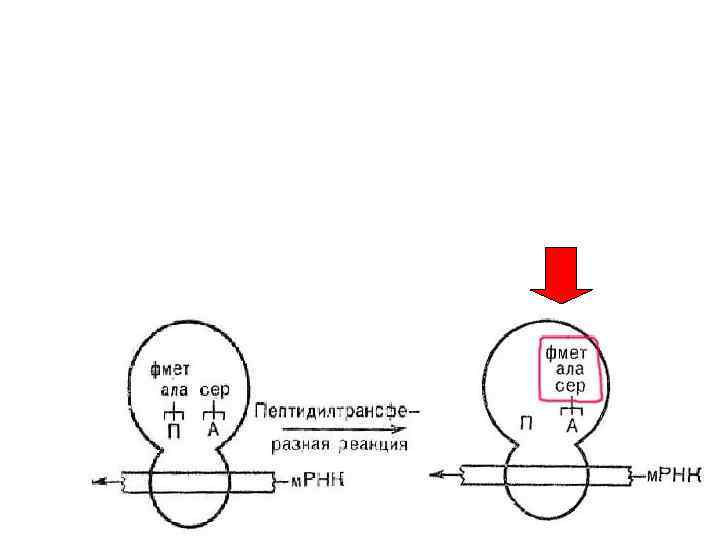

ЭТАПЫ БИОСИНТЕЗА 1. Активация аминокислот 2. Инициация полипептидной цепи 3. Элонгация 4. Терминация 5. Сворачивание и процессинг

Завершение синтеза полипептидной цепи в 70 S рибосоме осуществляется при участии трёх белковых факторов реализации: RF-1, RF-2, RF -3 у прокариот. В клетках животных открыт единственный белок с аналогичным свойством – фактор R. Белковые факторы RF-1 и RF-2 способны распознавать в молекуле матричной РНК терминирующие сборку полипептидной цепи: факторы RF-1 -УАГ и УАА, и фактор RF-2 УАА и УГА. Фактор RF-3 стимулирует действие факторов RF-1 и RF-2.

После того, как терминирующий кодон м-РНК займёт своё место в аминоацильном центре рибосомы, к нему присоединяется один из белковых факторов терминации и блокируется дальнейшая элонгация цепи, тем более, что терминирующему кодону не соответствует ни один из антикодонов в т-РНК. Считается, что терминирующие кодоны и белковые факторы индуцируют пептидилстеразную активность одного или двух рибосомных белков 50 S субчастицы, причём разрывается сложноэфирная связь между синтезированным полипептидом и т-РНК.

Следствием этого является отделение белковой молекулы от рибосомы, освобождение т-РНК и м-РНК. Одновременно 70 S рибосома распадается на две свои субчастицы 30 S и 50 S и они вновь могут быть использованы для синтеза белка.

ЭТАПЫ БИОСИНТЕЗА 1. Активация аминокислот 2. Инициация полипептидной цепи 3. Элонгация 4. Терминация 5. Сворачивание и процессинг

Чтобы принять биологически активную форму, полипептид должен свернуться, образуя определённую пространственную конфигурацию.
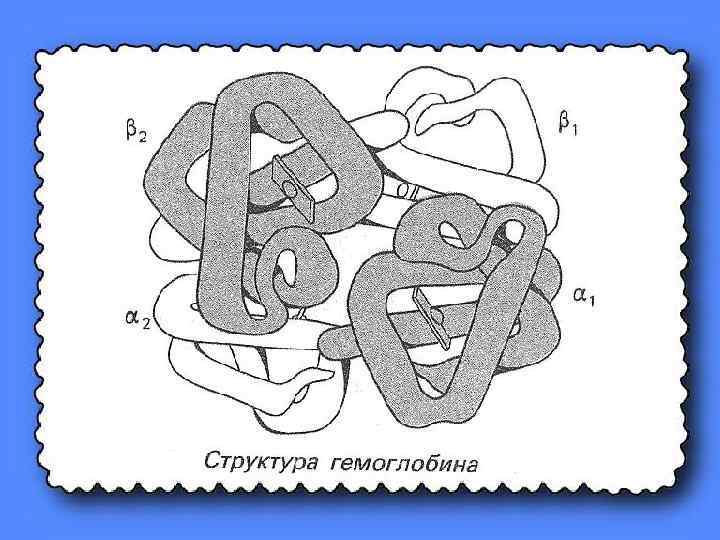

До и после сворачивания новосинтезированный полипептид может претерпевать процессинг, осуществляемый ферментами и заключающийся в следующем: 1)удалении инициирующих аминокислот 2)удалении лишних аминокислотных остатков 3)во введении в определённые аминокислотные остатки фосфатазных, метильных, карбоксильных и др. групп 4)в присоединении простетических групп.

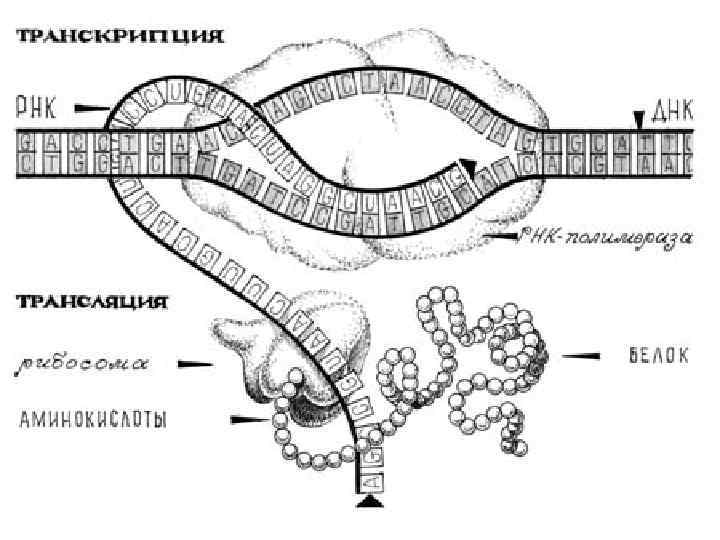
ОБЩАЯ СХЕМА БИОСИНТЕЗА БЕЛКА
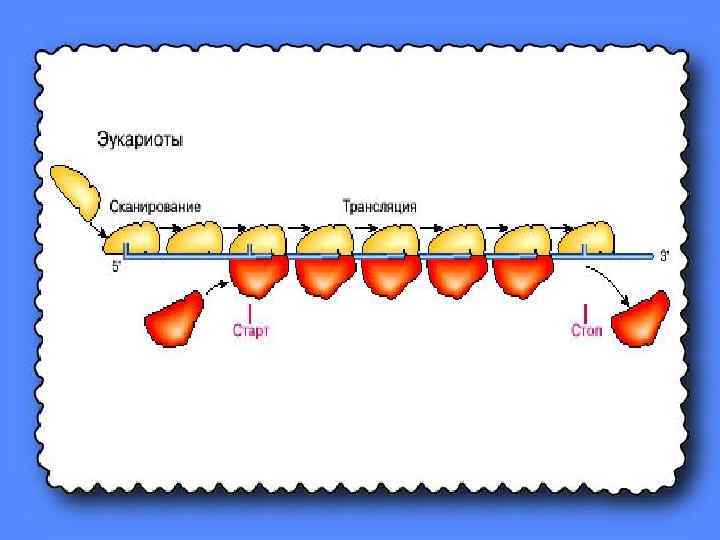
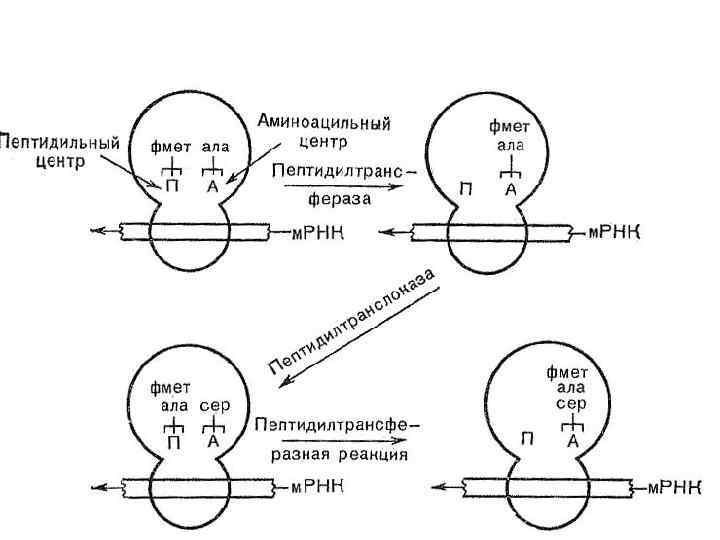
Механизм элонгации
14. БИОСИНТЕЗ БЕЛКА.ppt