Везикулярный транспорт lecture2- endo_and_exocytotic pathways.ppt
- Количество слайдов: 46
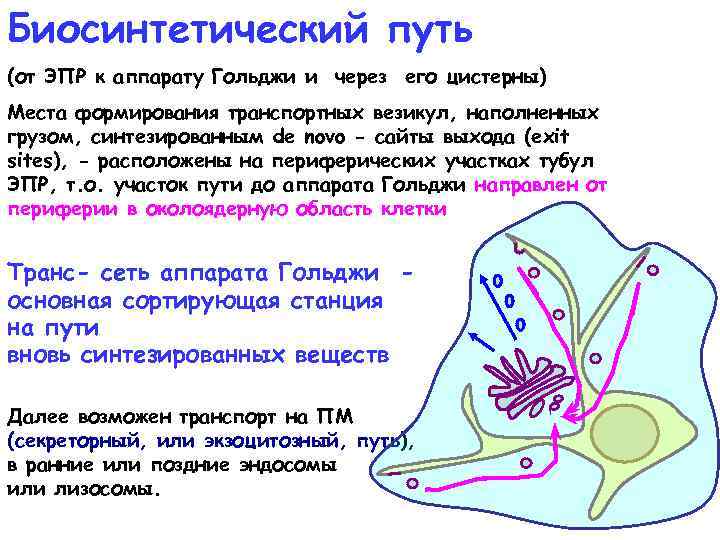
Биосинтетический путь (от ЭПР к аппарату Гольджи и через его цистерны) Места формирования транспортных везикул, наполненных грузом, cинтезированным de novo - cайты выхода (exit sites), - расположены на периферических участках тубул ЭПР, т. о. участок пути до аппарата Гольджи направлен от периферии в околоядерную область клетки Транс- сеть аппарата Гольджи основная сортирующая станция на пути вновь синтезированных веществ Далее возможен транспорт на ПМ (секреторный, или экзоцитозный, путь), в ранние или поздние эндосомы или лизосомы.
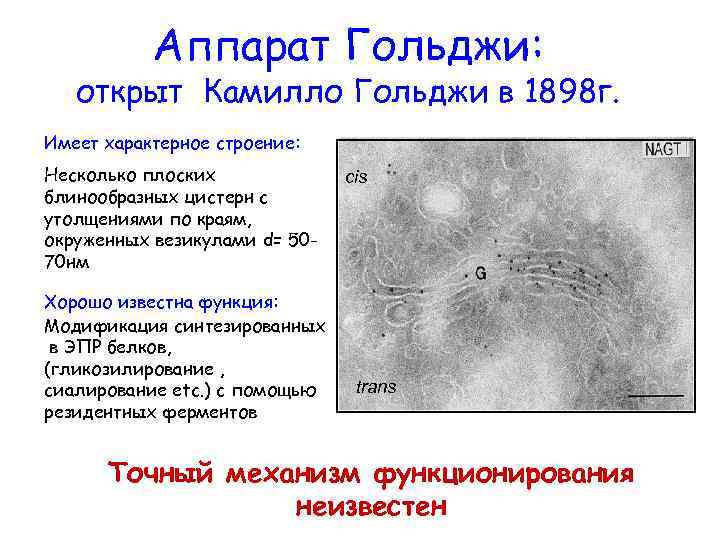
Аппарат Гольджи: открыт Камилло Гольджи в 1898 г. Имеет характерное строение: Несколько плоских блинообразных цистерн с утолщениями по краям, окруженных везикулами d= 5070 нм Хорошо известна функция: Модификация синтезированных в ЭПР белков, (гликозилирование , сиалирование etc. ) с помощью резидентных ферментов cis trans Точный механизм функционирования неизвестен
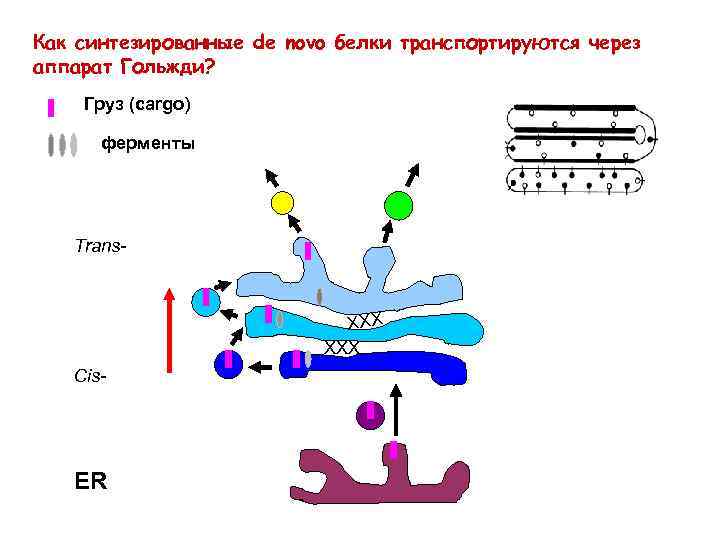
Как синтезированные de novo белки транспортируются через аппарат Гольжди? Груз (cargo) ферменты Trans- ХХХ Cis- ER
Гипотеза 1 • Груз едет – ферменты остаются; • Перенос материала идет от cis- к trans-цистерне с помощью пузырьков Аппарат Гольджи – стабильный, предсуществующий компартмент
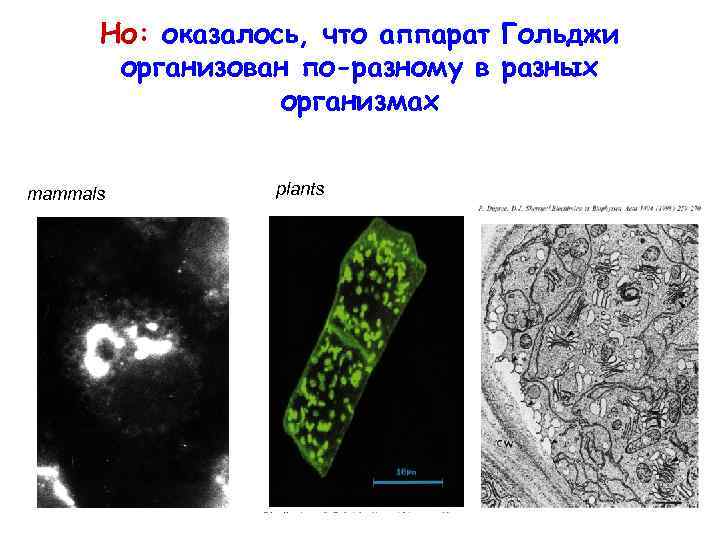
Но: оказалось, что аппарат Гольджи организован по-разному в разных организмах plants mammals ERD 2
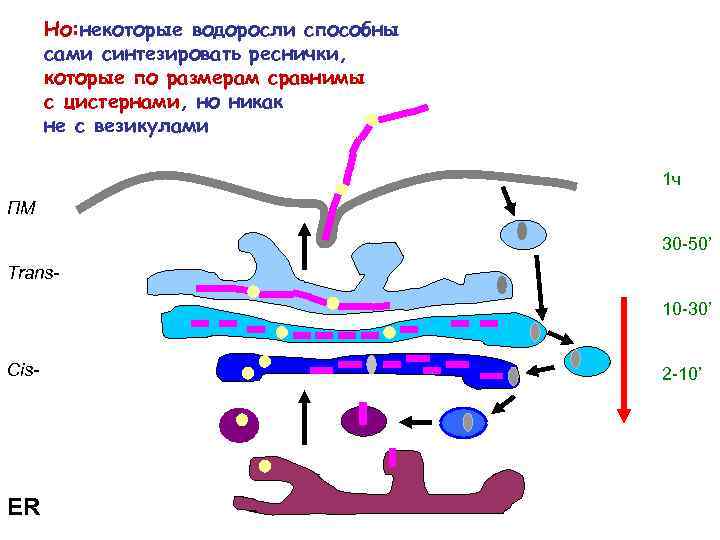
Но: некоторые водоросли способны сами синтезировать реснички, которые по размерам сравнимы с цистернами, но никак не с везикулами 1 ч ПМ 30 -50’ Trans 10 -30’ Cis- ER 2 -10’
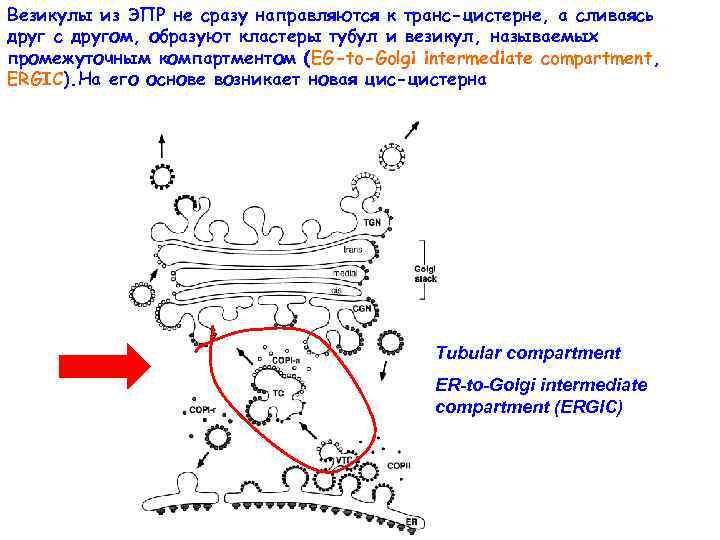
Везикулы из ЭПР не сразу направляются к транс-цистерне, а сливаясь друг с другом, образуют кластеры тубул и везикул, называемых промежуточным компартментом (EG-to-Golgi intermediate compartment, ERGIC). На его основе возникает новая цис-цистерна Tubular compartment ER-to-Golgi intermediate compartment (ERGIC)

Гипотеза 2 - созревания Груз неподвижен - путешествуют резидентные белки Таким образом, сам состав мембран цистерны постепенно изменяется, или цистерна «созревает» Аппарат Гольжди высокодинамичен, постоянно формируется de novo

А на самом деле? • Оказалось, что половина везикул содержит преимущественно груз, половина - преимущественно резидентные белки Крупные белковые аггрегаты секретируются приблизительно за час Обычные белки – за 5 -15 мин Реализуются оба пути
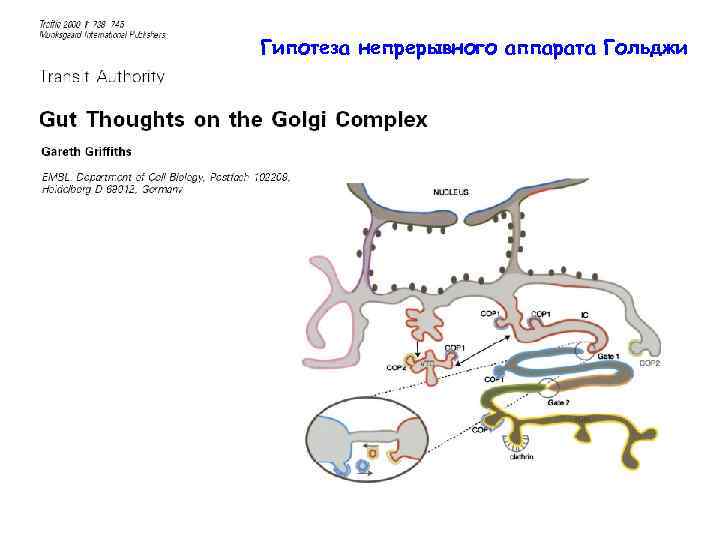
Гипотеза непрерывного аппарата Гольджи
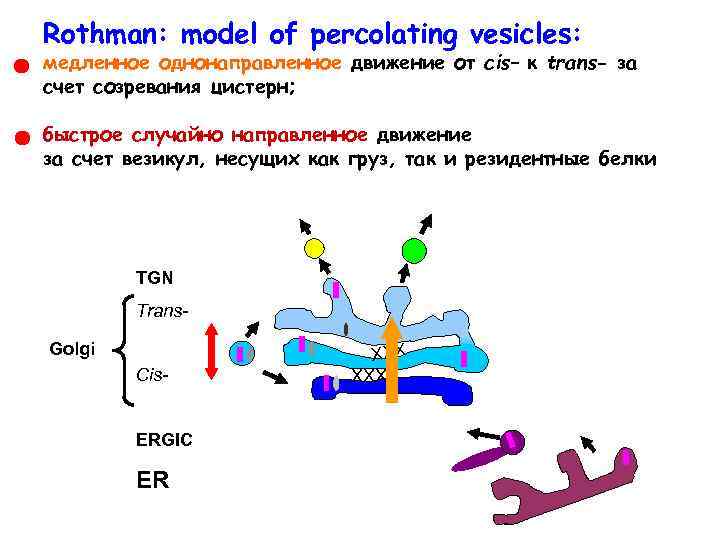
Rothman: model of percolating vesicles: медленное однонаправленное движение от cis– к trans- за счет созревания цистерн; быстрое случайно направленное движение за счет везикул, несущих как груз, так и резидентные белки TGN Trans. Golgi Cis. ERGIC ER ХХХ

Аппарат Гольджи очень сложно организован Трехмерная компьютерная модель: Marsh, Howell The mammalian Golgi – complex debates (Nature Rev. Mol. Cell. Biol. , 2002, v. 3)
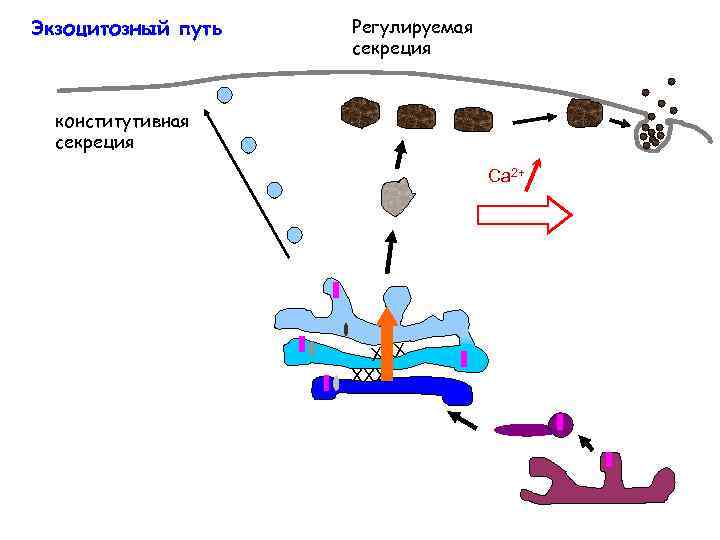
Экзоцитозный путь Регулируемая секреция конститутивная секреция Ca 2+ ХХХ

Эндоцитозный путь – это путь попадания макромолекул извне внутрь клетки, противоположен экзоцитозному Главная сортирующая станция – ранние эндосомы Из них возможны различные «выходы» Рециклирование обратно на ПМ, попадание в поздние эндосомы и затем в лизосомы (путь лизосомной деградации), В транс-Гольджи трансцитоз
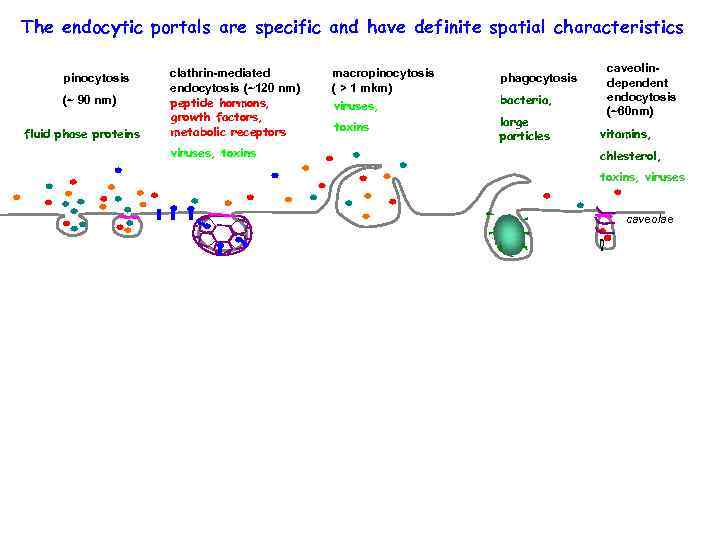
The endocytic portals are specific and have definite spatial characteristics pinocytosis (~ 90 nm) fluid phase proteins clathrin-mediated endocytosis (~120 nm) peptide hormons, growth factors, metabolic receptors macropinocytosis ( > 1 mkm) phagocytosis bacteria, viruses, large particles toxins viruses, toxins caveolindependent endocytosis (~60 nm) vitamins, chlesterol, toxins, viruses caveolae caveosome recycling early endosome phagosome ? late endosome Golgi lysosome secondary lysosome ER
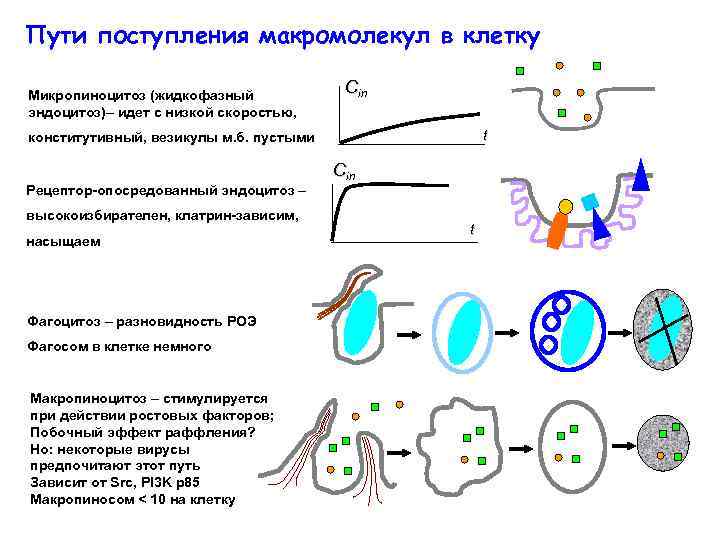
Пути поступления макромолекул в клетку Микропиноцитоз (жидкофазный эндоцитоз)– идет с низкой скоростью, Сin t конститутивный, везикулы м. б. пустыми Рецептор-опосредованный эндоцитоз – высокоизбирателен, клатрин-зависим, насыщаем Фагоцитоз – разновидность РОЭ Фагосом в клетке немного Макропиноцитоз – стимулируется при действии ростовых факторов; Побочный эффект раффления? Но: некоторые вирусы предпочитают этот путь Зависит от Src, PI 3 K p 85 Макропиносом < 10 на клетку Сin t
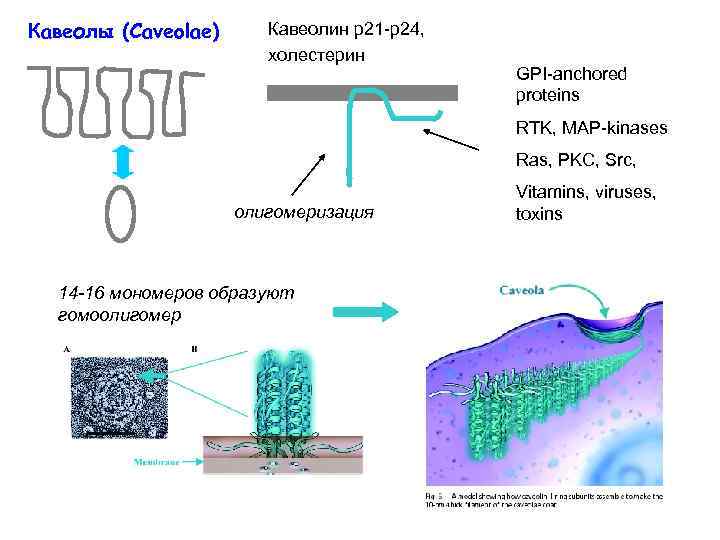
Кавеолы (Caveolae) Кавеолин р21 -р24, холестерин GPI-anchored proteins RTK, MAP-kinases Ras, PKC, Src, олигомеризация 14 -16 мономеров образуют гомоолигомер Vitamins, viruses, toxins
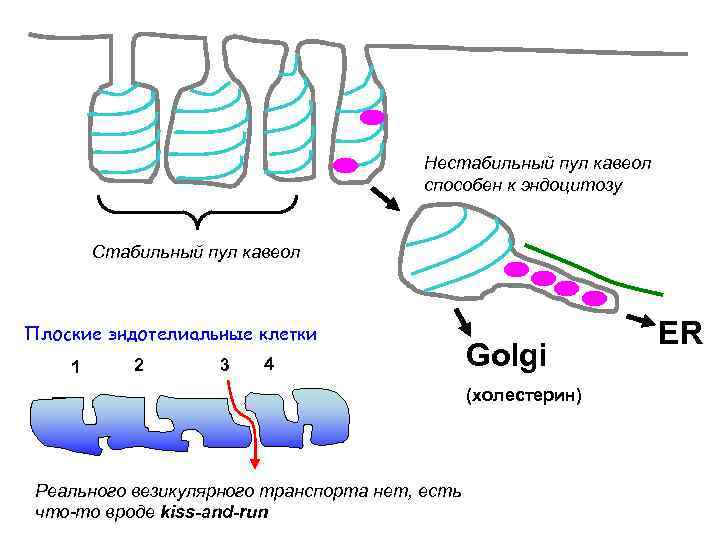
Нестабильный пул кавеол способен к эндоцитозу Cтабильный пул кавеол Плоские эндотелиальные клетки 1 2 3 4 Golgi (холестерин) Реального везикулярного транспорта нет, есть что-то вроде kiss-and-run ER

Фагоцитоз, макропиноцитоз, кавеолин-зависимый путь осуществляются только в клетках определенного типа или в определенных обстоятельствах; РОЭ и микропиноцитоз есть свойство всех без исключения клеток

При микропиноцитозе – более 90 % поглощенного материала рециклирует , 10% - идет на деградацию в лизосомы При РОЭ судьба поглощенных молекул (лигандов, L) и их рецепторов (R) различна Лиганды метаболических рецепторов ( асиалогликопротеины, LDL, трансферрин, etc. ) Пептидные гормоны и ростовые факторы (инсулин, EGF, FGF, PDGF etc) L деградация в лиз LR R рециклирование деградация в лиз LR переносчики, каналы LR рециклирование LR интернализуются, могут образовывать внутриклеточное «депо» и при внешнем сигнале встраиваться обратно, а могут доставляться в лизосомы ряд трансмембранных белков (гидролазы, липазы, Lgp, Lamp работают в лизосомах
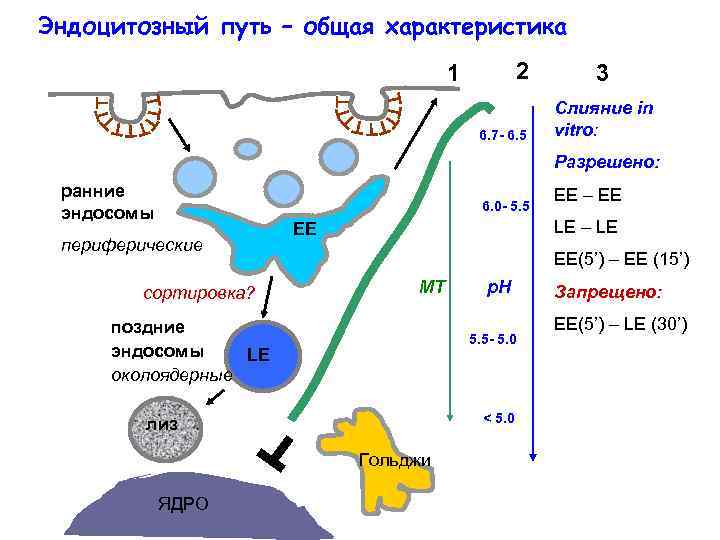
Эндоцитозный путь – общая характеристика 2 1 6. 7 - 6. 5 3 Слияние in vitro: Разрешено: ранние эндосомы 6. 0 - 5. 5 периферические сортировка? LE – LE EE EE(5’) – EE (15’) МТ поздние эндосомы LE околоядерные р. Н 5. 5 - 5. 0 < 5. 0 лиз Гольджи ЯДРО EE – EE Запрещено: EE(5’) – LE (30’)
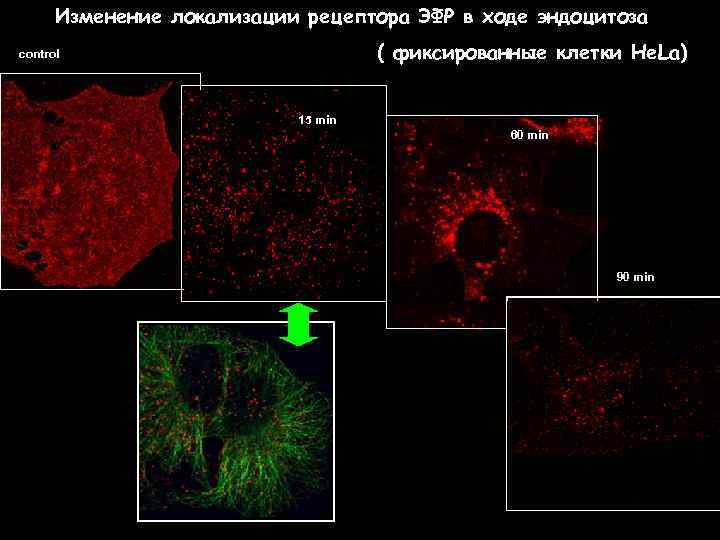
Изменение локализации рецептора ЭФР в ходе эндоцитоза ( фиксированные клетки He. La) control 15 min 60 min 90 min

Эндоцитозный путь: Где граница между РЭ и ПЭ? Как и где груз переходит из РЭ в ПЭ? Где на эндоцитозном пути конмпарменты, а где – транспортные везикулы? Какова функция МВТ и их место на эндоцитозном пути? Каков механизм сортировки (на рециклирование или деградацию? ) Как груз попадает в лизосомы? Где происходит деградация интернализованных молекул?
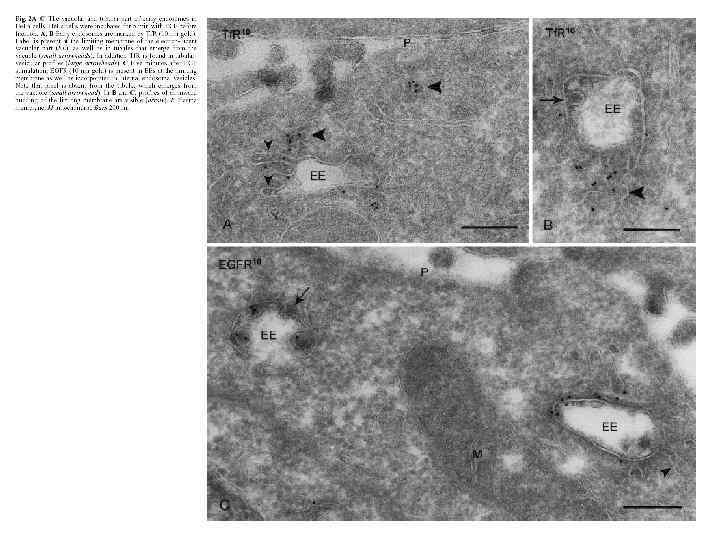
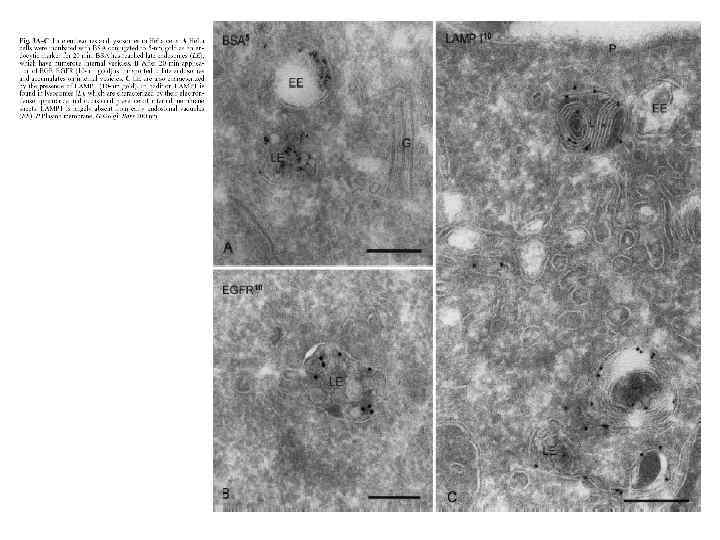
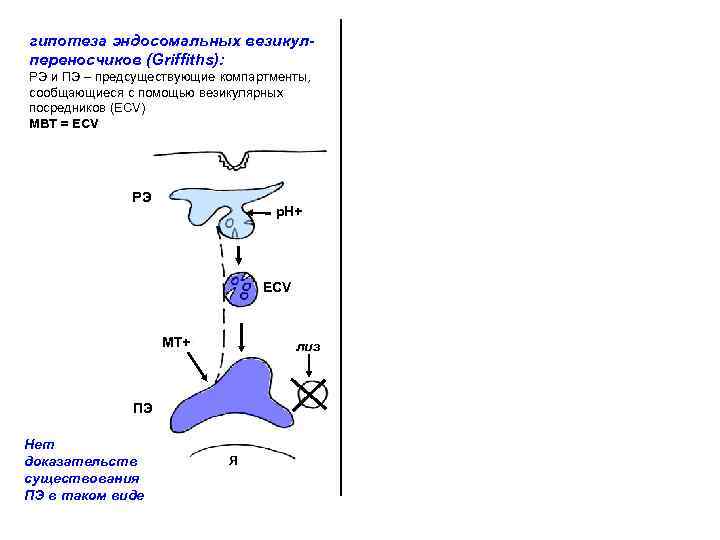
гипотеза эндосомальных везикулпереносчиков (Griffiths): РЭ и ПЭ – предсуществующие компартменты, сообщающиеся с помощью везикулярных посредников (ECV) МВТ = ECV теория созревания эндосом (Murphy): РЭ превращаются в ПЭ за счет постепенного изменения состава мембран МВТ = ПЭ ПМ РЭ р. Н+ ECV МТ+ лиз ПЭ Нет доказательств существования ПЭ в таком виде сеть транс. Гольджи Я лиз Я
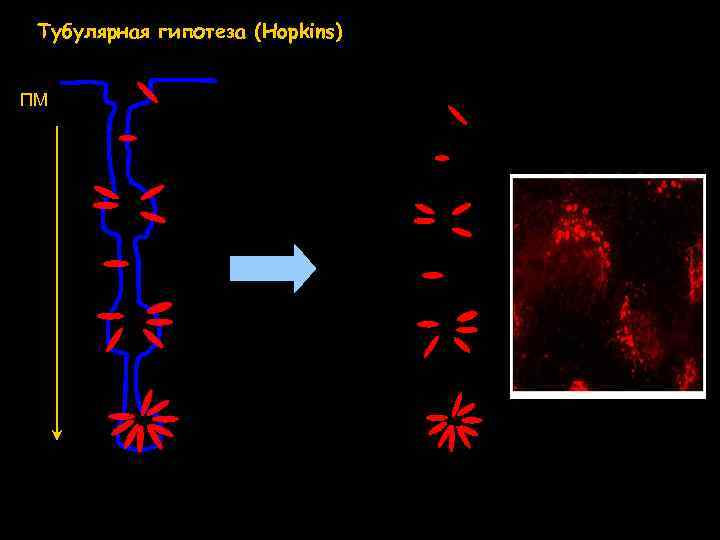
Тубулярная гипотеза (Hopkins) ПМ

Невозможность перехода ЭФР-Р в ПЭ не препятствует его накоплению в околоядерной области в составе везикулпредшественников МВТ ЭФР-ФЭ 15 мин 37 о. С ЭФР-ПХ, N ЭФР-ФЭ 15 мин 37 о. С, 3 ч 18 о. С
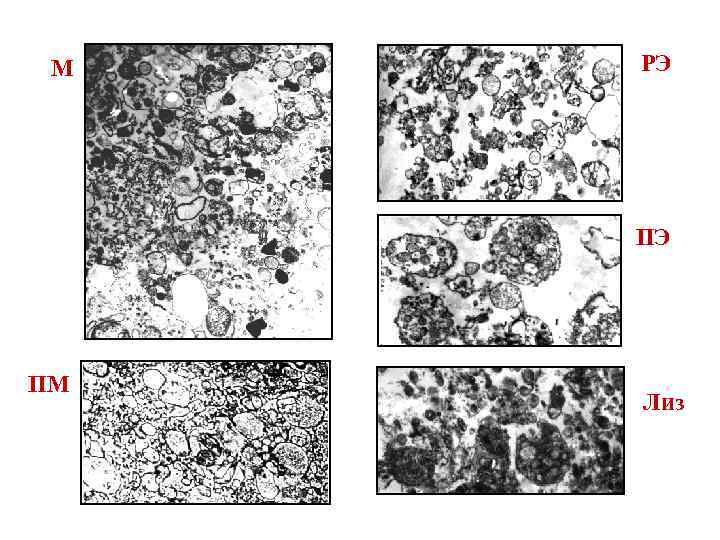
М РЭ ПЭ ПМ Лиз

• Слияния происходят постоянно (но редко) на эндоцитозном пути, за счет укрупнения эндосом создается «избыток мембраны» , из которого формируются внутренние пузырьки МВТ • Закисление эндосом существенно не только для активации лизосомных ферментов, но и для регуляции слияний эндосом • Закисление происходит благодаря работе везикулярной протонной помпы Vo/V 1. • В мембранах эндосом присутствуют несколько типов Са 2+-каналов, р. Н-чувствительных и р. Ннечувствительных, они регулируют локальные изменения уровня кальция, необходимого для слияний Bafilomycin A 1 (Baf. A 1) -ингибитор везикулярной протонной помпы Два нативных лиганда рецептора ЭФР : ЭФР – диссоциирует при р. Н <5. 0 ; деградирует в лизосомах TGFalpha- диссоциирует при р. Н 6. 0, рециклирует
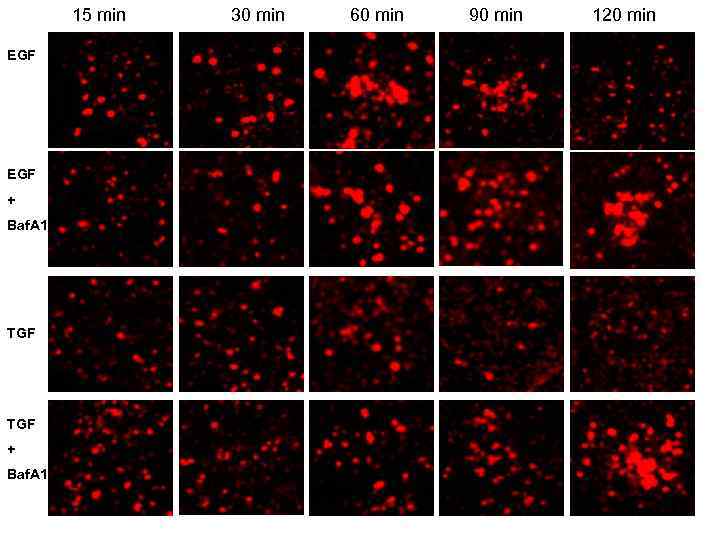
15 min EGF + Baf. A 1 TGF + Baf. A 1 30 min 60 min 90 min 120 min
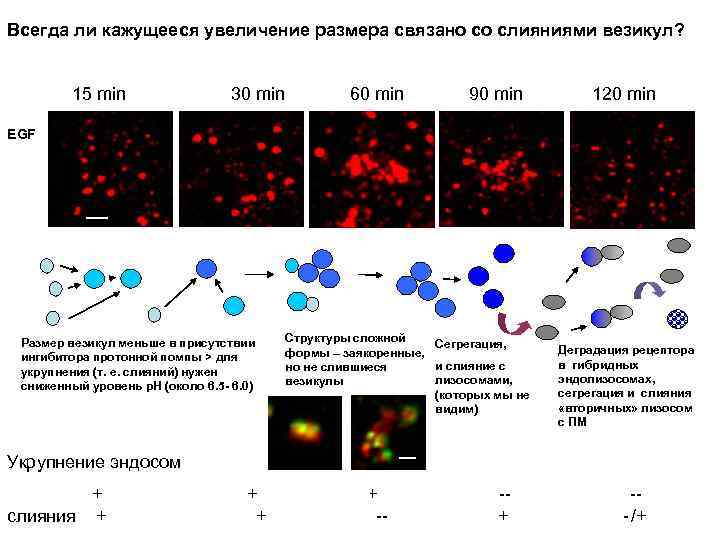
Всегда ли кажущееся увеличение размера связано со слияниями везикул? 15 min 30 min 60 min 90 min 120 min EGF Размер везикул меньше в присутствии ингибитора протонной помпы > для укрупнения (т. е. слияний) нужен сниженный уровень р. Н (около 6. 5 - 6. 0) Структуры сложной Сегрегация, формы – заякоренные, и слияние с но не слившиеся лизосомами, везикулы (которых мы не видим) Деградация рецептора в гибридных эндолизосомах, сегрегация и слияния «вторичных» лизосом с ПМ Укрупнение эндосом + слияния + + -- -+ --/+
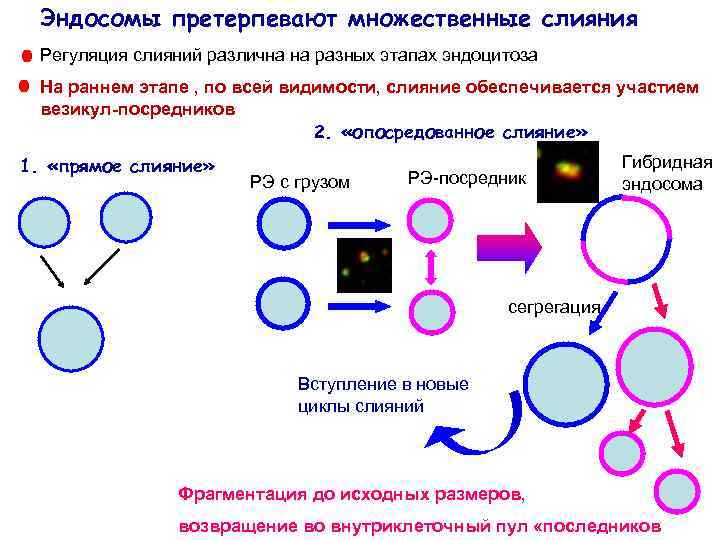
Эндосомы претерпевают множественные слияния Регуляция слияний различна на разных этапах эндоцитоза На раннем этапе , по всей видимости, слияние обеспечивается участием везикул-посредников 2. «опосредованное слияние» 1. «прямое слияние» РЭ с грузом РЭ-посредник Гибридная эндосома сегрегация Вступление в новые циклы слияний Фрагментация до исходных размеров, возвращение во внутриклеточный пул «последников
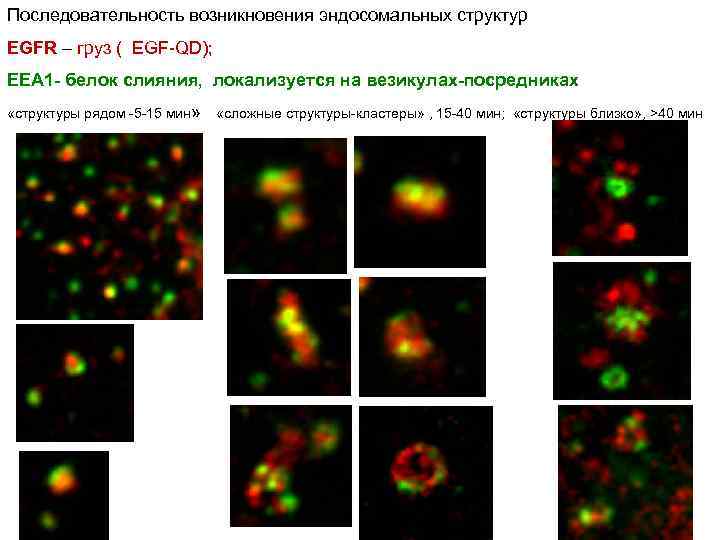
Последовательность возникновения эндосомальных структур EGFR – груз ( EGF-QD); EEA 1 - белок слияния, локализуется на везикулах-посредниках «структуры рядом -5 -15 мин» «сложные структуры-кластеры» , 15 -40 мин; «структуры близко» , >40 мин
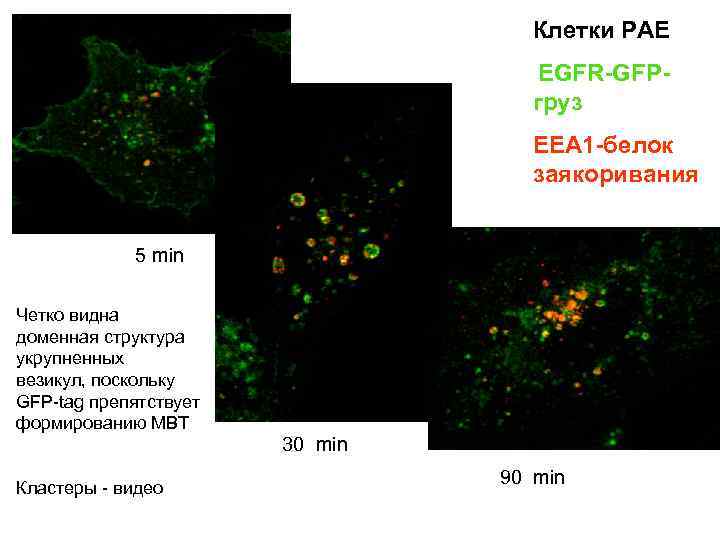
Клетки РАЕ EGFR-GFPгруз EEA 1 -белок заякоривания 5 min Четко видна доменная структура укрупненных везикул, поскольку GFP-tag препятствует формированию МВТ 30 min Кластеры - видео 90 min

Функция везикул-посредников – предоставить все белки, необходимые для правильных слияний тех пузырьков, которые несут только груз, и лишены этой машинерии. Строго говоря, если имеется пул долгоживущих структур, выполняющих определенную функцию и обладающих специфическим составом, то такие структуры являются компартментом. В случае эндоцитоза везикулы-посредники и являются ранним эндосомальным компартментом, представленным набором везикул , обеспечивающих определенное преобразование груза ( его сортировку и упаковку направляемых на деградацию в лизосомы молекул во внутренние пузырьки) эта гипотеза объединяет и гипотезу везикулпереносчиков, и гипотезу созревания

«Ранние эндосомы» не обязательно расположены на периферии клетки Они могут локализоваться и в околоядерной области, МВТ начинают формироваться, как только будет превышен «лимит мембраны» домена, содержащего груз, хотя локализация эндосомы и начало формирования внутренних пузырьков не коррелируют. Более того, это происходит ДО сегрегации ЕЕА 1 - и рецепторобогащенных доменов
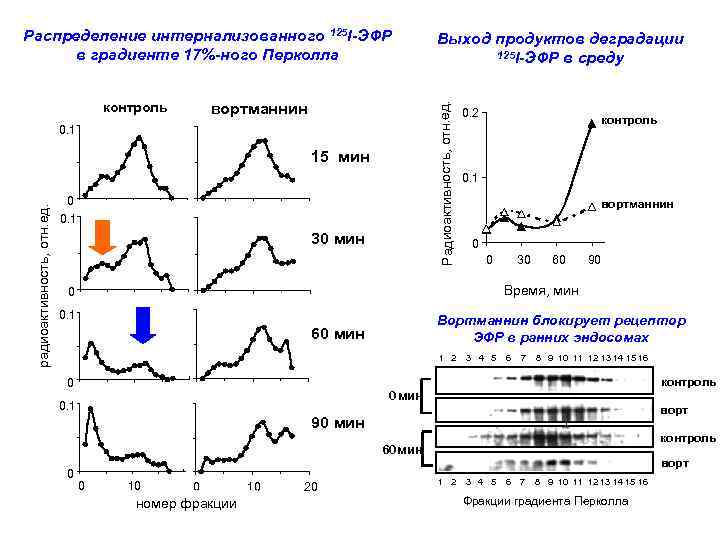
контроль вортманнин 0. 1 15 мин радиоактивность, отн. ед. Выход продуктов деградации 125 I-ЭФР в среду Радиоактивность, отн. ед. Распределение интернализованного 125 I-ЭФР в градиенте 17%-ного Перколла 0 0. 1 30 мин 0. 2 контроль 0. 1 вортманнин 0 0 30 60 90 Время, мин 0 0. 1 Вортманнин блокирует рецептор ЭФР в ранних эндосомах 60 мин 1 2 0 3 4 5 6 7 8 9 10 11 12 13 14 15 16 контроль 0 мин 0. 1 ворт 90 мин контроль 60 мин 0 0 10 0 номер фракции 10 20 ворт 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Фракции градиента Перколла
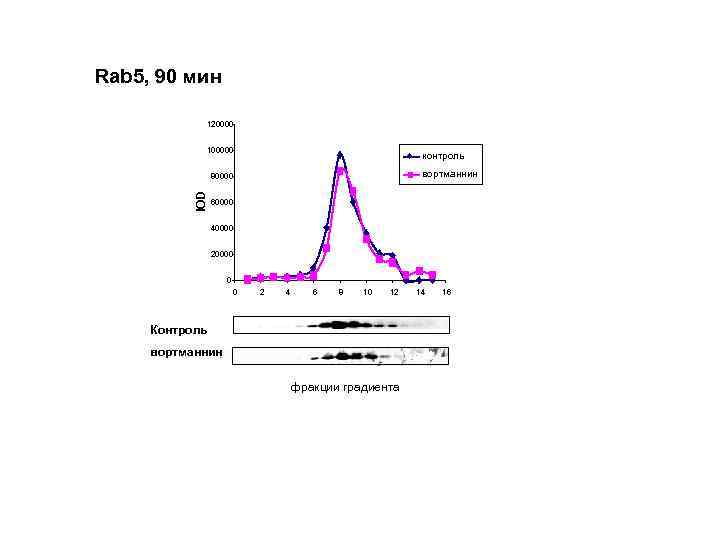
Rab 5, 90 мин 120000 100000 контроль вортманнин IOD 80000 60000 40000 20000 0 0 2 4 6 8 10 12 Контроль вортманнин фракции градиента 14 16
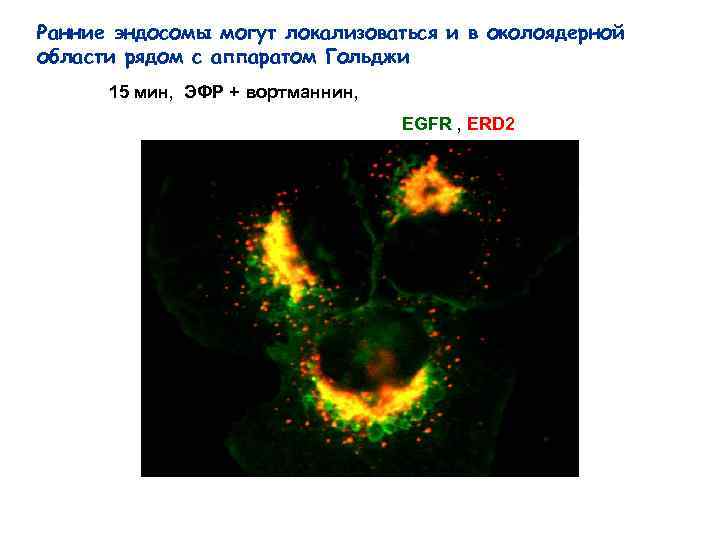
Ранние эндосомы могут локализоваться и в околоядерной области рядом с аппаратом Гольджи 15 мин, ЭФР + вортманнин, EGFR , ERD 2

Если следить за эндоцитозом «с точки зрения груза» , то наиболее вероятной является гипотеза созревания; МВТ и есть поздние эндосомы Поздние эндосомы возникают из ранних в результате множественных слияний на ранних стадиях эндоцитоза и формирования внутренних пузырьков на поздних стадиях. Одновременно их свойства постепенно изменяются как за счет слияния с везикулами из TGN, так и за счет рециклирования части мембран. Однако, учитывая наличие везикул-посредников, можно считать, что эндосомы с грузом – это транспортные пузырьки, идущие от одного предсуществующего (но везикулярного) компартмента к другому. Тогда именно везикулыпосредники и являются истинными эндосомами
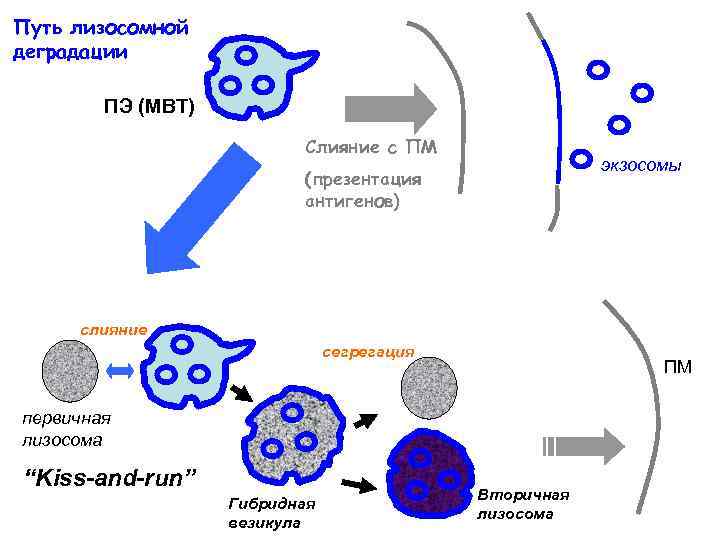
Путь лизосомной деградации ПЭ (МВТ) Слияние с ПМ экзосомы (презентация антигенов) слияние сегрегация ПМ первичная лизосома “Kiss-and-run” Гибридная везикула Вторичная лизосома
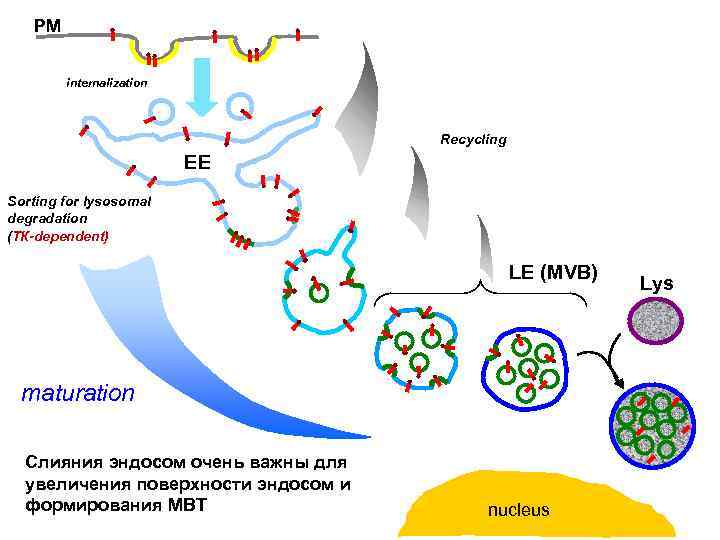
PM internalization Recycling EE Sorting for lysosomal degradation (ТК-dependent) LE (МVB) maturation Слияния эндосом очень важны для увеличения поверхности эндосом и формирования МВТ nucleus Lys

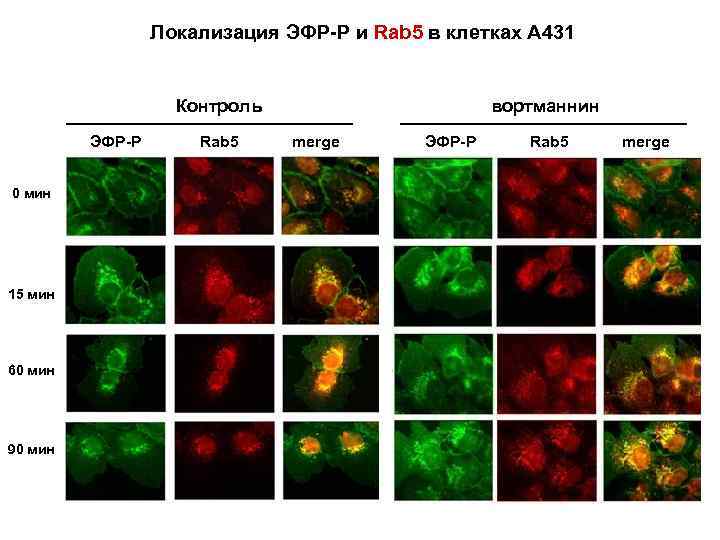
Локализация ЭФР-Р и Rab 5 в клетках А 431 Контроль ЭФР-Р 0 мин 15 мин 60 мин 90 мин Rab 5 вортманнин merge ЭФР-Р Rab 5 merge
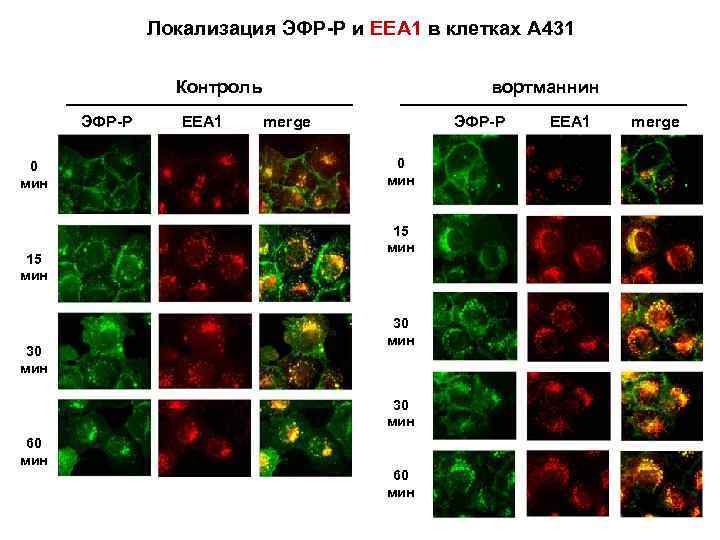
Локализация ЭФР-Р и ЕЕА 1 в клетках А 431 Контроль ЭФР-Р 0 мин 15 мин 30 мин ЕЕА 1 вортманнин merge ЭФР-Р 0 мин 15 мин 30 мин 60 мин ЕЕА 1 merge
Везикулярный транспорт lecture2- endo_and_exocytotic pathways.ppt