Биороль воды.ppt
- Количество слайдов: 35

БИОРОЛЬ ВОДЫ КАК УНИВЕРСАЛЬНОГО РАСТВОРИТЕЛЯ И УЧАСТНИКА БИОХИМИЧЕСКИХ ПРОЦЕССОВ
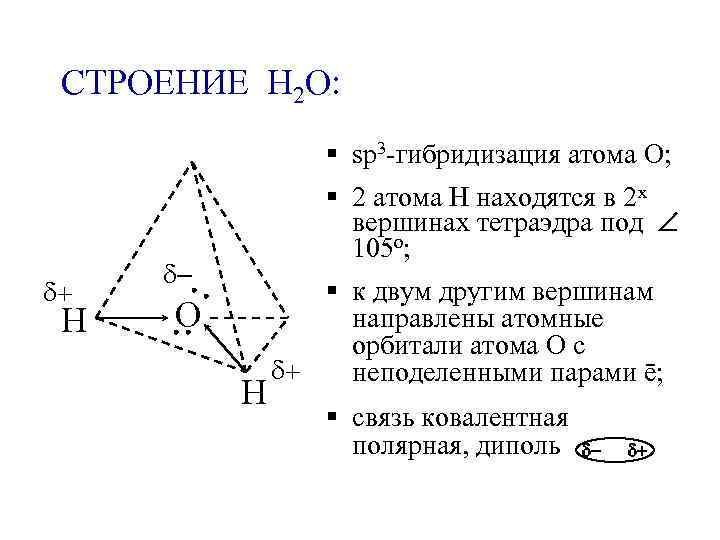
СТРОЕНИЕ H 2 O: § sp 3 -гибридизация атома О; d+ H § 2 атома Н находятся в 2 х вершинах тетраэдра под 105 о; d- O H § к двум другим вершинам направлены атомные орбитали атома О с d+ неподеленными парами ē; § связь ковалентная полярная, диполь d- d+

СВОЙСТВА H 2 O: § АМФОТЕРНОСТЬ: + - + HOH H + OH , донор H , слабая кислота + + + H 2 O + H H 3 O , акцептор H , слабое основание § наличие H-связи, влияющей на аномально Т кип и Тзам воды и ее строение в т-, ж-, гсостоянии.

• У льда каждая молекула Н 2 О может образовывать 4 Н-связи с соседними молекулами Н 2 О в виде трехмерного каркаса с пустотами внутри, льда < Н 2 О(ж). • При плавлении льда часть Н-связей разрывается и появляются свободные молекулы Н 2 О и ассоциаты каркасной структуры. При 4°С между ними устанавливается равновесие, Н 2 О = 1 г/мл (max) • При Т Н-связи разрыхляются, , но водные ассоциаты возникают при любой Т.

СОСТОЯНИЕ ВОДЫ В ОРГАНИЗМЕ § определяется степенью упорядоченности водных структур в гидратных оболочках биосубстратов (S); § зависит от соотношения структурированной и деструктурированной Н 2 О.
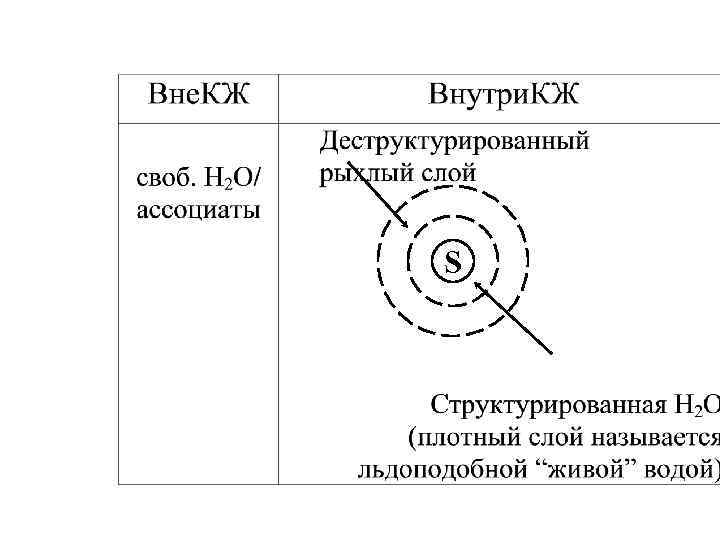
S

§ В такой упаковке клетка субстрата не деформируется и не погибает. § “Живая” вода легко усваивается организмом, т. к. ей не нужно перестраиваться при гидратации белков, тканей и т. д. § содержание структурированной Н 2 О имеет талая вода (сохраняется при Т<10°С); родниковая вода (при длительном контакте с минералами: кварц, шунгит, апатит, глина. . . ); Н 2 О под действием магнитного, электрического, акустического полей.

ФУНКЦИИ H 2 O В ОРГАНИЗМЕ 1. Содержание (%) воды в разные периоды жизни и в биосистемах

§ Чем моложе организм, тем он богаче водой и > υ обменных процессов. § Чем > интенсивность биохимических реакций, тем > требуется Н 2 О. § У взрослого человека (m 70 кг) содержится 40 -45 л Н 2 О, из них ~ 25 л во внутри. КЖ и ~15 л во вне. КЖ: внутрисосудистой и интерстициальной (межтканевой) жидкости.

§ Суточная потребность взрослого человека 35 г на 1 кг массы тела (~2, 5 л), а грудного ребенка - в 3 -4 раза больше. § Вся Н 2 О обновляется за 1 месяц, потеря 20% Н 2 О смертельна.

УНИКАЛЬНЫЕ СВОЙСТВА Н 2 О, обеспечивающие жизнедеятельность биосистем: § теплоемкость и испарения поддерживают постоянную Т тела, защищая его от перегрева; § вязкость и поверхностное натяжение обеспечивают транспортные функции: всасывание, распределение питательных веществ и метаболитов, их выведение, а также образование структурированной Н 2 О в гидратных оболочках биосубстратов (S); Вода – «матрица жизни» - поддержиает структуры рибосом их способность синтезировать белок.

§ дипольный момент и диэлектрическая проницаемость, а также наличие Н-связей обеспечивают: 1. хорошую растворимость электролитов, их диссоциацию на ионы, а также полярных веществ по правилу: “подобное растворяется в подобном”; 2. υ биохимических реакций и практически мгновенную υ передачи нервных импульсов; 3. быструю миграцию ионов через биомембраны. 4. участие в реакциях гидролиза белков, жиров, полисахаридов и т. д. 5. сохранение информации.
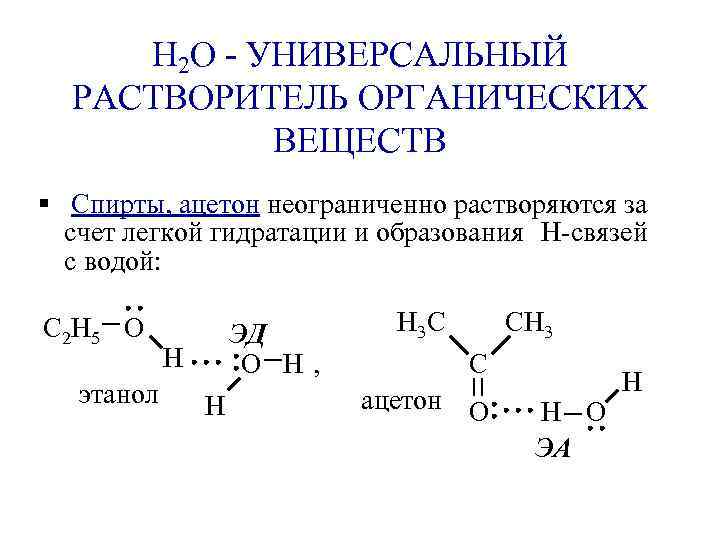
Н 2 О - УНИВЕРСАЛЬНЫЙ РАСТВОРИТЕЛЬ ОРГАНИЧЕСКИХ ВЕЩЕСТВ § Спирты, ацетон неограниченно растворяются за счет легкой гидратации и образования Н-связей с водой: C 2 H 5 O этанол ЭД O H, H H H 3 C CH 3 C ацетон O H O ЭА H

§ Бифильные молекулы (белки, липиды, фосфолипиды), содержащие гидрофильные функциональные группы и гидрофобные радикалы (R), при растворении в Н 2 О образуют компактные структуры, например, альбумины и глобулины сворачиваются в глобулы, в которых R направлены внутрь, а f -группы находятся снаружи. Диполи воды взаимодействуют с f-группами, изменяя их пространственную конфигурацию и их биологическую активность.
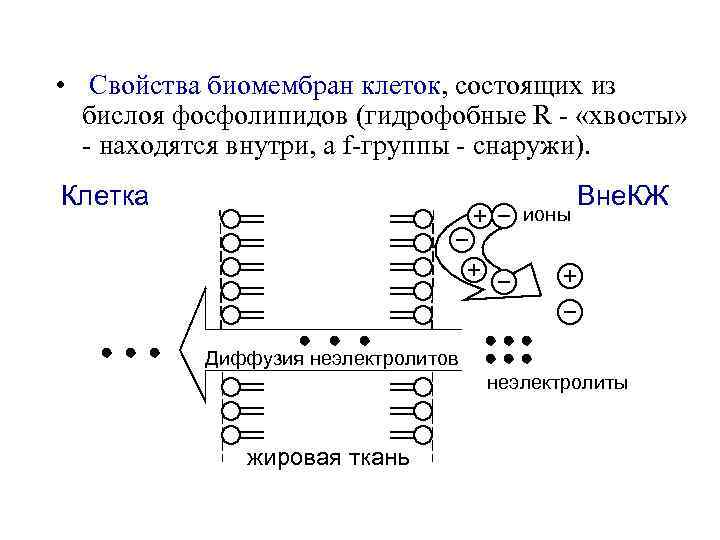
• Свойства биомембран клеток, состоящих из бислоя фосфолипидов (гидрофобные R - «хвосты» - находятся внутри, а f-группы - снаружи). Клетка ионы Вне. КЖ Диффузия неэлектролитов неэлектролиты жировая ткань

• Ионы электролитов сами не могут пройти через мембрану. • Диффундируют неионизированные молекулы, например, жирорастворимые витамины А, Д, Е, К. Они способны накапливаться в жировой ткани, поэтому их применяют в малых дозах, например, рыбий жир - для профилактики рака и СС-заболеваний.

§ Растворение в Н 2 О неполярных молекул, например, газов (N 2, O 2, CH 4 и др. ) происходит путем их внедрения в пустоты водных ассоциатов, где они удерживаются соседними молекулами Н 2 О.

ТЕРМОДИНАМИКА ПРОЦЕССА РАСТВОРЕНИЯ По II закону ТД: если GP=( P - T SP) < 0, то он идет самопроизвольно. § Влияние энтропийного фактора SP: При растворении т. ж. веществ SP , SP > 0 и вклад SP при Т. При растворении газов (г. ) SP < 0, т. е. решающий фактор - энтальпийный P.

§ Влияние P, которое может быть < 0 (экзотермич. ) или > 0 (эндотермич. процесс). Растворение т. и ж. веществ включает 2 стадии: 1) Разрушение кристаллической решетки физический эндотермический процесс всегда требует затрат Е, КР > 0. 2) Гидратация растворенных частиц химический экзотермический процесс идет по схеме: Э + n Н 2 О [Э (Н 2 О)n], Г < 0.

По закону Гесса: P = КР + Г • Если КР > Г , то P > 0 (эндотермич. процесс) (растворение нитритов, мочевины и др. при Т). • Если КР < Г , то P < 0 (экзотермич. процесс) (растворение электролитов, спиртов, сахаров и др. при Т).

• Растворение газов - всегда экзотермический процесс, т. к. P = Г < 0 и при Т.

РАСТВОРИМОСТЬ ГАЗОВ (СГ) В НОРМЕ И ПРИ ПАТОЛОГИИ. ГАЗОВЫЕ ЗАКОНЫ. СГ - зависит от природы газа, Т, р и присутствия электролитов. 1) Наибольшая СГ у полярных молекул (H 2 S, HCl, SO 3, NH 3 и т. д. ) благодаря их химическому взаимодействию с водой. Например, в 1 объеме Н 2 О растворяется 0, 02 V(He), 500 V(HCl), 750 V(NH 3). 2) СГ при Т, т. к. P (газов) < 0.

3) Закон Генри: “Растворимость газа прямо пропорциональна его парциальному давлению”. СГ = k. Г р. Г, где константа Генри k. Г зависит от природы газа и растворителя, и Т. (этот частный случай используют приготовлении шипучих напитков)

Закон Дальтона: “При растворении смеси газов в жидкости растворимость каждого компонента прямо пропорциональна его парциальному давлению и не зависит от общего давления смеси газов”. Ci(x) = ki pi (x), где парциальное давление данного газа pi(x) равно доле pi(x) от общего давления смеси газов.

Например, доля О 2 в воздухе - 0, 21 (21%). Общее давление p = 760 мм. рт. ст. р (О 2) = 760 0, 21 = 160 мм. рт. ст.

Закон Сеченова: “Растворимость газов понижается в присутствии электролитов”. -kca СГ = Со е , где Со - растворимость газа в чистом растворителе, е = 2, 3 (основание натурального логарифма), константа Сеченова k. C зависит от природы газа и Т, а - активность электролита, а с (эл-та). Причина СГ: в присутствии электролитов часть несвязанных молекул Н 2 О затрачивается на гидратацию ионов, и на растворение прежнего количества газов молекул Н 2 О не хватает. (высаливающий эффект)

ГАЗОВЫЙ ОБМЕН В ОРГАНИЗМЕ В НОРМЕ И ПАТОЛОГИИ. Он связан с транспортом О 2 в ткани и выведением метаболического СО 2 за счет разного парциального давления в легких, крови и тканях. § в легких р (О 2) > > p (СО 2) СО 2, доставленный из тканей в легкие, удаляется при выдохе, т. к. p (СО 2)возд < < p (СО 2)в легких. О 2 активно растворяется в венозной крови, т. к. р (О 2) > >. В эритроцитах: Hb + О 2 Hb. О 2 (оксигемоглобин). Артериальная кровь, насышенная О 2, поступает в ткани.

§ в тканях р (О 2) < < p (СО 2), особенно в мелких капиллярах. По закону Генри растворимость (О 2) , и Hb. О 2 Hb + О 2 диффундирует в ткани для участия в био. Ох б. ж. у. Конечный продукт био. Ох - СО 2, растворяется, т. к. p (СО 2) > >, поступает в кровяное русло. E + В эритроцитах СО 2 + Н 2 О H 2 CO 3 H + HCO 3
![СО 2 + Hb [Нb. СО 2] карбгемоглобин Венозная кровь поступает в легкие - СО 2 + Hb [Нb. СО 2] карбгемоглобин Венозная кровь поступает в легкие -](https://present5.com/presentation/22416208_22152199/image-29.jpg)
СО 2 + Hb [Нb. СО 2] карбгемоглобин Венозная кровь поступает в легкие - газовое пространство альвеол, где p (СО 2) резко и удаляется из организма. Кровь вновь насыщается О 2 и через 23 мин цикл повторяется.

p(О 2)в крови ПАТОЛОГИИ р (N 2) в крови ГИПОКСИЯ (горная болезнь) У альпинистов, парашютистов, летчиков КЕССОННАЯ БОЛЕЗНЬ У кессонщиков, водолазов, летчиков при разгерметизации спускаемого аппарата

Горная болезнь На высоте намного выше уровня моря атмосферное давление и р(О 2) в альвеолярном воздухе легких. Дефицит О 2 в артериальной крови вызывает вентиляцию легких, ЧСС, АД, ухудшение снабжения тканей и органов О 2 , головокружение, м. б. потеря сознания. Нужны: О 2 - маски и адаптация ( число эритроцитов)

Кессонная болезнь • При погружении под воду на 10 м р (газа) на 1 атм и на глубине 40 м р. Г 4 атм, вызывая СГ (N 2, О 2). Может произойти даже отравление О 2 (эйфрия, потеря сознания). • Если водолаза быстро поднять на поверхность, то СГ резко и растворимый ранее N 2 начнет выделяться в виде пузырьков, закупоривая мелкие кровеносные сосуды в тканях и органах “закипание крови”.

Развивается газовая эмболия. Ее модель: образование обильной пены при откупоривании бутылки шампанского. Симптомы: резкая боль в мышцах, головокружение, рвота, одышка, потеря сознания, паралич нижних конечностей и даже смерть.

Нужны барокамеры для замедления декомпрессии путем очень медленного снижения давления в течение нескольких суток и даже недель. ГБО - гипербарическая оксигенация - лечение О 2 под р(О 2) = 2 3 атм в барокамерах при анемической (кровопотери) или токсической гипоксии при отравлении СО, О 3, ожогах, газовой гангрене, стафилококковой пневмонии, родах женщин с тяжелыми пороками сердца и т. д.

При ГБО улучшается снабжение тканей О 2. “Жизнь без крови”, а только за счет физически растворенного О 2 , т. к. при 2 - 3 атм (О 2) его растворимость до 6%, что достаточно для поддержания жизни. При ГБО стало возможным длительное отключение кровоснабжения головного и спинного мозга в нейро- и кардиохирургии.
Биороль воды.ppt