f53e867784f7598e874a328b6bb1a314.ppt
- Количество слайдов: 17

БИООРГАНИК ВА БИОЛОГИК КИМЁ КАФЕДРАСИ БИОАНОРГАНИК КИМЁ I КУРС МАЪРУЗА № 3 МАВЗУ: БУФЕР СИСТЕМАЛАР LECTURE 3. THE BUFFER SYSTEMS. МАЪРУЗАЧИ : ПРОФЕССОР A. Ж. ЖЎРАЕВ

THE LECTURE PURPOSE: • In many alive organism including in organism of the person, is supported constant value of p. H basically to account of the buffer systems. When change p. H in alive organism occurs the slowing-down or acceleration of the different biochemical processes that brings to pathological change and even to deaths. • The study the particularities of the organism to save the constancy of p. H under the different external influence is one of the problems to modern physiology and biochemistry. • The investigation of the topic "Buffer systems" required for successful assimilation of some divisions of biochemistry, as well as special medical discipline. • Considering of important role of the buffer systems in vital activity of the organism, For physician it is necessary to know the characteristics of the buffer systems, mechanism of their action, to know how to prepare the solutions with given value of p. H.

КЎРИЛАДИГАН МАСАЛАЛАР • Буфер системаларнинг тузилиши ва турлари • Буфер системаларнинг p. Hини ҳисоблаш • Буфер системаларнинг таъсир этиш механизми • Буфер сиғими • Одам организмнинг буфер системалари • Буфер системаларнинг тиббиёт ва биологиядаги аҳамияти

БУФЕР ЭРИТМАЛАР ВА БУФЕР СИСТЕМАЛАР Биологик суюқликларнинг р. Н қийматлари ошқозон ширасининг p. H қиймати 1, 85 ± 0, 15 ичак ширасининг 6, 4 ± 0, 4 сулакнинг 6, 6 ± 0, 3 кон плазмасининг 7, 4 ± 0, 04 сийдикнинг 5 -8 Буфер системаларнинг р. Н қийматлари: ацетатли буфер система - 3, 72 - 5, 57 фосфатли буфер система - 5, 91 - 7, 73 аммиакли буфер система - 8, 43 - 10, 28 ТМА web сайт: www. tma. uz

Буфер системаларнинг турлари Буфер системалар икки турга бўлинади: 1. Кучсиз кислота ва шу кислотанинг кучли асос билан ҳосил қилган тузнинг аралашмаси. Масалан: CH 3 COOH + CH 3 COONa - ацетатли буфер эритма 2. Кучсиз асос ва шу асоснинг кучли кислота билан ҳосил қилган тузнинг аралашмаси. Масалан: NH 4 OH + NH 4 Cl - аммиакли буфер эритма ТМА web сайт: www. tma. uz

Кўриладиган буфер системалар • CH 3 COOH + CH 3 COONa - ацетатли буфер система • NH 4 OH + NH 4 Cl – аммиакли буфер система • H 2 CO 3 + Na. HCO 3 - гидрокарбонатли буфер система • Na. H 2 PO 4 + Na 2 HPO 4 – фосфатли буфер система • Pt. COOH + Pt. COONa – оқсилли буфер система • HHb + KHb – гемоглобинли буфер система • HHb. O 2 + KHb. O 2 – оксигемоглобинли буфер система

Кислотали буфер система учун Гендерсон. Гассельбах тенгламаси CH 3 COOH CH 3 COONa CH 3 COO- + H+ CH 3 COO- + Na+ [H+][CH 3 COO-] Кислота учун: Kdis. =---------- ёки: [CH 3 COOH] [H+] = Kdis. --------[CH 3 COO-]
![Кислотали буфер система учун Гендерсон-Гассельбах тенгламаси [CH 3 COOH] -lg [H+] = -lg. Kdis. Кислотали буфер система учун Гендерсон-Гассельбах тенгламаси [CH 3 COOH] -lg [H+] = -lg. Kdis.](https://present5.com/presentation/f53e867784f7598e874a328b6bb1a314/image-8.jpg)
Кислотали буфер система учун Гендерсон-Гассельбах тенгламаси [CH 3 COOH] -lg [H+] = -lg. Kdis. - lg--------[CH 3 COO-] C tuz p. H = p. Kk-ta + lg -----C k-ta

Асосли буфер система учун Гендерсон-Гассельбах тенгламаси NH 4 OH NH 4 Cl NH 4+ + OHNH 4+ + Cl[NH 4+][OH-] Асос учун: Kdis. =---------- ёки: [NH 4 OH] [OH-] = Kdis. --------[NH 4+]
![Асосли буфер система учун Гендерсон-Гассельбах тенгламаси [NH 4 OH] -lg [OH-] = -lg. Kdis. Асосли буфер система учун Гендерсон-Гассельбах тенгламаси [NH 4 OH] -lg [OH-] = -lg. Kdis.](https://present5.com/presentation/f53e867784f7598e874a328b6bb1a314/image-10.jpg)
Асосли буфер система учун Гендерсон-Гассельбах тенгламаси [NH 4 OH] -lg [OH-] = -lg. Kdis. - lg--------[NH 4+] C tuz p. OH = p. Kasos + lg ----Casos C tuz p. H = 14 - p. Kasos - lg ----Casos

Буфер таъсирининг механизми CH 3 COOH CH 3 COO- + H+ CH 3 COONa CH 3 COO- + Na+ Оз миқдорда кучли кислота қўшилганда: H+ + CH 3 COO- = CH 3 COOH мувозанат кучсиз электролит CH 3 COOH ҳосил бўлиш томонга силжийди. Оз миқдорда кучли асос қўшилганда: OH- + H+ = H 2 O мувозанат кучсиз электролит H 2 O ҳосил бўлиш томонга силжийди. ТМА web сайт: www. tma. uz

БУФЕР СИҒИМИ C B = ------- ммол p. H 1 - p. H 0 Бу ерда: B - буфер сиғими; ммол C - қўшилаётган кучли кислота асоснинг ммолдаги миқдори p. H 0 - бошланғич муҳит p. Hи охирги муҳит p. Hи p. H 1 - ТМА web сайт: www. tma. uz

БУФЕР СИҒИМИ N ·V B = ------- ммол p. H 1 - p. H 0 Бу ерда: B - буфер сиғими; ммол N - титрловчи эритманинг моляр эквивалент концентрацияси; ммол/л V - титрловчи эритманинг хажми; л p. H 0 - бошланғич муҳит p. Hи p. H 1 - охирги муҳит p. Hи ТМА web сайт: www. tma. uz

Организмнинг буфер системалари Гидрокарбонатли буфер система - қоннинг асосий буфер системаси: H 2 CO 3 H+ + HCO 3 Na. HCO 3 Na+ + HCO 3 Оз миқдорда кучли кислота қўшилганда кучсиз электролит H 2 CO 3 ҳосил бўлади: H+ + HCO 3 - = H 2 CO 3 Оз миқдорда кучли асос қўшилганда кучсиз электролит H 2 O ҳосил бўлади: OH- + H+ = H 2 O ТМА web сайт: www. tma. uz

Организмнинг буфер системалари Фосфатли буфер система - хужайра ичидаги суюқликларнинг асосий буфер системаси: Na. H 2 PO 4 Na+ + H 2 PO 4 Na 2 HPO 4 2 Na+ + HPO 42 Оз миқдорда кучли кислота қўшилганда кучсиз электролит H 2 PO 4 - ҳосил бўлади: H+ + HPO 42 - = H 2 PO 4 Оз миқдорда кучли асос қўшилганда кучсиз электролит H 2 O ва HPO 42 - ҳосил бўлади: OH- + H 2 PO 4 - = H 2 O + HPO 42 ТМА web сайт: www. tma. uz

Организмнинг буфер системалари Оқсилли буфер система - барча тўқималардаги буфер система Pt. COOH Pt. COO- + H+ Pt. COONa Pt. COO- + Na+ Оз миқдорда кучли кислота қўшилганда кучсиз электролит Pt. COOH ҳосил бўлади: H+ + Pt. COO- = Pt. COOH Оз миқдорда кучли асос қўшилганда кучсиз электролит H 2 O ҳосил бўлади: OH- + H+ = H 2 O ТМА web сайт: www. tma. uz
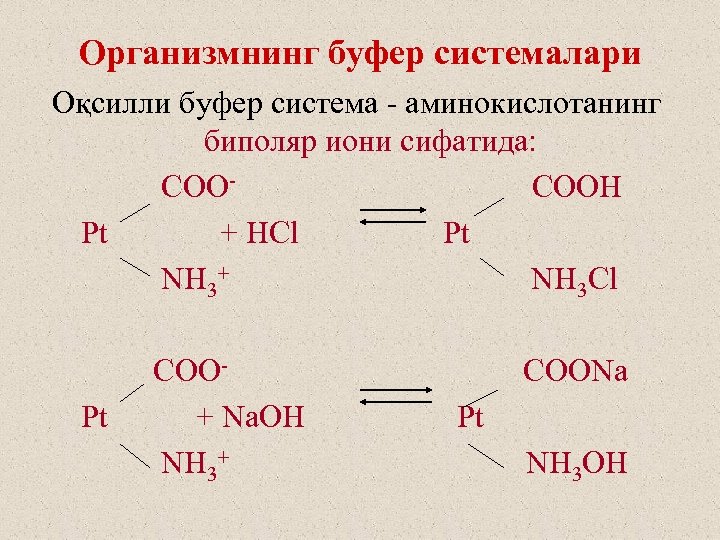
Организмнинг буфер системалари Оқсилли буфер система - аминокислотанинг биполяр иони сифатида: COOCOOH Pt + HCl Pt NH 3+ NH 3 Cl Pt COO+ Na. OH NH 3+ COONa Pt NH 3 OH
f53e867784f7598e874a328b6bb1a314.ppt