Биоорганическая химия (БОХ)

Предмет и задачи БОХ. • Электронное влияние заместителя (индуктивный и мезомерный эффекты). • Сопряжение. • Ароматичность.

Предметом изучения БОХ являются соединения организма – биополимеры и биорегуляторы.

В задачу БОХ входит рассмотрение реакционной способности этих соединений и факторов на неё влияющих.

Реакционная способность зависит от: • Природы атомов, образующих соединение; • Типа связи между атомами; • Влияния заместителя, введеного в молекулу.

Известны два пути передачи электронного влияния заместителя – индуктивный и мезомерный эффекты.

Индуктивный эффект (I) – смещение электронной плотности по цепи σ – связей под влиянием введенного в молекулу заместителя.

Направление I – эффекта качественно оценивают по водороду, эффект которого принят за 0.

Положительный I – эффект (+ I) дают X – заместители, которые по сравнению с водородом повышают электронную плотность в цепи σ – связей. Они являются электродонорами ( ЭД ): анионы, металлы, алифатические радикалы – CH 3 - < C 2 H 5 - < C 3 H 7 – и т. д.

Отрицательный I – эффект (- I ) дают Y – заместители. Они понижают электронную плотность в цепи и потому являются электроноакцепторами ( ЭА ). Это катионы и все функциональные группы : - СООН, - SO 3 H, - NO 2, - NH 2, - OH, галогены и др.
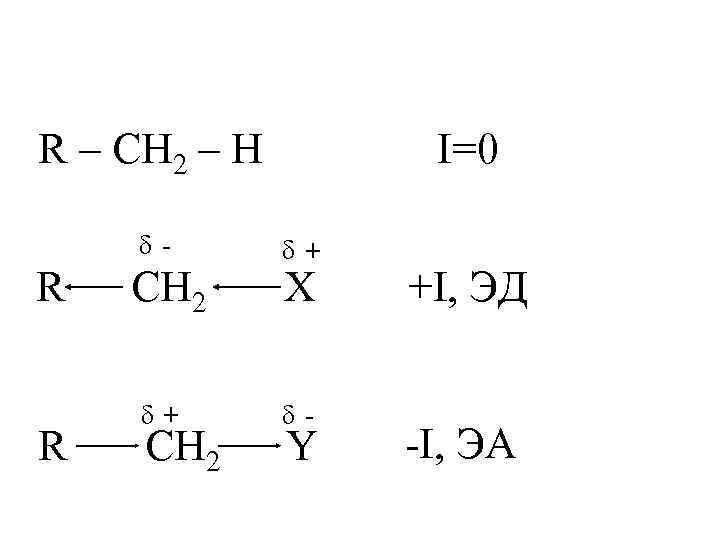
R – CH 2 – H δ- I=0 δ+ R CH 2 X δ+ δ- R CH 2 Y +I, ЭД -I, ЭА

Графически I – эффект изображают стрелкой по σ– связи. Остриё стрелки направлено в сторону более электроотрицательного атома.

Электроотрицательность (ЭО) – это способность атома удерживать валентные электроны. Самый электроотрицательный в ПСЭ – фтор.

Исходя из значений энергии связей Л. Полинг ввёл шкалу ЭО (шкала Полинга): F O N Cl Br I C S H Li Na 4, 0 3, 5 3, 0 2, 8 2, 6 2, 5 2, 1 1, 0 0, 9

I – эффект из-за слабой поляризуемости σ – связи быстро затухает, через 3 – 4 связи. Его действие наиболее сильно проявляется на двух ближайших к заместителю атомах углерода.
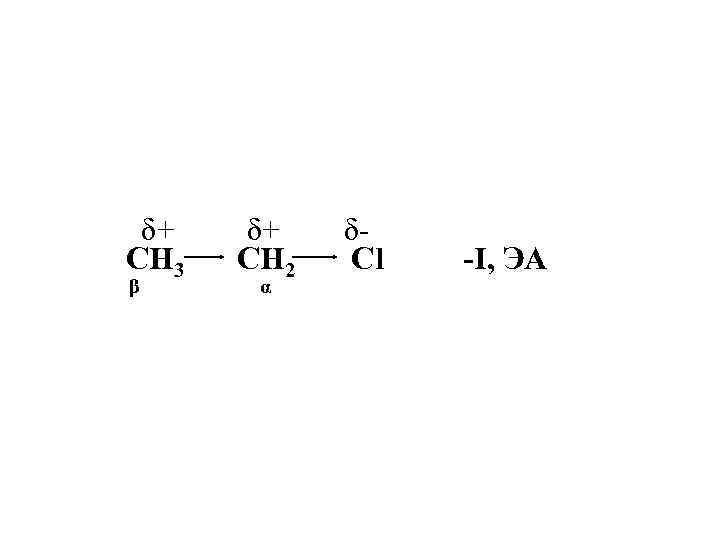
δ+ δCH 3 CH 2 Cl β α -I, ЭА

В молекуле этана все углерод-водородные связи были равноценны и замещение на хлор было возможно с любого атома водорода. Введённый заместитель перераспределяет электронную плотность в молекуле и дальнейшее замещение пойдёт преимущественно по α – водородным атомам.
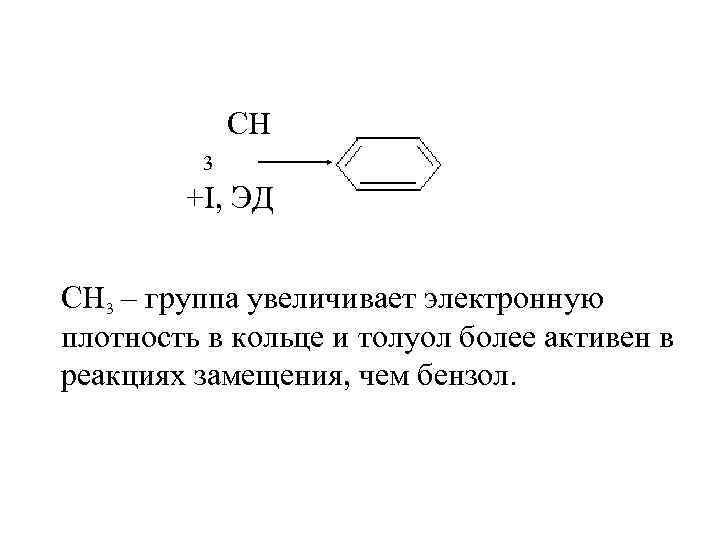
CH 3 +I, ЭД CH 3 – группа увеличивает электронную плотность в кольце и толуол более активен в реакциях замещения, чем бензол.

Сопряжённые системы. Сопряжение. Ковалентная π - связь может быть локализованной и делокализованной.
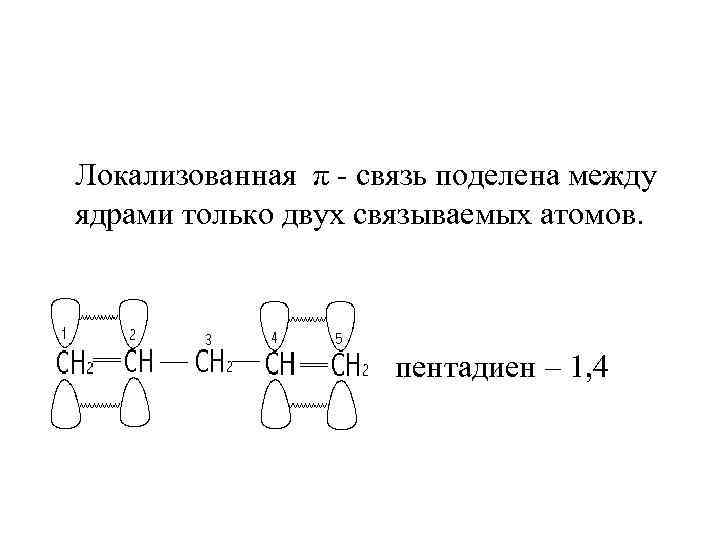
Локализованная π - связь поделена между ядрами только двух связываемых атомов. пентадиен – 1, 4

Одна π - связь принадлежит ядрам C 1 и C 2, а другая - только ядрам C 4 и C 5. Такая π - связь локализована, а система называется изолированной.

Молекулярная орбиталь делокализованной π- связи охватывает более двух связываемых атомов. Такая связь характерна для сопряжённых систем.

Система называется сопряжённой, если в ней кратная связь одной простой связью отделена от соседнего атома имеющего p – орбиталь. . . CH 2=CH – CH=CH 2 CH 2=CH - OH бутадиен – 1, 3 виниловый спирт

В сопряжённых системах наблюдается особый вид влияния атомов – сопряжение.

Сопряжённые системы бывают: • с открытой цепью сопряжения, • замкнутой, • содержащие гетероатомы.
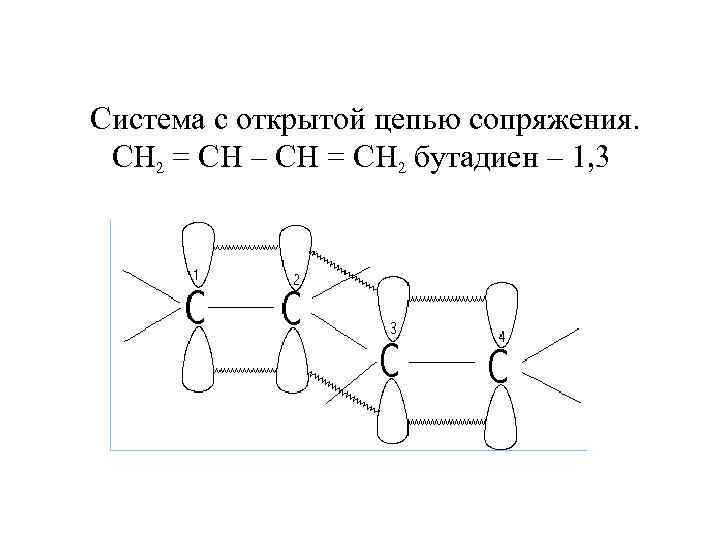
Система с открытой цепью сопряжения. CH 2 = CH – CH = CH 2 бутадиен – 1, 3

Все атомы углерода в бутадиене находятся в sp² - гибридизации и образуют в плоскости под углом 120º три σ – связи.

Негибридизированные p – AO каждого атома углерода перпендикулярны плоскости σ – скелета и параллельны другу, что является необходимым условием для их перекрывания.

p – AO C 1 и C 2, C 3 и C 4, перекрываясь дают π - связи. Однако здесь перекрываются p – AO C 2 и C 3, т. к. отделены одной простой связью.

В результате образуется единая π- молекулярная орбиталь, охватывающая все четыре атома углерода, и происходит частичное выравнивание связей: двойные становятся длиннее, а одинарные короче.

Явление выравнивания связей и зарядов в реальной молекуле по сравнению с идеальной, но не существующей структурой и называется сопряжением.

Pазличают два типа сопряжения: - π, π - сопряжение; - p, π - сопряжение.
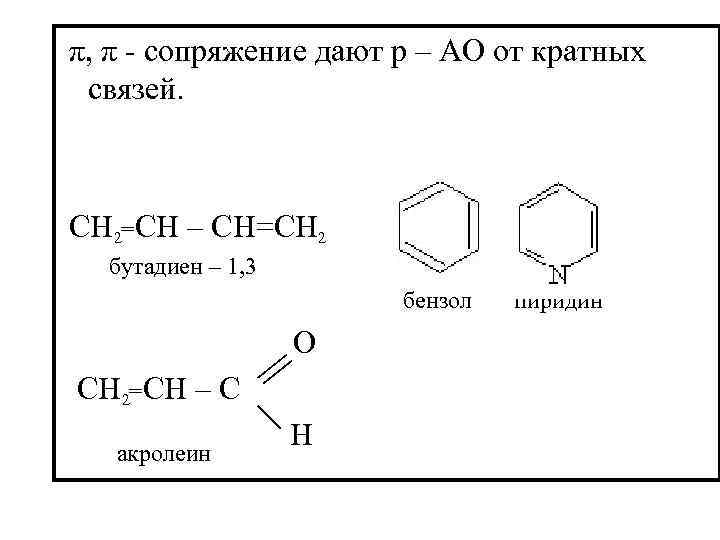
π, π - сопряжение дают p – AO от кратных связей. СH 2=CH – CH=CH 2 бутадиен – 1, 3 бензол пиридин O CH 2=CH – C H акролеин
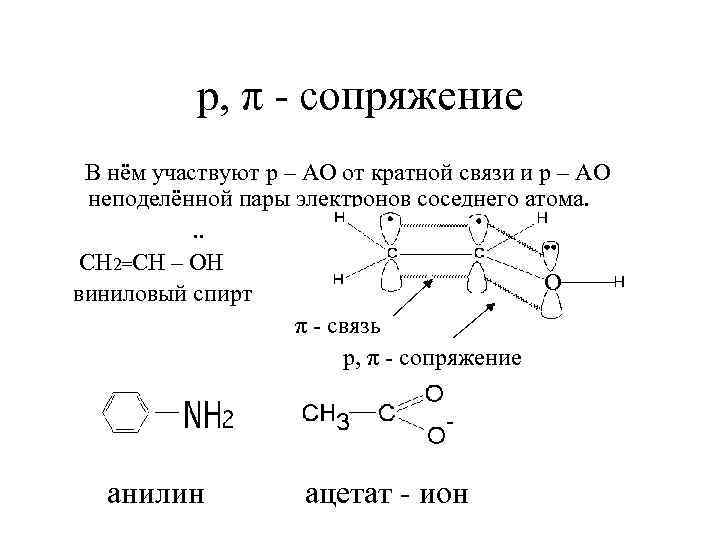
p, π - сопряжение В нём участвуют p – AO от кратной связи и p – AO неподелённой пары электронов соседнего атома. . . CH 2=CH – OH О виниловый спирт π - связь р, π - сопряжение анилин ацетат - ион

Сопряжение энергетически выгодный процесс, всегда сопровождается выделением энергии и образованием термодинамически более устойчивых систем.

Количественно степень устойчивости сопряжённой системы оценивают энергией сопряжения (Eсопр. ). Чем ↑ Eсопр. , тем устойчивее система. Высокие Eсопр. у полиенов. К ним относятся каратиноиды - раcтительные пигменты, обуславливающие окраску моркови, томатов. Очень устойчивые системы.

Eсопр. бутадиена невелика, около 15 к. Дж/моль. Однако наличие сопряжения в молекуле бутадиена обуславливает особенность его поведения в реакциях присоединения: преимущественно образуется продукт 1, 4 – присоединения как более устойчивый (см. лекцию 2).
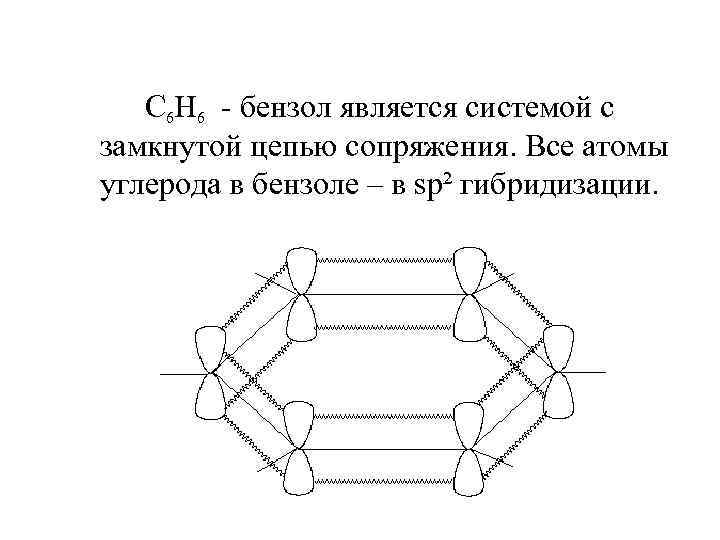
C 6 H 6 - бензол является системой с замкнутой цепью сопряжения. Все атомы углерода в бензоле – в sp² гибридизации.

Негибридизированные p – AO всех атомов углерода в бензоле, перекрываясь, образуют единую π - молекулярную орбиталь над и под плоскостью σ – скелета. Происходит полное выравнивание связей, все связи в бензоле равноценны с длиной 0, 14 нм.

В бензоле абсолютно делокализованная π - связь. Eсопр. бензола 228 к. Дж/моль. Бензол очень устойчивая система. В результате, несмотря на большую ненасыщенность, для бензола характерны реакции замещения (SE). Присоединение по месту разрыва углеродных связей идёт только в жестких условиях.

Соединения типа бензола получили название ароматических. Ароматичность значит устойчивость.

В 1931 г. Хюккель ввёл три критерия ароматичности. Соединение ароматично, если имеет: • плоский замкнутый цикл; • все атомы цикла образуют единую сопряжённую систему; • эта система содержит (4 n+2) π - электрона, где n = 1, 2, 3 и т. д. (чаще n обозначает число циклов).
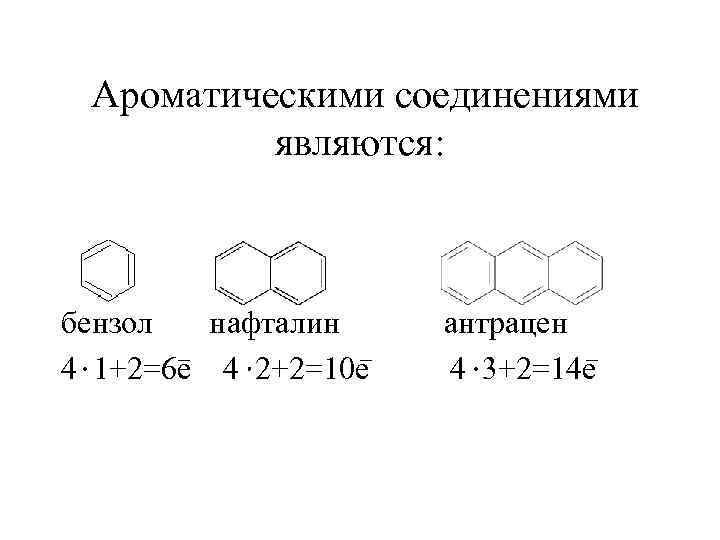
Ароматическими соединениями являются: бензол нафталин антрацен 4 1+2=6 е 4 2+2=10 е 4 3+2=14 е

• Среди ароматических соединений много гетероциклических систем, содержащих гетероатомы N, S, O. В ряду этих соединений встречаются оба вида сопряжения π, π и p, π.
π, π - сопряжение характерно для шестичленных гетероциклов с одним или несколькими гетероатомами, простейший из них пиридин.

Атом азота в пиридине находится как и атомы углерода в sp² - гибридизации. +7 N 1 s¹ 2 s² 3 p³ 2 s 2 p S – AO Px Py Pz - АО
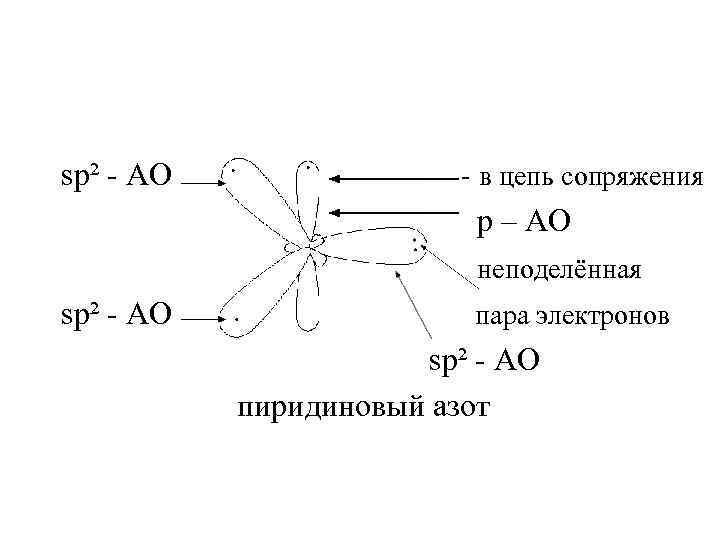
sp² - AO - в цепь сопряжения p – AO неподелённая sp² - AO пара электронов sp² - AO пиридиновый азот

Две из трёх sp² - гибридных орбиталей образуют две σ – связи. Третья sp² - AO содержит неподелённую пару электронов, которая придаёт пиридиновому азоту донорные, основные свойства.

• Негибридизированная p – AO поставляет в ароматическое кольцо один p – электрон.

Таким образом, для пиридина выполняются все три критерия Хюккеля: • плоский замкнутый цикл; • все атомы цикла в sp² - гибридизации; • в цикле 1ē + 5ē = 6ē

p, π - сопряжение – в пятичленных гетероциклах с атомами азота, кислорода, серы.
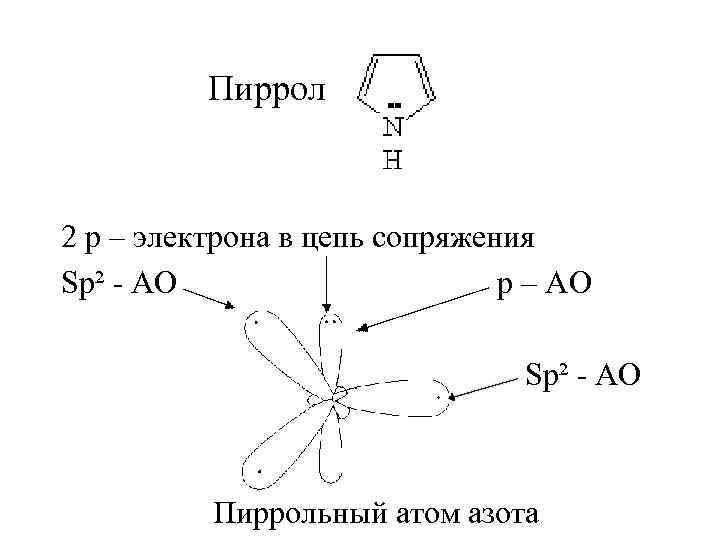
Пиррол 2 p – электрона в цепь сопряжения Sp² - AO p – AO Sp² - AO Пиррольный атом азота

• Пиррольный азот тоже находится в sp² - гибридизации. Три гибридые AO дают три σ – связи под углом 120 o°. • Негибридная p – AO поставляет в цикл два электрона ( 2ē N + 4 ē C = 6 ē ). Выполняются все критерии Хюккеля, пиррол – ароматическое соединение.

Примеры ароматических гетероциклов: фуран тиофен имидазол пурин пиримидин

Мезомерный эффект (M) – влияние заместителя по π - связям в сопряжённой систе при условии, что заместитель становится участником цепи сопряжения.

+M дают заместители, имеющие на валентном уровне неподелённые пары электронов и вступающие в p, π - сопряжение с системой ( - NH 2, - OH, -OR, -SH, галогены, анионы).
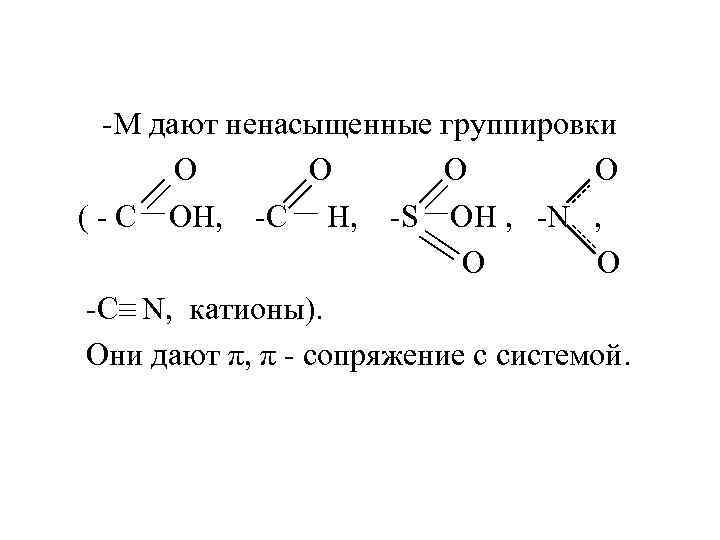
-M дают ненасыщенные группировки O O ( - C OH, -C H, -S OH , -N , O -C N, катионы). Они дают π, π - сопряжение с системой.

M – эффект в отличие от I – эффекта не затухает, т. к. π - связь легко поляризуема.

M – эффект изображают изогнутой стрелкой, начало которой на паре электронов или π - связи заместителя, а остриё направлено в сторону атома или связи к которым происходит смещение.

Чтобы определить ЭД или ЭА является заместитель в сопряжённой системе, оба эффекта суммируют. Для всех заместителей M – эффект сильнее I – эффекта, кроме галогенов. Их -I сильнее +M.
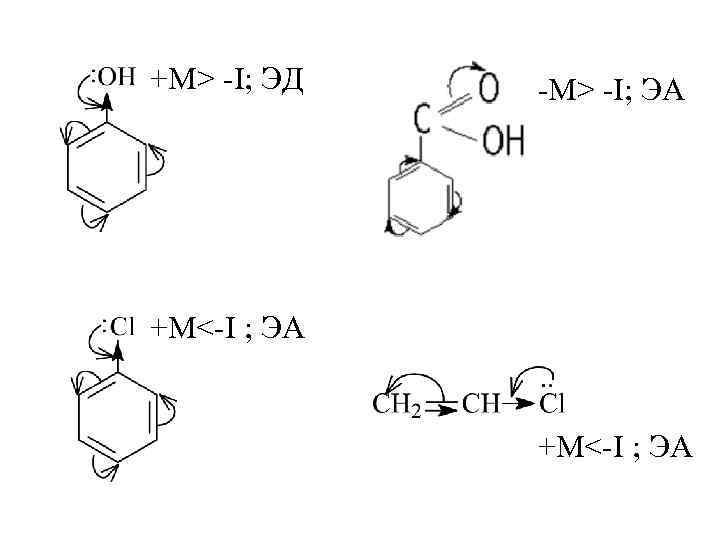
+M> -I; ЭД -M> -I; ЭА +M<-I ; ЭА